Настоящее изобретение относится к полициклическим ксантонам и их противоопухолевому применению.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
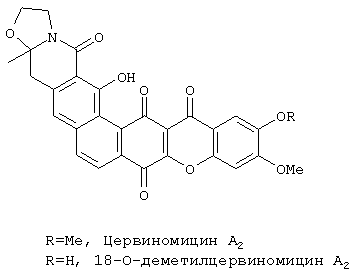
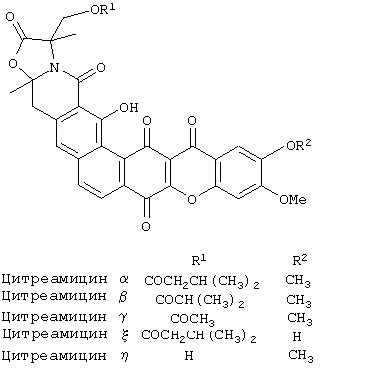
Цервиномицины (ЕР 00246091; ЕР 0054801; J. Antibiot., 1982, 35, 645-652; J. Am. Chem. Soc., 1986, 108, 6088-6089, J. Antibiot., 1987, 40, 301-308; J. Antibiot., 1994, 47, 342-348; синтетические производные J. Antibiot., 1986, 39, 1636-1639 и ЕР 0259496) и цитреамицины (J. Antibiot., 1989, 42, 846-851; J. Antibiot., 1990, 43, 504-512; EP 0405151) принадлежат к семейству встречающихся в природе антибиотиков, каждый из которых содержит ксантоновую структурную единицу, включенную в более крупную полициклическую структуру.
Указанные соединения обладали сильной активностью в отношении аэробных и анаэробных бактерий и микоплазм, однако противоопухолевая активность была описана только для цервиномицинов (ЕР 0246091).
Недавно в международной заявке PCT/GB01/02148 авторами изобретения также была описана противоопухолевая активность цитреамицинов.
Для лечения многих опухолей человека до сих пор существует потребность в новых противоопухолевых лекарственных средствах. Соответственно, целью настоящего изобретения являлось создание новых противоопухолевых агентов, имеющих полициклическую ксантоновую структуру.
Другой целью настоящего изобретения являлось создание фармацевтических композиций для введения активного соединения нуждающимся в лечении пациентам.
Еще одна цель изобретения была направлена на производство полициклического ксантона путем контролируемой аэробной ферментации с применением биологически чистой культуры микроорганизма в подходящей питательной среде, а также на разработку способов его выделения и концентрирования из ферментационного бульона, и окончательной очистки активного соединения.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
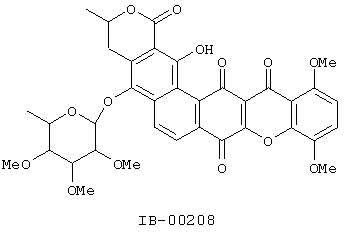
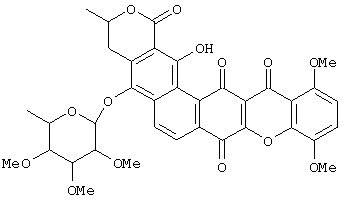
Настоящее изобретение относится к новому классу активных ксантоновых соединений, основанному на открытии нового выделенного из бактерий соединения IB-00208, полезного в качестве противоопухолевого лекарственного средства формулы:
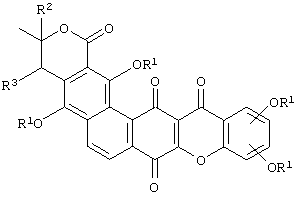
Таким образом, настоящее изобретение относится к соединениям общей формулы:
или
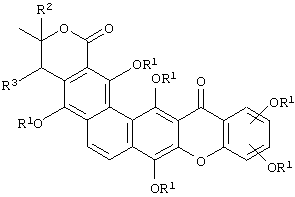
где каждый заместитель R1 является одинаковым или различным и может представлять собой водород, ацил, алкил, алкенил, арил, бензил, щелочной металл и/или сахар, а R2 и R3 могут представлять собой водород, алкил или образовывать вместе ненасыщенную связь.
Настоящее изобретение также относится к способам получения данных соединений, включая способ получения соединения IB-00208.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
IB-00208 и родственные соединения обладают противоопухолевой активностью в отношении опухолей млекопитающих, таких как карцинома легких человека, карцинома толстой кишки человека, меланома человека, и подобных. Таким образом, настоящее изобретение включает способ лечения любого млекопитающего, страдающего злокачественной опухолью, чувствительной к нему, который включает введение больному терапевтически эффективного количества соединения - или его фармацевтической композиции.
Настоящее изобретение также относится как к фармацевтическим препаратам, которые включают в качестве активного ингредиента соединение IB-00208 или любое его производное, или их фармацевтически приемлемую соль, а также к способам их получения. Используется фармацевтически приемлемый носитель.
Фармацевтические композиции обычно получают из активного соединения и включают любые твердые формы (таблетки, пилюли, капсулы, гранулы, и подобные) или жидкие формы (растворы, суспензии иди эмульсии) в комбинации с любым носителем или другими фармакологически активными соединениями.
Правильная доза фармацевтической композиции соединения IB-00208 или его производных может изменяться в соответствии с конкретным соединением, препаративной формой, способом введения, и местом локализации у хозяина и типом подвергаемой лечению опухоли.
Другие факторы, такие как возраст, вес тела, пол, рацион питания, время введения, скорость выведения, состояние пациента, комбинация лекарственных средств, индивидуальная чувствительность и тяжесть заболевания, должны быть приняты во внимание. Введение может производиться постоянно или периодически в пределах максимально переносимой дозы.
Ацильные группы могут представлять собой алифатический ацил, ароматический ацил или смешанный алифатический/ароматический ацил. Так, например, они могут соответствовать формуле RCO-, где R представляет собой алкильную группу, алкенильную группу, арильную группу, арилалкильную группу или алкиларильную группу. Примеры включают бензоил.
Алкильные группы обычно содержат от 1 до 18 атомов углерода. Алкильные группы предпочтительно содержат от 1 до приблизительно 12 атомов углерода, более предпочтительно от 1 до приблизительно 8 атомов углерода, еще более предпочтительно от 1 до приблизительно 6 атомов углерода, и наиболее предпочтительно 1, 2, 3 или 4 атома углерода. Особенно предпочтительными алкильными группами в соединениях по настоящему изобретению являются метильная, этильная и пропильная, включая изопропильную. Используемый здесь термин «алкильная», если не определено иначе, относится как к циклическим, так и к нециклическим группам, хотя циклические группы должны содержать в кольце по крайней мере три атома углерода. Алкильные группы могут быть с неразветвленной или с разветвленной цепью.
Алкенильные группы обычно содержат от 1 до 18 атомов углерода. Предпочтительные алкенильные группы в соединениях по настоящему изобретению содержат одну или несколько ненасыщенных связей и от 2 до приблизительно 12 атомов углерода, более предпочтительно от 2 до приблизительно 8 атомов углерода, еще более предпочтительно от 2 до приблизительно 6 атомов углерода, и еще более предпочтительно 2, 3 или 4 атома углерода. Используемый здесь термин «алкенильная» относится как к циклическим, так и к нециклическим группам, хотя неразветвленные или разветвленные нециклические группы являются в общем более предпочтительными.
Арильные группы могут быть карбоциклическими или гетероциклическими и могут содержать одно или несколько конденсированных колец. Карбоциклические арильные группы обычно содержат 6 или 10 атомов углерода, как в фенильной или нафтильной группах. Гетероциклические арильные группы обычно содержат от 5 до 12 атомов, более часто 4, 5, 6, 10, 11 или 12 атомов, из которых 1, 2, 3 или более представляют собой гетероатомы, обычно выбираемые из кислорода, серы или азота. Подходящие гетероциклические арильные группы в соединениях по настоящему изобретению включают кумаринил, включая 8-кумаринил, хинолинил, включая 8-хинолинил, пиридил, пиразинил, пиримидил, фурил, пирролил, тиенил, тиазолил, оксазолил, имидазолил, индолил, бензофуранил и бензотиазол.
Типичные щелочные металлы включают натрий и калий.
Применяемые в качестве заместителей сахара обычно представляют собой моно-, ди- или трисахариды, или сахаридные производные, предпочтительно моно- или дисахариды. Предпочтительными являются соединения пентозы или гексозы. Производные включают сахарные гликозиды, N-гликозиламины, O-ацильные производные, O-метильные производные, сахарные спирты, сахарные кислоты, дезоксисахара или родственные соединения. Примеры включают триметилдезоксипиранозу гексозу соединения IB-00208.
В настоящем изобретении описан новый полициклический ксантон IB-00208, выделенный из ферментационного бульона микроорганизма, предпочтительно штамма Actinomadura sp. PO13-046, культура которого была помещена в Colección Espanola de Cultivos Tipo Университета Валенсии, Испания под номером доступа СЕСТ 5318. Депозит данной культуры был совершен в соответствие с положениями Будапештского Договора, и все ограничения доступа к нему общественности будут сделаны до момента выдачи патента по настоящей заявке.
Штамм микроорганизмов был выделен из неидентифицированных морских многощетинковых червей, собранных в Бискайском заливе.
Хотя депозитированный микроорганизм несомненно является предпочтительным, настоящее изобретение не относится к или не ограничивается каким-либо конкретным штаммом или микроорганизмом. В объем настоящего изобретения включены другие продуцирующие соединение IB-00208 микроорганизмы, штаммы или мутанты.
Штамм Actinomadura sp. PO13-046, культивируемый в контролируемых условиях в подходящей среде, продуцирует антибиотик IB-00208. Указанный штамм предпочтительно растет в водной питательной среде в аэробных и мезофильных условиях.
Антибиотик IB-00208 может быть выделен из осадка мицелия экстракцией подходящей смесью растворителей, такой как CHCl3:СН3ОН:Н2O. Активность концентрируется в нижнем слое. Экстракты двух повторных экстракций могут быть объединены и упарены досуха в вакууме.
Выделение и очистка соединения IB-00208 из неочищенного активного экстракта может быть выполнена с применением подходящей комбинации традиционных хроматографических методик.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1 представляет собой 1Н-ЯМР-спектр очищенного соединения IB-00208;
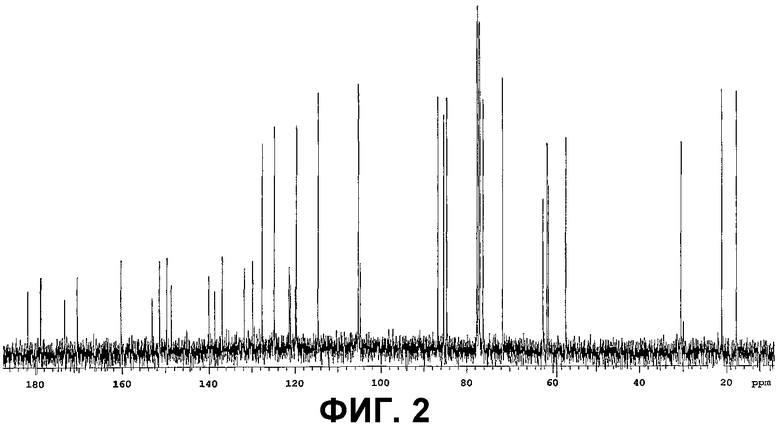
Фигура 2 представляет собой 13С-ЯМР-спектр очищенного соединения IB-00208;
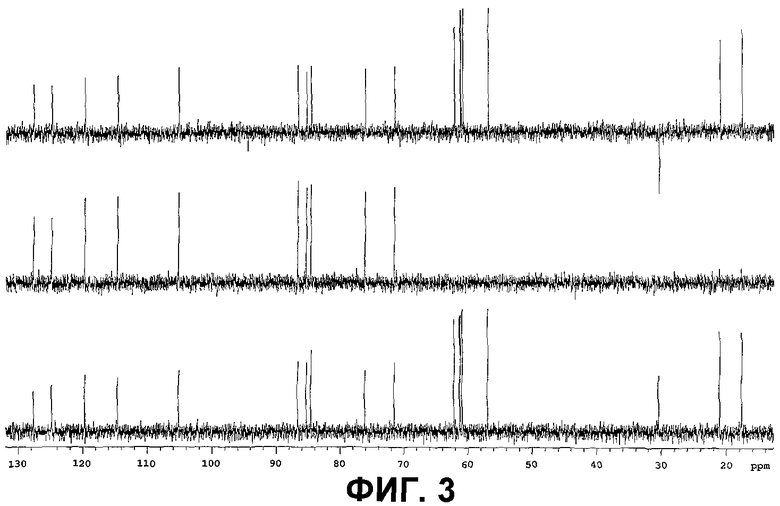
Фигура 3 представляет собой DEPT эксперимент очищенного соединения IB-00208;
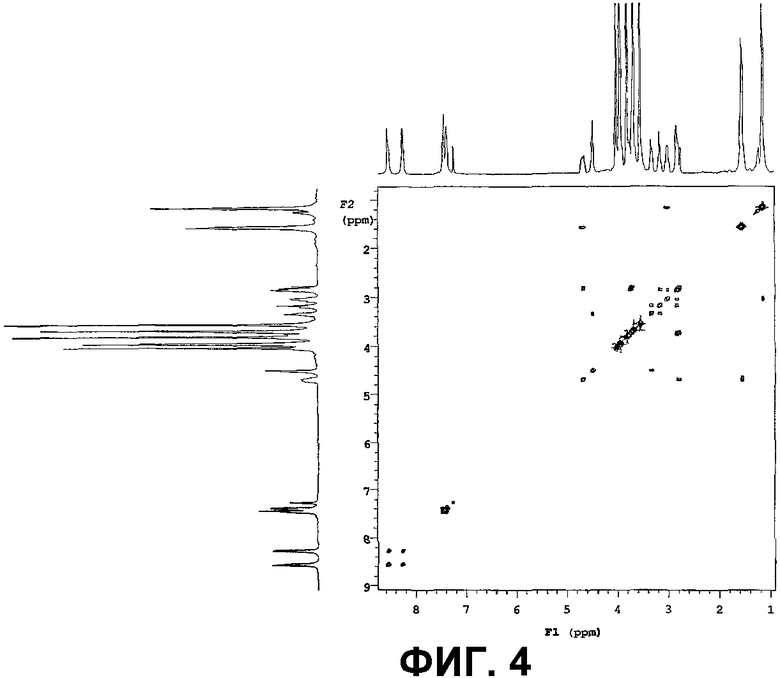
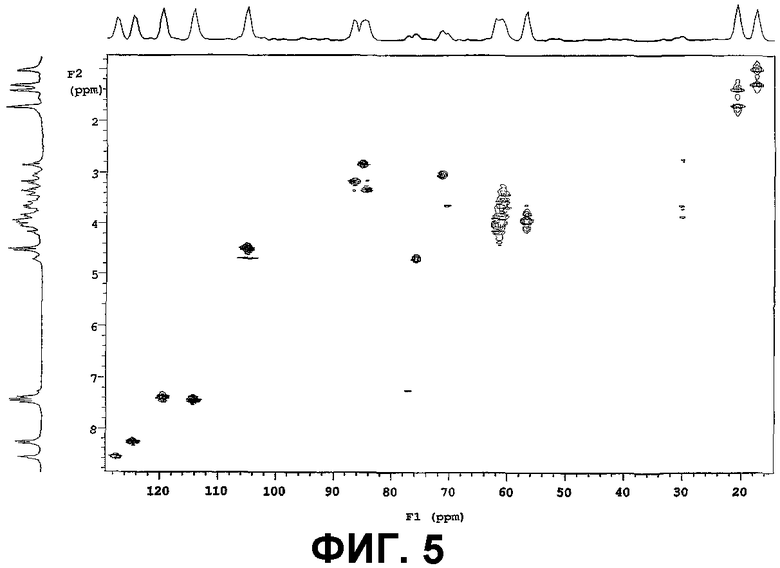
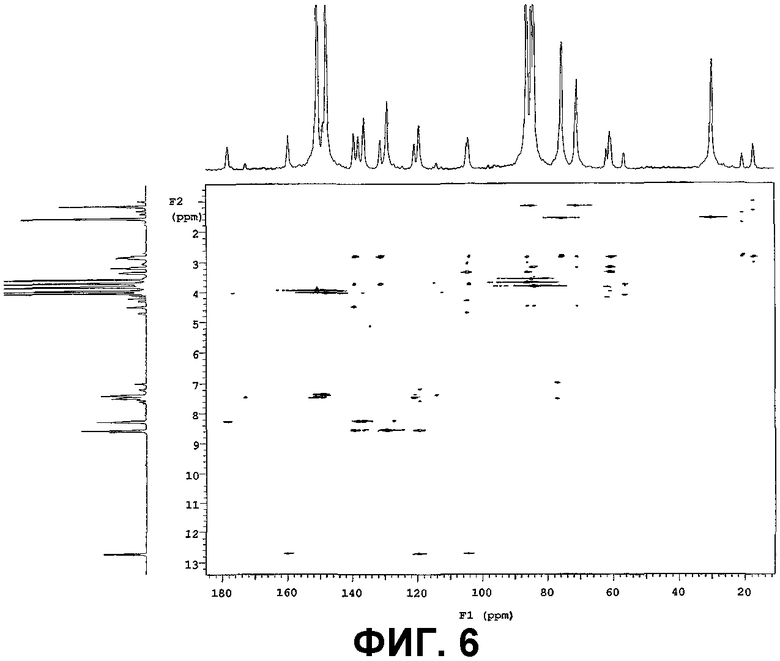
Фигуры 4, 5, и 6 представляют собой COSY 45, HMQC и НМВС спектры очищенного соединения IB-00208, соответственно;
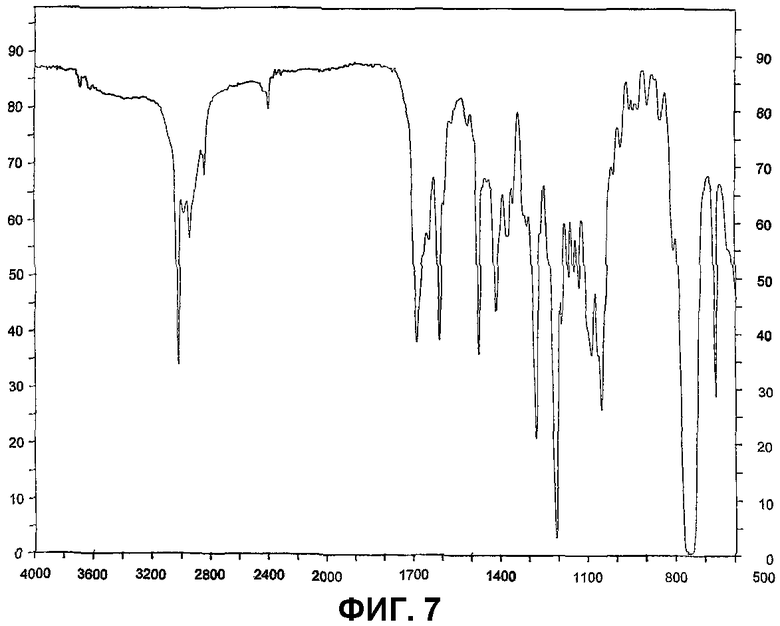
Фигура 7 представляет собой ИК-спектр очищенного соединения IB-00208;
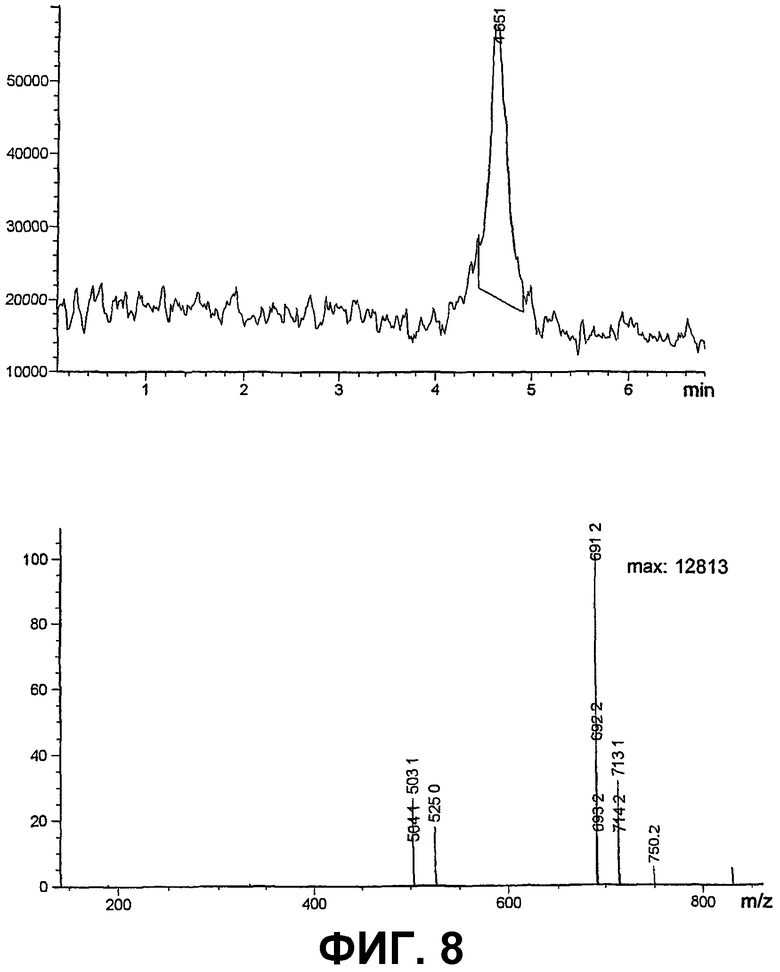
Фигура 8 представляет собой ВЭЖХ/МС-хроматограмму и ESI-MS-спектр соединения IB-00208; и
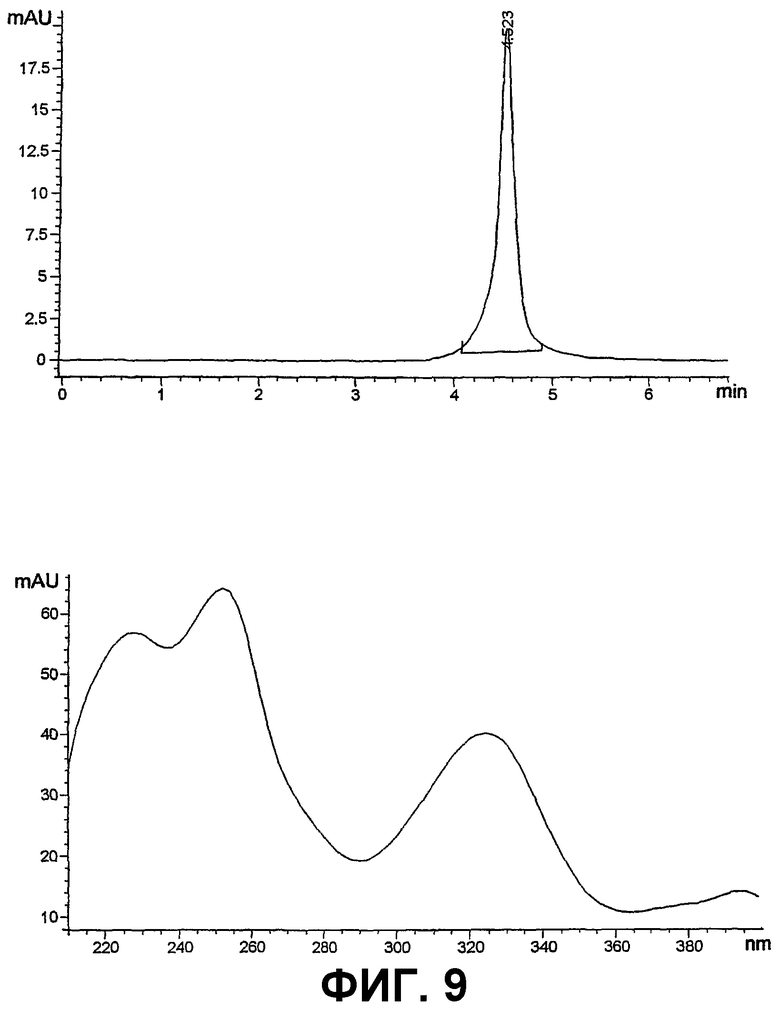
Фигура 9 представляет собой ВЭЖХ/УФ-хроматограмму и УФ-спектр очищенного соединения IB-00208.
Разделение на фракции может проводиться по принципу противоопухолевой активности фракций, или методом ТСХ с проявлением ванилином в концентрированной H2SO4, или методом аналитической ВЭЖХ с фотодиодом и МС-детектором. ВЭЖХ-анализ проводят при комнатной температуре с применением аналитической колонки Symmetry C18 (5 мкм), используя в качестве подвижной фазы смесь метанол: Н2О: уксусная кислота (99:1:1) со скоростью потока 0,3 мл/мин и регистрируя значения при 325 нм, причем в данных условиях время удерживания для соединения IB-00208 составляет 4,5 минуты, как показано на фиг.9.
На основании детального анализа его различных спектральных характеристик чистое соединение было идентифицировано как соединение IB-00208 (смотри данные, представленные на фигурах 1-9). Поэтому установленная структура соответствует представленной выше.
Данные соединения IB-00208 суммированы в Таблице 1.
Таблица 1
Максимумы поглощения УФ-спектра: 225, 255 нм и 325 нм, как представлено на фиг.9.
1H-, 13С- и DEPT ЯМР-спектры представлены на фиг.1, фиг.2 и фиг.3, соответственно.
Результаты 2D ЯМР-экспериментов COSY, HMQC и НМВС представлены на фиг.4, фиг.5 и фиг.6, соответственно.
Инфракрасный спектр поглощения представлен на фиг.7.
ES-MC-спектр обнаруживает (М+Н)- пик при 691 и (M+Na) пик при 713, как показано на фиг.8.
Различные производные соединения IB-00208 могут также быть получены с применением известных в данной области техники методик. В качестве примера, данные изменения могут быть внесены с применением химических и биологических методов.
Данные изменения включают:
- получение агликоновой части;
- добавление к агликону различных известных и новых сахаров;
- модификацию агликона.
Могут быть получены соединения с различными ацильными, алкильными, алкенильными, арильными, бензильными группами и/или группами сахаров в R1. Таким образом, например, ацилгалогениды и алкильные, алкенильные, арильные или бензильные ангидриды могут быть использованы в качестве электрофилов для реакций ацилирования IB-00208 в соответствующих основных или кислотных условиях в соответствующих растворителях. Альтернативно, для реакций алкилирования IB-00208 в подходящих условиях могут применяться алкил-, алкенил-, арил- или бензилгалогениды, мезилаты или тозилаты. Дополнительно, различные производные сахаров, известные и новые, могут использоваться в качестве реагентов для реакций гликозидирования в стандартных условиях для данного типа реакции.
С другой стороны, соединения, содержащие гидрохиноновое кольцо, могут быть получены из соединения IB-00208 восстановлением хинона подходящим восстанавливающим агентом [например: NaBH4 (Т.Ross Kelly et al., J. Am. Chem. Soc., 1989, 111, 4522-4524), Na2S204 (A.V.Rama Rao et al., Tetrahedron Lett., 1991, 32, 5199-5202)] в подходящем растворителе, с последующим (когда R1≠Н) проведением взаимодействия гидрохинона с ацилирующим или алкилирующим или подходящим агентом в подходящем растворителе. Как описано выше, различные ацильные, алкильные, алкенильные, арильные, бензильные и/или группы сахаров могут быть введены также в R1. Также различные алкильные группы могут быть введены в R2 и R3. Кроме того, R2 и R3 могут быть связаны посредством ненасыщенной связи, например, посредством реакции метатеза с внутримолекулярным замыканием цикла между двумя концевыми двойными связями.
Настоящее изобретение со ссылкой на предпочтительные воплощения ниже дополнительно проиллюстрировано примерами, которые имеют целью помочь в понимании настоящего изобретения и только проиллюстрировать его, и не должны истолковываться как ограничивающие его.
ПРИМЕРЫ ИЗОБРЕТЕНИЯ
Все указанные здесь проценты, если не определено иначе, представлены по весу. Все указанные температуры выражены в градусах Цельсия. Все инкубации проводили при 28°, если не оговорено иначе, и колбы встряхивали на круговом шейкере со скоростью 250 об/мин. Все среды и реципиенты являлись стерильными, а все операции с культурами асептическими.
Примеры 1-3 относятся к получению соединения IB-00208 указанной выше формулы. Примеры 4-9 относятся к получению соединений 1-6 по изобретению. Пример 10 касается определения биологической активности соединения IB-00208.
ПРИМЕР 1
Продуцирующий микроорганизм.
Применяемые здесь таксономические методы представляют собой методы, обычно применяемые в классической таксономии Actinomycete, и описаны в литературе.
Все культуры были изучены после инкубации, и все записи результатов делались еженедельно вплоть до 21 суток. В случае необходимости добавлялся NaCl.
Описание микроорганизма представляет собой следующее.
Через 21 сутки наблюдался хороший рост в колониях ISP 2, ISP 6, Bennet и 172 АТСС с ASW. Колонии имели светло-коричневый цвет. В колониях ISP 3, ISP 5, Czapek и ISP 7 с ASW наблюдался худший рост и растворимый пигмент обнаружен не был. Воздушный мицелий не образовывался. Субстратный мицелий был разветвленным. На субстратном мицелии могли образовываться изолированные споры. Споры были удлиненными и редкими. Никаких других образований не наблюдалось.
В колонии ISP-1, как и в других твердых средах, образовывались способные к диффузии коричневые пигменты. Устойчивость к NaCl превышала 5%. Оптимальный для роста диапазон температур составлял от 25° до 35°С. Микроорганизм мог расти на глюкозе, галактозе, рамнозе и ксилозе в качестве единственного источника углерода, однако, рост на фруктозе, рафинозе, м-инозитоле, сахарозе и α-мелибиозе не наблюдался, а на манните и мелезитозе был колеблющимся.
Исследования химического состава микроорганизма показали, что в гидролизате цельных клеток штамма РO13-046 содержится мезо-2,6-диаминопимелиновая кислота.
Сравнение метиловых эфиров жирных кислот штамма РO13-046 с другими подобными штаммами описаны в Таблице 2.
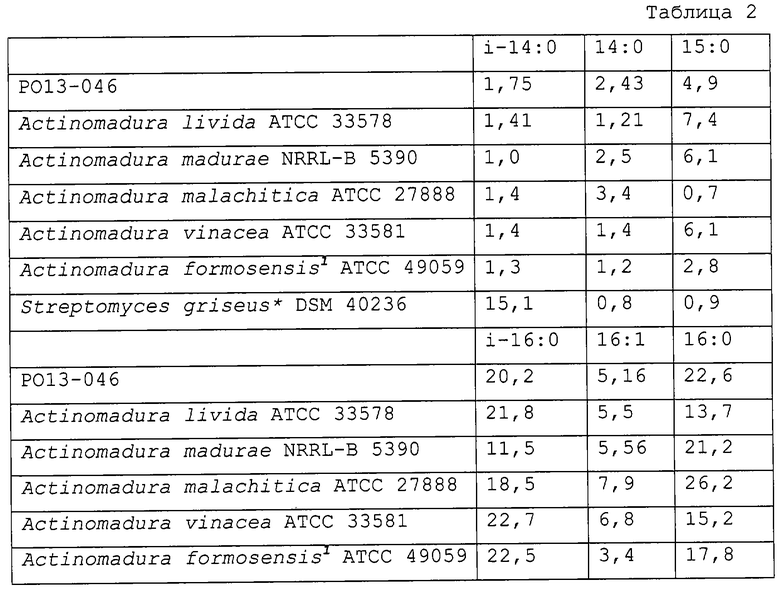
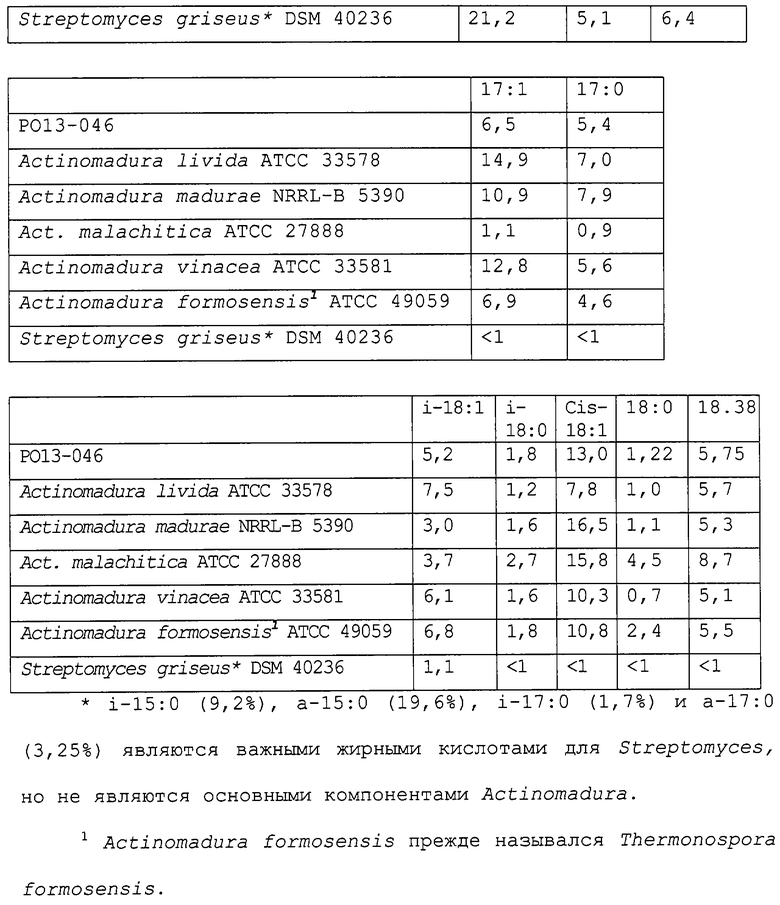
Основываясь на предшествующих характеристиках, культура была определена как вид рода Actinomadura, с 94% идентичностью штамму A. vinacea.
ПРИМЕР 2
Ферментация IB-00208:
Этапами, необходимыми для продуцирования соединения IB-00208 предпочтительным микроорганизмом, являются:
Исходная культура: Полный бульон штамма Р013-046 чистой культуры Actinomadura sp.хранился замороженным в 20% глицерине.
Посевная культура: Замороженную культуру или хорошо растущую культуру на скошенном агаре применяли для засева 100 мл описанной ранее посевной среды в 250 мл встряхиваемой колбе. Колбу инкубировали в течение 48 часов и использовали в качестве посевной культуры первого этапа. 500 мл той же самой среды в двухлитровой колбе Эрленмейера засевали 10% указанной посевной культуры первого этапа. Колбу инкубировали в течение 48 часов.
Ферментация: В 75-литровой емкости для брожения 50 литров уже описанной продукционной среды засевали 2,5 литрами посевной культуры второго этапа. Ферментацию проводили в течение 96 часов при перемешивании со скоростью 400 об/мин при токе воздуха 0,5 об./об.мин.
Выход соединения IB-00208 оценивали путем определения активности в отношении лейкоза мышей Р-388 в полном бульоне или методом ВЭЖХ.
ПРИМЕР 3
Выделение соединения IB-00208.
4,5 литра полного культивируемого бульона фильтровали для отделения биомассы и других твердых веществ. Осадок мицелия дважды экстрагировали 1,5 л смеси растворителей CHCl3:СН3ОН:Н2O (2:1:1), причем активность концентрировалась в нижнем слое. Органический растворитель концентрировали и упаривали досуха в вакууме с получением 1,2 г неочищенного экстракта.
Экстракт разделяли хроматографически на силикагеле, элюируя смесями н-гексана/этилацетата и этилацетата/метанола. 110 мг фракции, содержащей обладающее противоопухолевой активностью соединение IB-00208, элюировали этилацетатом/метанолом (1:1).
Дальнейшую очистку содержащей соединение IB-00208 фракции проводили методом колоночной хроматографии на силикагеле и элюировали хлороформом/метанолом (95:5) 18 мг чистого соединения IB-00208.
Пример 4
Получение Соединения 1:
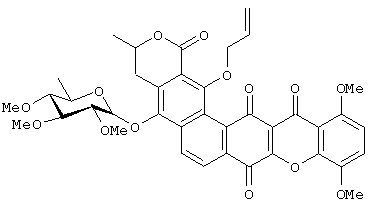
Раствор IB-00208 (150 мг, 0,22 ммоль) в толуоле (15 мл) обрабатывают Ag2O (183 мг, 0,79 ммоль) и аллилбромидом (0,76 мл) при комнатной температуре в атмосфере аргона. Реакционную смесь перемешивают в течение 5 часов при 70°С. После охлаждения до комнатной температуры смесь фильтруют через целит® и промывают дихлорметаном. Растворитель выпаривают при пониженном давлении и остаток очищают флэш-хроматографией (CHCl3:МеОН 10:0,4) с получением соответствующего чистого продукта (выход 34%).
Пример 5.
Получение Соединения 2:
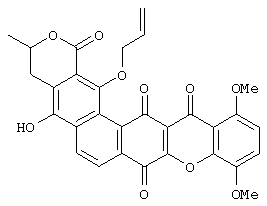
Раствор Соединения 1 (10 мг, 0,014 ммоль) в смеси метанол/дихлорметан 9:1 (3 мл) обрабатывают водным раствором 10 М Н2SO4 (0,5 мл). После охлаждения до комнатной температуры смесь разбавляют СН2Cl2 и добавляют насыщенный водный раствор NaCl. Водную фазу экстрагируют дихлорметаном и сушат над безводным сульфатом натрия. После выпаривания растворителя при пониженном давлении и флэш-хроматографии (CHCl3:МеОН 10:0,4) получают чистое Соединение 2 (выход 30%).
Пример 6.
Получение Соединения 3:
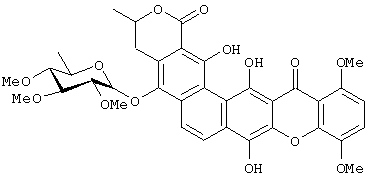
Раствор IB-00208 (50 мг, 0,072 ммоль) в дихлорметане (0,7 мл) обрабатывают палладием на угле (10 мг Pd/C) и перемешивают при комнатной температуре в атмосфере водорода в течение 4 часов. Смесь отфильтровывают и растворитель выпаривают при пониженном давлении. Соответствующий восстановленный продукт с гидрохиноновым фрагментом получают с количественным выходом (100%).
Пример 7.
Получение Соединения 4:
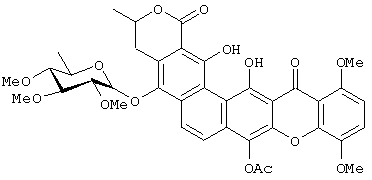
К раствору Соединения 3 (169 мг, 0,24 ммоль) в дихлорметане в атмосфере аргона при 0°С добавляют 0,02 мл пиридина (0,24 ммоль). Реакционную смесь перемешивают при 0°С в течение 1 часа и добавляют 0,2 экв пиридина и 0,2 экв уксусного ангидрида до общего количества, равного 1 экв. Протекание реакции сопровождают ТСХ и далее реакционную смесь выливают в лед. рН регулируют до 1-2 с помощью 1М HCl и реакционную смесь экстрагируют дихлорметаном. Органическую фазу промывают насыщенным водным раствором NaCl и сушат над безводным сульфатом натрия. После выпаривания растворителя при пониженном давлении и флэш-хроматографии получают чистое моноацетилированное соединение Соединение 4 (выход 87%).
Пример 8
Получение Соединения 5:
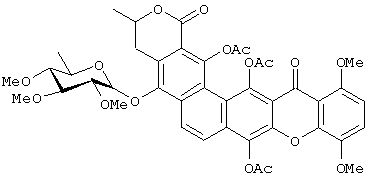
К раствору Соединения 3 (92 мг, 0,133 ммоль) в пиридине в атмосфере аргона при комнатной температуре добавляют 0,4 мл Et3N (2,9 мл) и 0,64 мл уксусного ангидрида (6,78 ммоль).
Реакционную смесь перемешивают при комнатной температуре в течение 1 минуты и далее добавляют дробленый лед. Смесь выливают в раствор 1 М HCl при 0°С и экстрагируют дихлорметаном. Органическую фазу промывают насыщенным водным раствором NaCl и сушат над безводным сульфатом натрия. После выпаривания растворителя при пониженном давлении и флэш-хроматографии получают чистое триацетилированное Соединение 5 (выход 74%).
Пример 9.
Получение Соединения 6:
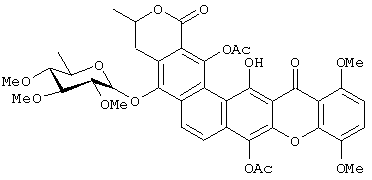
Используют такую же методику, что и описанная выше для Соединения 5. В данном случае реакционную смесь перемешивают в течение 5 минут перед обработкой для получения диацетилированного продукта Соединения 6 в качестве основного соединения.
ПРИМЕР 10
Получение соединения 15 и соединения 16
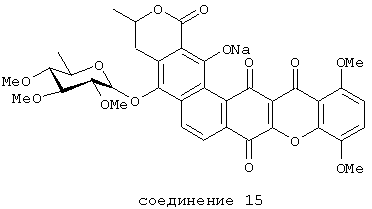
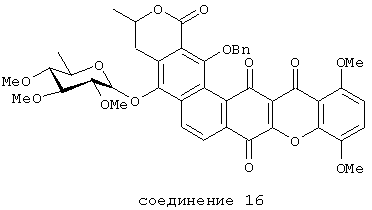
Раствор IB-00208 (18 мг, 0,027 ммол) в ТГФ (1 мл) NaH 60% (1,16 мг, 0,029 ммол) при 0°С в атмосфере аргона. Реакционную смесь перемешивают в течение 5 минут при этой температуре. Раствор становится зеленым, и образуется твердое вещество (натриевая соль, соединение 15).
Затем при 0°С добавляют бензилбромид (3,5 мкл, 0,029 ммол) и йодид тетрабутиламмония (1,1 мг, 0,003 ммол). Охлаждающую баню удаляют и реакционную смесь перемешивают в течение 4 часов. Гашение реакции осуществляют добавлением 0,1 н HCl. Затем смесь экстрагируют дихлорметаном (дважды). Объединенные органические экстракты сушат над безв. Na2SO4, фильтруют и выпаривают растворитель при пониженном давлении. Соединение 16 наблюдают в следовых количествах с помощью 1H-ЯМР сырого продукта.
Получение соединения 16:
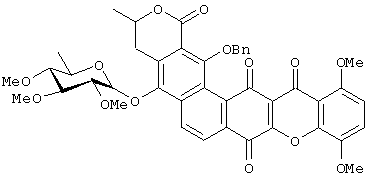
Раствор IB-00208 (18,5 мг, 0,012 ммол) в толуоле (15 мл) обрабатывают Ag2O (12 мг, 0,05 ммол) и бензилбромидом (6 мкл, 0,05 ммол) при комнатной температуре в атмосфере аргона. Реакционную смесь перемешивают в течение 6 часов при 70°С. После охлаждения до компнатной температуры, смесь фильтруют через целит® и промывают дихлорметаном. Растворитель выпаривают при пониженном давлении и остаток очищают флэш-хроматографией (СН2Cl2:МеОН 100:1) с получением чистого соединения 15 (5 мг, выход 52%) в виде оранжевого твердого вещества.
ПРИМЕР 11
Биологическая активность.
Противоопухолевую активность соединения IB-00208 определяли in vitro в культурах клеток лейкоза мышей Р-388, карциномы легких человека А-549, карциномы толстой кишки человека НТ-29 и меланомы человека MEL-28. Процедуру выполняли по методике, описанной в Bergeron et al. Было показано, что значение IC50 для всех 4 клеточных линий клеток составляло 0,001, 0,001, 0,001 и 0,001 мкг/мл, соответственно. Аналогичные результаты были получены по той же методике для соединений 1-6.
ССЫЛКИ
В описание настоящего изобретения включены следующие ссылки:
АТСС Catalog 1996;
Bergeron et al., Biochem. Biophys. Res. Comm., 121: 848, 1984;
Guerrant and Moss, Anal. Chem., 56: 633, 1984;
Hasegawa et al., J. Gen. Appl. Microbiol., 29: 319, 1983;
Shirling and Gotlieb, Int. J. Syst. Bacterial., 16: 313, 1966;
Van der Auwera et al., J. Microbiol. Methods, 4: 265, 1986;
Waksman, The Actinomycetes, vol.II: 331, 1961.
Настоящее изобретение было описано подробно, включая его предпочтительные воплощения. Однако понятно, что специалист в данной области на основании описания настоящего изобретения может вносить изменения и/или усовершенствования, не выходящие за рамки настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДЫ С БОЛЬШИМ ЧИСЛОМ МОСТИКОВЫХ СВЯЗЕЙ, ВЫДЕЛЯЕМЫЕ ИЗ ACTINOMADURA NAMIBIENSIS | 2009 |
|
RU2498995C2 |
| ПРОТИВООПУХОЛЕВЫЙ АНТИБИОТИК ВМУ-46164 И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2089614C1 |
| ПРОТИВОВИРУСНОЕ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО | 2004 |
|
RU2350600C2 |
| ГЕКСАГИДРОНАФТАЛИНОВЫЕ СЛОЖНОЭФИРНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2104997C1 |
| АНТИБАКТЕРИАЛЬНЫЕ ПЕПТИДЫ ИЗ ACTINOMADURA NAMIBIENSIS | 2007 |
|
RU2451028C2 |
| Способ получения полиэфирного антибиотика А 80190 | 1985 |
|
SU1531861A3 |
| НОВЫЕ АНТИБАКТЕРИАЛЬНЫЕ СОЕДИНЕНИЯ | 2007 |
|
RU2444526C2 |
| 42-ОКСИМЫ И ГИДРОКСИЛАМИНЫ РАПАМИЦИНА, СПОСОБ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЙ ПРОДУКТ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ | 1995 |
|
RU2172316C2 |
| ПРОИЗВОДНЫЕ АРТЕМИЗИНИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 1999 |
|
RU2236413C2 |
| ПРОИЗВОДНЫЕ ОКТАГИДРОНАФТАЛИНОКСИМА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2125043C1 |
Настоящее изобретение относится к новому классу противоопухолевых соединений, обнаруженному при выделении из новых, принадлежащих к роду Actinomadura sp., морских микроорганизмов штамма РО13-046, а именно к соединению, обозначенному как IB-00208
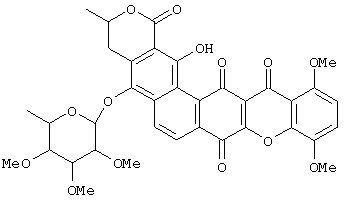
к классу соединений формулы (I) или (II):
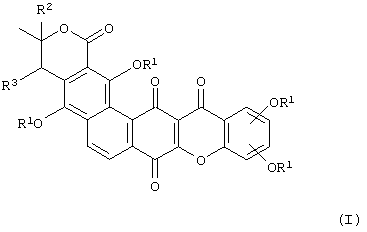
или
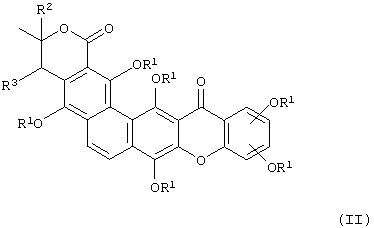
где каждый заместитель R1 является одинаковым или различным и может представлять собой водород, ацил, алкил, алкенил, арил, бензил, щелочной металл и/или моносахарид, дисахарид, трисахарид или их производное, а R2 и R3 могут представлять собой водород или алкил. Указанные соединения обладают противоопухолевой активностью. 5 н. и 3 з.п. ф-лы, 3 табл., 9 ил.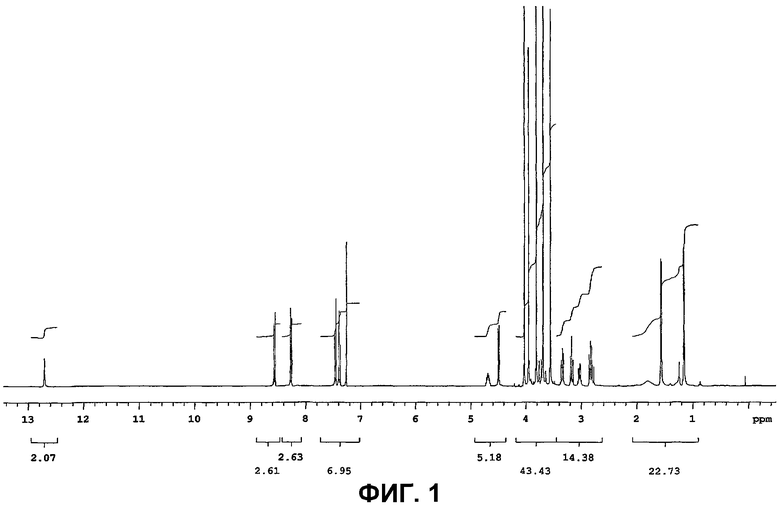
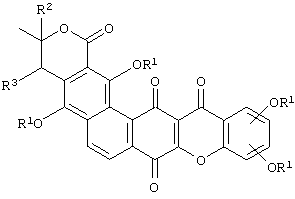
или
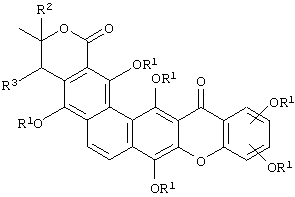
где каждый заместитель R1 является одинаковым или различным и может представлять собой водород, ацил, алкил, алкенил, арил, бензил, щелочной металл и/или моносахарид, дисахарид, трисахарид или их производное, a R2 и R3 могут представлять собой водород или алкил.
| ЕР 0 405 151 A1, 02.01.1991 | |||
| Термос с дополнительным подогревом | 1925 |
|
SU4814A1 |
| Станок для изготовления валяной обуви | 1922 |
|
SU1344A1 |
Авторы
Даты
2006-10-10—Публикация
2001-06-29—Подача