Область изобретения
Настоящее изобретение относится к производному бензофурана, которое может найти применение в качестве лекарственного средства, особенно в качестве ингибитора активированного фактора Х коагуляции крови или его фармацевтически приемлемой соли.
Уровень техники
В последние годы по мере вестернизации жизненных привычек и старения населения, год от года увеличивается количество тромбоэмболических заболеваний, таких как инфаркт миокарда, церебральный инфаркт и периферический артериальный тромбоз, поэтому и социальная важность лечения таких заболеваний все более повышается.
Среди методов терапии тромбоэмболических болезней антикоагулирующая терапия, так же как фибринолитическая терапия и антитромбоцитная терапия, включаются в медицинскую терапию для лечения и профилактики тромбоза (Sogorinsho 41: 2141-2145, 1989). В частности, существенными для предотвращения тромбоза являются постоянная безопасность при длительном введении и надежная, а также адекватная экспрессия антикоагулирующей активности. Во всем мире часто используют производное кумарина, особенно варфарин калия, в качестве только антикоагулирующего средства, доступного перорально. Однако, основываясь на характеристиках, являющихся результатом механизма действия, требуется длительное время для проявления эффективности этого лекарственного средства, поскольку он имеет очень длинный период полужизни в крови, хотя диапазон концентрации для проявления эффективности лекарственного средства является относительно узким, и при этом демонстрирует значительные различия в отношении эффективной дозы среди индивидуумов. По этим причинам способность антикоагулирующего средства может контролироваться с трудом (Journal of Clinical Pharmacology, 1992, vol.32, pp.196-209; NEW ENGLAND JOURNAL OF MEDICINE, 1991, vol.324, no.26, pp.1865-1875). Кроме того, могут быть неблагоприятные побочные эффекты у лекарственного средства, такие как риск кровотечения, тошнота, рвота, понос, выпадение волос, и т.д., и поэтому клиническое применение его очень затруднено и требуется организация поиска антикоагулирующих средств, которые являются полезными и легко переносятся.
Кроме того, повышение способности к свертыванию крови представляет собой один из значительных причинных факторов нестабильной ангины, церебрального инфаркта, мозговой эмболии, инфаркта миокарда, легочного инфаркта, легочной эмболии, болезни Бюргера, глубокого венозного тромбоза, диссеминированного внутрисосудистого свертывания, тромбогенеза после смещения искусственного клапана сердца, переокклюзии после реконструкции кровообращения и тромбогенеза во время искусственного кровообращения, и т.д. Поэтому была бы желательна разработка действенного антикоагулирующего средства, которое быстро действует после введенной дозы и имеет более низкий риск вызова кровотечения с немногими побочными эффектами, при этом могло бы быть достаточно эффективным при пероральном приеме (Thrombosis Research, 1992, vol.68, pp.507-512). Тромбин участвует не только в преобразовании фибриногена в фибрин, который является заключительной стадией каскада процесса коагуляции, но также и в основном в активации и аггрегации тромбоцитов в крови (Matsuo, О., "t-PA и Pro-UK", Gakusaikikaku, 1986, pp.5-40), и его ингибитор в течение длительного времени находился в центре поиска антикоагулянтов при разработке новых препаратов. Однако ингибитор тромбина демонстрирует низкую биопригодность при пероральном приеме и также имеет недостатки в отношении безопасности, такие, как тенденцию к кровотечению, как одного из побочных эффектов (Biomedica Biochimica Acta, 1985, Vol.44, р.1201-1210), при этом ранее не было известно никаких доступных ингибиторов тромбина, которые могли бы вводиться перорально.
Активированный фактор Х коагуляции крови представляет собой ключевой фермент, локализованный в позиции, находящейся на общем направлении обеих - как внешней, так и внутренней реакции каскада коагуляции. Фактор Ха локализован выше по течению относительно тромбина в каскаде коагуляции. Поэтому ингибирование фактора Ха является, возможно, более эффективным и специфичным при ингибировании системы коагуляции по сравнению с ингибированием тромбина (Thrombosis Research, 1980, Vol.19, pp.339-349).
Таким образом, среди ингибиторов активированного фактора Х коагуляции крови вещество, которое ингибирует фактор Ха коагуляции крови и демонстрирует отличную ферментативную селективность, а также высокую биодоступность, как ожидается, обеспечит контролирование его антикоагулирующей активности в течение длительного периода времени и позволит достичь более высокого терапевтического эффекта при пероральном приеме по сравнению с существующими антикоагулянтами. Соответственно настоятельно требуется проведение поиска нового ингибитора активированного фактора Х коагуляции крови (ингибитор FXa), который может вводиться перорально.
Примеры известных соединений, оказывающих ингибирующее действие на активированный фактор Х коагуляции крови, включают производные тиобензамида, которые являются полезными в профилактике или лечении тромбоза (WO 99/42439).
Следующие производные бензофурана были также известны (Indian Journal of Heterocyclic Chemistry, 1994, Vol.3, pp.3247-3252), но указанный источник не упоминает об ингибирующем действии соединений на активированный фактор Х коагуляции крови.
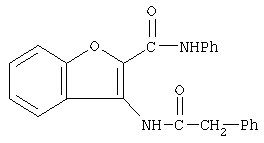
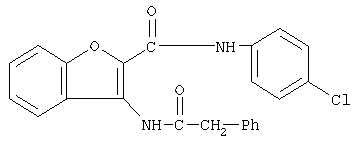
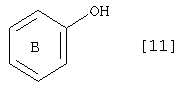
Также известны конденсированные бициклические амидные соединения формулы:
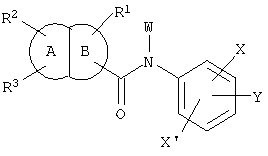
которые имеют активность, заключающуюся в подавлении роста активированных лимфоцитов и полезны в качестве лекарственного средства для профилактики или лечения аутоиммунных заболеваний (WO 02/12189). В WO 02/12189 при этом не упоминается об ингибирующем действии на активированный фактор Х коагуляции крови. В брошюре раскрыты соединения, имеющие конденсированные кольца пиридина и фурана, где амидная и карбамоильная группы являются дизамещенными; однако все указанные соединения имеют бензольное кольцо по атому азота карбамоильной группы и указанное бензольное кольцо является замещенным по Х и Y одновременно.
Сущность изобретения
Настоящее изобретение обеспечивает новое производное бензофурана, обладающее превосходным ингибирующим воздействием на активированный фактор Х коагуляции крови, или его фармацевтически приемлемые соли.
Было изучено и найдено, что производное бензофурана формулы, представленной ниже, оказывает сильное ингибирующее действие на активированный фактор Х коагуляции крови, что решает задачу настоящего изобретения.
То есть настоящее изобретение представляет собой следующее:
(i) Производное бензофурана формулы [1]:
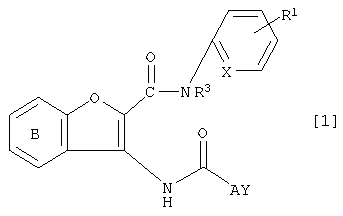
где Х представляет собой группу формулы: 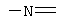 или формулы:
или формулы: 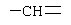 ;
;
Y представляет собой необязательно замещенную аминогруппу, необязательно замещенную циклоалкильную группу или необязательно замещенную насыщенную гетероциклическую группу;
А представляет собой простую связь, углеродную цепь, необязательно имеющую двойную связь внутри или на конце(ах) цепи или атом кислорода;
R1 представляет собой атом водорода, атом галогена, низшую алкильную группу, низшую алкоксигруппу, цианогруппу или аминогруппу, необязательно замещенную с помощью низшей алкильной группы;
Кольцо В формулы:
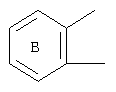
представляет собой необязательно замещенное бензольное кольцо; и
R3 представляет собой атом водорода или низшую алкильную группу,
или его фармацевтически приемлемая соль.
(ii) Соединение в соответствии с (i), где кольцо В представляет собой бензольное кольцо, необязательно замещенное группой(ами), независимо выбранной из атома галогена, необязательно замещенной низшей алкильной группы, гидроксигруппы, необязательно замещенной низшей алкоксигруппы, оксигруппы, замещенной необязательно замещенной насыщенной гетероциклической группой, замещенной карбонильной группы, необязательно замещенной аминогруппы, нитрогруппы, цианогруппы, 4,5-дигидроксазолильной группы или группы формулы:
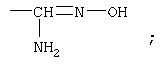 и
и
"необязательно замещенная циклоалкильная группа" для Y представляет собой циклоалкильную группу, необязательно замещенную с помощью группы, выбранной из необязательно замещенной аминогруппы, необязательно замещенной группы формул, выбранных из:
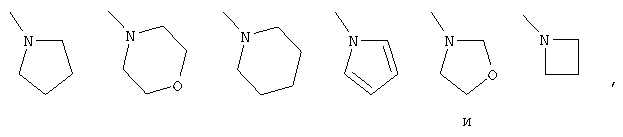
и необязательно замещенной низшей алкильной группы.
(iii) Соединение в соответствии с (ii), где "необязательно замещенная насыщенная гетероциклическая групп" для Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из следующих:
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидильной группы, 4,5-дигидроксазолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы, и
(13) оксогруппы:
"необязательно замещенная аминогруппа" для Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из следующих:
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы, и
(3) низшей алкоксикарбонильной группы;
"необязательно замещенная аминогруппа" в качестве заместителя на циклоалкильной группе для Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из следующих:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксильной группы, и
(23) гидрокси-низшей алканоильной группы;
"необязательно замещенная группа формулы, выбранная из:
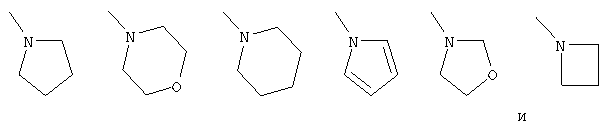
в качестве заместителя на циклоалкильной группе для Y является группа, выбранная из:
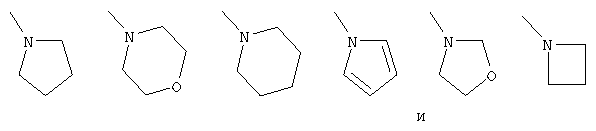
которая является необязательно замещенной с помощью оксогруппы;
"необязательно, замещенная низшая алкильная группа" в качестве заместителя на циклоалкильной группе для Y представляет собой низшую алкильную группу, необязательно замещенную с помощью группы, выбранной из следующих групп:
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы, и
(3) аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы;
"необязательно замещенная низшая алкильная группа" в качестве заместителя для кольца В представляет собой низшую алкильную группу, необязательно замещенную с помощью группы, выбранной из:
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной с помощью пиперидильной группы и
(8) гидроксильной группы;
"необязательно замещенная низшая алкоксигруппа" в качестве заместителя для кольца В представляет собой низшую алкоксигруппу, необязательно замещенную с помощью группы, выбранной из:
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы: 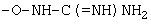 ;
;
"оксигруппа, замещенная необязательно замещенной с помощью насыщенной гетероциклической группы" в качестве заместителя для кольца В представляет собой оксигруппу, замещенную гетероциклической группы, необязательно замещенной с помощью арильной группы;
"замещенная карбонильная группа" в качестве заместителя для кольца В представляет собой карбонильную группу, замещенную с помощью группы, выбранной из:
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы и
(8) низшей алкилпиперазинильной группы;
"необязательно замещенная аминогруппа" в качестве заместителя для кольца В представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из:
(1) низшей алкильной группы,
(2) низшей алкокси-низшей алкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) низшей алканоильной группы,
(5) низшей алкокси-низшей алканоильной группы,
(6) гидрокси-низшей алканоильной группы,
(7) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(8) низшей алканоильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) низшей алканоильной группы,
(9) низшей алкоксикарбонильной группы,
(10) низшей алкоксикарбонильной группы, замещенной с помощью арильной группы,
(11) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(12) низшей алкилсульфонильной группы и
(13) низшей алкилсульфонильной группы, замещенной с помощью морфолинильной группы.
(iv) Соединение в соответствии с (iii), где В представляет собой ненасыщенное бензольное кольцо; и
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из:
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксазолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы и
(13) оксогруппы.
(v) Соединение в соответствии с (iii), где В представляет собой ненасыщенное бензольное кольцо; и
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из:
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
(vi) Соединение в соответствии с (iii), где В представляет собой ненасыщенное бензольное кольцо; и
Y представляет собой циклоалкильную группу, необязательно замещенную следующими группами:
А) аминогруппой, необязательно замещенной с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы и
(23) гидрокси-низшей алканоильной группы;
В) группой формулы, выбранной из структуры:
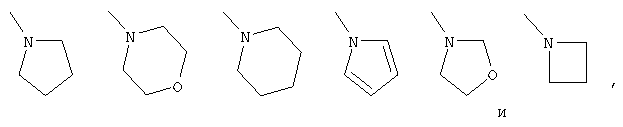
которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группой, необязательно замещенной группой, выбранной из:
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
(vii) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из:
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной с помощью пиперидильной группы и
(8) гидроксильной группы; и
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из:
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксаолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы и
(13) оксогруппы.
(viii) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из:
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной с помощью пиперидильной группы и
(8) гидроксильной группы; и
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из:
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
(ix) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из:
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной пиперидильной группы и
(8) гидроксильной группы; и
Y представляет собой циклоалкильную группу, необязательно замещенную с помощью следующих групп:
А) аминогруппы, необязательно замещенной с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы и
(23) гидрокси-низшей алканоильной группы;
В) группы формулы, выбранной из структуры:
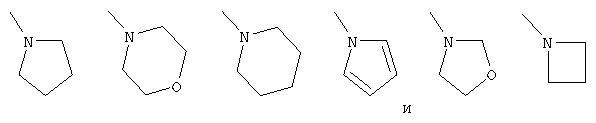
которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из следующих групп:
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
(х) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью низшей алкоксигруппы, необязательно замещенной с помощью группы, выбранной из:
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы: 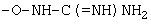 ; и
; и
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из:
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксаолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы и
(13) оксогруппы.
(xi) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью низшей алкоксигруппы, необязательно замещенной с помощью группы, выбранной из:
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы: 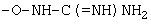 ; и
; и
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из:
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
(xii) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью низшей алкоксигруппы, необязательно замещенной с помощью группы, выбранной из:
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы: 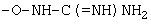 ; и
; и
Y представляет собой циклоалкильную группу, необязательно замещенную с помощью следующих групп:
А) аминогруппы, необязательно замещенной с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы и
(23) гидрокси-низшей алканоильной группы;
В) группы формулы, выбранной из структуры:
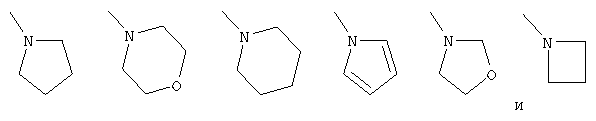
которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из:
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
(xiii) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенной с помощью карбонильной группы, замещенной с помощью группы, выбранной из:
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы и
(8) низшей алкил-пиперазинильной группы; и
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из:
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксаолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы и
(13) оксогруппы.
(xiv) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью карбонильной группы, замещенной с помощью группы, выбранной из:
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы и
(8) низшей алкил-пиперазинильной группы; и
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из:
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
(xv) Соединение в соответствии с (iii), где кольцо В представляет собой бензольное кольцо, замещенное с помощью карбонильной группы, замещенной с помощью группы, выбранной из:
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы, и
(8) низшей алкилпиперазинильной группы; и
Y представляет собой циклоалкильную группу, необязательно замещенную с помощью следующих групп:
А) аминогруппы, необязательно замещенной с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы и
(23) гидрокси-низшей алканоильной группы;
В) группы формулы, выбранной из структуры:
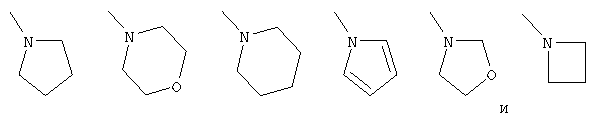
которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из:
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
(xvi) Соединение в соответствии с (i), (ii), (iii), (iv), (vii), (x) или (xiii), где насыщенное гетероциклическое кольцо представляет собой насыщенную 4-7-членную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из атома азота, кислорода и серы.
(xvii) Соединение в соответствии с (i), (ii), (iii), (iv), (vii), (x) или (xiii), где насыщенная гетероциклическая группа представляет собой имидазолидинил, пиперазолидинил, пиперидил, пиперазинил, морфолинил, тиоморфолинил, гомопиперазинил, гомопиперидил, пирролидинил, оксазолидинил или 1,3-диоксанил.
(xviii) Соединение в соответствии с (iii), где группа формулы:
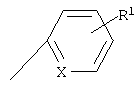
представляет собой группу формулы:
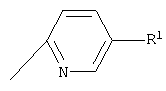
и группа формулы:

представляет собой группу формулы:
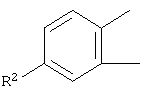 или
или 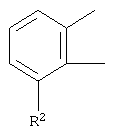
R1 представляет собой атом галогена или низшую алкильную группу;
R2 представляет собой группу, выбранную из следующих групп:
A) атом водорода,
B) низшая алкильная группа, необязательно замещенная с помощью группы, выбранной из:
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной пиперидильной группы и
(8) гидроксильной группы;
C) низшая алкоксигруппа, необязательно замещенная с помощью группы, выбранной из:
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы и
(14) группы формулы: 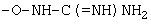 ; или
; или
D) карбонильная группа, замещенная с помощью группы, выбранной из:
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы и
(8) низшей алкил-пиперазинильной группы;
А представляет собой простую связь; и
R3 представляет собой атом водорода.
(xix) Соединение в соответствии с (xviii), где Y представляет собой группу, выбранную из следующих групп:
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) циклоалкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(3) циклоалкильной группы, замещенной с помощью группы формул, выбранных из структуры:
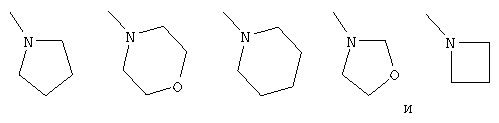
которая является необязательно замещенной с помощью оксогруппы,
(4) циклоалкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алканоильной группы и (b) низшей алкоксикарбонильной группы и
(5) циклоалкильной группы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы; и
R2 представляет собой группу, выбранную из:
(1) атома водорода,
(2) цианогруппы,
(3) аминогруппы, необязательно замещенной с помощью низшей алкильной группы,
(4) гидроксильной группы,
(5) низшей алкоксигруппы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) низшей алкоксигруппы, замещенной с помощью гидроксильной группы,
(8) низшей алкоксигруппы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы,
(9) низшей алкоксикарбонильной группы,
(10) карбоксильной группы,
(11) аминокарбонильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, и (b) гидрокси-низшей алкильной группы,
(12) морфолинилкарбонильной группы, пирролидинилкарбонильной группы, пиперидилкарбонильной группы или тиоморфолинилкарбонильной группы,
(13) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы или пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(14) низшей алкильной группы,
(15) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(16) карбокси-низшей алкильной группы,
(17) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) гидрокси-низшей алкильной группы,
(18) низшей алкильной группы, замещенной с помощью морфолинилкарбонильной группы,
(19) низшей алкильной группы, замещенной с помощью пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы или низшей алкильной группы, замещенной с помощью пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы или
(20) гидрокси-низшей алкильной группы.
(хх) Соединение в соответствии с (xviii), где Y представляет собой циклоалкильную группу, замещенную с помощью группы формул, выбранных из структуры:
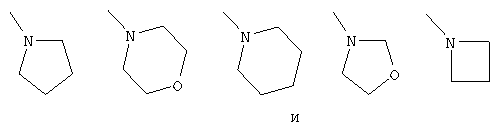
которая является необязательно замещенной с помощью оксогруппы или циклоалкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) низшей алканоильной группы; и R2 представляет собой группу, выбранную из:
(1) атома водорода,
(2) аминогруппы замещенной карбонильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) низшей алкокси-низшей алкильной группы,
(3) низшей алкоксикарбонильной группы,
(4) морфолинилкарбонильной группы, пирролидинилкарбонильной группы, пиперидилкарбонильной группы или тиоморфолинилкарбонильной группы,
(5) низшей алкильной группы, замещенной с помощью низшей алкильной группы, замещенной карбамоильной группы,
(6) карбокси-низшей алкильной группы,
(7) низшей алкильной группы, замещенной с помощью морфолинилкарбонильной группы и
(8) гидрокси-низшей алкильной группы.
(xxi) Соединение в соответствии с (xviii), где Y представляет собой циклоалкильную группу, замещенную с помощью оксопирролидинильной группы, циклоалкильную группу, замещенную с помощью оксоморфолинильной группы или циклоалкильную группу, замещенную с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) низшей алканоильной группы; и
R2 представляет собой группу, выбранную из:
(1) атома водорода,
(2) гидрокси-низшей алкильной группы,
(3) карбокси-низшей алкильной группы,
(4) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы или
(5) карбонильной группы, замещенной с помощью группы, выбранной из (а) аминогруппы, необязательно замещенной с помощью низшей алкильной группы и (b) морфолинильной группы.
(xxii) Соединение в соответствии с (xviii), где Y представляет собой группу, выбранную из:
(1) циклоалкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, имеющей от 1 до 3 атомов углерода,
(2) циклоалкильной группы, замещенной с помощью аминогруппы, замещенный с помощью низшей алканоильной группы, имеющей от 1 до 2 атомов углерода,
(3) циклоалкильной группы, замещенной с помощью пирролидин-1-ильной группы, необязательно замещенной с помощью оксогруппы,
(4) циклоалкильной группы, замещенной с помощью пиперидин-1-ильной группы, необязательно замещенной с помощью оксогруппы,
(5) циклоалкильной группы, замещенной с помощью морфолин-4-ильной группы, необязательно замещенной с помощью оксогруппы,
(6) циклоалкильной группы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, имеющей от 1 до 3 атомов углерода или
(7) циклоалкильной группы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алканоильной группы, имеющей от 1 до 2 атомов углерода.
(xxiii) Соединение выбрано из
транс-5-диметиламинокарбонил-3-[4-(N-формил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида;
транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-(2-гидроксиэтил)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида;
транс-5-(морфлин-4-илкарбонил)-3-[4-(2-оксо-пирроридин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида; и
транс-3-(4-диметиламиноциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида или его фармацевтически приемлемой соли.
(xxiv) Производное бензофурана, имеющее частичную структуру в виде формулы [1-1]:
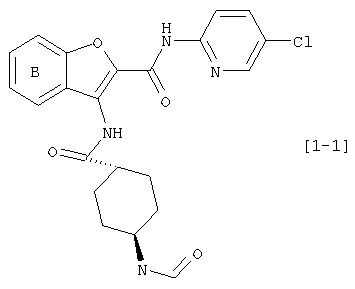
где символы являются теми же самыми как определено выше, или его фармацевтически приемлемая соль.
(xxv) Производное бензофурана формулы [2]:
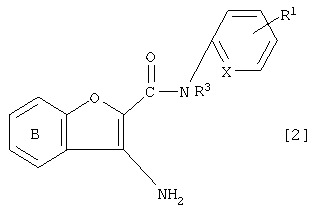
где символы являются теми же самыми, как определено выше, или его соль.
(xxvi) Фармацевтическая композиция, которая содержит в качестве активного ингредиента соединение в соответствии с любым одним пунктом от (i) до (xxiv), указанном выше или его фармацевтически приемлемую соль.
(xxvii) Способ лечения тромбоза, который включает введение эффективного количества соединения в соответствии с любым одним пунктом от (i) до (xxiv), указанном выше или его фармацевтически приемлемой соли, пациенту, нуждающемуся в этом.
(xxviii) Применение соединений в соответствии с любым одним пунктом от (i) до (xxiv), указанном выше или его фармацевтически приемлемой соли при лечении пациентов, страдающих от тромбоза.
(xxix) Лекарственное средство для лечения тромбоза, существенно снижающее фосфолипидоз, содержащее в качестве активного ингредиента ингибитор фактора Ха (FXa), демонстрирующее величину распределения от 0,1-3,0 л/кг и ингибирующий эффект FXa с величиной IC50 от 100 нМ или ниже.
(ххх) Лекарственное средство для лечения тромбоза, по существу не обладающее гепатотоксичностью, которое содержит в качестве активного ингредиента ингибитор FXa, имеющее величину распределения от 0,1-3,0 л/кг или ниже и ингибирующий эффект FXa с величиной IC50 от 100 нМ или ниже.
(xxxi) Лекарственное средство для орального введения при лечении тромбоза, существенно снижающее фосфолипидоз, который содержит в качестве активного ингредиента ингибитор Ха фактора (FXa), имеющее величину распределения от 0,1-3,0 л/кг и ингибирующий эффект FXa с величиной IC50 от 100 нМ или ниже.
(xxxii) Лекарственное средство для орального введения при лечении тромбоза, по существу не обладающее гепатотоксичностью, которое содержит в качестве активного ингредиента ингибитор FXa, имеющее величину распределения от 0,1-3,0 л/кг или ниже и ингибирующий эффект FXa с величиной IC50 от 100 нМ или ниже.
(xxxiii) Лекарственное средство для лечения тромбоза, существенно снижающее фосфолипидоз, которое содержит в качестве активного ингредиента ингибитор FXa, имеющий частичную структуру формулы:
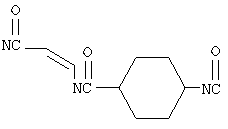
и имеющее величину распределения от 0,1-3,0 л/кг и ингибирующий эффект FXa с величиной IC50 от 100 нМ или ниже.
(xxxiv) Лекарственное средство для лечения тромбоза, по существу не обладающее гепатотоксичностью, которое содержит в качестве активного ингредиента ингибитор FXa, имеющий частичную структуру формулы:

и имеющий величину распределения от 0,1-3,0 л/кг и ингибирующий эффект FXa со значением IC50 от 100 нМ или ниже.
(xxxv) Лекарственное средство для орального введения при лечении тромбоза, существенно снижающее фосфолипидоз, которое содержит в качестве активного ингредиента ингибитор FXa, имеющий частичную структуру формулы:

и имеющий величину распределения от 0,1-3,0 л/кг и ингибирующий эффект FXa со значением IC50 от 100 нМ или ниже.
(xxxvi) Лекарственное средство для орального введения при лечении тромбоза, по существу не обладающее гепатоксичностью, которое содержит в качестве активного ингредиента ингибитор FXa, имеющий частичную структуру формулы:

и имеющий величину распределения от 0,1-3,0 л/кг и ингибирующий эффект FXa с величиной IC50 от 100 нМ или ниже.
Предпочтительный способ осуществления изобретения
Далее соединение [1] настоящего изобретения рассмотрено более подробно.
Термин "низший", используемый в определениях формул в настоящем изобретении, подразумевает, если иное не отмечено, прямую или разветвленную углеродную цепь, имеющую от 1 до 6 атомов углерода.
Соответственно примеры "низшей алкильной группы" включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, неопентил, трет-пентил, 1-метилбутил, 2-метилбутил, 1,2-диметилпропил, гексил, изогексил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 2,2-диметилбутил, 1,3-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил, 1-этил-2-метилпропил и так далее. Среди них алкильные группы, имеющие от 1 до 4 атомов углерода, являются предпочтительными, а метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил и трет-бутил являются особенно предпочтительными.
Термин "низшая алкоксигруппа" означает заместитель, в котором атом кислорода присоединен к упомянутой выше алкильной группе. Среди них алкокси группы, имеющие от 1 до 4 атомов углерода, являются предпочтительными, а метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси и трет-бутокси группы, являются особенно предпочтительными.
Примеры "углеродной цепи, необязательно имеющей двойную связь внутри или на конце(ах) цепи" включают "низшую алкиленовую группу", "низшую алкениленовую группу" и "низшую алкенилиденовую группу".
Примеры "низшей алкиленовой группы" включают прямую или разветвленную цепь алкиленовой группы, имеющей от 1 до 6 атомов углерода, в особенности метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен и так далее. Среди них алкиленовая группа, имеющая от 1 до 5 атомов углерода, является предпочтительной.
Примеры "низшей алкениленовой группы" включают прямую или разветвленную цепь алкениленовой группы, имеющей от 2 до 6 атомов углерода, в особенности винилен, пропенилен, бутенилен, пентенилен и так далее. Среди них алкениленовая группа, имеющая от 2 до 5 атомов углерода, является предпочтительной.
Примеры "низшей алкенилиденовой группы" включают алкенилидены, имеющие от 2 до 6 атомов углерода, в особенности винилиден, пропенилиден, бутенилиден, пентенилиден, и так далее.
Примеры "низшей алканоильной группы" включают алканоильные группы, образованные путем удаления "ОН" группы из карбоксильной группы низшей карбоновой кислоты, в особенности, формил, ацетил, пропионил, бутирил, и так далее.
Термин "насыщенная гетероциклическая группа" означает насыщенную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из атома азота, кислорода и серы, предпочтительно 4-7-членную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из атома азота, атома кислорода и атома серы. Конденсируемое гетероциклическое кольцо включено. Конкретные примеры включают имидазолидинил, пиразолидинил, пиперидил, пиперазинил, морфолинил, тиоморфолинил, гомопиперазинил, гомопиперидил, пирролидинил, оксазолидинил, 1,3-диоксанил, и так далее. Среди всех пиперидил, пиперазинил, гомопиперазинил и пирролидинил являются предпочтительными.
Термин "ненасыщенная гетероциклическая группа" означает ненасыщенную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из атома азота, кислорода и серы, предпочтительно 4-7-членную гетероциклическую группу, содержащую от 1 до 4 гетероатомов, независимо выбранных из группы, состоящей из атома азота, кислорода и серы. Конденсируемое гетероциклическое кольцо включено. Конкретные примеры включают пиридил, пиримидинил, пиразинил, фурил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, 4,5-дигидрооксазолил, тиазолил, изотиазолил и так далее. Среди всех пиридил, пиримидинил, пиразинил, тиенил, оксазолил, 4,5-дигидро-оксазолил и тиазолил являются предпочтительными.
Примеры "атома галогена " включают атом фтора, хлора, брома или иода. Среди всех атом фтора, хлора или брома, которые являются предпочтительными.
Термин "циклоалкильная группа" означает циклическую низшую алкильную группу, предпочтительно циклогексильную группу.
Термин "арильная группа" означает фенильную или нафтильную группу, предпочтительно фенильную группу.
Символ "Y", когда А и Y связаны через двойную связь, относится к соответствующей двухвалентной группе.
Фармацевтически приемлемая соль соединения [1] включает соль с неорганической кислотой, такой как соляная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и так далее; соль с органической кислотой, такой как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, винная кислота, лимонная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота и т.д.; соль с кислой аминокислотой, такой как аспарагиновая кислота, глутаминовая кислота и так далее; соль с металлом, такими как натрий, калий, магний, кальций, алюминий и так далее; соль с органическим основанием, таким как метиламин, этиламин, этаноламин и так далее; или соль с основной аминокислотой, такой как лизин, орнитин и так далее.
Соединение [1] настоящего изобретения может быть в виде четвертичной соли аммония, и такие четвертичные соли аммония находятся внутри границ настоящего соединения [1].
Более того, соединение [1] настоящего изобретения включает внутримолекулярную соль, гидрат, сольват или кристаллический полиморфизм, и так далее.
Кроме того, когда соединение [1] имеет двойную связь(и), оно может существовать в виде геометрического изомера (цис, транс), когда соединение [1] имеет ненасыщенную связь, такую как карбонил, он может существовать в виде таутомеров, когда соединение [1] имеет асимметричный атом(ы) углерода, оно может существовать в виде оптического изомера, и настоящее изобретение охватывает все эти изомеры и их смеси.
Кроме того, соединение [1] настоящего изобретения охватывает пролекарства соединений, как упомянуто выше. Примеры пролекарств включают те, которые получают путем защиты функциональной группы, такой как амино или карбоксигруппы соединений, с помощью обычной защитной группой.
Соединение настоящего изобретения могут быть получены с помощью следующих процессов.
[Процесс А]
Среди соединений [1] настоящего изобретения соединение, где А представляет собой простую связь или углеродную цепь, необязательно имеющую двойную связь внутри или на конце(ах) цепи, то есть соединение, которое имеет формулу [1-А]:
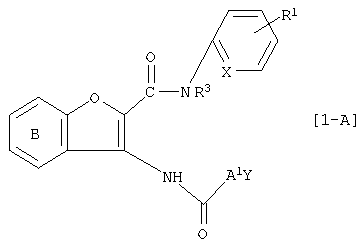
где А1 представляет собой простую связь или углеродную цепь, необязательно имеющую двойную связь внутри или на конце(ах) цепи, и другие символы являются теми же самыми, как определено выше, может быть получено с помощью реакции аминосоединения, имеющего формулу [2]:
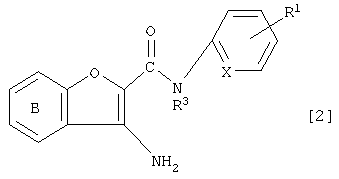
где символы являются теми же самыми как определено выше, с соединением карбоновой кислоты, имеющей формулу [3-А]:
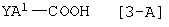
где значения символов являются теми же самыми как определено выше, или его реакционноспособное производное по карбоксильной группе.
[Процесс В]
Среди соединений [1] настоящего изобретения соединение, где А представляет собой атом кислорода или А представляет собой простую связь и Y представляет собой необязательно замещенную аминогруппу, то есть соединение, которое имеет формулу [1-В]:
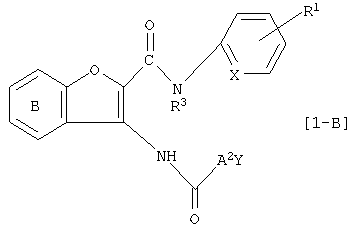
где А представляет собой атом кислорода и другие символы имеют те же самые значения, как определено выше или, когда А2 представляет собой простую связь и другие символы имеют те же самые значения, как определено выше, оно может быть получено с помощью реакции соединения [2] указанного выше с соединением, которое имеет формулу [3-В1]:

где символы имеют те же самые значения, как определено выше, и с соединением, которое имеет формулу [3-В2]:
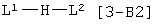
где L1 и L2 имеют те же самые значения или различными и каждая группа - уходящая.
Соединение [1] может также получено, если необходимо, посредством общего преобразования, когда остаток Y и/или заместитель кольца В (R2) полученного соединения [1-А] или [1-В] адекватно превращают в соединение [1] посредством общего преобразования путем алкилирования, восстановительного алкилирования, амидирования, сульфониламидирования, амидиноэтерификации, арилирования, восстановления, деалкилирования, гидролиза, четвертичного аминирования, формилирования, пирролирования, защиты амино или карбоксильной группы и снятия защиты и так далее.
[Процесс получения исходных материалов: Получение соединения [2]]
Соединение [2] может быть получено с помощью способа, включающего:
превращение альдегидной группы соединения формулы [10]:
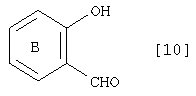
где символы имеют те же самые значения, как определено выше, в цианогруппу, что дает соединение, которое имеет формулу [9]:
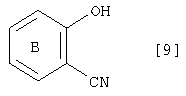
где символы имеют те же самые значения, как определено выше, реакцию соединения [9] с соединением, которое имеет формулу [8]:
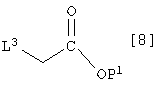
где L3 представляет собой уходящую группу и Р1 является защитной группой для карбоксильной группы, что дает соединение, которое имеет формулу [7]:
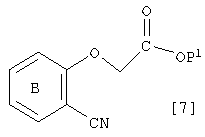
где символы имеют те же самые значения, как определено выше, снятие защиты с защитной группы Р1 соединения [7] дает соединение, которое имеет формулу [6]:
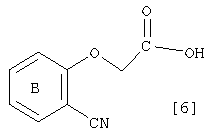
где символы имеют те же самые значения, как определено выше,
взаимодействие соединения [6], если необходимо, после превращения в реакционноспобное производное по его карбоксильной группе с соединением [5]:
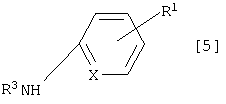
где символы имеют те же самые значения, как определено выше, что дает соединение, которое имеет формулу [4]:
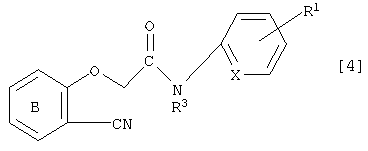
и осуществление циклизации соединения [4].
Кроме того, соединение [4] может быть также получено с помощью реакции соединения, которое имеет формулу [9], с соединением, которое имеет формулу [12]:
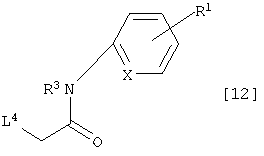
где L4 представляет собой уходящую группу и другие символы имеют те же самые значения, как определено выше.
Соединение [4] может также получено с помощью реакции соединения, которое имеет формулу [13]:
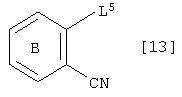
где L5 представляет собой уходящую группу и другие символы имеют те же самые значения, как определено выше, с соединением, которое имеет формулу [14]:
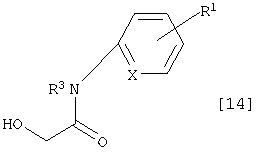
где символы имеют те же самые значения, как определено выше.
Кроме того, соединение, которое имеет формулу [10], может быть получено с помощью формилирования соединения, которое имеет формулу [11]:
где символы имеют те же самые значения, как определено выше.
Процессы [А] и [В], описанные выше, могут быть выполнены следующим образом.
[Процесс А]
Реакция, в которой соединение [1-А] получают, используя соединение [2] и соединение [3-А], может быть выполнена по обычной методике процесса амидирования. То есть реакция может быть выполнена путем взаимодействия соединения [2] с соединением [3-А], его реакционноспособным производным или его солью в присутствии или в отсутствие конденсирующего агента и, если необходимо, в присутствии акцептора кислоты в соответствующем растворителе.
Конденсирующий агент включает обычные агенты, такие как N,N-дициклогексилкарбодиимид (DCC), 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC) или его гидрохлорид, карбонилдиимидазол (CDI), дифенилфосфорилазид (DPPA), диэтиловый цианофосфонат (DEPC) и так далее. Среди всех DCC, EDC или его гидрохлорид являются предпочтительнее.
Примеры реакционноспобного производного соединения [3-А] включают традиционно используемые соединения, такие как галоидангидрид, смешанный ангидрид, реактивноспособный эфир и так далее. Примеры активатора, который может использоваться, чтобы преобразовать соединение [3-А] в его реактивное производное, включают хлористый тионил, бромистый тионил, хлорангидрид щавелевой кислоты, N-гидроксиламины, такие как 1-гидроксисукцинимид, 1-гидроксибензотриазол и так далее, и фенолы, такие как п-нитрофенол и так далее. Среди всех хлористый тионил, хлорангидрид щавелевой кислоты, 1-гидроксисукцинимид и 1-гидроксибензотриазол предпочтены. Способ с использованием хлорангидрида кислоты особенно предпочтителен.
Примеры соли соединений [3-А] или реакционноспобного производного соединения [3-А] включают соль неорганической кислоты, такой как соляная кислота, бромистоводородная кислота, серная кислота и так далее. Кислотный акцептор также пригоден в зависимости от используемого способа, который включает неорганические или органические основания.
Протекание указанной реакции может быть облегчено, когда ее проводят в присутствии основания или используют такое основание, являющееся растворителем. Примеры неорганических оснований включают неорганические основания, такие как карбонаты щелочного металла (карбонат натрия, карбонат калия, карбонат цезия и так далее), щелочноземельные металлические карбонаты (углекислый кальций и так далее), кислые карбонаты щелочных металлов (гидрокарбонат натрия, гидрокарбонат калия и так далее), гидрокисиды щелочных металлов (гидроксид натрия, гидроксид калия, гидроксид лития и так далее). Примеры органических оснований включают три-низшие алкиламины (триэтиламин, трибутиламин, диизопропилэтиламин и так далее), третичные амины (1,4-диазабицикло[2.2.2]октан, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,8-диазабицикло[5.4.0]ундек-7-ен и так далее), амины (N,N-диметиланилин, N,N-диэтиланилин, 4-диметиламинопиридин и так далее), пиридин, диметилпиридин, этилметилпиридин и так далее. Среди них предпочтительны для проведения реакции триэтиламин, диизопропилэтиламин, 4-диметиламинопиридин или пиридин. Настоящая реакция может быть проведена при наличии или отсутствии растворителя, предпочтительно при наличии растворителя.
Примеры растворителя включают любой инертный растворитель, который не прерывает реакцию, такие как галоидированные углеводороды (хлороформ, дихлорметан, дихлорэтан и так далее), ароматические углеводороды (бензол, толуол, ксилол и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), сложные эфиры (этилацетат и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон и так далее), нитрилы (ацетонитрил и так далее), диметилсульфоксид, пиридин, 2,6-лутидин и так далее, смешанный растворитель, включающий два или больше число этих растворителей, в случае необходимости, а также смесь любого(ых) этих растворителей и воды. Предпочтительно выбрать подходящий растворитель в зависимости от используемого способа. Среди них дихлорметан, хлороформ, толуол, ксилол, тетрагидрофуран, диоксан, N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, пиридин и т.п. предпочтительнее, а дихлорметан, хлороформ, N,N-диметилформамид и пиридин особенно предпочтительны. Настоящая реакция может быть проведена в широких пределах температуры от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно проведена при температуре от -10°С до точки кипения реакционной смеси, особенно от температуры образования льда до 60°С.
[Процесс В]
Процесс, где соединение [1-В] получают с помощью реакции соединения [2] с соединениями формул [3-В1] и [3-В2] соответственно, может быть выполнен в соответствии с обычным способом карбонилирования в присутствии соответствующего акцептора кислота в соответствующем растворителе.
Примеры уходящей группы для соединения, которое имеет формулу [3-В2], включают атом галогена. Примеры соединений [3-В2] включают фосген, трифосген, CDI и так далее, а трифосген является предпочтительнее.
Примеры акцептора кислоты, используемого в реакции, включают неорганические и органические основания. Примеры неорганических оснований включают карбонаты щелочного металла (карбонат натрия, карбонат калия, карбонат цезия и так далее) гидрокарбонаты щелочного металла (гидрокарбонат натрия, гидрокарбонат калия и так далее). Примеры органических оснований включают тринизшие алкильные амины (триэтиламин, трибутиламин, диизопропилэтиламин и так далее), третичные амины (1,4-диазабицикло[2.2.2]октан, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,8-диазабицикло[5.4.0]-ундек-7-ен и так далее), амины (N,N-диметиланилин, N,N-диэтиланилин, 4-диметиламинопиридин и так далее), пиридин, лутидин, коллидин и так далее. Среди них триэтиламин, диизопропилэтиламин, 4-диметиламинопиридин и пиридин являются предпочтительными.
Примеры растворителя включают любой инертный растворитель, который не прекращает реакцию, такие как галоидированные углеводороды (хлороформ, дихлорметан, дихлорэтан и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), сложные эфиры (этилацетат и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон и так далее), нитрилы (ацетонитрил и так далее), пиридин, 2,6-лутидин и так далее, и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа. Среди них дихлорметан, тетрагидрофуран, N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, пиридин и им подобные являются предпочтительными, а дихлорметан и N,N-диметилформамид являются особенно предпочтительными. Настоящая реакция может быть выполнена в широком диапазоне температур от -78°С до точки кипения реакционной смеси. Например, реакция может быть предпочтительно выполнена при температуре от -10°С до точки кипения реакционной смеси, особенно от температуры образования льда до комнатной температуры.
Кроме того, после осуществления процессов [А] и [В] целевое соединение [1] может также быть получено, если необходимо, посредством общего превращения с помощью проведения следующей реакции(ий) при условии того, что полученные соединения формулы [1-А] и/или [1-В] имеют одну или большее число остатков, способных к дальнейшей реакции(иям) с заместителем(ями) для группы Y и/или кольца В (главным образом относительно к, например, защитной группе для амина, спиртового или фенольного ОН, сложного эфира, карбоновой кислоты, нитро, галогену и так далее)
Реакции алкилирования, восстановительного алкилирования, амидирования, сульфонил-амидирования, амидиноэтерификации, арилирования, восстановления, деалкилирования, гидролиза, четвертичного аминирования, пирролирования, защиты и снятия защиты с амино или карбоксильной группы, которые проводят, когда необходимо, могут быть выполнены следующим образом.
Алкилирование может быть выполнено обычным способом, когда необходимо. Например, эта реакция может быть проведена с помощью реакции соединения [1] с алкилгалоидом, таким как алкилхлорид, алкилбромид, алкилиодид и так далее, в присутствии или в отсутствие основания в соответствующем растворителе.
Примеры пригодных оснований включают неорганические и органические основания. Неорганические основания включают карбонаты щелочного металла (карбонат натрия, карбонат калия, карбонат цезия и так далее), гидрокарбонаты щелочного металла (гидрокарбонат натрия, гидрокарбонат калия и так далее), гидроксиды щелочного металла (гидроксид натрия, гидроксид калия, гидроксид лития и так далее). Примеры органических оснований включают тринизшые алкильные амины (триэтиламин, трибутиламин, диизопропилэтиламин и так далее), третичные амины (1,4-диазабицикло[2.2.2]октан, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,8-диазабицикло[5.4.0]ундек-7-ен и так далее), пиридин, лутидин, коллидин и так далее. Среди них карбонаты щелочного металла, такие как карбонат натрия, карбонат калия и карбонат цезия, триэтиламин, диизопропилэтиламин, пиридин и так далее являются предпочтительными.
Йодид щелочного металла, такой как йодистый литий, йодистый натрий, йодистый калий, и так далее, могут также быть добавлены, поскольку они могут облегчить протекание реакции.
Любые инертные растворители, которые не нарушают реакцию, могут использоваться без ограничения, и примеры их включают эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон и так далее), нитрилы (ацетонитрил и так далее), спирты (метанол, этанол, пропанол и так далее), диметилсульфоксид, пиридин, 2,6-лутидин и так далее, и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа. Среди них тетрагидрофуран, N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, ацетонитрил, этанол, диметилсульфоксид и так далее, являются предпочтительными, а N,N-диметилформамид, ацетонитрил, этанол и их смеси растворителей являются особенно предпочтительными.
Настоящая реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания, предпочтительно от -10°С до точки кипения реакционной смеси.
Восстановительное алкилирование может быть выполнено обычным способом, если необходимо. Например, эта реакция может быть выполнена с помощью реакции соединения [1] с соответствующим карбонильным соединением в присутствии соответствующего агента восстановления, такого как гидрид металла, или в условиях каталитического восстановления в присутствии соответствующего металлического катализатора в соответствующем растворителе.
В этой реакции любые обычные агенты восстановления, такие как гидриды металлов, могут быть использованы без ограничения; тем не менее, агент восстановления, который не воздействует на амидные связи и так далее, такие как боргидрид натрия, боргидридтриацетоксид натрия, боргидрид цианонатрия и так далее являются предпочтительными.
Кроме того, органические кислоты, такие как уксусная кислота и так далее, или неорганические кислоты, такие как соляная кислота и так далее, могут также быть добавлены к настоящей реакции, которая может облегчить реакцию.
Кроме того, когда используемое соединение [1] представляет собой амин в виде соли с неорганической кислотой, такой как соляная кислота и так далее, подходящий нейтрализующий агент, такой как органическое основание (например, триэтиламин) или ацетат щелочного металла (например, уксуснокислый натрий) может быть добавлен к реакции, что может облегчить реакцию.
Любой инертный растворитель, который не нарушает реакцию, может быть использован без ограничения, и их примеры включают галоидированные углеводороды (хлороформ, дихлорметан, дихлорэтан, и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон и так далее), нитрилы (ацетонитрил и так далее), ароматические углеводороды (бензол, толуол, ксилол и так далее), спирты (метанол, этанол, пропанол и так далее), вода и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа. Среди них дихлорметан, дихлорэтан, тетрагидрофуран, 1,2-диметоксиэтан, метанол, этанол, пропанол и так далее являются предпочтительными, а дихлорметан, дихлорэтан и тетрагидрофуран являются особенно предпочтительными.
Реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно выполнена при температуре от -10°С до точки кипения реакционной смеси, особенно от температуры образования льда до точки кипения смеси.
Настоящая реакция может аналогично быть выполнена в соответствии с процессом каталитической гидрогенизации в присутствии металлического катализатора. Примеры металлического катализатора включают палладий на угле, платину на угле, оксид платины, никель Ренея, и так далее.
Кроме того, органические кислоты, такие как уксусная кислота и так далее, или неорганические кислоты, такие как соляная кислота и так далее, могут также быть добавлены к настоящей реакции, что может облегчить ее протекание.
Кроме того, когда используемое соединение [1] представляет собой амин в виде соли неорганической кислоты, такой как соляная кислота и так далее, соответствующий нейтрализующий агент, такой как органическое основание (например, триэтиламин) или ацетат щелочного металла (например, уксуснокислый натрий) может быть добавлен к реакции, что может ее облегчить ее протекание.
Любой инертный растворитель, который не нарушает реакцию, может быть использован без ограничения и их примеры включают эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон и так далее), ароматические углеводороды (бензол, толуол, ксилол, и так далее), спирты (метанол, этанол, пропанол и так далее), воду и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа. Среди них тетрагидрофуран, N,N-диметилформамид, метанол, этанол и так далее являются предпочтительными, а тетрагидрофуран, метанол, этанол и так далее являются особенно предпочтительными.
Реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно выполнена при температуре от -10°С до точки кипения реакционной смеси, особенно от температуры образования льда до комнатной температуры.
Амидирование может быть выполнено аналогичным способом по упомянутой выше реакции между соединением [2] и соединением [3-А], когда необходимо.
Сульфониламидирование может быть выполнено обычным способом, когда необходимо. Например, эта реакция может быть выполнена с помощью реакции соединения [1] с необязательно замещенным галоидом алкилсульфоновой кислоты в присутствии или в отсутствие основания в соответствующем растворителе. Для проведения реакции могут быть использованы аналогичный кислотный поглотитель, растворитель и температура реакции, как та, которая используют в реакции амидирования между соединением [2] и соединением [3-А], указанные выше.
Амидиноэтерификации может быть выполнена обычным способом, когда необходимо. Например, реакция может быть выполнена с помощью реакции соединения [1] с 2-бромэтилизоцианатом или 2-хлорэтилизоцианатом в присутствии или в отсутствие соответствующего акцептора кислота в соответствующем растворителе.
Примеры пригодных оснований включают неорганические и органические основания. Неорганические основания включают карбонаты щелочного металла (карбонат натрия, карбонат калия, карбонат цезия и так далее), гидрокарбонаты щелочного металла (гидрокарбонат натрия, гидрокарбонат калия и так далее) и так далее. Примеры органических оснований включают тринизшие алкильные амины (триэтиламин, трибутиламин, диизопропилэтиламин и так далее), трет-амины (1,4-диазабицикло[2.2.2]октан, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,8-диазабицикло[5.4.0]ундек-7-ен и так далее), амины (N,N-диметиланилин, N,N-диэтиланилин, 4-диметил-аминопиридин и так далее), пиридин, лутидин, коллидин, и так далее. Среди них, триэтиламин и диизопропилэтиламин являются предпочтительными.
Настоящая реакция может быть выполнена в присутствии или в отсутствие растворителя, предпочтительно в присутствии растворителя.
Любой инертный растворитель, который не нарушает реакцию, может быть использован без ограничения, и их примеры включают галоидированные углеводороды (хлороформ, дихлорметан, дихлорэтан и так далее), ароматические углеводороды (бензол, толуол, ксилол и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон и так далее), нитрилы (ацетонитрил и так далее), диметилсульфоксид, пиридин, 2,6-лутидин и так далее, и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Среди них, дихлорметан, тетрагидрофуран, N,N-диметилформамид и так далее являются предпочтительными, а тетрагидрофуран является более предпочтительным.
Реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно выполнена при температуре от -10°С до точки кипения реакционной смеси, особенно от температуры образования льда до комнатной температуры.
Арилирование может быть выполнено обычным способом, когда необходимо. Например, реакция может быть выполнена с помощью реакции соединения [1] с галоидированным соединением арила в присутствии или в отсутствие соответствующего основания в соответствующем растворителе.
Примеры пригодных оснований включают неорганические и органические основания. Неорганические основания включают карбонаты щелочного металла (карбонат натрия, карбонат калия, карбонат цезия и так далее), гидрокарбонаты щелочного металла (гидрокарбонат натрия, гидрокарбонат калия и так далее) и так далее. Примеры органических оснований включают тринизшие алкильные амины (триэтиламин, трибутиламин, диизопропилэтиламин и так далее), трет-амины (1,4-диазабицикло[2.2.2]октан, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,8-диазабицикло[5.4.0]ундек-7-ен и так далее), амины (N,N-диметиланилин, N,N-диэтиланилин, 4-диметиламинопиридин и так далее), пиридин, лутидин, коллидин и так далее. Среди них триэтиламин, диизопропилэтиламин, карбоната калия и так далее, являются предпочтительными.
Настоящая реакция может быть выполнена в присутствии или в отсутствие растворителя, предпочтительно в присутствии растворителя.
Любой инертный растворитель, который не нарушает реакцию, может быть использован без ограничения, и их примеры включают ароматические углеводороды (бензол, толуол, ксилол и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил и так далее), спирты (метанол, этанол, пропанол, 2-бутанол и так далее), диметилсульфоксид, пиридин, 2,6-лутидин и так далее, и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Среди них ксилол, тетрагидрофуран, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, этанол, 2-бутанол и так далее являются предпочтительными, а тетрагидрофуран, N,N-диметилацетамид и 2-бутанол являются особенно предпочтительными.
Реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно выполнена при температуре от -10°С до точки кипения реакционной смеси, особенно из комнатной температуре до точки кипения реакционной смеси.
Восстановление может быть выполнено обычным способом, когда необходимо. Например, реакция может быть выполнена с помощью реакции соединения [1] с соответствующим агентом восстановления или с водородом в присутствии металлического катализатора в соответствующем растворителе.
В реакции любые обычные агенты восстановления могут быть использованы без ограничения; тем не менее, агенты восстановления, такие как гидриды металлов, а именно литий алюмогидрид лития, боргидрид лития, боргидрид натрия и так далее, металлы, такие как цинк, железо, олово, и так далее, и соли металла, такие как хлорид олова, и так далее, являются предпочтительными и металлы, такие как олово, и так далее, и соли металла, такие как хлорид олова, и так далее, являются особенно предпочтительными. При каталитической гидрогенизации любой обычный металлический катализатор может быть использован без ограничения; тем не менее, палладий на угле, никель Ренея, кобальт Ренея, оксид платины, и так далее являются предпочтительными, а металлы, такие как никель Ренея и так далее, являются особенно предпочтительными. Кроме того, в зависимости от используемого способа реакция может иногда лучше протекать, когда ее проводят в кислотных условиях при наличии неорганической кислоты, такой как соляная кислота, и так далее.
В реакции, где используется агент восстановления, такой как гидрид металла, любой инертный растворитель, который не нарушает реакцию, может быть использован без ограничения, и их примеры включают эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), ароматические углеводороды (бензол, толуол, ксилол, и так далее), спирты (метанол, этанол, пропанол, и так далее), воду, и так далее, и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа.
В реакции, где используется металл, такой как цинк, железо, олово, и так далее, или соль металла, такие как хлорид олова, и так далее, любые инертные растворители, которые не нарушают реакцию, могут использоваться без ограничения, и их примеры включают воду, спирты (метанол, этанол, пропанол и так далее), сложные эфиры (этилацетат, и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, 1,2-диметоксиэтан, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил, и так далее), ароматические углеводороды (бензол, толуол, ксилол, и так далее) и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа. Среди них этилацетат, вода или смеси растворителей, содержащие воду и спирт, эфир, амид, нитрил и так далее, что является предпочтительным.
В реакции, где гидрогенизацию выполняют в присутствии металлического катализатора, любой инертный растворитель, который не нарушает реакцию, может быть использован без ограничения, и их примеры включают спирты, эфиры, алифатические углеводороды, ароматические углеводороды, амиды, сложные эфиры (этилацетат, и так далее), органические кислототы (муравьиная кислота, уксусная кислота, пропионовая кислота, трифторуксусная кислота, и так далее) и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа.
Настоящая реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно выполнена при температуре от -10°С до точки кипения реакционной смеси.
Давление водорода, используемого в реакции каталитической гидрогенизации, обычно составляет около 1-100 атмосфер.
Время реакции для настоящей реакции меняется в зависимости от вида агента восстановления или активности используемого катализатора; тем не менее, оно обычно находится в интервале от около 10 минут до 24 часов.
Деалкилирование может быть выполнено обычным способом, когда необходимо. Например, эта реакция может быть выполнена с помощью реакции соединения [1] с соответствующим агентом деалкилирования в соответствующем растворителе или без растворителя.
Любые обычные агенты деалкилирования могут быть использованы без ограничения, и предпочтительные их примеры включают трибромид бора, трихлорид бора, иодтриметилсилан, хлорид алюминия(III), хлорид пиридиния, и так далее, а трибромид бора, иодтриметилсилан, и так далее являются предпочтительными.
Любой инертный растворитель, который не нарушает реакцию, может быть использован без ограничения, и их примеры включают галоидированные углеводороды (хлороформ, дихлорметан, дихлорэтан, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил, и так далее) и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа.
Реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания, предпочтительно от -78°С до точки кипения реакционной смеси.
Гидролиз может быть выполнен обычным способом, когда необходимо.
Четвертичное аминирование может быть выполнено обычным способом, когда необходимо. Эта реакция может быть проведена аналогичным способом до упомянутого выше алкилирования.
Пирролилирование может быть выполнено путем, например, реакции соединения, имеющего аминогруппу, с тетрагидро-2,5-диметоксифураном в присутствии кислоты в соответствующем растворителе.
Примеры кислот включают органические кислоты, такие как муравьиная кислота, уксусная кислота, пропионовая кислота, трифторуксусная кислота, и так далее, и неорганические кислоты, такие как соляная кислота, и так далее, которые могут также быть использованы в качестве растворителя.
Любые инертные растворители в дополнение к упомянутым выше органическим кислотам и неорганическим кислотам, которые не нарушает реакцию, могут быть использованы без ограничения, и их примеры включают галоидированные углеводороды (хлороформ, дихлорметан, дихлорэтан, и так далее), ароматические углеводороды (бензол, толуол, ксилол, и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил, и так далее), и так далее, а органические кислоты являются предпочтительными.
Реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания, предпочтительно из -78°С до точки кипения реакционной смеси.
Защита амино- или карбоксигруппы или снятие защиты с защищенной группы могут быть выполнены, когда необходимо, в соответствии с любыми известными способами.
[Процесс получения исходных материалов: Получение соединение [2]
(1) Реакция преобразования альдегидной группы соединения [10] в цианогруппу для получения соединения [9] может быть выполнена с помощью реакции соединения [10] с гидроксиламином или его гидрохлоридом в присутствии или в отсутствие формиата натрия в соответствующем растворителе. Может быть добавлен дегидратирующий агент. Доступный растворитель органическую низшую жирную кислоту, такую как муравьиная кислота; тем не менее, предпочтительнее является выбор соответствующего растворителя в зависимости от используемого способа.
Настоящая реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно выполнена от температуры образования льда до точки кипения реакционной смеси, особенно при точке кипения реакционной смеси.
(2) Следующая реакция между полученным соединением [9] и соединением [8] для получения соединения [7] может быть выполнена обычным способом для O-алкилирования фенольного соединения. Настоящая реакция может быть выполнена с помощью реакции соединения [9] с соединением [8] в соответствующем растворителе в присутствии основания или путем использования такого основания как растворитель.
Уходящая группа в соединении [8] может быть предпочтительна, например, в виде атома галогена. Примеры предпочтительных защитных групп для карбоксильной группы соединения [8] включают низшую алкильную группу и фенил-низшую алкильную группу.
Примеры пригодных оснований включают неорганические и органические основания, такие как карбонаты щелочного металла (карбонат натрия, карбонат калия, и так далее), гидрокарбонаты щелочного металла (гидрокарбонат натрия, гидрокарбонат калия, и так далее), гидроксиды щелочного металла (гидроксид натрия, гидроксид калия, гидроксид лития, и так далее), гидриды щелочного металла (гидрид натрия, и так далее), алкоксиды щелочного металла, (метоксид натрия, трет-бутоксид калия, и так далее), тринизшие алкиламины (триэтиламин, трибутиламин, диизопропилэтиламин, и так далее), третичные амины (1,4-диазабицикло[2.2.2]октан, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,8-диазабицикло[5.4.0]ундек-7-ен, и так далее), амины (N,N-диметиланилин, N,N-диэтиланилин, 4-диметиламинопиридин, и так далее), пиридин, лутидин, коллидин, и так далее. Среди них карбонат щелочного металла, диизопропилэтиламин, пиридин, и так далее являются предпочтительными.
Примеры растворителя включают любой инертный растворитель, который не нарушает реакцию, такие как кетоны (например, ацетон, метилэтиловый кетон, и так далее), ароматические углеводороды (бензол, толуол, ксилол, и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил, и так далее), спирты (метанол, этанол, пропанол, 2-бутанол, и так далее), диметилсульфоксид, пиридин, 2,6-лутидин, и так далее, и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Среди них кетоны, такие как ацетон, метилэтиловый кетон, и так далее, а амиды, такие как N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее, являются предпочтительными.
Настоящая реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания. Например, реакция может быть предпочтительно выполнена при температуре от температуры образования льда до точки кипения реакционной смеси.
Йодид щелочного металла, такой как иодид лития, иодид натрия, иодид калия, и так далее, может также быть добавлен, чтобы облегчить протекание реакции.
(3) Реакция удаления защитной группы из соединения [7] для получения соединения [6] может быть выполнена, как правило, с помощью способа, используемого для снятия защиты с карбоксильной группы.
(4) Реакция конденсирования соединения [5] с соединением [6] для получения соединения [4] может быть выполнена аналогичным способом, таким как для реакции соединения [2] с соединением [3-А].
(5) Реакция циклизации соединения [4], для получения соединения [2], может быть выполнена путем обработки соединения [4] основанием в соответствующем растворителе.
Примеры пригодных оснований включают неорганические и органические основания, такие как карбонаты щелочного металла (карбонат натрия, карбонат калия, и так далее), гидроксиды щелочного металла (гидроксид натрия, гидроксид калия, гидроксид лития, и так далее), гидриды щелочного металла (гидрид натрия, и так далее), алкоксиды щелочного металла (метоксид натрия, трет-бутоксид калия, и так далее), тринизшие алкильные амины (триэтиламин, трибутиламин, диизопропилэтиламин, и так далее), трет-амины (1,4-диазабицикло[2.2.2]октан, 1, 5-диазабицикло[4.3.0]-нон-5-ен, 1,8-диазабицикло[5.4.0]ундек-7-ен, и так далее), амины (N,N-диметиланилин, N,N-диэтиланилин, 4-диметиламинопиридин, и так далее), пиридин, лутидин, коллидин, и так далее. Среди них, карбонат щелочного металла, алкоксиды щелочного металла, диизопропилэтиламин, пиридин, и так далее, являются предпочтительными.
Настоящая реакция может быть выполнена в присутствии или в отсутствие растворителя, предпочтительно в присутствии растворителя. Примеры растворителя включают любой инертный растворитель, который не нарушает реакцию, такие как ароматические углеводороды (бензол, толуол, ксилол, и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил, и так далее), спирты (метанол, этанол, пропанол, 2-бутанол, и так далее), диметилсульфоксид, пиридин, 2,6-лутидин, и так далее, и смеси растворителей, содержащие два или большее число указанных растворителей, если необходимо. Среди них ксилол, тетрагидрофуран, N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, метанол, пиридин, и так далее являются предпочтительными, а N,N-диметилацетамид и 1,3-диметил-2-имидазолидинон являются особенно предпочтительными.
Настоящая реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания, предпочтительно от температуры образования льда до точки кипения реакционной смеси.
(6) Реакция соединения [9] и соединением [12] для получения соединения [4] может быть проведена в присутствии основания в соответствующем растворителе, если необходимо. Уходящей группой в соединении [12] может быть предпочтительно, например, атом галогена.
Примеры пригодных оснований в настоящей реакции включают неорганические и органические основания. Неорганические основания включают карбонаты щелочного металла (карбонат натрия, карбонат калия, и так далее), гидрокарбонаты щелочного металла (кислый углекислый натрий, кислый углекислый калий, и так далее), гидроксиды щелочного металла (гидроксид натрия, гидроксид калия, гидроксид лития, и так далее), гидриды щелочного металла (гидрид натрия, и так далее). Смесь карбоната цезия и йодистого натрия может также использоваться. Органические основания включают алкоксиды щелочного металла (метоксид натрия, трет-бутоксид калия, и так далее), тринизшие алкиламины (триэтиламин, трибутиламин, диизопропилэтиламин, и так далее), трет-амины (1,4-диазабицикло[2.2.2]октан, 1,5-диазабицикло[4.3.0]нон-5-ен, 1,8-диазабицикло[5.4.0]-ундек-7-ен, и так далее), амины (N,N-диметиланилин, N,N-диэтиланилин, 4-диметиламинопиридин, и так далее), пиридин, лутидин и коллидин, и так далее. Среди них карбонаты щелочного металла, диизопропилэтиламин, пиридин, и так далее являются предпочтительными. В настоящей реакции основания, указанные выше, могут также использоваться в качестве растворителя.
Примеры растворителей, пригодных в настоящей реакции, включают любой инертный растворитель, который не нарушает реакцию, такие как кетоны (например, ацетон, метилэтиловый кетон, и так далее), ароматические углеводороды (бензол, толуол, ксилол, и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил, и так далее), спирты (метанол, этанол, пропанол, 2-бутанол, и так далее), диметилсульфоксид, пиридин, 2,6-лутидин, и так далее. Смесь растворителей, содержащая два или большее число указанных растворителей, может также использоваться. Среди них кетоны и амиды являются предпочтительными.
Настоящая реакция может, как правило, выполняться от температуры образования льда до температуры кипения растворителя.
Время реакции для настоящей реакция находится, как правило, между 30 минутами и 24 часами; тем не менее длительное или короткое соответствующее время реакции может быть выбрано, если необходимо. Более того, иодид щелочного металла, такой как иодид лития, иодид натрия, иодид калия, и так далее, может также быть добавлен, чтобы облегчить протекание реакции.
Реакция соединения [13] и соединением [14] может быть выполнена в присутствии основания в соответствующем растворителе, если необходимо. Уходящей группой в соединении [13] может быть предпочтительно, например, атом галогена или нитрогруппа.
Примеры пригодных оснований в настоящей реакции включают карбонаты щелочного металла (карбонат натрия, карбонат калия, карбонат цезия, и так далее), гидриды щелочного металла (гидрид натрия, и так далее) и алкоксиды щелочного металла (метоксид натрия, трет-бутоксид калия, и так далее). Среди них гидрид натрия является предпочтительным.
Примеры растворителей, пригодных в настоящей реакции, включают амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), а эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее) и N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее являются предпочтительными.
Реакция формилирования соединения [11] для получения соединения [10] может быть выполнена обычным способом, если необходимо. Например, реакция может быть выполнена с помощью реакции агента формилирования в соответствии со способом для реакции по Дуффу, реакции по Каттерману-Коху, реакции по Вильмайеру, и так далее в соответствующем растворителе.
Любой обычный агент формилирования может быть использован без ограничения, а гексаметилентетрамин, и так далее являются предпочтительными.
Примеры растворителей включают любые инертные растворители, которые не нарушают реакцию, такие как органические кислоты (уксусная кислота, пропионовая кислота, трифторуксусная кислота, метансульфоновая кислота, и так далее), галоидированные углеводороды (хлороформ, дихлорметан, дихлорэтан, и так далее), ароматические углеводороды (бензол, толуол, ксилол, и так далее), эфиры (диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран, диоксан, 1,2-диметоксиэтан, и так далее), кетоны (ацетон, метилэтиловый кетон, и так далее), сложные эфиры (этилацетат, и так далее), амиды (N,N-диметилформамид, N,N-диметилацетамид, 1,3-диметил-2-имидазолидинон, и так далее), нитрилы (ацетонитрил, и так далее), вода и смеси растворителей, содержащие два или большее число этих растворителей, если необходимо. Является предпочтительным выбрать любой соответствующий растворитель в зависимости от используемого способа.
Настоящая реакция может быть выполнена в широком диапазоне температур от температуры охлаждения до температуры нагревания, предпочтительно от -78°С до точки кипения реакционной смеси.
Полученные таким образом соединения настоящего изобретения могут быть выделены и очищены с помощью методик, хорошо известных в области органической химии, таких как перекристаллизация, хроматография на колонке, и так далее.
Настоящее соединение [1] или его фармацевтически приемлемая соль обладают сильным ингибирующим эффектом в отношении активированного фактора Х коагуляции крови и, следовательно, применимы для профилактики и лечения различных заболеваний, вызванных тромбом и эмболом у млекопитающих (например, человека, обезьяны, кролика, собаки, кота, свиньи, лошади, быка, мыши, крысы, гвинейской свинки, и так далее), такие заболевания включают, например, устойчивую стенокардию, нестабильную стенокардию, мозговой тромбоз, мозговое образование инфаркта, мозговую эмболию, кратковременный ишемический криз (TIA), ишемическую цереброваскулярную болезнь, такие как цереброваскулярная судорога после субарахноидального кровотечения, ишемическая сердечная болезнь, вызванная коронарным тромбогенезисом артерии, застойная хроническая сердечная недостаточность, инфаркт миокарда, острый инфаркт миокарда, легочный инфаркт, легочная эмболия, легочные сосудистые нарушения, синдромом экономического класса, почечная болезнь (диабетическая почечная болезнь, хронический гломерулонефрит, IgA нефропатия, и так далее), тромбогенез с атеросклерозом, периферическая артериальная окклюзия, периферическая венозная окклюзия, болезнь Бюрдгера, глубокий тромбоз вены, диссеминированное внутрисосудистое свертывание (DIC), тромбогенезис после имплантации синтетического сосудистого протеза или замены искусственного клапана сердца или сустава, неустойчивая хромота, тромбогенезис и переокклюзия после реконструкции кровообращения, такие как чрескожная транслюминальная коронарная ангиопластика (РТСА) или чрескожное транслюминальное восстановление проходимости коронарной артерии (PTCR), синдром системного воспалительного ответа (SIRS), полиорганная недостаточность (MODS), тромбогенез в искусственном кровообращении, коагуляция крови в случае взятия крови, диабетического циркулирующего нарушения режима, отторжения трансплантата, защита органа и функции выздоровления в случае трансплантации, и так далее
Настоящее соединение характеризуется тем, что оно оказывает сильное ингибирующее воздействие на активированный фактор Х коагуляции крови, способствует снижению токсичности и вызывает лишь незначительные побочные эффекты (отбор конденсатных фракций, и так далее), которые замечены для существующих антикоагулирующих средств.
Когда ингибитор FXa имеет малый объем распределения (терапия/концентрация крови), он, в основном, не обладает побочными эффектами, такими как фосфолипидоз, гепатотоксичность, и так далее. Соответственно ингибиторы FXa, особенно те, которые имеют величину распределения 0,1-3,0 л/кг и FXa ингибирующее эффект с величиной IC50, равной 100 нМ или ниже, в основном не обладают побочными эффектами, такими как фосфолипидоз, гепатотоксичность, и так далее, и полезны как лекарственное средство для того, чтобы лечить тромбоз. Например, транс-5-диметиламинокарбонил-3-[4-(N-формил-N-метиламино)-циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид имеет объемное распределение 0,8 л/кг и ингибирующий эффект FXa с величиной IC50, равной значению, меньше, чем 100 нМ, и может быть превосходным лекарственным средством, в основном не обладающим побочным эффектом, таким как фосфолипидоз, гепатотоксичность, и так далее.
Ингибиторы FXa, имеющие малую величину объемного распределения, имеют предпочтительно следующую частичную структуру:

и более предпочтительно следующую частичную структуру:
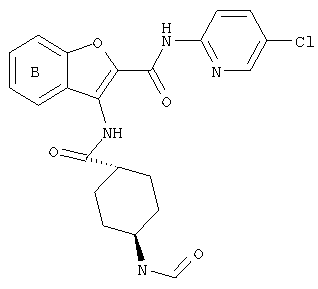
Настоящее соединение (1) или его фармацевтически приемлемая соль могут быть введены в фармацевтическую композицию, содержащую терапевтически эффективное количество соединения (1) и его фармацевтически приемлемый носитель. Фармацевтически приемлемые носители включают разбавители, связующие вещества (например, сироп, аравийская камедь, желатин, сорбит, трагакант, поливинилпирролидон), инертные наполнители (например, лактоза, сахароза, кукурузный крахмал, фосфорнокислый калий, сорбит, аминоуксусная кислота), смазки (например, стеарат магния, тальк, полиэтиленгликоль, кремнезем), разрыхлители (например, картофельный крахмал) и смачивающие вещества (например, сульфат лаурила натрия), и так далее
Соединение [1] настоящего изобретения или его фармацевтически приемлемая соль могут вводиться орально или парентерально и использоваться как соответствующие фармацевтические препараты. Примеры соответствующих препаратов для орального введения включают получение твердых веществ (таблетки, гранулы, капсулы, порошки, и так далее), растворы, суспензии и эмульсии. Примеры соответствующих препаратов для парентерального введения включают свечи, инъекции или препараты для постоянного экстрагированию, полученные с использованием дистиллированной воды для инъекции, физиологического соляного раствора или водного раствора глюкозы, и так далее, или ингалятор.
Доза соединения [1] или его фармацевтически приемлемой соли настоящего изобретения может изменяться в зависимости от пути введения, возраста, веса и состояния пациента или вида или серьезности болезни, но она находится обычно в диапазоне приблизительно от 0,1 до 50 мг/кг/день, предпочтительно приблизительно от 0,1 до 30 мг/кг/день.
ПРИМЕРЫ
Настоящее изобретение далее раскрывается с помощью примеров и сравнительных примеров, которые не должны рассматриваться как ограничивающие границы указанного изобретения
Пример 1: Транс-5-метоксикарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид
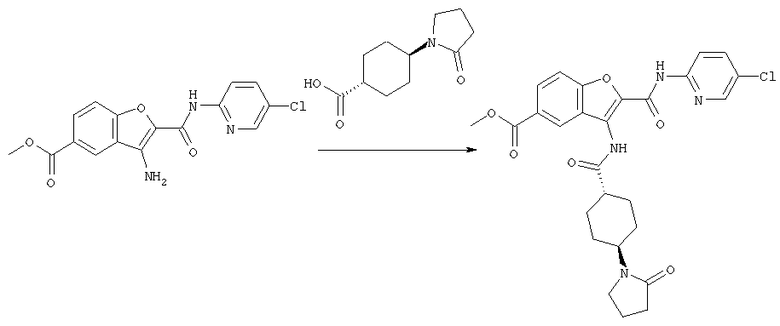
Транс-4-(2-оксопирролидин-1-ил)циклогексанкарбоновую кислоту (634 мг), полученную в примере приготовления 113, растворяют в тионилхлориде (10 мл) и смесь перемешивают при комнатной температуре в течение 4 часов. Реакционный раствор концентрируют при пониженном давлении и осадок растворяют в хлороформе (5 мл). Смесь добавляют по каплям в суспензию 3-амино-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида (691 мг), полученного в примере приготовления 72, в пиридине (15 мл) при охлаждении льдом. После добавления реакционный раствор нагревают до комнатной температуры и затем перемешивают в течение 17 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ), что дает названное соединение (785 мг). APCI-MS М/Е: 539/541 [M+H]+.
Пример 2: Транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-метоксикарбонилметил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
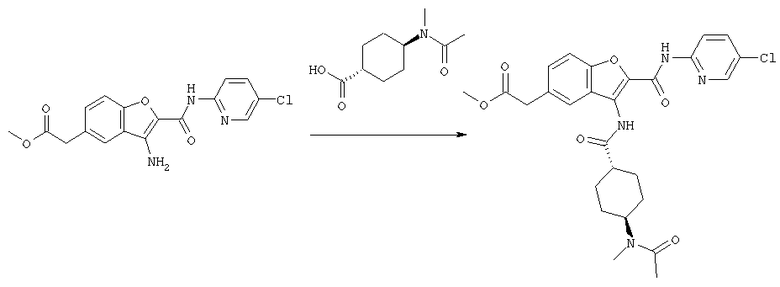
Транс-4-(N-ацетил-N-метиламино)циклогексанкарбоновую кислоту (1,80 г), полученную в примере приготовления 114, растворяют в тионилхлориде (20 мл) и смесь перемешивают при комнатной температуре в течение 12 часов. Реакционный раствор концентрируют при пониженном давлении и осадок растворяют в хлороформе (70 мл) и добавляют 3-амино-5-метоксикарбонилметил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,20 г), полученный в примере приготовления 73, при охлаждении льдом. К смеси дополнительно добавляют пиридин (4,95 мл) и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 3 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =1/1, затем только этилацетат), что дает названное соединение (2,97 г). APCI-MS М/Е: 541/543 [M+H]+.
Пример 3: 3-[2-(1-Изопропилпиперидин-4-ил)ацетиламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
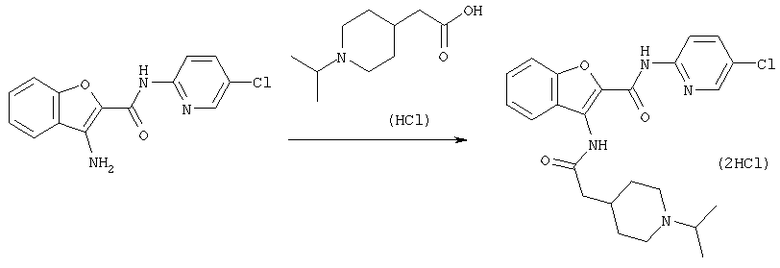
Гидрохлорид (1-изопропилпиперидин-4-ил)уксусной кислоты (432 мг), полученный в примере приготовления 129, растворяют в тионилхлориде (5 мл) и смесь перемешивают при комнатной температуре в течение 3 часов. Тионилхлорид выпаривают при пониженном давлении и полученный осадок растворяют в дихлорметане (10 мл) и охлаждают льдом. К этому раствору добавляют 3-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (374 мг), полученный в примере приготовления 74, и пиридин (420 мкл) и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 3 часов. В реакционный раствор добавляют воду и насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ, затем хлороформ/метанол =10/1, затем 6/1), что дает 3-[2-(1-изопропилпиперидин-4-ил)ацетиламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (489 мг), который затем растворяют в дихлорметане (10 мл) и добавляют 4N хлористый водород в диоксане (5 мл) и смесь перемешивают при комнатной температуре в течение 30 минут. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в смеси метанол-хлороформ. Осадки собирают фильтрованием, что дает названное соединение (423 мг). APCI-MS М/Е: 455/457 [M+H]+.
Примеры 4-75
Соответствующие аминосоединения и соединения карбоновой кислоты обрабатывают способом, аналогичным описанным в примере 1, примере 2 или в примере 3, что дает последующие соединения в свободном виде, которые затем обрабатывают хлористым водородом, что приводит к образованию их гидрохлоридов.
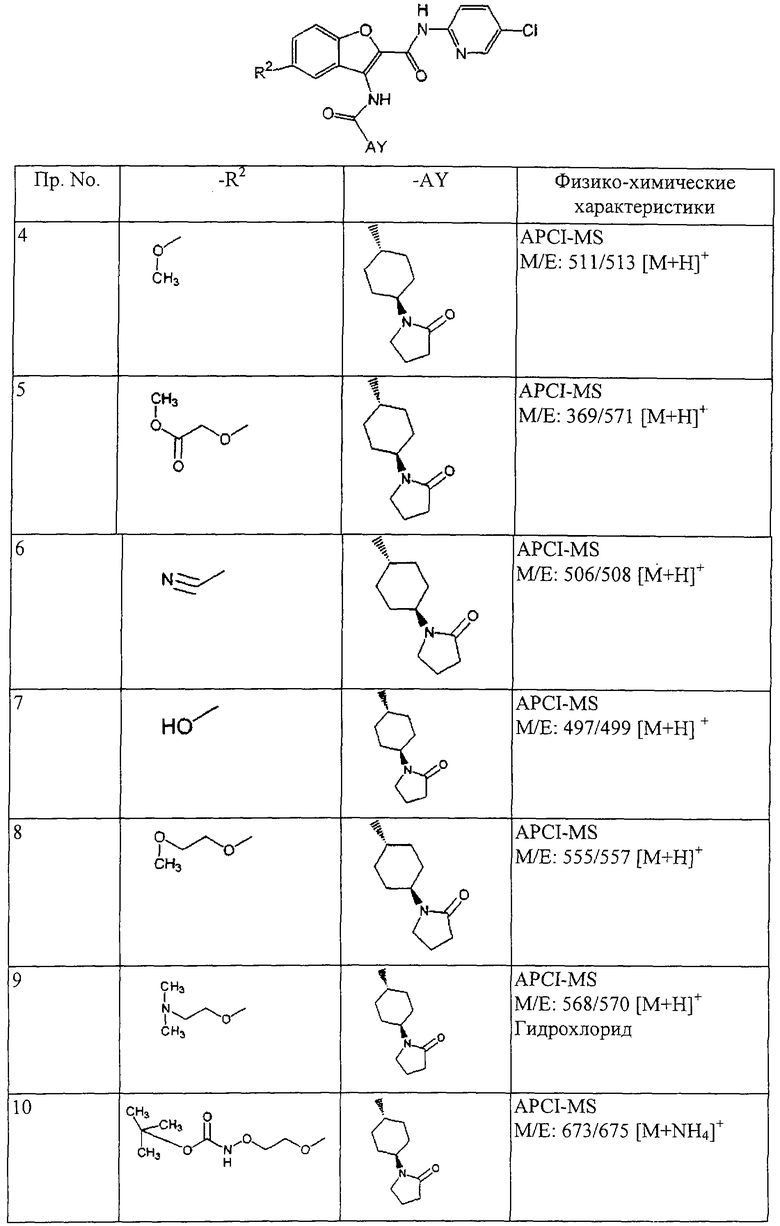
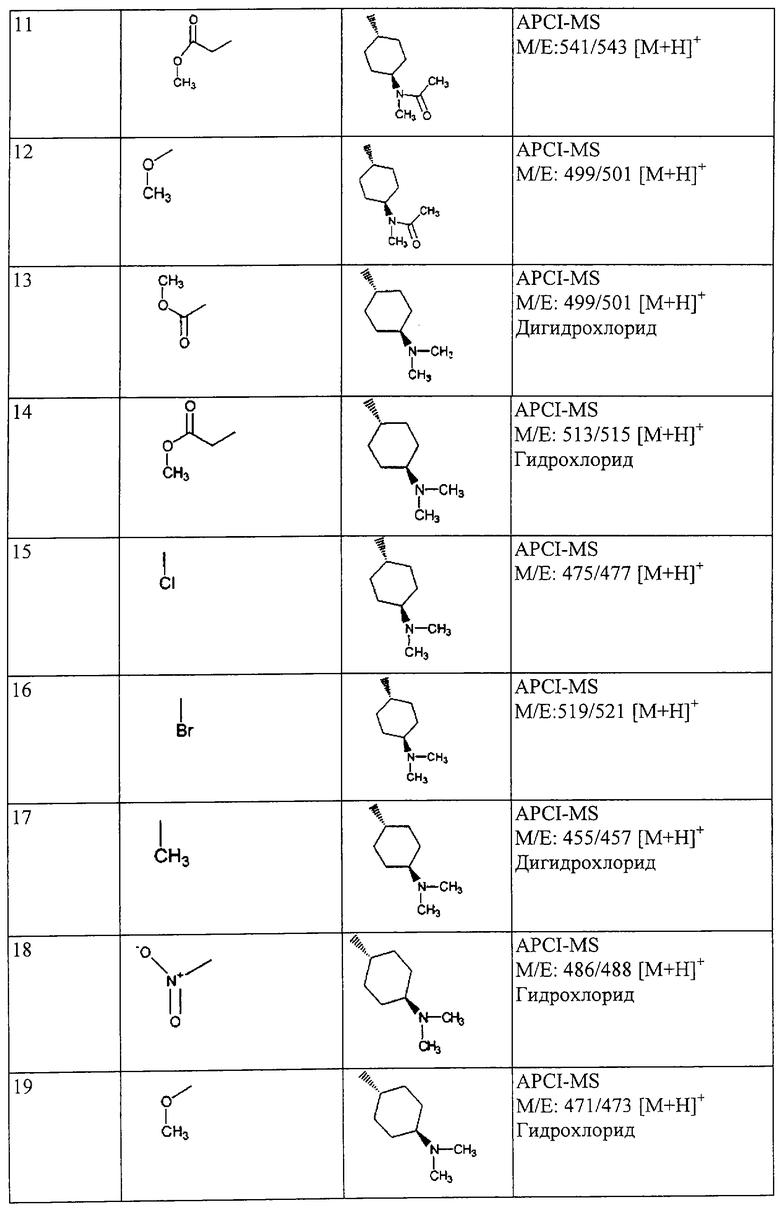
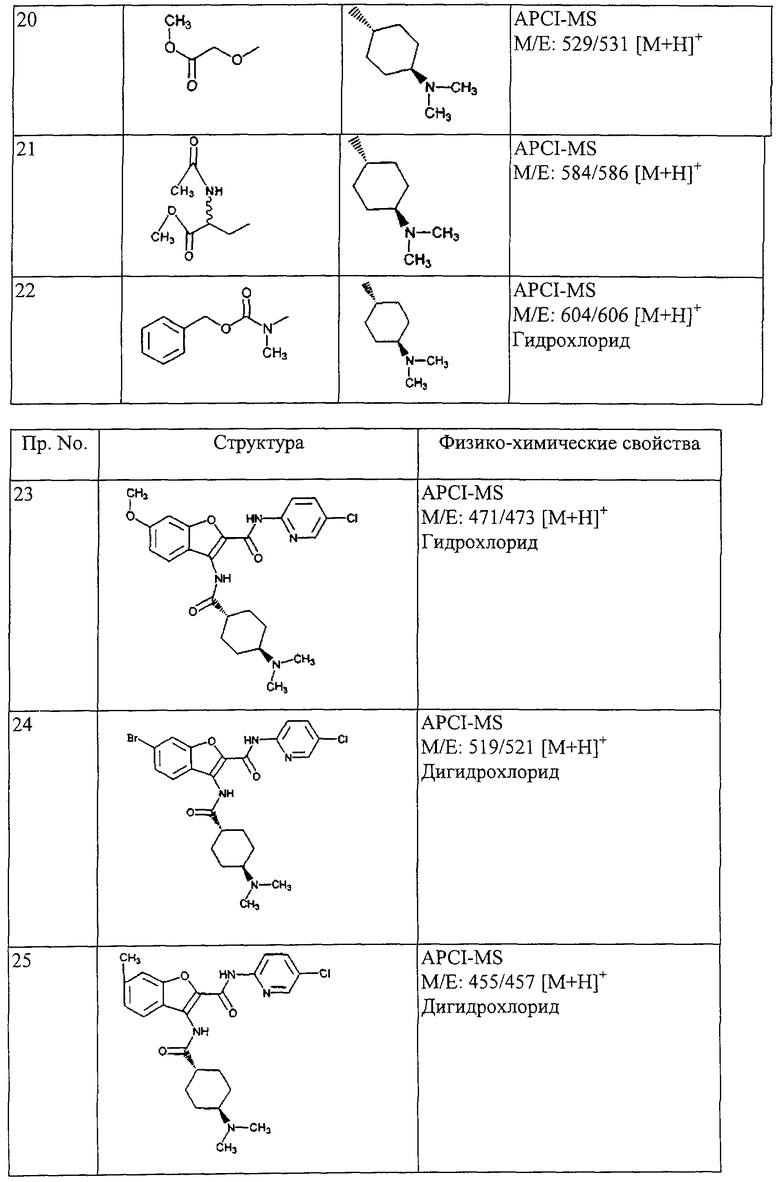
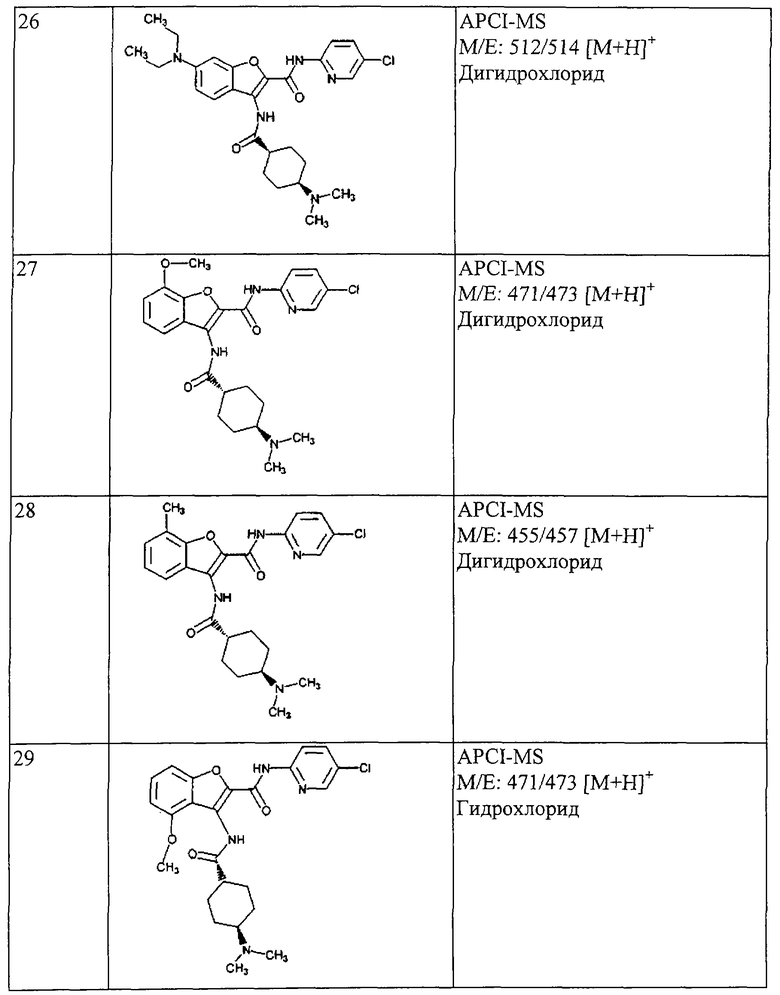
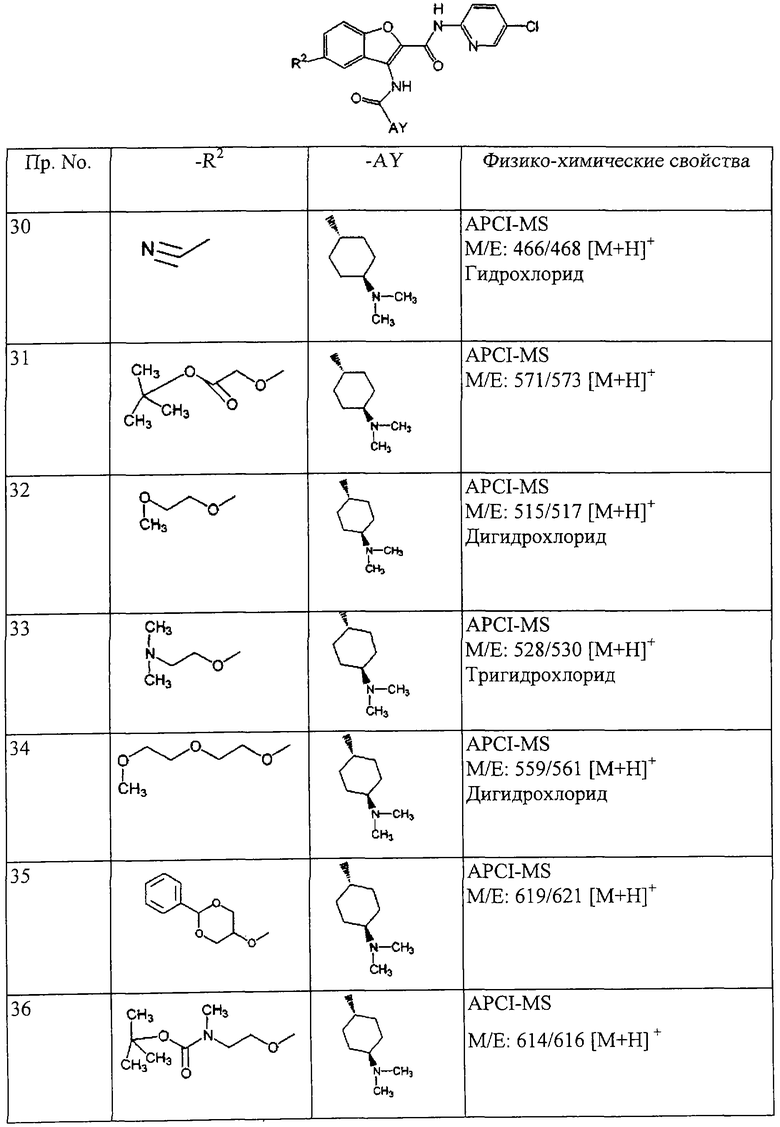
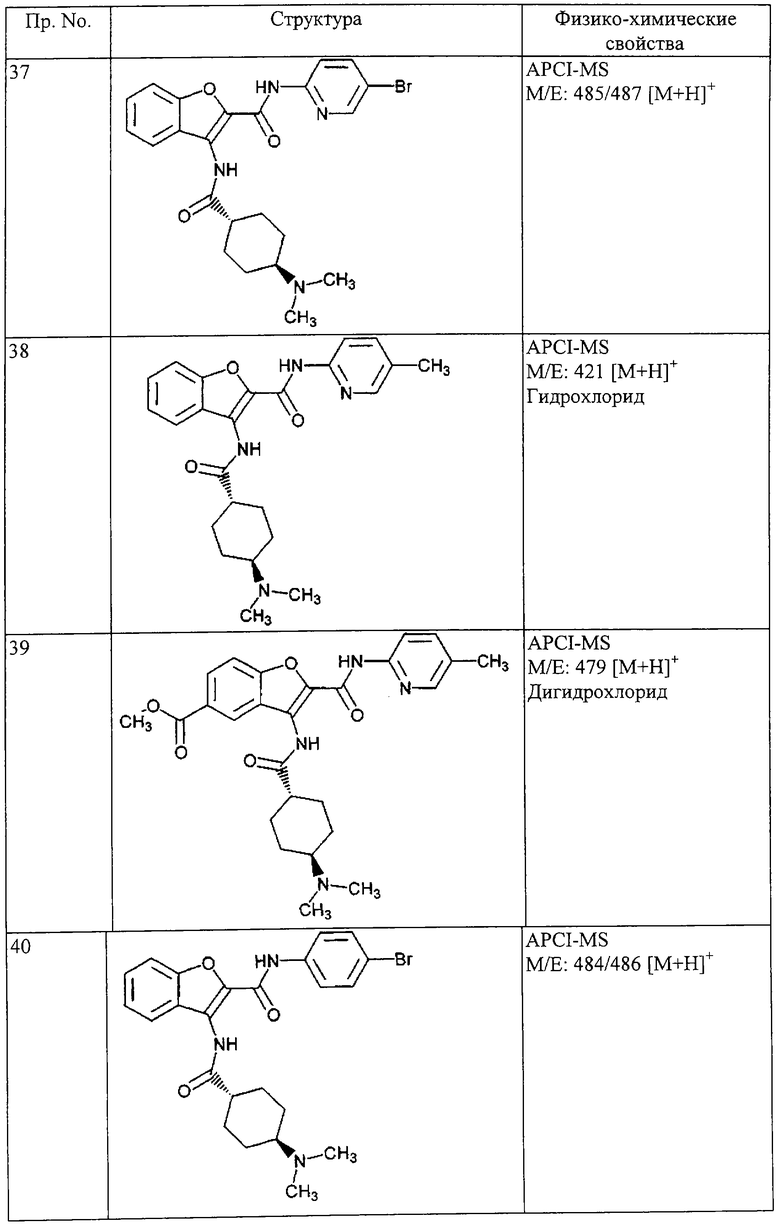
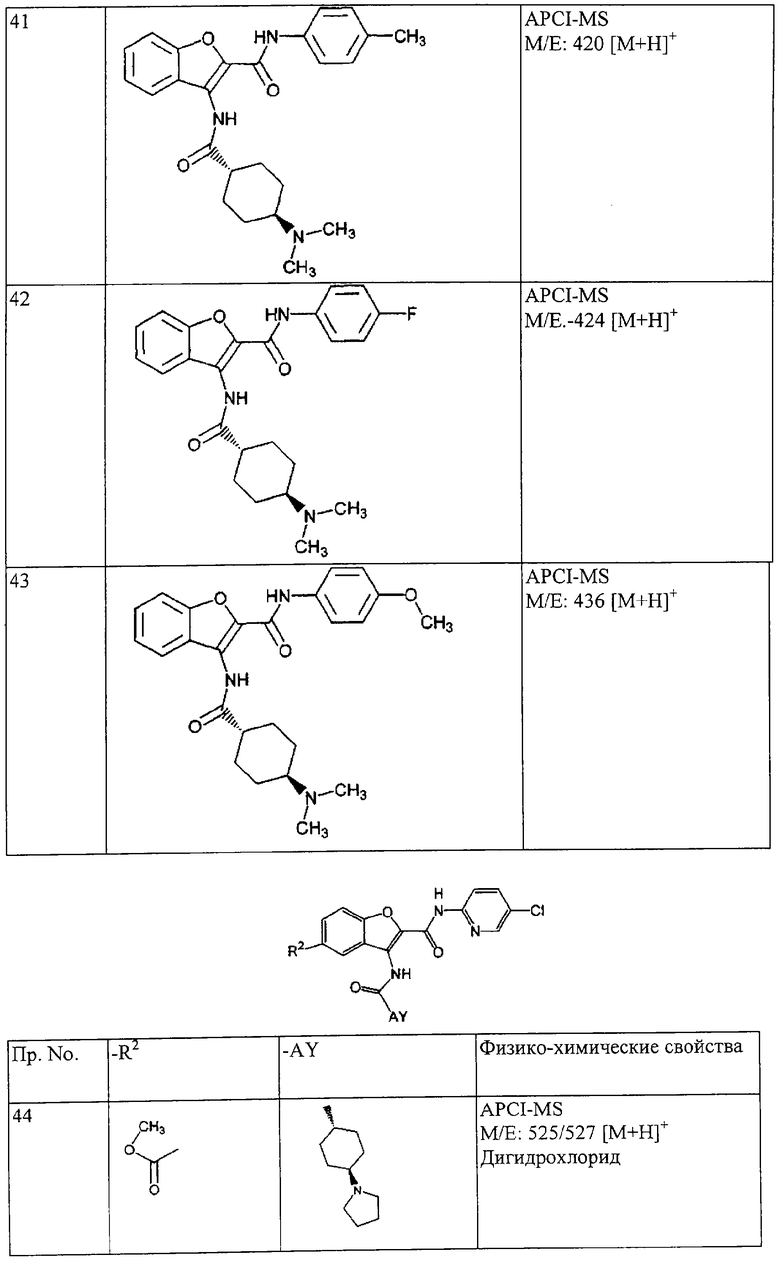
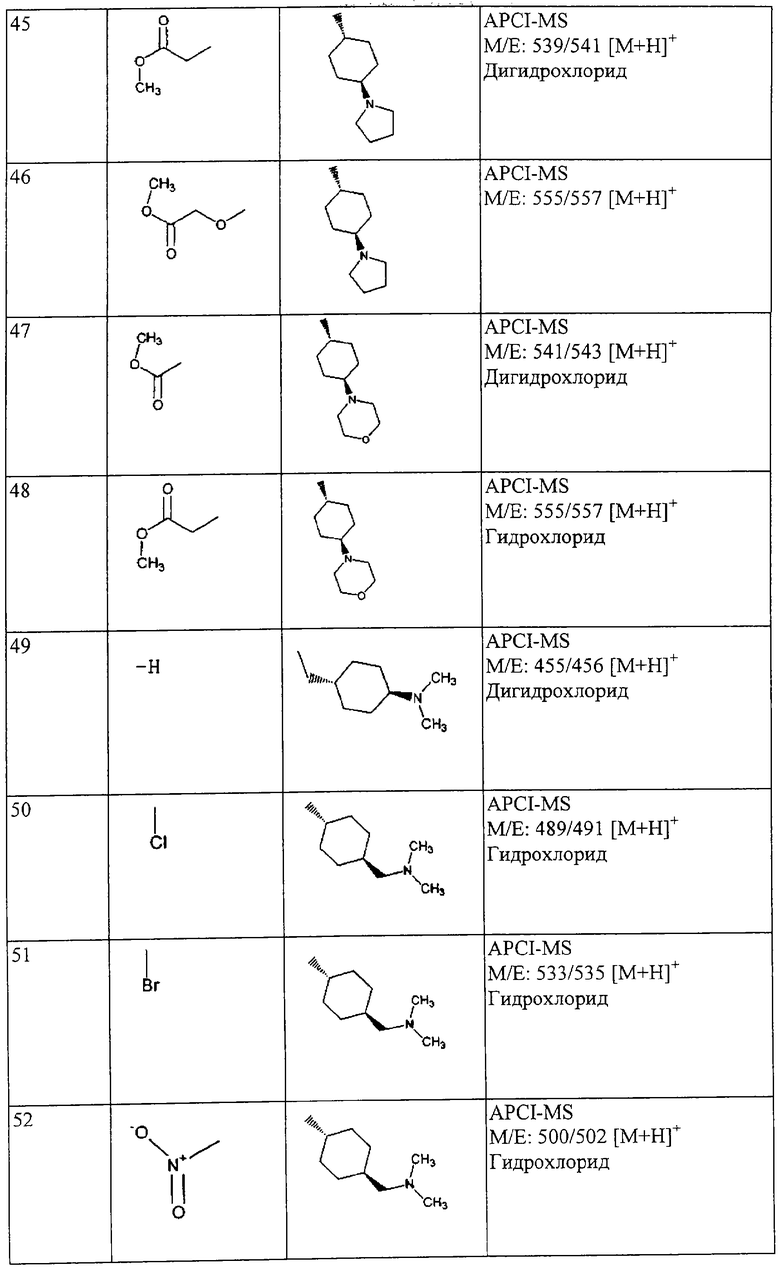
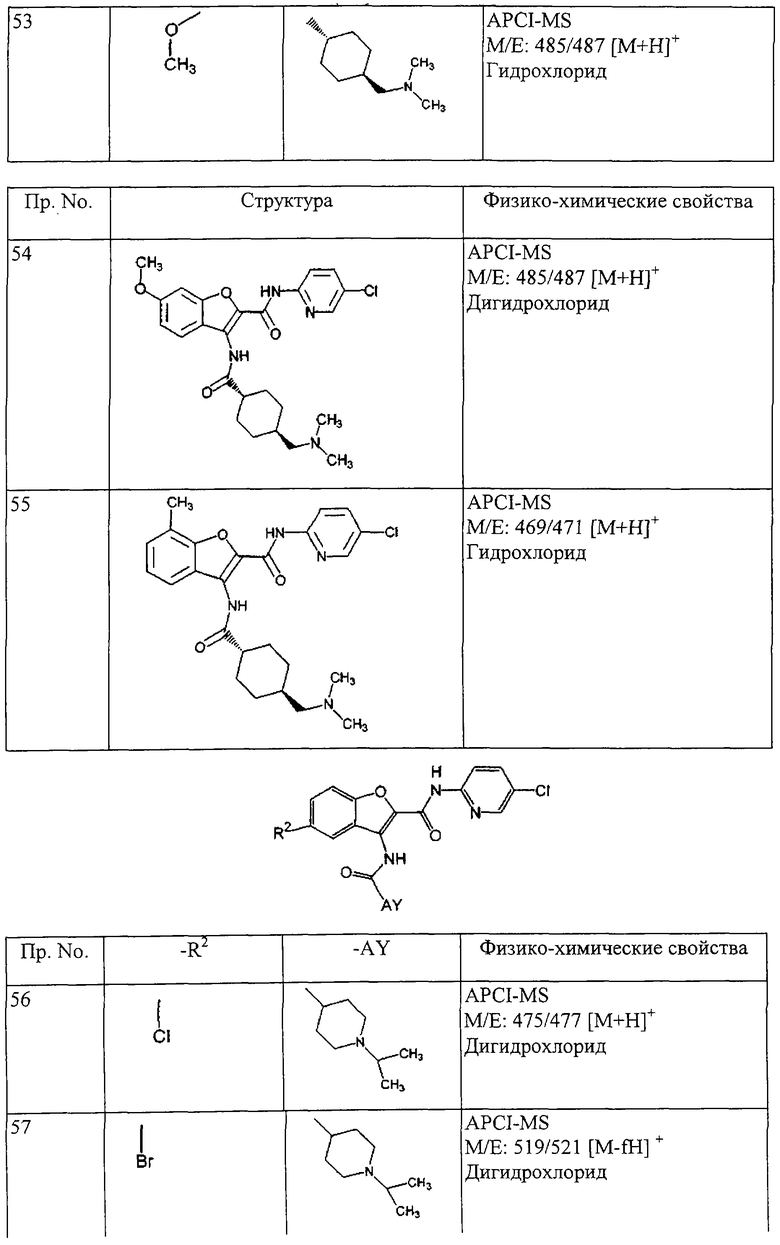
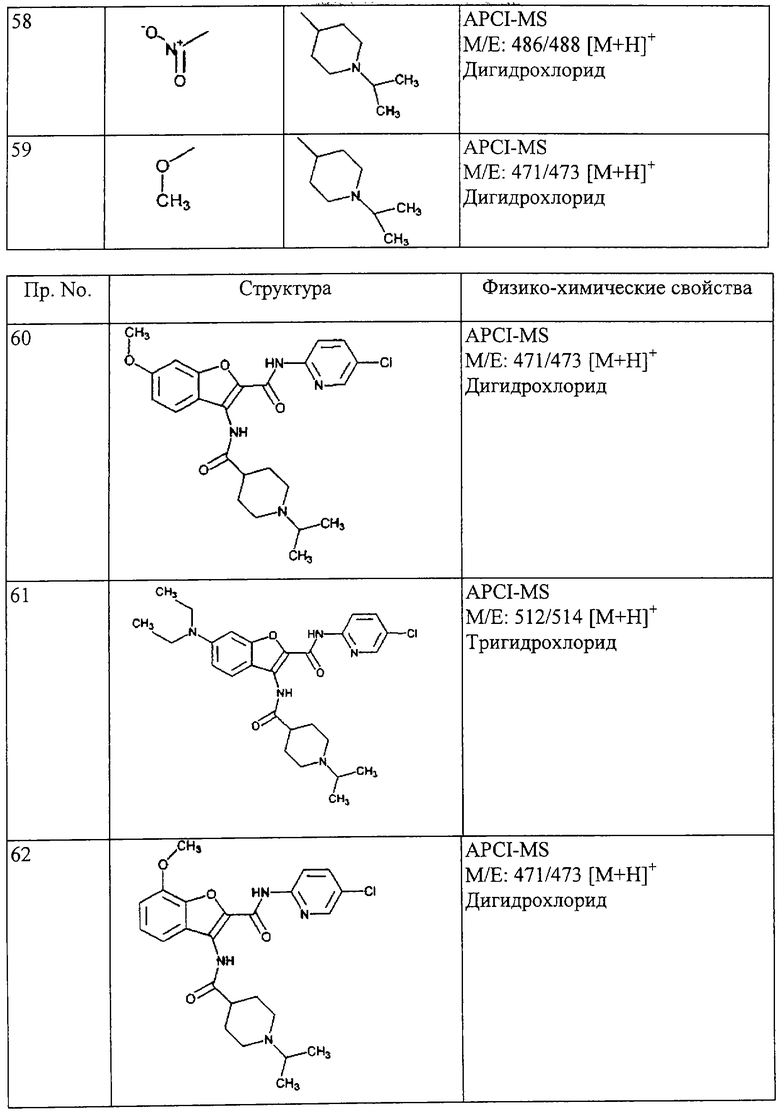
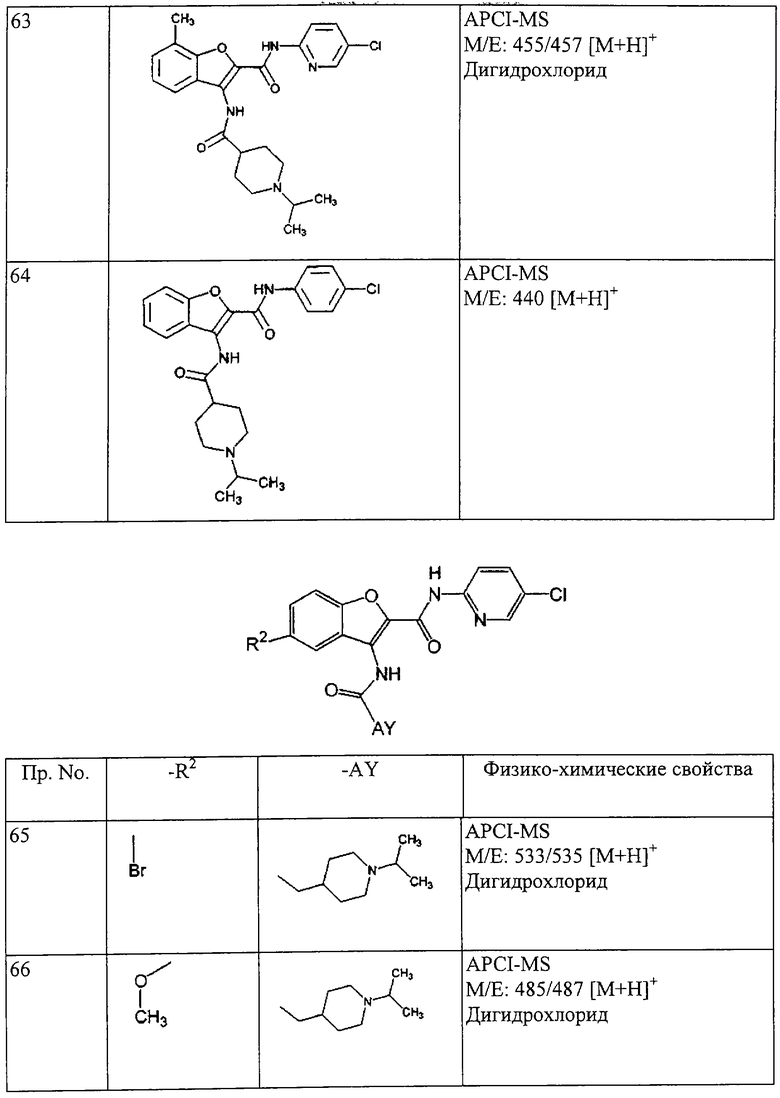
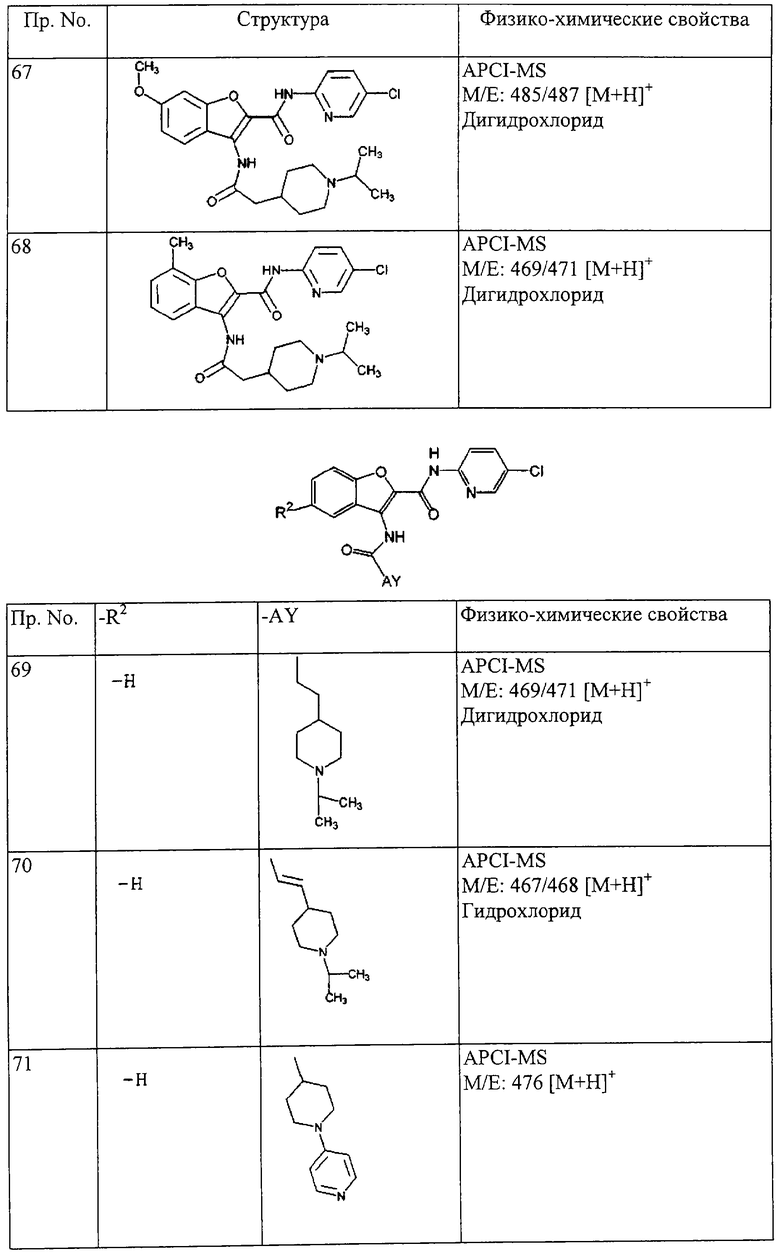
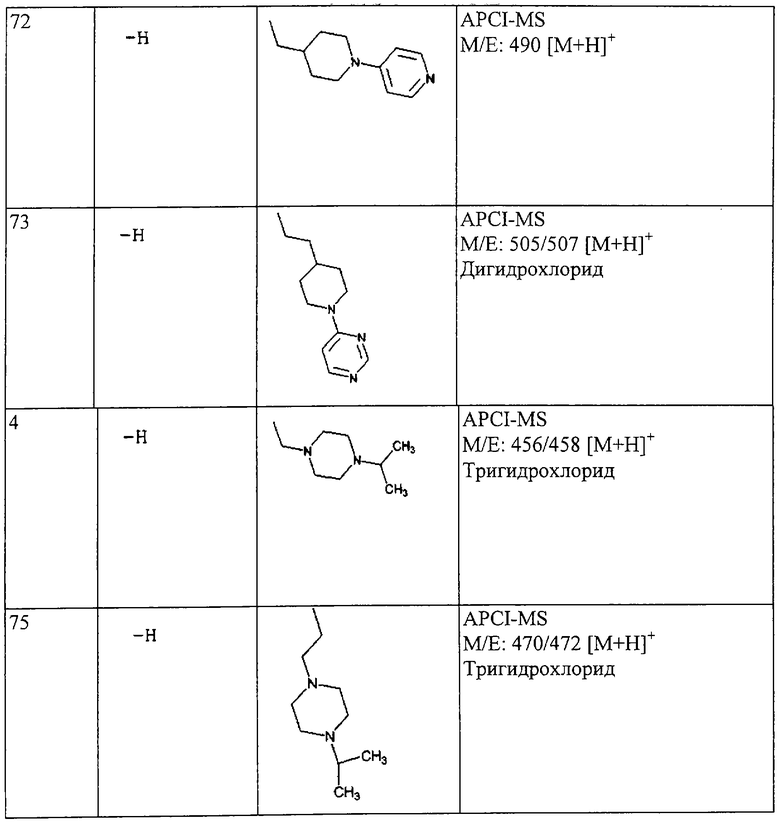
Пример 76: 3-[(1-Изопропилпиперидин-4-ил)карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
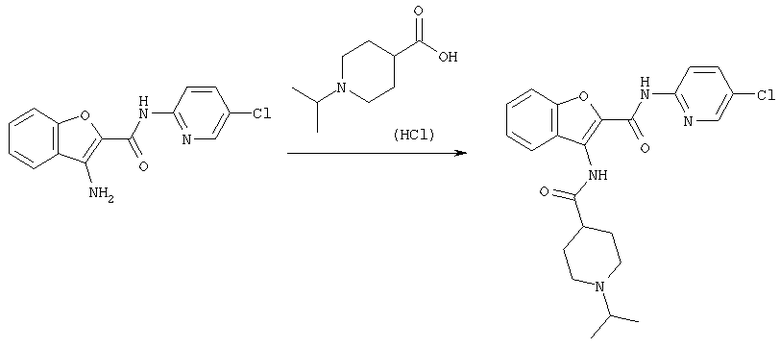
3-Амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (201 мг), полученный в примере приготовления 74, растворяют в N,N-диметилформамиде (6 мл) и последовательно добавляют гидрохлорид (1-изопропилпиперидин-4-ил) карбоновой кислоты (199 мг), полученный в примере приготовления 130, 4-диметиламинопиридин (137 мг) и гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (203 мг), после чего смесь перемешивают при температуре 60°С в течение 4 часов. Реакционный раствор разбавляют этилацетатом и водой и выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и пропускают через подушку из NH-силикагеля. Растворитель выпаривают при пониженном давлении и полученный осадок очищают HPLC с рециклом и суспендируют в смеси диэтиловый эфир/н-гексан. Осадки собирают фильтрованием, что дает названное соединение (174 мг). APCI-MS М/Е: 441 [M+H]+.
Пример 77: Транс-5-карбокси-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
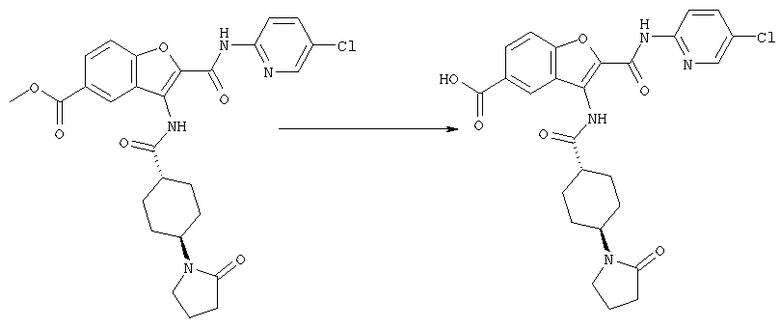
Транс-5-метоксикарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (710 мг), полученный в примере 1, суспендируют в смеси тетрагидрофуран-метанол (1:1, 10 мл) и добавляют 4N водный раствор гидроксида натрия (2 мл) при охлаждении льдом. Смесь нагревают до комнатной температуры и перемешивают в течение 18 часов. Реакционный раствор концентрируют при пониженном давлении и выливают ледяную воду и смесь нейтрализуют 10% соляной кислотой. Осадки собирают фильтрованием, промывают водой и сушат, что дает названное соединение (655 мг).
ESI-MS М/Е: 523/525 [M-Н]-.
Примеры 78-86
Соответствующие сложные эфиры карбоновой кислоты обрабатывают способом, аналогичным образом, как в примере 77, что дает следующие соединения в свободном виде, которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.

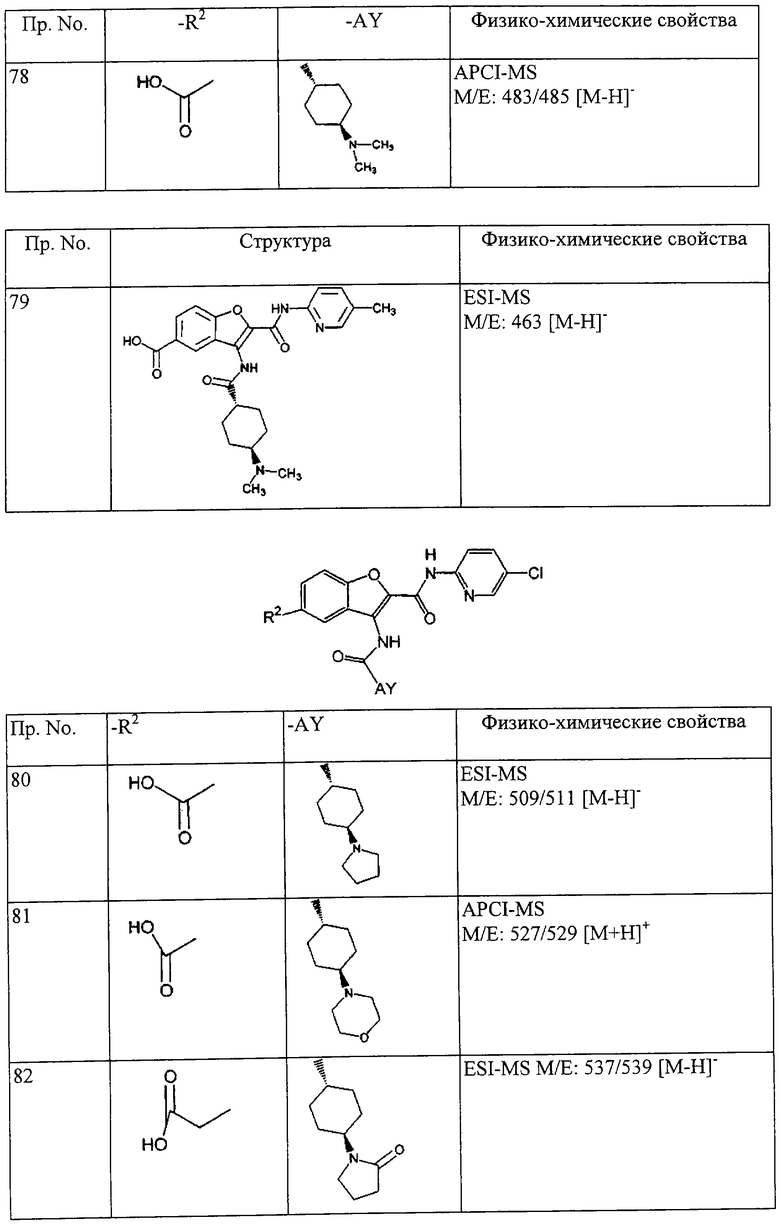
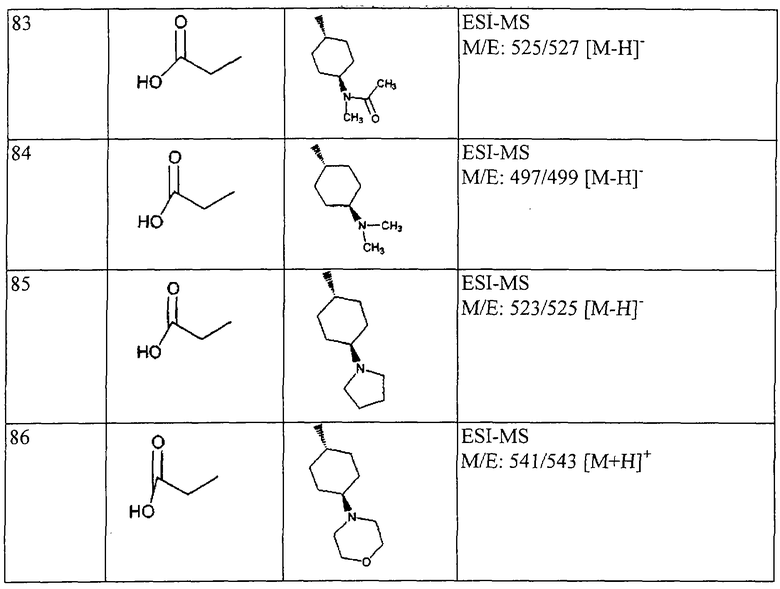
Пример 87: Транс-5-(морфолин-4-илкарбонил)-3-[4-(2-оксо-пирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
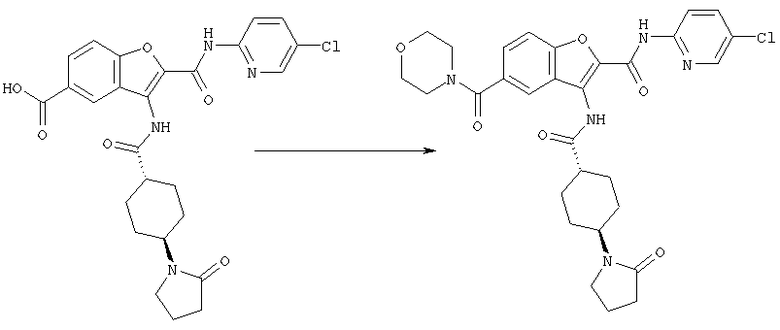
Транс-5-карбокси-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (830 мг), полученный в примере 77, суспендируют в N,N-диметилформамидпиридине (1:1, 30 мл) и добавляют последовательно морфолин (196 мг), 1-гидроксибензотриазол (406 мг) и гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (576 мг) при охлаждении льдом, после чего смесь перемешивают при комнатной температуре в течение 17 часов. В реакционный раствор выливают ледяную воду и насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют этилацетатом, промывают водой и насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ). Полученный осадок суспендируют в смеси этилацетат-н-гексан и осадки собирают фильтрованием и сушат, что дает названное соединение (805 мг). APCI-MS М/Е: 594/596 [M+H]+.
Примеры 88-143
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере 87, что дает следующие соединения в свободной форме, которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
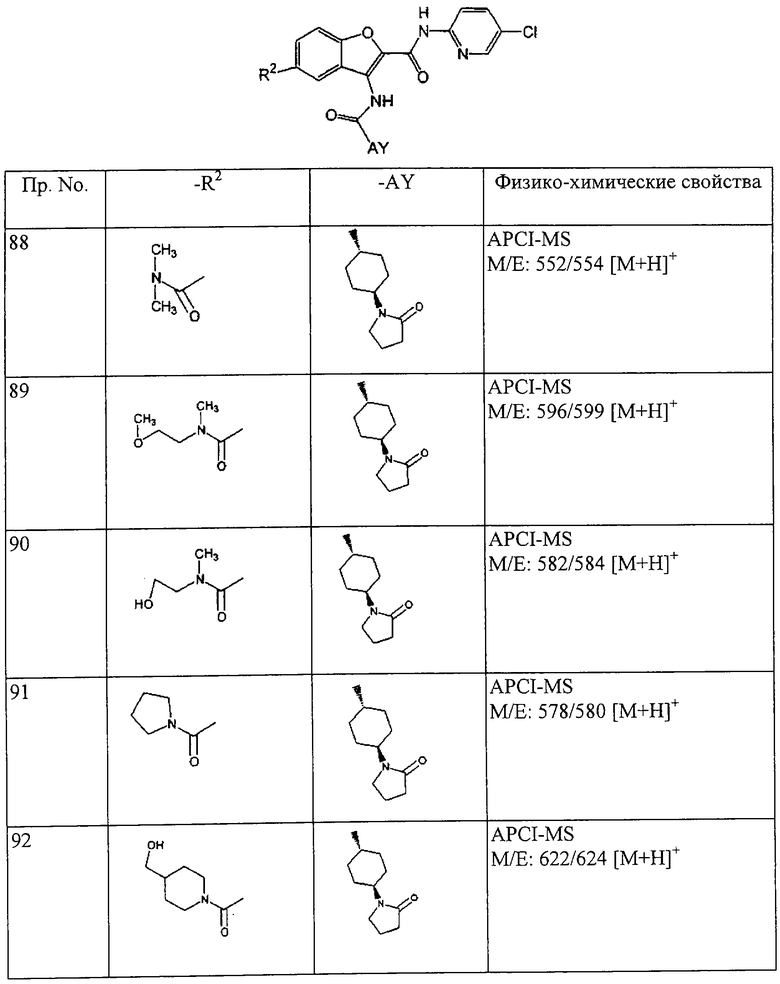
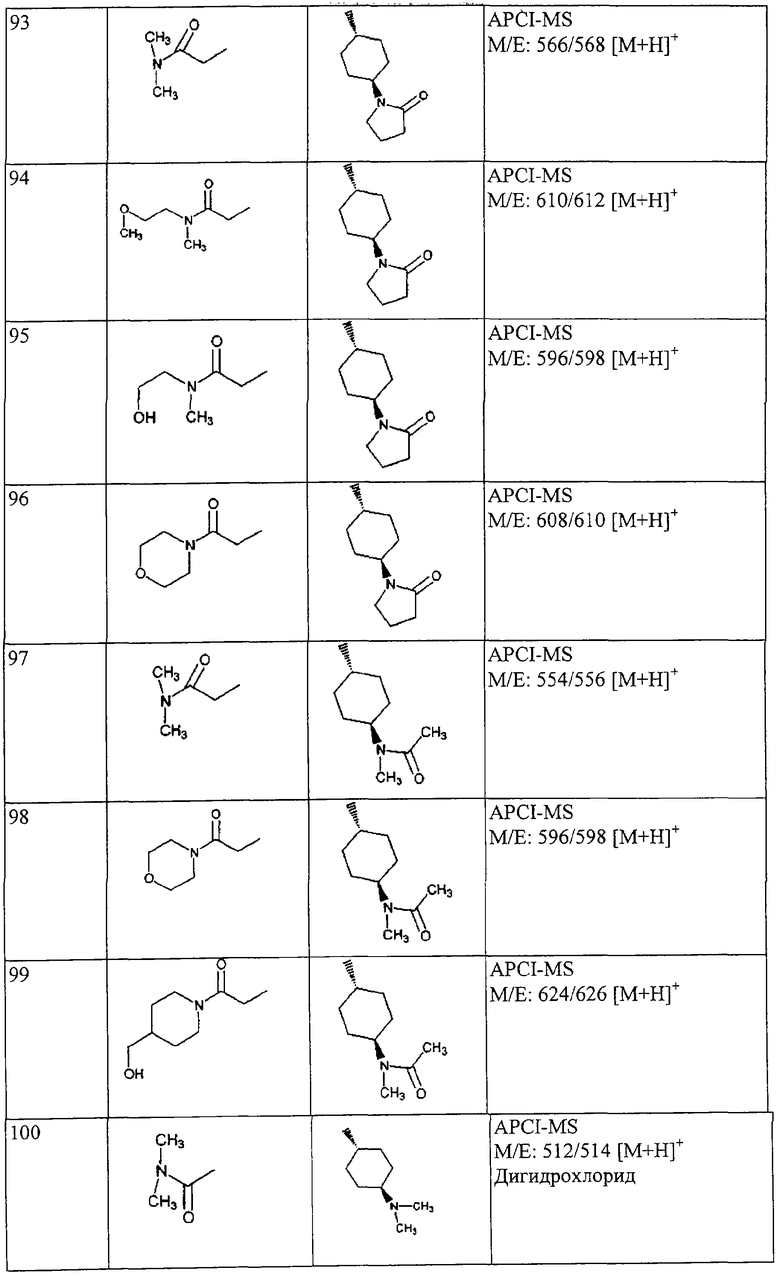
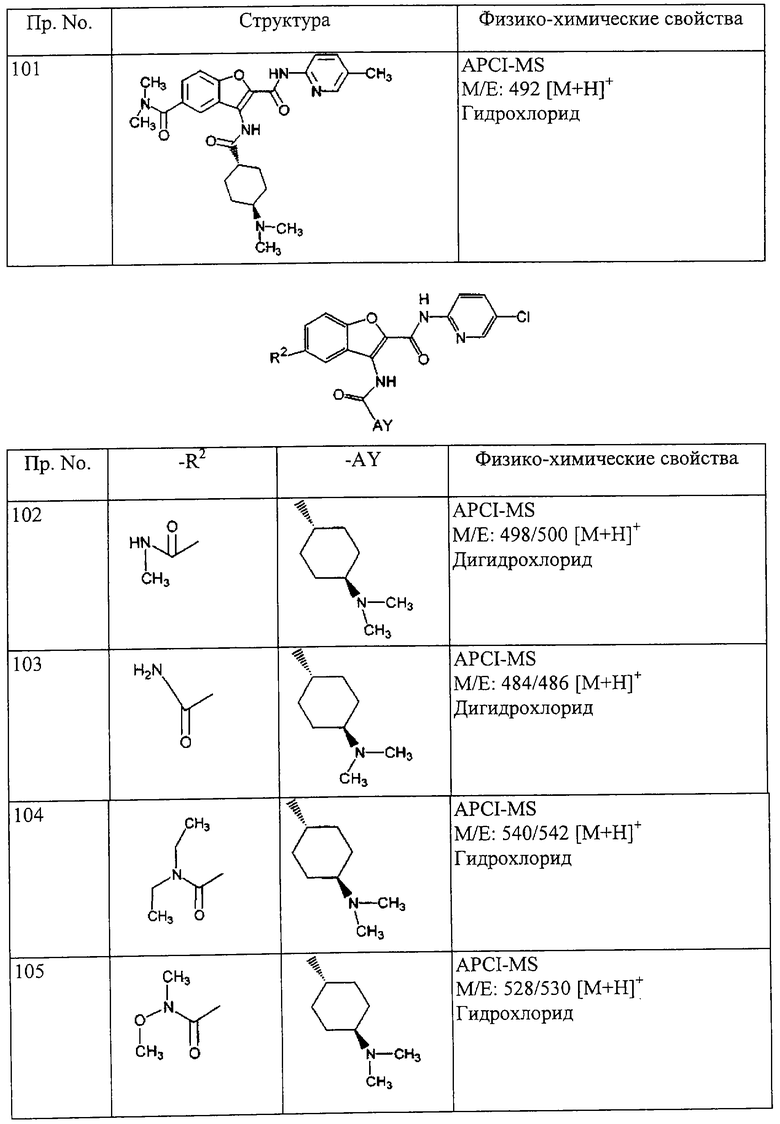
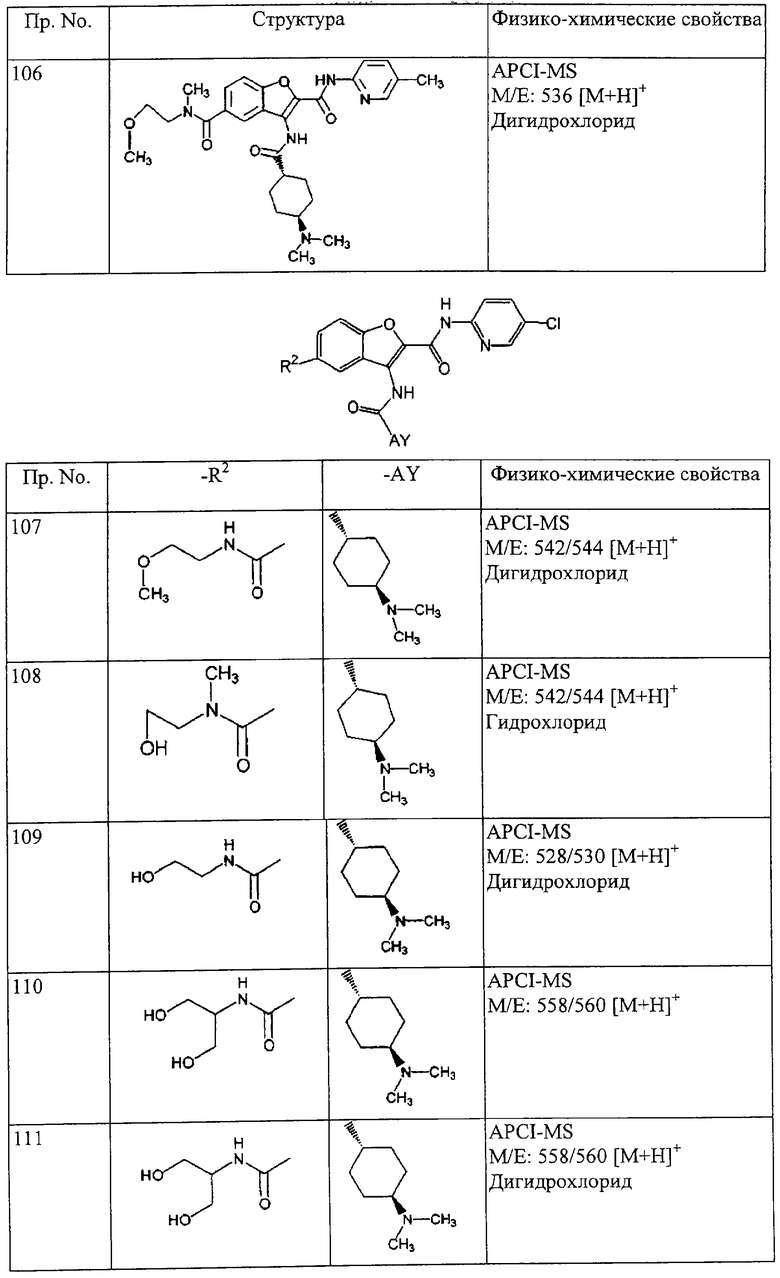
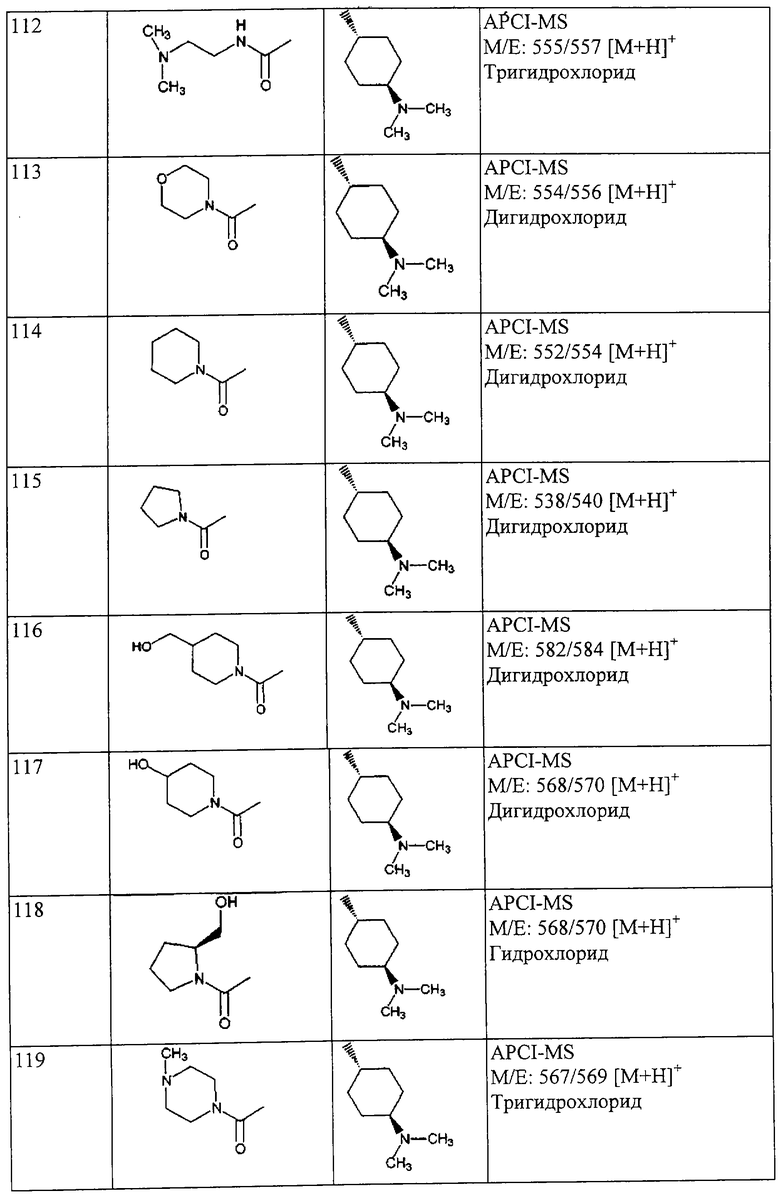
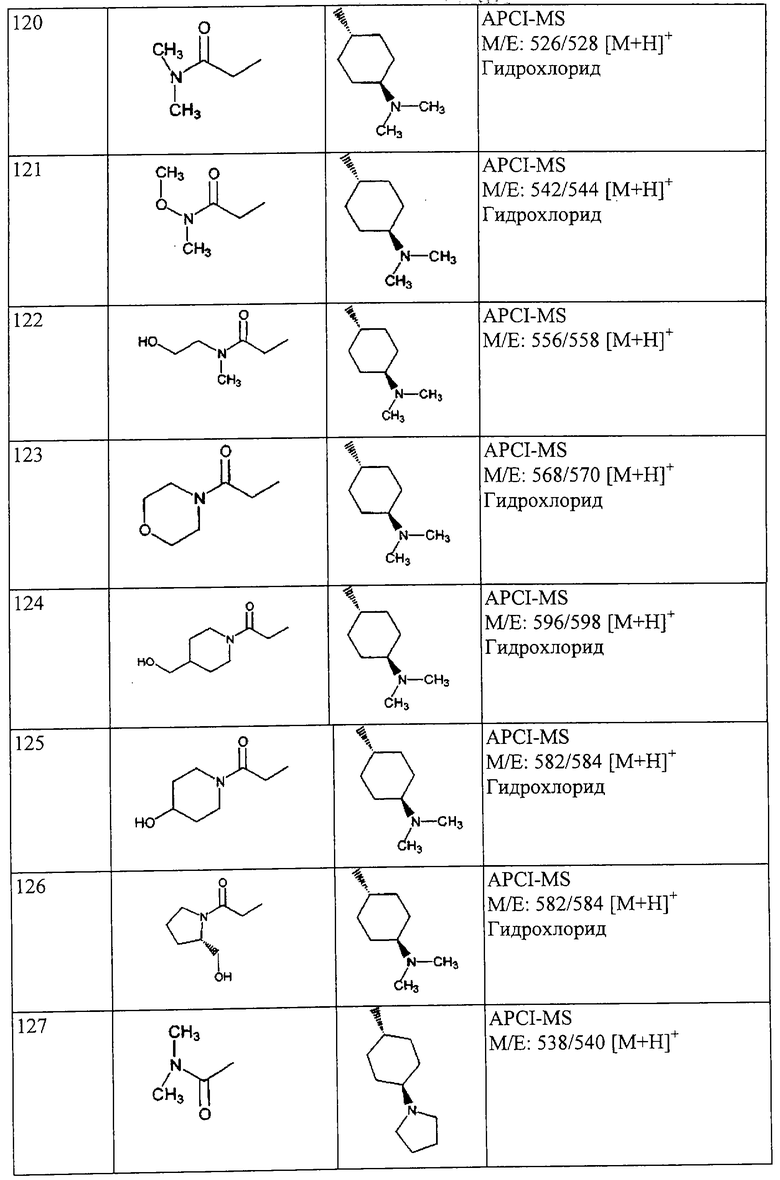
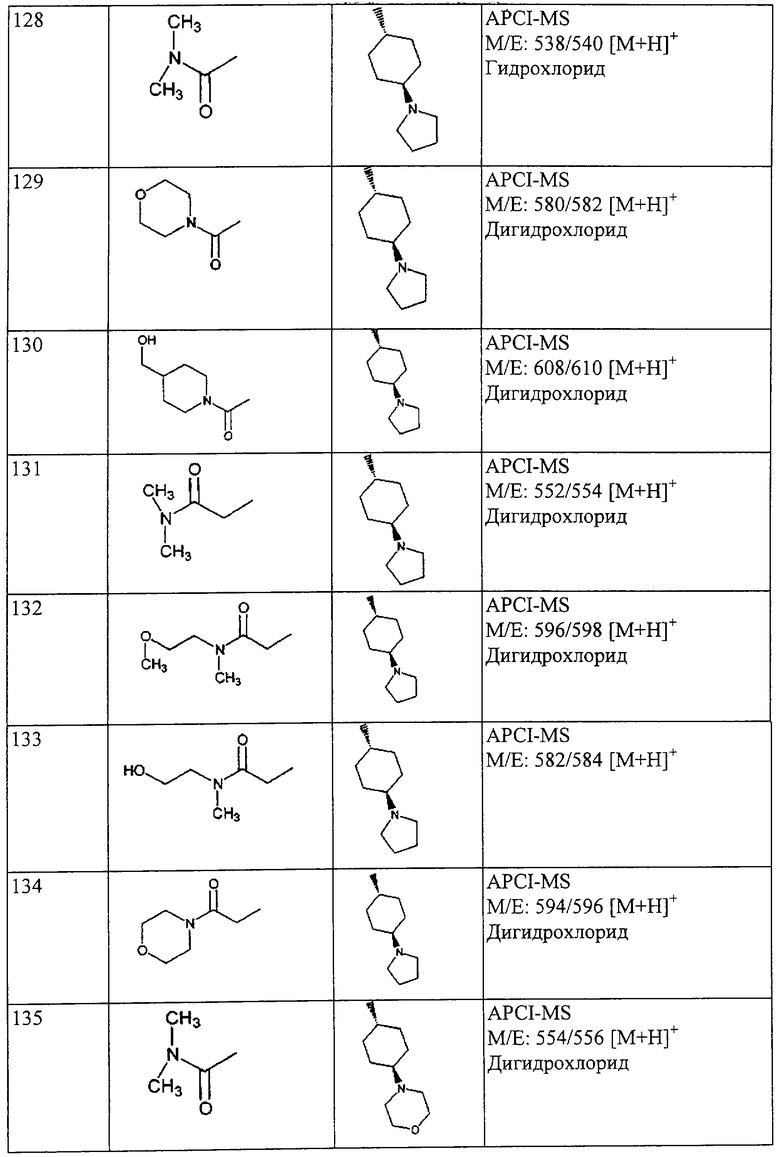
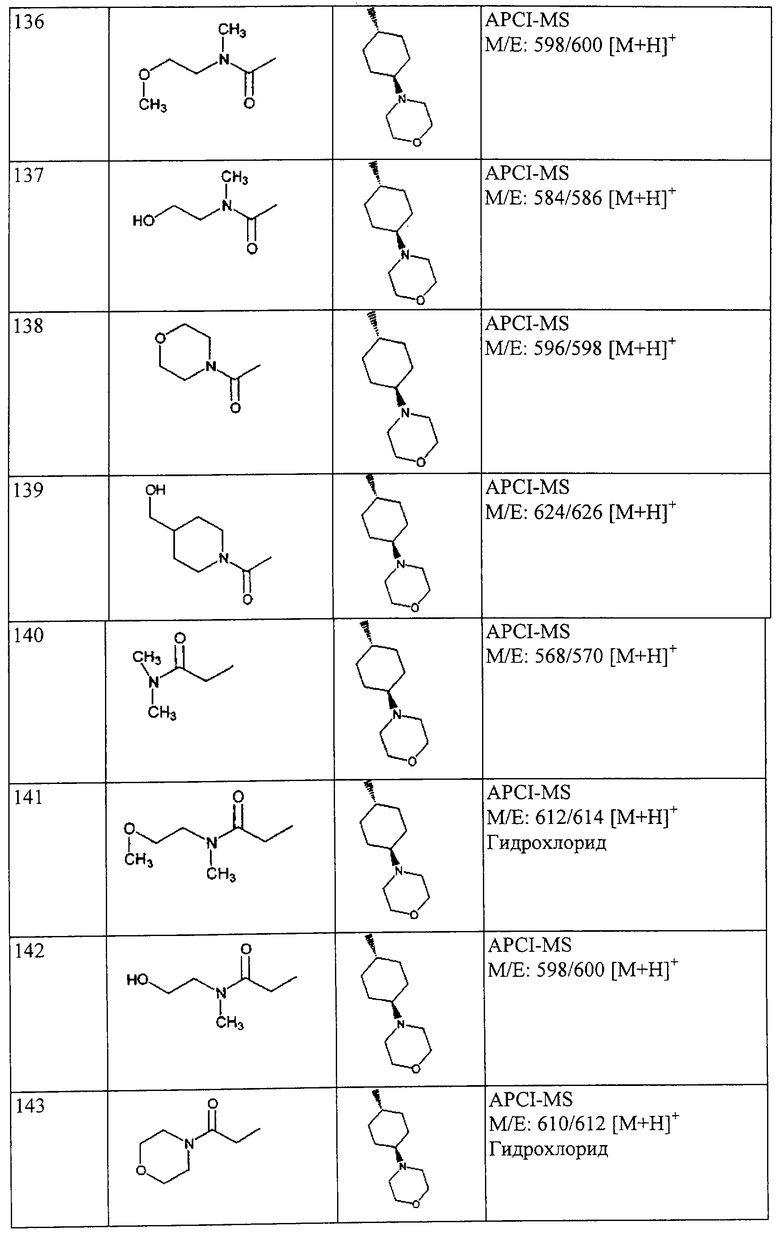
Пример 144: Транс-5-(4,5-дигидроксазол-2-ил)-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
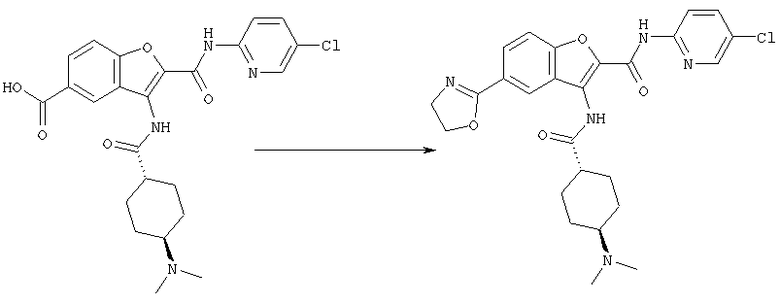
Транс-5-карбокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (220 мг), полученный в примере 78, суспендируют в пиридине (3 мл) и добавляют последовательно 2-бромид бромэтиламмония (125 мг), раствор 1,0 М 1-гидрокси-бензотриазол-N,N-диметил-формамида (600 мкл) и гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (115 мг) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 2,5 дней. Реакционный раствор выливают в ледяную воду и насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ, затем хлороформ/этилацетат =4/1) и полученный осадок суспендируют в диизопропиловом эфире. Осадки собирают фильтрованием и сушат, что дает названное соединение (117 мг). APCI-MS М/Е: 510/512 [M+H]+.
Пример 145: Транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-(2-гидроксиэтил)-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид
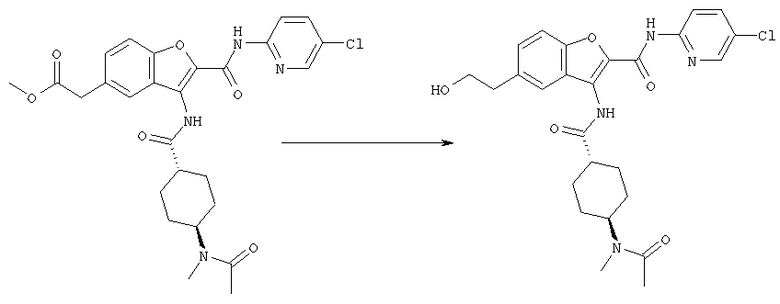
Транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-метоксикарбонилметил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,95 г), полученный в примере 2, суспендируют в тетрагидрофуране (65 мл) и добавляют боргидрид лития (238 мг), после этого смесь перемешивают при комнатной температуре в течение 12 часов. В реакционный раствор вливают 10% раствор соляной кислоты при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 15 минут. Затем реакционный раствор нейтрализуют насыщенным водным раствором гидрокарбоната натрия и экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат, затем хлороформ/метанол =40/1) и полученный осадок суспендируют в диэтиловый эфир. Осадки собирают фильтрованием, что дает названное соединение (2,24 г). APCI-MS М/Е: 513/515 [M+H]+.
Примеры 146-149
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере 145, что дает последующие соединения в свободном виде, которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
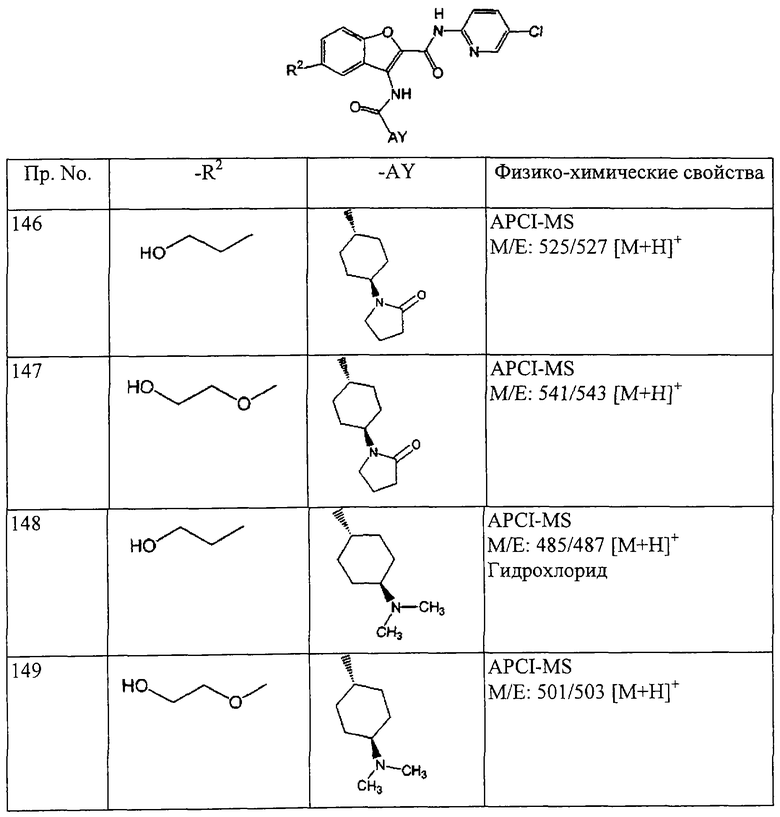
Пример 150: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-гидроксиметил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
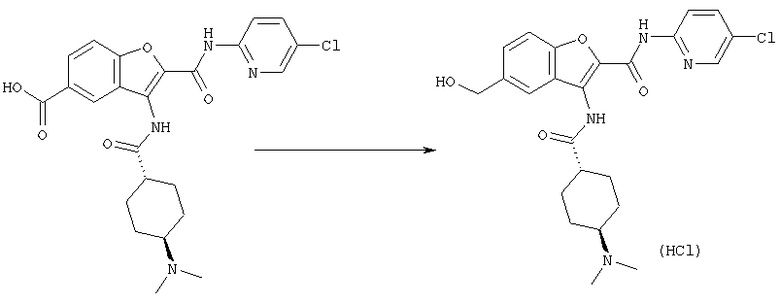
Транс-5-карбокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (243 мг), полученный в примере 78, суспендируют в тионилхлориде (2,5 мл) и смесь перемешивают при комнатной температуре в течение 10 минут, затем перемешивают при температуре 50°С в течение 10 минут. Смесь охлаждают до комнатной температуры и вновь перемешивают в течение часа. Реакционный раствор концентрируют досуха при пониженном давлении. Полученный осадок суспендируют в смеси тетрагидрофуран/хлороформ (2:1, 15 мл), добавляют боргидрид натрия (150 мг) и смесь перемешивают при комнатной температуре в течение ночи. Затем в реакционный раствор выливают 1N соляную кислоту при охлаждении льдом и смесь перемешивают в течение 0,5 часа. Затем выливают насыщенный водный раствор гидрокарбоната натрия, после чего смесь экстрагируют хлороформом. Органический слой промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ, затем смесь хлороформ/метанол =200/1), что дает транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-гидроксиметил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (46 мг). Этот продукт растворяют в хлороформе (1 мл) и добавляют 2N хлористый водород в метаноле (0,1 мл) и реакционный раствор концентрируют при пониженном давлении. Полученный осадок суспендируют в смеси этилацетат-метанол и осадки собирают фильтрованием и сушат, что дает названное соединение (45 мг). APCI-MS М/Е: 471/473 [M+H]+.
Пример 151: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-6-гидрокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
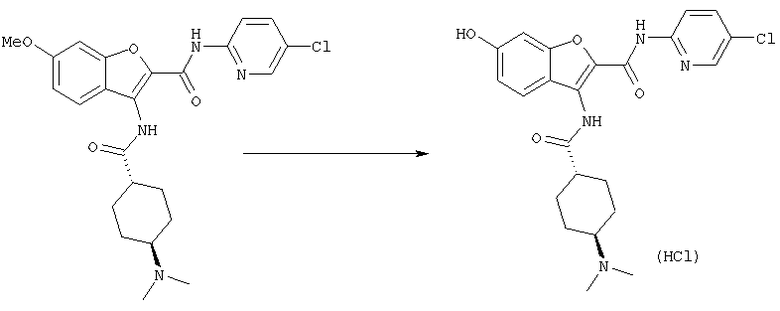
В суспензию транс-3-[4-(диметиламино)циклогексилкарбониламино]-6-метокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида (473 мг), полученную в примере 23, в дихлорметане (20 мл) добавляют по каплям трибромид бора (3,5 г) в течение 2 минут при температуре -78°С. Смесь перемешивают при комнатной температуре в течение 4 дней и реакционный раствор выливают в ледяную воду, нейтрализуют насыщенным водным раствором гидрокарбоната натрия и экстрагируют смесью растворителей из этилацетат-тетрагидрофурана. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок суспендируют в смеси хлороформ/диэтиловый эфир и осадки собирают фильтрованием и сушат, что дает транс-3-[4-(диметиламино)циклогексилкарбониламино]-6-гидрокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (335 мг). Этот продукт (48 мг) суспендируют в метаноле и обрабатывают 4N хлористым водородом в диоксане, что дает названное соединение (54 мг).
APCI-MS M/E: 457/459 [M+H]+.
Пример 152: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-гидрокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
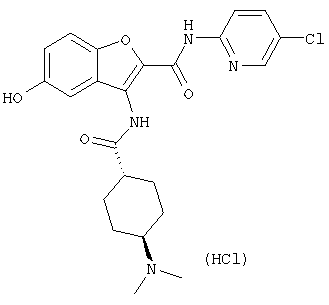
Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-метилокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (473 мг), полученный в примере 19, обрабатывают способом, аналогичным описанному в примере 151, что дает названное соединение (33 мг). APCI-MS M/E: 457/459 [М+H]+.
Пример 153: Транс-6-трет-бутоксикарбонилметокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
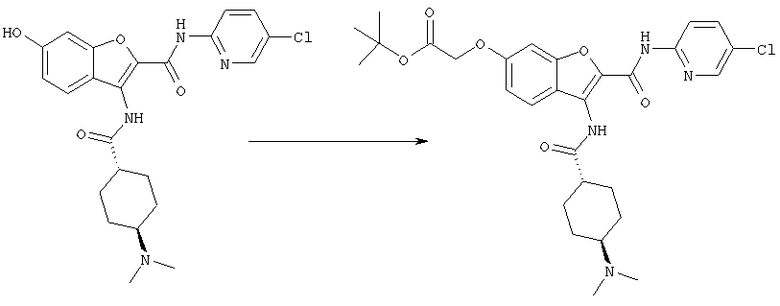
Транс-3-[4-(диметиламино)циклогексилкарбониламино]-6-гидрокси-N-(5-хлор-пиридин-2-ил)бензофуран-2-карбоксамид (90 мг), полученный в примере 151, растворяют в N,N-диметилформамиде (2 мл) и добавляют карбонат цезия (110 мг) и бромацетат трет-бутила (35,5 мкл). Смесь перемешивают при комнатной температуре в течение 12 часов и затем перемешивают при температуре 50°С в течение 2,5 часов. Реакционному раствору дают возможность отстояться, чтобы остыть, и затем его разбавляют водой и экстрагируют этилацетатом. Органический слой концентрируют при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь гексан/этилацетат =1/1, затем этилацетат), что дает названное соединение (21 мг). APCI-MS М/Е: 571/573 [M+H]+.
Примеры 154-155
Транс-3-[4-(диметиламино)циклогексилкарбониламино]-6-гидрокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид, полученный в примере 151, и соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 153, что дает последующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
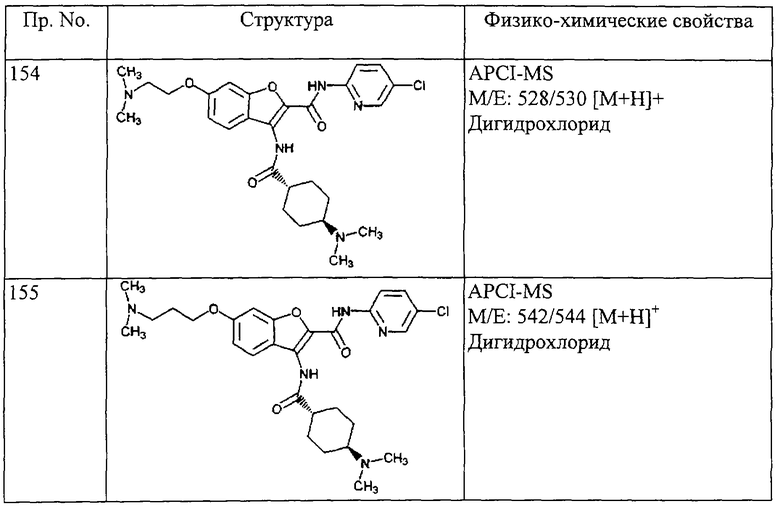
Пример 156: Транс-6-карбоксиметилокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
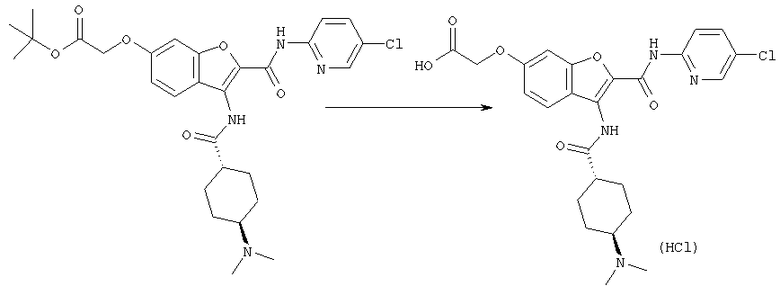
Транс-6-трет-бутоксикарбонилметилокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (21 мг), полученный в примере 153, суспендируют в смеси 4N хлористый водород в диоксане (8 мл) и смесь перемешивают при комнатной температуре в течение 28 часов. Реакционный раствор разбавляют диэтиловым эфиром и осадки собирают фильтрованием, промывают несколько раз диэтиловым эфиром и сушат, что дает названное соединение (17 мг). APCI-MS М/Е: 515/517 [M+H]+.
Пример 157: Транс-5-карбоксиметилокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
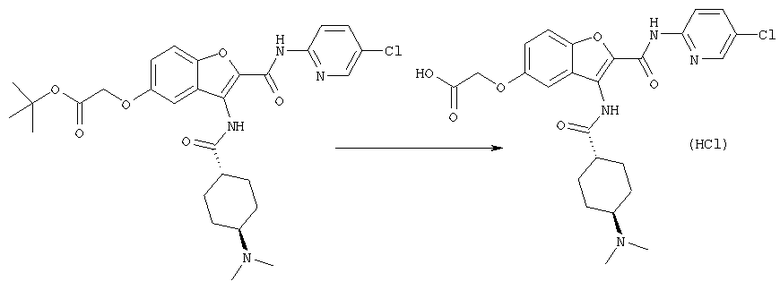
Транс-5-трет-бутоксикарбонилметокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (1,92 г), полученный в примере 31, растворяют в 6N соляной кислоте (40 мл) и смесь перемешивают при комнатной температуре в течение 2 часов. В реакционный раствор добавляют изопропанол (100 мл) и выпавшее в осадок твердое вещество собирают фильтрованием, промывают изопропанолом и диэтиловым эфиром и сушат при пониженном давлении, что дает названное соединение (1,86 г). APCI-MS М/Е: 515/517 [M+H]+.
Примеры 158-179
Транс-5-карбоксиметилокси-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид, полученный в примере 157, и соответствующие исходные соединения, обрабатывают способом, аналогичным описанному в примере 87, что дает последующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
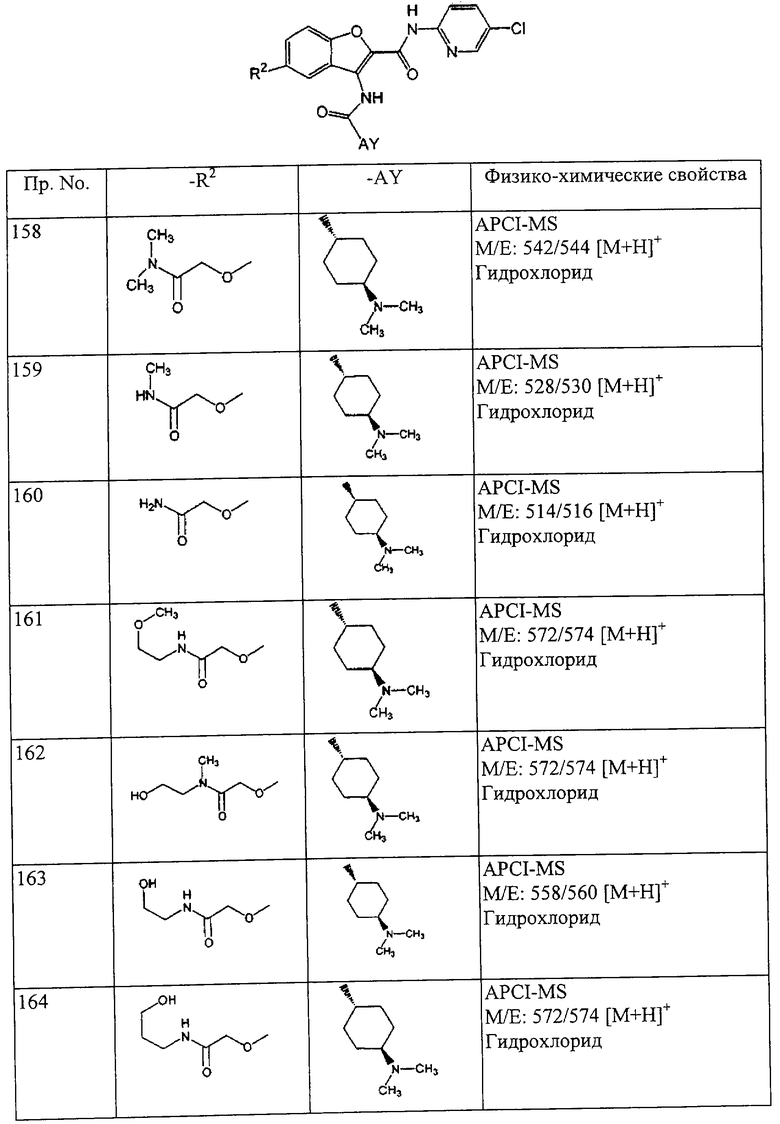
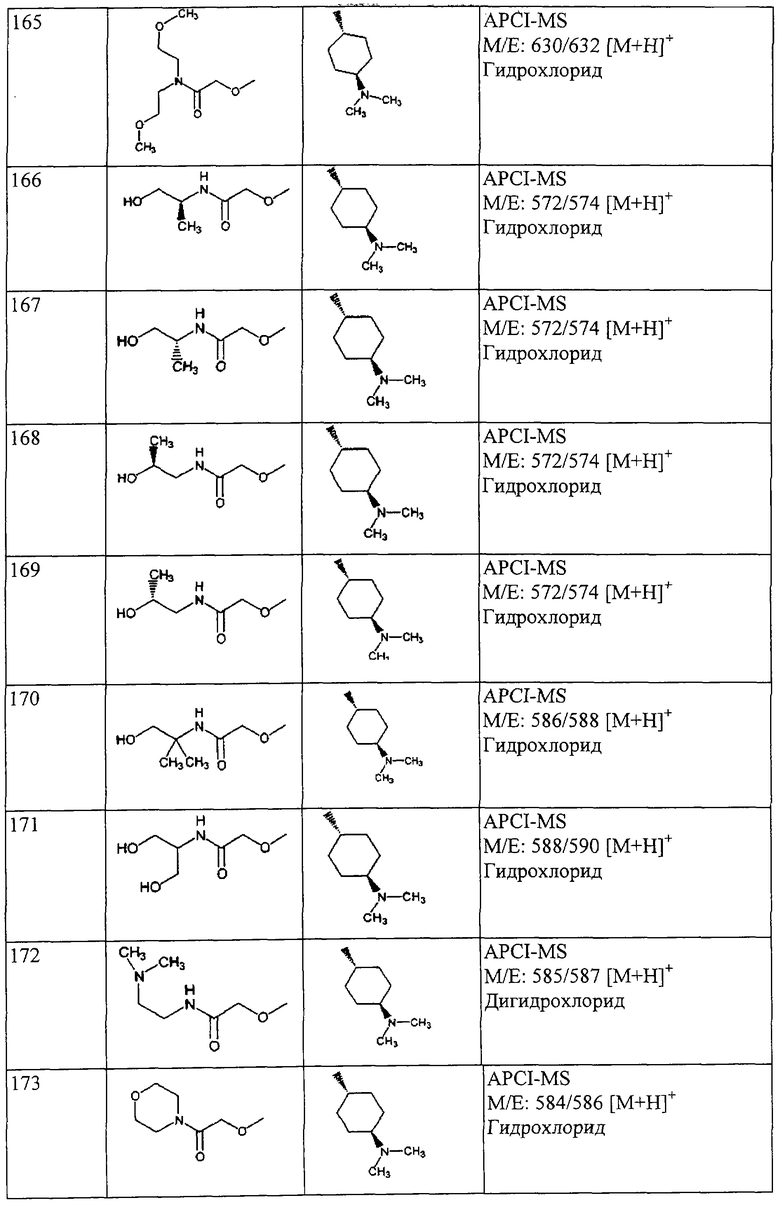
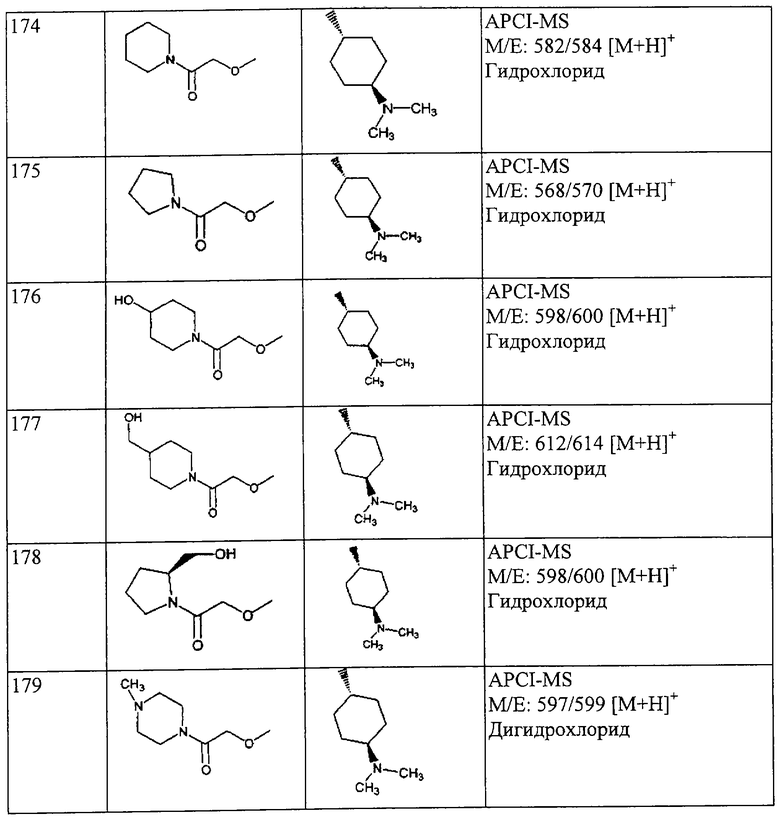
Пример 180: Транс-5-амино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
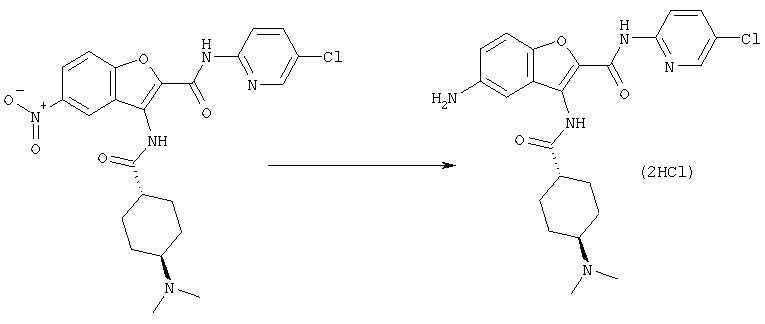
Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-нитро-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (3,00 г), полученный в примере 18, суспендируют в этаноле (100 мл) и добавляют хлорид олова(II) (безводный) (7,02 г) и воду (1,0 мл). Смесь нагревают при температуре кипения с обратным холодильником в течение 7 часов и дают возможность отстояться, чтобы остыть. В реакционный раствор добавляют 10% водный раствор гидроксида натрия (30 мл) и тетрагидрофуран (200 мл) и смесь перемешивают при комнатной температуре в течение часа. Нерастворимые продукты отфильтровывают через целит, фильтрат концентрируют при пониженном давлении и очищают с помощью хроматографии на колонке из силикагеля (элюент: н-гексан/этилацетат =1/1, затем хлороформ/этилацетат =1/1). Полученный осадок суспендируют в смеси этилацетат/н-гексан и осадки собирают фильтрованием и сушат, что дает транс-5-амино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид (1,43 г). Этот продукт (35 мг) растворяют в этаноле и обрабатывают 4N хлористым водородом/этилацетатом, что дает названное соединение (43 мг). APCI-MS М/Е: 456/458 [M+H]+.
Пример 181: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-метиламино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
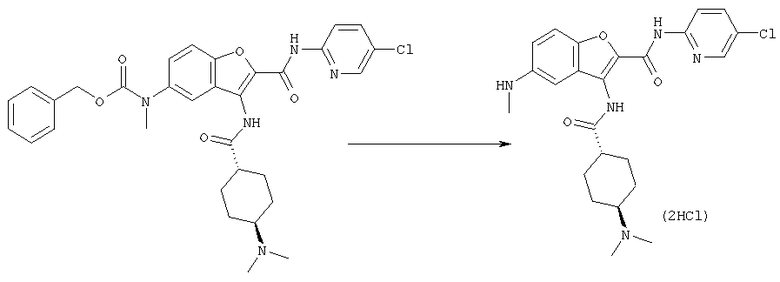
В транс-5-[N-(бензилоксикарбонил)-N-метиламино]-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (100 мг), полученный в примере 22, добавляют 30% бромистый водород в уксусной кислоте (2 мл) и смесь перемешивают при комнатной температуре в течение 2 часов. В реакционный раствор добавляют диэтиловый эфир (20 мл) и осадки собирают фильтрованием и суспендируют в насыщенный водный раствор гидрокарбоната натрия и экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении, что дает транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-метиламино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид. Потом этот продукт растворяют в этаноле и обрабатывают 4N хлористым водородом в этилацетате, что дает названное соединение (88 мг). APCI-MS М/Е: 470/472 [M+H]+.
Пример 182: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-(2-метиламино-этокси)-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид тригидрохлорид
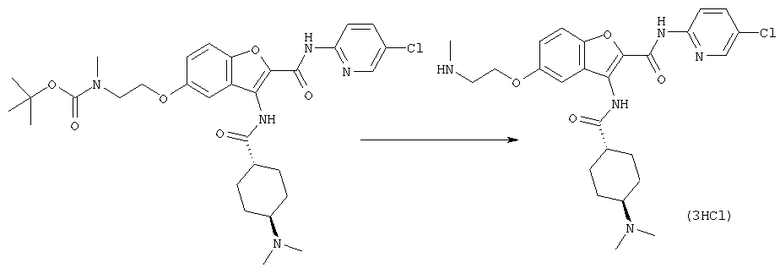
Транс-5-[2-(N-трет-бутоксикарбонил-N-метиламино)этокси]-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (300 мг), полученный в примере 36, растворяют в диоксане (5 мл) и добавляют 4N хлористый водород в диоксане (10 мл) и смесь перемешивают при комнатной температуре в течение 5 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире. Осадки собирают фильтрованием и сушат, что дает названное соединение (301 мг). APCI-MS М/Е: 514/516 [M+H]+.
Пример 183: Транс-5-(2-аминоксиэтокси)-3-[4-(2-оксо-пирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
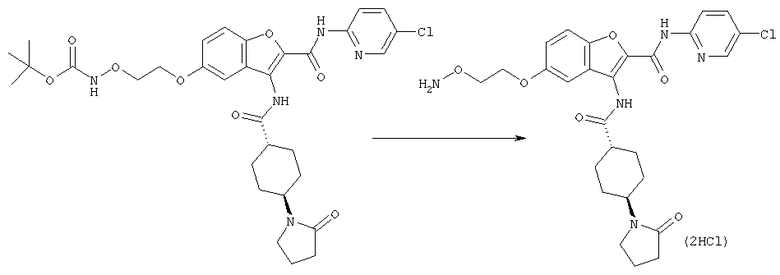
Транс-5-[2-(трет-бутоксикарбониламинокси)этокси]-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (250 мг), полученный в примере 10, обрабатывают способом, аналогичным описанному в примере 182, что дает названное соединение (334 мг). APCI-MS М/Е: 556/558 [M+H]+.
Пример 184: Транс-5-метоксиацетиламино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид гидрохлорид
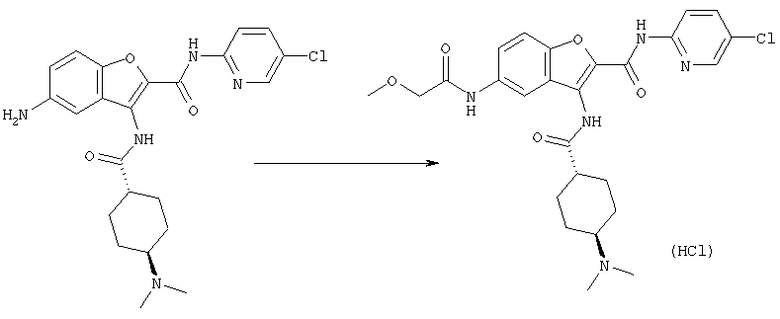
Транс-5-амино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (100 мг), полученный в примере 180, суспендируют в N,N-диметилформамид (6 мл) и добавляют последовательно метоксиуксусную кислоту (23 мг), 1-гидроксибензотриазол (39 мг) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (55 мг) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 17 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ, затем хлороформ/метанол =30/1), что дает транс-5-метоксиацетиламино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид. Потом этот продукт растворяют в этаноле и обрабатывают 4N хлористым водородом в этилацетате, что дает названное соединение (84 мг).
APCI-MS WE: 528/530 [M+H]+.
Примеры 185-188
Транс-5-амино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид, полученный в примере 180, и соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 184, в соединения в свободном виде или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.

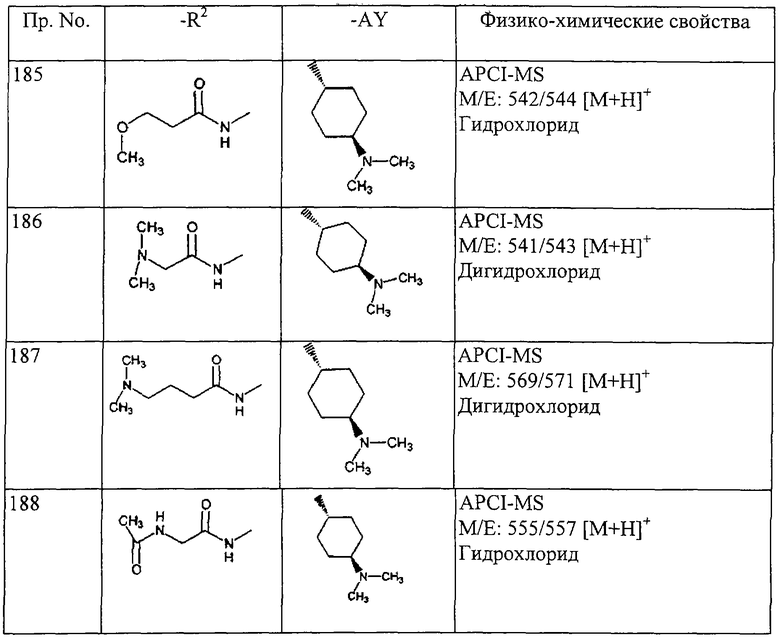
Пример 189: Транс-5-ацетоксиацетиламино-3-[4-(диметиламино)-циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид гидрохлорид
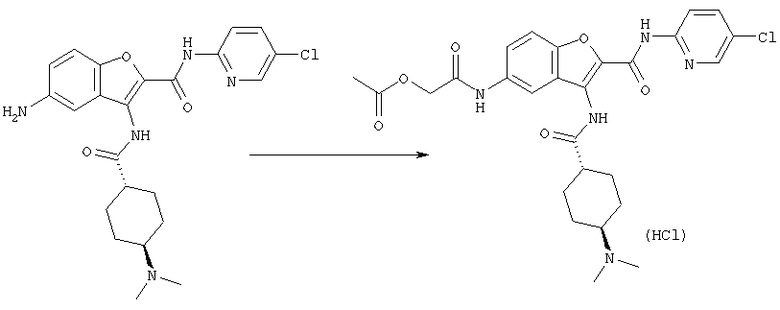
Транс-5-амино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (100 мг), полученный в примере 180, растворяют в дихлорметане (8 мл) и добавляют ацетоксиацетилхлорид (36 мг) и пиридин (36 мкл) при охлаждении льдом, после чего смесь перемешивают при комнатной температуре в течение 17 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ, затем хлороформ/метанол =50/1), что дает транс-5-ацетоксиацетиламино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (110 мг). Часть этого продукта растворяют в этаноле и обрабатывают 4N хлористым водородом в этилацетате, что дает названное соединение (16 мг). APCI-MS М/Е: 556/558 [M+H]+.
Примеры 190-196
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере 189, что дает последующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
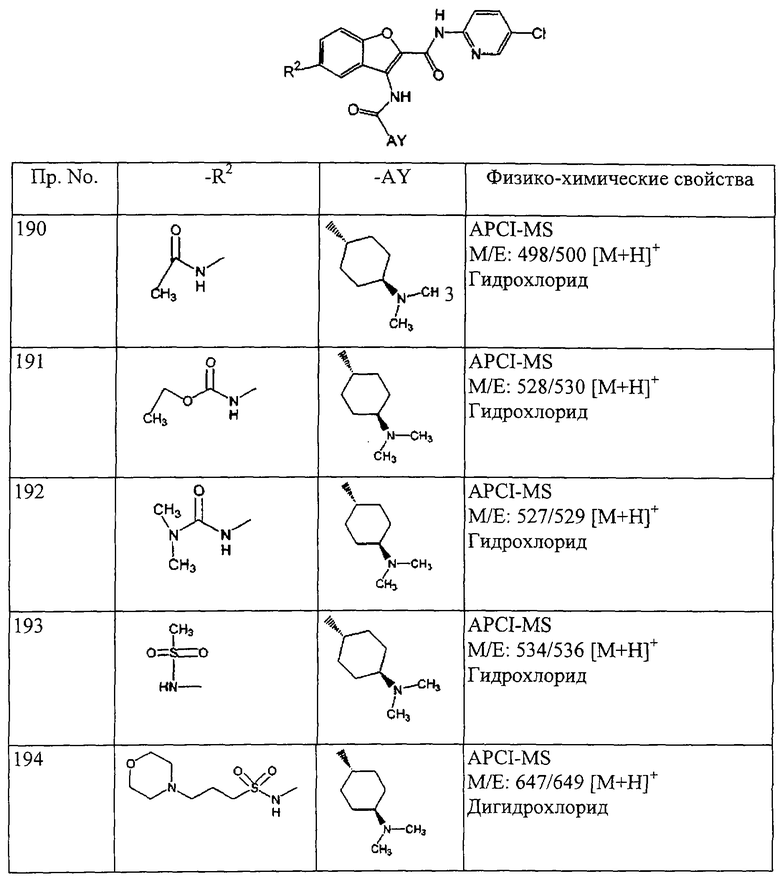
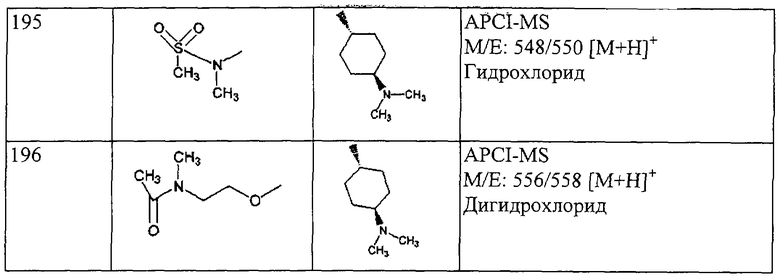
Пример 197: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-гидроксиацетил-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
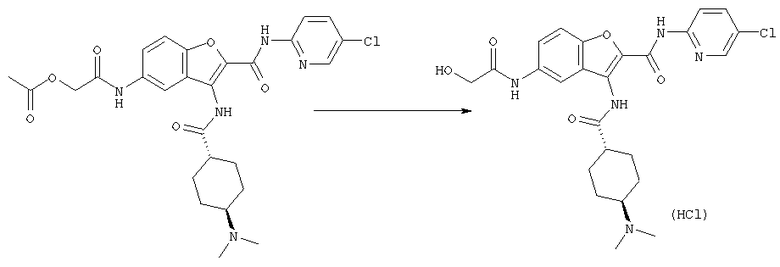
Транс-5-ацетоксиацетиламино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (70 мг), полученный в примере 189, растворяют в смеси тетрагидрофуран/метанол (1:1,8 мл) и добавляют карбонат калия (5 мг) и смесь перемешивают при комнатной температуре в течение 48 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ/метанол =30/1). Полученный транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-гидроксиацетил-амино-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид растворяют в этаноле и обрабатывают 4N хлористым водородом в этилацетате, что дает названное соединение (46 мг). APCI-MS М/Е: 514 [M+H]+.
Пример 198: Транс-5-диметиламино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
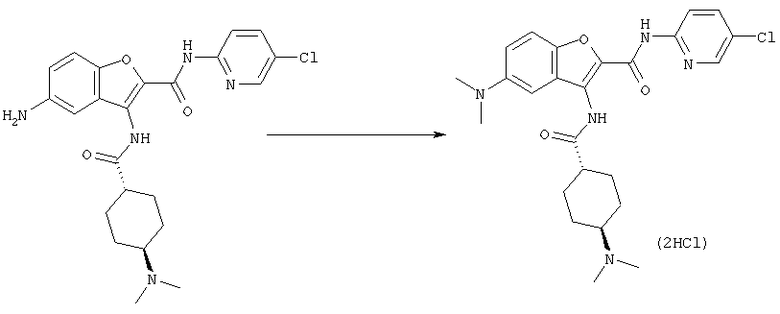
Транс-5-амино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (50 мг), полученный в примере 180, суспендируют в дихлорметане (3 мл) и добавляют последовательно 35% водный раствор формальдегида (82 мкл) и триацетоксиборгидрид натрия (70 мг) при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры и перемешивают в течение 11,5 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия при охлаждении льдом и смесь экстрагируют дихлорметаном. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат), что дает транс-5-диметиламино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (44 мг). Этот продукт суспендируют в метаноле и обрабатывают 4N хлористым водородом в этилацетате, что дает названное соединение (49 мг). APCI-MS М/Е: 528/530 [M+H]+.
Примеры 199-200
Транс-5-амино-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид, полученный в примере 180, и соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 198, что дает последующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
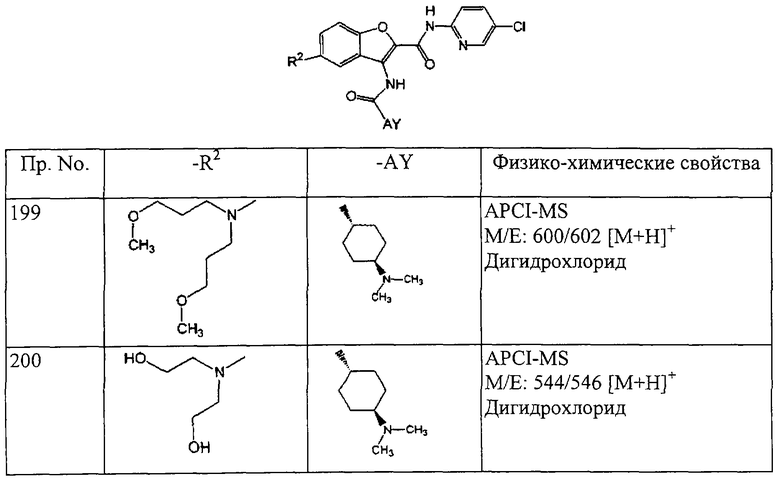
Пример 201: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-(2-гидрокси-1-гидроксиметилэтокси)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
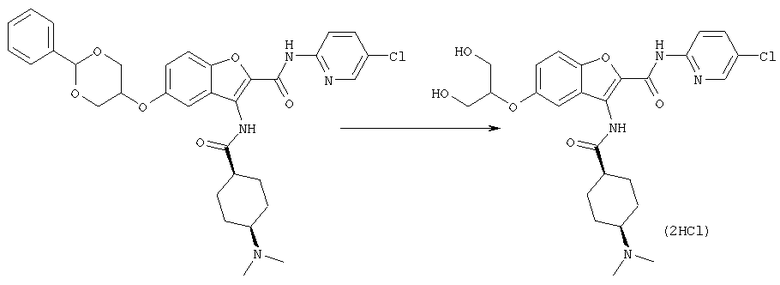
Транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-(2-фенил-[1,3]диоксан-5-илокси)-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид (200 мг), полученный в примере 35, растворяют в тетрагидрофуране (5 мл) и добавляют 2N соляную кислоту (5 мл), после чего смесь перемешивают при комнатной температуре в течение 3 часов. Реакционный раствор подщелачивают насыщенным водным раствором гидрокарбоната натрия и карбоната калия и экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: метанол/этилацетат =1/20 → метанол/этилацетат =1/5), что дает транс-3-[4-(диметиламино)циклогексилкарбониламино]-5-(2-гидрокси-1-гидроксиметилэтокси)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (162 мг). Этот продукт растворяют в метаноле и добавляют 4N хлористый водород в этилацетате (1 мл). Растворитель выпаривают при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире и осадки собирают фильтрованием, что дает названное соединение (141 мг).
APCI-MS М/E: 531/533 [M+H]+.
Пример 202: Транс-3-[4-(N-трет-бутоксикарбонил-N-метиламино)-циклогексилкарбониламино]-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
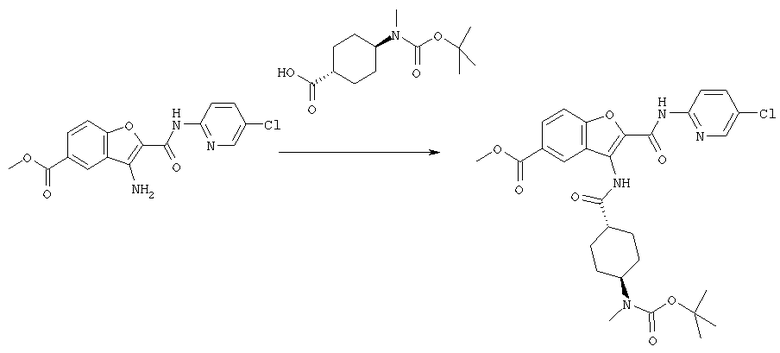
Транс-4-(N-трет-бутоксикарбонил-N-метиламино)-циклогексан-карбоновую кислоту (4,12 г), полученную в примере приготовления 115, растворяют в дихлорметане (80 мл) и добавляют пиридин (7,9 мл). Затем в смесь добавляют по каплям тионилхлорид (1,04 мл) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 3 часов. Реакционный раствор концентрируют и к полученному осадку добавляют последовательно пиридин (80 мл), 3-амино-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,76 г), полученный в примере приготовления 72, и 4-диметиламинопиридин (195 мг) при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры и перемешивают в течение 17 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и осадки собирают фильтрованием, промывают последовательно водой и диэтиловым эфиром и сушат, что дает названное соединение (4,63 г). APCI-MS М/Е: 585 [M+H]+.
Пример 203: Транс-3-[4-(трет-бутоксикарбониламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
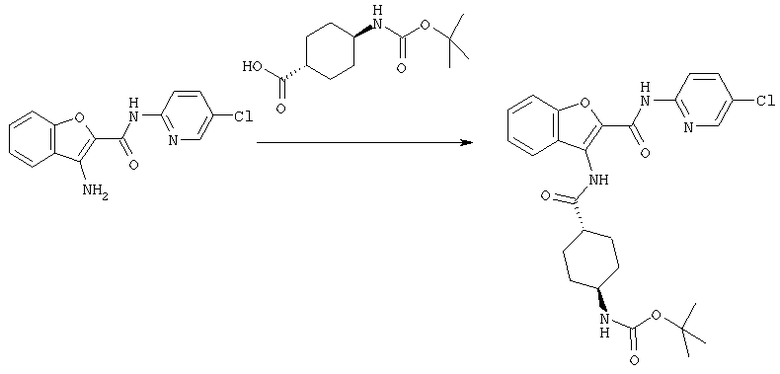
Транс-4-(трет-бутоксикарбониламино)циклогексанкарбоновую кислоту (2,54 г), полученную в примере приготовления 116, растворяют в дихлорметане (50 мл) и добавляют пиридин (4,22 мл) и смесь охлаждают льдом. В смесь добавляют по каплям тионилхлорид (0,76 мл), после чего смесь перемешивают при комнатной температуре в течение 5 часов. Реакционный раствор снова охлаждают льдом и добавляют 3-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,00 г), полученный в примере приготовления 74, и дихлорметан (20 мл) и смесь перемешивают при комнатной температуре в течение 15 часов. В реакционный раствор выливают воду и смесь экстрагируют хлороформом. Органический слой промывают последовательно водой, 5% водным раствором лимонной кислотой, водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ) и суспендируют в диэтиловом эфире. Осадки собирают фильтрованием, что дает названное соединение (2,94 г). APCI-MS М/Е: 513/515 [M+H]+.
Примеры 204-217
Соответствующие исходные соединения обрабатывают аналогичным способом по примеру 202 или примеру 203, что дает следующие соединения.
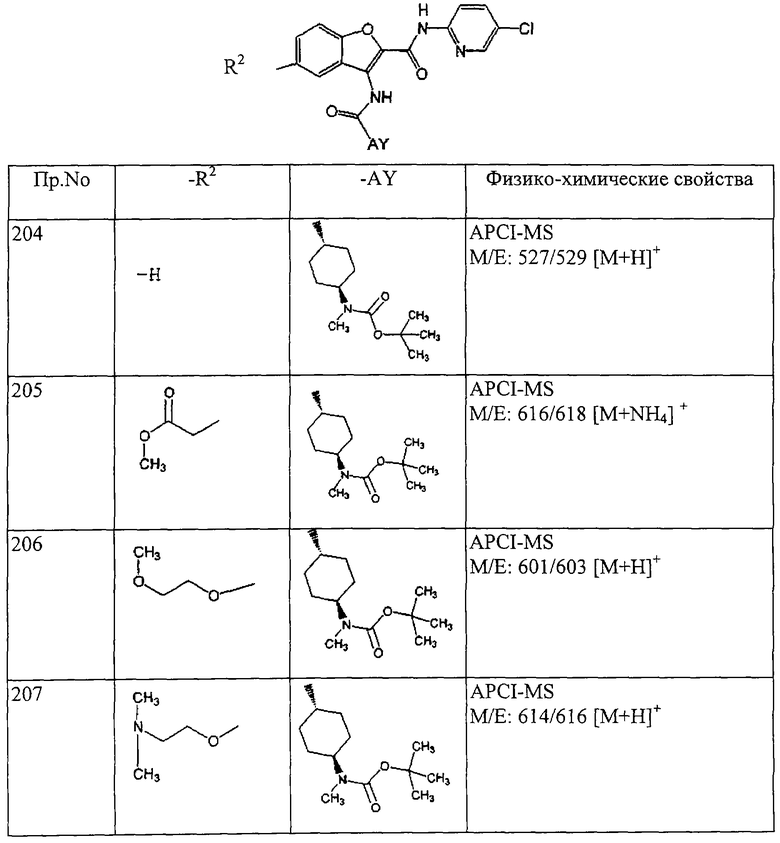
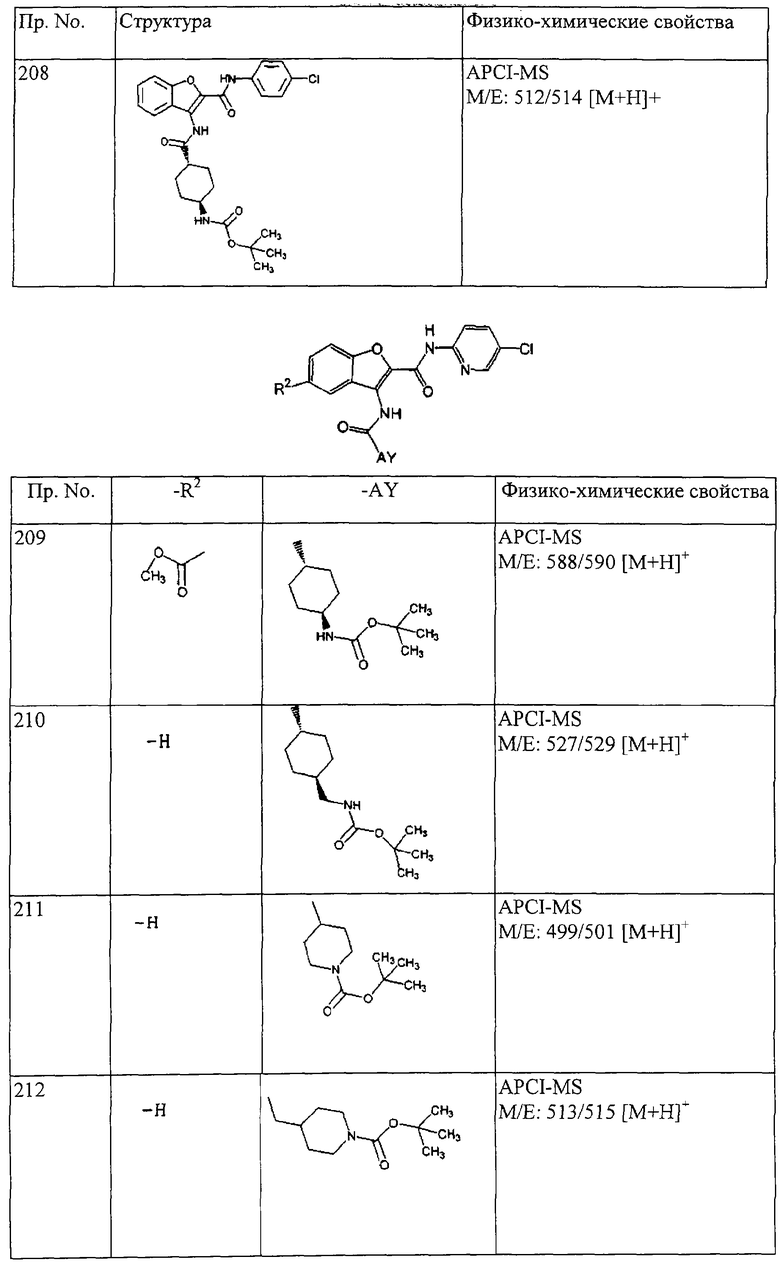
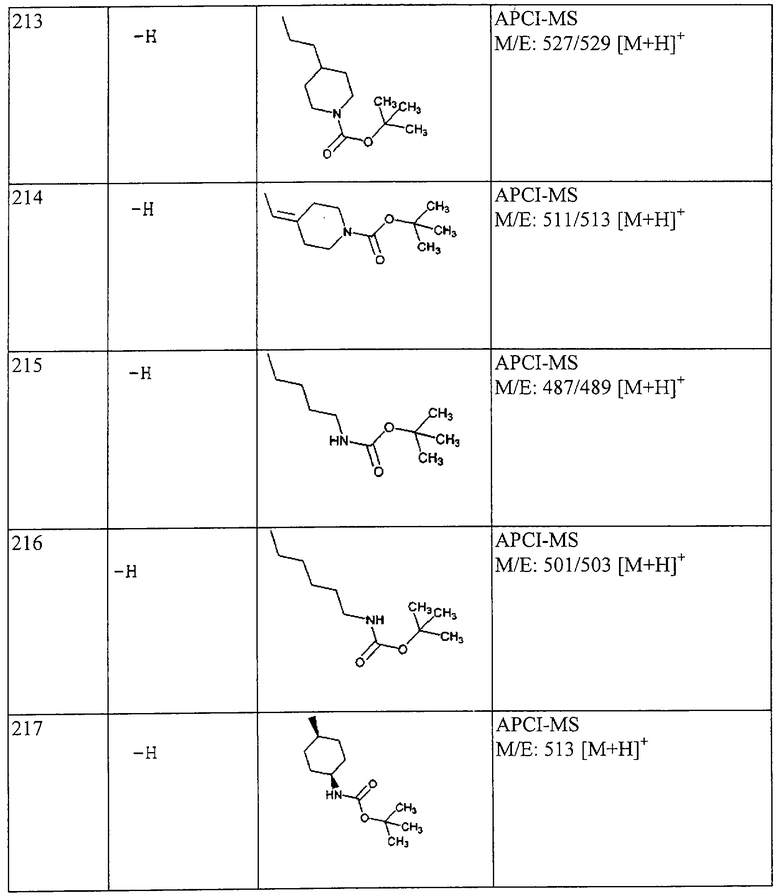
Пример 218: Транс-5-метоксикарбонил-3-[4-(метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
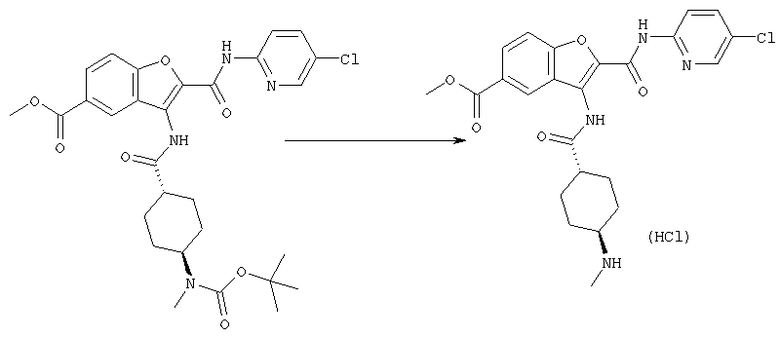
Транс-3-[4-(N-трет-бутоксикарбонил-N-метиламино)циклогексилкарбониламино]-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (4,60 г), полученный в примере 202, растворяют в диоксане (20 мл) и добавляют 4N хлористый водород в диоксане (10 мл), после чего смесь перемешивают при комнатной температуре в течение 48 часов. Реакционный раствор разбавляют диэтиловым эфиром и осадки собирают фильтрованием, промывают несколько раз диэтиловым эфиром и сушат, что дает названное соединение (4,02 г). APCI-MS М/Е: 485/487 [M+H]+.
Пример 219: Транс-3-(4-аминоциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
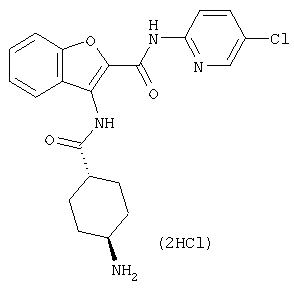
Транс-3-[4-(трет-бутоксикарбониламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (10,70 г), полученный в примере 203, растворяют в диоксане (150 мл) и добавляют 4N хлористый водород в диоксане (150 мл). Смесь перемешивают при комнатной температуре в течение 12 часов и концентрируют при пониженном давлении. Осадок размельчают в диэтиловом эфире и собирают фильтрованием, что дает названное соединение (9,80 г). APCI-MS М/Е: 412/414 [M+H]+.
Пример 220: 3-[2-(пиперидин-4-ил)ацетиламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
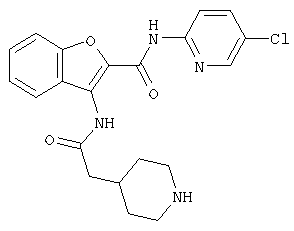
3-[2-(1-трет-Бутоксикарбонилпиперидин-4-ил)ацетиламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,34 г), полученный в примере 212, суспендируют в этилацетате (30 мл) и добавляют 2,6N хлористый водород в этилацетате (30 мл) и смесь перемешивают при комнатной температуре в течение 5 часов. Реакционный раствор концентрируют при пониженном давлении и в полученный осадок добавляют хлороформ и водный раствор гидрокарбоната натрия. Осадки собирают фильтрованием, что дает названное соединение (1,47 г). APCI-MS М/Е: 413/415 [M+H]+.
Примеры 221-233
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 218, примере 219 или в примере 220, что дает последующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
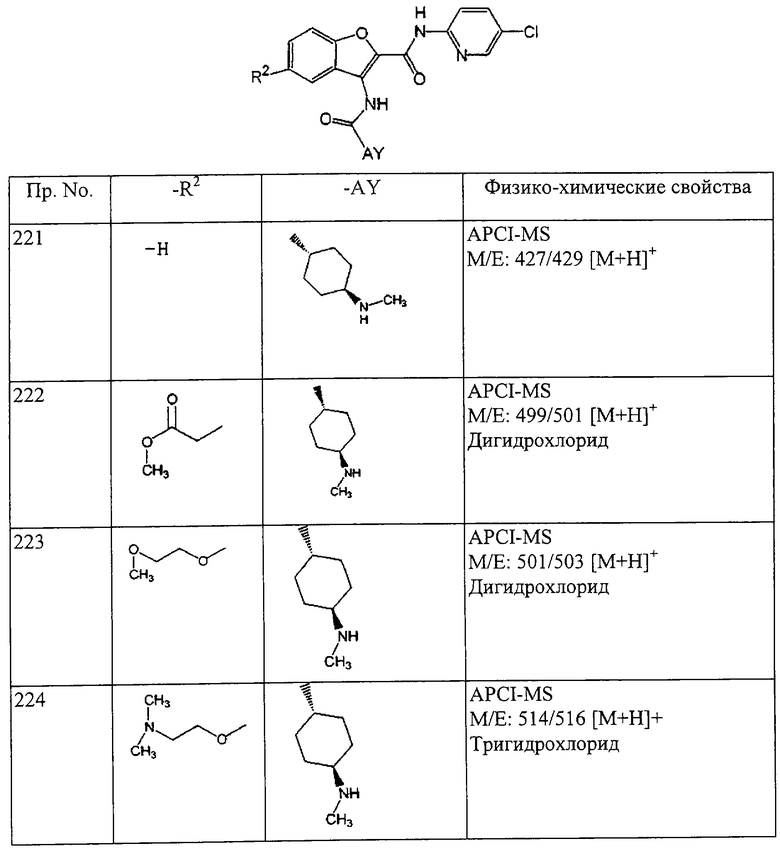
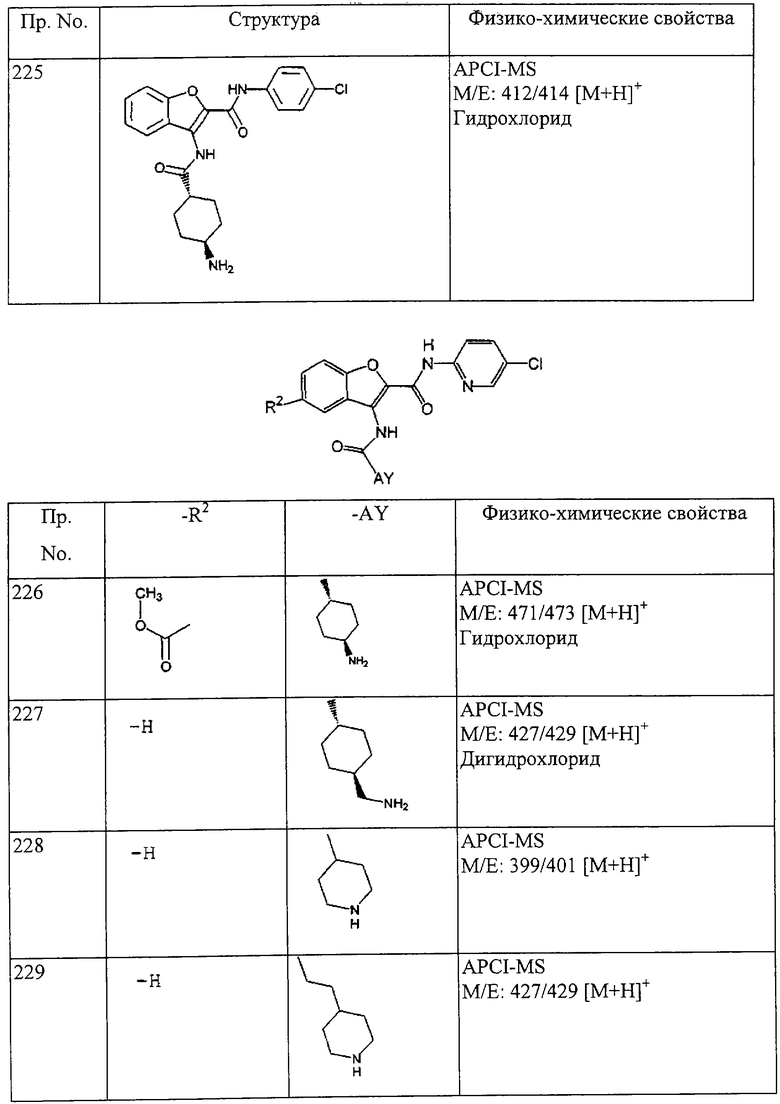
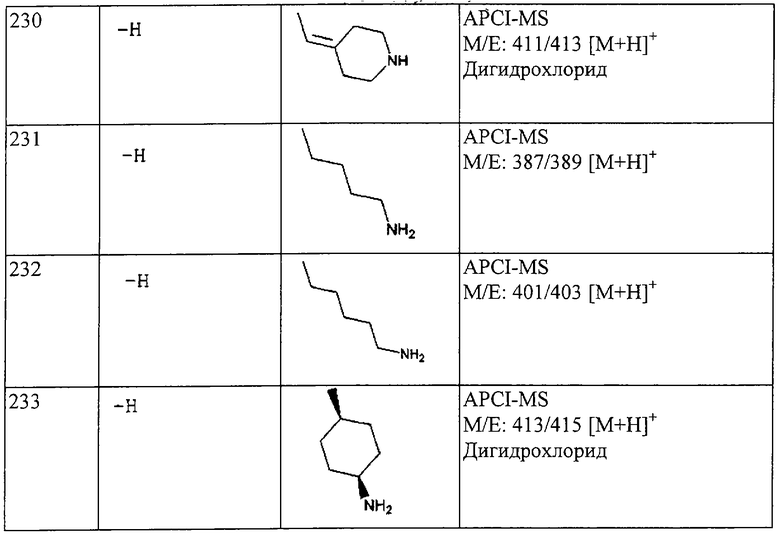
Пример 234: Транс-3-[4-(N-формил-N-метиламино)циклогексилкарбониламино]-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
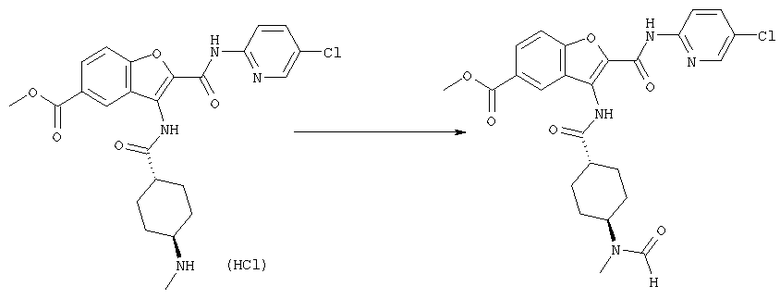
В раствор имидазола (783 мг) и триэтиламина (2,41 мл) в хлороформе (80 мл) добавляют по каплям муравьиную кислоту (709 мкл) с перемешиванием при охлаждении льдом. Затем добавляют оксалилхлорид (1,00 мл) в хлороформе (10 мл) и смесь перемешивают при комнатной температуре в течение 0,5 часа. Реакционный раствор снова охлаждают льдом и добавляют транс-5-метоксикарбонил-3-[4-(метиламино)-циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид (1,50 г), полученный в примере 218. Смесь нагревают до комнатной температуры и перемешивают в течение 3 часов. В реакционный раствор выливают ледяную воду и насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Экстракт промывают насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ), что дает названное соединение (1,45 г). APCI-MS М/Е: 513/515 [M+H]+.
Примеры 235-238
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 234, что дает следующие соединения.
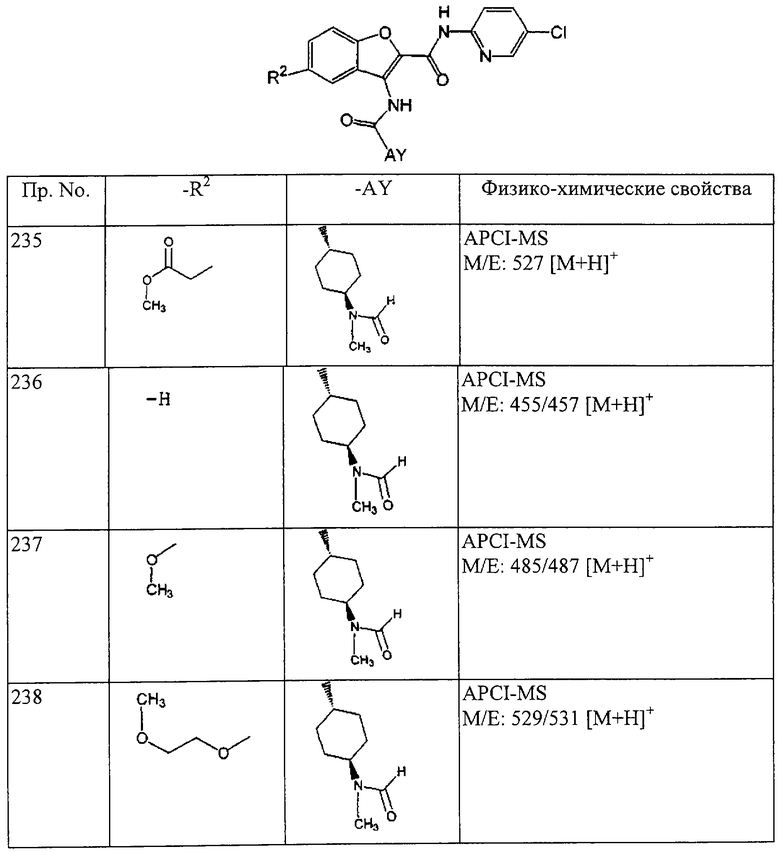
Пример 239: Транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
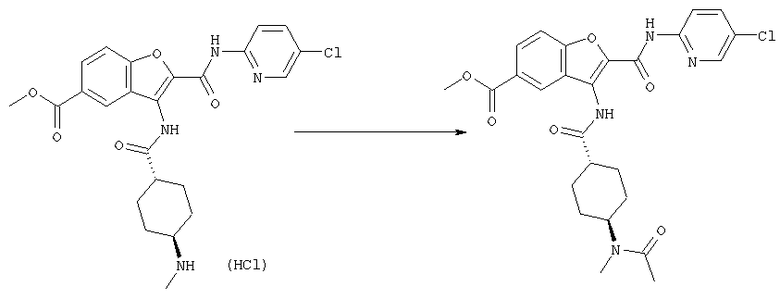
Транс-5-метоксикарбонил-3-[4-(метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид (1,50 г), полученный в примере 218, суспендируют в дихлорметане (80 мл) и добавляют ацетилхлорид (307 мкл) и триэтиламин (1,60 мл) при охлаждении льдом. Смесь нагревают до комнатной температуры и перемешивают в течение 2 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом, промывают водой и насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ), что дает названное соединение (1,51 г). APCI-MS М/Е: 527/529 [M+H]+.
Пример 240: 3-[(1-Ацетилпиперидин-4-ил)карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
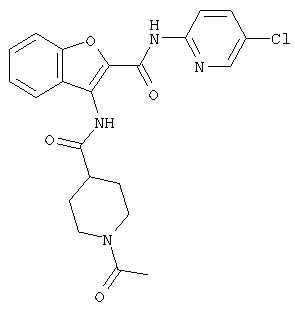
3-[(Пиперидин-4-ил)карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (140 мг), полученный в примере 228, суспендируют в дихлорметане (10 мл) и добавляют ацетилхлорид (30 мкл) и триэтиламин (74 ил) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 6 часов. Реакционный раствор разбавляют хлороформом, промывают последовательно водой, 5% водным раствором лимонной кислоты, насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок растворяют в этилацетате и обрабатывают активированным углем. Полученный осадок перекристаллизовывают из этилацетата, что дает названное соединение (38 мг). APCI-MS М/Е: 441/443 [M+H]+.
Примеры 241-245
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 239 или в примере 240, что дает последующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
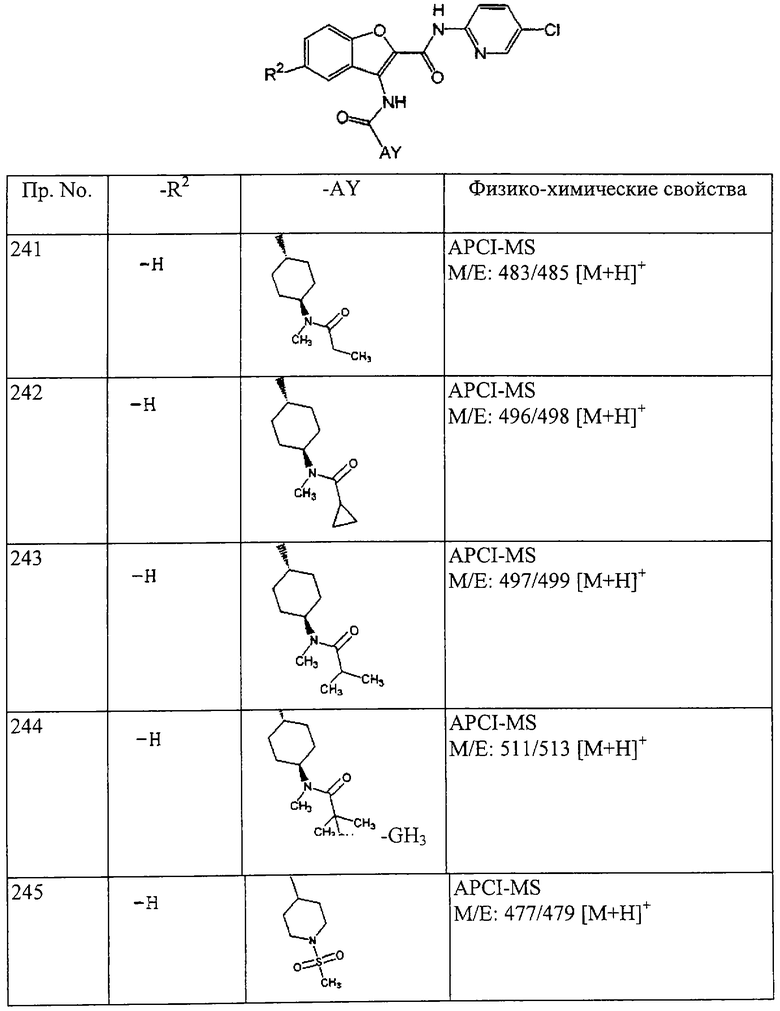
Пример 246: Транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-(2-метоксиэтокси)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
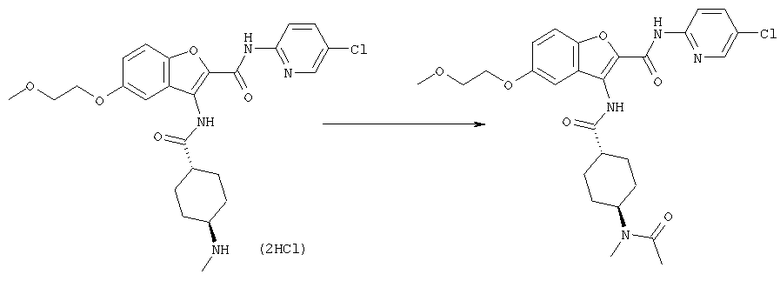
Транс-5-(2-метоксиэтокси)-3-[4-(метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (110 мг), полученный в примере 223, суспендируют в N,N-диметилформамиде (5 мл) и добавляют последовательно уксусную кислоту (13,2 мкл), 1-гидроксибензотриазол (31 мг), триэтиламин (80 мкл) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (44 мг) и смесь перемешивают при комнатной температуре в течение 15 часов. В реакционный раствор добавляют уксусную кислоту (8,2 мкл), 1-гидроксибензотриазол (20 мг), триэтиламин (67 мкл) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (28 мг) и смесь затем перемешивают при комнатной температуре в течение 20 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =1/1, затем этилацетат). Полученное твердое вещество суспендируют в смеси н-гексан/диизопропиловый эфир и собирают фильтрованием, что дает названное соединение (42 мг). APCI-MS М/Е: 543/545 [M+H]+.
Пример 247: 3-[1-((Пиридин-3-ил)карбонил)пиперидин-4-ил-карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
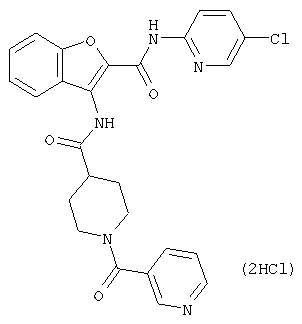
3-[(Пиперидин-4-ил)карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (100 мг), полученный в примере 228, растворяют в N,N-диметилформамиде (3 мл) и добавляют последовательно никотиновую кислоту (34 мг), 1-гидроксибензотриазол (37 мг) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (53 мг) и смесь перемешивают при комнатной температуре в течение 4 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и воду и осадки собирают фильтрованием, промывают хлороформом и сушат, что дает 3-[1-((пиридин-3-ил)карбонил)пиперидин-4-илкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (103 мг). Этот продукт обрабатывают хлористым водородом в диоксане, что дает названное соединение (115 мг). APCI-MS М/Е: 504/506 [M+H]+.
Примеры 248-257
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 246 или в примере 247, что дает следующие соединения в свободном виде, или которые обрабатывают хлористым водородом, что дает их гидрохлориды.
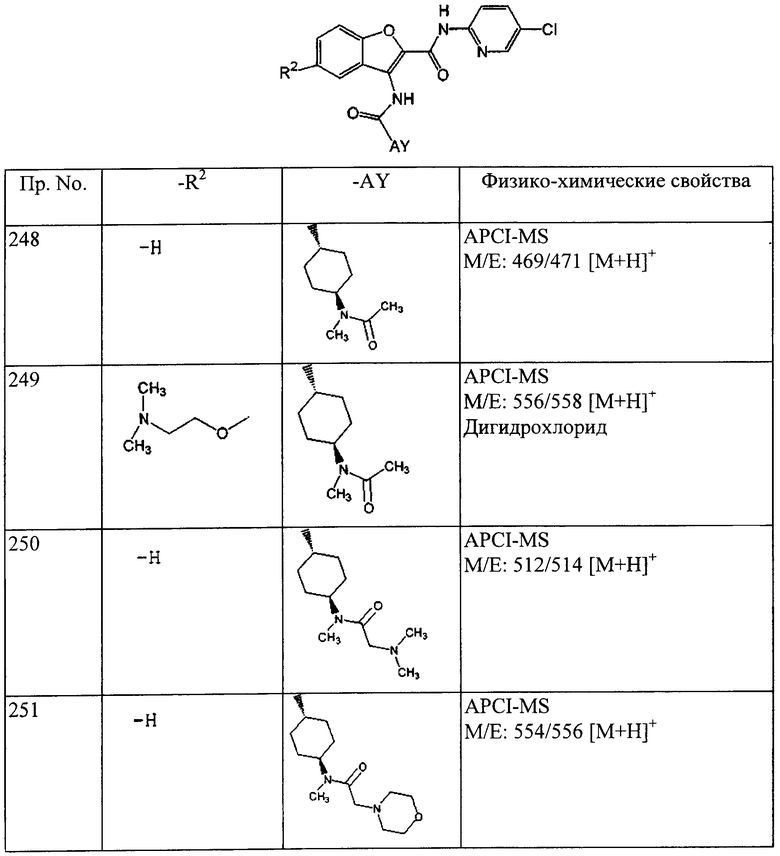
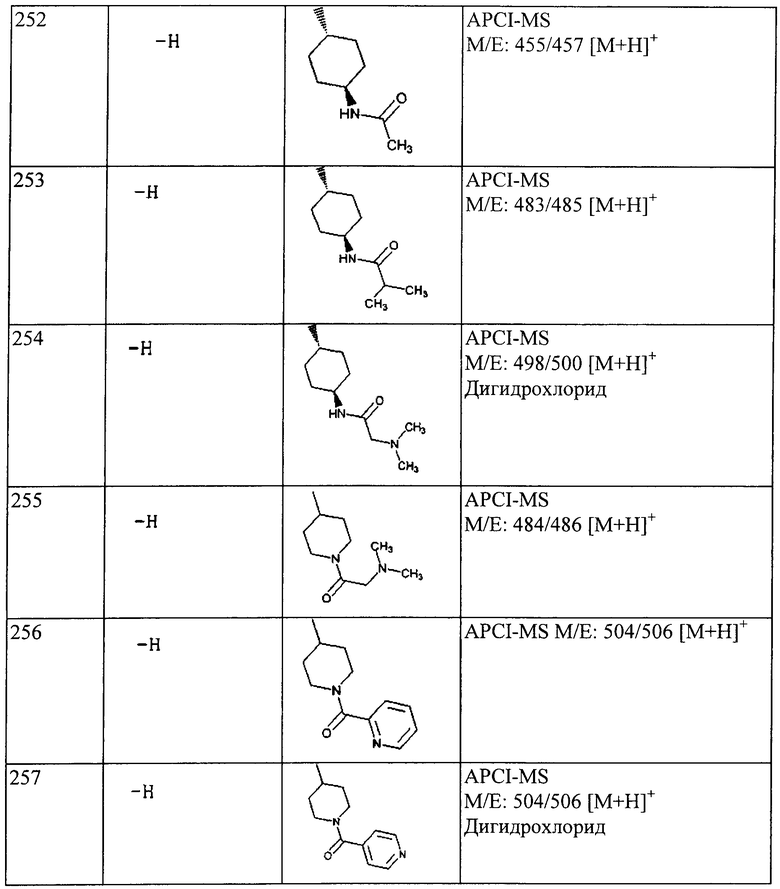
Пример 258: Транс-5-карбокси-3-[4-(N-формил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
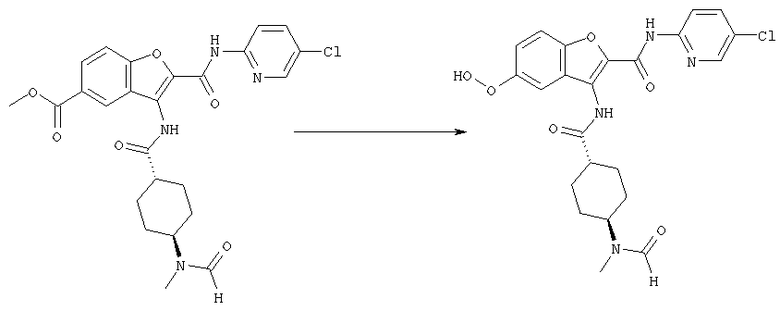
Транс-3-[4-(N-формил-N-метиламино)циклогексилкарбониламино]-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (1,90 г), полученный в примере 234, суспендируют в смеси тетрагидрофуран/метанол (1:1, 50 мл) и добавляют 4N водный раствор гидроксида натрия (5 мл) при охлаждении льдом. Смесь нагревают до комнатной температуры и перемешивают в течение 17 часов. Реакционный раствор концентрируют при пониженном давлении и в осадок выливают ледяную воду и смесь нейтрализуют 10% раствором соляной кислоты. Осадки собирают фильтрованием, промывают последовательно водой и тетрагидрофураном и сушат, что дает названное соединение (1,59 г). ESI-MS М/Е: 497/499 [M-Н]-.
Примеры 259-260
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 258, что дает последующие соединения в свободном виде, или которые обрабатывают хлористым водородом, что дает их гидрохлориды.
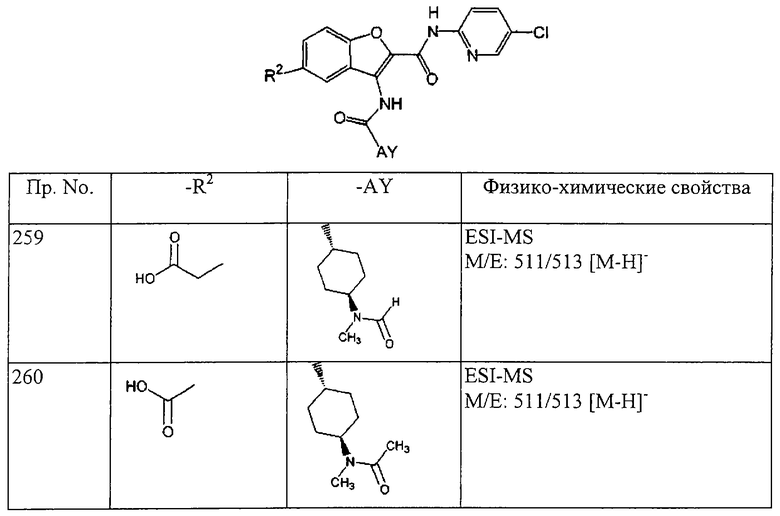
Пример 261: Транс-5-диметиламинокарбонил-3-[4-(N-формил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
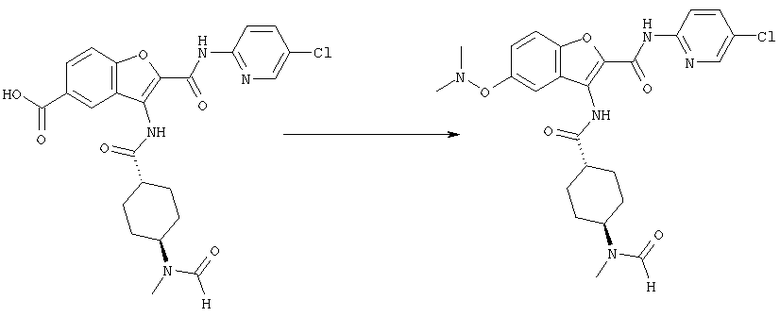
Транс-5-карбокси-3-[4-(N-формил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (196 мг), полученный в примере 258, суспендируют в смеси N,N-диметилформамид/пиридин (1:1, 8 мл) и добавляют последовательно диметиламингидрохлорид (49 мг), 1-гидроксибензотриазол (108 мг) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (153 мг) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 48 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют этилацетатом. Экстракт промывают водой и насыщенным рассолом, сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат). Полученный осадок суспендируют в смеси диэтиловый эфир/н-гексан и осадки собирают фильтрованием, что дает названное соединение (141 мг). APCI-MS М/Е: 526/528 [M+H]+.
Примеры 262-275
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 261, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
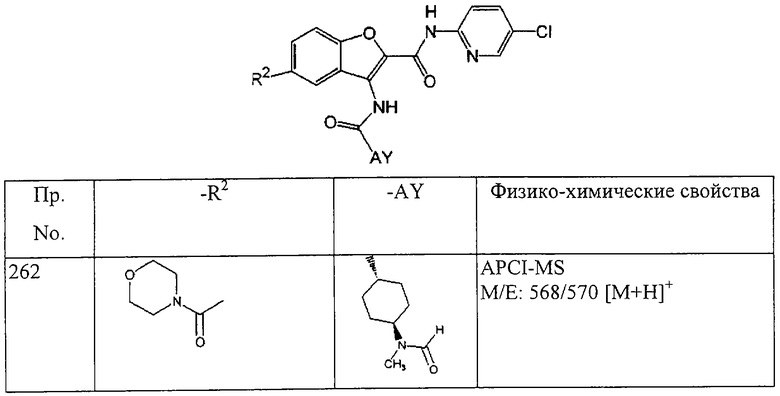
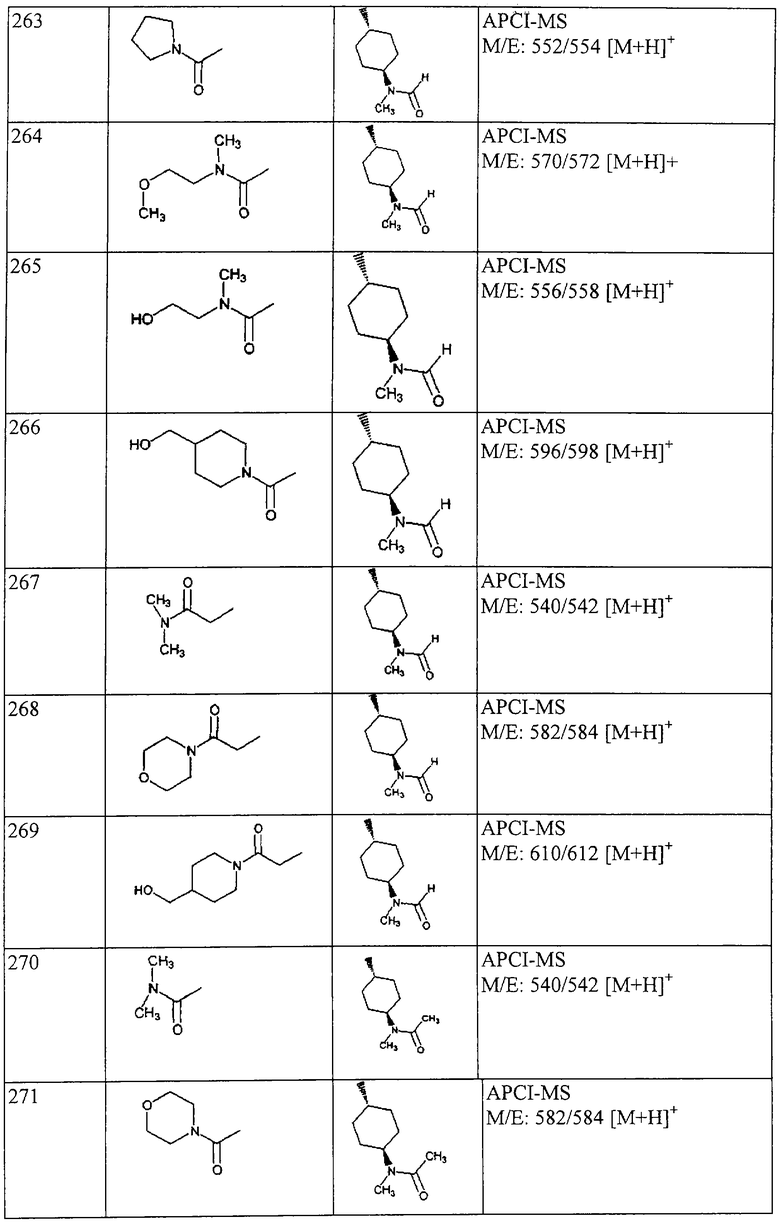
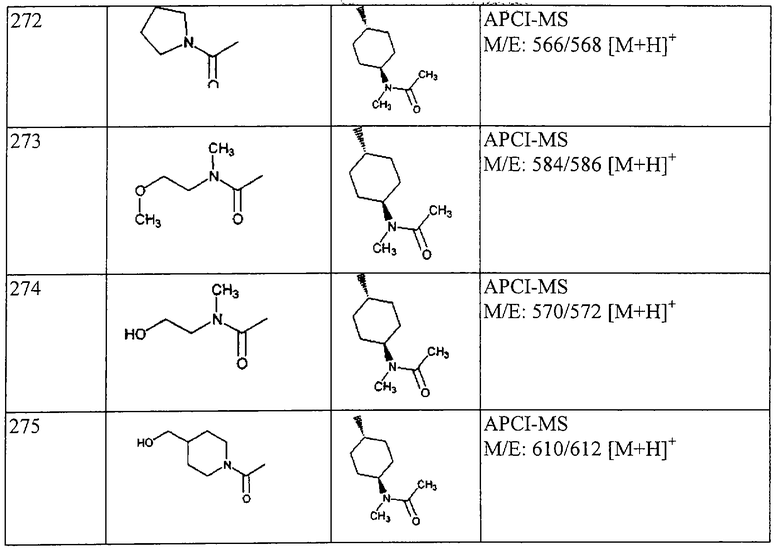
Примеры 276-277
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 145, что дает следующие соединения.
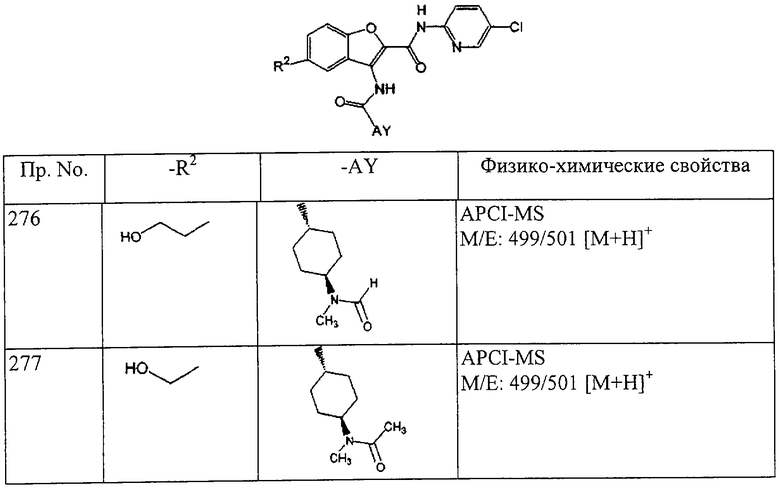
Пример 278: Транс-3-[4-(N-(2-гидроксиэтил)-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
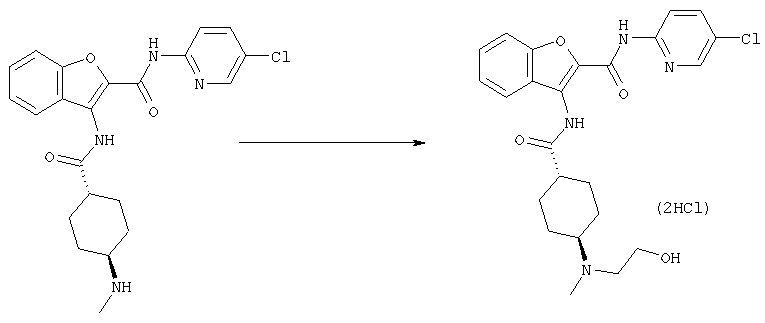
Транс-3-[4-(метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (125 мг), полученный в примере 221 суспендируют в этаноле (5 мл) и добавляют 2-иодэтанол (105 мкл) и карбонат натрия (57 мг) и смесь перемешивают при температуре 50°С в течение 15 часов. К смеси дополнительно добавляют 2-иод-этанол (53 мкл) и смесь затем перемешивают при температуре 80°С в течение 6 часов. В смесь снова добавляют 2-иодэтанол (53 мкл) и смесь перемешивают при температуре 80°С в течение 24 часов. Реакционный раствор концентрируют при пониженном давлении и в осадок выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают водой, насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =1/2, затем этилацетат), что дает транс-3-[4-(N-(2-гидроксиэтил)-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (53 мг). Затем этот продукт растворяют в смеси хлороформ/метанол (5/1, 6 мл) и добавляют 4N хлористый водород в этилацетате (1 мл). Растворитель выпаривают при пониженном давлении. Полученный осадок суспендируют в диэтиловом эфире и собирают фильтрованием, что дает названное соединение (55 мг). APCI-MS М/Е: 471/473 [M+H]+.
Пример 279: 3-[[1-((Пиридин-4-ил)метил)пиперидин-4-ил]карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
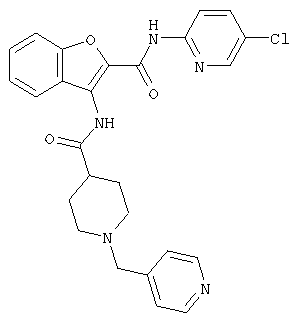
3-((Пиперидин-4-ил)карбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (100 мг), полученный в примере 228, суспендируют в N,N-диметилацетамиде (3 мл) и добавляют гидрохлорид 4-(хлорметил)пиридина (45 мг), карбонат натрия (80 мг) и иодид натрия (41 мг), после чего смесь перемешивают при комнатной температуре в течение 12 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =2/1, затем 1/1), что дает названное соединение (109 мг). APCI-MS М/Е: 490/492 [M+H]+.
Примеры 280-289
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 278 или в примере 279, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
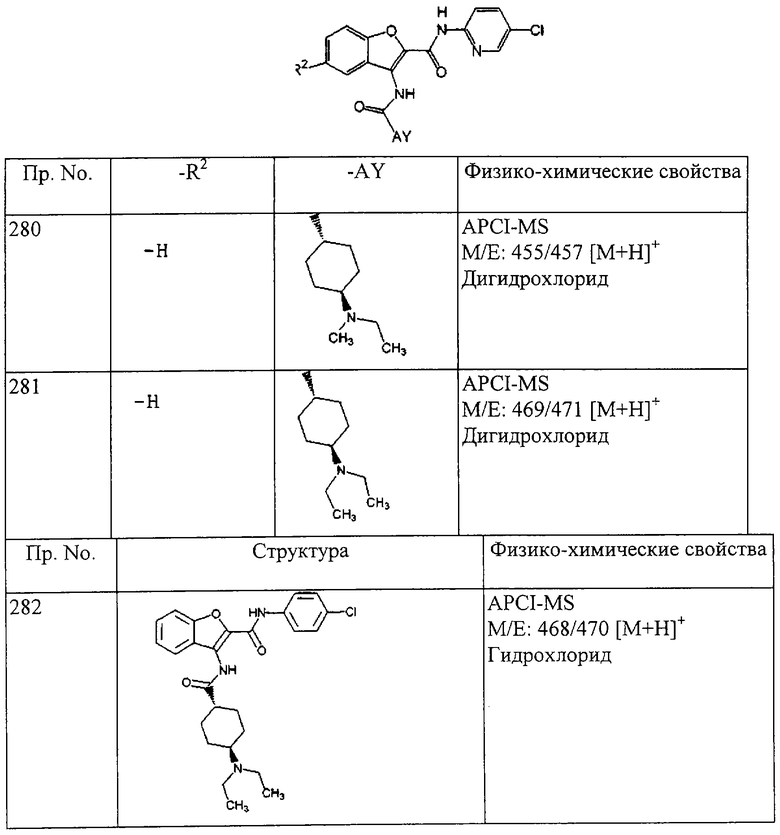
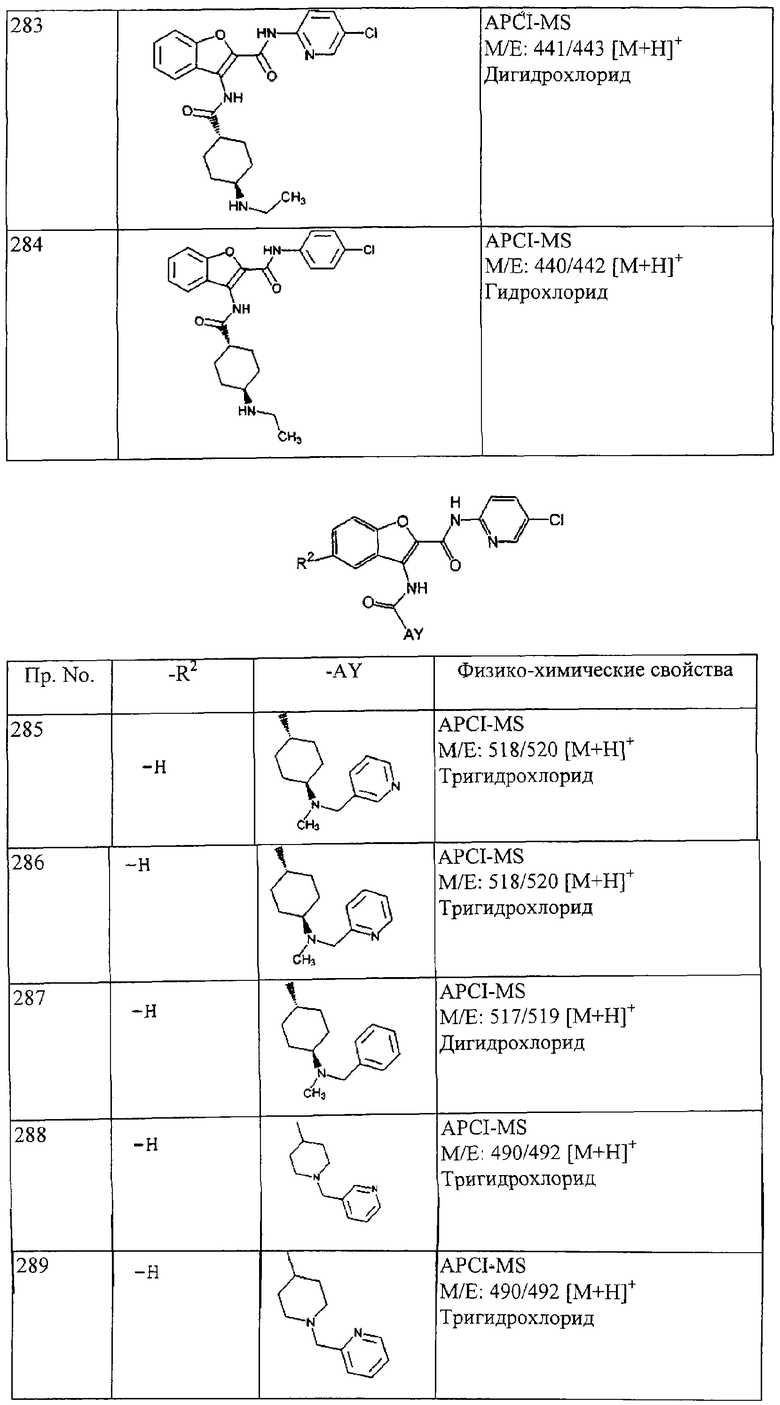
Пример 290: Транс-3-[4-(2-гидроксиэтиламино)циклогексилкарбониламино]-N-(4-хлорфенил)бензофуран-2-карбоксамид гидрохлорид
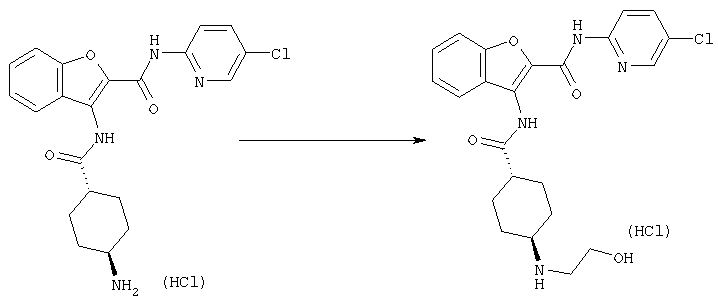
Транс-3-[4-аминоциклогексилкарбониламино]-N-(4-хлорфенил)бензофуран-2-карбоксамид гидрохлорид (150 мг), полученный в примере 225, суспендируют в смеси ацетонитрил/метанол (5/1, 6 мл) и добавляют триэтиламин (93 мкл), после чего смесь перемешивают при комнатной температуре в течение несколько минут. Реакционный раствор охлаждают льдом и добавляют 2-иодэтанол (29 мкл) и смесь перемешивают при температуре 50°С в течение 3 часов. Затем добавляют еще порцию 2-иодэтанола (58 мкл) и смесь перемешивают при температуре 50°С в течение 3 часов. Снова к реакционной массе добавляют 2-иодэтанол (58 мкл) и смесь затем перемешивают при температуре 50°С в течение 15 часов. Реакционный раствор концентрируют при пониженном давлении и в осадок выливают воду и насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат, затем этилацетат/метанола =20/1), что дает транс-3-[4-(2-гидроксиэтиламино)циклогексилкарбониламино]-N-(4-хлорфенил)бензофуран-2-карбоксамид (104 мг). Этот продукт (104 мг) растворяют в смеси хлороформ/метанол (5/1, 6 мл) и добавляют 4N хлористый водород в этилацетате (1 мл). Растворитель выпаривают при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире и собирают фильтрованием, что дает названное соединение (95 мг).
APCI-MS М/Е: 456/458 [M+H]+.
Примеры 291-296
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 290, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
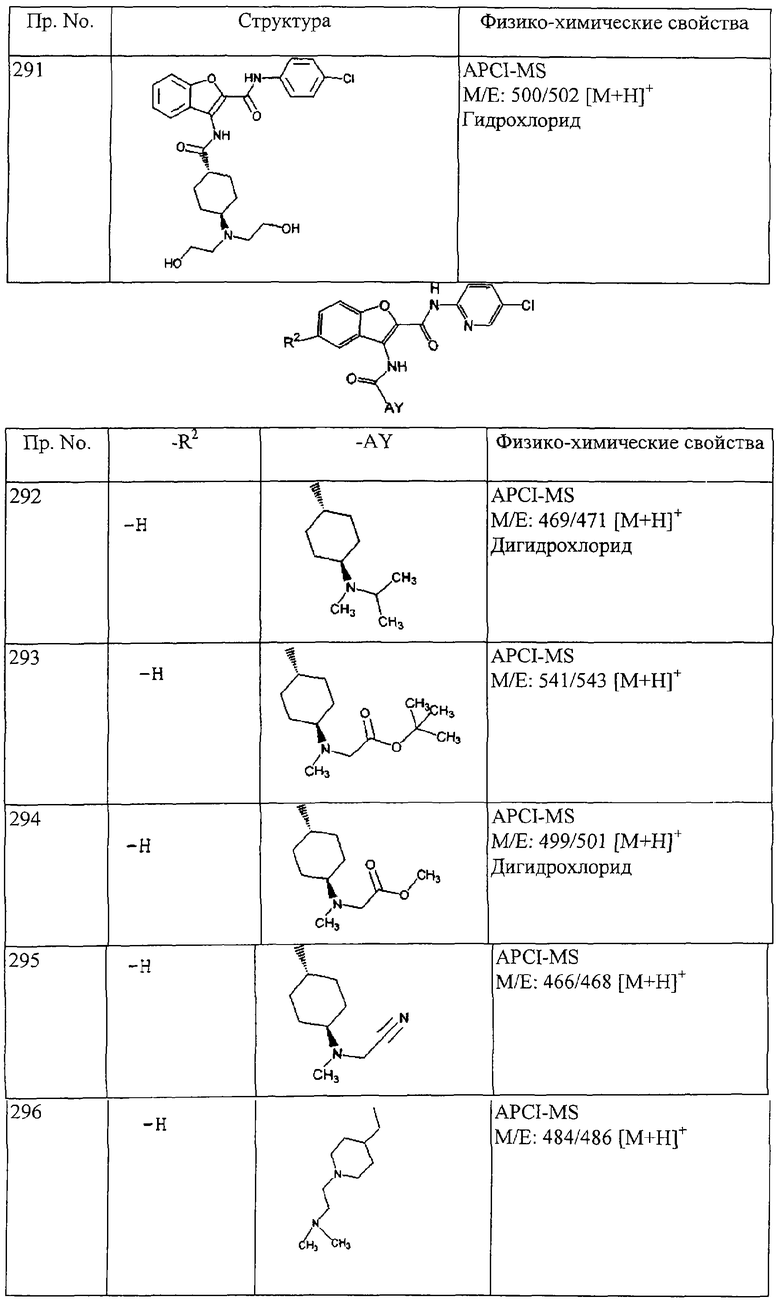
Пример 297: Транс-3-[4-(морфолин-4-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
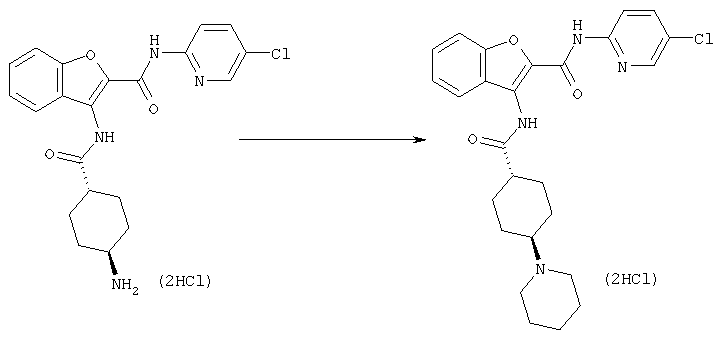
Транс-3-[4-аминоциклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (200 мг), полученный в примере 219, суспендируют в N,N-диметилацетамиде (10 мл) и добавляют бис(2-хлорэтил)эфир (73 мкл), иодид натрия (185 мг) и карбонат натрия (131 мг) и смесь перемешивают при температуре 50°С в течение 5 часов и затем перемешивают при температуре 89°С в течение 3 часов. Затем добавляют бис(2-хлорэтил)эфир (73 мкл) и смесь перемешивают при температуре 80°С в течение 15 часов. Реакционный раствор концентрируют при пониженном давлении и в осадок выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =5/1, затем 1/1), что дает транс-3-[4-(морфолин-4-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (70 мг). Потом этот продукт растворяют в смеси хлороформ/метанол (5/1, 6 мл) и добавляют 4N хлористый водород в этилацетате (1 мл) и растворитель выпаривают при пониженном давлении. Полученный осадок суспендируют в диэтиловом эфире и собирают фильтрованием, что дает названное соединение (65 мг). APCI-MS М/Е: 483/485 [M+H]+.
Примеры 298-301
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 297, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
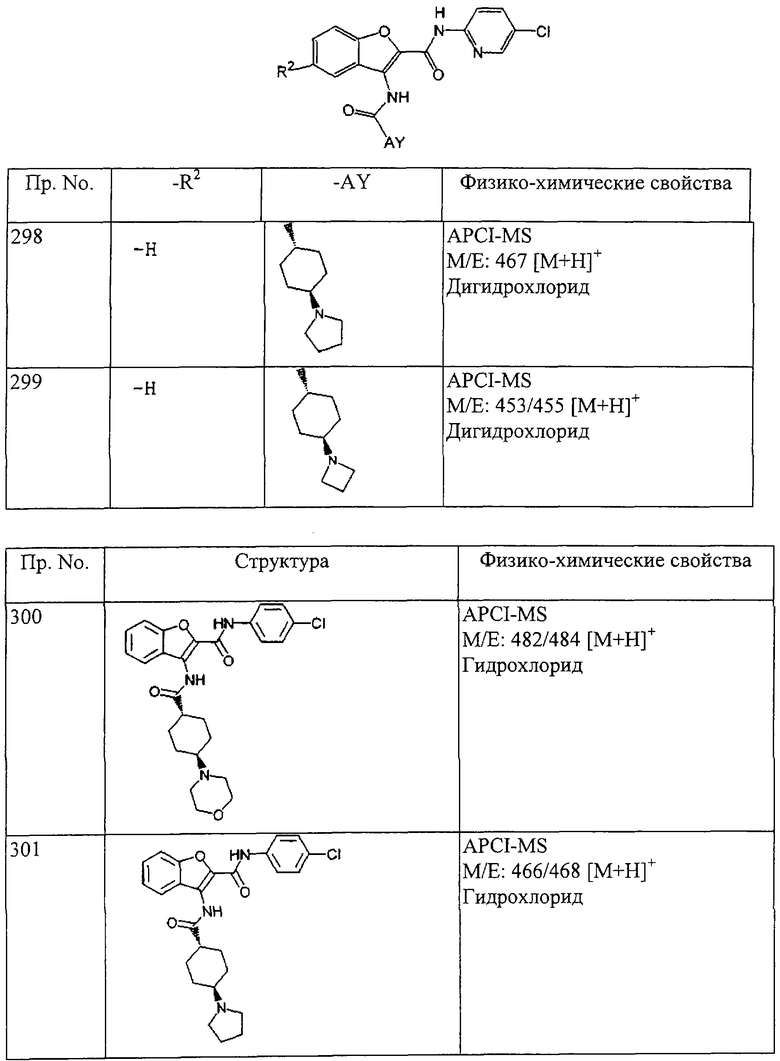
Пример 302: Транс-3-[4-(N-карбоксиметил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
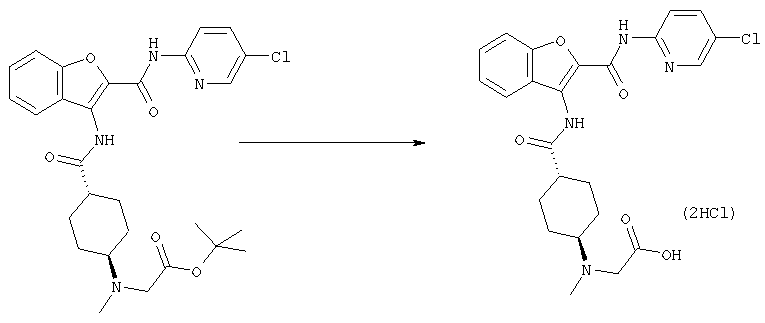
Транс-3-[4-(N-трет-бутоксикарбонилметил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (820 мг), полученный в примере 293, обрабатывают способом, аналогичным описанному в примере 156, что дает названное соединение (778 мг). ESI-MS М/Е: 507/509 [M+Na]+.
Примеры 303-305
Транс-3-[4-(N-карбоксиметил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид, полученный в примере 302, обрабатывают способом, аналогичным описанному в примере 87, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
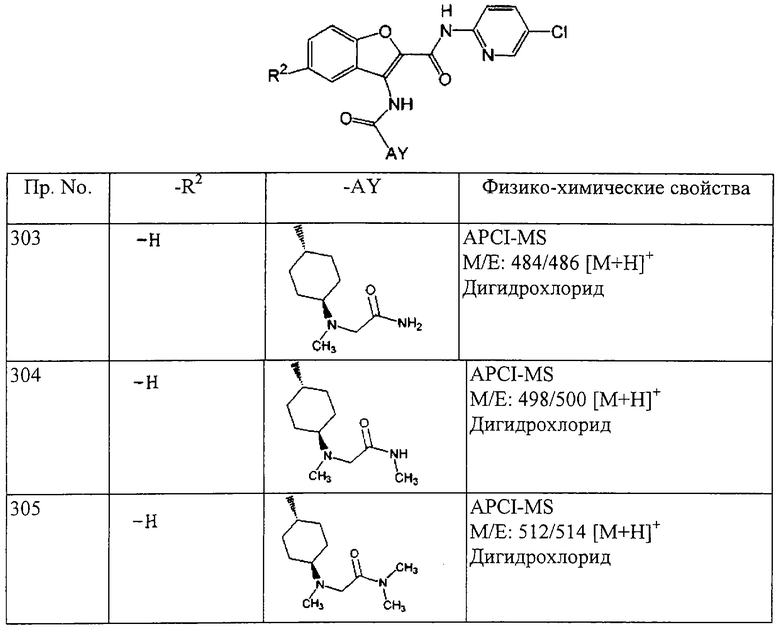
Пример 306: Транс-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
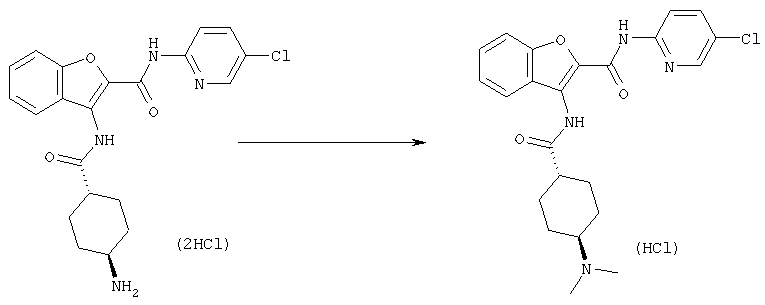
Транс-3-(4-аминоциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (9,30 г), полученный в примере 219, суспендируют в дихлорметане (430 мл) и добавляют триэтиламин (7,99 мл) при охлаждении льдом и смесь перемешивают в течение нескольких минут. Затем последовательно к реакционной смеси добавляют 35% водный раствор формальдегида (7,59 мл) и триацетоксиборгидрида натрия (12,10 г) и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 12 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия при охлаждении льдом и смесь экстрагируют хлороформом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =3/1, затем этилацетат), что дает транс-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида (6,92 г). Этот продукт растворяют в смеси хлороформ/метанол (5/1, 60 мл) и добавляют 4N хлористый водород в этилацетате (50 мл) при охлаждении льдом. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире и собирают фильтрованием, что дает названное соединение (7,83 г). APCI-MS М/Е: 441/443 [M+H]+.
Пример 307: Транс-3-[4-[N-[3-(трет-бутоксикарбониламино)пропил]-N-метиламино]циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
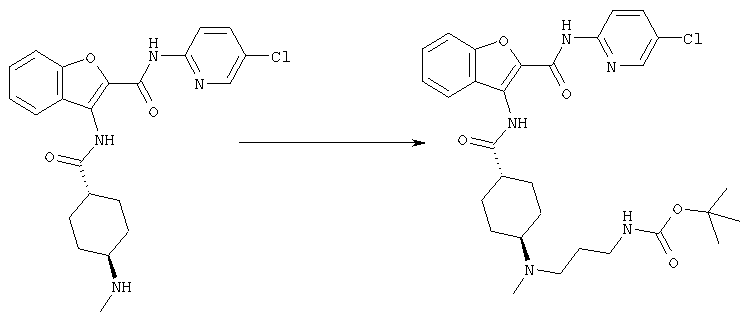
Транс-3-[4-(метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (250 мг), полученный в примере 221, суспендируют в дихлорметане (8 мл) и к смеси добавляют 3-трет-бутоксикарбониламинопропанал (198 мг) и триэтиламин (160 мкл) при охлаждении льдом и смесь перемешивают в течение нескольких минут. Затем добавляют триацетоксиборгидрид натрия (243 мг) и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 4 часов. В реакционный раствор выливают насыщенный водный раствор бикарбоната натрия при охлаждении льдом и смесь экстрагируют хлороформом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =3/1, затем 1/1), что дает названное соединение (312 мг).
APCI-MS М/Е: 584/586 [M+H]+.
Примеры 308-326
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 306 или в примере 307, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
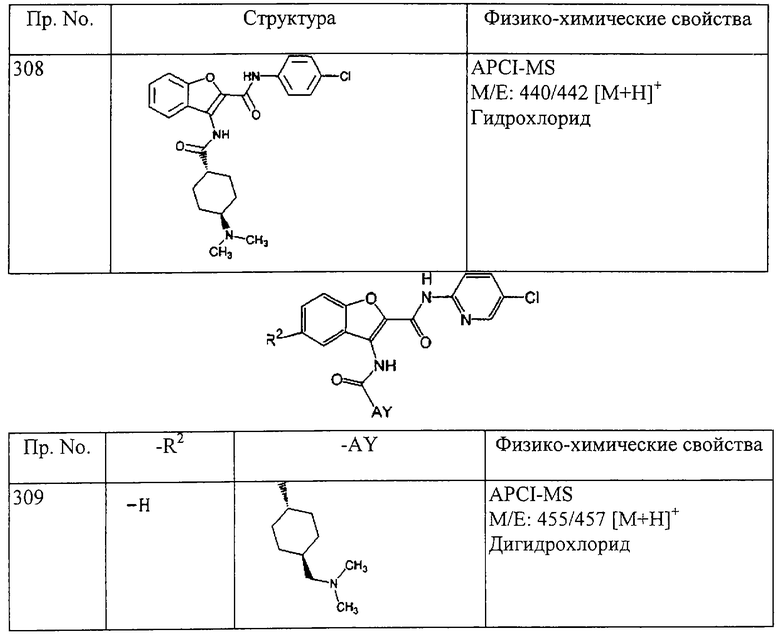
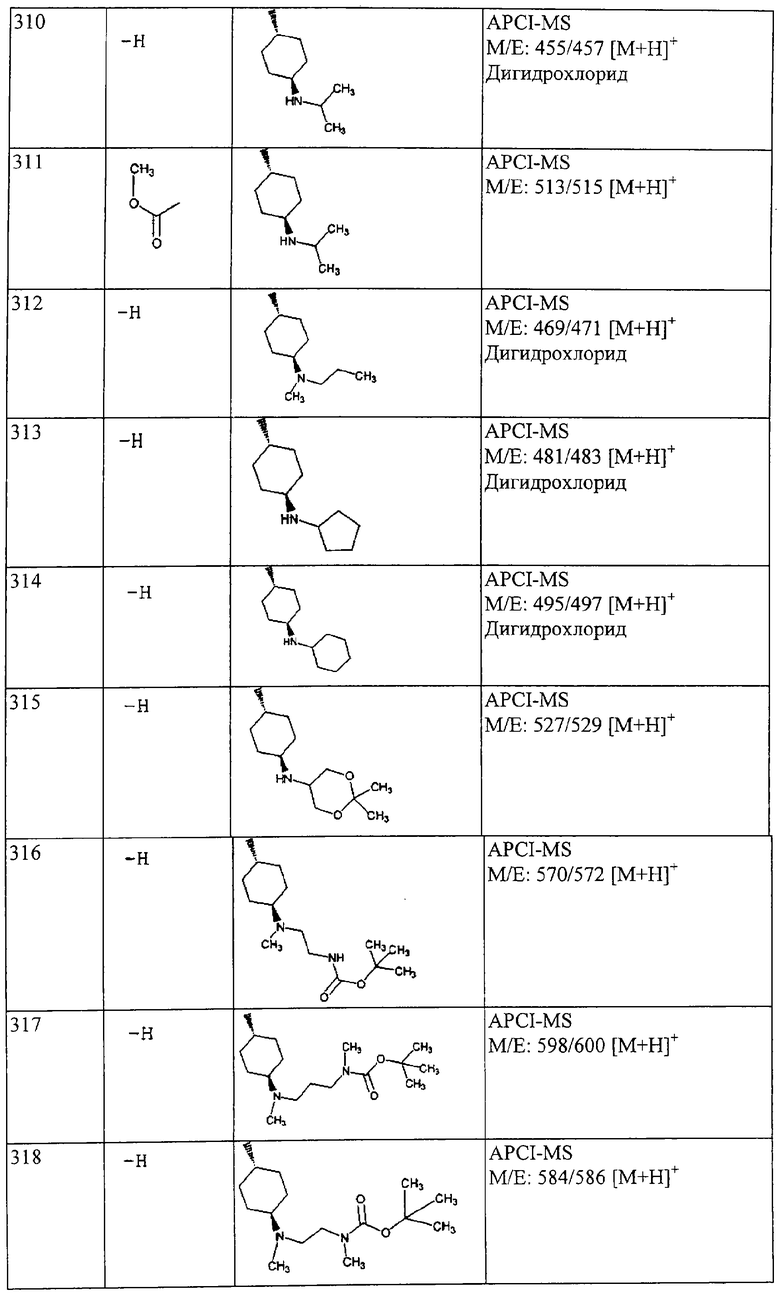
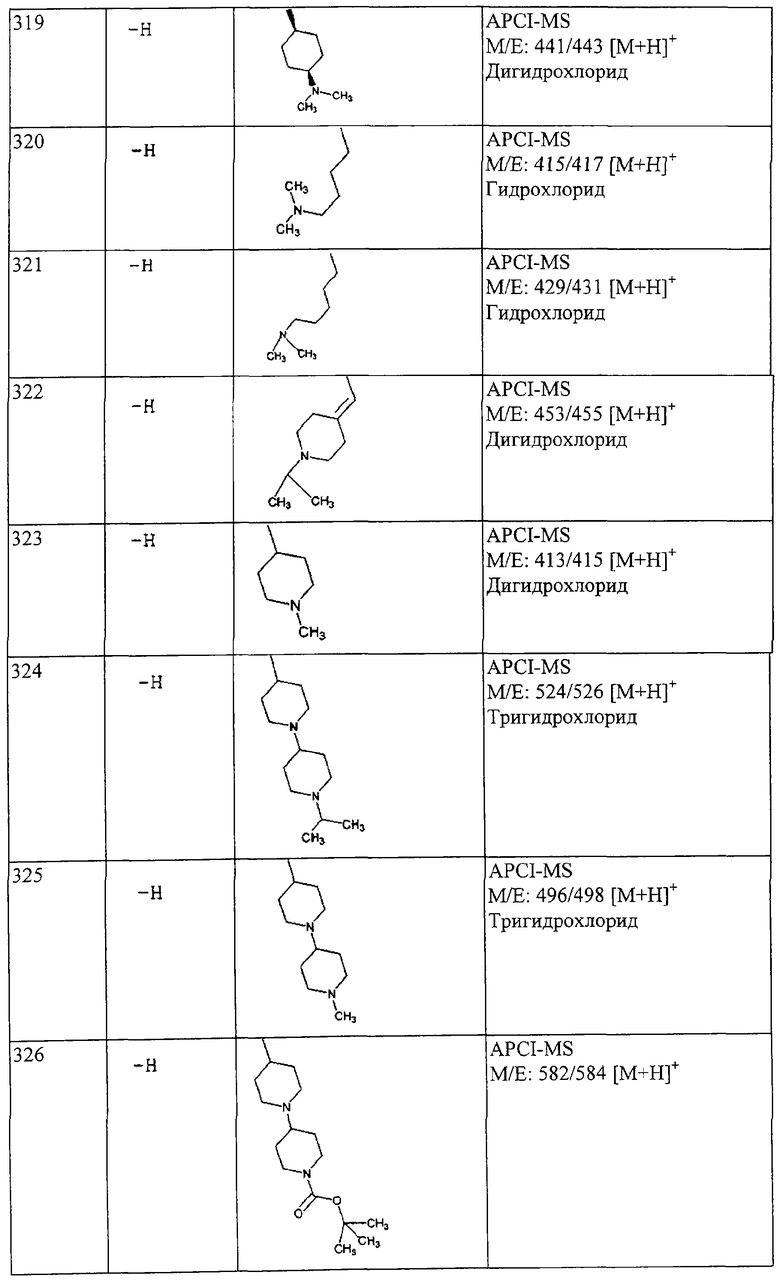
Пример 327: Транс-3-[4-[N-[3-(диметиламино)пропил]-N-метиламино]циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид тригидрохлорид
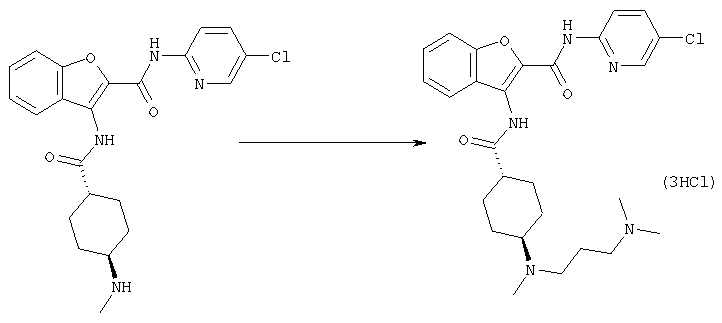
(1) 3-Аминопропиональдегид диэтилацеталь (5,00 г) растворяют в дихлорметане (70 мл) и к смеси добавляют последовательно 35% водный раствор формальдегида (13,5 мл) и триацетоксиборгидрид натрия (18,0 г) при охлаждении льдом и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 6 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия при охлаждении льдом и затем добавляют карбонат калия. Смесь экстрагируют хлороформом и органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении, что дает сырой 3-(диметиламино)пропиональдегид диэтилацеталь (5,31 г).
(2) 3-(Диметиламино)пропиональдегид диэтилацеталь (284 мг), полученный в примере 327-(1), растворяют в тетрагидрофуране (3 мл) и к раствору добавляют концентрированную соляную кислоту (3 мл), после чего смесь перемешивают при комнатной температуре в течение 15 часов. Реакционный раствор концентрируют досуха при пониженном давлении и полученный осадок растворяют в дихлорметане (7 мл). Добавляют транс-3-[4-(метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (150 мг), полученный в примере 221, и триэтиламин (226 мкл) и смесь перемешивают в течение нескольких минут. Затем к смеси добавляют триацетоксиборгидрид натрия (137 мг) и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 15 часов. В реакционный раствор добавляют насыщенный водный раствор гидрокарбоната натрия при охлаждении льдом и смесь экстрагируют хлороформом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат, затем смесь этилацетат/метанол =20/1), что дает транс-3-[4-[N-[3-(диметиламино)пропил]-N-метиламино]циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (99 мг). Потом этот продукт растворяют в смеси хлороформ/метанол (5/1, 6 мл) и добавляют 4N хлористый водород в этилацетате (1 мл), затем растворитель выпаривают при пониженном давлении. Полученный осадок суспендируют в диэтиловом эфире и собирают фильтрованием, что дает названное соединение (106 мг). APCI-MS М/Е: 512/514 [M+H]+.
Примеры 328-332
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 327, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
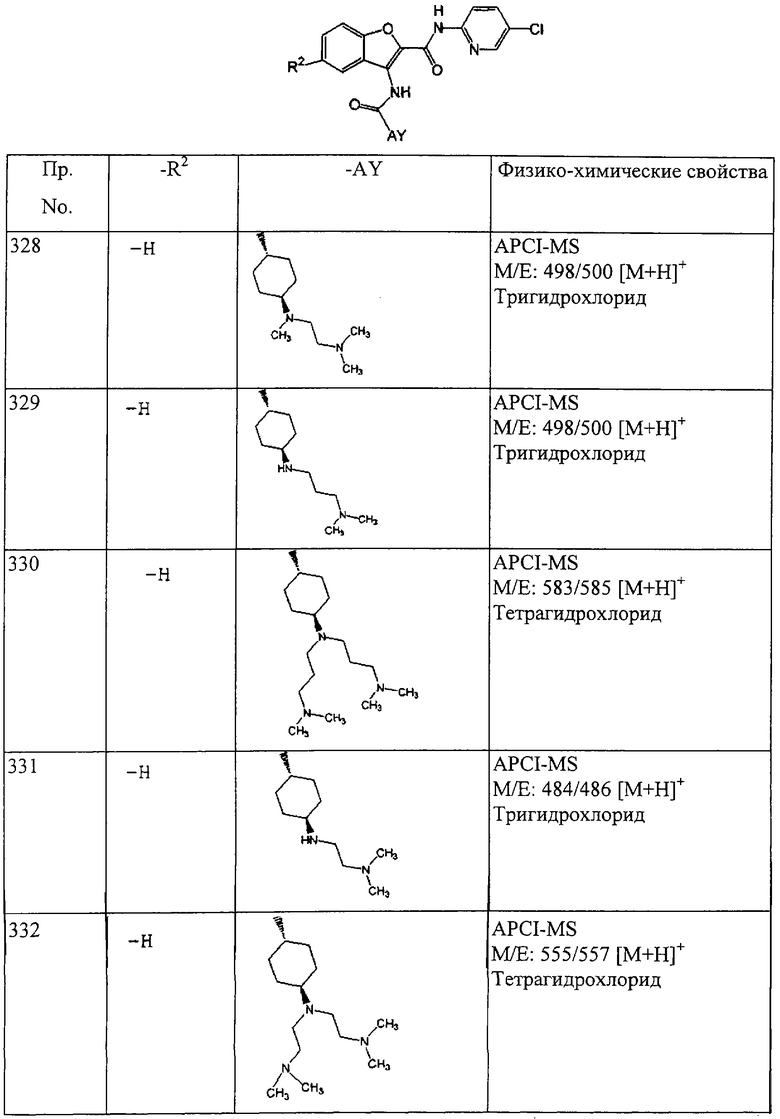
Пример 333: Транс-3-[4-(пиперидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
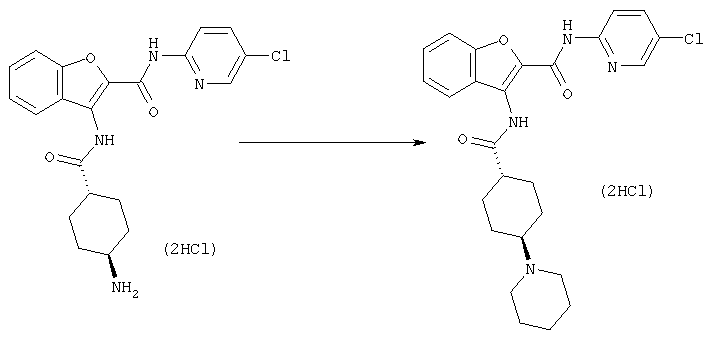
Транс-3-(4-аминоциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (125 мг), полученный в примере 219, суспендируют в дихлорметане (10 мл) и к смеси добавляют триэтиламин (102 мкл) при охлаждении льдом, после чего смесь перемешивают в течение нескольких минут. Затем последовательно добавляют около 25% водного раствора глутаральдегида (150 мг) и триацетоксиборгидрида натрия (155 мг), смесь перемешивают при охлаждении льдом в течение 2 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =3/1, затем 1/1), что дает транс-3-[4-(пиперидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (106 мг). Затем этот продукт растворяют в смеси хлороформ/метанол (5/1, 6 мл) и добавляют 4N хлористый водород в этилацетате (5 мл) при охлаждении льдом. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире и собирают фильтрованием, что дает названное соединение (107 мг).
APCI-MS М/Е: 481/483 [M+H]+.
Пример 334: Транс-3-[4-(N-ацетил-N-изопропиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
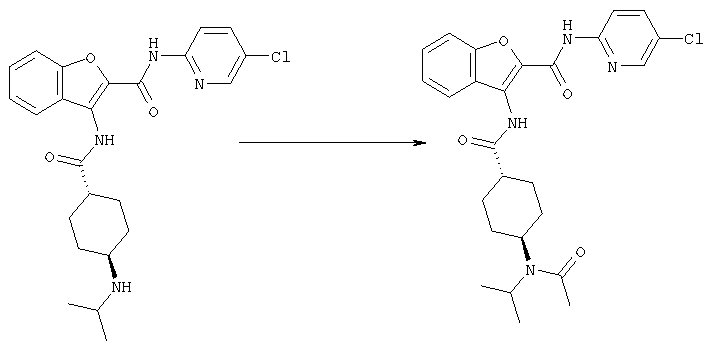
Транс-3-[4-(изопропиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (100 мг), полученный в примере 310, и триэтиламин (61 мкл) растворяют в хлороформе (5 мл) и в смесь добавляют ацетилхлорид (24 мкл). Смесь перемешивают при комнатной температуре в течение часа и выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь н-гексан/этилацетат =1/1, затем этилацетат). Полученный осадок суспендируют в н-гексане и собирают фильтрованием, что дает названное соединение (60 мг). APCI-MS М/Е: 497/499 [M+H]+.
Пример 335: Транс-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
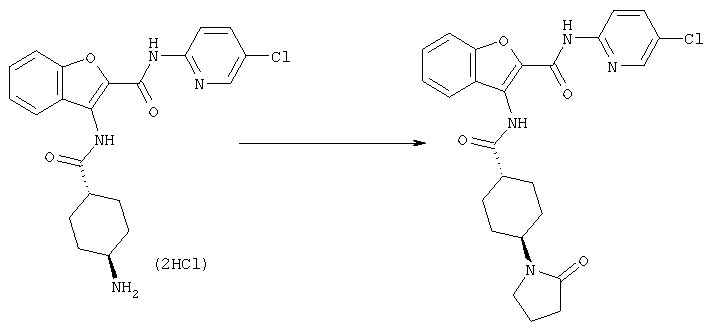
Транс-3-(4-аминоциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (150 мг), полученный в примере 219, суспендируют в дихлорметане (5 мл) и добавляют триэтиламин (129 мкл) при охлаждении льдом и смесь перемешивают в течение нескольких минут. Затем последовательно добавляют 15% водный раствор янтарного полуальдегида (290 мкл) и триацетоксиборгидрида натрия (131 мг) и при охлаждении льдом, смесь перемешивают в течение 0,5 часа. Затем последовательно добавляют 1-гидроксибензотриазол (63 мг), 1-этил-3-(3-диметил-аминопропил)карбодиимид гидрохлорид (118 мг) и N,N-диметилформамид (3 мл) и смесь перемешивают при комнатной температуре в течение 15 часов. Реакционный раствор концентрируют при пониженном давлении и выливают хлороформ. Смесь промывают последовательно насыщенным водным раствором гидрокарбоната натрия, водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =1/1, затем этилацетат) и полученный осадок суспендируют в н-гексане и собирают фильтрованием, что дает названное соединение (29 мг). APCI-MS М/Е: 481/483 [MH-H]+.
Пример 336: Транс-3-[4-(трет-бутоксикарбониламино)циклогексилкарбониламино]-5-карбокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
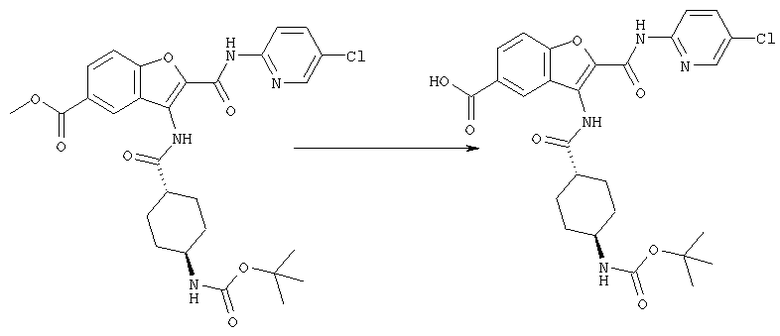
Транс-3-[4-(трет-бутоксикарбониламино)циклогексилкарбониламино]-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (540 мг), полученный в примере 209, обрабатывают способом, аналогичным описанному в примере 77, что дает названное соединение (475 мг). ESI-MS М/Е: 555/557 [M-Н]-.
Пример 337: Транс-3-[4-(N-трет-бутоксикарбонил-N-метиламино)циклогексилкарбониламино]-5-карбокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
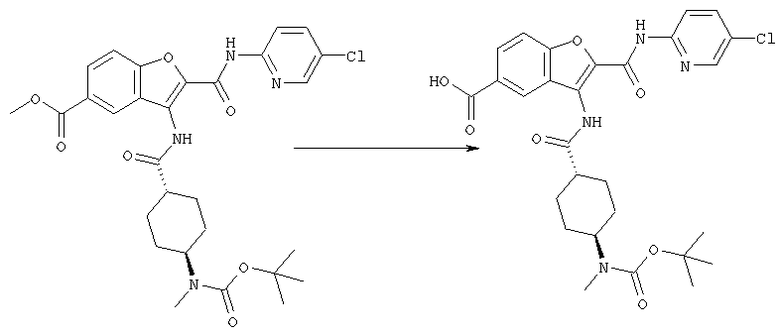
Транс-3-[4-(N-трет-бутоксикарбонил-N-метиламино)циклогексилкарбониламино]-5-метоксикарбонил-N-5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (3,52 г), полученный в примере 202, обрабатывают способом, аналогичным описанному в примере 77, что дает названное соединение (3,19 г). ESI-MS М/Е: 569/571 [M-Н]-.
Примеры 338-340
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 87, что дает следующие соединения.
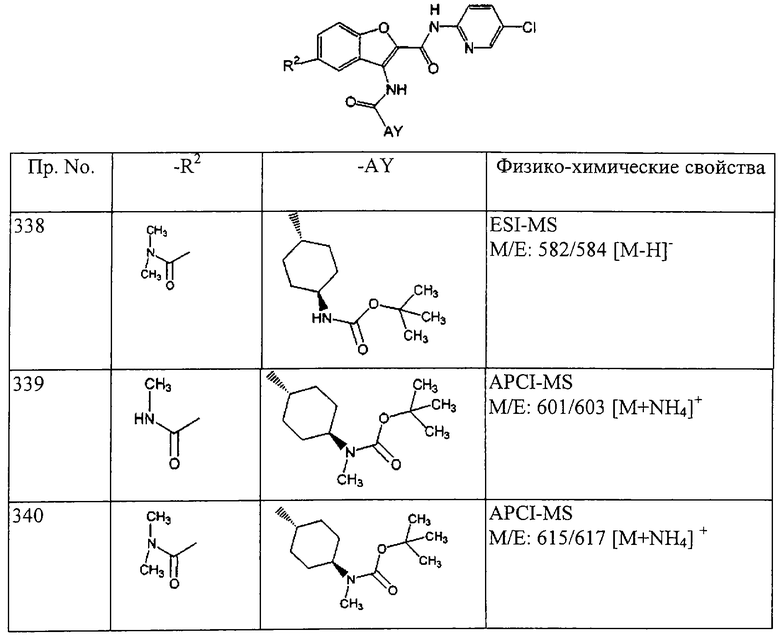
Примеры 341-344
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 218, что дает следующие соединения в свободном виде или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
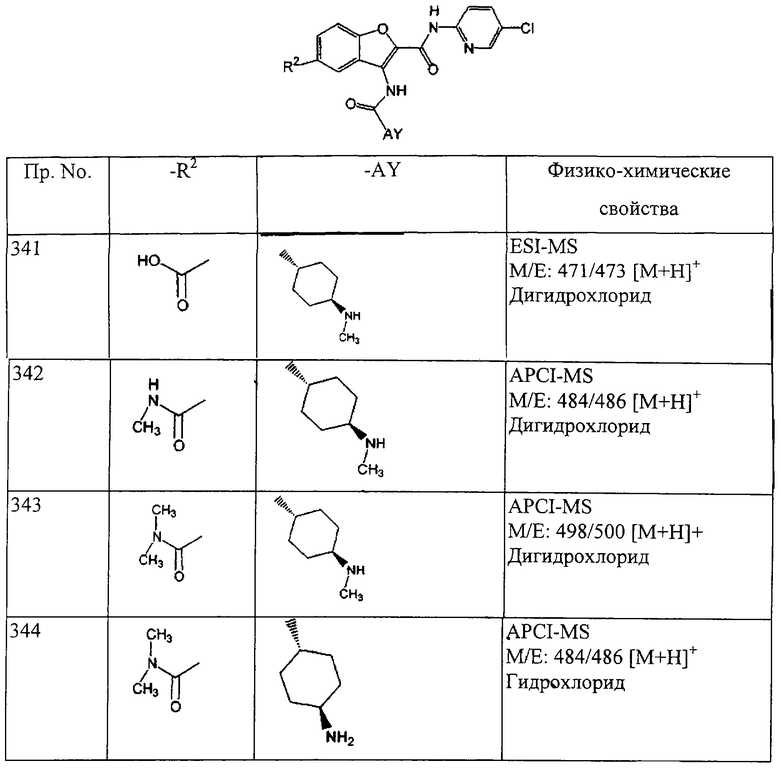
Пример 345: Транс-5-диметиламинокарбонил-3-[4-(изопропиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид гидрохлорид
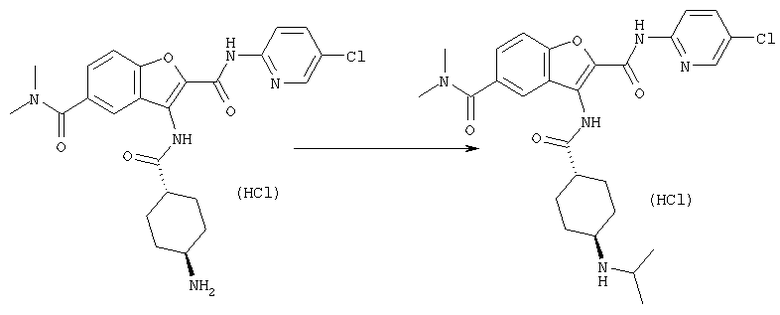
Транс-3-(4-аминоциклогексилкарбониламино)-5-диметиламинокарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид (160 мг), полученный в примере 344, суспендируют в дихлорметане (8 мл) и добавляют последовательно триэтиламин (129 мкл), ацетон (113 мкл) и триацетоксиборгидрид натрия (130 мг) при охлаждении льдом и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 17 часов. При охлаждении льдом в реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат, затем хлороформ/метанол =30/1). Полученный осадок растворяют в этаноле и добавляют 4N хлористый водород в этилацетате. Реакционный раствор концентрируют и полученный осадок суспендируют в диэтиловом эфире. Осадки собирают фильтрованием, что дает названное соединение (94 мг). APCI-MS М/Е: 526/528 [M+H]+.
Пример 346: Транс-5-карбокси-3-[4-(изопропиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
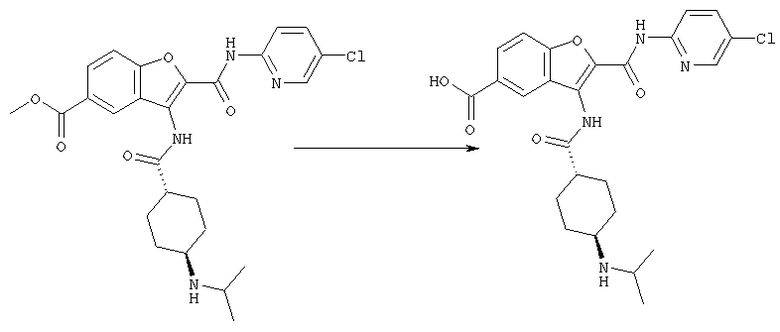
Транс-3-[4-(изопропиламино)циклогексилкарбониламино]-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (690 мг), полученный в примере 311, суспендируют в смеси тетрагидрофуран/метанол (1:1, 10 мл) и при охлаждении льдом добавляют 4N водный раствор гидроксида натрия (3 мл). Смесь нагревают до комнатной температуры и перемешивают в течение 18 часов. Реакционный раствор концентрируют при пониженном давлении и выливают в ледяную воду. Смесь нейтрализуют 10% раствором соляной кислоты и осадки собирают фильтрованием, промывают последовательно водой, тетрагидрофураном и диэтиловым эфиром и сушат, что дает названное соединение (702 мг). ESI-MS М/Е: 497/499 [M-Н]-.
Примеры 347-349
Транс-5-карбокси-3-[4-(изопропиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид, полученный в примере 346, обрабатывают способом, аналогичным описанному в примере 87, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
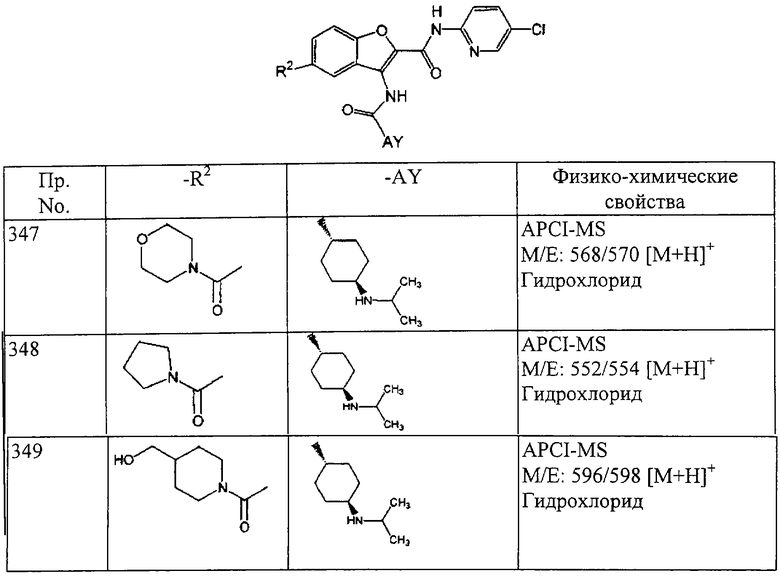
Примеры 350-354
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 218, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
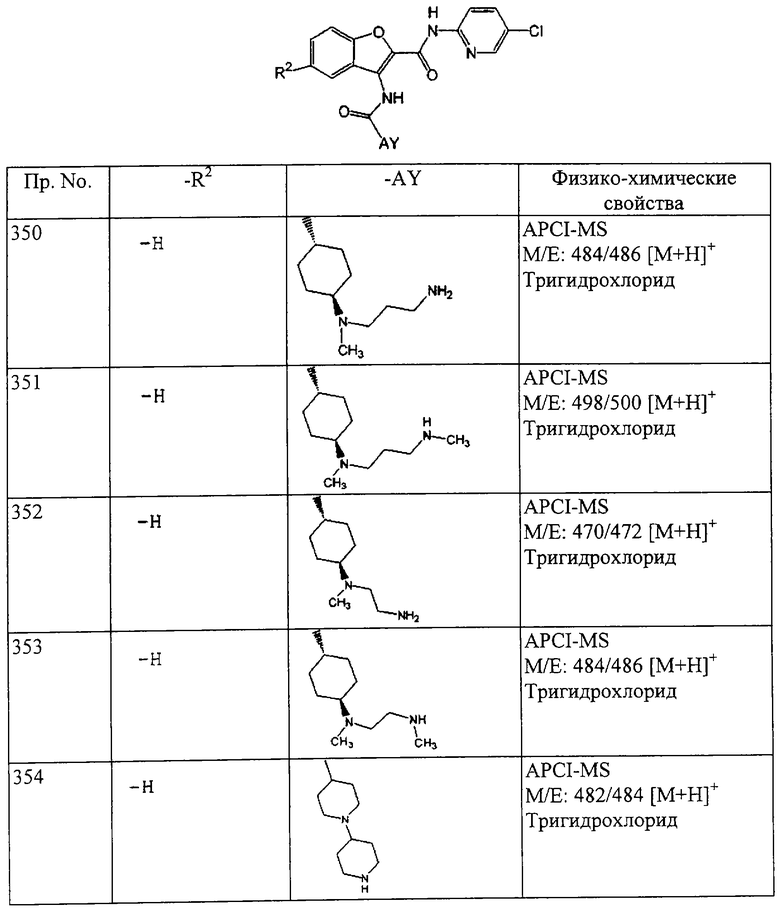
Примеры 355-362
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 239 или в примере 246, что дает следующие соединения в свободном виде или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
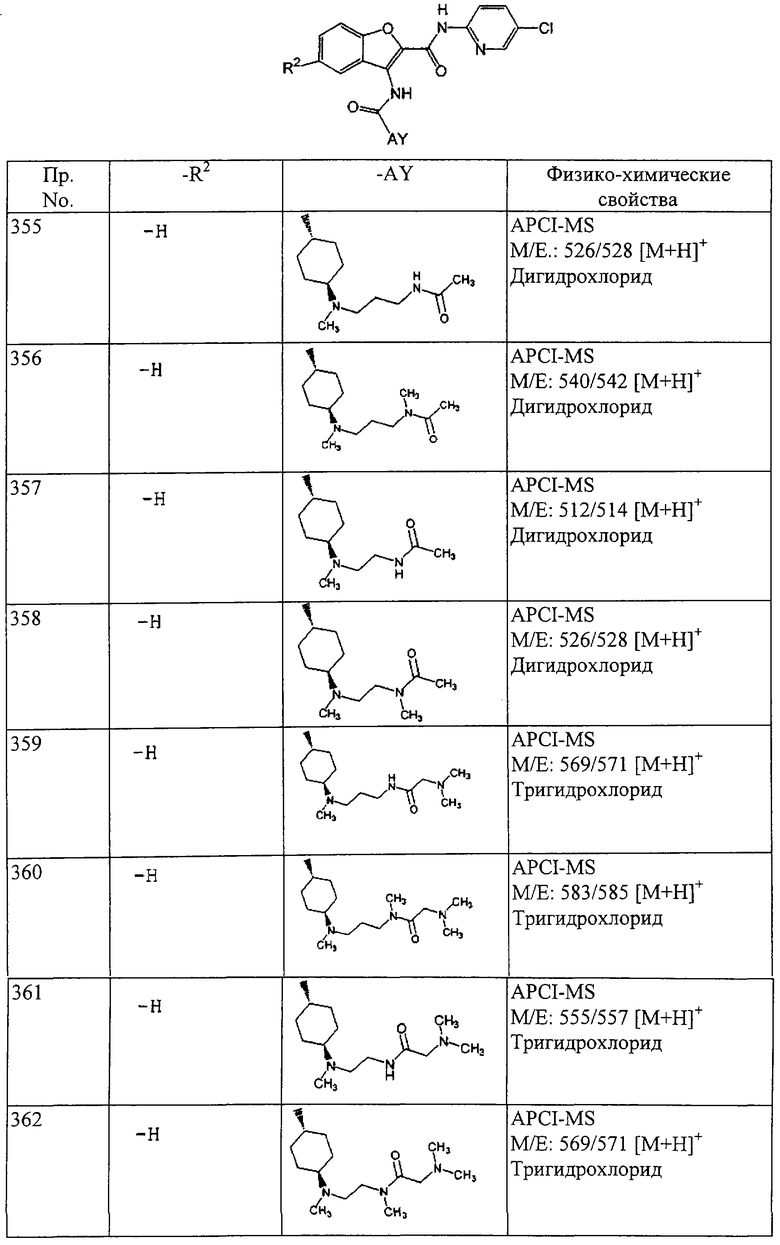
Примеры 363-364
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 306, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
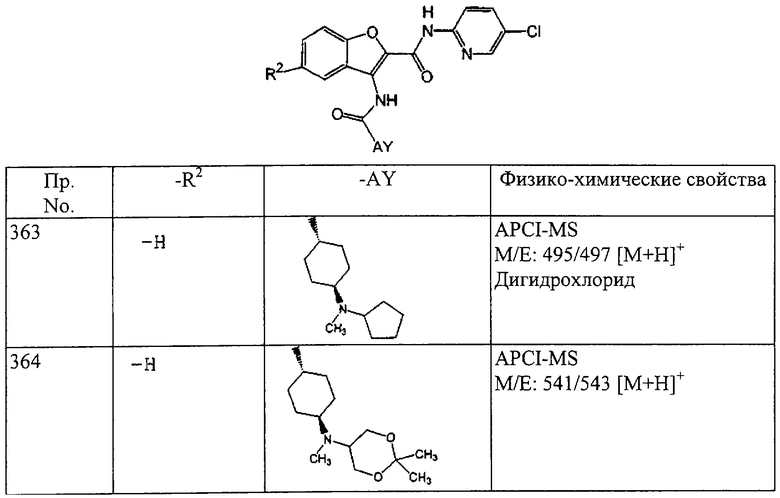
Примеры 365-366
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 201, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
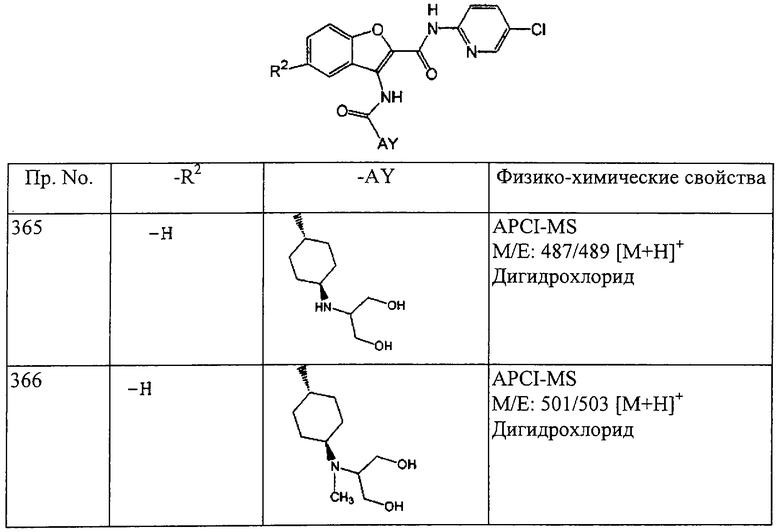
Пример 367:
Иодид [4-[2-(4-хлорфенилкарбамоил)бензофуран-3-илкарбамоил]циклогексил]триметиламмония
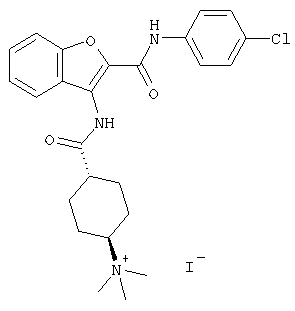
Транс-3-[4-(диметиламино)циклогексилкарбониламино]-N-(4-хлорфенил)бензофуран-2-карбоксамид (106 мг), полученный в примере 308, растворяют в дихлорметане (5 мл) и добавляют йодистый метил (30 мкл), после чего смесь перемешивают при комнатной температуре в течение 5 часов. В реакционный раствор выливают дихлорметандиэтиловый эфир (1/5, 25 мл) и осадки собирают фильтрованием, что дает названное соединение (126 мг). ESI-MS М/Е: 454/456 [M-I]+.
Пример 368: Иодид [4-[2-(5-хлорпиридин-2-илкарбамоил)бензофуран-3-илкарбамоил]циклогексил]триметиламмония
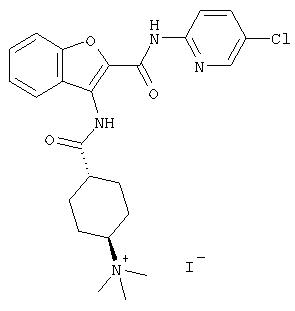
Транс-3-[4-(диметиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (150 мг), полученный в примере 306, и йодистый метил (21 мкл) обрабатывают способом, аналогичным описанному в примере 367, что дает названное соединение (137 мг). ESI-MS М/Е: 455/457 [M-I]+.
Пример 369: 3-[2-[1-(4,5-Дигидроксазо1-2-ил)пиперидин-4-ил]ацетиламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
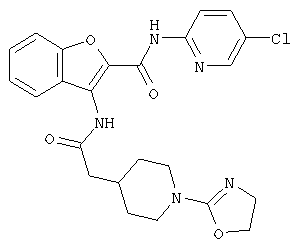
3-[2-(Пиперидин-4-ил)ацетиламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (103 мг), полученный в примере 220, суспендируют в тетрагидрофуране (5 мл) и добавляют изоцианат-2-бромэтил (27 мкл), после чего смесь перемешивают при комнатной температуре в течение часа добавляют триэтиламин (280 мкл) и смесь затем перемешивают при комнатной температуре в течение 6 часов. В реакционный раствор выливают воду и этилацетат и осадки собирают фильтрованием, промывают этилацетатом и сушат, что дает названное соединение (50 мг). APCI-MS М/Е: 482/484 [M+H]+.
Примеры 370-372
Соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 369, что дает следующие соединения.
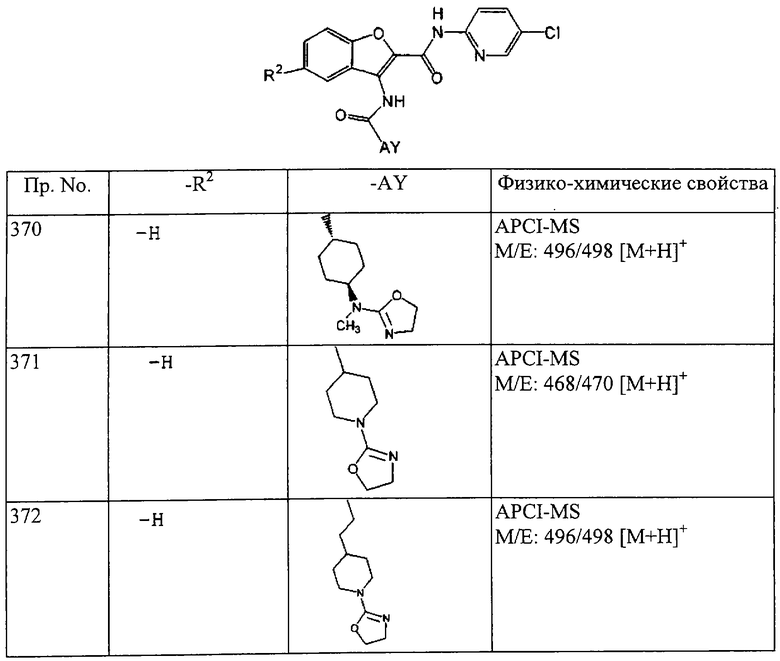
Пример 373: 3-[[1-(2-Тиазолил)пиперидин-4-ил]карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
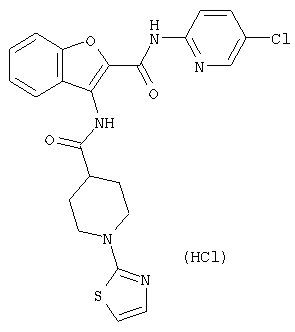
3-[(Пиперидин-4-ил)карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (100 мг), полученный в примере 228, суспендируют в 2-бутаноле (5 мл) и добавляют 2-бромтиазол (113 мкл) и N,N-диизопропилэтиламин (131 мкл) и смесь нагревают при температуре кипения с обратным холодильником в течение 24 часов. В реакционный раствор добавляют 2-бромтиазол (57 мкл) и N,N-диметилацетамид (2 мл) и смесь вновь нагревают при температуре кипения с обратным холодильником в течение 24 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают водой и насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь н-гексан/этилацетат =3/1, затем этилацетат), что дает 3-[[1-(2-тиазолил)пиперидин-4-ил]-карбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (38 мг). Этот продукт затем обрабатывают хлористым водородом в диоксане, что дает названное соединение (25 мг). APCI-MS М/Е: 482/484 [M+H]+.
Пример 374: Транс-3-[4-((пиримидин-2-ил)амино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
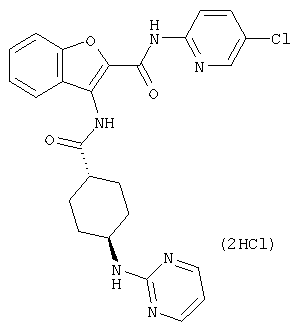
Транс-3-[4-аминоциклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (350 мг), полученный в примере 219, и 2-хлорпиримидин (99 мг) обрабатывают способом, аналогичным описанному в примере 373, что дает названное соединение (65 мг). APCI-MS М/Е: 491/493 [M+H]+.
Пример 375: Транс-3-[4-(пиррол-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
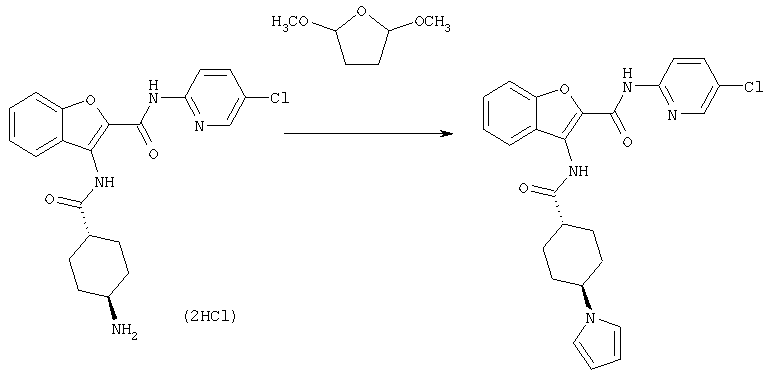
Транс-3-(4-аминоциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (200 мг), полученный в примере 219, тетрагидро-2,5-диметоксифуран (53 мкл), ацетат натрия (68 мг) перемешивают при температуре 80°С в течение 2 часов в уксусной кислоте (3 мл). В смесь добавляют тетрагидро-2,5-диметоксифуран (26 мкл) и смесь затем перемешивают при температуре 80°С в течение 2 часов. После охлаждения реакционный раствор выливают в ледяную воду и смесь экстрагируют хлороформом. Органический слой промывают насыщенным водным раствором гидрокарбоната натрия, насыщенным рассолом и сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат/гексан =1/5 → этилацетат/гексан =1/3), что дает названное соединение (96 мг). APCI-MS М/Е: 463/465 [M+H]+.
Пример 376: 3-[(1-трет-Бутоксикарбонилпиперидин-4-ил)оксикарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
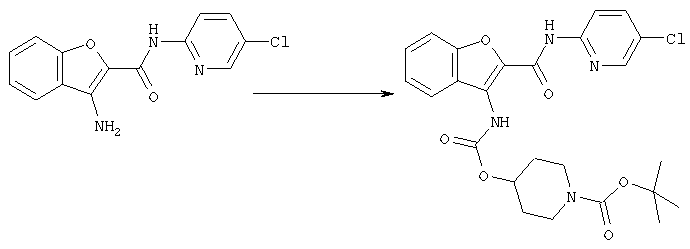
трет-Бутил-4-гидрокси-1-пиперидинкарбоксилат (175 мг) и трифосген (90 мг) растворяют в дихлорметане (5 мл) и добавляют при перемешивании пиридин (77 мкл) при охлаждении льдом. Реакционный раствор перемешивают при комнатной температуре в течение 3 часов и затем снова охлаждают льдом. К смеси добавляют 3-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (250 мг), полученный в примере приготовления 74, и смесь перемешивают в течение нескольких минут. Затем к смеси добавляют пиридин (105 мкл) и смесь перемешивают при комнатной температуре в течение 3 часов. Реакционный раствор выливают в воду и смесь экстрагируют хлороформом. Органический слой промывают последовательно 5% водным раствором лимонной кислоты, водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =10/1, затем 5/1), что дает названное соединение (406 мг).
APCI-MS М/Е: 515/517 [M+H]+.
Пример 377: Транс-3-[4-(трет-бутоксикарбониламино)циклогексилоксикарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
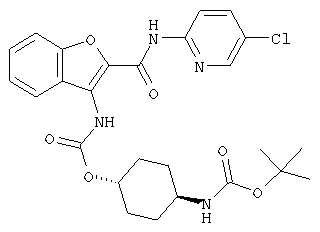
3-Амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (500 мг), полученный в примере приготовления 74, и трет-бутил транс-(4-гидроксициклогексил)карбамат (375 мг) обрабатывают способом, аналогичным описанному в примере 376, что дает названное соединение (680 мг). APCI-MS М/Е: 529/531 [МН-Н]+.
Примеры 378-379
Соединение, полученное в примере 376 или примере 377, обрабатывают способом, аналогичным описанному в примере 220, что дает следующие соединения.
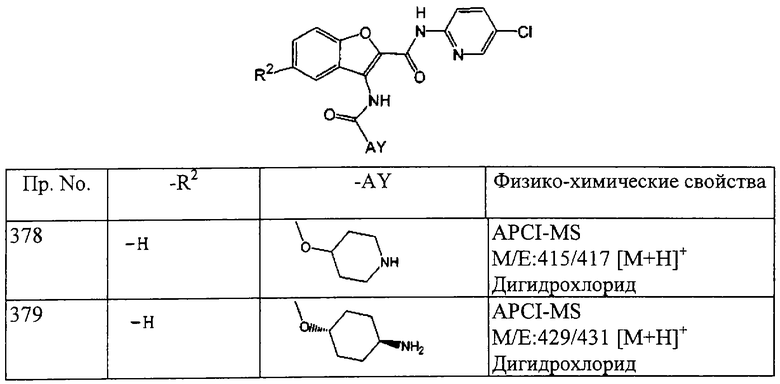
Примеры 380-381
Соединение, полученное в примере 378 или примере 379, обрабатывают способом, аналогичным описанному в примере 345, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
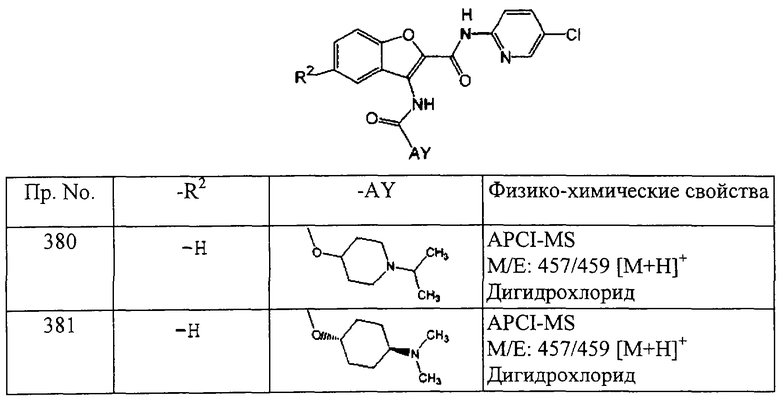
Пример 382: 3-[3-(1-Изопропилпиперидин-4-ил)уреидо]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
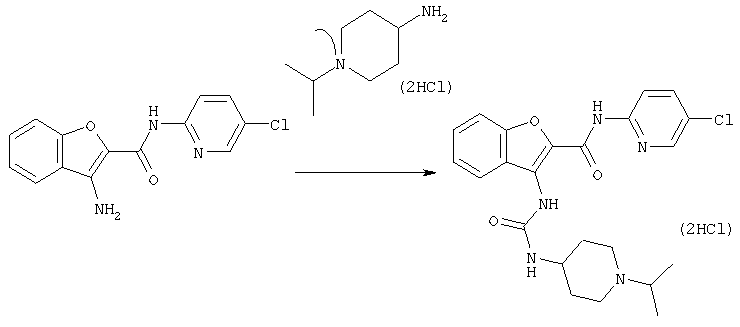
(1) Гидрохлорид 1-изопропилпиперидин-4-карбоновой кислоты (3,00 г), полученный в примере 130, суспендируют в толуоле (180 мл) и к смеси добавляют триэтиламин (5,0 мл) и дифенилфосфорилазид (4,0 мл), после чего ее нагревают при температуре 100°С в течение 2 часов. После охлаждения в реакционный раствор добавляют бензиловый спирт (4,5 мл) при комнатной температуре и смесь нагревают при температуре кипения с обратным холодильником в течение 4 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок разбавляют этилацетатом и промывают последовательно насыщенным водным раствором гидрокарбоната натрия, водой и насыщенным рассолом. Продукт сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/диэтиловый эфир =2/1, затем н-гексан/этилацетат =2/1), что дает сырой продукт (6,32 г), содержащий бензил (1-изопропилпиперидин-4-ил)карбамат. APCI-MS М/Е: 277 [M+H]+.
(2) Сырой продукт (6,32 г), содержащий бензил(1-изопропилпиперидин-4-ил)карбамат, полученный в примере 382-(1), растворяют в этаноле (100 мл) и добавляют 10% палладий на угле (600 мг), после чего смесь перемешивают при температуре окружающей среды в атмосфере водорода в течение ночи. Нерастворимые продукты удаляют фильтрованием и фильтрат концентрируют при пониженном давлении и подвергают азеотропной дистилляции с толуолом. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =1/1, затем хлороформ/метанол =20/1 и затем 10/1), что дает 4-амино-1-изопропилпиперидин (1,90 г). Полученный 4-амино-1-изопропилпиперидин обрабатывают 4N хлористым водородом в диоксане, что дает 4-амино-1-изопропилпиперидин дигидрохлорид. APCI-MS М/Е: 143 [M+H]+.
(3) 4-Амино-1-изопропилпиперидин дигидрохлорид (112 мг), полученный в примере 382-(2), и трифосген (54 мг) суспендируют в дихлорметане (3 мл) и добавляют пиридин (253 мкл) с перемешиванием при охлаждении льдом. Реакционный раствор перемешивают при комнатной температуре в течение 3 часов и добавляют 3-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (150 мг), полученный в примере приготовления 74, и смесь перемешивают при комнатной температуре в течение 12 часов, затем ее нагревают при температуре кипения с обратным холодильником в течение 15 часов. В реакционный раствор выливают воду и насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =4/1, затем 2/1), что дает 3-[3-(1-изопропилпиперидин-4-ил)уреидо]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (112 мг). Потом этот продукт обрабатывают 4N хлористым водородом в этилацетате (2 мл), что дает названное соединение (114 мг). APCI-MS М/Е: 456/458 [M+H]+.
Пример 383: Транс-3-(4-метилгомопиперизин-1-илкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
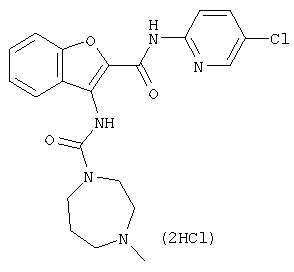
3-Амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (200 мг), полученный в примере приготовления 74, и 1-метилгомопиперазин (86 мкл) обрабатывают способом, аналогичным описанному в примере 382-(3), что дает названное соединение (110 мг). APCI-MS М/Е: 428/430 [M+H]+.
Пример 384: Транс-3-[4-(2-оксопиперидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
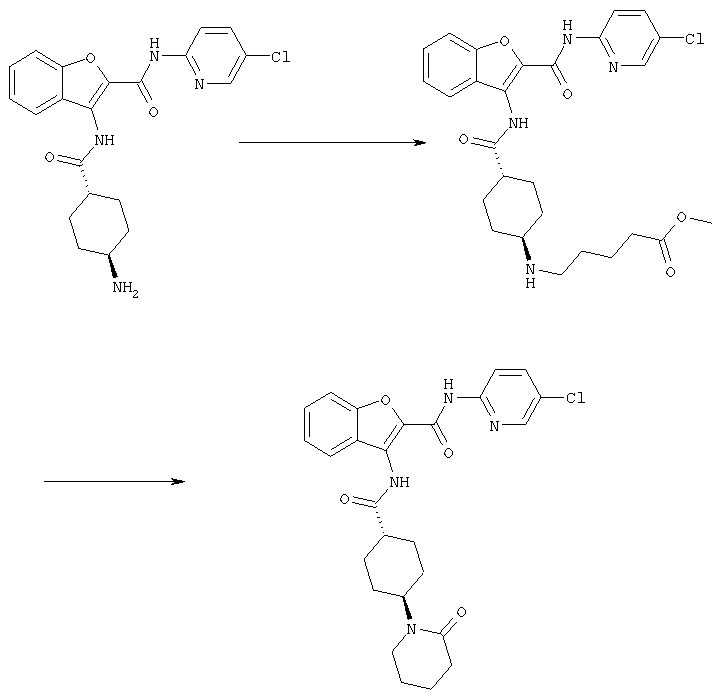
(1) Транс-3-(4-аминоциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (300 мг), полученный в примере 219, суспендируют в N,N-диметилацетамиде (5 мл) и добавляют метил-5-бромвалерат (106 мкл), N,N-диизопропилэтиламин (537 мкл) и иодид калия (111 мг) и смесь перемешивают при температуре 100°С в течение 24 часов. Затем добавляют метил- 5-бромвалерат (106 мкл), N,N-диизопропилэтиламин (537 мкл) и иодид калия (111 мг) и смесь вновь перемешивают при температуре 100°С в течение 12 часов. Реакционный раствор разбавляют этилацетатом и промывают последовательно насыщенным водным раствором гидрокарбоната натрия, водой, насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =1/1, затем этилацетат), что дает транс-3-[4-(4-метоксикарбонилбутиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид (101 мг). APCI-MS М/Е: 527/529 [M+H]+.
(2) Транс-3-[4-(4-метоксикарбонилбутиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (95 мг), полученный выше (1), растворяют в тетрагидрофуране (3 мл) и добавляют 1N водный раствор гидроксида натрия (216 мкл) и смесь перемешивают при комнатной температуре в течение 4 часов. В смесь добавляют 1N водный раствор гидроксида натрия (684 мкл) и затем смесь перемешивают в течение 2 дней. Реакционный раствор концентрируют досуха при пониженном давлении и в полученный осадок добавляют N,N-диметилформамид (3 мл), 1-гидроксибензотриазол (73 мг) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (104 мг). Смесь перемешивают при комнатной температуре в течение одного дня и затем добавляют 1-гидроксибензотриазол (73 мг) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (104 мг) и смесь затем перемешивают в течение одного дня. В реакционный раствор выливают насыщенный водный раствором гидрокарбоната натрия и смесь экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом и сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: этилацетат), что дает названное соединение (40 мг). APCI-MS М/Е: 495/497 [M+H]+.
Пример 385: Транс-5-(N2-гидрокси)амидино-3-[4-(2-оксо-пирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
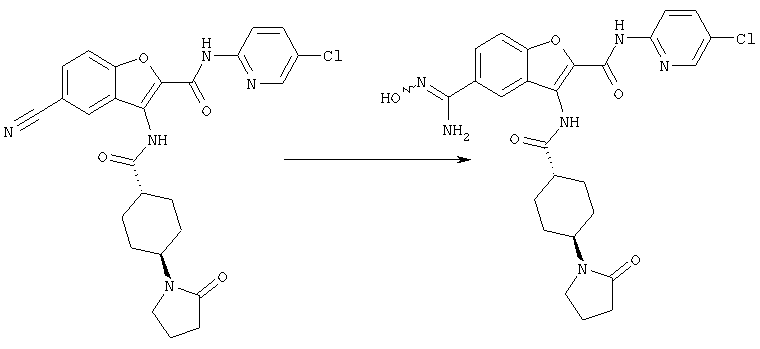
Транс-5-циано-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (107 мг), полученный в примере 6, суспендируют в диметилсульфоксиде (2 мл) и добавляют хлорид гидроксиаммония (36 мг) и 28% раствор метоксида натрия в метаноле (100 мкл). Смесь нагревают при температуре 50°С в течение 2 часов, а затем при температуре 80°С в течение 2 часов. Реакционный раствор выливают в ледяную воду и осадки собирают фильтрованием и очищают с помощью HPLC с рециклом, что дает названное соединение (25 мг; APCI-MS М/Е: 539/541 [M+H]+) и транс-5-аминокарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (18 мг; APCI-MS М/Е: 524/526 [M+H]+).
Пример 386: Транс-5-[2-(гуанидинокси)этокси]-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
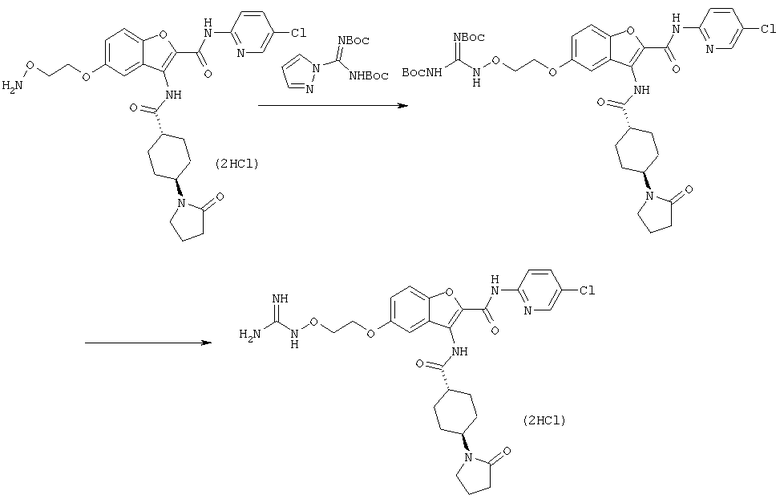
(1) Транс-5-(2-аминоксиэтокси)-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид (90 мг), полученный в примере 183, растворяют в N,N-диметилформамиде (3 мл) и добавляют N,N-диизопропилэтиламин (38 мкл) и N,N-бис(трет-бутоксикарбонил)-1Н-пиразол-1-карбоксамидин (57 мг) и смесь перемешивают при комнатной температуре в течение одного дня. Реакционный раствор концентрируют при пониженном давлении и осадок выливают в воду и экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =1/1, затем этилацетат), что дает транс-5-{2-[N,N'-бис(трет-бутоксикарбонил)гуанидинокси]этокси}-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (82 мг). ESI-MS М/Е: 820/822 [M+Na]+, 798/800 [M+H]+.
(2) К транс-5-{2-[N,N'-бис(трет-бутоксикарбонил)гуадинокси]этокси}-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамиду (73 мг), полученному выше (1), добавляют трифторуксусную кислоту (2 мл) и смесь перемешивают при комнатной температуре в течение 12 часов. Реакционный раствор концентрируют при пониженном давлении и осадок нейтрализуют насыщенным водным раствором карбоната калия и экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: хлороформ, затем смесь хлороформ/метанол =97/3), что дает транс-5-[2-(гуанидинокси)этокси]-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (15 мг). Затем этот продукт (15 мг) суспендируют в метаноле (0,5 мл) и добавляют 4N хлористый водород в диоксане (25 мкл). В смесь выливают диэтиловый эфир и осадки промывают диэтиловым эфиром и сушат, что дает названное соединение (17 мг). ESI-MS М/Е: 598/600 [M+H]+.
Примеры 387-391
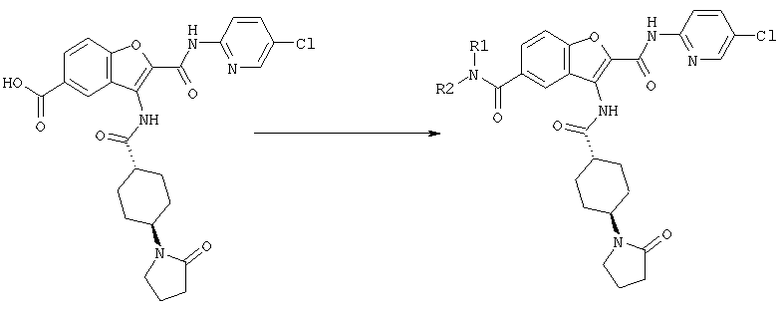
Транс-5-карбокси-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид, полученный в примере 77, и соответствующие исходные соединения обрабатывают способом, аналогичным описанному в примере 87, что дает следующие соединения.
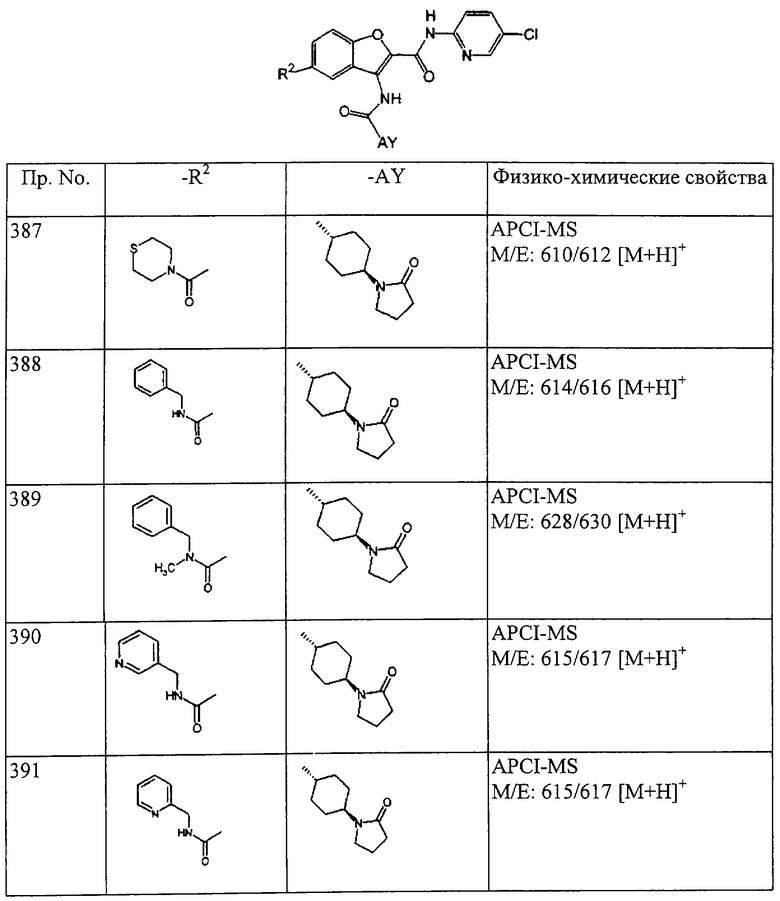
Примеры 392-393
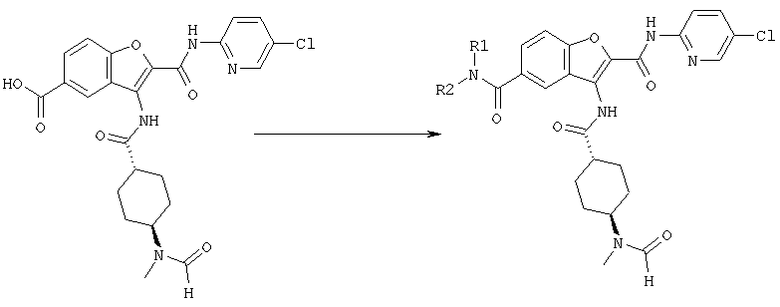
Транс-5-карбокси-3-[4-(N-формил-N-метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид, полученный в примере 258, и аминосоединения обрабатывают способом, аналогичным описанному в примере 261, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
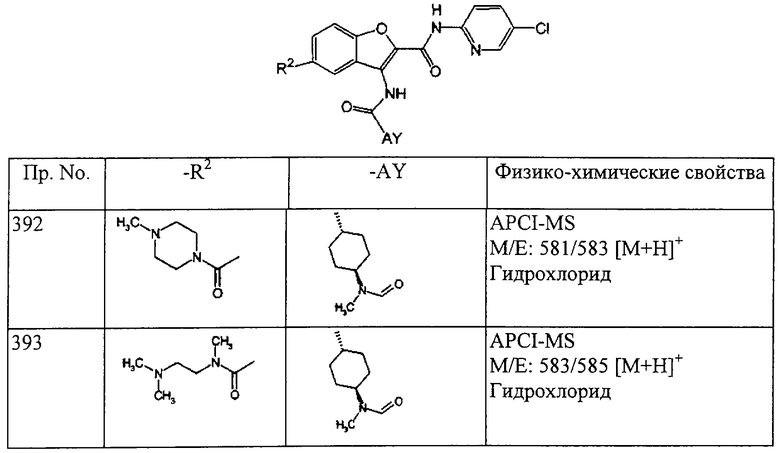
Примеры 394-399
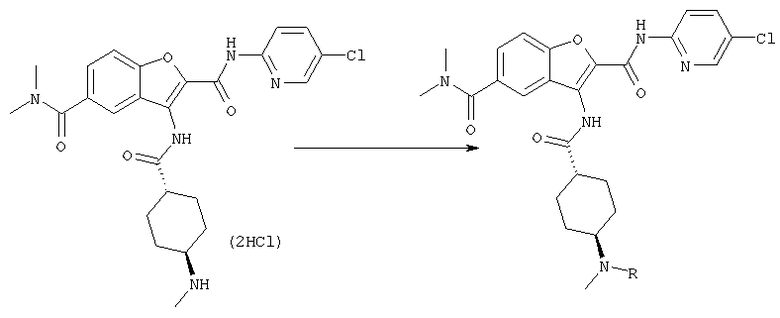
Транс-5-диметиламинокарбонил-3-[4-(метиламино)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид, полученный в примере 343, и хлорангидриды кислот обрабатывают способом, аналогичным описанному в примере 239, что дает следующие соединения.
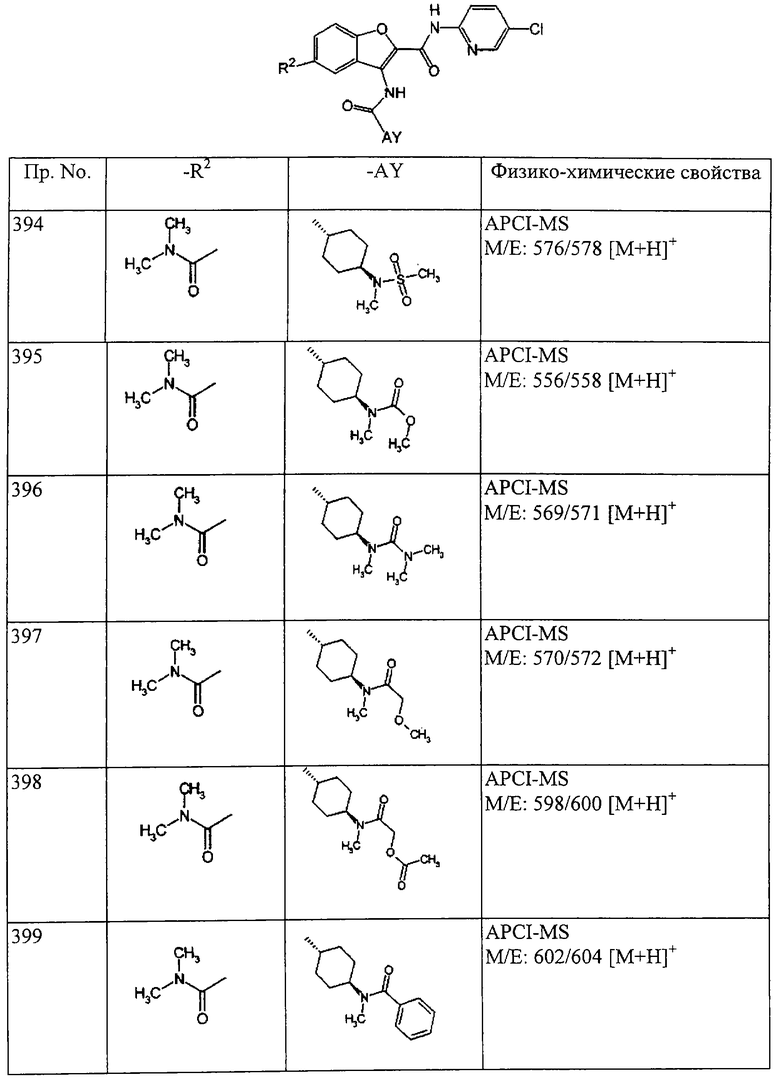
Пример 400: Транс-5-диметиламинокарбонил-3-[4-(N-гидроксиацетил-N-метиламино)-циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
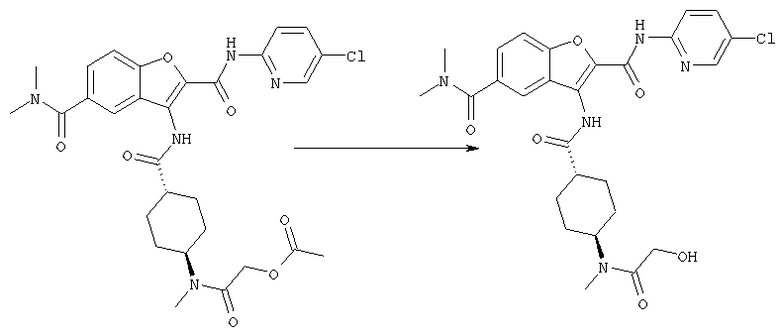
Транс-3-[4-(N-ацетоксиацетил-N-метиламино)циклогексилкарбониламино]-5-диметиламинокарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (91 мг), полученный в примере 398, растворяют в смеси тетрагидрофуран/метанол (2:3, 5 мл) и добавляют при комнатной температуре 2N водный раствор гидроксида натрия (300 мкл) и смесь перемешивают в течение 4 часов. Реакционный раствор подкисляют разбавленной соляной кислотой, а затем разбавляют хлороформом. Смесь сушат над сульфатом натрия, и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью HPLC с рециклом, что дает названное соединение (44 мг). APCI-MS М/Е: 556/558 [M+H]+.
Примеры 401-403
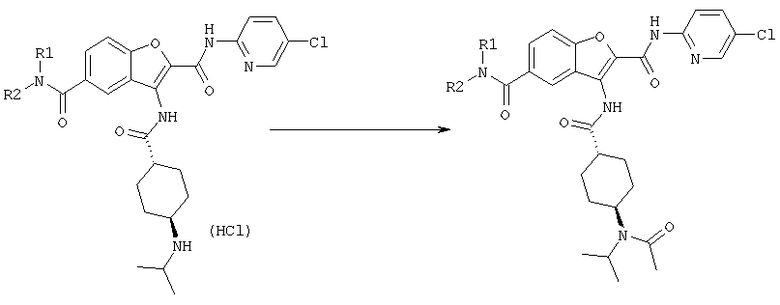
Соединение, полученное в примере 345, 347 или 348, и ацетилхлорид обрабатывают способом, аналогичным описанному в примере 334, что дает следующие соединения.
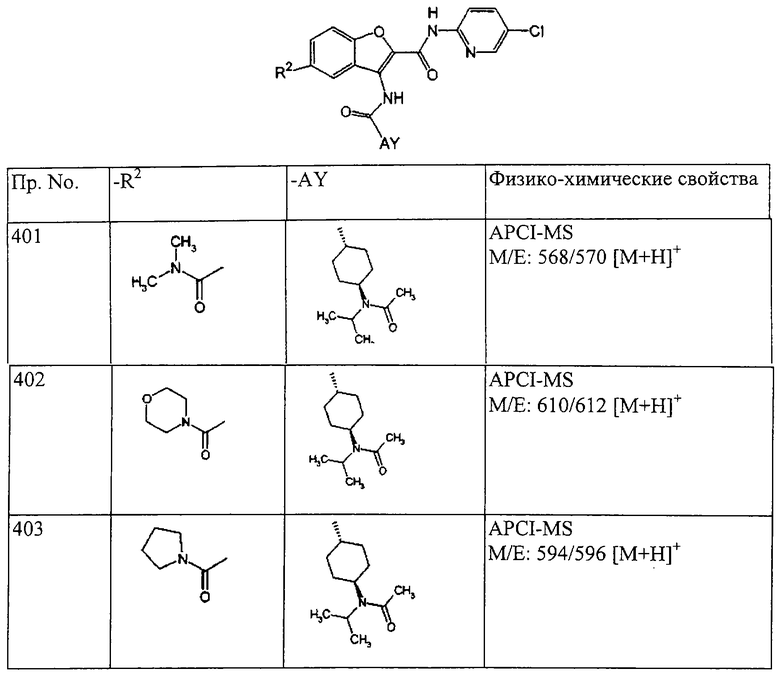
Примеры 404-405
3-Амино-5-нитро-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид, полученный в примере приготовления 86, и карбоновую кислоту обрабатывают способом, аналогичным описанному в примере 1 или в примере 2, что дает следующие соединения.
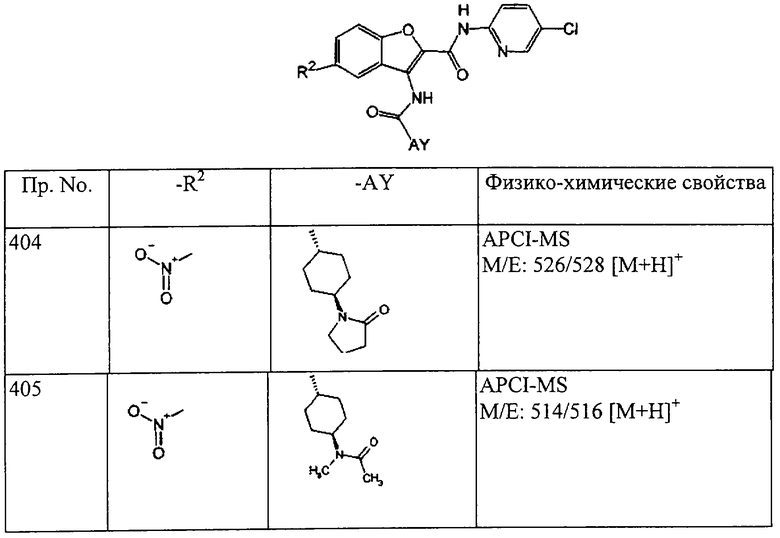
Пример 406: Транс-5-амино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
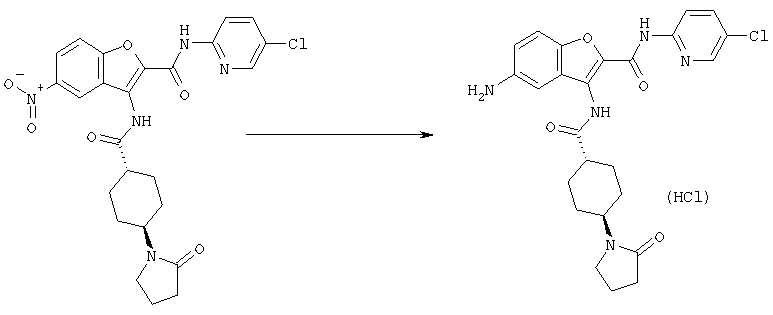
Транс-5-нитро-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,50 г), полученный в примере 404, суспендируют в смеси этанол/тетрагидрофуран (1:1, 400 мл) и добавляют никель Ренея, после чего смесь перемешивают при комнатной температуре под давлением атмосферы водорода в течение 12 часов. В полученную суспензию желтого цвета выливают хлороформ (200 мл) и смесь перемешивают при комнатной температуре в течение 0,5 часа. Нерастворимые продукты удаляют фильтрованием и фильтрат концентрируют при пониженном давлении. Осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ в хлороформ/метанол =4/1), суспендируют в смеси этилацетат/диэтиловый эфир. Осадки собирают фильтрованием, промывают диэтиловым эфиром и сушат, что дает транс-5-амино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (1,94 г). Этот продукт (150 мг) суспендируют в метаноле и смесь обрабатывают 4N хлористым водородом в диоксане, что дает названное соединение (158 мг). APCI-MS М/Е: 496/498 [M+H]+
Пример 407: Транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид
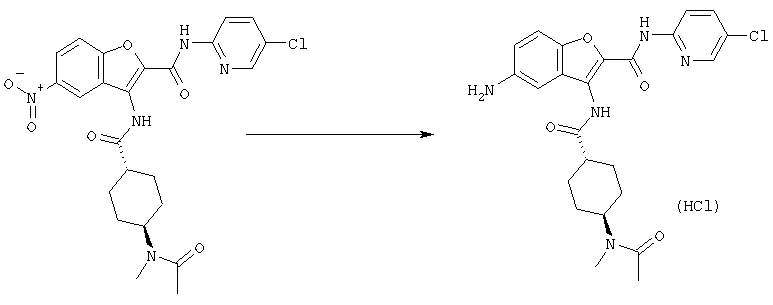
Транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-нитро-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,27 г), полученный в примере 405, обрабатывают способом, аналогичным описанному в примере 406, что дает транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (1,62 г). Полученное свободное соединение (150 мг) суспендируют в метаноле и обрабатывают 4N хлористым водородом в диоксане, что дает названное соединение (158 мг). APCI-MS М/Е: 484/486 [M+H]+.
Примеры 408-409
Транс-5-амино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид, полученный в примере 406, или транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид гидрохлорид, полученный в примере 407, обрабатывают способом, аналогичным описанному в примере 198, что дает следующие соединения в свободном виде, или которые затем обрабатывают хлористым водородом, что дает их гидрохлориды.
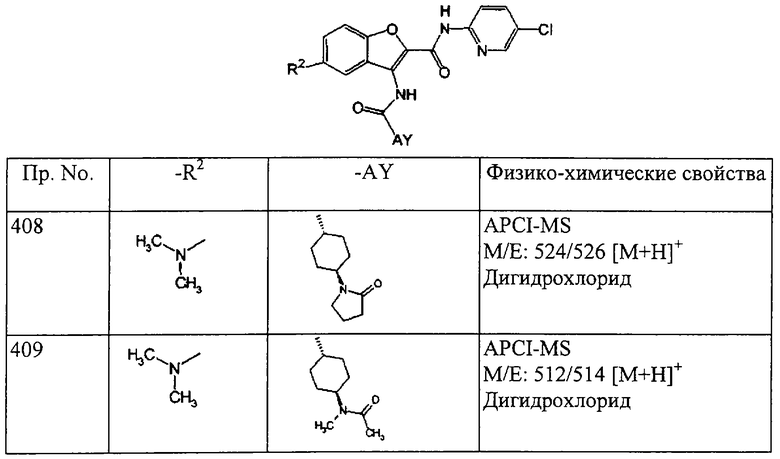
Пример 410: Транс-5-диметиламинокарбонил-3-[4-(3-оксоморфолин-4-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
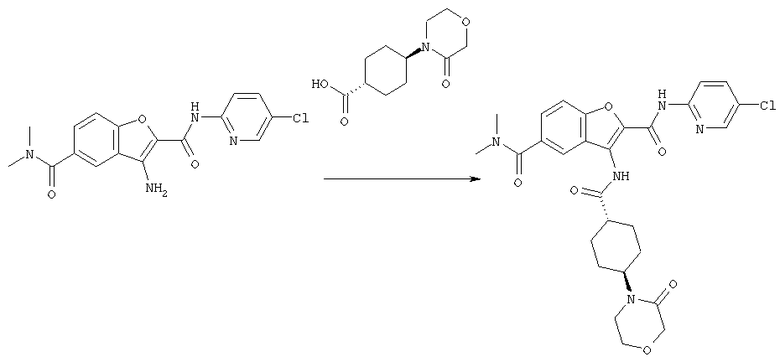
Транс-4-(3-оксоморфолин-4-ил)циклогексанкарбоновую кислоту (85 мг), полученную в примере приготовления 141, растворяют в хлороформе (3 мл) и добавляют тионилхлорид (30 мкл) и по каплям N,N-диметилформамид и смесь перемешивают при комнатной температуре в течение 15 часов. В полученный реакционный раствор добавляют 3-амино-5-диметиламинокарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (96 мг), полученный в примере приготовления 156, и пиридин (2 мл) и смесь перемешивают при комнатной температуре в течение 2 часов. В реакционный раствор выливают насыщенный водный раствор гидрокарбоната натрия и смесь экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =2/1, затем этилацетат) и затем очищают с помощью HPLC с рециклом, что дает названное соединение (28 мг). APCI-MS М/Е: 568/570 [M+H]+.
Примеры 411-417
Аминосоединения, полученные в примерах приготовления 156-158, и соответствующие карболовые кислоты обрабатывают способом, аналогичным описанному в примере 410, что дает следующие соединения.
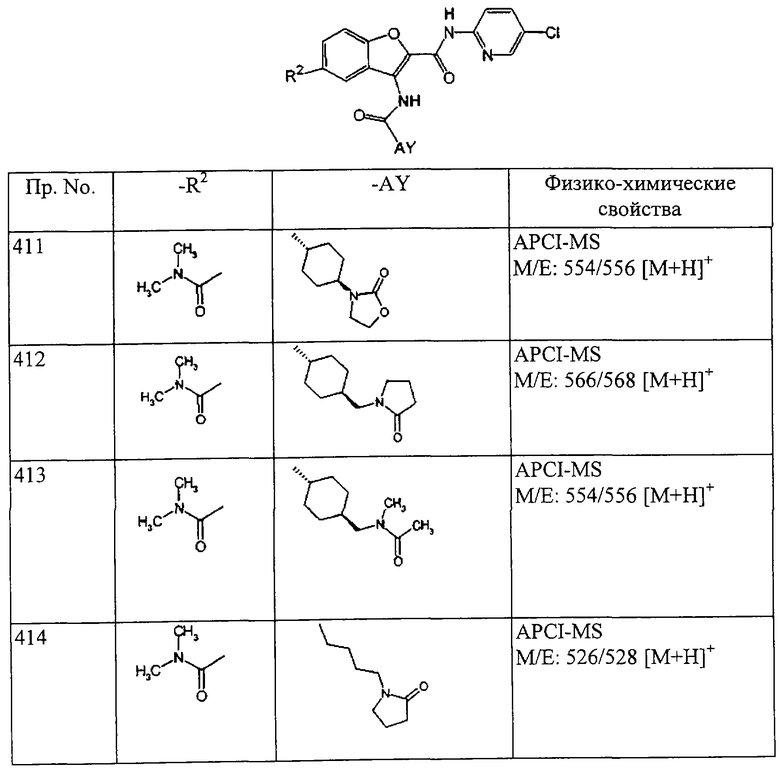
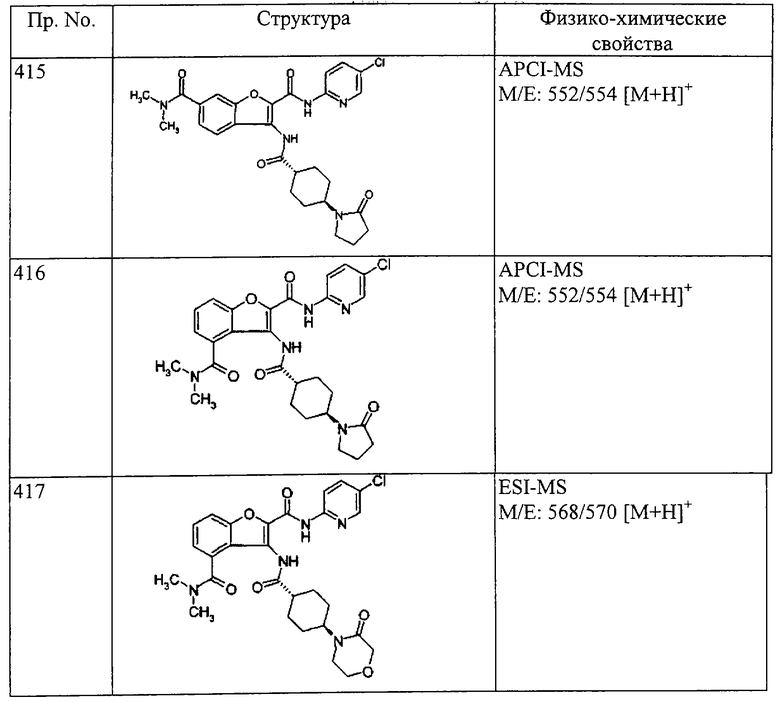
Пример 418: Транс-4-метоксикарбонил-3-[4-(2-оксооксазолидин-3-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
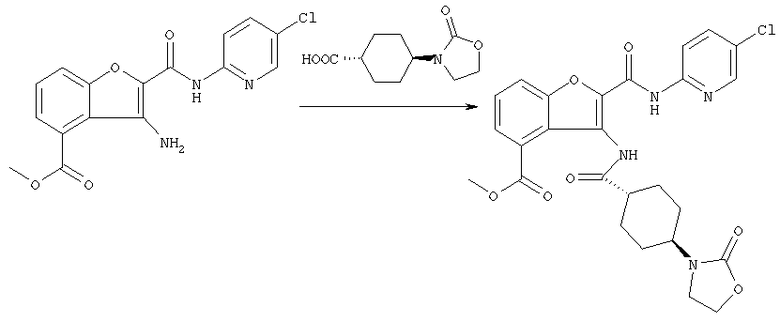
3-Амино-4-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (351 мг), полученный в примере приготовления 152, и транс-4-(2-оксооксазолидин-3-ил)циклогексанкарбоновую кислоту (432 мг), полученную в примере приготовления 142, обрабатывают способом, аналогичным описанному в примере 1, что дает названное соединение (129 мг). APCI-MS М/Е: 541/543 [M+H]+.
Пример 419: Транс-4-карбокси-3-[4-(2-оксооксазолидин-3-ил)-циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
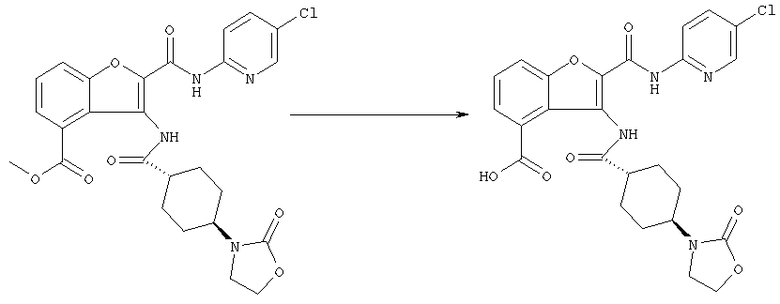
Транс-4-метоксикарбонил-3-[4-(2-оксо-оксазолидин-3-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (107 мг), полученный в примере 418, обрабатывают способом, аналогичным описанному в примере 77, что дает названное соединение (80,4 мг). ESI-MS М/Е: 525/527 [M-Н]-.
Пример 420: Транс-4-диметиламинокарбонил-3-[4-(2-оксооксазолидин-3-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
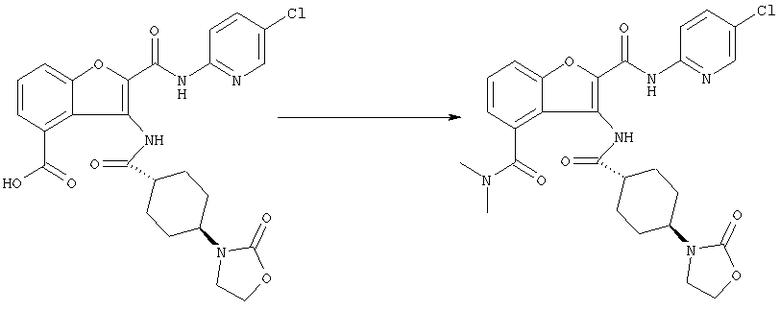
Транс-4-карбокси-3-[4-(2-оксооксазолидин-3-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (50 мг), полученный в примере 419, обрабатывают способом, аналогичным описанному в примере 87, что дает названное соединение (36,4 мг). APCI-MS М/Е: 554/556 [M+H]+.
Пример 421: Транс-4-метоксикарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
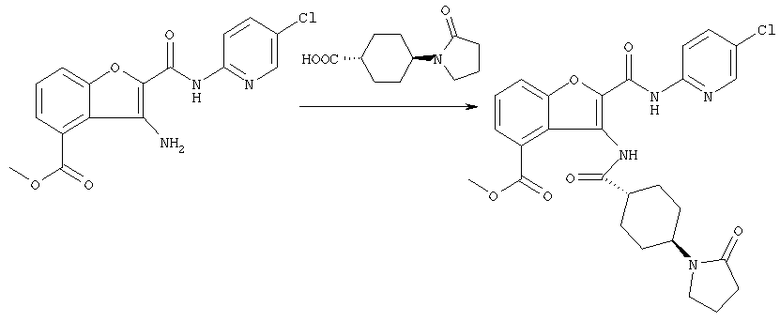
3-Амино-4-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,33 г), полученный в примере приготовления 152, и транс-4-(2-оксопирролидин-1-ил)циклогексанкарбоновую кислоту (2,06 г), полученную в примере приготовления 142, обрабатывают способом, аналогичным описанному в примере 1, что дает названное соединение (1,90 г). APCI-MS М/Е: 539/541 [M+H]+.
Пример 422: Транс-4-карбокси-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
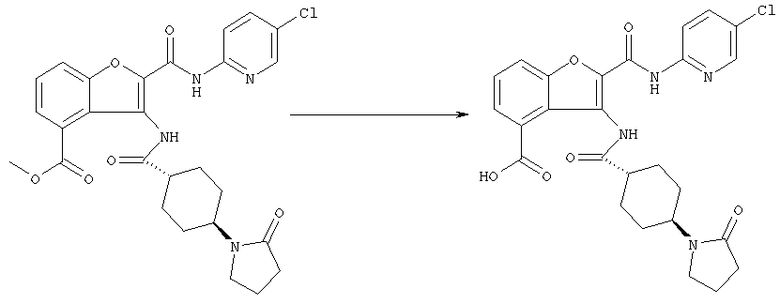
Транс-4-метоксикарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (880 мг), полученный в примере 421, обрабатывают способом, аналогичным описанному в примере 77, что дает названное соединение (623 мг).
ESI-MS М/Е: 523/525 [M-Н]-.
Пример 423: Транс-4-гидроксиметил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
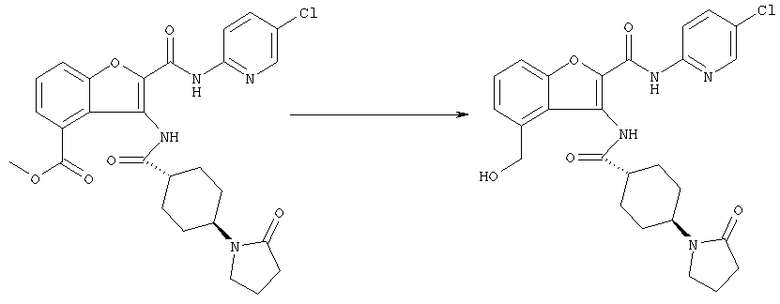
Транс-4-метоксикарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (350 мг), полученный в примере 421, обрабатывают способом, аналогичным описанному в примере 145, что дает названное соединение (40,9 мг). ESI-MS М/Е: 511/513 [M+H]+.
Пример 424: Транс-4-[N-(2-диметиламиноэтил)-N-метил]аминокарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид дигидрохлорид
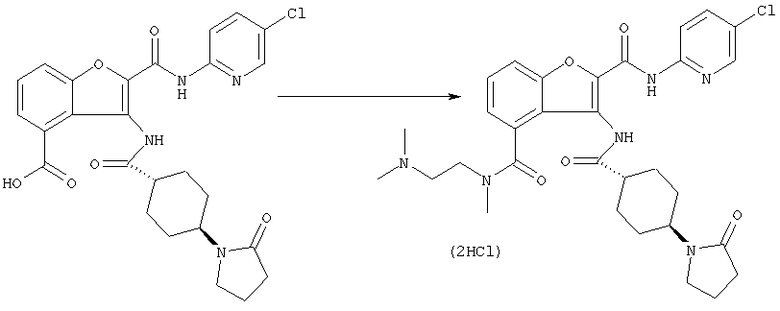
Транс-4-карбокси-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (70 мг), полученный в примере 422, обрабатывают способом, аналогичным описанному в примере 87, что дает транс-4-[N-(2-диметиламиноэтил)-N-метил]аминокарбонил-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (40,7 мг). Этот продукт растворяют в метаноле и обрабатывают 4N хлористым водородом в диоксане (50 мкл), что дает названное соединение (35,7 мг). APCI-MS М/Е: 609/611 [M+H]+.
Пример 425: Транс-4-трет-бутоксикарбониламино-3-[4-(2-оксо-пирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
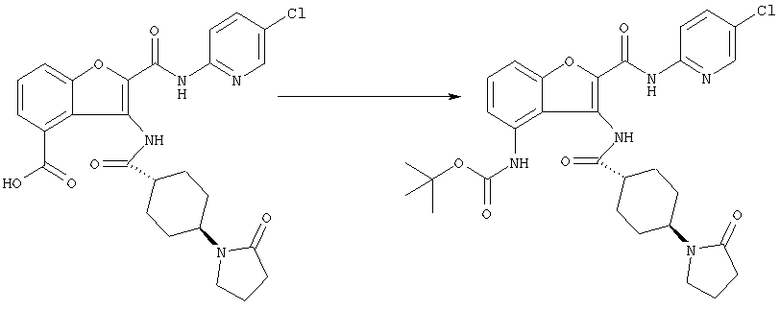
Транс-4-карбокси-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (325 мг), полученный в примере 422, растворяют в трет-бутаноле (8 мл) и добавляют при комнатной температуре триэтиламин (91 мкл) и дифенилфосфорилазид (140 ил) и смесь перемешивают при температуре 60°С в течение 1,5 часов и затем нагревают при температуре кипения с обратным холодильником в течение 5,5 часов. Реакционный раствор разбавляют насыщенным водным раствором гидрокарбоната натрия и экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь хлороформ/метанол =100/1, затем 10/1), что дает названное соединение (141,7 мг). ESI-MS М/Е: 596/598 [M+H]+.
Пример 426: Транс-4-амино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
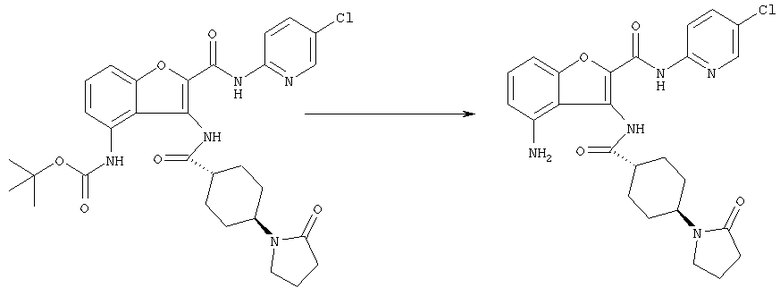
Транс-4-трет-бутоксикарбониламино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (108 мг), полученный в примере 425, растворяют в трифторуксусной кислоте (2 мл) и смесь перемешивают при комнатной температуре в течение 2 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок нейтрализуют насыщенным водным раствором гидрокарбоната натрия и экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =1/1, затем этилацетат), что дает названное соединение (85,4 мг). ESI-MS М/Е: 496/498 [M+H]+.
Пример 427: Транс-4-диметиламино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
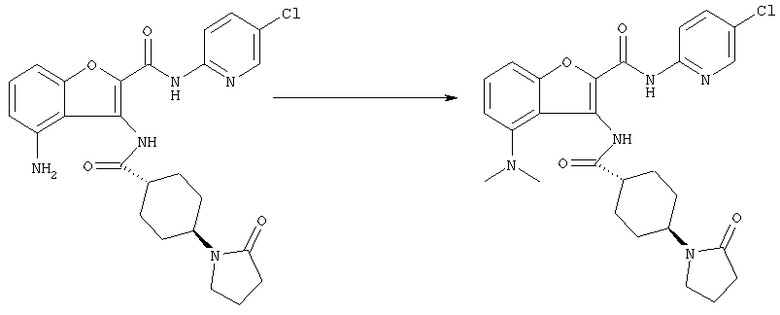
Транс-4-амино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (41,7 мг), полученный в примере 426, обрабатывают способом, аналогичным описанному в примере 198, что дает названное соединение (8,0 мг).
APCI-MS М/Е: 524/526 [M+H]+.
Пример 428: Транс-4-метансульфониламино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
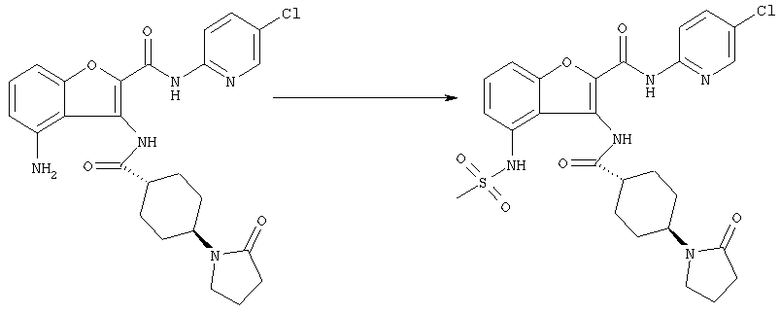
Транс-4-амино-3-[4-(2-оксопирролидин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (27 мг), полученный в примере 426, растворяют в пиридине (2 мл) и добавляют метансульфонилхлорид (7 мкл) при охлаждении льдом. Смесь перемешивают при комнатной температуре в течение ночи и затем вновь добавляют пиридин (3 мл) и метансульфонилхлорид (500 мкл) при охлаждении льдом. Смесь перемешивают при комнатной температуре в течение 6 часов. В реакционный раствор добавляют воду и смесь экстрагируют хлороформом. Растворитель выпаривают при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ, затем хлороформ/метанол =9/1), что дает названное соединение (21,2 мг). APCI-MS М/Е: 574/576 [M+H]+.
Пример 429: Транс-3-[4-(3-оксо-морфолин-4-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
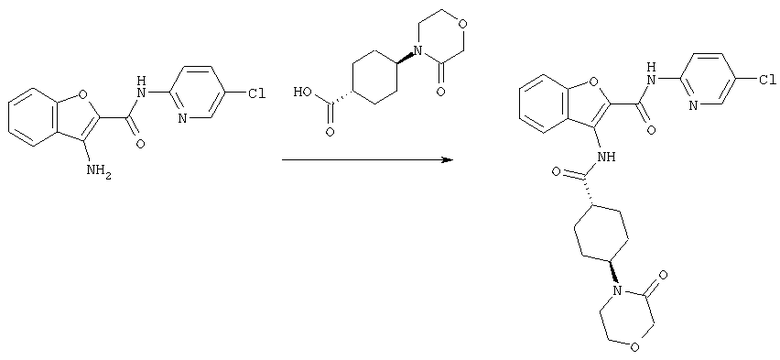
3-Амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (66 мг), полученный в примере приготовления 74, и транс-4-(3-оксо-морфолин-4-ил)циклогексанкарбоновую кислоту (68 мг), полученную в примере приготовления 141, обрабатывают способом, аналогичным описанному в примере 410, что дает названное соединение (74 мг). APCI-MS М/Е: 497/499 [M+H]+.
Пример приготовления 1: Метил 3-формил-4-гидроксибензоат
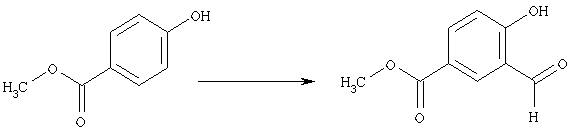
Метил-4-гидроксибензоат (1,52 г) растворяют в трифторуксусной кислоте (20 мл), добавляют гексаметилентетрамин (700 мг) и смесь нагревают при температуре кипения с обратным холодильником в течение 2 часов. Реакционный раствор концентрируют при пониженном давлении, выливают ледяную воду и затем смесь экстрагируют этилацетатом. Органический слой промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении. Полученный осадок растворяют в хлороформе и затем отфильтровывают, чтобы удалить нерастворимые продукты. Фильтрат концентрируют при пониженном давлении и затем очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь н-гексан/этилацетат =4/1), что дает названное соединение (540 мг).
ESI-MS M/E. - 179 [M-Н]-.
Пример приготовления 2: Метил (3-формил-4-гидроксифенил)ацетат
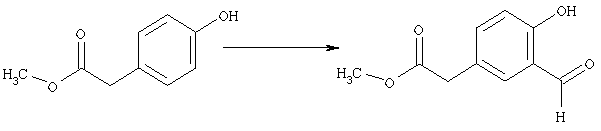
Метил-(4-гидроксифенил)ацетат (1,66 г) растворяют в трифторуксусной кислоте (20 мл), добавляют гексаметилентетрамин (700 мг) и смесь нагревают при температуре кипения с обратным холодильником в течение 2 часов. Реакционный раствор концентрируют при пониженном давлении, выливают ледяную воду и затем смесь экстрагируют этилацетатом. Органический слой промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: н-гексан/этилацетат =9/1, затем =4/1), что дает названное соединение (1,08 г).
ESI-MS М/Е: 193 [M-Н]-.
Примеры приготовления 3-4
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 1 или в примере приготовления 2, что дает последующие соединения.
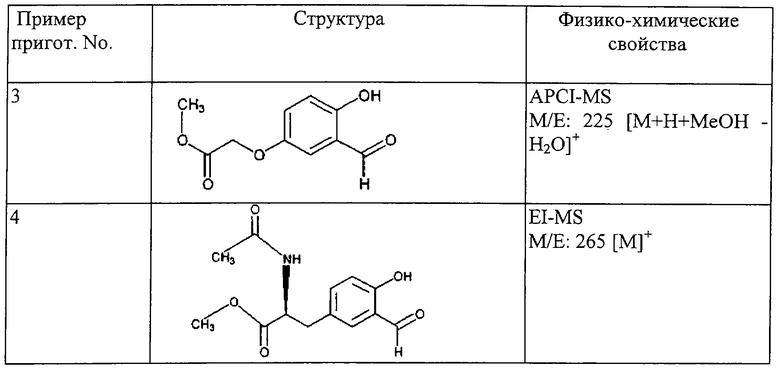
Пример приготовления 5: Метил-3-циано-4-гидроксибензоат
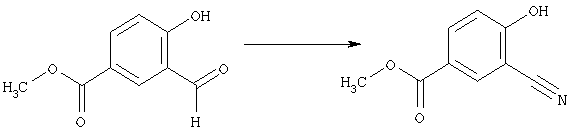
Метил-3-формил-4-гидроксибензоат (28,60 г), полученный в примере приготовления 1, растворяют в муравьиной кислоте (120 мл), добавляют хлорид гидроксиламмония (14,30 г) и смесь нагревают при температуре кипения с обратным холодильником в течение 15 часов. Реакционный раствор концентрируют при пониженном давлении, разбавляют этилацетатом, промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении, что дает названное соединение (24,25 г). ESI-MS М/Е: 176 [M-Н]-.
Пример приготовления 6: Метил(3-циано-4-гидроксифенил)ацетат
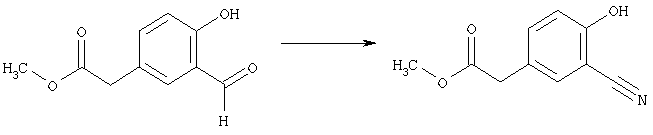
Метил(3-формил-4-гидроксифенил)ацетат (1,05 г), полученный в примере приготовления 2, растворяют в муравьиной кислоте (15 мл) и добавляют хлорид гидроксиламмония (0,49 г) и формиат натрия (0,81 г) и смесь нагревают при температуре кипения с обратным холодильником в течение 8 часов. Реакционный раствор концентрируют при пониженном давлении, разбавляют этилацетатом, промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и растворитель выпаривают при пониженном давлении, что дает названное соединение (520 мг). ESI-MS М/Е: 190 [M-Н]-.
Примеры приготовления 7-19
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 5 или в примере приготовления 6, что дает следующие соединения.
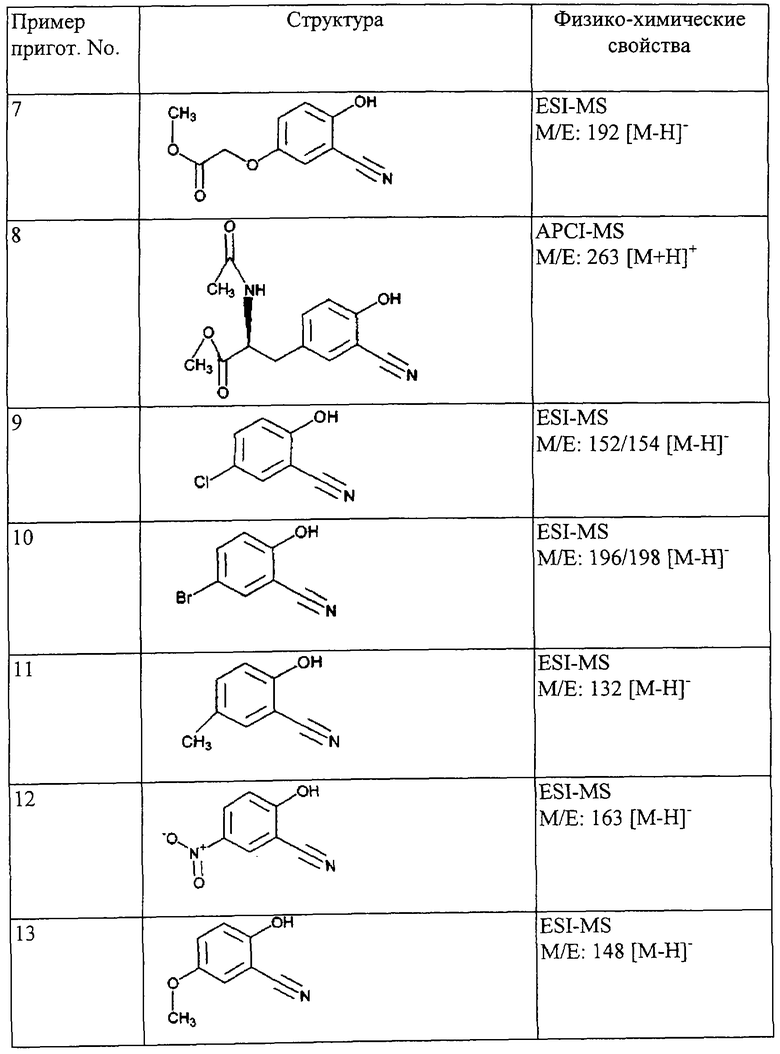
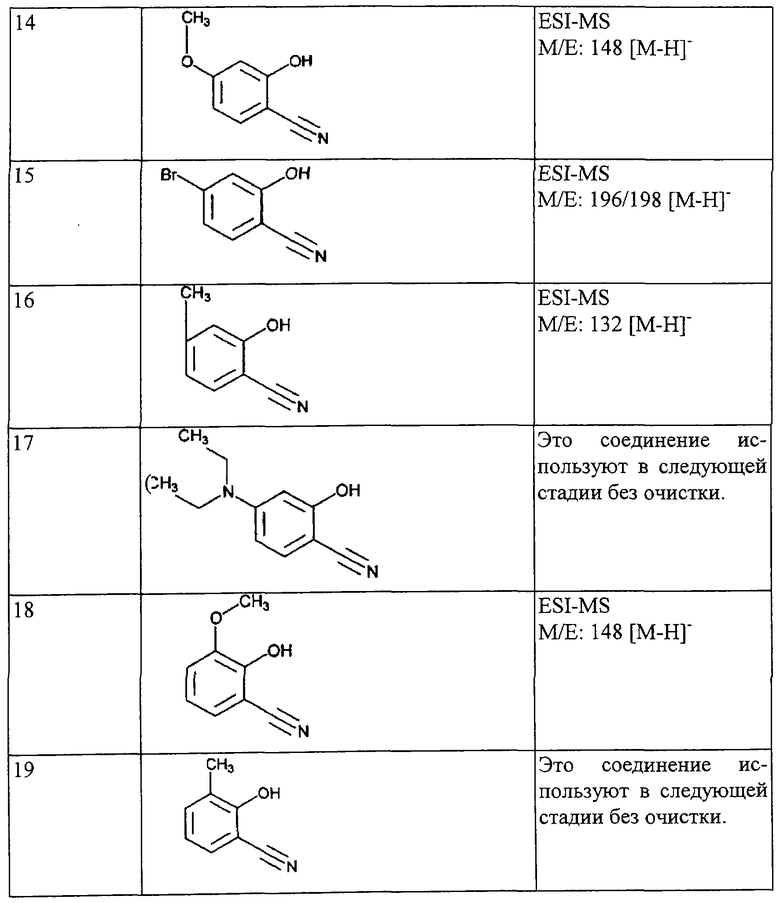
Пример приготовления 20: 2-(4-Метоксикарбонил-2-цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид
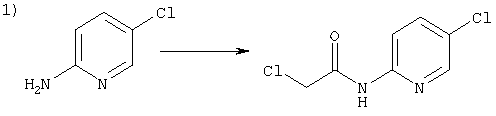
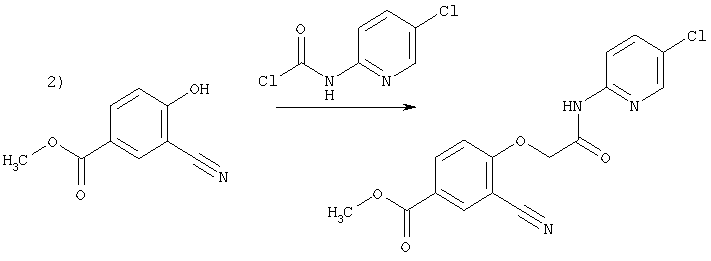
(1) Хлорацетилхлорид (95,5 мл) растворяют в дихлорметане (500 мл) и добавляют по каплям суспензию 2-амино-5-хлорпиридина (128,6 г) и триэтиламин (169 мл) в дихлорметане (1000 мл) при охлаждении льдом и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 0,5 часа. Затем реакционный раствор концентрируют при пониженном давлении, выливают ледяную воду и затем реакционную смесь экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и обрабатывают активированным древесным углем. После фильтрования, чтобы удалить нерастворимые продукты, фильтрат концентрируют при пониженном давлении и полученный осадок суспендируют в диизопропиловом эфире. Осадки собирают фильтрованием, промывают диизопропиловым эфиром и сушат, что дает 2-хлор-N-(5-хлорпиридин-2-ил)ацетамид (153,4 г). APCI-MS М/Е: 205/207 [M+H]+.
(2) Метил-3-циано-4-гидроксибензоат (500 мг), полученный в примере приготовления 5, растворяют в ацетоне (25 мл), добавляют 2-хлор-N-(5-хлорпиридин-2-ил)ацетамид (695 мг), полученный в примере приготовления 20(1), карбонат калия (546 мг) и иодид натрия (550 мг) и смесь нагревают при температуре кипения с обратным холодильником в течение 2 часов. После охлаждения нерастворимые продукты удаляют фильтрованием и нерастворимые продукты промывают ацетоном несколько раз. Фильтрат и промывку объединяют и концентрируют при пониженном давлении и затем очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ, затем хлороформ/этилацетат =4/1). Полученный осадок суспендируют в диэтиловом эфире и затем осадки собирают фильтрованием, что дает названное соединение (660 мг). APCI-MS М/Е: 346/348 [M+H]+.
Пример приготовления 21: 2-[2-Циано-4-(метоксикарбонилметил)фенокси]-N-(5-хлорпиридин-2-ил)ацетамид
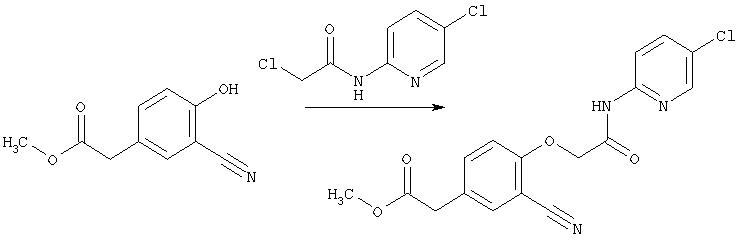
Метил-(3-циано-4-гидроксифенил)ацетат (500 мг), полученный в примере приготовления 6, растворяют в ацетоне (25 мл), добавляют 2-хлор-N-(5-хлорпиридин-2-ил)ацетамид (640 мг), полученный в примере приготовления 20(1), карбонат цезия (1,20 г) и иодид натрия (510 мг) и смесь нагревают при температуре кипения с обратным холодильником в течение 5 часов. После охлаждения нерастворимые продукты удаляют фильтрованием и затем их промывают ацетоном несколько раз. Фильтрат и промывку объединяют, концентрируют при пониженном давлении, в осадок выливают воду и экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь н-гексан/этилацетат/хлороформ =3/1/1). Полученный осадок суспендируют в смеси диэтиловый эфир-н-гексан и затем осадки собирают фильтрованием, что дает названное соединение (570 мг). APCI-MS М/Е: 360/362 [M+H]+.
Примеры приготовления 22-23
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 20 или в примере приготовления 21, что дает следующие соединения.
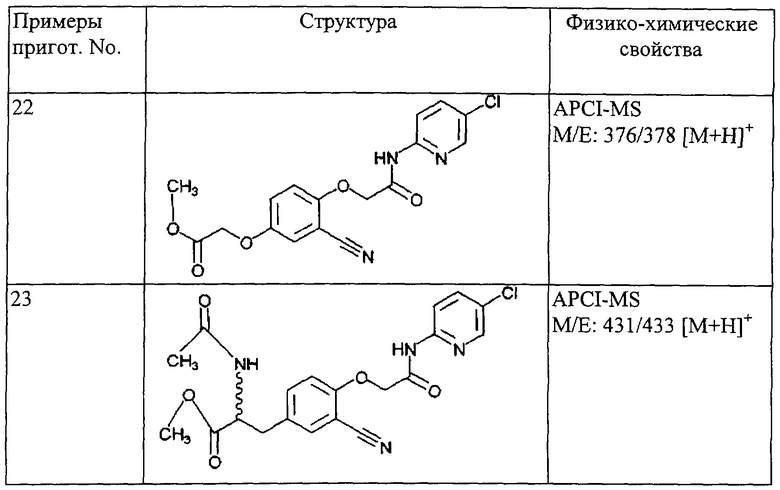
Пример приготовления 24: трет-Бутил(2-цианофенокси)ацетат
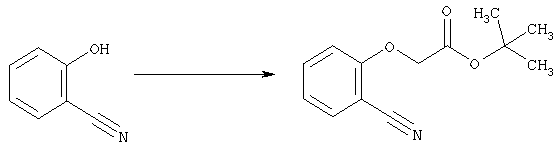
2-Цианофенол (107,1 г) растворяют в ацетоне (1000 мл) и добавляют трет-бутил бромацетат (200,0 г). Потом добавляют карбонат калия (141,6 г), а затем реакционный раствор нагревают при температуре кипения с обратным холодильником в течение 2 часов. После охлаждения нерастворимые продукты удаляют фильтрованием, а затем их промывают ацетоном несколько раз. Фильтрат и промывку объединяют, концентрируют при пониженном давлении и обрабатывают диизопропиловым эфиром азеотропно. Полученный осадок кристаллизуют из смеси н-гексан-диизрпропиловый эфир (5/1) (600 мл) и затем перемешивают при охлаждении льдом. Осадки собирают фильтрованием, промывают несколько раз холодной смесью н-гексан-диизопропиловый эфир (10/1) (600 мл) и сушат, что дает названное соединений (194,5 г). APCI-MS М/Е: 251 [M+NH4]+.
Примеры приготовления 25-36
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 24, что дает следующие соединения.
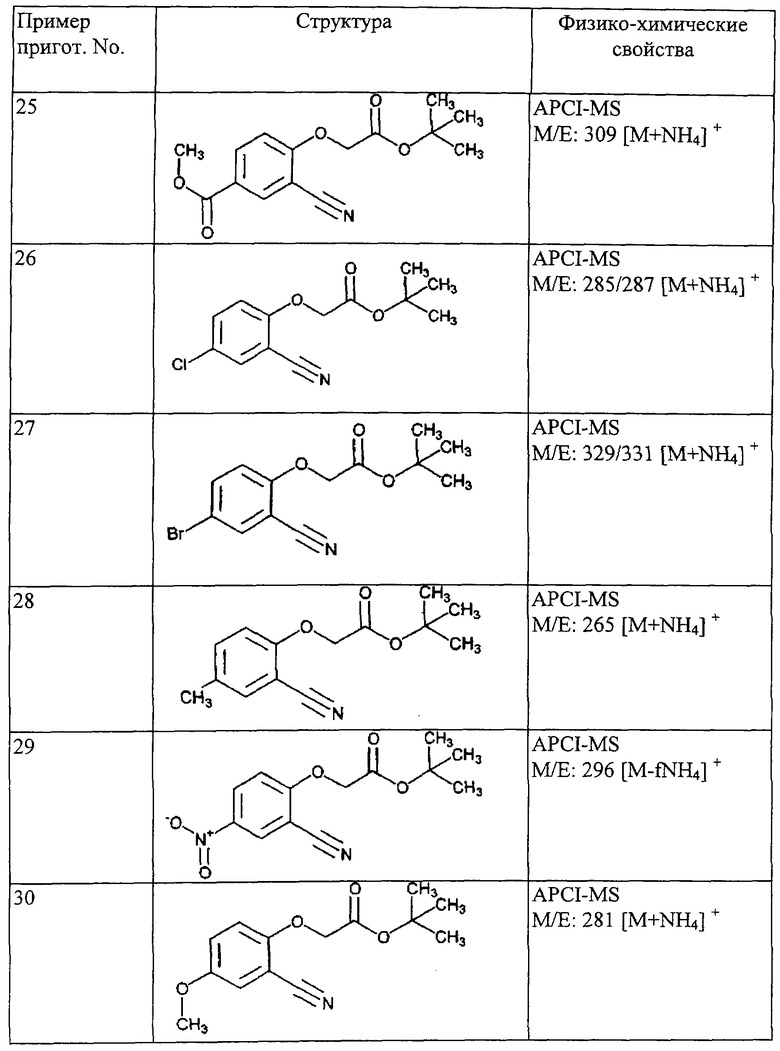
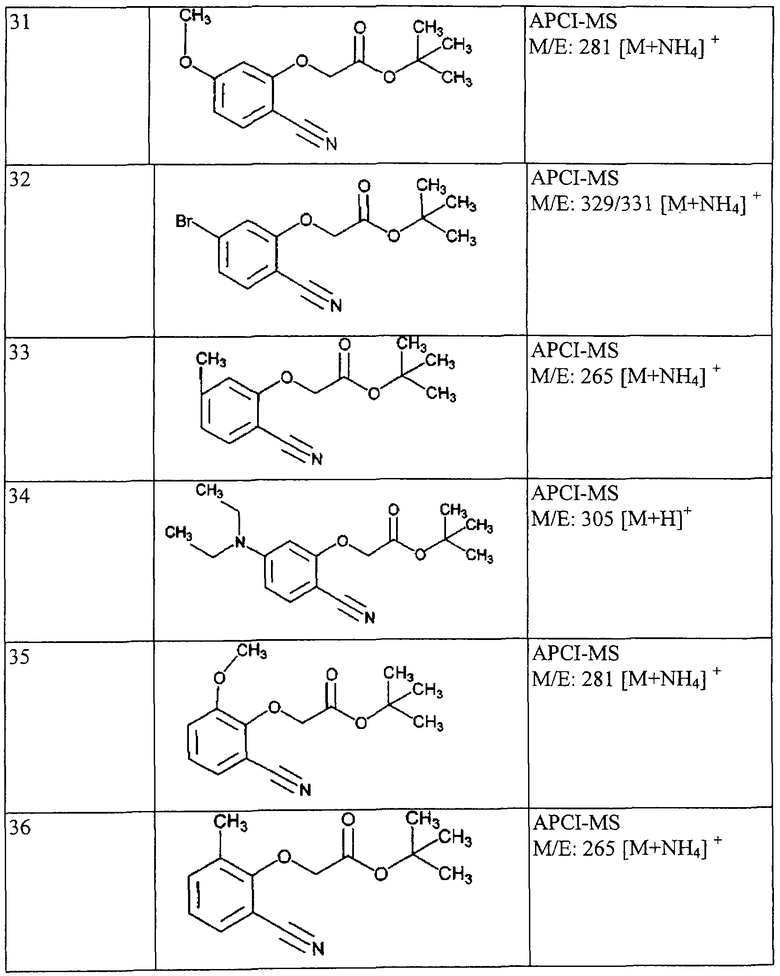
Пример приготовления 37: (2-Цианофенокси)уксусная кислота
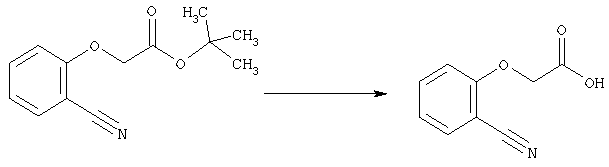
трет-Бутил(2-цианофенокси)ацетат (300,0 г), полученный в примере приготовления 24, растворяют в дихлорметане (400 мл) и добавляют трифторуксусную кислоту (990 мл) и смесь перемешивают при комнатной температуре в течение 4 часов. Реакционный раствор концентрируют при пониженном давлении, полученный осадок суспендируют в диэтиловом эфире (100 мл) и выливают в полученную смесь диизопропиловый эфир (500 мл). Осадки собирают фильтрованием, промывают диизопропиловым эфиром несколько раз и сушат, что дает названное соединение (198,4 г). ESI-MS М/Е: 176 [M-Н]-.
Примеры приготовления 38-49
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 37, что дает следующие соединения.
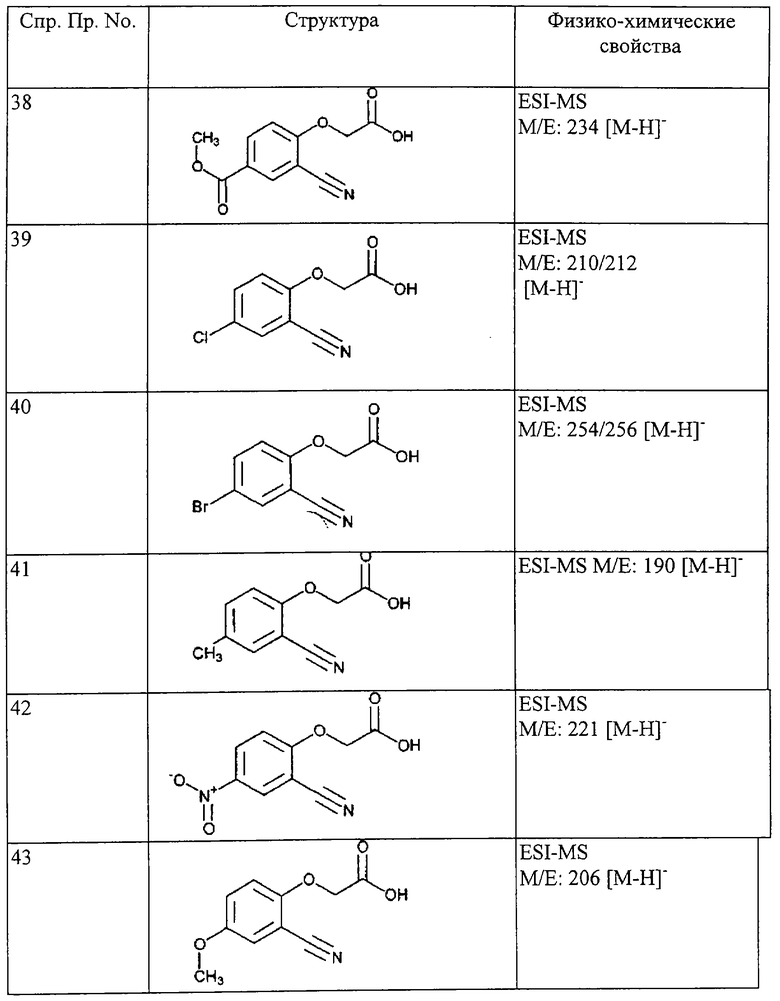
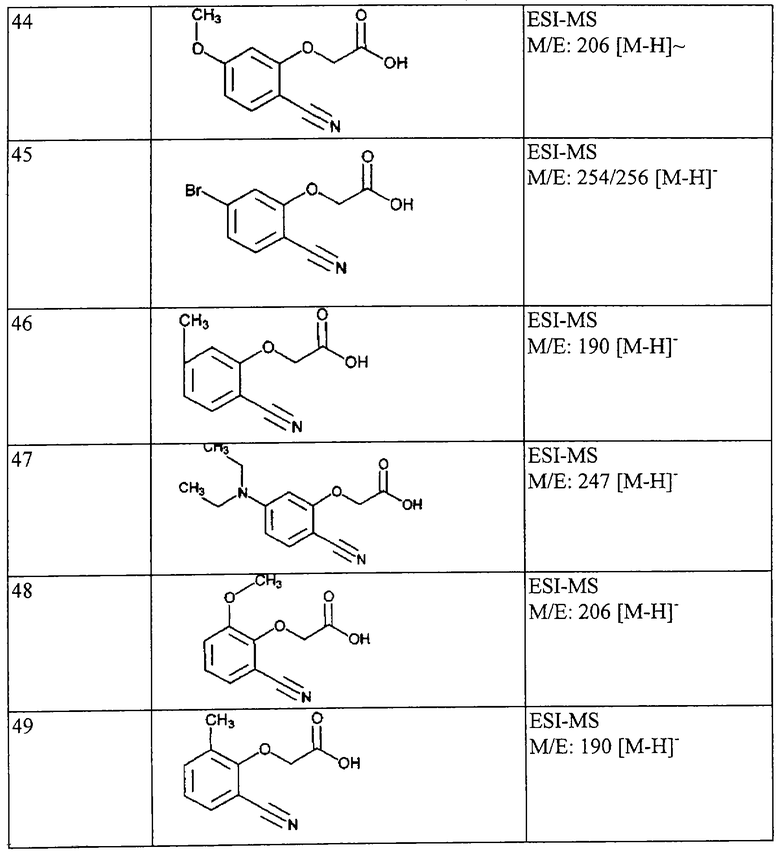
Пример приготовления 50: [4-(N-Бензилоксикарбонил-N-метиламино)-2-цианофенокси]уксусная кислота
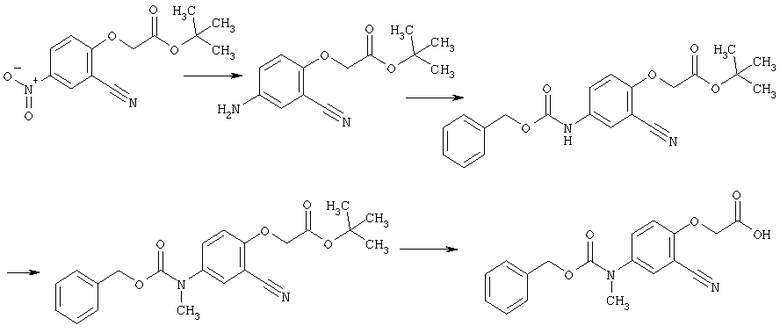
(1) трет-Бутил-2-(4-нитро-2-цианофенокси)ацетат (500 мг), полученный в примере приготовления 29, растворяют в тетрагидрофуране (20 мл), добавляют 10% палладий на угле (100 мг) и смесь перемешивают в течение 2 часов под давлением атмосферы водорода. Нерастворимые продукты удаляют фильтрованием и затем фильтрат концентрируют при пониженном давлении, что дает трет-бутил(4-амино-2-цианофенокси)ацетат (440 мг). APCI-MS М/Е: 249 [M+H]+.
(2) трет-Бутил(4-амино-2-цианофенокси)ацетат (430 мг), полученный в примере приготовления 50(1), растворяют в тетрагидрофуране (10 мл), добавляют насыщенный раствор гидрокарбоната натрия (10 мл) и затем добавляют бензилхлороформиат (355 мг) при охлаждении льдом. Далее при охлаждении льдом реакционный раствор перемешивают в течение часа и экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия, выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: н-гексан/этилацетат =9/1, затем 3/1), что дает трет-бутил(4-бензилоксикарбониламино-2-цианофенокси)ацетат (540 мг). APCI-MS M/E: 383 [M+H]+.
(3) трет-Бутил(4-бензилоксикарбониламино-2-цианофенокси)ацетат (100 мг), полученный в примере приготовления 50(2), растворяют в N,N-диметилформамиде (3 мл) и добавляют 60% маслянистый гидрид натрия (12,5 мг). Затем смесь перемешивают в течение 20 минут при комнатной температуре, добавляют по каплям йодистый метил (24,4 мкл) и затем смесь перемешивают в течение часа. В реакционный раствор выливают насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь н-гексан/этилацетат =9/1, затем 3/1), что дает трет-бутил[4-(N-бензилоксикарбонил-N-метиламино)-2-цианофенокси]ацетат (91 мг). APCI-MS М/Е: 414 [M+NH4]+.
(4) трет-Бутил[4-(N-бензилоксикарбонил-N-метиламино)-2-цианофенокси]ацетат (2,42 г), полученный в примере приготовления 50(3), обрабатывают способом, аналогичным описанному в примере приготовления 37, что дает названное соединение (2,06 г). ESI-MS М/Е: 339 [M-Н]-.
Пример приготовления 51: (2-Цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид
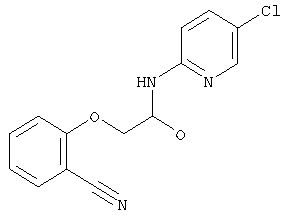
(2-Цианофенокси)уксусную кислоту (48,63 г), полученную в примере приготовления 37, растворяют в дихлорметане (1000 мл), добавляют оксалилхлорид (26,34 мл) и N,N-диметилформамид (10 капель) и смесь перемешивают при комнатной температуре в течение 3,5 часов. Реакционный раствор охлаждают на бане со льдом, добавляют 2-амино-5-хлорпиридин (32,08 г) и затем добавляют пиридин (60,54 мл). Через 5 минут реакционный раствор нагревают до комнатной температуры и перемешивают в течение ночи. В реакционный раствор добавляют ледяную воду и значение рН раствора доводят до 4 с помощью 10% раствора соляной кислоты и затем экстрагируют хлороформом. Органический слой промывают последовательно водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель. Полученный осадок суспендируют в смеси хлороформ-этилацетат и собирают фильтрованием, что дает (2-цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид (51,58 г). Затем фильтрат концентрируют при пониженном давлении и затем очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ), что дает названное соединение (11,50 г). APCI-MS М/Е: 288/290 [M+H]+.
Примеры приготовления 52-66
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 51, что дает следующие соединения.
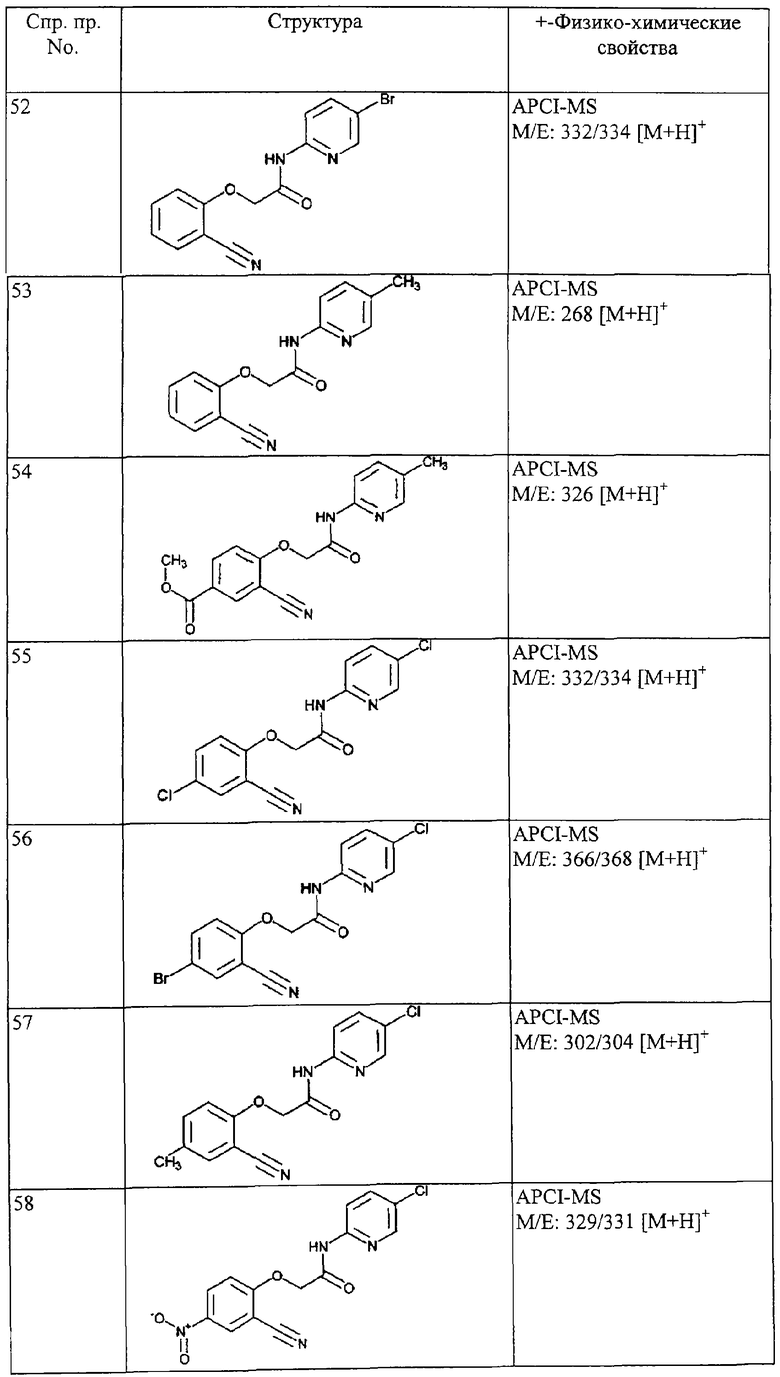
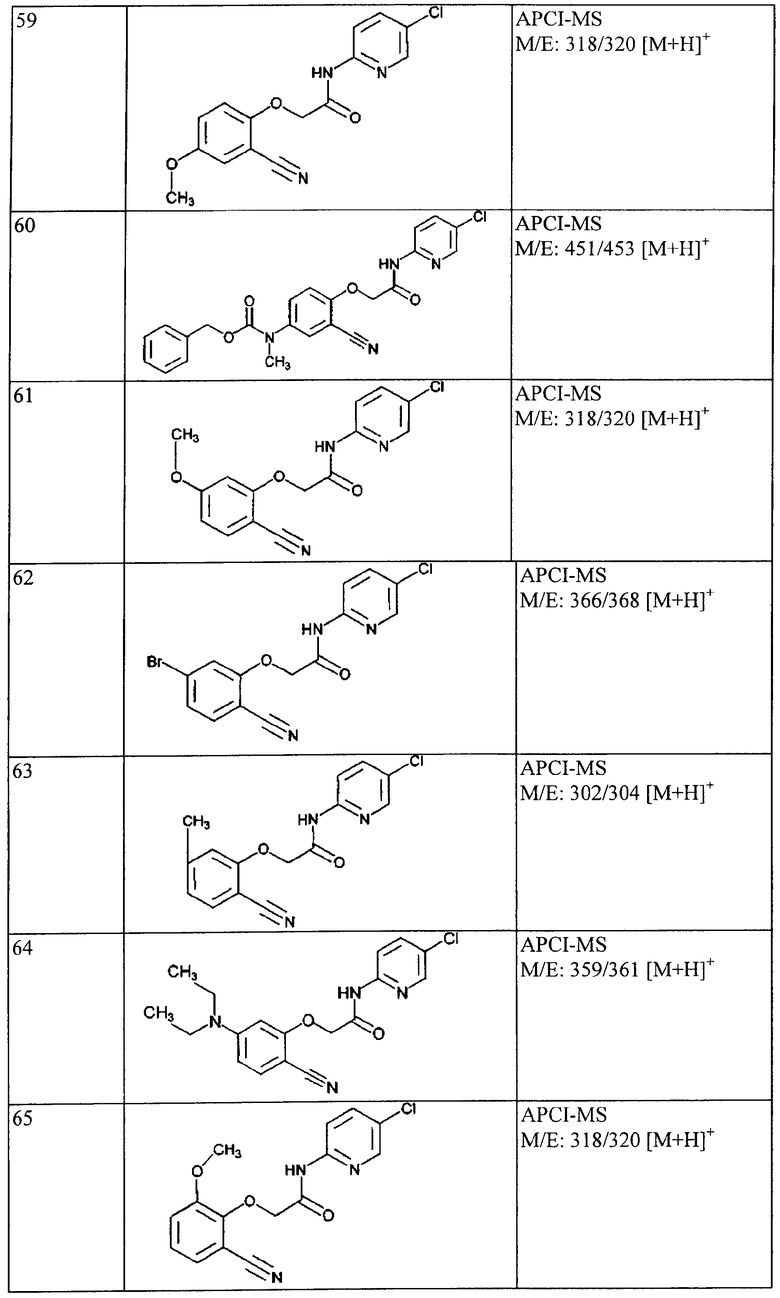
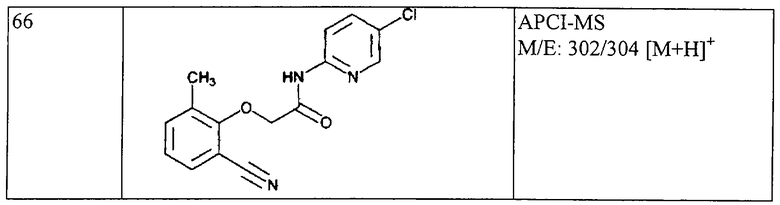
Пример приготовления 67: (2-Цианофенокси)-N-(4-хлорфенил)ацетамид
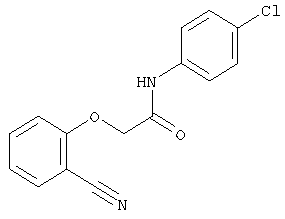
(2-Цианофенокси)уксусную кислоту (30,00 г), полученную в примере приготовления 37, растворяют в N,N-диметилформамиде (300 мл), последовательно добавляют 4-хлоранилин (25,9 г), 4-диметиламинопиридин (22,7 г) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (35,6 г) и смесь перемешивают в течение 3 часов при комнатной температуре. Реакционный раствор концентрируют при пониженном давлении и полученный осадок разбавляют смесью этилацетат-тетрагидрофуран, промывают последовательно водой, 5% раствором соляной кислоты, водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель. Полученный осадок суспендируют в диизопропиловом эфире и затем осадки собирают фильтрованием, что дает названное соединение (44,00 г). APCI-MS М/Е: 287/289 [M+H]+.
Примеры приготовления 68-71
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 67, что дает следующие соединения.
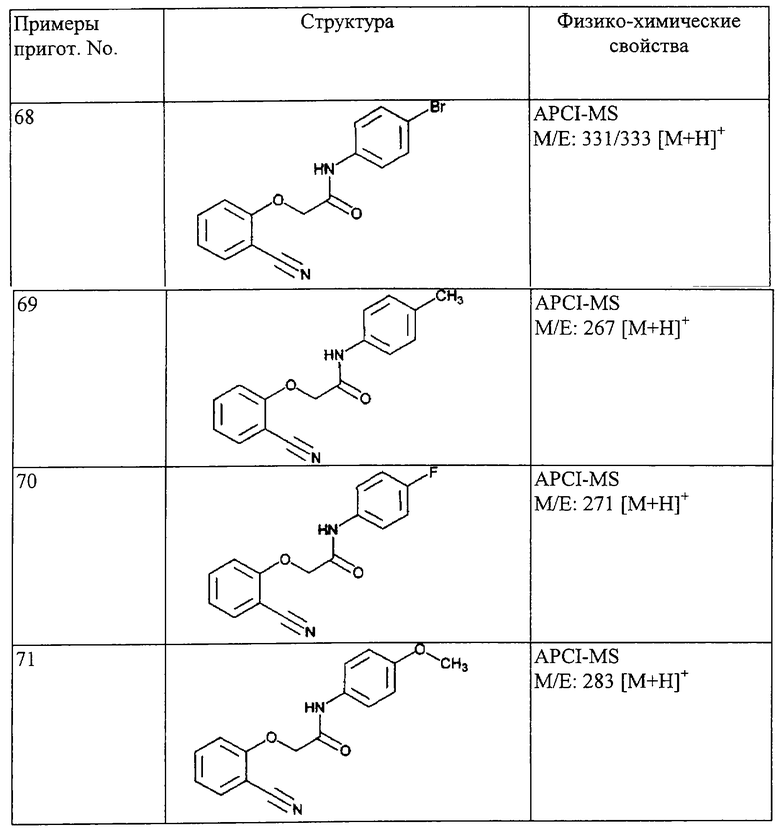
Пример приготовления 72: 3-Амино-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида
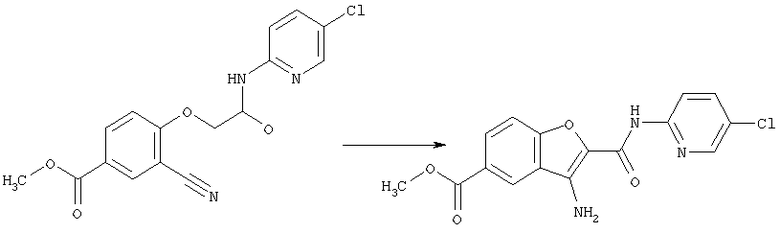
2-(4-Метоксикарбонил-2-цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид (1,73 г), полученный в примере приготовления 20, растворяют в N,N-диметилацетамиде (15 мл), добавляют карбонат натрия (160 мг) и смесь перемешивают при температуре 100°С в течение 2 часов. После охлаждения в реакционный раствор выливают ледяную воду и полученные осадки собирают фильтрованием, промывают последовательно водой, тетрагидрофураном и диэтиловым эфиром и сушат, что дает названное соединение (1,20 г). APCI-MS М/Е: 346/348 [M+H]+.
Пример приготовления 73: 3-Амино-5-метоксикарбонилметил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида
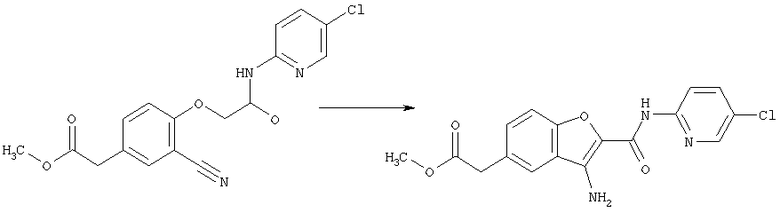
2-[2-Циано-4-(метоксикарбонилметил)фенокси]-N-(5-хлорпиридин-2-ил)ацетамид (500 мг), полученный в примере приготовления 21, растворяют в N,N-диметилацетамиде (15 мл), добавляют карбонат натрия (74 мг) и смесь перемешивают при температуре 100°С в течение 16 часов. После охлаждения в реакционный раствор выливают ледяную воду и экстрагируют этилацетатом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: н-гексан/этилацетат/хлороформ =3/1/1), суспендируют в диэтиловом эфир-н-гексане и затем осадки собирают фильтрованием, что дает названное соединение (180 мг). APCI-MS М/Е: 360/362 [МН-Н]+.
Пример приготовления 74: 3-Амино-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
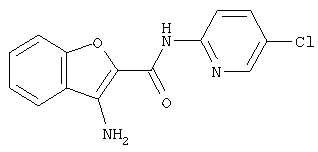
(2-Цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид (150,00 г), полученный в примере приготовления 51, растворяют в N,N-диметилацетамиде (1500 мл), добавляют карбонат натрия (60,8 г) и смесь перемешивают при температуре 70°С в течение 7 часов. После охлаждения реакционный раствор выливают в ледяную воду и полученные осадки собирают фильтрованием и промывают несколько раз водой. Осадки растворяют в этилацетате, промывают водой и насыщенным рассолом, сушат над сульфатом натрия и органический слой обрабатывают активированным древесным углем. Нерастворимые продукты отфильтровывают и затем фильтрат концентрируют при пониженном давлении и полученный осадок суспендируют в смеси диэтиловый эфир-этилацетат. Осадки собирают фильтрованием, промывают диэтиловым эфиром и сушат, что дает названное соединение (119,33 г).
APCI-MS М/Е: 288/290 [M+H]+.
Пример приготовления 75-96
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 72, 73 или 74, что дает следующие соединения.
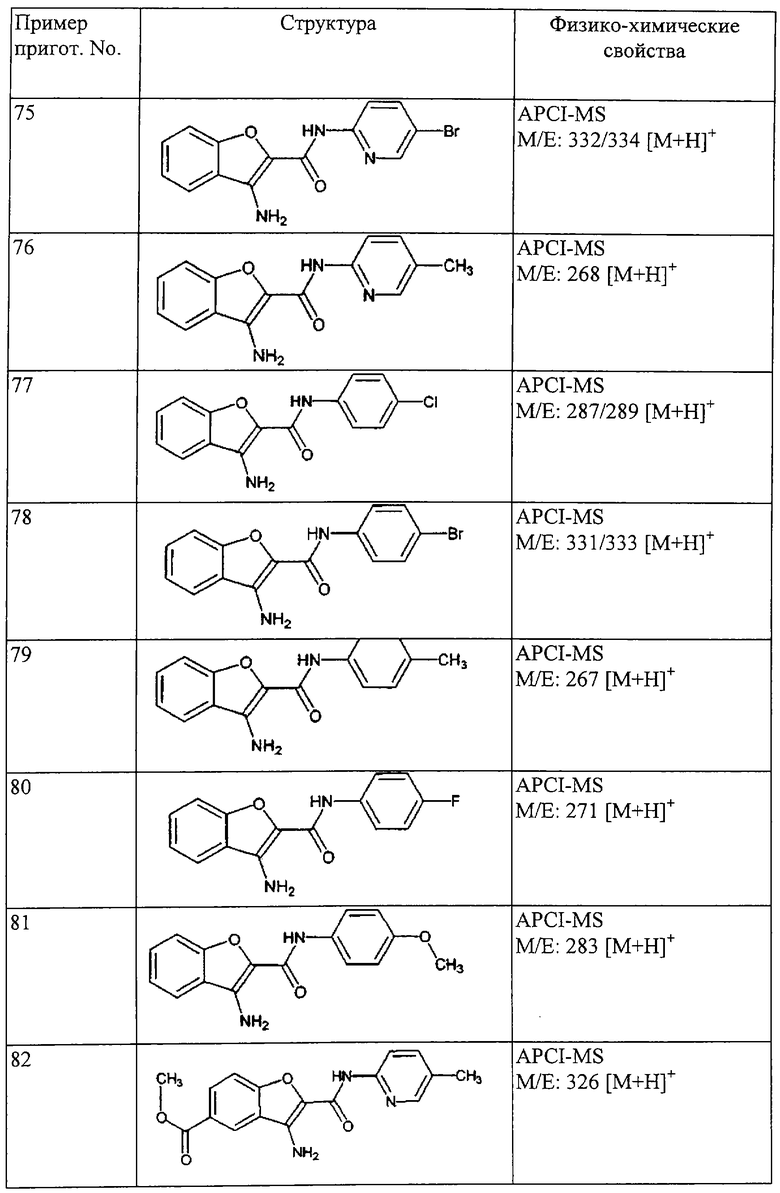
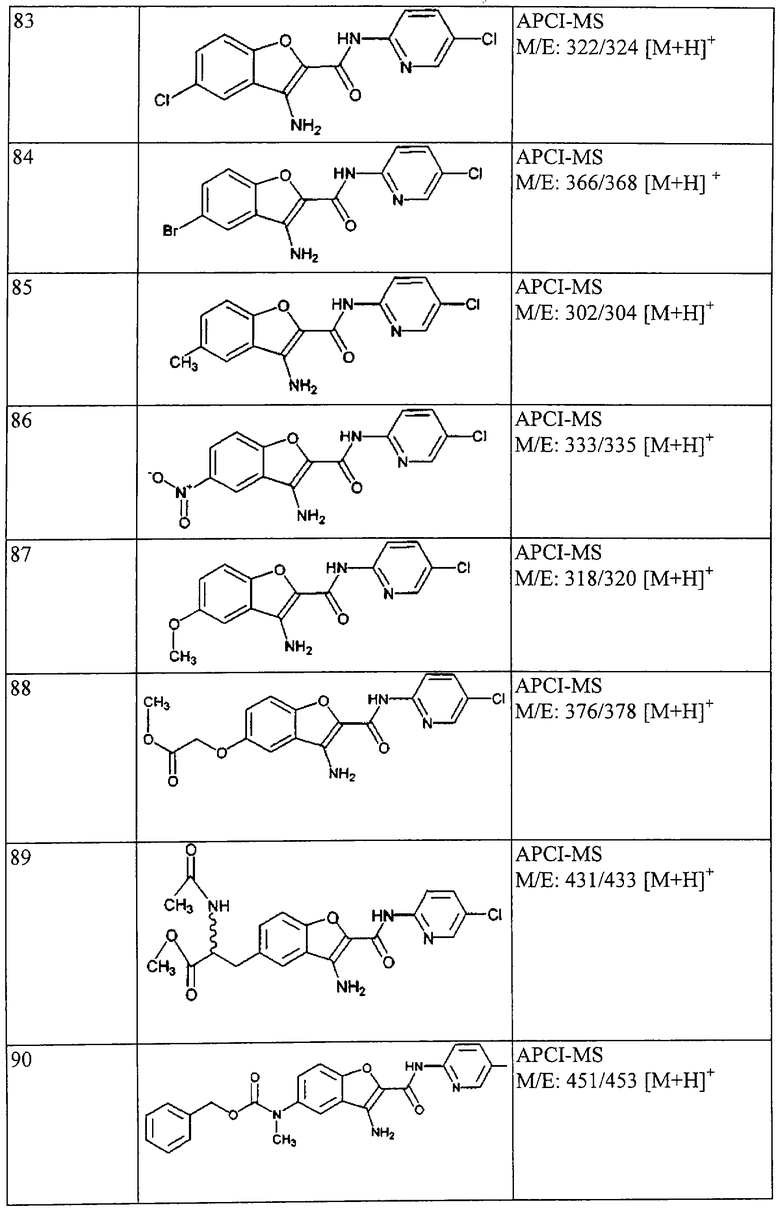
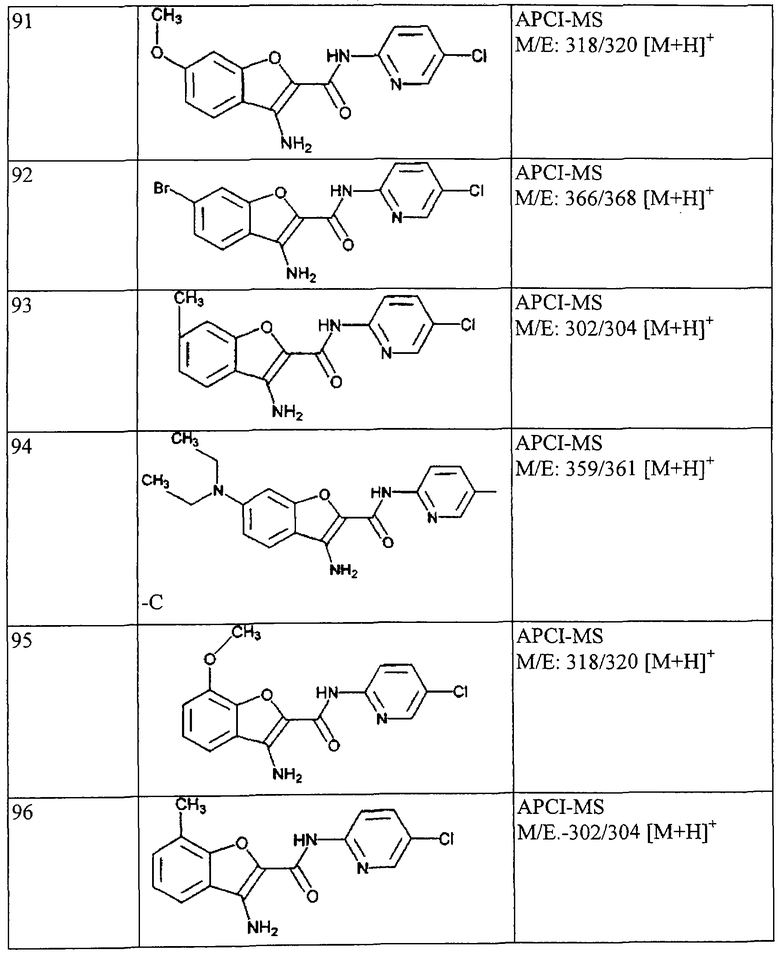
Пример приготовления 97: (2-Циано-4-гидроксифенокси)-N-(5-хлорпиридин-2-ил)-ацетамид
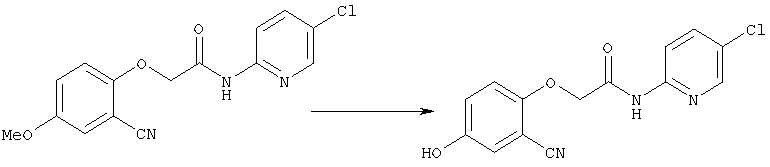
В суспензию (2-циано-4-метоксифенокси)-N-(5-хлорпиридин-2-ил)ацетамида (40,0 г), полученную в примере приготовления 59, в дихлорметане (2000 мл) добавляют по каплям при температуре -58°С в течение 40 минут трибромид бора (173 г). Реакционный раствор перемешивают в течение 26 часов с поддержанием внутренней температуры между -20°С и 0°С и затем выливают в ледяную воду. Осажденное твердое вещество собирают фильтрованием, промывают водой и затем сушат при пониженном давлении. Часть из полученного твердого вещества (37,2 г), то есть 24,3 г, очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ/метанол =50/1-10/1), что дает названное соединение (17,0 г). APCI-MS М/Е: 304/306 [M+H]+.
Пример приготовления 98: 3-Амино-5-гидрокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
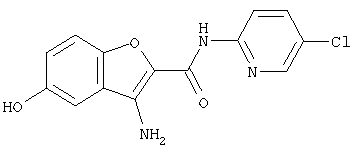
(2-Циано-4-гидроксифенокси)-N-(5-хлорпиридин-2-ил)ацетамид (321 мг), полученный в примере приготовления 97, обрабатывают способом, аналогичным описанному в примере приготовления 73, что дает названное соединение (274 мг). APCI-MS М/Е: 304/306 [M+H]+.
Пример приготовления 99: (4-трет-Бутоксикарбонилметокси-2-цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид
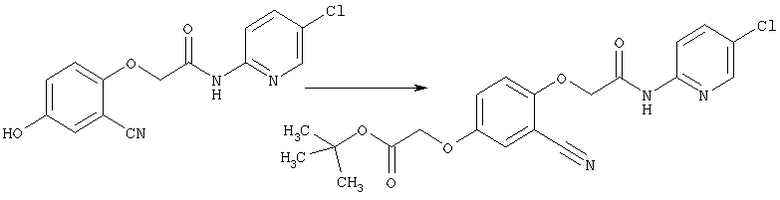
(2-Циано-4-гидроксифенокси)-N-(5-хлорпиридин-2-ил)ацетамид (5,75 г), полученный в примере приготовления 97, растворяют в ацетоне (160 мл) и в раствор добавляют карбонат цезия (8,08 г), трет-бутилбромацетат (4,58 г) и иодид натрия (3,64 г). Реакционный раствор нагревают при температуре кипения с обратным холодильником в течение 8 часов, добавляют еще порцию карбоната цезия (1,89 г), трет-бутилбромацетата (840 мкл) и иодида натрия (875 мг) и смесь нагревают при температуре кипения с обратным холодильником в течение дополнительных 14 часов. После охлаждения реакционный раствор выливают в ледяную воду, доводят значение рН до величины 1-2 с помощью 10% раствора соляной кислоты и экстрагируют этилацетатом. Органический слой сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: гексан/этилацетат =3/1, 2/1, затем 1/1) и затем очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: гексан/этилацетат =2/1, затем 1/1), что дает названное соединение (4,02 г). APCI-MS М/Е: 418/420 [M+H]+.
Пример приготовления 100: 3-Амино-5-трет-бутоксикарбонилметокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
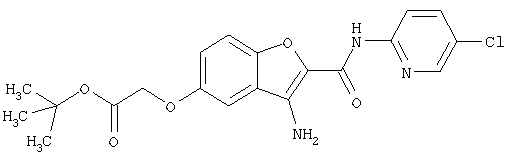
(4-трет-Бутоксикарбонилметокси-2-цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид (8,18 г), полученный в примере приготовления 99, обрабатывают способом, аналогичным описанному в примере приготовления 73, что дает названное соединение (5,72 г). APCI-MS М/Е: 418/420 [M+H]+.
Пример приготовления 101: 3-Амино-5-(2-метоксиэтокси)-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамид
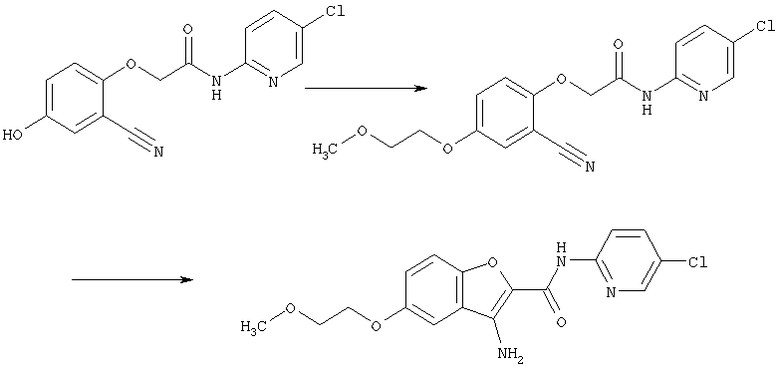
(1) (2-Циано-4-гидроксифенокси)-N-(5-хлорпиридин-2-ил)ацетамид (100 мг), полученный в примере приготовления 97, растворяют в тетрагидрофуране и добавляют 2-метоксиэтанол (9,30 мл) и трифенилфосфин (31,0 г), а затем добавляют по каплям при охлаждении льдом диэтилазодикарбоксилат (22,2 мл). Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 17 часов и концентрируют при пониженном давлении. В полученный осадок выливают диизопропиловый эфир и нерастворимые продукты удаляют фильтрованием и затем фильтрат концентрируют при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ/этилацетат =10/1), что дает [4-(2-метоксиэтокси)-2-цианофенокси]-N-(5-хлорпиридин-2-ил)ацетамид (71,48 г) в виде сырого продукта, который используют на следующей стадии без дальнейшей очистки. APCI-MS М/Е: 362/364 [M+H]+.
(2) Сырой продукт, содержащий [4-(2-метоксиэтокси)-2-цианофенокси]-N-(5-хлорпиридин-2-ил)ацетамид (71,48 г), полученный в примере приготовления 101(1), обрабатывают способом, аналогичным описанному в примере приготовления 72, что дает названное соединение (24,40 г). APCI-MS М/Е: 362/364 [M+H]+.
Примеры приготовления 102-106
(2-Циано-4-гидроксифенокси)-N-(5-хлорпиридин-2-ил)ацетамид, полученный в примере приготовления 97, и соответствующий спирт обрабатывают способом, аналогичным описанному в примере приготовления 101, что дает следующие соединения.
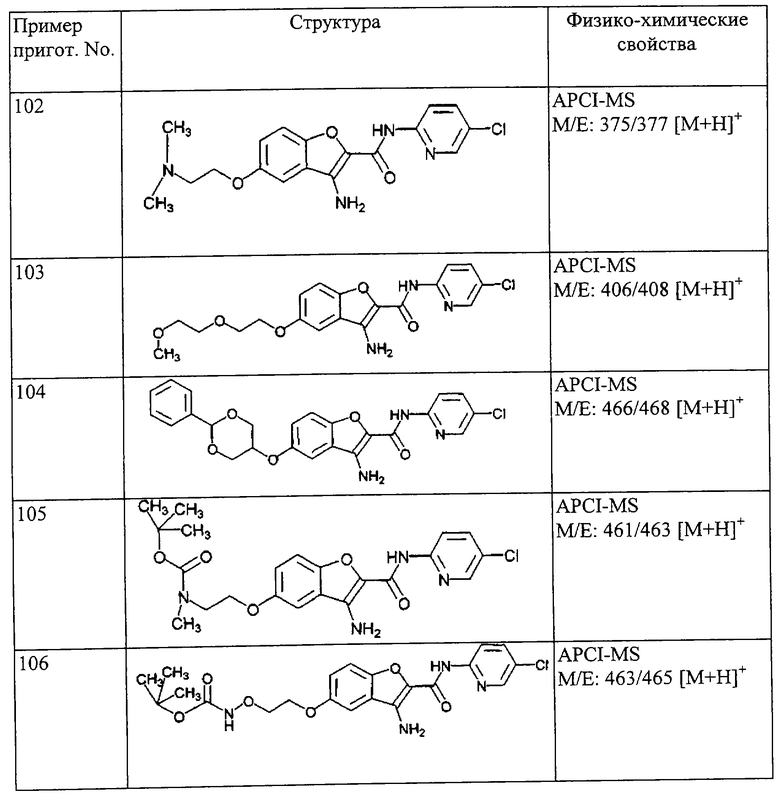
Пример приготовления 107: (2,4-Дицианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид
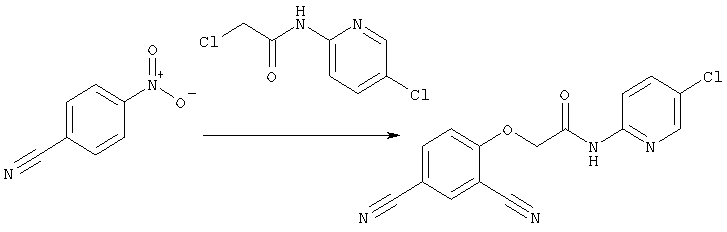
4-Нитробензонитрил (3,02 г) и цианид калия (2,02 г) растворяют в диметилсульфоксиде (100 мл) и перемешивают при температуре 100°С в течение часа. Реакционному раствору дают возможность остыть до комнатной температуры и в него добавляют карбонат калия (1,49 г), 2-хлор-N-(5-хлорпиридин-2-ил)ацетамид (10,42 г), полученный в примере приготовления 20(1), и иодид натрия (8,76 г) и смесь перемешивают при температуре 60°С в течение 4,5 часов. Реакционный раствор выливают в воду и выпавшие в осадок твердые вещества собирают фильтрованием, промывают водой и сушат на воздухе. Полученное твердое вещество растворяют в этилацетате, сушат над сульфатом натрия, выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: гексан/этилацетат =5/1 до 1/1) и затем полученный осадок суспендируют в смеси этилацетат-диизопропиловый эфир. Осадки собирают фильтрованием и сушат, что дает названное соединение (2,81 г). APCI-MS М/Е: 313/315 [M+H]+.
Пример приготовления 108: 3-Амино-5-циано-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
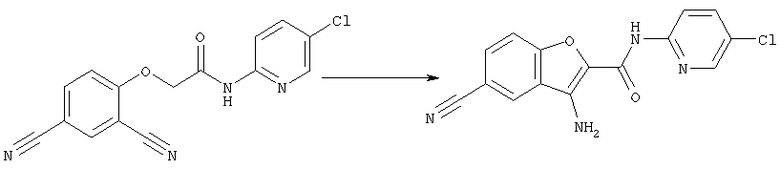
(2,4-Дицианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид (1,02 г), полученный в примере приготовления 107, обрабатывают способом, аналогичным описанному в примере приготовления 73, что дает названное соединение (0,96 г).
APCI-MS М/Е: 313/315 [M+H]+.
Пример приготовления 109: (3-Хлор-2-цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид
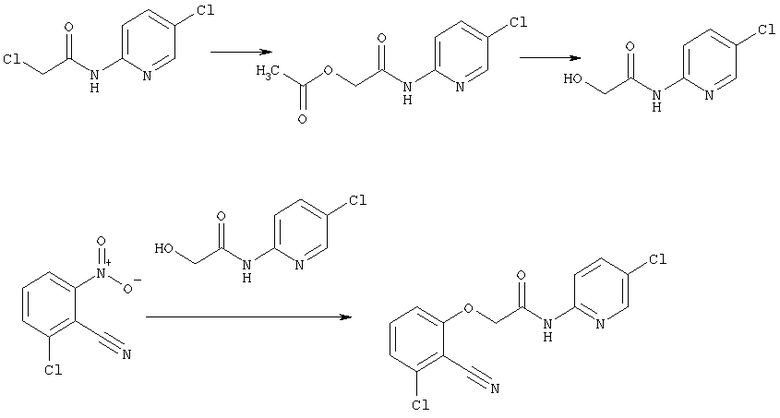
(1) 2-Хлор-N-(5-хлорпиридин-2-ил)ацетамид (30,68 г), полученный в примере приготовления 20(1), растворяют в N,N-диметилформамиде (500 мл), добавляют ацетат натрия (24,55 г) и смесь перемешивают при температуре 60°С в течение 5 часов. Реакционный раствор разбавляют этилацетатом, промывают последовательно водой и насыщенным рассолом. Раствор сушат над сульфатом магния, обрабатывают активированным древесным углем и фильтрат концентрируют при пониженном давлении. Полученный осадок суспендируют в н-гексане и полученные кристаллы собирают фильтрованием, промывают н-гексаном и сушат, что дает N-(5-хлорпиридин-2-ил)-2-ацетоксиацетамид (30,58 г). APCI-MS М/Е: 229/231 [M+H]+.
(2) 2-Ацетокси-N-(5-хлорпиридин-2-ил)ацетамид (30,36 г), полученный в примере приготовления 109(1), суспендируют в метаноле (1200 мл) и добавляют карбонат калия (22,0 г) при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 0,5 часа и концентрируют при пониженном давлении. В полученный осадок выливают этилацетат (1500 мл) и ледяную воду (1000 мл) и затем смесь экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в небольшое количество этилацетата, добавляют диизопропиловый эфир и выпавшее в осадок кристаллы собирают фильтрованием, промывают диизопропиловым эфиром и сушат, что дает 2-гидрокси-N-(5-хлорпиридин-2-ил)ацетамид (22,85 г). APCI-MS М/Е: 187/189 [M+H]+.
(3) 2-Хлор-6-нитробензонитрил (187 мг) и 2-гидрокси-N-(5-хлорпиридин-2-ил)ацетамид (183 мг), полученный в примере приготовления 109(2), растворяют в N,N-диметилформамиде (2 мл) и добавляют 60% маслянистый гидрид натрия (80 мг) при охлаждении льдом. После перемешивания в течение 6 часов с охлаждением, в реакционный раствор выливают насыщенный водный раствор хлорида аммония и экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в н-гексан-диизопропиловый эфир, полученный продукт собирают фильтрованием и сушат, что дает названное соединение (286 мг). APCI-MS М/Е: 322/324 [M+H]+.
Пример приготовления 110: 3-Амино-4-хлор-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
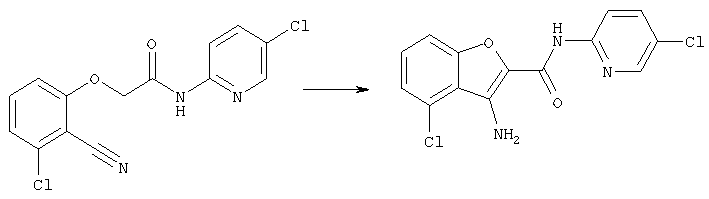
(3-Хлор-2-цианофенокси)-N-(5-хлорпиридин-2-ил)ацетамид (274 мг), полученный в примере приготовления 109, растворяют в N,N-диметилацетамиде (10 мл), добавляют карбонат цезия (333 мг) и смесь перемешивают при температуре 100°С в течение 8 часов. После охлаждения в реакционный раствор добавляют ледяную воду, осадки собирают фильтрованием и промывают водой. Осадки растворяют в горячем этилацетате, промывают насыщенным рассолом и сушат над сульфатом натрия. В органический слой добавляют активированный древесный угль и NH-силикагель (5 г) и смесь отфильтровывают, чтобы удалить нерастворимые продукты. Фильтрат концентрируют при пониженном давлении, полученный осадок суспендируют в смеси этилацетат-диэтиловый эфир и полученный продукт собирают фильтрованием, что дает названное соединение (112 мг). APCI-MS М/Е: 322/324 [M+H]+.
Пример приготовления 111: 3-Амино-4-метокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
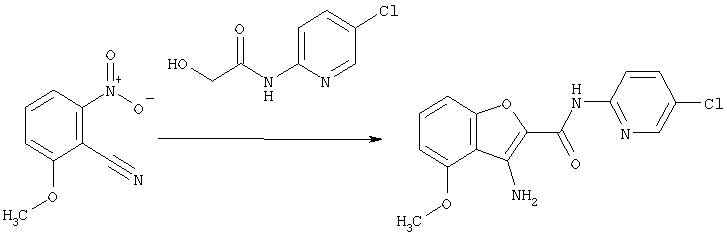
2-Метокси-6-нитробензонитрил (589 мг) и 2-гидрокси-N-(5-хлорпиридин-2-ил)ацетамид (560 мг), полученный в примере приготовления 109(2), растворяют в N,N-диметилацетамиде (10 мл) и добавляют карбонат калия (810 мг). Реакционный раствор перемешивают при температуре 60°С в течение ночи, добавляют еще порцию карбоната калия (810 мг) и смесь перемешивают при температуре 100°С в течение 4 часов. После охлаждения в реакционный раствор выливают ледяную воду и экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и обрабатывают активированным древесным углем. Нерастворимые продукты удаляют фильтрованием, промывают смесью хлороформ-метанол и фильтрат и промывку объединяют и концентрируют при пониженном давлении. Полученный осадок суспендируют в диизопропиловый эфир, а затем полученный продукт собирают фильтрованием, что дает названное соединение (104 мг). APCI-MS М/Е: 317/319 [M+H]+.
Пример приготовления 112: Метил-транс-4-(трет-бутоксикарбониламино)циклогексан-карбоксилат
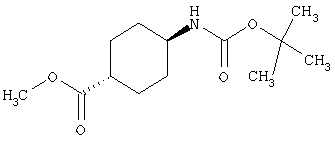
(1) Тионилхлорид (254 мл) добавляют по каплям в метанол (1500 мл) при охлаждении до температуры -30°С в течение около часа. После добавления реакционную смесь перемешивают при комнатной температуре в течение 0,5 часа, добавляют транс-циклогексан-1,4-дикарбоновую кислоту (500,0 г) и смесь перемешивают при комнатной температуре в течение 17 часов. Реакционный раствор концентрируют при пониженном давлении, осадок разбавляют хлороформом и затем промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом. Органический слой сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок кристаллизуют из н-гексана, полученный продукт собирают фильтрованием, сушат, что дает диметил транс-циклогексан-1,4-дикарбоксилат (545,0 г). APCI-MS М/Е: 201 [M+H]+.
(2) Диметил-транс-циклогексан-1,4-дикарбоксилат (150,0 г), полученный в примере приготовления 112(1), растворяют в тетрагидрофуране (1500 мл) и в раствор добавляют по каплям смесь 28% метоксида натрия в метаноле (149 г) и воду (13,2 г) при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 3,5 часов, добавляют н-гексан (1500 мл) и смесь отфильтровывают и собирают осадки. Полученное твердое вещество добавляют в смесь концентрированной соляной кислоты (50 мл), воды (450 мл) и хлороформа (1000 мл) при охлаждении льдом и перемешивают при комнатной температуре в течение 20 минут. Слой хлороформа отделяют и водный слой экстрагируют хлороформом. Органические слои объединяют, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок кристаллизуют из н-гексана, а полученный продукт собирают фильтрованием и сушат, что дает монометил-транс-циклогексан-1,4-дикарбоксилат (106,0 г). ESI-MSM/E: 185[M-Н]-.
(3) Монометил-транс-циклогексан-1,4-дикарбоксилат (100,0 г), полученный в примере приготовления 112(2), растворяют в трет-бутаноле (1000 мл), добавляют дифенилфосфорилазид (155 г) и триэтиламин (78,6 мл). Смесь нагревают при температуре около 60°С в течение часа и затем нагревают при температуре кипения с обратным холодильником в течение еще 17 часов. После охлаждения в реакционный раствор добавляют ледяную воду и смесь экстрагируют этилацетатом. Органический слой промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок растворяют в метаноле (250 мл), добавляют воду (750 мл) и смесь перемешивают при охлаждении льдом. После 0,5 часа осадки собирают фильтрованием, промывают последовательно смесью вода-метанол (3:1, 1000 мл) и н-гексаном и сушат, что дает названное соединение (117,0 г). APCI-MS М/Е: 275 [M+H]+.
Пример приготовления 113: Транс-4-(2-оксопирролидин-1-ил)циклогексанкарбоновая кислота
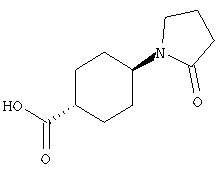
(1) Метил-транс-4-(трет-бутоксикарбониламино)циклогексанкарбоксилат (234,0 г), полученный в примере приготовления 112, растворяют в диоксане (500 мл) и добавляют 4N раствор хлористого водорода в диоксане (500 мл) и смесь перемешивают при комнатной температуре в течение 19 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в диэтиловый эфир и затем осадки собирают фильтрованием, что дает гидрохлорид метил-транс-4-аминоциклогексанкарбоксилата (121,9 г).
APCI-MS М/Е: 158 [M+H]+.
(2) Гидрохлорид метил-транс-4-аминоциклогексанкарбоксилата (45,31 г) суспендируют в дихлорметане (1000 мл), добавляют 4-хлорбутирилхлорид (31,5 мл) при охлаждении льдом и в смесь добавляют по каплям раствор триэтиламина (81,5 мл) в дихлорметане (80 мл). Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 3 часов и затем его концентрируют при пониженном давлении. В полученный осадок выливают этилацетат и 5% раствор соляной кислоты и органический слой отделяют, промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом. Органический слой сушат над сульфатом натрия и обрабатывают активированным углем и фильтрат концентрируют при пониженном давлении. Полученный осадок суспендируют в диизопропиловом эфире, отфильтровывают в собирают осадки, сушат, что дает метил-транс-4-(4-хлорбутириламино)-циклогексанкарбоксилат (38,81 г). APCI-MS М/Е: 262/264 [M+H]+.
(3) 60% Гидрид натрия в масле (9,60 г) суспендируют в N,N-диметиацетамиде (500 мл), в эту смесь постепенно добавляют метил-транс-4-(4-хлорбутириламино)-циклогексанкарбоксилат (52,32 г), полученный в примере приготовления 113(2), при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 24 часов и выливают насыщенный водный раствор хлорида аммония и ледяную воду и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом магния и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: этилацетат) и полученное твердое вещество суспендируют в смеси н-гексан-диизопропиловый эфир. Полученные кристаллы собирают фильтрованием и сушат, что дает метил-транс-4-(2-оксо-пирролидин-1-ил)циклогексанкарбоксилат (39,20 г). APCI-MS М/Е: 226 [M+H]+.
(4) Метил-транс-4-(2-оксо-пирролидин-1-ил)циклогексанкарбоксилат (39,15 г), полученный в примере приготовления 113(3), растворяют в метаноле (400 мл) и добавляют 2N водный раствор гидроксида натрия (60 мл) и смесь перемешивают при комнатной температуре в течение 3 часов. Значение рН реакционного раствора доводят до 1-2 с помощью вливания 10% раствора соляной кислоты при охлаждении льдом, насыщенного хлорида натрия и затем экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и затем выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в небольшое количество этилацетата и выливают диизопропиловый эфир и полученные кристаллы собирают фильтрованием. Кристаллы промывают диизопропиловым эфиром несколько раз и сушат, что дает названное соединение (35,94 г). ESI-MS М/Е: 210 [M-Н]-.
Пример приготовления 114: Транс-4-(N-ацетил-N-метиламино)циклогексанкарбоновая кислота
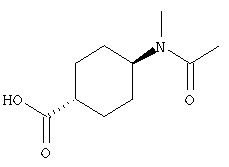
(1) Метил-транс-4-(трет-бутоксикарбониламино)циклогексанкарбоксилат (30,00 г) растворяют в N,N-диметилформамиде (150 мл) и добавляют 60% гидрид натрия в масле (5,60 г) при охлаждении льдом. После перемешивания в течение 0,5 часа при охлаждении в реакционный раствор последовательно добавляют йодистый метил (14,5 мл) и метанол (0,15 мл) и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 4 часов. При охлаждении льдом в реакционный раствор выливают насыщенный хлорид аммония и ледяную воду и смесь экстрагируют этилацетатом. Органический слой последовательно промывают водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: н-гексан/этилацетат =10/1, затем 7/1), что дает метил-транс-4-(N-трет-бутоксикарбонил-N-метиламино)циклогексанкарбоксилат (26,33 г).
APCI-MS М/Е: 272 [M+H]+.
(2) Метил-транс-4-(N-трет-бутоксикарбонил-N-метиламино)циклогексанкарбоксилат (26,32 г), полученный в примере приготовления 114(1), растворяют в диоксане (100 мл) и добавляют 4N раствор хлористого водорода-диоксана (100 мл). Реакционный раствор перемешивают при комнатной температуре в течение 4 часов и в полученный раствор выливают диизопропиловый эфир (500 мл). Осадки собирают фильтрованием, промывают диизопропиловым эфиром и сушат, что дает гидрохлорид метил-транс-4-(метиламино)циклогексанкарбоксилата (19,01 г). APCI-MS М/Е: 172 [M+H]+.
(3) Гидрохлорид метил-транс-4-(метиламино)циклогексанкарбоксилата (18,93 г), полученный в примере приготовления 114(2), суспендируют в дихлорметане (400 мл) и в полученный раствор добавляют ацетилхлорид (8,42 мл) при охлаждении льдом и затем добавляют по каплям раствор триэтиламина (38,1 мл) в дихлорметане (40 мл). Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 2 часов, добавляют 5% раствор соляной кислоты и смесь экстрагируют дихлорметаном. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат), что дает метил-транс-4-(N-ацетил-N-метиламино)циклогексанкарбоксилат (19,05 г). APCI-MS М/Е: 214 [M+H]+.
(4) Метил-транс-4-(N-ацетил-N-метиламино)-циклогексанкарбоксилат (19,00 г), полученный в примере приготовления 114(3), растворяют в метаноле (200 мл), добавляют водный 2N раствор гидроксида натрия (60 мл) и смесь перемешивают при комнатной температуре в течение 3 часов. При охлаждении льдом, рН реакционного раствора доводят до 1-2 с помощью 10% раствора соляной кислоты, насыщенного хлорида натрия и затем экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и затем выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в небольшое количество этилацетата, в смесь выливают диизопропиловый эфир и кристаллы собирают фильтрованием. Кристаллы промывают диизопропиловым эфиром несколько раз и сушат, что дает названное соединение (16,31 г). ESI-MS М/Е: 198 [M-Н]-.
Пример приготовления 115: Транс-4-(N-трет-бутоксикарбонил-N-метиламино)-циклогексанкарбоновая кислота
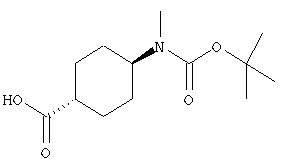
Метил-транс-4-(N-трет-бутоксикарбонил-N-метиламино)циклогексанкарбоксилат (44,78 г), полученный в примере приготовления 114(1), растворяют в метаноле (300 мл), добавляют водный 2N раствор гидроксида натрия (100 мл) и смесь перемешивают при комнатной температуре в течение 6 часов. Реакционный раствор концентрируют при пониженном давлении, в осадок добавляют ледяную воду, этилацетат и 10% раствор соляной кислоты при охлаждении льдом и затем смесь экстрагируют этилацетатом. Органический слой последовательно промывают водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в небольшое количество этилацетата, в смесь выливают н-гексан и кристаллы собирают фильтрованием. Кристаллы промывают несколько раз смесью н-гексан-диизопропиловый эфир и сушат, что дает названное соединение (39,20 г). ESI-MS М/Е: 256 [M-Н]-.
Пример приготовления 116: Транс-4-(трет-бутоксикарбониламино)циклогексанкарбоновая кислота
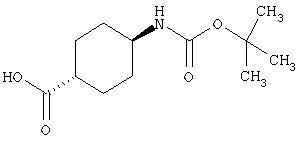
Метил-транс-4-(трет-бутоксикарбониламино)циклогексанкарбоксилат (44,78 г), полученный в примере приготовления 112, обрабатывают способом, аналогичным описанному в примере приготовления 115, что дает названное соединение (24,04 г), ESI-MS М/Е: 242 [M-Н]-.
Пример приготовления 117: Гидрохлорид транс-4-диметиламиноциклогексанкарбоновой кислоты
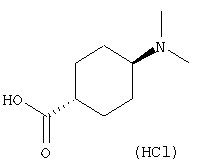
(1) Гидрохлорид метил-транс-4-аминоциклогексанкарбоксилата (93,0 г), полученный в примере приготовления 113(1), растворяют в метаноле (1000 мл), добавляют водный 35% раствор формальдегида (95,4 мл), ацетат натрия (39,4 г) и 10% раствор палладия на угле (10 г) и смесь перемешивают в течение 3,5 часов в атмосфере давления водорода. Нерастворимые продукты удаляют фильтрованием, фильтрат концентрируют при пониженном давлении, в полученный осадок добавляют водный 20% раствор карбоната калия (500 мл) и реакционную смесь экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и карбонатом калия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: н-гексан/этилацетат =2/1), что дает метил-транс-4-диметиламиноциклогексанкарбоксилат (87,3 г). APCI-MS М/Е: 186 [M+H]+.
(2) Метил-транс-4-диметиламиноциклогексан-карбоксилат (27,6 г), полученный в примере приготовления 117(1), растворяют в диоксане (300 мл) и воде (100 мл), добавляют 6N соляную кислоту (50 мл) и смесь нагревают при температуре кипения с обратным холодильником в течение 4 часов. В смесь добавляют еще 6N соляную кислоту (50 мл) и реакционную смесь нагревают при температуре кипения с обратным холодильником еще в течение часа. Реакционный раствор концентрируют при пониженном давлении, подвергают азеотропной дистилляции с толуолом и затем полученный осадок суспендируют в диизопропиловом эфире. Осадки собирают фильтрованием, промывают диизопропиловым эфиром и сушат, что дает названное соединение (27,5 г). APCI-MS М/Е: 172 [M+H]+.
Пример приготовления 118: Гидрохлорид транс-4-(пирролидин-1-ил)циклогексанкарбоновой кислоты
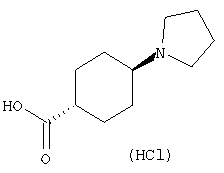
(1) Гидрохлорид метил-транс-4-аминоциклогексанкарбоксилат (10 г), полученный в примере приготовления 113(1), 1,4-дииодобутан (19,2 г), карбонат натрия (16,4 г) суспендируют в смеси тетрагидрофурана (300 мл) и N,N-диметилацетамида (60 мл) и смесь перемешивают при температуре 70°С в течение 20 часов. Реакционный раствор концентрируют при пониженном давлении, осадок растворяют в смеси этилацетат-вода и органический слой отделяют. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: этилацетат/гексан =1/5), что дает метил-транс-4-(пирролидин-1-ил)циклогексанкарбоксилат (10,9 г). APCI-MS М/Е: 212 [M+H]+.
(2) В раствор метил-транс-4-(пирролидин-1-ил)циклогексанкарбоксилата (10,9 г), полученного в примере приготовления 118(1), в диоксане (150 мл), добавляют 2N соляную кислоту (80 мл) и смесь перемешивают при температуре 110°С в течение 3 часов при выпаривании, чтобы удалить метанол. Реакционный раствор концентрируют при пониженном давлении, полученный осадок суспендируют в диэтиловом эфире и затем собирают фильтрованием, что дает названное соединение (11,1 г). APCI-MS М/Е: 198 [M+H]+.
Пример приготовления 119: Гидрохлорид транс-4-(морфолин-4-ил)циклогексанкарбоновой кислоты
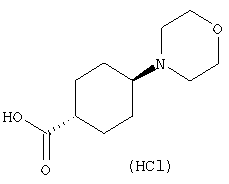
(1) Гидрохлорид метил-транс-4-аминоциклогексанкарбоксилата (47,5 г), полученный в примере приготовления 113(1), бис(2-хлорэтил)эфир (34,5 мл), карбонат натрия (77,9 г) и иодид натрия (88 г) суспендируют в смеси тетрагидрофурана (1400 мл) и N,N-диметилацетамида (280 мл) и смесь нагревают при температуре кипения с обратным холодильником в течение 18 часов. В реакционный раствор добавляют бис(2-хлорэтил) эфир (23 мл) и иодид натрия (22 г) и смесь нагревают до температуры кипения с обратным холодильником в течение еще 6 часов. Реакционный раствор концентрируют при пониженном давлении и осадок растворяют в смеси этилацетат-вода и органический слой отделяют. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь этилацетат/гексан =1/30, затем этилацетат/гексан =1/5 и затем 1/3), что дает метил-транс-4-(морфолин-4-ил)циклогексанкарбоксилат (53,9 г).
APCI-MS М/Е: 228 [M+H]+.
(2) В раствор метил-транс-4-(морфолин-4-ил)циклогексанкарбоксилата (53,8 г), полученного в примере приготовления 119(1), в диоксане (750 мл), добавляют 2N соляную кислоту (400 мл) и смесь перемешивают при температуре 110°С в течение 4 часов при выпаривании, чтобы удалить метанол. Реакционный раствор концентрируют и полученный осадок суспендируют в диэтиловом эфире и затем полученный продукт собирают фильтрованием, что дает названное соединение (54,8 г).
APCI-MS М/Е: 214 [M+H]+.
Пример приготовления 120: Гидрохлорид транс-[4-(диметиламино)циклогексил]уксусной кислоты
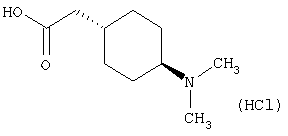
(1) Гидроксид калия (12,8 г) растворяют в воде (30 мл) и добавляют диэтиловый эфир (45 мл). При охлаждении льдом в полученную смесь добавляют N-нитрозо-N-метилмочевину (5,07 г). Реакционный раствор перемешивают в течение 10 минут при охлаждении и органический слой отделяют и сушат над гидроксидом калия, что дает раствор диазометана в диэтиловом эфире.
(2) В атмосфере аргона транс-4-(трет-бутоксикарбониламино)-циклогексанкарбоновую кислоту (3,0 г), полученную в примере приготовления 116, суспендируют в диэтиловом эфире (40 мл), добавляют триэтиламин (1,89 мл) при температуре -10°С и затем в смесь добавляют по каплям изобутилхлорформиат (1,75 мл). Реакционный раствор перемешивают при температуре -10°С в течение 30 минут и в реакционный раствор при температуре -10°С добавляют по каплям раствор диазометана в диэтиловом эфире, полученный в примере приготовления 120(1) и смесь нагревают до комнатной температуры и перемешивают в течение 15 часов. При охлаждении льдом 10% водный раствор лимонной кислоты выливают в раствор и органический слой отделяют. Органический слой промывают насыщенным водным раствором гидрокарбоната натрия, водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь этилацетат/гексан =1/3, затем смесь этилацетат/гексан =1/2), что дает трет-бутил-транс-[4-(2-диазоацетил)циклогексил]карбамат (1,86 г). APCI-MS М/Е: 285 [M+NH4]+.
(3) трет-Бутил-транс-[4-(2-диазоацетил)циклогексил]-карбамат (1,62 г), полученный в примере приготовления 120(2), растворяют в метаноле (30 мл) в свете, экранирующем реакционный сосуд в атмосфере аргона, и смесь охлаждают до температуры -25°С. В реакционный раствор добавляют раствор бензоата серебра (153 мг) в триэтиламин (2,4 мл) и смесь нагревают до комнатной температуры и перемешивают в течение 3 часов. Реакционный раствор концентрируют при пониженном давлении, полученный осадок растворяют в этилацетате, промывают последовательно насыщенным водным раствором гидрокарбоната натрия, насыщенным водным раствором хлорида аммония и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, который обеспечивает получение метил-транс-4-(трет-бутоксикарбониламино)циклогексил]ацетата (1,25 г).
APCI-MS М/Е: 289 [M+NH4]+.
(4) В раствор метил-транс-[4-(трет-бутоксикарбониламино)циклогексил]ацетата (1,23 г), полученного в примере приготовления 120(3), в 1,4-диоксане (8 мл), добавляют 4N раствор хлористого водорода-диоксана (8 мл) и смесь перемешивают при комнатной температуре в течение 5 часов. Реакционный раствор концентрируют досуха при пониженном давлении, что дает метил-транс-(4-аминоциклогексил)ацетат гидрохлорид (898 мг). APCI-MS М/Е: 172 [M+H]+.
(5) При охлаждении льдом в суспензию гидрохлорида метил-транс-(4-аминоциклогексил)ацетата (895 мг), полученную в примере приготовления 120(4), в дихлорметане (30 мл), добавляют триэтиламин (1,2 мл) и смесь перемешивают. Последовательно добавляют при охлаждении льдом водный 35% раствор формальдегида (1,71 мл) и триацетоксиборгидрид натрия (2,74 г). Реакционный раствор нагревают до комнатной температуры и перемешивают в течение 6 часов. Насыщенный водный раствор гидрокарбоната натрия выливают в смесь при охлаждении льдом и смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и затем растворитель удаляют при пониженном давлении, что дает метил-транс-[4-(диметиламино)циклогексил]ацетат (771 мг). APCI-MS М/Е: 200 [M+H]+.
(6) В раствор метил-транс-[4-(диметиламино)циклогексил] ацетата (760 мг), полученный в примере приготовления 120(5), в диоксане (25 мл), добавляют 1N соляную кислоту (15 мл) и смесь нагревают при температуре кипения с обратным холодильником в течение 3 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире. Осадки собирают фильтрованием и сушат, что дает названное соединение (795 мг).
APCI-MS М/Е: 186 [М+H]+.
Пример приготовления 121: Гидрохлорид транс-4-(диметиламинометил)циклогексанкарбоновой кислоты
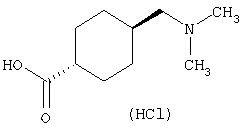
(1) Транс-4-(аминометил)циклогексанкарбоновую кислоту (6,29 г) суспендируют в метаноле (32 мл) и в суспензию добавляют по каплям тионилхлорид (6 мл) при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры, перемешивают в течение ночи и концентрируют досуха при пониженном давлении, который обеспечивает получение гидрохлорида метил-транс-4-(аминометил)-циклогексанкарбоксилата (8,69 г).
APCI-MS М/Е: 172 [M+H]+.
(2) Гидрохлорид метил-транс-4-(аминометил)циклогексанкарбоксилата (8,69 г), полученный в примере приготовления 121(1), суспендируют в дихлорметане (400 мл), добавляют триэтиламин (11,2 мл) и смесь перемешивают при комнатной температуре в течение нескольких минут и добавляют 35% водный раствор формальдегида (15,9 мл) и триацетоксиборогидрид натрия (25,43 г) при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 2 часов, в раствор выливают насыщенный водный раствор гидрокарбоната натрия и раствор экстрагируют хлороформом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, что дает метил-транс-4-(диметиламинометил)циклогексанкарбоксилат (7,42 г). APCI-MS М/Е: 200 [M+H]+.
(3) Метил-транс-4-(диметиламинометил)-циклогексанкарбоксилат (7,41 г), полученный в примере приготовления 121(2), растворяют в диоксане (140 мл), добавляют 2N соляную кислоту (70 мл) и смесь нагревают при температуре кипения с обратным холодильником в течение 3 часов. После охлаждения реакционный раствор концентрируют при пониженном давлении, полученный осадок подвергают азеотропной дистилляции с толуолом и затем полученный продукт сушат, что дает названное соединение (8,45 г). APCI-MS М/Е: 186 [M+H]+.
Пример приготовления 122: Транс-4-(трет-бутоксикарбониламинометил)циклогексанкарбоновая кислота
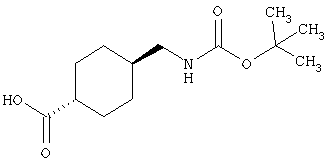
Транс-4-(аминометил)циклогексанкарбоновую кислоту (8,35 г) суспендируют в диоксане (100 мл), добавляют воду (50 мл) и 1N водный раствор гидроксида натрия (50 мл) и затем добавляют по каплям при охлаждении льдом ди-трет-бутил дикарбонат (12,7 г). Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 4 часов и реакционный раствор концентрируют при пониженном давлении. Полученный осадок разбавляют этилацетатом, значение рН доводят до 3-4 путем добавления водного раствора лимонной кислотой и экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в н-гексане и полученный продукт собирают фильтрованием и сушат, что дает названное соединение (13,30 г). ESI-MS М/Е: 256 [M-Н]-.
Пример приготовления 123: Гидрохлорид этил-3-(пиперидин-4-ил)пропионата
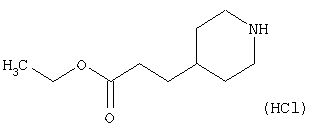
(1) 60% гидрид натрия в масле (33,6 г) суспендируют в тетрагидрофуране (600 мл) и добавляют по каплям при охлаждении льдом раствор триэтилфосфоноацетата (188,4 г) в тетрагидрофуране (100 мл). Смесь перемешивают в течение 0,5 часа при охлаждении льдом и добавляют по каплям раствор пиридин-4-карбальдегида (75,00 г) в тетрагидрофуране (100 мл) и смесь перемешивают в течение часа. В реакционный раствор выливают ледяную воду (1000 мл) при охлаждении льдом и смесь экстрагируют этилацетатом. Органический слой промывают последовательно водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в небольшом количестве диизопропилового эфира при охлаждении льдом и осадки собирают фильтрованием. Осадки промывают последовательно небольшим количеством диизопропилового эфира и н-гексана и сушат, что дает этил 3-(пиридин-4-ил)акрилат (77,53 г). APCI-MS М/Е: 178 [M+H]+.
(2) Этил-3-(пиридин-4-ил)акрилат (28,00 г), полученный в примере приготовления 123(1), растворяют в уксусной кислоте (280 мл), добавляют оксид платины (1,80 г) и смесь встряхивают под давлением атмосферы водорода 55 пси при комнатной температуре в течение 24 часов. Нерастворимые продукты удаляют фильтрованием и фильтрат концентрируют при пониженном давлении. Полученный осадок растворяют в диоксане (200 мл), добавляют 4N хлористый водород-диоксан (200 мл) и смесь выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в смеси диэтиловый эфир-диизопропиловый эфир, осадки собирают фильтрованием, промывают диизопропиловым эфиром и сушат, что дает названное соединение (33,50 г). APCI-MS М/Е: 186 [M+H]+.
Пример приготовления 124: Гидрохлорид этил (пиперидин-4-ил) ацетата
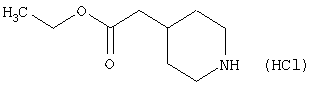
Этил-(пиридин-4-ил)ацетат (50,00 г) растворяют в уксусной кислоте (500 мл), добавляют оксид платины (3,44 г) и смесь встряхивают при давлении атмосферы водорода 55 пси при комнатной температуре в течение 20 часов. Нерастворимые продукты удаляют фильтрованием, и фильтрат концентрируют при пониженном давлении. Полученный осадок растворяют в диоксане (200 мл), добавляют 4N хлористый водород-диоксан (400 мл) и затем смесь выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в смесь диэтиловый эфир-диизопропиловый эфир и осадки собирают фильтрованием, промывают диизопропиловым эфиром и затем сушат, что дает названное соединение (61,80 г). APCI-MS М/Е: 172 [M+H]+.
Пример приготовления 125: Этил-3-(1-изопропилпиперидин-4-ил)пропионат
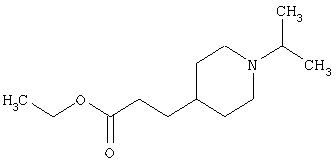
Гидрохлорид этил-3-(пиперидин-4-ил)пропионата (70,83 г), полученный в примере приготовления 123, растворяют в этаноле (700 мл), добавляют 2-иодопропан (38,2 мл) и карбонат калия (132.3 г) и смесь нагревают при температуре кипения с обратным холодильником в течение 6 часов. Нерастворимые продукты удаляют фильтрованием и фильтрат концентрируют при пониженном давлении. Полученный осадок разбавляют этилацетатом (800 мл), промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =20/1, затем 9/1), что дает названное соединение (57,13 г). APCI-MS М/Е: 228 [M+H]+.
Примеры приготовления 126-127:
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 125, что дает следующие соединения.
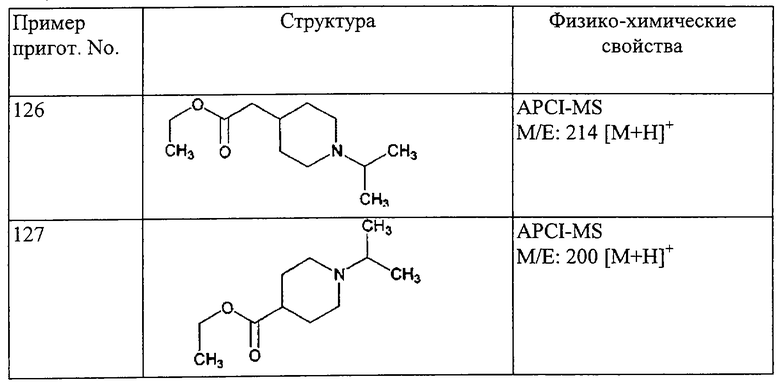
Пример приготовления 128: Гидрохлорид 3-(1-изопропилпиперидин-4-ил)пропановой кислоты
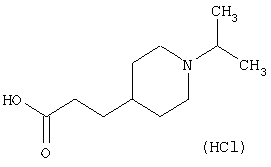
Этил-3-(1-изопропилпиперидин-4-ил)пропионат (57,12 г), полученный в примере приготовления 125, растворяют в диоксане (1200 мл), добавляют 2N соляную кислоту (600 мл) и смесь нагревают при температуре кипения с обратным холодильником в течение 3 часов. Реакционный раствор концентрируют при пониженном давлении, подвергают азеотропной дистилляции с диоксаном и полученный осадок суспендируют в смеси диэтиловый эфир-диизопропиловый эфир (1:1, 500 мл). Осадки собирают фильтрованием, промывают диизопропиловым эфиром и сушат, что дает названное соединение (55,36 г). APCI-MS М/Е: 200 [M+H]+.
Примеры приготовления 129-130
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 128, что дает следующие соединения.
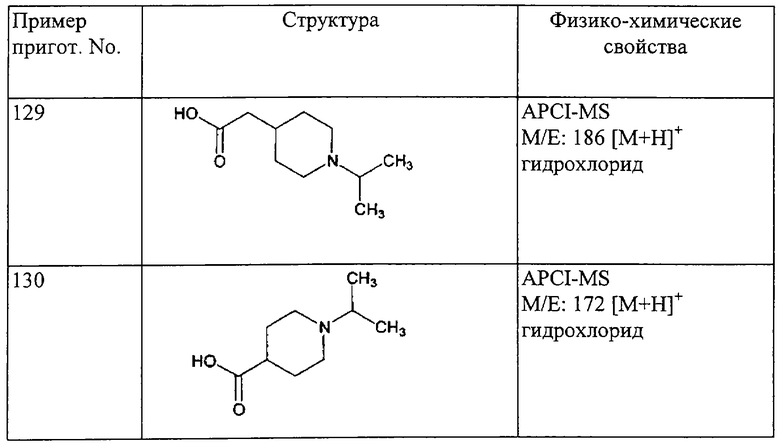
Пример приготовления 131: 1-(Пиридин-4-ил)пиперидин-4-карбоновой кислоты
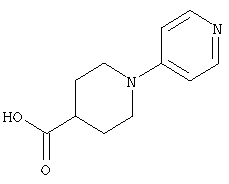
Гидрохлорид 4-хлорпиридина (9,55 г) и триэтиламин (26,0 мл) растворяют в этаноле (10 мл) и воде (30 мл), добавляют этилизоникотинат (10,00 г) и затем реакционный раствор нагревают при температуре 150°С в течение 96 часов в герметичной колбе. После охлаждения в реакционный раствор добавляют этанол и нерастворимые продукты удаляют фильтрованием. Фильтрат концентрируют при пониженном давлении, полученный осадок суспендируют в хлороформе, осадки собирают фильтрованием и перекристаллизовывают из смеси вода-N,N-диметилформамид, что дает названное соединение (10,34 г). APCI-MS М/Е: 207 [M+H]+.
Пример приготовления 132: Гидрохлорид [1-(пиридин-4-ил)пиперидин-4-ил]уксусной кислоты
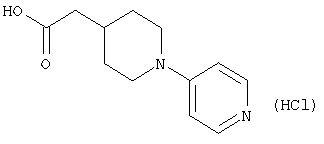
(1) Гидрохлорид этил-(пиперидин-4-ил)ацетат (5,00 г), полученный в примере приготовления 124, гидрохлорид 4-хлорпиридина (3,62 г) и триэтиламин (10,1 мл) суспендируют в ксилоле (130 мл) и нагревают при температуре кипения с обратным холодильником в течение 20 часов. Реакционный раствор охлаждают водой и нерастворимые продукты удаляют фильтрованием. Фильтрат концентрируют при пониженном давлении, полученный осадок разбавляют хлороформом, промывают водой, сушат над сульфатом магния и затем выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь хлороформ/этилацетат =4/1), что дает этил-[1-(пиридин-4-ил)пиперидин-4-ил]ацетат (4,15 г). APCI-MS М/Е: 249 [M+H]+.
(2) Этил-[1-(пиридин-4-ил)пиперидин-4-ил]ацетат (4,15 г), полученный в примере приготовления 132(1), растворяют в диоксане (200 мл), добавляют 1N соляную кислоту (70 мл) и смесь нагревают при температуре кипения с обратным холодильником в течение 4 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок лиофилизуют, что дает названное соединение (3,90 г). APCI-MS М/Е: 221 [M+H]+.
Пример приготовления 133: Гидрохлорид 3-[1-(пиримидин-4-ил)пиперидин-4-ил]-пропановой кислоты
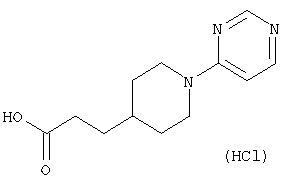
(1) Гидрохлорид этил-3-(пиперидин-4-ил)пропионата (5,00 г), полученный в примере приготовления 123, суспендируют в тетрагидрофуране (50 мл) и добавляют 4,6-дихлорпиримидин (2,80 г) и диизопропилэтиламин (13,1 мл) при комнатной температуре. Реакционный раствор перемешивают в течение 3 часов при комнатной температуре, добавляют воду и смесь экстрагируют этилацетатом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь н-гексан/этилацетат =5/1, затем 3/1), что дает этил-3-[1-(6-хлорпиримидин-4-ил)пиперидин-4-ил]пропионат (5,58 г). APCI-MS М/Е: 298/300 [M+H]+.
(2) Этил-3-[1-(6-хлорпиримидин-4-ил)пиперидин-4-ил]пропионат (5,54 г), полученный в примере приготовления 133(1), растворяют в этаноле (100 мл), добавляют 10% раствор палладия на угле (0,55 г) и смесь перемешивают в течение 4 часов в атмосфере водорода при нормальном давлении. Нерастворимые продукты удаляют фильтрованием и фильтрат концентрируют при пониженном давлении. Этилацетат и насыщенный водный раствор гидрокарбоната натрия выливают в полученный осадок, органический слой отделяют, промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении, что дает этил-3-[1-(пиримидин-4-ил)пиперидин-4-ил]пропионат (3,57 г). APCI-MS М/Е: 264 [M+H]+.
(3) Этил-3-[1-(пиримидин-4-ил)пиперидин-4-ил]-пропионат (3,54 г), полученный в примере приготовления 133(2), растворяют в диоксане (140 мл), добавляют 1N соляную кислоту (70 мл) и смесь нагревают при температуре кипения с обратным холодильником в течение 3 часов. После охлаждения реакционный раствор концентрируют при пониженном давлении и подвергают диазеотропной дистилляции с диоксаном. Полученный осадок суспендируют в диэтиловом эфире и полученный продукт собирают фильтрованием, промывают диэтиловым эфиром и затем сушат, что дает названное соединение (3,63 г).
ESI-MS М/Е: 234 [M-Н]-.
Пример приготовления 134: Гидрохлорид 3-(1-изопропилпиперидин-4-ил)акриловой кислоты
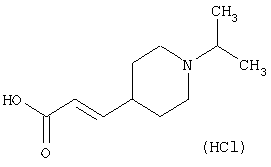
(1) Алюминийгидрид лития (1,10 г) суспендируют в тетрагидрофуране (80 мл) и добавляют по каплям при охлаждении льдом раствор этил-1-изопропилпиперидин-4-карбоксилата (5,00 г), полученный в примере приготовления 127, в тетрагидрофуране (30 мл). Реакционный раствор перемешивают в течение 2 часов при охлаждении льдом и водой (1,1 мл), последовательно добавляют по каплям 15% водный раствор гидроксида натрия (1,1 мл) и воду (3,3 мл) и перемешивают в течение еще 10 минут. В полученный реакционный раствор добавляют карбонат калия и смесь перемешивают в течение 20 минут, а затем их удаляют фильтрованием. Фильтрат концентрируют при пониженном давлении и затем полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь хлороформ/этилацетат =1/1), что дает (1-изопропилпиперидин-4-ил)метанол (4,29 г). APCI-MS М/Е: 158 [M+H]+.
(2) Оксалилхлорид (2,0 мл) растворяют в дихлорметане (120 мл) и добавляют по каплям раствор диметилсульфоксида (3,3 мл) в дихлорметане (15 мл) при охлаждении сухим льдом-ацетоном. После перемешивания в течение 10 минут при охлаждении льдом по каплям добавляют в течение 15 минут раствор (1-изопропилпиперидин-4-ил)метанола (3,00 г), полученный в примере приготовления 134(1), в дихлорметане (30 мл). После добавления реакционный раствор перемешивают в течение 2 часов при охлаждении льдом и добавляют по каплям триэтиламин (13,3 мл) в течение 10 минут. Реакционный раствор перемешивают в течение часа, пока он не нагреется до комнатной температуры, и затем раствор выливают в насыщенный водный раствор гидрокарбоната натрия. Смесь экстрагируют дихлорметаном и выпаривают, чтобы удалить растворитель, при пониженном давлении. Водный слой экстрагируют этилацетатом и экстракт объединяют с осадком, полученным путем удаления растворителя из указанного выше экстракта дихлорметана, промывают водой и насыщенным рассолом и сушат над сульфатом натрия. Растворитель выпаривают при пониженном давлении, что дает сырой 1-изопропилпиперидин-4-карбальдегид (1,96 г). APCI-MS М/Е: 156 [M+H]+.
(3) Триэтилфосфоноацетат (7,96 г) растворяют в тетрагидрофуране (50 мл) и добавляют постепенно 60% гидрид натрия в масле (1,45 г) при охлаждении льдом. После перемешивания в течение 20 минут при охлаждении льдом в смесь добавляют 1-изопропилпиперидин-4-карбальдегид (5,03 г), полученный в примере приготовления 134(2), в тетрагидрофуране (25 мл). Реакционный раствор перемешивают в течение 3 часов, разбавляют диэтиловым эфиром, добавляют воду и смесь экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из NH-силикагеля (элюент: смесь н-гексан/этилацетат =9/1), что дает этил 3-(1-изопропилпиперидин-4-ил)акрилат (6,87 г). APCI-MS М/Е: 226 [M+H]+.
(4) Этил-3-(1-изопропилпиперидин-4-ил)акрилат (1,01 г), полученный в примере приготовления 134(3), растворяют в этаноле (20 мл), добавляют 2N водный раствор гидроксида натрия (4,5 мл) и смесь перемешивают при комнатной температуре в течение 24 часов. В реакционный раствор добавляют 2N соляную кислоту (9 мл) и смесь концентрируют при пониженном давлении и затем полученный осадок лиофилизуют, что дает названное соединение (1,43 г). APCI-MS М/Е: 198 [M+H]+.
Пример приготовления 135: (1-трет-Бутоксикарбонилпиперидин-4-ил)уксусная кислота
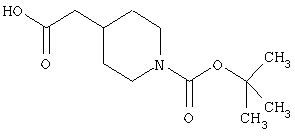
(1) Гидрохлорид этил-(пиперидин-4-ил)ацетата, полученный в примере приготовления 124 (10,00 г), суспендируют в тетрагидрофуране (95 мл) и по каплям при охлаждении льдом добавляют гидрокарбонат натрия (12,14 г) и воду (150 мл) и затем добавляют раствор ди-трет-бутилдикарбоната (11,60 г) в тетрагидрофуране (55 мл). Реакционный раствор перемешивают при комнатной температуре в течение 20 часов, водный раствор карбоната калия выливают в раствор и смесь экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом магния и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: н-гексан/этилацетат =5/1), что дает этил-(1-трет-бутоксикарбонилпиперидин-4-ил)ацетат (13,06 г). APCI-MS М/Е: 272 [M+H]+.
(2) Этил-(1-трет-бутоксикарбонилпиперидин-4-ил)ацетат (13,00 г), полученный в примере приготовления 135(1), растворяют в смеси тетрагидрофуран-этанол (2:1, 180 мл) и добавляют раствор гидроксида натрия (4,80 г) в воде (60 мл). Реакционный раствор перемешивают при комнатной температуре в течение ночи, концентрируют при пониженном давлении и полученный водный слой промывают диэтиловым эфиром. Водный слой подкисляют 1N соляной кислотой при охлаждении льдом и затем экстрагируют этилацетатом. Органический слой промывают водой и насыщенным рассолом и затем сушат сульфатом магния. Растворитель выпаривают при пониженном давлении, что дает названное соединение (11,10 г). ESI-MS М/Е: 242 [M-Н]-.
Примеры приготовления 136-137
Соответствующие соединения обрабатывают способом, аналогичным описанному в примере приготовления 135, что дает следующие соединения.
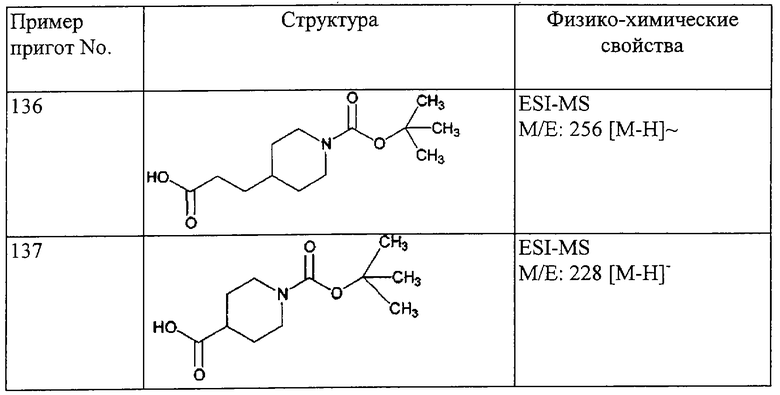
Пример приготовления 138: трет-Бутил 4-карбоксиметилен-1-пиперидинкарбоксилат
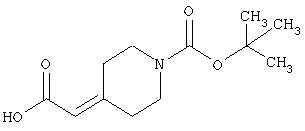
(1) трет-Бутоксикалий (4,49 г) суспендируют в N,N-диметилформамиде в атмосфере аргона и в смесь добавляют по каплям триэтилфосфоноацетат (5,83 г) при охлаждении льдом. После перемешивания в течение 0,5 часа при охлаждении льдом в реакционный раствор добавляют по каплям трет-бутил-4-оксо-1-пиперидинкарбоксилат (4,07 г) и смесь нагревают до комнатной температуры и перемешивают в течение 1,5 часов. В реакционный раствор добавляют ледяную воду при охлаждении льдом и осадки собирают фильтрованием и сушат, что дает трет-бутил-4-этоксикарбонилметилен-1-пиперидинкарбоксилат (3,02 г). APCI-MS М/Е: 287 [M+NH4]+.
(2) трет-Бутил-4-этоксикарбонилметилен-1-пиперидинкарбоксилат (1,08 г), полученный в примере приготовления 138(1), растворяют в диоксане (12 мл), добавляют 1N водный раствор гидроксида натрия (8 мл) и смесь перемешивают при комнатной температуре в течение ночи. Реакционный раствор подкисляют 1N соляной кислотой и затем экстрагируют этилацетатом. Органический слой промывают последовательно водой и насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ/метанол =50/1), что дает названное соединение (0,72 г). ESI-MS М/Е: 240 [M-Н]-.
Пример приготовления 139: (4-Изопропилпиперазин-1-ил)уксусная кислота
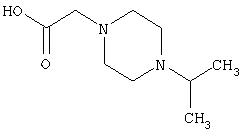
(1) 1-Изопропилпиперазин (1,21 г) растворяют в ацетонитриле (12 мл), добавляют карбонат калия (3,15 г) и затем добавляют по каплям раствор бензилбромацетата (2,08 г) в ацетонитриле (2 мл). Реакционный раствор нагревают при температуре кипения с обратным холодильником в течение часа, после охлаждения нерастворимые продукты удаляют фильтрованием и фильтрат концентрируют при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ/метанол =50/1, затем 9/1), что дает бензил(4-изопропилпиперазин-1-ил)ацетат (2,84 г).
APCI-MS М/Е: 277 [M+H]+.
(2) Бензил-(4-изопропилпиперазин-1-ил)ацетат (2,83 г), полученный в примере приготовления 139(1), растворяют в метаноле (40 мл), добавляют 10% раствор палладия на угле (0,31 г) и затем смесь перемешивают в течение 7 часов в атмосфере водорода при нормальном давлении. Нерастворимые продукты удаляют фильтрованием, фильтрат концентрируют при пониженном давлении, что дает названное соединение (1,82 г). APCI-MS М/Е: 187 [M+H]+.
Пример приготовления 140: Дигидрохлорид 3-(4-изопропилпиперазин-1-ил)пропановой кислоты
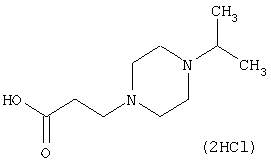
(1) 1-Изопропилпиперазин (650 мг) растворяют в ацетонитриле (7 мл) и добавляют трет-бутилакрилат (743 мкл) при охлаждении льдом. Реакционный раствор нагревают до комнатной температуры и перемешивают в течение 4 часов и добавляют еще порцию трет-бутилакрилата (148 мкл) и затем смесь перемешивают при комнатной температуре в течение еще 10 часов. В реакционный раствор дополнительно добавляют трет-бутилакрилат (222 мкл) и смесь перемешивают в течение 6 часов, затем выливают воду и раствор экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ/метанол =20/1, затем 10/1), что дает трет-бутил-3-(4-изопропилпиперазин-1-ил)пропионат (1,18 г). APCI-MS М/Е: 257 [M+H]+.
(2) трет-Бутил-3-(4-изопропилпиперазин-1-ил)пропионат (1,15 г), полученный в примере приготовления 140(1), растворяют в диоксане (10 мл) и добавляют 4N хлористый водород-диоксан (25 мл) и реакционный раствор перемешивают при комнатной температуре в течение 48 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире. Осадки собирают и сушат, что дает названное соединение (1,06 г). APCI-MS М/Е: 201 [M+H]+.
Пример приготовления 141: Транс-4-(3-оксо-морфолин-4-ил)циклогексанкарбоновая кислота
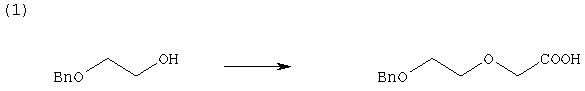
60% Гидрид натрия в масле (6,80 г) суспендируют в N,N-диметилацетамиде (80 мл) и в смесь добавляют по каплям в течение 10 минут при охлаждении льдом раствор 2-бензилоксиэтанола (12,9 г) в N,N-диметилацетамиде (50 мл). После перемешивания при комнатной температуре в течение 15 минут реакционный раствор охлаждают льдом, постепенно добавляют хлоруксусную кислоту (8,13 г) и смесь перемешивают при комнатной температуре в течение 11 часов. Реакционный раствор концентрируют при пониженном давлении, в полученный осадок добавляют водный раствор гидрокарбоната натрия и смесь промывают диэтиловым эфиром. Водный слой подкисляют концентрированной соляной кислотой и затем экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении, что дает (2-бензилоксиэтокси)уксусную кислоту (18,24 г). ESI-MS М/Е: 209 [M-Н]-.
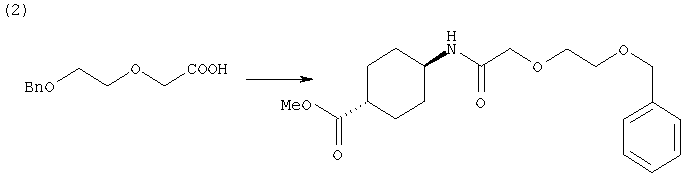
(2-Бензилоксиэтокси)уксусную кислоту (6,51 г), полученную в (1), гидрохлорид метил-транс-4-аминоциклогексанкарбоксилата (5,27 г), полученный в примере приготовления 113(1), и 1-гидроксибензотриазол (5,06 г) растворяют в N,N-диметилформамиде (100 мл). В смесь последовательно добавляют гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (7,10 г) и триэтиламин (4,50 мл) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 3 дней. Реакционный раствор концентрируют при пониженном давлении, в полученный осадок добавляют водный раствор гидрокарбоната натрия и смесь экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: гексан/этилацетат =1:1, затем этилацетат), что дает метил-транс-4-[2-(2-бензил-оксиэтокси)ацетиламино]циклогексанкарбоксилат (8,24 г). APCI-MS М/Е: 350 [M+H]+.
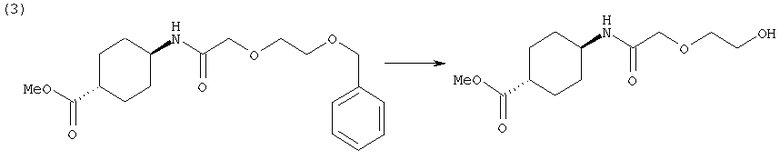
Метил-транс-4-[2-(2-бензилоксиэтокси)ацетиламино]циклогексанкарбоксилат (5,09 г), полученный в (2), растворяют в уксусной кислоте (150 мл) и добавляют 5% раствор палладия на угле (1,01 г) и смесь перемешивают в течение 2,4 часов в атмосфере водорода при нормальном давлении. Реакционный раствор отфильтровывают, чтобы удалить катализатор и затем фильтрат концентрируют при пониженном давлении. Полученный осадок растворяют в хлороформе, промывают насыщенным раствором гидрокарбоната натрия, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, что дает метил-транс-4-[2-(2-гидроксиэтокси)ацетиламино]циклогексанкарбоксилат (3,32 г). APCI-MS М/Е: - 260 [M+H]+.
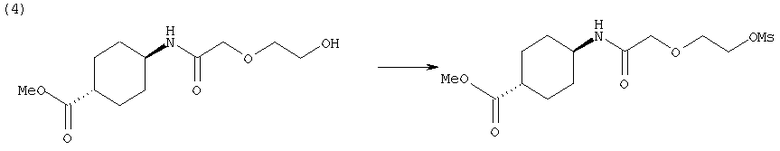
Метил-транс-4-[2-(2-гидроксиэтокси)ацетиламино]-циклогексанкарбоксилат (1,37 г), полученный в (3), растворяют в хлороформе (15 мл) и добавляют триэтиламин (890 мкл) при охлаждении льдом. Затем добавляют по каплям при той же температуре метансульфонилхлорид (450 мкл). Реакционный раствор перемешивают в течение 3 часов при охлаждении льдом, разбавляют водой и экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и удаляют растворитель путем выпаривания при пониженном давлении, что дает метил-транс-4-[2-(2-метансульфонилоксиэтокси)ацетиламино]циклогексанкарбоксилат (1,83 г). APCI-MS М/Е: 338 [M+H]+.
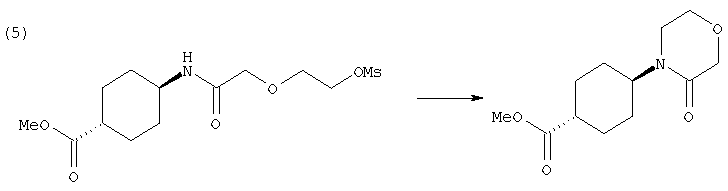
Метил-транс-4-[2-(2-метансульфонилоксиэтокси)ацетиламино]циклогексанкарбоксилат (1,08 г), полученный в (4), растворяют в N,N-диметилацетамиде (15 мл), добавляют 60% гидрид натрия в масле (135 мг) при охлаждении льдом и смесь перемешивают в течение 16 часов при комнатной температуре. В осадок, полученный путем концентрирования реакционного раствора при пониженном давлении, добавляют воду и избыток хлорида натрия и смесь экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь гексан/этилацетат =1:1, затем этилацетат), что дает метил-транс-4-(3-оксо-морфолин-4-ил)циклогексанкарбоксилат (715 мг). APCI-MS М/Е: 242 [M+H]+.
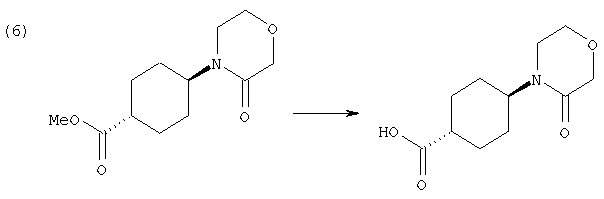
Метил-транс-4-(3-оксо-морфолин-4-ил)циклогексанкарбоксилат (500 мг), полученный в (5), обрабатывают аналогично, как в примере приготовления 113(4), что дает названное соединение (322 мг). ESI-MS М/Е: 226 [M-Н]-.
Пример приготовления 142: Транс-4-(2-оксо-оксазолидин-3-ил)циклогексанкарбоновая кислота
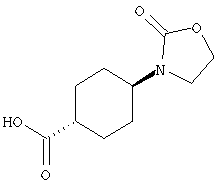
(1) Гидрохлорид метил-транс-4-аминоциклогексанкарбоксилата (5,00 г), полученный в примере приготовления 113(1), растворяют в хлороформе (60 мл), добавляют триэтиламин (11 мл) при охлаждении льдом и затем добавляют по каплям раствор 2-хлорэтилхлороформиата (3,3 мл) в хлороформе (10 мл). После перемешивания при комнатной температуре в течение 2,5 часов в реакционный раствор добавляют 5% раствор соляной кислоты и затем смесь экстрагируют хлороформом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и затем выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в смеси хлороформ-диизопропиловый эфир, осадки собирают фильтрованием и сушат, что дает метил-транс-4-(2-хлор-этилоксикарбониламино)циклогексанкарбоксилат (5,11 г). APCI-MS М/Е: 264/266 [M+H]+.
(2) Метил-транс-4-(2-хлорэтилоксикарбониламино)циклогексанкарбоксилат (3,70 г), полученный в (1), растворяют в N,N-диметилацетамиде (50 мл), добавляют 60% раствор гидрида натрия в масле (630 мг) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 16,5 часов. В реакционный раствор добавляют воду, смесь экстрагируют этилацетатом, органический слой промывают водой и насыщенным рассолом и затем сушат над сульфатом натрия. Растворитель удаляют путем выпаривания при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: гексан/этилацетат =1/1, затем этилацетат), что дает метил транс-4-(2-оксо-оксазолидин-3-ил)циклогексанкарбоксилат (1,83 г). APCI-MS М/Е: 228 [M+H]+.
(3) Метил-транс-4-(2-оксо-оксазолидин-3-ил)циклогексанкарбоксилат (1,84 г), полученный в (2), обрабатывают способом, аналогичным описанному в примере приготовления 113(4), что дает названное соединение (1,75 г). ESI-MS М/Е: 212 [M-Н]-.
Пример приготовления 143: Транс-4-(2-оксо-пирролидин-1-илметил)циклогексанкарбоновая кислота
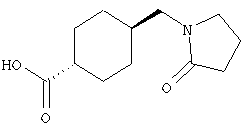
(1) Гидрохлорид метил-транс-4-(аминометил)циклогексанкарбоксилата (4,57 г), полученный в примере приготовления 121(1), обрабатывают способом, аналогичным описанному в примере приготовления 113(2), что дает метил-транс-4-(4-хлорбутириламинометил)циклогексанкарбоксилат (5,35 г). APCI-MS М/Е: 276/278 [M+H]+.
(2) Метил-транс-4-(4-хлорбутириламинометил)циклогексанкарбоксилат (3,75 г), полученный в (1), обрабатывают способом, аналогичным описанному в примере приготовления 113(3), что дает метил-транс-4-(2-оксо-пирролидин-1-илметил)-циклогексанкарбоксилат (2,07 г). APCI-MS М/Е: 240 [M+H]+.
(3) Метил-транс-4-(2-оксо-пирролидин-1-илметил)циклогексанкарбоксилат (2,04 г), полученный в (2), обрабатывают способом, аналогичным описанному в примере приготовления 113(4), что дает транс-4-(2-оксо-пирролидин-1-илметил)-циклогексанкарбоновую кислоту (2,41 г).
ESI-MS М/Е: 224 [M-Н]-.
Пример приготовления 144: Транс-4-[(N-ацетил-N-метиламино)метил]циклогексанкарбоновая кислота
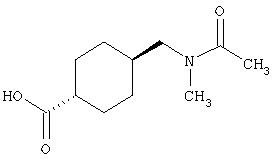
(1) Гидрохлорид метил-транс-4-(аминометил)циклогексанкарбоксилата (5,86 г), полученный в примере приготовления 121(1), растворяют в хлороформе (100 мл), добавляют триэтиламин (12 мл) при охлаждении льдом и затем добавляют ацетилхлорид (2,69 г). Смесь перемешивают при комнатной температуре в течение часа и 40 минут и в реакционный раствор добавляют воду и смесь экстрагируют хлороформом. Органический слой промывают последовательно 10% раствором соляной кислоты, насыщенным рассолом, насыщенным водным раствором гидрокарбоната натрия и насыщенным рассолом, сушат над сульфатом магния и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: гексан/этилацетат =1/1, затем этилацетат), что дает метил-транс-4-(ацетиламинометил)циклогексанкарбоксилат (5,92 г). APCI-MS М/Е: 214 [M+H]+.
(2) Метил-транс-4-(ацетиламинометил)циклогексанкарбоксилат (4,32 г), полученный в (1), растворяют в N,N-диметилформамиде (50 мл) и добавляют последовательно 60% раствор гидрида натрия в масле (1,00 г), йодистый метил (5,91 г) и метанол (5 капель) при охлаждении льдом. После перемешивания в течение 8 часов при комнатной температуре, добавляют еще гидрид натрия (430 мг), йодистый метил (1,5 мл) и метанол (2 капель) и смесь перемешивают в течение 2 часов. В реакционный раствор добавляют воду и смесь экстрагируют этилацетатом. Органический слой промывают водой и сушат над сульфатом натрия. Растворитель удаляют путем выпаривания и полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: смесь гексан/этилацетат =1/2, затем этилацетат), что дает метил-транс-4-[(N-ацетил-N-метиламино)метил]циклогексанкарбоксилат (3,04 г). APCI-MS М/Е: 228 [M+H]+.
(3) Метил-транс-4-[(N-ацетил-N-метиламино)-метил]циклогексанкарбоксилат (3,03 г), полученный в (2), обрабатывают способом, аналогичным описанному в примере приготовления 113(4), что дает названное соединение (2,67 г).
ESI-MS М/Е: 212 [M-Н]-.
Пример приготовления 145: 5-(2-Оксо-пирролидин-1-ил)пентановая кислота
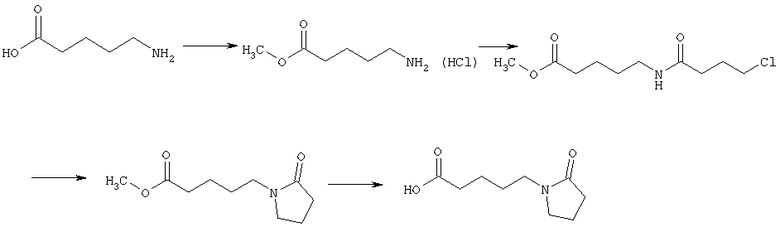
(1) 5-Аминовалериановую кислоту (7,35 г) растворяют в метаноле (50 мл), добавляют по каплям тионилхлорид (4,9 мл) при охлаждении льдом и реакционный раствор нагревают до комнатной температуры и перемешивают в течение 17 часов. Реакционный раствор концентрируют при пониженном давлении и полученный осадок суспендируют в диэтиловом эфире и осадки собирают фильтрованием, что дает гидрохлорид метил-5-аминовалерата (9,93 г). APCI-MS М/Е: 132 [M+H]+.
(2) Гидрохлорид метил-5-аминовалерата (1,68 г), полученный в (1), суспендируют в хлороформе (20 мл). В суспензию добавляют при охлаждении льдом триэтиламин (2,54 г) и затем добавляют по каплям 4-хлорбутирилхлорид (1,55 г). Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 2 часов, ледяную воду выливают в реакционный раствор и смесь экстрагируют хлороформом. Органический слой промывают 10% раствором соляной кислоты, насыщенным водным раствором бикарбонатп натрия и насыщенным рассолом и затем сушат над сульфатом натрия. Остаток выпаривают, чтобы удалить растворитель, при пониженном давлении, что дает метил-5-(4-хлорбутириламино)пентаноат (2,34 г). APCI-MS М/Е: 236/238 [M+H]+.
(3) Метил-5-(4-хлорбутириламино)пентаноат (2,33 г), полученный в (2), растворяют в N,N-диметилацетамиде (20 мл) и постепенно добавляют при охлаждении льдом 60% раствор гидрида натрия в масле (0,47 г). Реакционный раствор нагревают до комнатной температуры, перемешивают в течение 20 часов и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: хлороформ, затем хлороформ/этилацетат =20/1), что дает метил 5-(2-оксо-пирролидин-1-ил)пентаноат (2,15 г). APCI-MS M/E: 200 [M+H]+.
(4) Метил-5-(2-оксо-пирролидин-1-ил)пентаноат (1,00 г), полученный в (3) растворяют в метаноле (20 мл), добавляют 4N водный раствор гидроксида натрия (2,5 мл), реакционный раствор нагревают до комнатной температуры и перемешивают в течение 18 часов. Реакционный раствор промывают диэтиловым эфиром, добавляют 2N соляную кислоту (5,0 мл) и затем концентрируют при пониженном давлении. Полученный осадок экстрагируют хлороформом и сушат над сульфатом натрия. Продукт упаривают, чтобы удалить растворитель, при пониженном давлении, что дает названное соединение (0,90 г). ESI-MS M/E: 184 [M-Н]-
Пример приготовления 146: Метил-2-формил-3-гидроксибензоат и метил-4-формил-3-гидроксибензоат
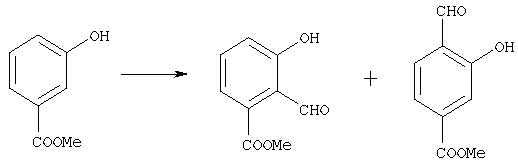
Метил-3-гидроксибензоат (75,5 г) растворяют в трифторуксусной кислоте (2 л), добавляют при комнатной температуре гексаметилентетрамин (141,4 г) и смесь нагревают при температуре кипения с обратным холодильником в течение 3 часов. Реакционный раствор концентрируют при пониженном давлении, в полученный осадок добавляют воду, значение рН смеси доводят до 8 с помощью карбоната калия и гидрокарбоната натрия, разбавляют водой и экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: гексан/этилацетат =8/1, 5/1, затем 2/1), что дает метил-2-формил-3-гидроксибензоат (54,6 г) (ESI-MS м/z: 179 [M-Н]-) и метил-4-формил-3-гидроксибензоат (4,4 г).
(ESI-MS м/z: 179 [M-Н]-).
Пример приготовления 147: Метил-4-циано-3-гидроксибензоат
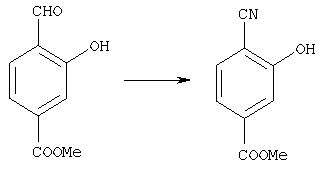
Метил-4-формил-3-гидроксибензоат (1,96 г), полученный в примере приготовления 146, растворяют в муравьиной кислоте (50 мл), добавляют хлорид гидроксиламмония (0,85 г) и формиат натрия (0,85 г) и смесь нагревают при температуре кипения с обратным холодильником в течение 14 часов. Реакционный раствор концентрируют при пониженном давлении, разбавляют водой и экстрагируют этилацетатом. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в смеси хлороформ/диизопропиловый эфир и затем осадки собирают фильтрованием, что дает названное соединение (0,66 г). Потом фильтрат концентрируют при пониженном давлении и полученный осадок очищают с помощью хроматографии на колонке из силикагеля (элюент: гексан/этилацетат =3/2), что дает названное соединение (1,08 г). ESI-MS М/Е: 176 [M-Н]-.
Пример приготовления 148: 2-(2-Циано-5-метоксикарбонилфенокси)-N-(5-хлорпиридин-2-ил)ацетамид
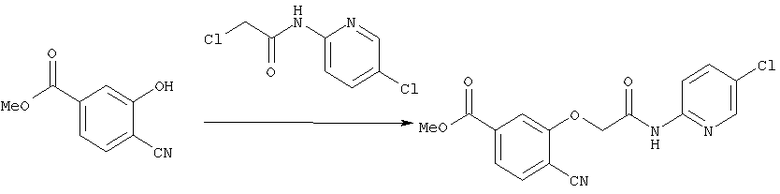
Метил-4-циано-3-гидроксибензоат (655 мг), полученный в примере приготовления 147, растворяют в ацетоне (20 мл), добавляют 2-хлор-N-(5-хлорпиридин-2-ил)ацетамид (897 мг), полученный в примере приготовления 20(1), карбонат калия (773 мг) и иодид натрия (657 мг) и смесь нагревают при температуре кипения с обратным холодильником в течение 40 минут. Реакционный раствор концентрируют при пониженном давлении, добавляют воду и смесь экстрагируют этилацетатом-тетрагидрофураном. Органический слой промывают насыщенным рассолом, сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок суспендируют в смеси хлороформ-диизопропиловый эфир и осадки собирают фильтрованием, что дает названное соединение (1,16 г).
APCI-MS М/Е: 346/348 [M+H]+.
Пример приготовления 149: 3-Амино-6-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
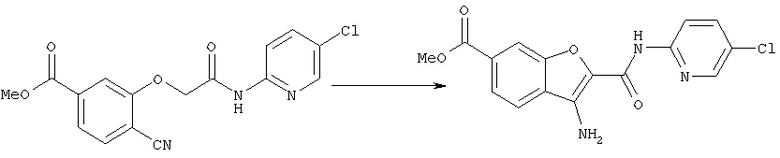
2-(2-Циано-5-метоксикарбонилфенокси)-N-(5-хлорпиридин-2-ил)ацетамид (1,03 г), полученный в примере приготовления 148, растворяют в N,N-диметилацетамиде (10 мл), добавляют карбонат натрия (97 мг) и смесь перемешивают при температуре 100°С в течение 4 часов. Реакционный раствор выливают в воду (50 мл), осадки собирают фильтрованием, промывают водой и этанолом и сушат, что дает названное соединение (839 мг). APCI-MS М/Е: 346/348 [M+H]+.
Пример приготовления 150: Метил-2-циано-3-гидроксибензоат
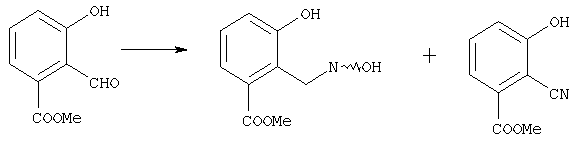
(1) Метил-2-формил-3-гидроксибензоат (9,23 г), полученный в примере приготовления 146, суспендируют в метаноле (150 мл) и водном растворе (15 мл) хлорида гидроксиламмония (3,56 г) и в суспензию добавляют при охлаждении льдом водный раствор (15 мл) ацетата натрия (4,36 г). Смесь нагревают до комнатной температуры, перемешивают в течение 2 часов и затем выпаривают, чтобы удалить метанол. Полученный осадок разбавляют водой и экстрагируют хлороформом. Органический слой сушат над сульфатом натрия и выпаривают, чтобы удалить растворитель, при пониженном давлении, что дает метил-2-гидроксииминометил-3-гидроксибензоат (9,89 г). APCI-MS М/Е: 196 [M+H]+.
(2) Метил-2-гидроксииминометил-3-гидроксибензоат (10,57 г), полученный в (1), суспендируют в хлороформе (100 мл) и добавляют триэтиламин (19,35 г) при охлаждении льдом. При той же температуре в полученный раствор добавляют по каплям трифторуксусный ангидрид (25,40 г) в течение 30 минут. Реакционный раствор перемешивают при комнатной температуре в течение 3 дней, добавляют насыщенный водный раствор гидрокарбоната натрия и экстрагируют хлороформом. Органический слой сушат над сульфатом магния и выпаривают, чтобы удалить растворитель, при пониженном давлении. Полученный осадок растворяют в метаноле (150 мл), добавляют карбонат калия (15,6 г) и смесь перемешивают при комнатной температуре в течение 50 минут. Реакционный раствор разбавляют водой, подкисляют концентрированной соляной кислотой и затем экстрагируют хлороформом. Органический слой сушат над сульфатом магния, растворитель удаляют путем выпаривания и полученный осадок суспендируют в смеси этилацетат-диизопропиловый эфир. Осадки собирают фильтрованием, что дает названное соединение (8,71 г). ESI-MS М/Е: 176 [M-Н]-.
Пример приготовления 151: 2-(2-Циано-3-метоксикарбонилфенокси)-N-(5-хлорпиридин-2-ил)ацетамид
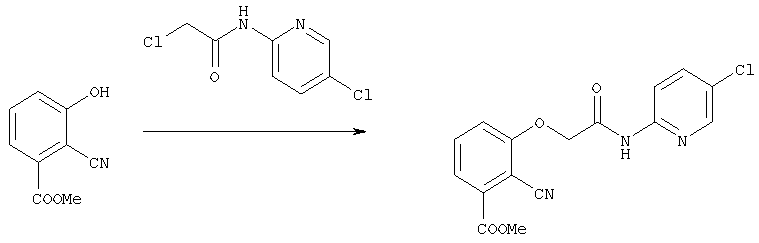
Метил-2-циано-3-гидроксибензоат (1,70 г), полученный в примере приготовления 150, обрабатывают способом, аналогичным описанному в примере приготовления 148, что дает названное соединение (2,69 г). APCI-MS М/Е: 346/348 [M+H]+.
Пример приготовления 152: 3-Амино-4-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
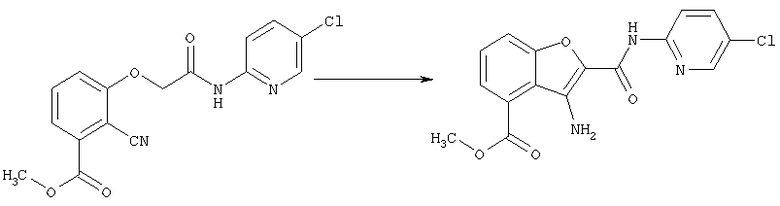
2-(2-Циано-3-метоксикарбонилфенокси)-N-(5-хлорпиридин-2-ил)ацетамид (1,51 г), полученный в примере приготовления 151, обрабатывают аналогичным способом в примере приготовления 149, что дает названное соединение (335 мг). APCI-MS М/Е: 346/348 [M+H]+.
Пример приготовления 153: 3-Амино-5-карбокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
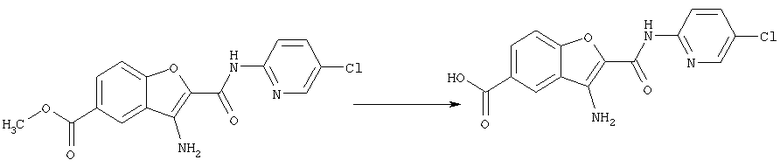
3-Амино-5-метоксикарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (2,01 г) суспендируют в тетрагидрофуране (20 мл) - метанол, добавляют 4N водный раствор гидроксида натрия (5 мл) при охлаждении льдом и реакционный раствор перемешивают при комнатной температуре в течение 13 часов. Реакционный раствор концентрируют при пониженном давлении, полученный осадок разбавляют водой и значение рН смеси доводят приблизительно до 3 с помощью вливания 10% раствора соляной кислоты. Осадки собирают фильтрованием, промывают последовательно водой и этанолом и сушат, что дает названное соединение (1,87 г). ESI-MS М/Е: 330 [M-Н]-.
Примеры приготовления 154-155
Сложный эфир, полученный в примере приготовления 149 или в примере приготовления 152, обрабатывают способом, аналогичным описанному в примере приготовления 153, что дает следующие соединения.
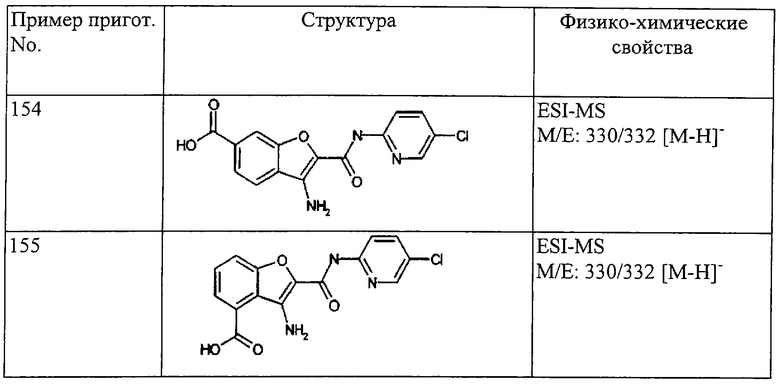
Пример приготовления 156: 3-Амино-5-диметиламинокарбонил-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид
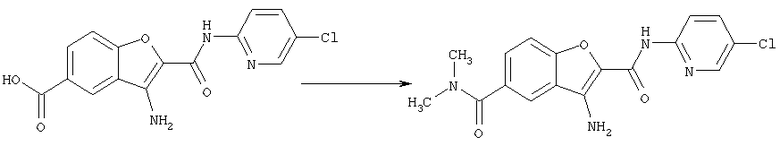
3-Амино-5-карбокси-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамид (1,51 г), полученный в примере приготовления 153, суспендируют в пиридине (15 мл), последовательно добавляют гидрохлорид диметиламина (0,77 г), 1-гидрокси-бензотриазол (1,37 г) и гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (1,79 г) при охлаждении льдом и смесь перемешивают при комнатной температуре в течение 14 часов. Реакционный раствор разбавляют водой (100 мл) и добавляют насыщенный водный раствор гидрокарбоната натрия, доводя значение рН до 8-9. Осадки собирают фильтрованием, промывают последовательно водой и этанолом и затем сушат, что дает названное соединение (1,50 г). APCI-MS M/E: 359/361 [M+H]+.
Примеры приготовления 157-158
Карбоновую кислоту, полученную в примере приготовления 154 или в примере приготовления 155, обрабатывают способом, аналогичным описанному в примере приготовления 156, что дает следующие соединения.
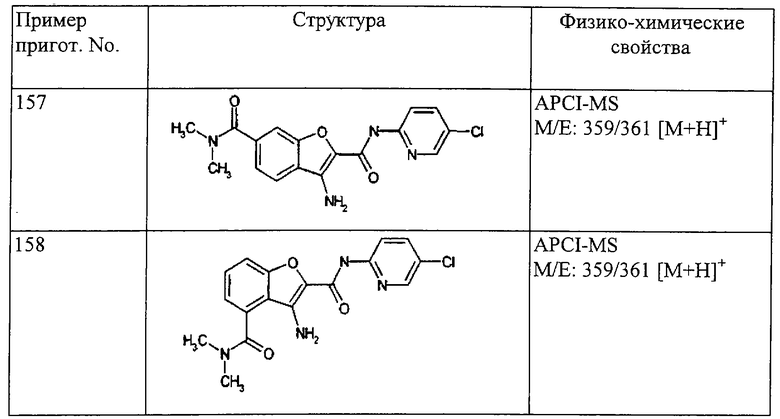
Промышленное применение
Соединение, которое имеет формулу [1], или его фармацевтически приемлемая соль, являются менее токсичными и безопасными и обладают сильным ингибирующим действием на активированный фактор Х коагуляции крови. Соответственно указанное соединение [1], полезно как лекарственное средство для профилактики и лечения заболеваний, вызванных тромбом или эмболом.
Приложение 1
Экспериментальный пример 1
Ингибирующий эффект на активированный фактор Х (FXa) свертывания (коагуляции)
крови.
Приготавливают раствор субстрата, растворением S-2222 (хромогенный субстрат) до конечной концентрации 0,625 мМ в 100 мМ трис-буфере (рН 8,4), содержащем 200 мМ хлорида натрия и 0,1% альбумина сыворотки коровы, и раствор тестируемого соединения в буфере, содержащем 10% диметилсульфоксид. 25 мкл тестируемого раствора добавляют к 200 мкл раствора субстрата. В контроле вместо раствора тестируемого соединения в раствору субстрата добавляют 25 мкл буфера, содержащего 10% диметилсульфоксид.
После предварительного нагревания в течение 3 минут при 37°С в контрольную и опытную пробы добавляют 25 мкл человеческого FXa (Enzyme Research Laboratories, I), растворенного в буфере в концентрации 0,5 Е/мл для инициирования реакции (конечная концентрация FXa: 0,05 Е/мл). После 5-минутного взаимодействия при 37°С непрерывно измеряют поглощение при 405 нм с помощью счетчика 96 луночных планшетов (Spectra МАХ250, Molecular Devices) и увеличение поглощения используют как индекс FXa активности. С целью определения FXa активности тестируемых соединений сравнивают концентрацию тестируемых соединений, ингибирующую FXa на 50% с контрольным образцом (IC50), используя аналитический способ (GraphPad Prism, GraphPad Software, Inc.). Примеры результатов показаны в таблице 1.
Экспериментальный пример 2.
Антитромбический эффект при артериальном тромбозе у крыс
Модель животного с тромбозом артерий выполняют согласно способу, описанному в JP.J.PharmacoL. 68.397 (1995); кратко - индуцируют тромбинообразование в нисходящей абдоминальной аорте 7-8 недельных крыс самцов линии Вистар (Charles River Japan, Inc.). Этот способ обеспечивает прилив крови и гиперкоагуляцию, что приводит к закупорке сосудов.
Тестируемое соединение растворяют или суспендируют в 0,1% водном растворе Nikkol PCO-60 (Nikko chemicals) и вводят опытному животному (перорально) в дозе 10 мл/кг. Контрольное животное получает 0,1% водный раствор Nikkol PCO-60 в тех же условиях, что и опытное. После введения тестируемого соединения индуцируют образование тромбина в крови. Когда уровень тестируемого соединения достигает пика, через 15 минут после введения образовавшийся тромбин удаляют и взвешивают после высушивания. Антитромботическую активность рассчитывают с помощью следующей формулы, где А - вес тромбина в тестируемой группе; В - вес тромбина в контрольной группе. Уменьшение веса тромбина (%)=(1-А/В)×100.
Далее рассчитывают величину дозы, которая уменьшает вес тромбина на 50% ED50 с использованием программного продукта GraphPad Prism (GraphPad Software, Inc.). Результаты представлены в таблице 2.
Антитромботический эффект на артериальном тромбозе у крыс
Модель животного с тромбозом вен выполняют согласно способу, описанному в Eur.J.PharmacoL, 330,151 (1997); кратко - индуцируют тромбинообразование в нисходящей абдоминальной аорте 9-10 недельных крыс самцов линии Вистар (Charles River Japan, Inc.) путем 4-часовой электризации. Тестируемое соединение растворяют или суспендируют в 0,1% водном растворе Nikkol PCO-60 (Nikko chemicals) и вводят опытному животному (перорально) в дозе 10 мл/кг животному. Контрольное животное получает 0,1% водный раствор Nikkol PCO-60 в тех же условиях, что и опытное. После введения тестируемого соединения проводят электризацию животного в течение 4 часов. Тестируемое соединение вводится таким образом, чтобы достигнуть пика его концентрации в плазме крови во время процесса электризации. Электризация индуцирует образование тромбина в крови. Когда уровень тестируемого соединения достигает пика, образовавшийся тромбин удаляют и взвешивают (сырой вес). Антитромботическую активность рассчитывают с помощью следующей формулы, где А - вес тромбина в тестируемой группе; В - вес тромбина в контрольной группе. Уменьшение веса тромбина (%)=(1-A/B)×100.
Далее рассчитывают величину дозы, которая уменьшает вес тромбина на 50% ED50 с использованием программного продукта GraphPad Prism (GraphPad Software, Inc.). Результаты представлены в таблице 2.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ КОНДЕНСИРОВАННОГО ФУРАНА | 2004 |
|
RU2302422C2 |
| НОВОЕ ПИРРОЛИДИНОВОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ АГОНИСТА РЕЦЕПТОРА МЕЛАНОКОРТИНА | 2015 |
|
RU2669938C2 |
| АЗОТСОДЕРЖАЩИЕ НАСЫЩЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2012 |
|
RU2595136C2 |
| ПРОИЗВОДНЫЕ БЕНЗОФУРАНА, СОДЕРЖАЩИЕ ГРУППУ КАРБАМОИЛЬНОГО ТИПА | 2004 |
|
RU2319700C1 |
| НОВОЕ ДИЗАМЕЩЕННОЕ 1,2,4-ТРИАЗИНОВОЕ СОЕДИНЕНИЕ | 2015 |
|
RU2726410C2 |
| ЗАМЕЩЕННЫЕ ИМИДАЗОПИРИДИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ HDM2 | 2013 |
|
RU2690663C2 |
| НОВОЕ ДИЗАМЕЩЕННОЕ 1,2,4-ТРИАЗИНОВОЕ СОЕДИНЕНИЕ | 2015 |
|
RU2693624C2 |
| ПРОИЗВОДНЫЕ 4,5,6,7-ТЕТРАГИДРОБЕНЗИМИДАЗОЛА | 1991 |
|
RU2033414C1 |
| ПРОИЗВОДНОЕ 1-ЗАМЕЩЕННОГО 4-НИТРОИМИДАЗОЛА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2324682C2 |
| КАРБОСТИРИЛЬНОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2430920C2 |
Изобретение относится к новым производным бензофурана формулы [1]:
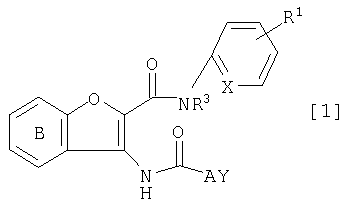
где Х представляет собой группу формулы: -N=или формулы: -СН=; Y представляет собой необязательно замещенную аминогруппу, необязательно замещенную циклоалкильную группу или необязательно замещенную насыщенную гетероциклическую группу; А представляет собой простую связь, углеродную цепь, необязательно имеющую двойную связь внутри или на конце(ах) цепи или атом кислорода; R' представляет собой атом водорода, атом галогена, низшую алкильную группу, низшую алкоксигруппу, цианогруппу или аминогруппу, необязательно замещенную с помощью низшей алкильной группы; кольцо В формулы:
 представляет собой необязательно замещенное бензольное кольцо; и R3 представляет собой атом водорода или низшую алкильную группу, или его фармацевтически приемлемой соли. Изобретение также относится к фармацевтической композиции на основе этих соединений, способу лечения тромбоза и применению. Технический результат - новые соединения для лечения тромбоза. 6 н. и 21 з.п. ф-лы, 2 табл.
представляет собой необязательно замещенное бензольное кольцо; и R3 представляет собой атом водорода или низшую алкильную группу, или его фармацевтически приемлемой соли. Изобретение также относится к фармацевтической композиции на основе этих соединений, способу лечения тромбоза и применению. Технический результат - новые соединения для лечения тромбоза. 6 н. и 21 з.п. ф-лы, 2 табл.
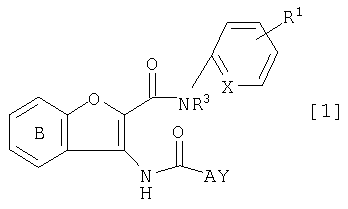
где х представляет собой группу формулы -N= или формулы -СН=;
Y представляет собой необязательно замещенную аминогруппу, необязательно замещенную циклоалкильную группу или необязательно замещенную насыщенную гетероциклическую группу;
А представляет собой простую связь, углеродную цепь, необязательно имеющую двойную связь внутри или на конце(ах) цепи или атом кислорода;
R1 представляет собой атом водорода, атом галогена, низшую алкильную группу, низшую алкоксигруппу, цианогруппу или аминогруппу, необязательно замещенную с помощью низшей алкильной группы;
Кольцо В формулы
представляет собой необязательно замещенное бензольное кольцо; и
R3 представляет собой атом водорода или низшую алкильную группу,
или его фармацевтически приемлемая соль.
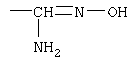
и необязательно замещенная циклоалкильная группа для Y представляет собой циклоалкильную группу, необязательно замещенную с помощью группы, выбранной из необязательно замещенной аминогруппы, необязательно замещенной группой формулы, выбранной из
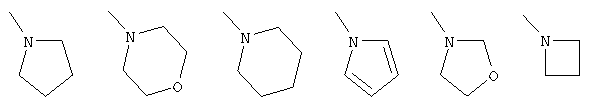
и необязательно замещенной низшей алкильной группы.
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидильной группы, 4,5-дигидроксазолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы, и
(13) оксогруппы;
необязательно замещенная аминогруппа для Y представляет собой аминогруппу,
необязательно замещенную с помощью группы, выбранной из
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы;
необязательно замещенная аминогруппа в качестве заместителя на циклоалкильной группе для Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксильной группы, и
(23) гидрокси-низшей алканоильной группы;
необязательно замещенная группа формулы, выбрана из структуры

и в качестве заместителя на циклоалкильной группе для Y является группа, выбранная из группы структуры

и которая является необязательно замещенной с помощью оксогруппы;
необязательно замещенная низшая алкильная группа в качестве заместителя на циклоалкильной группе для Y представляет собой низшую алкильную группу, необязательно замещенную с помощью группы, выбранной из
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы;
необязательно замещенная низшая алкильная группа в качестве заместителя для кольца В представляет собой низшую алкильную группу, необязательно замещенную с помощью группы, выбранной из
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной с помощью пиперидильной группы и
(8) гидроксильной группы;
необязательно замещенная низшая алкоксигруппа в качестве заместителя для кольца В представляет собой низшую алкоксигруппу, необязательно замещенную с помощью группы, выбранной из
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы -O-NH-C (=NH) NH2;
оксигруппа, замещенная необязательно замещенной с помощью насыщенной гетероциклической группы в качестве заместителя для кольца В представляет собой оксигруппу, замещенную гетероциклической группой, необязательно замещенной с помощью арильной группы;
замещенная карбонильная группа в качестве заместителя для кольца В представляет собой карбонильную группу, замещенную с помощью группы, выбранной из следующих групп:
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы и
(8) низшей алкилпиперазинильной группы;
необязательно замещенная аминогруппа в качестве заместителя для кольца В представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из
(1) низшей алкильной группы,
(2) низшей алкокси-низшей алкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) низшей алканоильной группы,
(5) низшей алкокси-низшей алканоильной группы,
(6) гидрокси-низшей алканоильной группы,
(7) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(8) низшей алканоильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) низшей алканоильной группы,
(9) низшей алкоксикарбонильной группы,
(10) низшей алкоксикарбонильной группы, замещенной с помощью арильной группы,
(11) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(12) низшей алкилсульфонильной группы и
(13) низшей алкилсульфонильной группы, замещенной с помощью морфолинильной группы.
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из следующих групп:
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксазолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы и
(13) оксогруппы.
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
Y представляет собой циклоалкильную группу, необязательно замещенную слудующими группами:
А) аминогруппой, необязательно замещенной с помощью с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы и
(23) гидрокси-низшей алканоильной группы;
В) группой формулы, выбранной из структуры

которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группой, необязательно замещенной группой, выбранной из
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной с помощью пиперидильной группы, и
(8) гидроксильной группы; и
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксаолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы и
(13)оксогруппы.
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной с помощью пиперидильной группы, и
(8) гидроксильной группы; и
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной пиперидильной группы, и
(8) гидроксильной группы; и
Y представляет собой циклоалкильную группу, необязательно замещенную с помощью
следующих групп:
А) аминогруппы, необязательно замещенной с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы, и
(23) гидрокси-низшей алканоильной группы;
В) группы формулы, выбранной из структуры

которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из следующих групп:
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы -O-NH-C(=NH)NH2; и
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы,
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксаолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы, и
(13) оксогруппы.
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы -O-NH-C(=NH)NH2; и
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы; и
(14) группы формулы -O-NH-C(=NH)NH2; и
Y представляет собой циклоалкильную группу, необязательно замещенную с помощью
A) аминогруппы, необязательно замещенной с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы, и
(23) гидрокси-низшей алканоильной группы;
B) группы формулы, выбранной из структуры

которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группы, необязательно замещенной с помощью группы, выбранной из следующих групп:
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы, и
(8) низшей алкил-пиперазинильной группы; и
Y представляет собой насыщенную гетероциклическую группу, необязательно замещенную с помощью группы, выбранной из:
(1) низшей алкильной группы,
(2) низшей алкильной группы, замещенной с помощью пиридильной группы
(3) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(4) пиперидильной группы,
(5) пиперидильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(6) ненасыщенной гетероциклической группы, выбранной из пиридильной группы, пиримидинильной группы, 4,5-дигидроксаолильной группы и тиазолильной группы,
(7) низшей алканоильной группы,
(8) низшей алканоильной группы, замещенной с помощью ди-низшей алкиламиногруппы,
(9) карбонильной группы, замещенной с помощью пиридильной группы,
(10) низшей алкилсульфонильной группы,
(11) низшей алкоксикарбонильной группы,
(12) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы, и
(13) оксогруппы.
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы и
(8) низшей алкил-пиперазинильной группы; и
Y представляет собой аминогруппу, необязательно замещенную с помощью группы, выбранной из следующих групп:
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) низшей алкильной группы и
(3) низшей алкоксикарбонильной группы.
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы, и
(8) низшей алкилпиперазинильной группы; и
Y представляет собой циклоалкильную группу, необязательно замещенную с помощью
следующих групп:
А) аминогруппы, необязательно замещенной с помощью следующих групп:
(1) низшей алкильной группы,
(2) циклоалкильной группы,
(3) гидрокси-низшей алкильной группы,
(4) 1,3-диоксанильной группы, замещенной с помощью низшей алкильной группы,
(5) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алканоильной группы, (с) низшей алканоильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы и (d) низшей алкоксикарбонильной группы,
(6) низшей алкильной группы, замещенной с помощью цианогруппы,
(7) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(8) низшей алкильной группы, замещенной с помощью карбоксильной группы,
(9) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью низшей алкильной группы,
(10) низшей алкильной группы, замещенной с помощью арильной группы,
(11) низшей алкильной группы, замещенной с помощью пиридильной группы,
(12) низшей алкоксикарбонильной группы,
(13) низшей алканоильной группы, замещенной с помощью ди-низшей алкильной аминогруппы,
(14) низшей алканоильной группы,
(15) пиримидинильной группы,
(16) низшей алканоильной группы, замещенной с помощью морфолинильной группы,
(17) низшей алкилсульфонильной группы,
(18) карбамоильной группы, замещенной с помощью низшей алкильной группы,
(19) карбонильной группы, замещенной с помощью арильной группы,
(20) низшей алканоильной группы, замещенной с помощью низшей алкоксигруппы,
(21) низшей алканоильной группы, замещенной с помощью низшей алканоилоксигруппы,
(22) арильной группы, замещенной с помощью гидроксигруппы, и
(23) гидрокси-низшей алканоильной группы;
В) группы формулы, выбранной из структуры

которая является необязательно замещенной с помощью оксогруппы; или
С) низшей алкильной группой, необязательно замещенной с помощью группы, выбранной из
(1) оксопирролидинильной группы,
(2) оксоморфолинильной группы и
(3) аминогруппы, необязательно замещенной с помощью (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы.
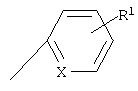
представляет собой группу формулы
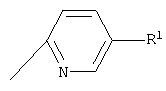
и группа формулы

представляет собой группу формулы
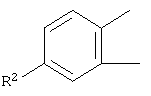 или
или 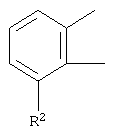
или R1 представляет собой атом галогена или низшую алкильную группу;
R2 представляет собой группу, выбранную из следующих групп:
A) атом водорода,
B) низшая алкильная группа, необязательно замещенная с помощью группы, выбранной из:
(1) низшей алкоксикарбонильной группы,
(2) карбоксильной группы,
(3) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкоксигруппы,
(4) карбонильной группы, замещенной с помощью морфолинильной группы,
(5) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(6) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) карбонильной группы, замещенной с помощью гидроксильной группы, замещенной пиперидильной группы и
(8) гидроксильной группы;
C) низшая алкоксигруппа, необязательно замещенная с помощью группы, выбранной из:
(1) карбоксильной группы,
(2) низшей алкоксикарбонильной группы,
(3) низшей алкоксигруппы,
(4) гидроксильной группы,
(5) аминооксигруппы, необязательно замещенной с помощью низшей алкоксикарбонильной группы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) карбонильной группы, замещенной с помощью морфолинильной группы, пиперидильной группы или пирролидинильной группы,
(8) карбонильной группы, замещенной с помощью гидроксипиперидильной группы,
(9) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(10) пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(11) карбонильной группы, замещенной с помощью низшей алкилпиперазинильной группы,
(12) аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы,
(13) карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкокси-низшей алкильной группы, (с) низшей алкильной группы, замещенной с помощью гидроксильной группы и (d) низшей алкильной группы, замещенной с помощью ди-низшей алкиламиногруппы, и
(14) группы формулы -O-NH-C(=NH)NH2; или
D) карбонильная группа, замещенная с помощью группы, выбранной из
(1) низшей алкоксигруппы,
(2) гидроксильной группы,
(3) аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксигруппы, (с) низшей алкокси-низшей алкильной группы, (d) гидрокси-низшей алкильной группы, (е) низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы, (f) низшей алкильной группы, замещенной с помощью арильной группы и (g) низшей алкильной группы, замещенной с помощью пиридильной группы,
(4) морфолинильной группы, пирролидинильной группы, пиперидильной группы или тиоморфолинильной группы,
(5) гидроксипиперидильной группы,
(6) пиперидильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(7) пирролидинильной группы, замещенной с помощью гидрокси-низшей алкильной группы, и
(8) низшей алкил-пиперазинильной группы;
А представляет собой простую связь; и
R3 представляет собой атом водорода.
(1) пиперидильной группы, замещенной с помощью низшей алкильной группы,
(2) циклоалкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, (b) низшей алкоксикарбонильной группы и (с) низшей алканоильной группы, (3) циклоалкильной группы, замещенной с помощью группы формул, выбранных из структуры
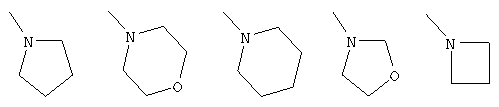
которая является необязательно замещенной с помощью оксогруппы,
(4) циклоалкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алканоильной группы и (b) низшей алкоксикарбонильной группы и
(5) циклоалкильной группы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы; и
R2 представляет собой группу, выбранную из
(1) атома водорода,
(2) цианогруппы,
(3) аминогруппы, необязательно замещенной с помощью низшей алкильной группы,
(4) гидроксильной группы,
(5) низшей алкоксигруппы,
(6) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы,
(7) низшей алкоксигруппы, замещенной с помощью гидроксильной группы,
(8) низшей алкоксигруппы, замещенной с помощью аминогруппы, необязательно замещенной с помощью низшей алкильной группы,
(9) низшей алкоксикарбонильной группы,
(10) карбоксильной группы,
(11) аминокарбонильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы, и (b) гидрокси-низшей алкильной группы,
(12) морфолинилкарбонильной группы, пирролидинилкарбонильной группы, пиперидилкарбонильной группы или тиоморфолинилкарбонильной группы,
(13) пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы или пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы,
(14) низшей алкильной группы,
(15) низшей алкильной группы, замещенной с помощью низшей алкоксикарбонильной группы,
(16) карбокси-низшей алкильной группы,
(17) низшей алкильной группы, замещенной с помощью карбамоильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) гидрокси-низшей алкильной группы,
(18) низшей алкильной группы, замещенной с помощью морфолинилкарбонильной группы,
(19) низшей алкильной группы, замещенной с помощью пиперидилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы или низшей алкильной группы, замещенной с помощью пирролидинилкарбонильной группы, замещенной с помощью гидрокси-низшей алкильной группы, или
(20) гидрокси-низшей алкильной группы.

которая является необязательно замещенной с помощью оксогруппы или циклоалкильной группы, замещенной с помощью аминогруппы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) низшей алканоильной группы; и
R2 представляет собой группу, выбранную из следующих групп:
(1) атома водорода,
(2) аминогруппы замещенной карбонильной группы, необязательно замещенной с помощью группы, выбранной из (а) низшей алкильной группы и (b) низшей алкокси-низшей алкильной группы,
(3) низшей алкоксикарбонильной группы,
(4) морфолинилкарбонильной группы, пирролидинилкарбонильной группы, пиперидилкарбонильной группы или тиоморфолинилкарбонильной группы,
(5) низшей алкильной группы, замещенной с помощью низшей алкильной группы, замещенной карбамоильной группы,
(6) карбокси-низшей алкильной группы,
(7) низшей алкильной группы, замещенной с помощью морфолинилкарбонильной группы, и
(8) гидрокси-низшей алкильной группы.
R2 представляет собой группу, выбранную из
(1) атома водорода,
(2) гидрокси-низшей алкильной группы,
(3) карбокси-низшей алкильной группы,
(4) низшей алкоксигруппы, замещенной с помощью низшей алкоксигруппы или
(5) карбонильной группы, замещенной с помощью группы, выбранной из (а) аминогруппы, необязательно замещенной с помощью низшей алкильной группы и (b) морфолинильной группы.
(1) циклоалкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, имеющей от 1 до 3 атомов углерода,
(2) циклоалкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алканоильной группы, имеющей от 1 до 2 атомов углерода,
(3) циклоалкильной группы, замещенной с помощью пирролидин-1-ильной группы, необязательно замещенной с помощью оксогруппы,
(4) циклоалкильной группы, замещенной с помощью пиперидин-1-ильной группы, необязательно замещенной с помощью оксогруппы,
(5) циклоалкильной группы, замещенной с помощью морфолин-4-ильной группы, необязательно замещенной с помощью оксогруппы,
(6) циклоалкильной группы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алкильной группы, имеющей от 1 до 3 атомов углерода, или
(7) циклоалкильной группы, замещенной с помощью низшей алкильной группы, замещенной с помощью аминогруппы, замещенной с помощью низшей алканоильной группы, имеющей от 1 до 2 атомов углерода.
транс-5-диметиламинокарбонил-3-[4-(N-формил-N-метиламино) циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида;
транс-3-[4-(N-ацетил-N-метиламино)циклогексилкарбониламино]-5-(2-гидроксиэтил)-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида;
транс-5-(морфлин-4-илкарбонил)-3-[4-(2-оксо-пирроридин-1-ил)циклогексилкарбониламино]-N-(5-хлорпиридин-2-ил)бензофуран-2-карбоксамида; и
транс-3-(4-диметиламиноциклогексилкарбониламино)-N-(5-хлорпиридин-2-ил)-бензофуран-2-карбоксамида или его фармацевтически приемлемая соль.
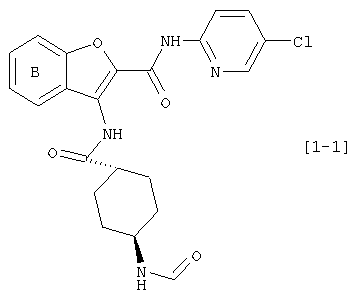
где символы имеют те же значения, как определено выше,
или его фармацевтически приемлемая соль.
| Giovanni Viti, J., Heterocyclic Chem.,1990, 27, p.1369-75 | |||
| Способ извлечения серы и битума из битуминозного серного сырья | 1934 |
|
SU39118A1 |
| КАРБОКСАМИДЫ БЕНЗОФУРАНА И ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1997 |
|
RU2162467C2 |
| АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ТРОМБОТИЧЕСКИХ ЗАБОЛЕВАНИЙ | 1995 |
|
RU2156763C2 |
| RU 95110110 A1, 27.12.1996 | |||
| СПОСОБ ПОЛУЧЕНИЯ 5-ОКСИПРОИЗВОДНЫХ 2,3-ДИГИДРО-4,6,7-ТРИМЕТИЛ-2-(RS)-БЕНЗОФУРАНУКСУСНОЙ КИСЛОТЫ | 1991 |
|
RU2035459C1 |
| RU 2070884 C1, 27.12.1996. | |||
Авторы
Даты
2006-10-27—Публикация
2003-03-27—Подача