Изобретение описывает новый процесс получения 5-оксипроизводных -2,3-дигидро-4,6,7-триметил-2-(RS)-бензофурануксусных кислот. Известны дигидробензофурановые структуры общей формулы I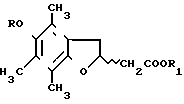 (I) R водород, остаток моно- или дикарбоновой кислоты, либо низший алкил;
(I) R водород, остаток моно- или дикарбоновой кислоты, либо низший алкил;
R1 водород, алкил, эфирный алкил, алкиламин или циклоэфирный алкил. Эти соединения, особенно 2,3-дигидро-5-ацетокси-4,6,7-триметил-2-(RS)-бензофурануксусная кислота и 2,3-дигидро-5-метокси-4,6,7-триметил-2-(RS)-бензофурануксусная кислота, как оказалось эффективны при лечении многих видов воспаления слизистых мембран в дыхательных системах со значительным антиоксидантным и радикалозахватным действием.
Изобретение это новый способ синтеза 2,3-дигидро-4,6,7-триметил-2-(RS)-бензофурануксусной кислоты, обозначенный здесь и далее как IRFI 005 и 5-оксипроизводных-2,3-дигидро-4,6,7-триметил-2-(2RS)-бензофурануксусной кислоты общей формулы II: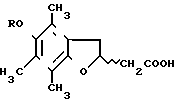 (II) где R водород,
(II) где R водород,
СОR2 ацил, в котором R2 это линейный или разветвленный алкил с числом атомов углерода от 1 до 4,
Новый процесс, с учетом вышесказанного, отличается тем, что субстрат более легкодоступен, требуется меньше стадий, следовательно, получение продукта становится легче и выгоднее. Множество токсичных реагентов и катализаторов также исключено, что делает процесс безопаснее. Этот процесс также легче воспроизводим, что облегчает его применение в промышленном масштабе.
Описываемый процесс состоит во взаимодействии между 4-(2,5-дигидрокси-3,4,6-триметилфенил)-2-бутановой кислотой (особенно ее метиловым эфиром) формулы III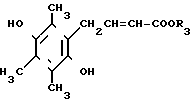 (III) в которой R3-водород, или низший алкил, особенно метил) и водного раствора щелочи, такой как КОН, в присутствии восстанавливающего агента, такого как Na2S2O4 при соответствующей температуре (обычно при температуре кипения раствора) за время от 1 до 12 ч.
(III) в которой R3-водород, или низший алкил, особенно метил) и водного раствора щелочи, такой как КОН, в присутствии восстанавливающего агента, такого как Na2S2O4 при соответствующей температуре (обычно при температуре кипения раствора) за время от 1 до 12 ч.
Соединения формулы III могут быть получены как описано Mhorner and A. Nissen в ДЕ 0,5%3.010-474 (1 октября 1984) с использованием алкилирования по Фриделю-Крафтсу триметилгидрохинона подходящим производным 2- или 3-бутановой кислоты как, например, 4-бром-2-бутаноат в присутствии одного или более неорганических кислых катализаторов. Соединения III могут использоваться после реакции алкилирования для циклизации без выделения и очистки. Таким образом, они могут представлять собой смесь с такими органическими продуктами, как триметилгидрохинон, и такими неорганическими продуктами, как хлорид цинка 2,3-динидро-5-гидрокси-4,6,7-триметил-2-(RS)-бензофурануксусная кислота образуется путем реакции циклизации и выделяется при подкислении реакционной смеси, а затем экстрагируется органическим растворителем. Этот продукт затем может быть отделен от некислотных примесей экстракцией его натриевой соли водным раствором бикарбоната натрия, или кристаллизацией одной из его солей с использованием органического основания, такого как циклогексиламин. Недиссоциированная форма IRFI 005 получена при осаждении в водном растворе кислоты.
Фенольная группа в IRFI 005 ацилируется при диспергировании 2,3-дигидро-5-гидрокси-4,6,7-триметил-2-(RS)-бензофурануксусной кислоты в подходящем количестве ангидрида кислота (особенно уксусного ангидрида с добавкой сильной минеральной кислоты (такой как серная) в качестве катализатора, после разбавления инертным растворителем. Реакционную смесь выдерживают при соответствующей температуре (обычно 60-90о С) от 0,5 до 12 ч.
После разбавления водой 2,3-дигидро-5-ацилокси-4,6,7-триметил-2-(RS)-бензофурануксусная кислота осаждается и может быть очищена кристаллизацией из подходящего растворителя или их смеси и обработана одним из обычных обеспечивающих агентов.
Алкилирование фенольного гидроксила IRFI 005 проводится при растворении в водно-щелочном растворе и постепенном прибавлении диалкил сульфата (особенно диметилсульфата). По окончании реакции 2,3-дигидро-5-алкокси-4,6,7-триметил-24(RS)-бензофурануксусная кислота выделяется при подкислении смеси. Как альтернатива, может быть использован двухстадийный процесс, включающий:
а) образование 2,3-дигидро-5-алкокси-4,6,7-триметил-2-(RS)-бензофурануксусного алкила при реакции IRFI 005 и избытка подходящего галоидалкила (особенно метилиодида) в таком органическом растворителе, как диметилформамид в присутствии акцептора кислоты, такого как карбонат калия;
б) гидролиз полученного таким образом сложного эфира до 2,3-дигидро-5-алкокси-4,6,7-триметил-2-(RS)-бензофурануксусной кислоты при обработке щелочью в водно-органическом растворителе. Продукт очищают кристаллизацией из подходящего растворителя их из смеси и обрабатывают обычным обесцвечивающим агентом.
П р и м е р 1. 1,2,3-дигидро-5-4,6,7-триметил-2-(RS)-бензофурануксусная кислота (IRFI 005).
Из смеси 152 г триметилгидрохинона, 23 г безводного хлорида цинка и 100 г метил 4-бром-2-бутаноата (транс и цис) в 1 л н-гептана после реакции в течение 2 ч при кипении в инертной атмосфере удаляют растворитель. Остаток обрабатывают 2,2 л 20%-ного раствора гидрата калия, содержащего 146 г гипосульфита натрия, и полученную смесь кипятят 3 ч в инертной атмосфере. После охлаждения добавляют раствор НСl до рН 3 и экстрагируют смесь этилацетатом. После промывки органического экстракта раствором хлорида натрия его обрабатывают насыщенным водным раствором бикарбоната натрия. Водный раствор, содержащий продукт, затем концентрируют и добавляют соляную кислоту до полного осаждения IRFI 005. Продукт (126 г) затем фильтруют и сушат кристаллизацией из н-гексана -этилацетата, т.пл. 176-7о С, ИК (КВr) 3374 (ОН), 1705 (СООН), ПМР (ДМСО d6) 12,2 (IH, sb) 7,4 (IH, sb) 5,35 -4,85 (IH, м) м 3,5-2,8 (2Н, м), 2,75-2,55 (2Н, д) 2,1 (6Н, с) 2,0 (3Н, с). Элементный анализ для С13Н16О4 (МВ 236, 27) выч. С 66,09% Н 6,83% (найдено С 66,1% Н 6,91%).
П р и м е р 2. 2,3-дигидро-5-ацетокси-4,6,7-триметил-2-(RS)-бензофурануксусная кислота.
Раствор 0,1 мл концентрированной серной кислоты в 5 мл уксусной кислота понемногу прибавляют к смеси 20 г 2,3-дигидро-5-гидрокси-4,6,7-триметил-2-(RS)-бензофурануксусной кислоты и 47 мл уксусного ангидрида.
Полученный раствор нагревают при 80о С 4 ч в инертной атмосфере. После охлаждения и постепенного добавления воды продукт осаждается, его фильтруют и сушат в вакууме. Его чистят с использованием агента с последующей кристаллизацией из толуола. Получают 16,8 г белого кристаллического вещества т.пл. 167-8о С, ИК(KBr) 1752 (АсО) 1710 (СООН) ПМР (СДСl3) 10,3 (IH, С), 5,3-4,8 (IH, м) 3,6-2,7 (4Н, м) 2,3 (3Н, с) 2,1 (3Н, с), 2,0 (6Н, с). Элементный анализ для С15Н18О5 вычислено: С 64,74% Н 6,52% найдено: С 64,74 Н 6,90%
П р и м е р 3. 2,3-дигидро-5-метокси-4,6,7-триметил-2-(RS)-бензофурануксусная кислота.
3,45 г карбоната калия и 1,5 мл метилиодида прибавляют к раствору 2,0 г 2,3-дигидро-5-гидрокси-4,6,7-триметил-2-(RS)-бензофурануксусной кислоты в 15 мл диметилформамида. Реакционную смесь перемешивают при комнатной температуре в инертной атмосфере 24 ч, затем разбавляют водой и экстрагируют этилацетатом. Органический раствор упаривают и сушат в вакууме, получая таким образом 2,4 г грязного 2,3-дигидро-5-гидрокси-4,6,7-триметил-2-бензофуранацетата (ИК/1740 см). Этот продукт затем растворяют в 10 мл ацетона и обрабатывают 34 г Iн. раствора гидроксида натрия при кипении 1 ч. Осадок, образующийся после охлаждения и подкисления смеси, фильтруют, сушат в вакууме, обрабатывают активированным углем и кристаллизуют из н-гексан/бензол, получая 1,8 г белых кристаллов 2,3-дигидро-5-метокси-4,6,7-триметил-2-(RS)-бензофурануксусной кислоты т.пл 135-136о С, ИК (KBr) 1702 см (СООН) ПМР (СДСl3) 10,2 (IH, С) 5,2-4,8 (IH, м) 3,6 (3Н, с) 3,4-2,5 (4Н, м) 2,1 (6Н) 2,05 (3Н, с).
Элементный анализ для С14Н18О4 (МВ 250 29), вычислено: С 67,18% Н 7,25% найдено: С 67,41% Н 7,42.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2,3-ДИГИДРО-5-ОКСИ-4,6,7-ТРИМЕТИЛБЕНЗОФУРАНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2068845C1 |
| ХИНОНОВЫЕ ПРОИЗВОДНЫЕ | 1992 |
|
RU2054412C1 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛОНА, СМЕСИ ИХ ИЗОМЕРОВ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ В КАЧЕСТВЕ АНТАГОНИСТА РЕЦЕПТОРА 5-HT*00I*00A И 5-НТ*002 | 1992 |
|
RU2096411C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ 7-НИТРО-8-ОКСИХИНОЛИНА | 1972 |
|
SU334697A1 |
| ТИАЗОЛИДИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, СПОСОБ СНИЖЕНИЯ СОДЕРЖАНИЯ САХАРА В КРОВИ У МЛЕКОПИТАЮЩИХ | 1992 |
|
RU2095354C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1994 |
|
RU2098411C1 |
| Способ получения производных дигидробензопирана или дигидробензотиопирана или их фармацевтически приемлемых солей | 1983 |
|
SU1321375A3 |
| N-ИМИДАЗОЛИЛЬНЫЕ ПРОИЗВОДНЫЕ ЗАМЕЩЕННЫХ АЛКОКСИИМИНОТЕТРАГИДРОНАФТАЛИНОВ ИЛИ ХРОМАНОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ АКТИВНОСТЬ АНТАГОНИСТА ТРОМБОКСАНА И ИНГИБИТОРА ТРОМБОКСАНСИНТАЗЫ | 1992 |
|
RU2083566C1 |
| СОЕДИНЕНИЕ ЦЕФЕМА И ЕГО ФАРМАЦЕВТИЧЕСКИ ИЛИ ВЕТЕРИНАРНО ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2074186C1 |
| ПРОИЗВОДНЫЕ ТИАЗОЛИДИН-2,4-ДИОНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2103265C1 |
Использование: в медицине в качестве антиишемического средства. Сущность изобретения: продукт-5-оксипроизводные 2,3-дигидро-4,6,7-триметил-2-RS-бензофурануксусной кислоты ф-лы I, где R-атом водорода или -COR2 ацил, где R2- линейный или разветвленный C1-C4 алкил. Реагент 1: производные 4-(2,5-дигидрокси-3,4,6-триметилфенил)-2-бутеновой кислоты ф-лы II, где R3- H или низший алкил, и конфигурация двойной связи может быть или транс-, или цис-. Способ позволяет упростить и удешевить процесс за счет уменьшения числа стадий. Структура соединений ф-л I и II: 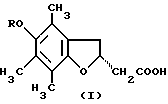
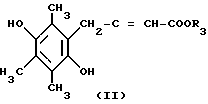 .
.
СПОСОБ ПОЛУЧЕНИЯ 5-ОКСИПРОИЗВОДНЫХ 2,3-ДИГИДРО-4,6,7-ТРИМЕТИЛ-2-(RS)-БЕНЗОФУРАНУКСУСНОЙ КИСЛОТЫ общей формулы I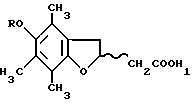
где R водород, линейный или разветвленный С1 С4-алкил, или COR2-ацил, в котором R2 линейный или разветвленный С1 С4-алкил,
отличающийся тем, что производные 4-(2,5-дигидрокси-3,4,6-триметилфенил)-2-бутеновой кислоты общей формулы II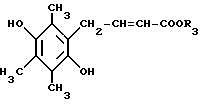
где R3 водород или низший алкил,
особенно метил и конфигурация двойной связи может быть или транс-, или цис-,
подвергают взаимодействию с водным раствором гидроксида щелочного металла в присутствии восстанавливающего агента, такого, как гипосульфит натрия, при кипячении подкислением реакционной смеси, экстракцией полученного продукта органическим растворителем, таким, как этилацетат, и переводом его в соль действием подходящего неорганического или органического основания с последующей обработкой ее водным раствором минеральной кислоты, фильтрацией, сушкой и, в случае необходимости, перекристаллизацией выпавшего осадка и получением соединения формулы I, где R водород, которое при необходимости подвергают реакции с подходящим ангидридом в присутствии каталитического количества сильной минеральной кислоты, такой как серная кислота, необязательно разбавленной инертным растворителем, таким, как уксусная кислота, и выделяют соединение формулы I, где R линейный или разветвленный ацил с числом атомов углерода 2 5, например ацетил, или соединение формулы I, где R водород, подвергают обработке водным щелочным раствором реагента, выбранного из подходящего диалкилсульфата, имеющего 1 4 атома углерода, и алкилгалогенидом в растворе органического растворителя, выбранного из ацетона и диметилформамида, при температуре 0 100oС в присутствии акцептора кислоты, выбранного из карбоната калия и гидроксида калия, с последующим гидролизом полученного продукта гидроксидом щелочного металла в водно-органическом растворителе и выделением соединения формулы I, где R - линейный или разветвленный С1 С4-алкил.
| Отводок для приводных ремней | 1930 |
|
SU21603A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Механическая топочная решетка с наклонными частью подвижными, частью неподвижными колосниковыми элементами | 1917 |
|
SU1988A1 |
Авторы
Даты
1995-05-20—Публикация
1991-03-11—Подача