Область техники, к которой относится изобретение
Настоящее изобретение относится к области химии, в частности к получению первичных аминов каталитическим гидрированием нитрилов.
Уровень техники
Гидрирование нитрилов до аминов приобретает важное техническое значение по причине все более расширяющегося применения аминов в производстве, например, органических растворителей, агрохимикатов, фармацевтических препаратов, поверхностно-активных веществ и особенно промежуточного продукта полиамида-6,6. Гидрирование проводится, как правило, в жидкой фазе над никелевыми катализаторами Ренея при повышенных температуре и давлении водорода, при этом для повышения выхода первичного амина за счет ингибирования образования вторичных и третичных аминов добавляется аммиак.
Гидрирование нитрилов до первичных аминов описывается, например, в следующих патентах и научных статьях.
E.J.Schwoegler и H.Adkins, J. Am. Chem. Soc. 61, 3499 (1939) выдвинули предположение, а позднее смогли показать, что при добавлении достаточного количества аммиака в процессе гидрирования нитрила образование вторичного амина сильно ингибируется и за счет этого, в основном, обеспечивается получение первичного амина.
В US 2165515 описан способ получения первичных аминов каталитическим гидрированием нитрилов с применением кобальта или кобальта, усиленного барием или марганцем.
S.Sakakibara et al., J. Chem. Soc. Japan, Ind. Chem. Sect., 56, 497 (1953) раскрывают способ получения первичных аминов, например додециламина, гидрированием нитрила, такого как лауронитрил, аммиаком с применением никелевых катализаторов Ренея.
В US 3574754 описан способ получения первичных аминов гидрированием нитрилов аммиаком с применением никелевых катализаторов Ренея.
В US 4739120 описан способ гидрирования нитрилов до первичного амина с применением родиевого катализатора. Реакция проводится в присутствии двухфазной системы растворителей, состоящей из водной фазы и не смешивающейся с водой органической фазы.
M.Besson et al., Stud. Surf. Sci. Catal, том 59, "Heterogeneous Catalysis and Fine Chemicals II", изд. M. Guisnet et al., 1991, с.113-120 раскрывают способ получения первичных аминов из нитрилов в присутствии циклогексана с применением никелевого катализатора Ренея, легированного молибденом или хромом.
В ЕРА 0547505 описан способ получения додециламина каталитическим гидрированием лауронитрила в присутствии аммиака с применением соосажденных на носителе магния-никелевого катализатора.
В PL 51350 для гидрирования алифатических нитрилов и, в частности, лауронитрила используется никелевый катализатор. С целью ингибирования образования вторичного амина добавляется аммиак.
В JP 7941804 описан способ получения первичных аминов гидрированием нитрила в смесях низшего спирта с циклическим углеводородом в присутствии никелевого катализатора Ренея, модифицированного гидроксидами щелочного или щелочноземельного металла и хромом.
В JP 6032767 описан способ гидрирования нитрилов до первичного амина с применением никелевого катализатора Ренея в присутствии аммиака.
D.Djaouadi et al., Catal. Org. Reactions, 423 (1995) получали никелевый катализатор Ренея, легированный хромом или железом, путем выщелачивания из интерметаллических сплавов типа Ni40Al60 или Ni25Al75. Селективное гидрирование валеронитрила до соответствующего первичного амина проводили в циклогексане в автоклаве с мешалкой. Достигаемое за счет легирования улучшение селективности к первичному амину объясняется, главным образом, снижением скорости гидрирования образующегося в качестве промежуточного продукта вторичного амина, что благоприятствует обратным реакциям.
S.Xie et al., Appl. Catal. A: General, 189, 45 (1999) сообщают, что благодаря добавлению аммиака селективность к первичному амину при селективном гидрировании стеаронитрила над аморфными Ni-В/SiO2-катализаторами значительно повышалась, хотя и наблюдалось некоторое снижение активности. Аморфная структура катализатора и используемого для легирования бора играет ключевую роль в повышении активности гидрирования и селективности к первичным аминам. Однако при использовании SiO2, легированного KNO3, не отмечалось выраженного промотирующего эффекта.
Для улучшения селективности при гидрировании органических нитрилов до аминов использовали также добавки гидроксидов щелочных металлов. Согласно Т.А.Johnson et al., Proceedings of the "18th Conference on Catalysis of Organic Reactions", изд. M.E.Ford, 2000, доклад 13 селективное гидрирование нитрилов можно проводить с применением катализаторов из губчатого никеля и кобальта, модифицированных гидроксидом лития.
В US 5874625 описан способ каталитического гидрирования органических нитрилов до первичных аминов с применением суспензии никелевого катализатора Ренея и водного гидроксида щелочного металла, при этом количество воды, вносимое с никелевым катализатором Ренея и водным гидроксидом щелочного металла, составляет примерно от 0,1 до 0,3%. Находящаяся в автоклаве партия насыщалась водородом, а затем нагревалась до конечной температуры примерно 110°С.
В US 5777166 описан способ гидрирования нитрилов до аминов, согласно которому: а) катализатор типа никеля Ренея легируется, по меньшей мере, одним дополнительным металлом из группы IVб Периодической системы элементов, при этом используется практикуемая в металлургии технология предварительного легирования Ni/Al/легирующий элемент, а массовое соотношение между легирующим элементом и Ni составляет от 0,05 до 10%; б) на катализатор можно воздействовать нитрилом в жидкой реакционной среде, в которой нитрил растворим, вместе с, по меньшей мере, одним неорганическим основанием из группы, включающей LiOH, NaOH, КОН, RbOH и CsOH, благодаря чему достигается гидрирование нитрила.
В US 5869653 описан способ каталитического гидрирования нитрилов, при котором нитрил в присутствии катализатора из губчатого кобальта в условиях отсутствия аммиака приводится в контакт с водородом с целью превращения нитрильной группы в первичный амин, при этом улучшение способа гидрирования состоит в том, что гидрирование проводится в присутствии катализатора из губчатого кобальта, обработанного каталитически эффективным количеством гидроксида лития, а превращение проводится в присутствии воды.
В WO 01/66511 раскрывается способ гидрирования нитрилов до аминов, при котором не проводится модификация катализатора гидрирования перед реакцией гидрирования.
С целью повышения селективности никелевых катализаторов Ренея для получения аминов при алкилировании аммиака или алкиламинов спиртами вводятся также карбонаты щелочных металлов. В FR 2351088, DE 2621449, DE 2625196 и DE 2639648 описан способ получения третичных аминов алкилированием вторичных аминов спиртами с отщеплением воды в жидкой фазе в присутствии катализатора гидрирования/дегидрирования, такого как никель Ренея или кобальт Ренея, и одного или более оснований щелочных или щелочноземельных металлов. Так, например, смесь из 774 кг н-додеканола, 500 кг этилбензола, 10 кг Na2СО3 и 300 кг никеля Ренея нагревали до 130-135°С и в условиях циркуляции воды подавали водород и диметиламин до тех пор, пока не выделилось теоретическое количество H2O, после чего катализатор отфильтровывали, а фильтрат очищали дистилляцией, что обеспечило получение 80% RNMe2, 15% R2NMe и 5% R3N (R=н-додецил).
В DE 2645712 описан способ получения вторичных аминов алкилированием аммиака спиртами в присутствии катализатора гидрирования/дегидрирования и основания щелочного или щелочноземельного металла. Так, например, в оборудованный дефлегматором реактор со стеариловым спиртом, никелем Ренея и Na2СО3 при 90-140°С и непрерывном удалении Н2O при атмосферном давлении подавали аммиак, что обеспечивало получение >95% дистеариламина.
Kalina М. и Pashek Yu. (Kinetika i Kataliz, 10, 574, 1969) сообщили о применении кобальтового и никелевого катализаторов, модифицированных Na2СО3, для жидкофазного гидрирования нитрила пальмитиновой кислоты. Добавление карбоната натрия в реакционную смесь с массовым отношением Na2CO3/катализатор/нитрил, равным 5/5/100, при 150°С и давлении водорода 50 бар приводило к снижению селективности ко вторичному амину. Селективность ко вторичному амину при 50% степени превращения над Со, Ni, Со+Na2СО3, Ni+Na2СО3-катализаторами составила соответственно 17,4, 20,1, 11,0 и 12,2%.
Для получения несимметричных алифатических вторичных алкиламинов применялась каталитическая система, содержащая никель на носителе и карбонат щелочного металла. В US 5254736 и ЕР 0526318 описан способ получения вторичных метилалкиламинов общей формулы R-NH-СН3, в которой R обозначает алифатическую цепь С10-С22, реакцией аминирования между спиртом и моноалкиламином. Реакция аминирования проводилась с применением никелевого катализатора на носителе в присутствии карбоната щелочного металла, предпочтительно карбоната калия, при массовом отношении карбонат калия/никелевый катализатор от 1:4 до 1:1 и давлении водорода от 10 до 50 бар. В типичном примере 422 г додециламина (2,3 моля), 1460 г метанола (45 молей), 38,6 г никелевого катализатора на носителе (Harshaw Ni 1404T) и 57,1 г К2СО3 при 180°С, давлении водорода 40 бар и 1800 об./мин автоклавировали в течение 6 часов. Продукт реакции состоял из 0% RNH2, 85,9% RNHMe, 1,3% RNMe2, 6,0% R2NH и 6,8% ROH, в то время как концентрации не модифицированного катализатора составляли соответственно 15,0%, 17,2%, 44,9%, 13,8% и 9,1%, (R=н-додецил, Me=метил).
Описанные выше соответствующие предыдущему уровню развития техники способы получения первичных аминов гидрированием нитрилов имеют следующие недостатки:
(i) для снижения селективности к вторичным и третичным аминам необходимо использовать аммиак;
(ii) несмотря на повышение селективности к первичным аминам за счет добавления гидроксида или карбоната щелочного металла, контролируемое и воспроизводимое взаимодействие между добавкой и катализатором не может быть гарантировано;
(iii) поскольку используемое в качестве добавки соединение щелочного металла вводится в сопоставимом с катализатором количестве, необходимым условием является присутствие определенного количества воды в реакционной смеси, что затрудняет повторное применение катализатора и разделение продуктов реакции.
Недостатки (ii) и (iii) присущи также способу получения вторичного амина из спирта и первичного амина над никелевым катализатором на носителе в присутствии большого количества вводимого в реакционную смесь карбоната щелочного металла (US 5254736 и ЕР 0526318).
Настоящее изобретение имеет целью устранение недостатков вышеописанных способов получения первичных аминов каталитическим гидрированием нитрилов. Следовательно, основная задача заключается в предупреждении образования вторичного и третичного аминов при гидрировании нитрилов до первичных аминов. Кроме того, изобретение имеет целью отказаться от использования аммиака или поддерживать его парциальное давление при гидрировании нитрилов по возможности на более низком уровне.
Раскрытие изобретения
Установлено, что для гидрирования нитрилов, например нитрилов жирных кислот, такого как лауронитрил, в отсутствие аммиака наиболее эффективным модификатором катализатора гидрирования для снижения селективности к вторичному амину является карбонат или гидрокарбонат щелочного металла, предпочтительно K2CO3, в количестве максимум 2%. Невысокую селективность к вторичному амину до степени превращения нитрила 99% поддерживают, используя карбонат или гидрокарбонат щелочного металла. Модификацию катализатора гидрирования карбонатом или гидрокарбонатом щелочного металла, таким как К2СО3 или КНСО3, можно проводить в суспензии с применением дистиллированной воды в качестве растворителя.
Таким образом, объектом настоящего изобретения является способ получения первичного амина гидрированием нитрилов, при котором реакция превращения протекает в реакционной смеси, которая содержит:
(а) по меньшей мере, один нитрил,
(б) водород,
(в) при необходимости, аммиак и
(г) по меньшей мере, один кобальтовый или никелевый катализатор, модифицированный ex situ адсорбцией карбоната щелочного металла или гидрокарбоната щелочного металла.
Другим объектом настоящего изобретения является модифицированный кобальтовый или никелевый катализатор, полученный адсорбцией карбоната щелочного металла или гидрокарбоната щелочного металла на обычном кобальтовом или никелевом катализаторе. Особенно предпочтительными являются никелевые катализаторы Ренея.
Модификация катализатора проводится карбонатом или гидрокарбонатом щелочных металлов. Под щелочными металлами имеются в виду Na, К, Rb, Cs. Предпочтительными являются карбонаты щелочных металлов, в частности К2СО3 или КНСО3. Адсорбция осуществляется предпочтительно из раствора карбоната или гидрокарбоната щелочного металла с концентрацией предпочтительно от 10 г/л до 400 г/л. Предпочтительной является адсорбция из водного раствора, в частности водного раствора концентрацией от 50 до 200 г/л.
В контексте настоящего описания ex situ обозначает, что катализатор модифицируется не в ходе реакции гидрирования нитрила в амин, которую он катализирует, а в частности, перед указанной реакцией.
Массовое отношение сухого катализатора к раствору карбоната или гидрокарбоната щелочного металла составляет предпочтительно от 50 до 350 г/л.
Под не модифицированным катализатором имеется в виду предпочтительно кобальт, никель, кобальт Ренея или никель Ренея. Катализаторы могут применяться без или с промоторами. Промоторами могут служить, например, Fe, Mo, Cr, Ti, Zr. Катализаторы можно наносить на материал-носитель. В качестве таких материалов-носителей можно использовать, например, SiO2, Al2О3, ZrO2, MgO, MnO, ZnO, Cr2О3.
Наиболее предпочтительными вариантами являются:
- никель Ренея без промоторов или с промоторами Fe, Mo, Cr, Ti, Zr;
- никель на носителях SiO2, Al2O3, ZrO2, MgO, MnO, ZnO, Cr2O3;
- кобальт Ренея без промоторов или с промоторами Ni, Cr; кобальт на носителях SiO2, Al2О3, MgO, MnO.
Не обработанный катализатор суспендируется предпочтительно в растворе карбоната или гидрокарбоната щелочного металла с перемешиванием в течение примерно от 1 до 16 часов в атмосфере водорода или инертного газа, такого как, например, азот.
Избыток раствора удаляется после адсорбции путем фильтрации в атмосфере инертного газа, предпочтительно в атмосфере азота. В предпочтительном варианте полученный катализатор после адсорбции промывается спиртом, а затем углеводородом.
В предпочтительном варианте модифицированный катализатор из суспензии получают декантацией с последующей трехкратной промывкой катализатора этанолом и двукратной промывкой циклогексаном.
Карбонат или гидрокарбонат щелочного металла содержится в модифицированном катализаторе предпочтительно в количестве примерно от 2 до 12 мас.%. В более предпочтительном варианте модифицированный катализатор содержит К2СО3 или КНСО3 в количестве примерно от 6 до 7 мас.%.
Способ согласно настоящему изобретению пригоден для гидрирования любого нитрила. Предпочтительными являются нитрилы с формулой R-CN, в которой R является насыщенным или ненасыщенным углеводородным радикалом с числом атомов углерода от 1 до 32, предпочтительно от 4 до 24, более предпочтительно от 8 до 22. Кроме того, R предпочтительно представляет собой алкильную группу, в частности линейную алкильную группу. Модифицированный катализатор присутствует в реакционной смеси в количестве, как правило, примерно от 1 до 10 мас.% в пересчете на нитрил.
Реакционная смесь может также содержать растворитель. Для этой цели наиболее пригодными являются короткоцепочечные спирты, в частности метанол, этанол и пропанол, а также углеводороды, такие как гексан, циклогексан и толуол. Растворитель может содержаться в смеси в количестве примерно от 0 до 90 мас.% в пересчете на реакционную смесь.
Если к реакционной смеси добавляется аммиак, то количество аммиака в реакционной смеси должно составлять от 1 до 10 мас.% в пересчете на нитрил.
Гидрирование нитрилов над модифицированным катализатором проводится предпочтительно при давлении водорода от 1 до 200, более предпочтительно - от 2 до 30 бар.
Гидрирование нитрилов над модифицированным катализатором проводится предпочтительно в диапазоне температур от 60 до 250°С, более предпочтительно - от 100 до 150°С.
Осуществление изобретения
Примеры
Модификация катализатора
В примерах с 1 по 14 речь идет о никелевых катализаторах Ренея.
Пример 1
2 г карбоната калия растворяют в 20 мл дистиллированной воды (концентрация с=100 г/л), в полученном растворе суспендируют 1,4 г увлажненного водой (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 2,4 мас.%.
Пример 2
3 г карбоната калия растворяют в 20 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 3,2 мас.%.
Пример 3
4 г карбоната калия растворяют в 20 мл дистиллированной воды (с=200 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 4,1 мас.%.
Пример 4
8 г карбоната калия растворяют в 20 мл дистиллированной воды (с=400 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 4,6 мас.%.
Пример 5
3 г карбоната калия растворяют в 20 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют. Содержание калия в катализаторе составило 7,1 мас.%.
Пример 6
3 г карбоната калия растворяют в 20 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию фильтруют в атмосфере азота. Содержание калия в катализаторе составило 3,2 мас.%.
Пример 7
3 г карбоната калия растворяют в 20 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в атмосфере азота в течение 16 часов при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 3,3 мас.%.
Пример 8
1,3 г карбоната калия растворяют в 5 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 3,1 мас.%.
Пример 9
4 кг карбоната калия растворяют в 28 л дистиллированной воды (с=143 г/л), в полученном растворе суспендируют 2 кг влажного (1,4 кг сухого) катализатора и перемешивают в атмосфере азота в течение 2 часов при комнатной температуре. Спустя 20 часов катализатор выпадает в осадок, избыток раствора карбоната калия отгоняют под вакуумом. Катализатор хранили под тонким слоем раствора карбоната калия. Перед использованием суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 3,8 мас.%.
Пример 10
140 г карбоната калия растворяют в 610 мл дистиллированной воды (с=229 г/л раствора карбоната щелочного металла), в полученном растворе суспендируют 300 г влажного (210 г сухого) катализатора и перемешивают в атмосфере азота в течение 2 часов при комнатной температуре. После модификации катализатор в течение ночи выпадает в осадок, избыток раствора отгоняют под вакуумом. Модифицированный никелевый катализатор Ренея отфильтровывают в атмосфере азота. Содержание калия в катализаторе составило 3,9 мас.%.
Пример 11
3 г гидрокарбоната калия растворяют в 20 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание калия в катализаторе составило 2,3 мас.%.
Пример 12
3 г карбоната натрия растворяют в 20 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание натрия в катализаторе составляло 2,4 мас.%.
Пример 13
3 г карбоната рубидия растворяют в 20 мл дистиллированной воды (с=150 г/л), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание рубидия в катализаторе составило 4,8 мас.%.
Пример 14
3 г карбоната цезия растворяют в 20 мл дистиллированной воды (с=150 г/л раствора карбоната щелочного металла), в полученном растворе суспендируют 1,4 г влажного (1 г сухого) катализатора и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают трижды 20 мл этанола и дважды 20 мл циклогексана. Содержание цезия в катализаторе составило 5,9 мас.%.
Пример 15
30 г карбоната калия растворяют в 200 мл дистиллированной воды (с=150 г/л). В полученном растворе суспендируют 10 г сухого никелевого катализатора на SiO2(кизельгур)/MgO (порошкообразный Ni 55/5 TS от фирмы Celanese) и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают пять раз 20 мл этанола и высушивают в вакууме. Содержание калия в катализаторе составило 3 мас.%.
Пример 16
30 г карбоната калия растворяют в 200 мл дистиллированной воды (с=150 г/л). В полученном растворе суспендируют 10 г сухого никелевого катализатора на кизельгуре/Al2O3 (порошкообразный Ni 62/15 TS от фирмы Celanese) и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют и катализатор промывают пять раз 20 мл этанола и высушивают в вакууме. Содержание калия в катализаторе составило 3,5 мас.%.
Пример 17
30 г карбоната калия растворяют в 200 мл дистиллированной воды (с=150 г/л). В полученном растворе суспендируют 10 г сухого кобальтового катализатора на кизельгуре (порошкообразный Со 45/20 TS от фирмы Celanese) и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют, катализатор промывают пять раз 20 мл этанола и высушивают в вакууме. Содержание калия в катализаторе составило 3,3 мас.%.
Пример 18
30 г карбоната калия растворяют в 200 мл дистиллированной воды (с=150 г/л). В полученном растворе суспендируют 14 г увлажненного водой кобальтового катализатора Ренея В 2112 Z и перемешивают в течение 1 часа при комнатной температуре. После модификации суспензию декантируют, катализатор отфильтровывают под давлением в атмосфере азота. Содержание калия в катализаторе составило 3 мас.%.
Гидрирование нитрилов: Сравнительный пример 19 (не согласно изобретению)
В реактор из нержавеющей стали объемом 300 мл помещают 100 мл (0,447 моля) лауронитрила и 1,4 г влажного не модифицированного никелевого катализатора Ренея. Реакцию проводят при давлении водорода 10 бар при 125°С в течение 2 часов, при этом реакционную смесь перемешивают со скоростью 1500 об./мин. Выход додециламина составил 83,2% при степени превращения 99,7%.
Сравнительный пример 20 (не согласно изобретению)
В реактор помещают 100 мл (0,447 моля) лауронитрила, 1,4 г влажного не модифицированного никелевого катализатора Ренея и 2,28 г (0,134 моля) аммиака. Реакцию проводят при давлении водорода 10 бар при 125°С в течение 4 часов, при этом реакционную смесь перемешивают со скоростью 1500 об./мин. Выход додециламина составил 93,6% при степени превращения 99,8%.
Пример 21
В реактор помещают 100 мл лауронитрила и 1,4 г влажного никелевого катализатора Ренея, модифицированного, согласно примеру 2, раствором К2СО3 концентрацией 150 г/л. Реакцию проводят при давлении водорода 10 бар при 125°С в течение 2 часов, при этом реакционную смесь перемешивают со скоростью 1500 об/мин. Выход додециламина составил 97,2% при степени превращения 99,8%.
Пример 22
В реактор помещают 100 мл лауронитрила, 1,4 г никелевого катализатора Ренея, модифицированного раствором К2СО3 концентрацией 150 г/л (пример 2), и 2,28 г (0,134 моля) аммиака. Реакцию проводят при давлении водорода 10 бар при 125°С в течение 2 часов, при этом реакционную смесь перемешивают со скоростью 1500 об/мин. Выход додециламина составил 99,4% при степени превращения 99,6%.
Пример 23
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 100 г/л согласно примеру 1. Спустя 2 часа реакции выход додециламина составил 95,9% при степени превращения 99,9%.
Пример 24
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 200 г/л согласно примеру 3. Спустя 2 часа реакции выход додециламина составил 91,0% при степени превращения 93,0%.
Пример 25
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 400 г/л согласно примеру 4. Спустя 2 часа реакции выход додециламина составил 68,3% при степени превращения 69,9%.
Пример 26
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 150 г/л согласно примеру 5. Спустя 4 часа реакции выход додециламина составил 60,5% при степени превращения 61,7%.
Пример 27
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 150 г/л согласно примеру 6. Спустя 2 часа реакции выход додециламина составил 95,8% при степени превращения 99,8%.
Пример 28
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 150 г/л согласно примеру 7. Спустя 2 часа реакции выход додециламина составил 96,1% при степени превращения 99,5%.
Пример 29
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 150 г/л согласно примеру 8. Спустя 2 часа реакции выход додециламина составил 95,4% при степени превращения 99,9%.
Пример 30
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором К2СО3 концентрацией 143 г/л согласно примеру 9. Спустя 2 часа реакции выход додециламина составил 92,3% при степени превращения 94,3%.
Пример 31
В реактор помещают 20 мл лауронитрила, 80 мл циклогексана и 1,4 г никелевого катализатора Ренея, модифицированного раствором К2СО3 концентрацией 150 г/л. Реакцию проводят при давлении водорода 10 бар и 125°С, при этом реакционную смесь перемешивают со скоростью 1500 об./мин. Степень превращения лауронитрила составила 99,6%, выход додециламина - 95,0%.
Пример 32
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором КНСО3 концентрацией 100 г/л согласно примеру 11. Спустя 1 час реакции выход додециламина составил 93,6% при степени превращения 99,4%.
Пример 33
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором Na2СО3 концентрацией 100 г/л согласно примеру 12. Спустя 1 час реакции выход додециламина составил 84,2% при степени превращения 98,9%.
Пример 34
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором Rb2СО3 концентрацией 150 г/л согласно примеру 13. Спустя 2 часа реакции выход додециламина составил 96,3% при степени превращения 99,7%.
Пример 35
Выполняют аналогично примеру 21, за исключением того, что никелевый катализатор Ренея модифицируют раствором Cs2СО3 концентрацией 150 г/л согласно примеру 14. Спустя 2 часа реакции выход додециламина составил 97,3% при степени превращения 99,2%.
Пример 36
В реактор помещают 100 мл нитрила лауриновой кислоты, 1 г никелевого катализатора Ренея, модифицируют раствором К2СО3 концентрацией 150 г/л на кизельгуре/MgO (пример 15) и 2 г (0,12 моля) аммиака. Реакцию проводят при давлении водорода 15 бар и 125°С в течение 3 часов, при этом реакционную смесь перемешивают со скоростью 1500 об/мин. Выход додециламина составил 99,2% при степени превращения 99,5%.
Пример 37
В реактор помещают 100 мл нитрила олеиновой кислоты, 1 г никелевого катализатора Ренея, модифицируют раствором К2СО3 концентрацией 150 г/л на кизельгуре/Al2O3 (пример 16) и 2 г (0,12 моля) аммиака. Реакцию проводят при давлении водорода 10 бар и 120°С в течение 2 часов, при этом реакционную смесь перемешивают со скоростью 1500 об/мин. Выход первичных аминов (олеиламина) составил 99,3% при степени превращения 99,7%.
Пример 38
В реактор помещают 100 мл нитрила олеиновой кислоты, 1 г кобальтового катализатора Ренея, модифицируют раствором К2СО3 концентрацией 150 г/л на кизельгуре (пример 17) и 3 г (0,12 моля) аммиака. Реакцию проводят при давлении водорода 60 бар и 140°С в течение 4 часов, при этом реакционную смесь перемешивают со скоростью 1500 об/мин. Выход первичных аминов (олеиламина) составил 99,6% при степени превращения 99,8%.
Пример 39
В реактор помещают 100 мл нитрила лауриновой кислоты, 1 г кобальтового катализатора Ренея, модифицируют раствором К2СО3 концентрацией 150 г/л (пример 18) и 2 г (0,12 моля) аммиака. Реакцию превращения проводят при давлении водорода 50 бар и 160°С в течение 4 часов, при этом реакционную смесь перемешивают со скоростью 1500 об/мин. Выход додециламина составил 98,8% при степени превращения 99,2%.
Примеры с 40 по 43
Изучали активность при повторном применении никелевого катализатора Ренея при гидрировании лауронитрила.
В автоклавы (объем 10 л) помещают 5 кг лауронитрила, 100 г никелевого катализатора Ренея и при необходимости 250 г аммиака. Реакцию превращения проводят при давлении водорода 10 бар, 125°С и скорости перемешивания 1000 об/мин. Превращение лауронитрила и селективность к додециламину определяют по уровню снижения количества катализатора вследствие его потерь при рециркуляции и отборе проб при различном времени реакции. Измерения проводят с модифицированным и не модифицированным катализатором. Модификацию катализатора осуществляют согласно примеру 10.
№
№
№
№
Дополнительные примеры осуществления изобретения
Пример 45
В реактор помещают 100 мл децилового эфира пропионитрила и 1,4 г влажного никелевого катализатора Ренея, модифицированного раствором К2СО3 (с - 150 г/л), как указано в примере 2. Реакцию проводят при давлении водорода 20 бар и температуре 100°С в течение 5 часов и полученную реакционную смесь перемешивают со скоростью 1500 об/мин. Выход децилового эфира пропиленамина составил 95,6% при степени конверсии 99,4%.
Дециловый эфир пропионитрила является соединением формулы
C10H21-O-(CH2)2-CN
Дециловый эфир пропиленамина является соединением формулы
C10H21-O-(CH2)3-NH2
Пример 46
В реактор помещают 100 мл октиламинодипропионитрила и 1,4 г влажного никелевого катализатора Ренея, модифицированного раствором К2СО3 (с - 150 г/л), как указано в примере 2. Реакцию проводят при давлении водорода 20 бар и температуре 100°C в течение 5 часов и полученную реакционную смесь перемешивают со скоростью 1500 об/мин. Выход октиламиноди(пропиленамина) составил 94,8% при степени конверсии 99,7%.
Октиламинодипропионитрил является соединением формулы

Октиламиноди(пропипропиленамин) является соединением формулы
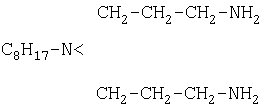
Сравнительные примеры
Примеры 45 и 46 были повторены с использованием других катализаторов, т.е. катализаторов, полученных не в соответствии с настоящим изобретением. Такими катализаторами были влажные не модифицированные никелевые катализаторы Ренея.
Пример 47 (сравнительный)
Повторяют пример 45 с использованием указанного выше катализатора не по изобретению. Выход децилового эфира пропиленамина составил 89.2% при степени конверсии 99,6%.
Пример 48(сравнительный)
Повторяют пример 46 с использованием указанного выше катализатора не по изобретению. Выход октиламиноди(пропиленамина) составил 87,6% при степени конверсии 99,6%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОМОЛЕКУЛЯРНЫХ АМИНОВ | 2008 |
|
RU2372323C1 |
| СПОСОБ ПРОИЗВОДСТВА 3-ДИМЕТИЛАМИНОПРОПИЛАМИНА (ДМАПА) ПРИ НИЗКОМ ДАВЛЕНИИ | 2003 |
|
RU2326108C2 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСИ ЭТИЛЕНАМИНОВ | 2008 |
|
RU2473537C2 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОВ | 2009 |
|
RU2484084C2 |
| СПОСОБ СИНТЕЗА ПЕРВИЧНЫХ ДИАМИНОВ И/ИЛИ ТРИАМИНОВ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ | 2007 |
|
RU2454400C2 |
| КАТАЛИЗАТОР НА ОСНОВЕ СМЕШАННЫХ ОКСИДОВ ДЛЯ ГИДРИРОВАНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ГИДРИРОВАНИЯ | 2007 |
|
RU2434676C9 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСЕЙ ЭТИЛЕНАМИНОВ | 2008 |
|
RU2478092C2 |
| СПОСОБ ПОЛУЧЕНИЯ (S)-3-[(1-ДИМЕТИЛАМИНО)ЭТИЛ]-ФЕНИЛ-N-ЭТИЛ-N-МЕТИЛ-КАРБАМАТА | 2005 |
|
RU2393148C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ДИБЕНЗОТИАЗЕПИНА | 1999 |
|
RU2233275C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛИФАТИЧЕСКИХ АЛЬФА, ОМЕГА-АМИНОНИТРИЛОВ | 1995 |
|
RU2154630C2 |
Изобретение относится к способу получения первичного амина гидрированием нитрилов, при котором реакция превращения протекает в реакционной смеси, которая содержит: (а) по меньшей мере, один нитрил, (б) водород, (в) при необходимости, аммиак и (г) по меньшей мере, один кобальтовый или никелевый катализатор, модифицированный ex situ адсорбцией карбоната щелочного металла или гидрокарбоната щелочного металла, который содержит карбонат или гидрокарбонат щелочного металла в количестве от 2 до 12 мас.%. Также изобретение относится к катализатору, применяемому в способе по п.1, представляющему собой модифицированный кобальтовый или никелевый катализатор, получаемый адсорбцией карбоната щелочного металла или гидрокарбоната щелочного металла в количестве от 2 до 12 мас.% на обычном кобальтовом или никелевом катализаторе. 2 н. и 22 з.п. ф-лы, 6 табл.
| Окрасочная камера | 1985 |
|
SU1242260A2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ НИКЕЛЕВОГО КАТАЛИЗАТОРА ГИДРИРОВАНИЯ РАСТИТЕЛЬНЫХ МАСЕЛ И ЖИРОВ | 1995 |
|
RU2102137C1 |
| US 3544485 A, 01.12.1970 | |||
| US 3980720 A, 14.09.1976. | |||
Авторы
Даты
2007-01-27—Публикация
2003-02-13—Подача