Настоящее изобретение относится к производным пиперидина, к способу их получения, к их применению и к содержащим их фармацевтическим композициям.
Более конкретно настоящее изобретение обеспечивает соединение формулы I
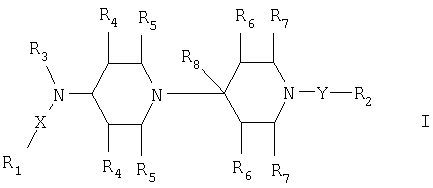
где X означает прямую связь, -СН2-, -СН2-СН2-, -CHR9-, -С(O)-, -О-, -NH- или NR9;
R1 означает необязательно R10- и/или R11-замещенный фенил, необязательно R10- и/или R11-замещенный гетероарил, N-окись необязательно R10- и/или R11-замещенного гетероарила или необязательно R10- и/или R11-замещенный нафтил;
R2 имеет одно из значений, приведенных для R1, или означает необязательно R10- и/или R11-замещенный флуоренил, необязательно R10-замещенный (С1-С6)алкил, необязательно R10-замещенный (С2-С6)алкенил, необязательно R10-замещенный (С3-С6)циклоалкил, необязательно R10-замещенный адамантил или необязательно R10-замещенный (С4-С8)пиклоалкенил;
R3 имеет одно из значений, приведенных для R1, или означает необязательно R10- и/или R11-замещенный флуоренил, R10-замещенный (С1-С6)алкил, необязательно R10-замещенный (С2-С6)алкенил, необязательно R10-замещенный (С3-С6)-циклоалкил, необязательно R10-замещенный адамантил или необязательно R10-замещенный (С4-С8)циклоалкенил;
или
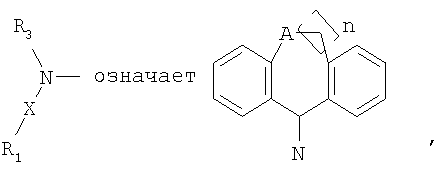
где
А означает -СН2-, -NH-, -NR9-, -S-, -SO-, SO2- или -О-, n означает 0, 1 или 2 и каждое из ароматических колец независимо является необязательно R10-замещенным;
каждый из R4 независимо имеет одно из значений, приведенных для R5, или означает циангруппу, гидроксил, OR9, фтор, хлор, бром или иод;
каждый из R5 означает независимо водород, (С1-С6)алкил, (С1-С6)гидроксиалкил, (С2-С6)алкоксиалкил, (С1-С6)галоидалкил, фенил, бензил или гетероарил;
каждый из R6 независимо имеет одно из значений, приведенных для R4;
каждый из R7 независимо имеет одно из значений, приведенных для R5;
R8 означает водород, (С1-С6)алкил, (С2-С6)алкенил, (С2-С6)алкинил, фенил, бензил, циангруппу, CH2NH2, CH2NHR9, CH2NR9R9, CH2NHC(O)R9, CH2NR9C(O)R9, CH2NHC(O)NHR9, CH2NR9C(O)NHR9, CH2NR9C(O)NR9R9, CH2NHC(O)OR9, CH2NR9C(O)OR9, CH2NHSO2R9, CH2N(SO2R9)2 или CH2NR9SO2R9;
R9 каждый независимо означает (С1-С6)алкил, (С3-С6)циклоалкил, (С2-С6)алкенил, (С2-С6)алкинил, фенил, бензил, гетероарил или CF3;
R10 представляет от 1 до 4 заместителей, независимо выбранных из (C1-С6)алкила, (С1-С6)гидроксиалкила, (С2-С6)алкоксиалкила, (C1-С6)галоидалкила, (С3-С6)-циклоалкила, (С2-С6)алкенила, (С3-С6)циклоалкенила, (С2-С6)алкинила, фенила, гетероарила, N-окиси гетероарила, фтора, хлора, брома, иода, гидроксила, OR9, CONH3, CONHR9, CONR9R9, OC(O)R9, OC(O)OR9, OC(O)NHR9, OC(O)NR9R9, OSO2R9, COOH, COOR9, CF3, CHF2, CH2F, CN, NO2, NH2, NHR9, NR9R9, NHC(O)R9, NR9C(O)R9, NHC(O)NHR9, NHC(O)NH2, NR9C(O)NHR9, NR9C(O)NR9R9, NHC(O)OR9, NR9C(O)OR9, NHSO2R9, N(SO2R9)2, NR9SO2R9, SR9, S(O)R9, SO2R9, Si(СН3)3 и В(ОС(СН3)2)2;
R11 представляет два соседних заместителя, которые образуют аннелированное 4-7-членное неароматическое кольцо, необязательно содержащее до двух гетероатомов, выбранных независимо из азота, кислорода и серы; и
Y означает прямую связь, -С(O)-, -С(O)СН2-, -S(O)-, -S(O2)-, -C(S)-, -CH2-, -С(-СН2-СН2-)-, -CH(R4)- или -C(R5)2-,
в свободной форме или в виде соли.
Любой алкил, алкенил или алкинил может быть линейным или разветвленным. Галоген означает фтор, хлор, бром или иод.
Под гетероарилом подразумевается циклическая ароматическая система, включающая моно-, би- или трициклические системы, которая содержит вплоть до 4 гетероатомов, независимо выбранных из азота, кислорода и серы, как, например, фурил, тиенил, пирролил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, изоксазолил, оксадиазолил, тиадиазолил, триазолил, тетразолил, пиридил, пиридазинил, пиримидинил, пиразинил, триазинил, тетразинил, индолил, бензотиофенил, бензофуранил, бензимидазолил, индазолил, бензотриазолил, бензотиазолил, бензоксазолил, хинолинил, изохинолинил, фталазинил, хиноксалинил, хиназолинил, циннолинил или нафтиридинил.
Предпочтительным аннелированным 4-7-членным неароматическим кольцом, представленным R11, является аннелированное 5- или 6-членное неароматическое кольцо, необязательно содержащее 1 или 2 атома кислорода и включающее, например, -О-СН2-О- или -О-СН2-СН2-О-, присоединенные к двум соседним атомам углерода.
Соединения формулы I могут существовать в свободной форме или в виде соли, например в виде аддитивных солей с, например, органическими или неорганическими кислотами, например с соляной кислотой, уксусной кислотой, когда R1, R2 и/или R3 содержит необязательно замещенную аминогруппу или гетероциклический остаток, которые могут образовывать аддитивные соли. Когда соединения формулы I содержат один или несколько асимметрических центров в молекуле, например, когда пиперидиновое кольцо замещено, то настоящее изобретение следует понимать как охватывающее различные оптические изомеры, а также рацематы, диастереоизомеры и их смеси.
В соединениях формулы I предпочтительны следующие значения в отдельности или в любой под-комбинации:
1. R1 означает необязательно R10-замещенный фенил, необязательно R10-замещенный гетероарил или необязательно R11-замещенный фенил.
2. R2 означает необязательно R10-замещенный фенил, необязательно R10-замещенный гетероарил, N-окись необязательно R10-замещенного гетероарила или необязательно R10-замещенный нафтил.
3. R3 означает необязательно R10-замещенный фенил, необязательно R10-замещенный гетероарил или необязательно R10-замещенный нафтил.
4. Каждый из R4, R5, R6 или R7 независимо означает водород, (С1-С6)алкил или бензил.
5. R8 означает водород, (С1-С6)алкил или (С2-С6)алкенил.
6. R9 означает (С1-С6)алкил, (С3-С6)циклоалкил, (С2-С6)алкенил, (С2-С6)алкинил, фенил, бензил, гетероарил или CF3.
7. R10 представляет от 1 до 3 заместителей, независимо выбранных из (C1-С6)алкила, (С1-С6)гидроксиалкила, (С2-С6)алкоксиалкила, (С1-С6)галоидалкила, (С3-С6)-циклоалкила, (С2-С6)алкенила, (С3-С6)циклоалкенила, (С2-С6)алкинила, фенила, гетероарила, N-окиси гетероарила, фтора, хлора, брома, иода, гидроксила, OR9, CONH2, CONHR9, CONR9R9, OC(O)R9, OC(O)OR9, OC(O)NHR9, OC(O)NR9R9, OSO2R9, COOH, COOR9, CF3, CHF2, CH2F, CN, NO2, NH2, NHR9, NR9R9, NHC(O)R9, NR9C(O)R9, NHC(O)NHR9, NHC(O)NH2, NR9C(O)NHR9, NR9C(O)NR9R9, NHC(O)OR9, NR9C(O)OR9, NHSO2R9, N(SO2R9)2, NR9SO2R9, SR9, S(O)R9, SO2R9 и Si(СН3)3.
8. R11 представляет -O-СН2-O-, связанный с двумя смежными углеродными атомами.
9. Х означает прямую связь или -СН2-.
10. Y означает -С(O)-.
В предпочтительных соединениях формулы I R10 может представлять 1-3 заместителя, выбранных из (С1-С6)алкила, фенила, гетероарила, N-окиси гетероарила, фтора, хлора, брома, иода, гидроксила, OR9, CONH2, CONHR9, CONR9R9, COOH, COOR9, CF3, CHF2, CH2F, NH2, NHR9, NR9R9, NHC(O)R9, NR9C(O)R9, NHC(O)NHR9, NHC(O)NH2, NR9C(O)NHR9, NR9C(O)NR9R9, NHC(O)OR9 и NR9C(O)OR9.
R9 предпочтительно означает (С1-С6)алкил, (С3-С6)циклоалкил, фенил, бензил или гетероарил, более предпочтительно (С1-С6)алкил.
Данное изобретение также включает способ получения соединения формулы I, который охватывает а) для получения соединения формулы I, где Х означает прямую связь, -СН2-, -СН2-СН2- или -CHR9- и Y означает -СО-, -С(O)СН2-, -S(O)- или -S(O2)-, амидирование соединения формулы II
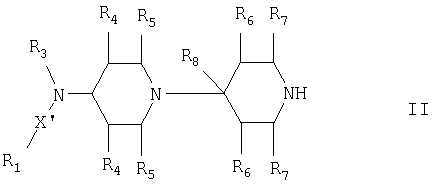
где R1 и R3-R8 являются такими, как указано выше, и X' означает прямую связь, -СН2-, -СН2-СН2- или -CHR9-,
с использованием соединения формулы III

где R2 является таким, как определено выше. Y' означает -СО-, -С(O)СН2-, -S(O)- или -S(O2)- и А' является уходящей группой, например, хлором или бромом,
б) для получения соединения формулы I, где Х является прямой связью и Y означает -СН2-, проведение восстановительного аминирования соединения формулы II, указанного выше, где X' означает прямую связь, или
в) для получения соединения формулы I, где Х означает -CH2-, -CH2-CH2- или -CHR9- и Y означает -СО-, -С(O)СН2-, -S(O)- или -S(O2)-, взаимодействие соединения формулы IV
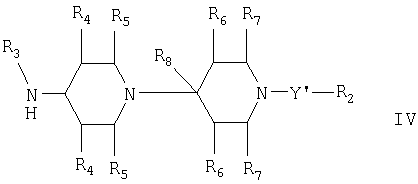
где R2-R8 и Y' являются такими, как определено выше, с соединением формулы V
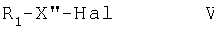
где R1 является таким, как определено выше, и X'' означает СН2- или -CHR9-, и, если требуется, превращение полученного в результате соединения формулы I в свободной форме в желаемую соль или наоборот.
Стадии реакций а), б) или в) могут быть осуществлены в соответствии со способами, известными в данной области или раскрытыми в приведенных ниже примерах. Когда R8 включает группу, которая не должна участвовать в реакции, эта группа может быть защищена в соответствии с известными в данной области способами.
Соединения формулы II, используемые в качестве исходных веществ, могут быть получены следующим образом:
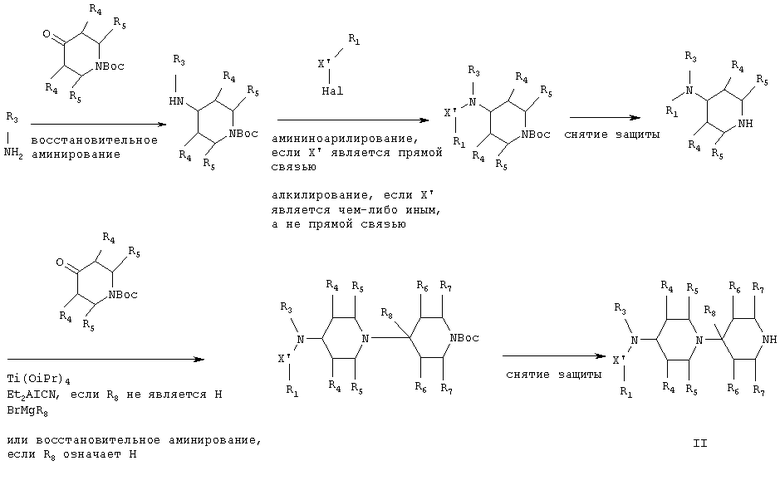
где X' и R1-R8 являются такими, как определено выше, и Hal означает хлор, бром или иод. В приведенных выше формулах Boc является защитной группой, означающей трет-бутоксикарбонил. Эта защитная группа может быть заменена в приведенной выше реакционной схеме любой защитной группой для аминогруппы, например, указанными Т.W.Greene в "Protective Groups in Organic Synthesis", J.Wiley & Sons NY, 2-е издание, глава 7, 1991, и в приведенных ссылках, например, бензилоксикарбонилом или 9-флуоренилметоксикарбонилом.
Соединения формулы IV, используемые в качестве исходного сырья, могут быть получены следующим образом:
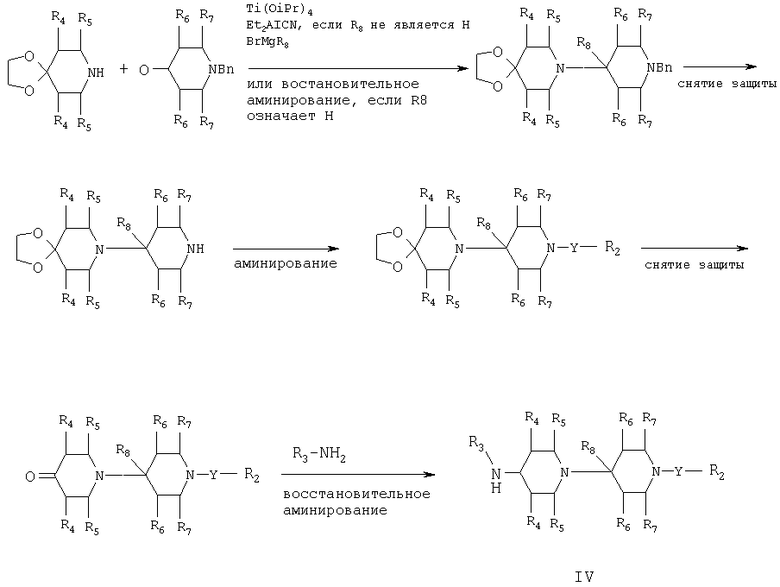
где R2-R8 и Y являются такими, как определено выше, и Bn означает бензил.
Указанные выше реакции могут быть осуществлены в соответствии со способами, известными в данной области или представленными далее.
Постольку получение исходных веществ не описывается в деталях, эти соединения известны или могут быть получены аналогично способам, известным в данной области или описанным ниже.
Следующие примеры иллюстрируют изобретение, не ограничивая этим. Использованы следующие сокращения:
Пример 1: (2,6-Диметилфенил)-(4-дифениламино-4'-метил-[1,4']-бипиперидинил-1'-ил)метанон
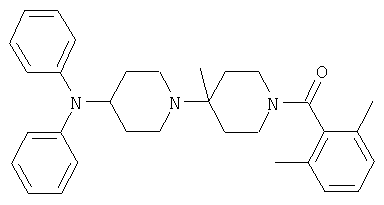
Смесь (4'-метил-[1,4']бипиперидинил-4-ил)дифениламина(0,25 г, 0,71 ммоля), 2,6-диметилбензойной кислоты (0,32 г, 2,13 ммоля), тетрафторбората 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (0,57 г, 1,5 ммоля), EtN(i-Pr)2 (0,6 мл) и ДМФА (5 мл) перемешивают 16 часов при 20°С. Смесь разбавляют (трет-бутил)-метиловым эфиром (25 мл), промывают 2 н. гидроокисью натрия (25 мл) и соляным раствором (25 мл) и сушат сульфатом натрия. Растворитель удаляют и остаток очищают с помощью хроматографии (SiO2, (трет-бутил)метиловый эфир/циклогексан 1:4→1:0). Указанное в заглавии соединение выделяют в виде бесцветного масла. Масс-спектрометрия (МС) с ионизацией электрораспылением (ESI) 482 (М+Н)+; 1H-ЯМР (400 MHz, ДМСО) δ=0,89 (3 Н, s), 1,14-1,25 (3 H, m), 1,39 (1 H, m), 1,59 (1 H, m), 1,75 (1 H, m), 1,83-1,95 (2 Н, m), 2,01 (3 H, s), 2,13 (3 H, s), 2,11-2,24 (2 H, m), 2,85 (2 H, m), 2,95 (1 Н, s), 3,01 (1 H, m), 3,35 (1 H, m), 3,70-3,83 (2 H, m), 6,77 (4 H, m). 6,92-7,05 (4 Н, m), 7,12 (1 H, m), 7,26 (4H, m).
(4'-Метил-[1,4']бипиперидинил-4-ил)дифениламин, используемый в качестве исходного вещества, может быть получен следующим образом:
а) Смесь фенилпиперидин-4-иламина (4,14 г, 15,0 ммолей), иодбензола (3,06 г, 15,0 ммолей), Pd(OAc)2 (0,14 г, 0,63 ммоля), 2,2'-бис(дифенилфосфино)-1,1'-бинафтила (0,43 г, 0,69 ммоля), t-BuOK (17,5 мл 1 M раствора в тетрагидрофуране) в толуоле (20 мл) нагревают при 110°С в течение 5 часов. Смесь разбавляют этилацетатом, экстрагируют бикарбонатом натрия и соляным раствором и сушат сульфатом натрия. Растворитель удаляют и остаток хроматографируют (SiO2, (трет-бутил)метиловый эфир/циклогексан 1:9→1:1). трет-Бутиловый эфир 4-дифениламинопиперидин-1-карбоновой кислоты выделяют в виде твердого вещества желтого цвета. MC/ESI 353 (М+Н)+.
б) Смесь трифторуксусной кислоты (5 мл), хлористого метилена (5 мл), воды (0,25 мл) и трет-бутилового эфира 4-дифениламинопиперидин-1-карбоновой кислоты (1,5 г, 4,2 ммоля) перемешивают 2 часа при 20°C. Прибавляют гидроокись натрия (4 н.) и смесь экстрагируют этилацетатом. Органическую фазу сушат сульфатом натрия и растворитель удаляют. Дифенилпиперидин-4-иламин выделяют в виде бесцветного масла. MC/ESI 253 (М+Н)+.
в) Суспензию дифенилпиперидин-4-иламина (1,26 г, 5,00 ммолей), 1-(трет-бутил-оксикарбонил)-4-пиперидона (1,00 г, 5,00 ммолей) и изопропилата титана(IV) (1,42 г, 5,00 ммолей) в 1,2-дихлорэтане (25 мл) перемешивают 1 час при 80°С и затем 16 часов при 20°С. Прибавляют цианид диэтилалюминия (10 мл 1 М раствора в толуоле) и смесь перемешивают еще 24 часа. Растворитель удаляют и технический продукт растворяют в тетрагидрофуране (25 мл). Прибавляют по каплям бромистый метилмагний (8,7 мл 3 М раствора в диэтиловом эфире) и смесь перемешивают 3 часа при 20°С. Прибавляют хлористый аммоний (10% раствор, 50 мл) и этилацетат (50 мл), органическую фазу промывают хлористым аммонием (10% раствор, 50 мл) и бикарбонатом натрия (10% раствор, 50 мл), сушат сульфатом натрия и растворитель удаляют. Остаток подвергают хроматографии (SiO2, этилацетат/циклогексан 1:9→1:1). трет-Бутиловый эфир 4-дифениламино-4'-метил-[1,4']бипиперидинил-1'-карбоновой кислоты выделяют в виде бесцветного твердого вещества. MC/ESI 450 (М+Н)+.
г) Смесь трифторуксусной кислоты (2 мл) и воды (0,1 мл) прибавляют по каплям к раствору соединения со стадии а) выше (0,81 г, 1,80 ммоля) в хлористом метилене (5 мл) и смесь перемешивают 3 часа при 20°С. Прибавляют бикарбонат натрия (10% раствор, 10 мл) и этилацетат (20 мл) и органическую фазу сушат сульфатом натрия. Растворитель удаляют и остаток подвергают хроматографии (колонка для обращенно-фазовой хроматографии RP-18, метанол/вода 1:3→0:1). Соединение выделяют в виде бесцветного масла. MC/ESI 350 (М+Н)+; 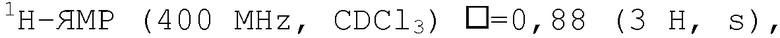 1,35 (4 H, m), 1,60 (4 Н, m), 1,93 (2 H, m), 2,15 (2 H, m), 2,58 (2 Н, m), 2,87 (2 Н, s), 2,96 (2 H, m), 3,76 (1 H, m), 6,78 (4 H, m), 6,94 (2 H, m), 7,22 (4 H, m).
1,35 (4 H, m), 1,60 (4 Н, m), 1,93 (2 H, m), 2,15 (2 H, m), 2,58 (2 Н, m), 2,87 (2 Н, s), 2,96 (2 H, m), 3,76 (1 H, m), 6,78 (4 H, m), 6,94 (2 H, m), 7,22 (4 H, m).
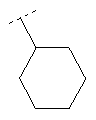
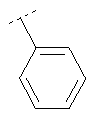
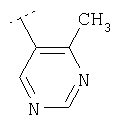
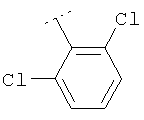
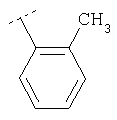
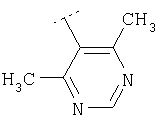
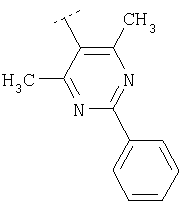
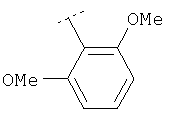
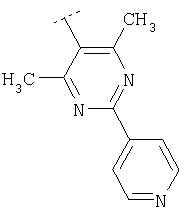
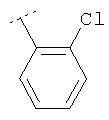
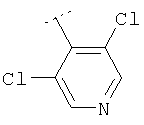
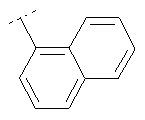
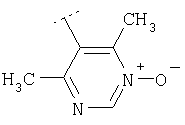
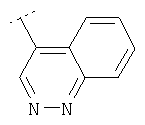
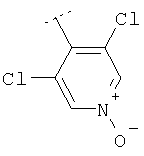
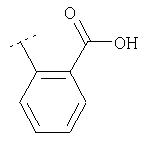
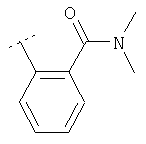
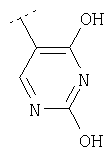
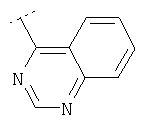
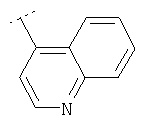
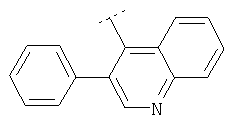
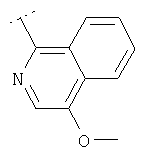
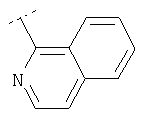
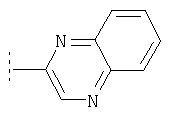
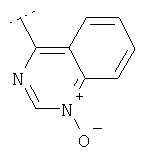
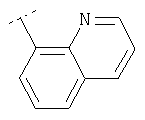
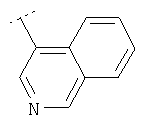
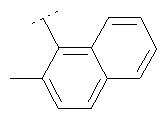
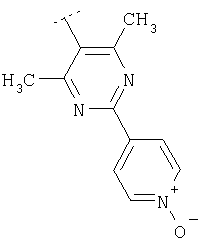
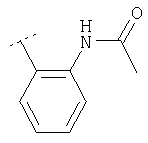
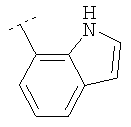
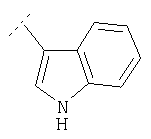
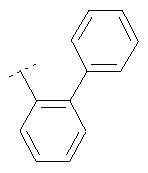
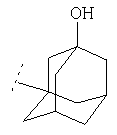
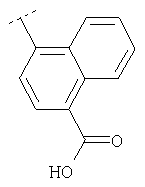
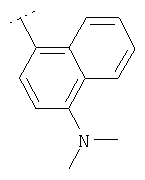
Следуя методике из примера 1 и применяя в качестве исходного вещества (4'-метил-[1,4']бипиперидинил-4-ил)дифениламин, можно получить соединения формулы X1
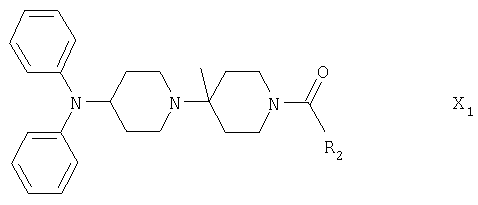
где R2 имеет значения, приведенные в табл.1.
Пример 41: [4'-Метил-1'-(2,4,6-триметилбензолсульфонил)-[1,4']-бипиперидинил-4-ил]дифениламин
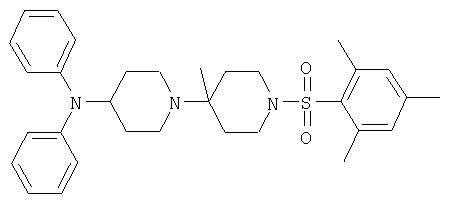
Смесь (4'-метил-[1,4']бипиперидинил-4-ил)дифениламина (70 мг, 0,20 ммоля), 2,4,6-триметилбензолсульфохлорида (65 мг, 0,30 ммоля) и диизопропилэтиламина (0,50 мл) в хлористом метилене (3 мл) перемешивают 4 часа при комнатной температуре. Смесь разбавляют этилацетатом, экстрагируют бикарбонатом натрия (10% раствор) и сушат сульфатом натрия. Растворитель удаляют и остаток подвергают хроматографии (SiO2, (трет-бутил)метиловый эфир/циклогексан 1:9→1:0). Указанное в заглавии соединение выделяют в виде бесцветного твердого вещества. MC/ESI 532 (М+Н)+.
Пример 42: [1'-(2,6-Диметилбензил)-4'-метил-[1,4']бипиперидинил-4-ил]-дифениламин
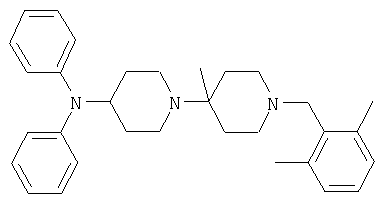
Смесь (4'-метил-[1,4']бипиперидинил-4-ил)дифениламина (70 мг, 0,20 ммоля), 2,6-диметилбензальдегида (34 мг, 0,25 ммоля) и Na(OAc)3BH (53 мг, 0,25 ммоля) в 1,2-дихлорэтане (10 мл) перемешивают при комнатной температуре 16 часов. Смесь разбавляют этилацетатом, экстрагируют бикарбонатом натрия (10% раствор) и сушат сульфатом натрия. Растворитель удаляют и остаток подвергают хроматографии (SiO2, (трет-бутил)метиловый эфир/метанол 1:0→10:1). Указанное в заглавии соединение выделяют в виде бесцветного твердого вещества. MC/ESI 468 (М+Н)+.
Пример 43: (2,6-Диметилфенил)-(4-дифениламино-[1,4']бипиперидинил-1'-ил)-метанон
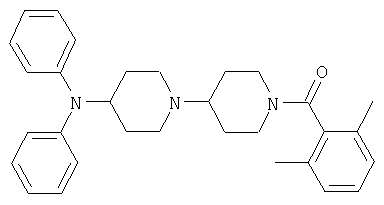
Смесь соли [1,4']бипиперидинил-4-илдифениламина с трифторуксусной кислотой (77 мг, 0,23 ммоля), 2,6-диметилбензойной кислоты (100 мг, 0,67 ммоля), тетрафторбората 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (254 мг, 0,67 ммоля), диизопропилэтиламина (2 мл) и диметилформамида (3 мл) перемешивают 5 часов при комнатной температуре. Смесь разбавляют (трет-бутил)метиловым эфиром (10 мл), промывают 2 н. гидроокисью натрия и соляным раствором и сушат сульфатом натрия. Растворитель удаляют и остаток очищают с помощью хроматографии (SiO2, (трет-бутил)метиловый эфир/циклогексан 1:1→этилацетат→этилацетат/вода 98:2). Указанное в заглавии соединение выделяют в виде бесцветного твердого вещества. MC/ESI 468 (М+Н)+.
[1,4']Бипиперидинил-4-илдифениламин, используемый в качестве исходного сырья, может быть получен следующим образом:
а) Смесь дифенилпиперидин-4-иламина (1,06 г, 4,2 ммоля), трет-бутилового эфира 4-оксопиперидин-1-карбоновой кислоты (1,0 г, 5,0 ммолей), уксусной кислоты (0,62 г, 10,3 ммоля) и Na(ОАс)3ВН (1,0 г, 4,7 ммоля) в 1,2-дихлорэтане (15 мл) перемешивают 4 часа при 65°С. Смесь разбавляют (трет-бутил)метиловым эфиром, экстрагируют 1 н. гидроокисью натрия и сушат сульфатом натрия. Растворитель удаляют и остаток подвергают хроматографии (SiO2, (трет-бутил)метиловый эфир/циклогексан 1:9→1:0). трет-Бутиловый эфир 4-дифениламино-[1,4']бипиперидинил-1'-карбоновой кислоты выделяют в виде бесцветного твердого вещества. MC/ESI 436 (М+Н)+.
б) Смесь трет-бутилового эфира 4-дифениламино-[1,4']бипиперидинил-1'-карбоновой кислоты (1,06 г, 2,4 ммоля), трифторуксусной кислоты (2,5 мл), воды (0,25 мл) и хлористого метилена (5 мл) перемешивают 4 часа при комнатной температуре. Смесь прибавляют по каплям к диэтиловому эфиру и образовавшийся осадок отфильтровывают. Соль [1,4']бипиперидинил-4-илдифениламина с трифторуксусной кислотой выделяют в виде твердого бесцветного вещества. MC/ESI 336 (М+Н)+.
Следуя методике из примера 2 выше и применяя в качестве исходного сырья [1,4']бипиперидинил-4-илдифениламин, можно получать соединения формулы Х2
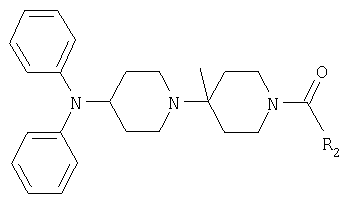
где R2 имеет одно из значений, приведенных в табл.2.



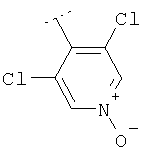
Пример 51:{4-[(4-Бромфенил)фениламино]-4'-метил-[1,4']бипиперидинил-1'-ил}-(2,6-диметилфенил)метанон
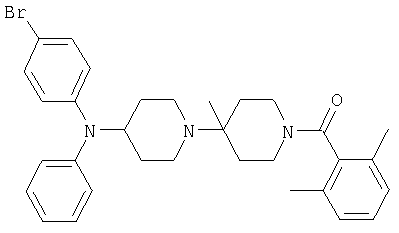
Смесь [4-(4-бромфениламино)-4'-метил-[1,4']-бипиперидинил-1'-ил]-(2,6-диметилфенил)метанона (97 мг, 0,20 ммоля), иодбензола (41 мг, 0,20 ммоля), Pd(OAc)2 (1,9 мг, 0,008 ммоля), 2,2'-бис(дифенилфосфино)-1,1'-бинафтила (5,7 мг, 0,009 ммоля) и трет-бутилата калия (0,23 мл 1 М раствора в тетрагидрофуране) в толуоле (3 мл) нагревают 16 часов при 110°С. Смесь разбавляют этилацетатом и фильтруют. Полученный в результате раствор экстрагируют 2 н. гидроокисью натрия и соляным раствором и сушат сульфатом натрия. Растворитель удаляют и остаток подвергают хроматографии (сначала на SiO2, (трет-бутил)метиловый эфир/циклогексан 1:4→1:0 и затем RP-18, метанол/вода 7:3). Указанное в заглавии соединение выделяют в виде твердого бесцветного вещества. MC/ESI 560 (М+Н)+.
[4-(4-Бромфениламино)-4'-метил-[1,4']бипиперидинил-1'-ил]-(2,6-диметилфенил)метанон, используемый в качестве исходного сырья, может быть получен следующим образом:
а) 8-(1-Бензил-4-метилпиперидин-4-ил)-1,4-диокса-8-аза-спиро[4.5]декан получают из 1,4-диокса-8-аза-спиро[4.5]декана и 1-бензилпиперидин-4-она, следуя методике, описанной в примере 1в). MC/ESI 331 (М+Н)+.
б) Смесь 8-(1-бензил-4-метилпиперидин-4-ил)-1,4-диокса-8-аза-спиро[4.5]декана (2,0 г, 6,1 ммоля) и Pd(OH)2 (20%) на угле (1 г) в метаноле (30 мл) гидрируют 16 часов при комнатной температуре. Катализатор отфильтровывают и растворитель удаляют. Технический 8-(4-метилпиперидин-4-ил)-1,4-диокса-8-аза-спиро[4.5]декан выделяют в виде масла желтого цвета MC/ESI 241 (М+Н)+.
в) (2,6-Диметилфенил)-[4-(1,4-диокса-8-аза-спиро[4.5]дец-8-ил)-4-метилпиперидин-1-ил]метанон получают из технического 8-(4-метилпиперидин-4-ил)-1,4-диокса-8-аза-спиро[4.5]декана и 2,6-диметилбензойной кислоты, следуя методике, описанной в примере 1. MC/ESI 373 (М+Н)+.
г) Раствор (2,6-диметилфенил)-[4-(1,4-диокса-8-аза-спиро[4.5]дец-8-ил)-4-метил-пиперидин-1-ил]метанона (915 мг, 2,46 ммоля) в диоксане (30 мл) и соляной кислоте (6 н., 30 мл) перемешивают 4 часа при 50°С. Смесь разбавляют этилацетатом (50 мл), экстрагируют 2 н. гидроокисью натрия и соляным раствором и сушат сульфатом натрия. После удаления растворителя получают 1'-(2,6-диметилбензоил)-4'-метил-[1,4']бипиперидинил-4-он, который выделяют в виде бесцветного твердого вещества. MC/ESI 329 (М+Н)+.
д) Смесь 1'-(2,6-диметилбензоил)-4'-метил-[1,4']бипиперидинил-4-она (49,3 мг, 0,15 ммоля), 4-бромфениламина (29 мг, 0,165 ммоля), уксусной кислоты (18 мг, 0,30 ммоля) и NaBH(OAc)3 (35 мг, 0,165 ммоля) в 1,2-дихлорэтане (4 мл) перемешивают 16 часов при комнатной температуре. Смесь разбавляют этилацетатом, экстрагируют 2 н. гидроокисью натрия и соляным раствором и сушат сульфатом натрия. Растворитель удаляют и остаток подвергают хроматографии (RP-18, метанол/вода 8:2→1:0). Выделяют [4-(4-бромфениламино)-4'-метил-[1,4']бипиперидинил-1'-ил]-2,6-диметилфенил)метанон в виде твердого бесцветного вещества. MC/ESI 484 (M+H)+.
Пример 52: {4-[Бензил-(4-бромфенил)амино]-4'-метил-[1,4']бипиперидинил-1'-ил}-(2,6-диметилфенил)метанон
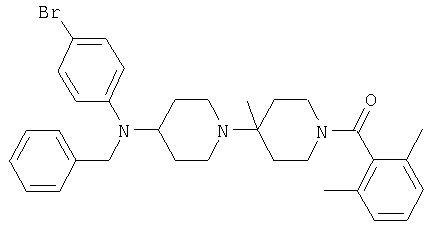
Смесь {4-[(4-бромфенил)фениламино]-4'-метил-[1,4']бипиперидинил-1'-ил}-(2,6-диметилфенил)метанона (97 мг, 0,20 ммоля), бромметилбензола (376 мг, 2,2 ммоля) и карбоната калия (138 мг, 1,0 ммоль) в диметилформамиде (3 мл) перемешивают при 100°С в течение 16 часов. Смесь разбавляют этилацетатом, экстрагируют 2 н. гидроокисью натрия и соляным раствором и сушат сульфатом натрия. Растворитель удаляют и остаток подвергают хроматографии (сначала на SiO2, (трет-бутил)метиловый эфир, и затем RP-18, метанол/вода 8:2). Указанное в заглавии соединение выделяют в виде твердого бесцветного вещества. MC/ESI 574 (М+Н)+.
Пример 53: [4-(Бензилфениламино)-4'-метил-[1,4']бипиперидинил-1'-ил]-(2,6-диметилфенил)метанон
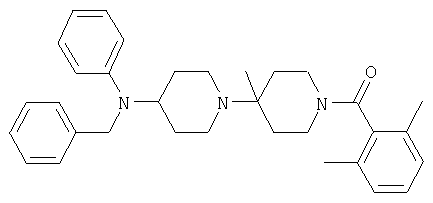
Соединение получают из (2,6-диметилфенил)-(4'-метил-4-фениламино-[1,4']бипиперидинил-1'-ил)метанона и бромистого бензила, следуя аналогичной методике, описанной в примере 52. MC/ESI 496 (М+Н)+. Исходное вещество может быть получено из 1'-(2,6-диметилбензоил)-4'-метил-[1,4']бипиперидинил-4-она, следуя подобной методике, описанной в примере 51д). MC/ESI 406 (М+Н)+.
Следуя методике из примера 53 выше и применяя подходящие исходные вещества, можно получить соединения формулы Х3
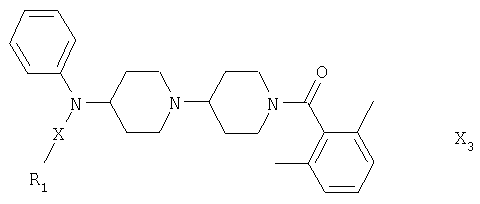
где -X-R1 имеет значения, указанные в табл.3 ниже.
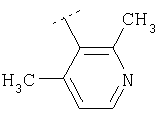
Пример 56: (2,4-Диметилпиридин-3-ил)-{4'-метил-4-[фенил-(4-трифторметил-фенил')амино]-[1,4']бипиперидинил-1'-ил)метанон
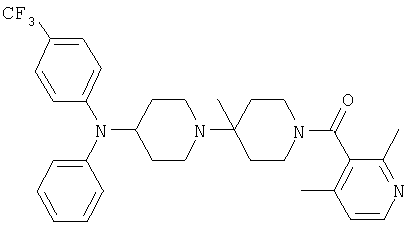
Это соединение получают из трет-бутилового эфира 4-(4-трифторметил-фениламино)пиперидин-1-карбоновой кислоты, используя методику, описанную в примере 1. MC/ESI 551 (М+Н)+. Исходное вещество получают из 4-трифторметил-фениламина и трет-бутилового эфира 4-оксопиперидин-1-карбоновой кислоты, следуя методике, описанной в примере 51д). MC/ESI 345 (М+Н)+.
Пример 57: [4-(Бифенил-4-илфениламино)-4'-метил-[1,4']бипиперидинил-1'-ил]-(2,6-диметилфенил)метанон
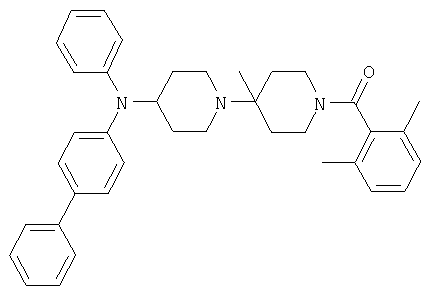
Это вещество получают из трет-бутилового эфира 4-фениламинопиперидин-1-карбоновой кислоты и 4-бромбифенила, используя методику, описанную в примере 1. MC/ESI 558 (М+Н)+.
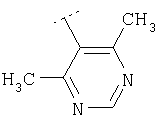
Пример 58: {4-[(4-Бромфенил)фениламино]-[1,4']бипиперидинил-1'-ил}-(4,6-диметилпиримидин-5-ил)метанон
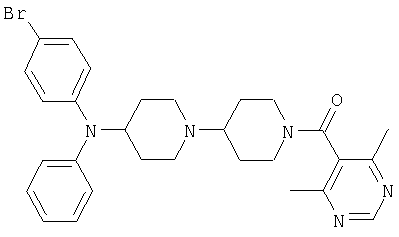
Это соединение получают из [1,4']бипиперидинил-4-ил-(4-бромфенил)фенил-амина и 4,6-диметилпиримидин-5-карбоновой кислоты, следуя методике, описанной в примере 1. MC/ESI 548 (М+Н)+.
[1,4']Бипиперидинил-4-ил-(4-бромфенил)фениламин, используемый в качестве исходного сырья, может быть получен следующим образом:
а) трет-Бутиловый эфир 4-(4-бромфениламино)пиперидин-1-карбоновой кислоты получают из 4-бромфениламина и трет-бутилового эфира 4-оксопиперидин-1-карбоновой кислоты, как описано в примере 51д). MC/ESI 355(M+H)+.
б) трет-Бутиловый эфир 4-[(4-бромфенил)фениламино]пиперидин-1-карбоновой кислоты получают из трет-бутилового эфира 4-(4-бромфениламино)пиперидин-1-карбоновой кислоты и иодбензола, как описано в примере 51. MC/ESI 431 (M+H)+.
в) (4-Бромфенил)фенилпиперидин-4-иламин получают из трет-бутилового эфира 4-[(4-бромфенил)фениламино]пиперидин-1-карбоновой кислоты, как описано в примере 1б). MC/ESI 331 (М+Н)+.
г) трет-Бутиловый эфир 4-[(4-бромфенил)фениламино]-[1,4']бипиперидинил-1'-карбоновой кислоты получают из (4-бромфенил)фенилпиперидин-4-иламина и трет-бутилового эфира 4-оксопиперидин-1-карбоновой кислоты, как описано в примере 43а). MC/ESI 514 (M+H)+.
д) [1,4']Бипиперидинил-4-ил-(4-бромфенил)фениламин получают из трет-бутилового эфира 4-[(4-бромфенил)фениламино]-[1,4']бипиперидинил-1'-карбоновой кислоты, как описано в примере 1б). MC/ESI 414 (М+Н)+.
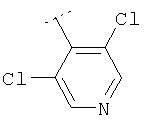
Используя методику, представленную выше, и соответствующие исходные вещества, можно получить соединения формулы Х4
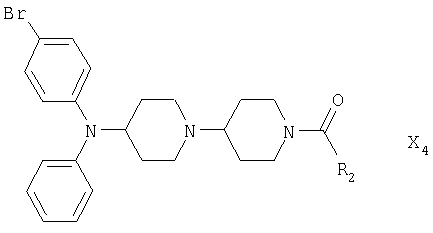
где R2 является таким, как приведено в табл.4 ниже.





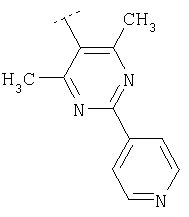
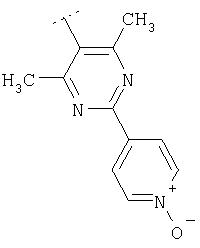
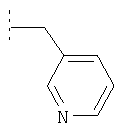
Пример 67: (2,6-Диметилфенил)-[4-(фенилпиридин-3-иламино)-[1,4']бипиперидинил-1'-ил]метанон
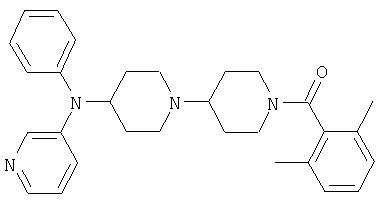
Это соединение получают из трет-бутилового эфира 4-фениламинопиперидин-1-карбоновой кислоты и 3-бромпиридина, используя методику, описанную в примере 58 и 58б) - д). MC/ESI 469 (М+Н)+.
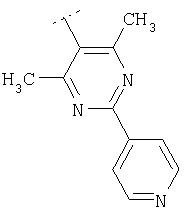
Следуя методике, описанной выше, могут быть получены соединения формулы Х5
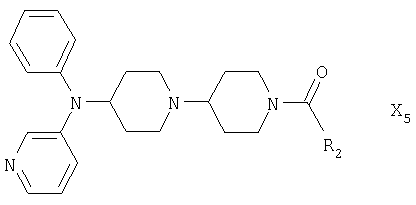
где R2 является таким, как приведено в табл.5 ниже.

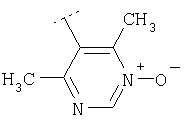
Пример 73: (4,6-Диметилпиримидин-5-ил)-[4'-метил-4-(фенилпиридин-3-ил-амино)-[1,4']бипиперидинил-1'-ил]метанон
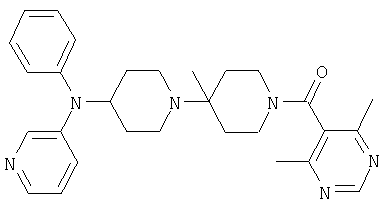
Это соединение получают из фенилпиперидин-4-илпиридин-3-иламина и трет-бутилового эфира 4-фениламинопиперидин-1-карбоновой кислоты, применяя методику, описанную в примере 1, 1в) и 1г). MC/ESI 485 (M+H)+.
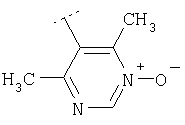
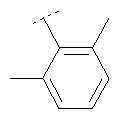
Следуя методике, представленной в примере 73, могут быть получены соединения формулы Х6
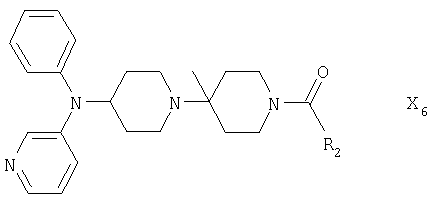
где R2 имеет значения, приведенные в табл.6.


Пример 77: {4-[(4-Бромфенил)фениламино]-4'-метил-[1,4']бипиперидинил-1'-ил}-(4,6-диметилпиримидин-5-ил)метанон
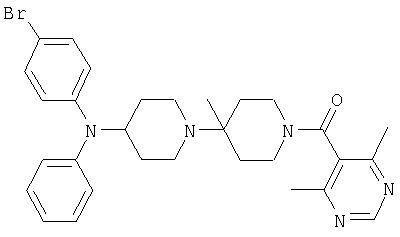
Это соединение получают из (4-бромфенил)фенилпиперидин-4-иламина и трет-бутилового эфира 4-фениламинопиперидин-1-карбоновой кислоты, применяя методику, описанную в примере 1, 1в) и 1г). MC/ESI 562 (М+Н)+.
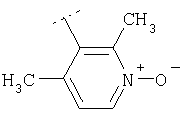
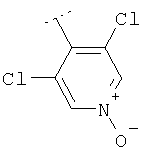
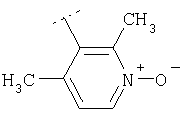
Пример 78: (4-[(4-Бромфенил)фениламино]-4'-метил-[1,4']бипиперидинил-1'-ил}-(2,4-диметил-1-оксипиридин-3-ил)метанон
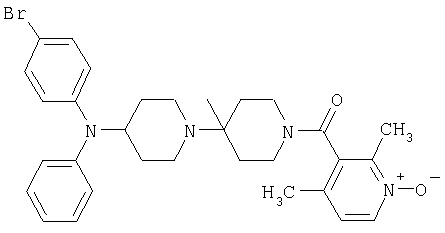
Это соединение получают из (4-бромфенил)фенилпиперидин-4-иламина и трет-бутилового эфира 4-фениламинопиперидин-1-карбоновой кислоты, применяя методику, описанную в примере 1, 1в) и 1г). MC/ESI 577 (М+Н)+.
Пример 79: [4-(Бензо[1,3]диоксол-5-илбензиламино)-4'-метил-[1,4']бипиперидинил-1'-ил]-(2,6-диметилфенил)метанон
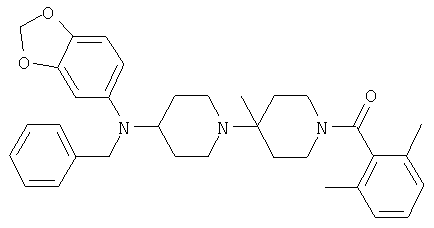
Это соединение получают из 1'-(2,6-диметилбензоил)-4'-метил-[1,4']бипиперидинил-4-она и бензо[1,3]диоксол-5-иламина, следуя методике, описанной в примерах 51 и 52. MC/ESI 540 (М+Н)+.
Пример 80: {4-[1,3-Бензодиоксол-5-ил-(2-метилтиазол-4-илметил)амино]-4'-метил-[1,4']бипиперидинил-1'-ил}-(2,6-диметилфенил)метанон
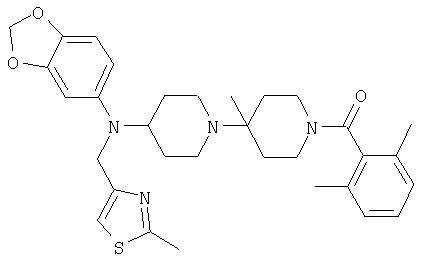
Это соединение получают из 1'-(2,6-диметилбензоил)-4'-метил-[1,4']бипиперидинил-4-она и бензо[1,3]диоксол-5-иламина, следуя методике, описанной в примерах 51 и 52. MC/ESI 561 (М+Н)+.
Пример 81: {4-[(4-Бромфенил)пиридин-3-иламино]-4'-метил-[1,4']бипиперидинил-1'-ил}-(2,4-диметил-1-оксипиридин-3-ил)метанон
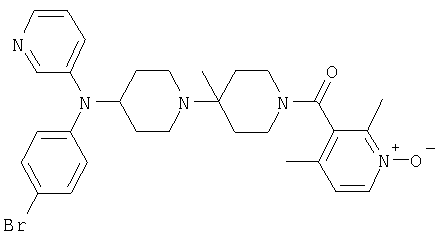
Это соединение получают из трет-бутилового эфира 4-(пиридин-3-иламино)-пиперидин-1-карбоновой кислоты и 1,4-дибромбензола, следуя методике, описанной в примере 1. MC/ESI 578 (М+Н)+.
Пример 82: [4-(Бензилфениламино)-4'-метил-[1,4']бипиперидинил-1'-ил]-(2,4-диметил-1-оксипиридин-3-ил)метанон
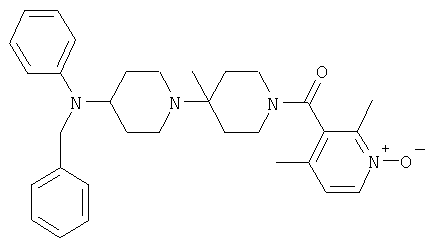
Это соединение получают из фенилпиперидин-4-иламина, следуя методике, описанной в примерах 52 и 1. MC/ESI 513 (М+Н)+.
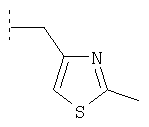
Пример 83: (2,4-Диметил-1-оксипиридин-3-ил)-{4'-метил-4-[(2-метилтиазол-4-илметил)фениламино]-[1,4']бипиперидинил-1'-ил}метанон
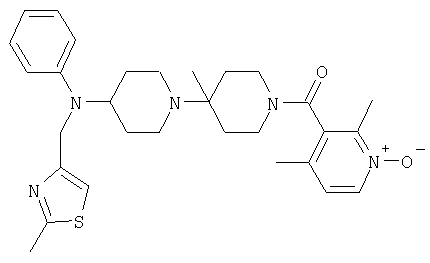
Это соединение получают из (4'-метил-[1,4']бипиперидинил-4-ил)-(2-метил-тиазол-4-илметил)фениламина, используя методику, описанную в примере 1. MC/ESI 534 (M+H)+.
(4'-Метил-[1,4']бипиперидинил-4-ил)-(2-метилтиазол-4-илметил)фениламин, используемый в качестве исходного сырья, получают следующим образом: смесь трет-бутилового эфира 4-(бензилфениламино)-4'-метил-[1,4']бипиперидинил-1'-карбоновой кислоты (1,0 г, 2,16 ммоля), муравьинокислого аммония (0,5 г, 7,92 ммоля) и Pd(OH)2 (20%) на угле (0,25 г) в метаноле (25 мл) кипятят с обратным холодильником в течение 3 часов. Катализатор отфильтровывают и промывают метанолом. Растворитель удаляют и остаток растворяют в этилацетате. Органический раствор экстрагируют 1 н. гидроокисью натрия и соляным раствором и сушат сульфатом натрия. После удаления растворителя получают технический трет-бутиловый эфир 4'-метил-4-фениламино-[1,4']бипиперидинил-1'-карбоновой кислоты, который применяют на следующей стадии без дальнейшей очистки. MC/ESI 374 (М+Н)+.
трет-Бутиловый эфир 4'-метил-4-фениламино-[1,4']бипиперидинил-1'-карбоновой кислоты превращают в (4'-метил-[1,4']бипиперидинил-4-ил)-(2-метил-тиазол-4-илметил)фениламин, используя методику, описанную в примерах 52 и 1г).
Соединения формулы I в свободной форме или в виде фармацевтически приемлемой соли проявляют ценные фармакологические свойства, например, в качестве антагонистов CCR5, например, как показано в исследованиях in vitro, и поэтому показаны для терапии.
а) Анализ связывания мембран CCR5
Человеческий CCR5 используется для генерирования устойчивых клеток, инфицированных вирусной нуклеиновой кислотой, в клетках К1 яичника китайского хомячка (СНО). Мембраны, полученные из этих подвергнутых трансфекции клеток CCR5, применяют в анализе связывания радиоактивного лиганда, используя в качестве лиганда 125-1 MIP-1α, и соединения формулы I исследуют на ингибиторную активность. Данные исследования приведены в значениях ИК50, то есть в величине концентрации соединения, требующейся для достижения 50%-го ингибирования связывания [I-125]MIP -1α. В данном анализе соединения формулы I характеризуются величиной ИК50≤1 мкМ. Соединения из примеров 16, 53 и 83 имеют ИК50 от 2 до 3 нМ соответственно.
б) Функциональный анализ CCR5 - мобилизация Са2+
Человеческий CCR5 используется для генерирования устойчивых клеток, инфицированных вирусной нуклеиновой кислотой, в клетках К1 СНО. Эти подвергнутые трансфекции клетки CCR5 применяют для оценки мобилизации Са2+ в ответ на стимулирование ССР5-лигандами MIP-1α, MIP-1β, HCC-1(9-74) или RANTES (регулируемый по активации нормальных Т-лимфоцитов экспрессированный и секретированный цитокин). Для анализа клетки нагружают чувствительным к Са2+ флуорохромом (Fluo3 или Fluo4). Используют концентрации лиганда между 0,01-100 нМ для индуцирования мобилизации Са2+, которую регистрируют с помощью флуорометра с соответствующей настройкой.
Для оценки активности исследуемых соединений снимается показание флуоресценции, соответствующее нулевой линии, после чего прибавляют к клеткам соединения в желаемой концентрации и затем снимают показания флуоресценции в течение определенного времени для оценки того, проявляют ли соединения агонистические эффекты. Затем к смеси прибавляют агонист и регистрируют флуоресценцию. Ингибирование потока Са2+ в присутствии исследуемых соединений рассчитывается, исходя из ингибирования максимальной флуоресценции, вызванного агонистом. Значения ИК50 рассчитываются по кривым зависимости от дозы, полученным для исследуемых соединений. В данном анализе соединения формулы I имеют значение ИК50≤1 мкМ. Например, соединения из примеров 1, 18 и 52 имеют значения ИК50 10, 9 и 4 соответственно,
в) Функциональный анализ CCR5 - хемотаксис
Подвергнутые трансфекции клетки CCR5 генерируются в Т-лимфоцитах Jurkat или в мышиной линии В-клеток-предшественников L1.2. Миграцию подвергнутых трансфекции клеток CCR5 исследуют в системе вставок транслуночных тканевых камер с использованием агониста CCR5 MIP-1α, в концентрации 1-100 нМ. Клетки, мигрирующие в ответ на агонист, количественно оценивали по сравнению с контролем при использовании буфера в проточном цитометре. Предназначенные для испытания соединения прибавляют к клеткам и в компартменты агонистов. Значения ИК50 рассчитывают из кривых зависимости от концентрации, полученных в опытах с соединениями в присутствии MIP-1α. Согласно этому анализу соединения формулы I имеют величину ИК50≤1мкМ.
г) Эксперименты, проведенные на мышиных животных моделях, показывают, что коррекция стенки сосуда после экспериментального повреждения (например, вызванного аллотрансплантацией) существенно тормозится в отсутствие функционального CCR5.
Соединения формулы I являются поэтому полезными для предупреждения и/или лечения заболеваний или нарушений, опосредствованных взаимодействиями между хемокиновыми рецепторами, например CCR5, и их лигандами, например, при трансплантации, как, например, острое или хроническое отторжение органа, тканевых или клеточных аллотрансплантатов или ксенотрансплантатов или замедленное функционирование трансплантата, таких заболеваний, как аутоиммунные заболевания, например ревматоидный артрит, системная красная волчанка, тиреоидит Хашимото, рассеянный склероз, тяжелая миастения, диабет типа I или II и связанные с этим нарушения, васкулит, пернициозная анемия, синдром Шегрена, увеит, псориаз, гнездная алопеция и другие аллергические заболевания, например алергическая астма, атопический дерматит, аллергический ринит/конъюнктивит, аллергический контактный дерматит, воспалительные заболевания необязательно со скрытыми аберрантными реакциями, например воспалительное заболевание кишечника, болезнь Крона или язвенный колит, наследственная бронхиальная астма, воспалительное поражение легкого, воспалительное поражение печени, воспалительное поражение почечных клубочков, атеросклероз, остеоартрит, вызывающий раздражение контактный дерматит и другие экзематозные дерматиты, себорейная экзема, кожные проявления иммунологически опосредствованных нарушений, воспалительное заболевание глаз, кератоконъюнктивит, миокардит или гепатит, ишемия/нарушение повторной перфузии, например инфаркт миокарда, удар, ишемия пищеварительного канала, почечная недостаточность или геморрагический шок, травматический шок и другие, рак, например солидные опухоли или рак лимфатической системы, как, например, Т-клеточные лимфомы или лимфолейкозы, метастазирование или ангиогенез, инфекционные заболевания, например токсический шок (например, индуцированный суперантигеном), септический шок, респираторный дистресс-синдром взрослых или вирусные инфекции, например СПИД. Под трансплантацией подразумеваются алло- или ксенотрансплантаты, например, клеток, тканей или солидных органов, например панкреатических островков, стволовых клеток, костного мозга, роговичной ткани, нейронной ткани, сердца, легкого, объединенного сердца-легкого, почки, печени, кишечника, поджелудочной железы, трахеи или пищевода. Хроническое отторжение также называется заболеваниями трансплантированных сосудов.
Для указанных выше применений требуемая дозировка, конечно, варьируется в зависимости от способа введения, от конкретного состояния, подвергающегося лечению, и от желаемого эффекта. В общем, показано, что удовлетворительные результаты получают систематически при дневных дозах примерно от 0,01 до 10 мг/кг массы тела. Как показано, дневная доза для более крупных млекопитающих, например для людей, находится в пределах примерно от 0,5 мг до примерно 1000 мг, обычно она вводится, например, в виде дробных доз до четырех раз в день или в виде формы с замедленным высвобождением лекарственного вещества. Подходящие формы со стандартными дозами для перорального введения содержат примерно от 1 до 500 мг активного ингредиента.
Соединения формулы I могут вводиться любым общепринятым способом, в частности, через тонкий кишечние, например, перорально, например, в виде таблеток или капсул, или парентерально, например, в виде инъекционных растворов или суспензий, местно, например, в виде лосьонов, гелей, мазей или кремов, или в форме для введения через нос или в виде суппозиториев. Фармацевтические композиции, включающие соединение формулы I в свободной форме или в виде фармацевтически приемлемой соли вместе с, как минимум, одним фармацевтически приемлемым носителем или разбавителем, могут быть приготовлены общепринятым способом путем смешения с фармацевтически приемлемым носителем или разбавителем.
Соединения формулы I могут применяться в свободной форме или в виде фармацевтически приемлемой соли, например, как указано выше. Такие соли могут быть получены общепринятым способом и они проявляют активность такого же порядка, что и соединения в свободной форме.
В соответствии с упомянутым выше настоящее изобретение также обеспечивает:
1.1. Способ предупреждения или лечения нарушений или заболеваний, опосредствованных взаимодействиями между хемокиновыми рецепторами и их лигандами, например, такими, как указано выше, у субъекта при необходимости такого лечения, этот способ включает введение упомянутому субъекту эффективного количества соединения формулы I или его фармацевтически приемлемой соли.
1.2. Способ предупреждения или лечения острого или хронического отторжения трансплантата или воспалительных, или аутоиммунных заболеваний, например, таких, как указано выше, у субъекта при необходимости такого лечения, способ включает введение упомянутому субъекту эффективного количества соединения формулы I или его фармацевтически приемлемой соли.
2. Соединение формулы I или его фармацевтически приемлемую соль для использования в качестве фармацевтического препарата, например, по любому из способов, указанных в п.п.1.1 или 1.2 выше.
3. Фармацевтическую композицию, например, для применения в любом из способов, указанных в п.п.1.1 или 1.2 выше, включающую соединение формулы I или его фармацевтически приемлемую соль в сочетании с фармацевтически приемлемым разбавителем или носителем для него.
4. Соединение формулы I или его фармацевтически приемлемую соль для применения с целью получения фармацевтической композиции для использования в любом из способов, описанных в п.п.1.1 или 1.2 выше.
Соединения формулы I могут быть применены в виде только одного активного ингредиента или в сочетании, например, в виде адъюванта к другим лекарственным средствам, например, при иммунодепрессивных или иммуномодулирующих схемах лечения, или к другим противовоспалительным средствам, например, для лечения или предупреждения острого или хронического отторжения алло- или ксенотрансплантатов или воспалительных, или аутоиммунных заболеваний, к химиотерапевтическому средству или противоинфекционному средству, например противовирусному средству, как, например, к антиретровирусному средству или к антибиотику. Например, соединения формулы I могут быть применены в комбинации с ингибитором кальцинеурина, например с циклоспорином А или FK 506; с макроциклическим лактоном, обладающим иммунодепрессивными свойствами, например рапамицином, 40-O-(2-гидроксиэтил)-рапамицином, СС1779 или АВТ578; с аскомицином, обладающим иммунодепрессивными свойствами, например АВТ-281, ASM981, и т.д.; с кортикостероидами; циклофосфамидом; азатиоприном; метотрексатом; лефлуномидом; мизорибином; микофеноловой кислотой; микофенолятом мофетила; 15-дезоксиспергуалином или его иммунодепрессивными гомологами, аналогами или производными; с ускоряющим хоминг лимфоцитов средством, например, FTY720; моноклональными антителами к рецепторам лейкоцитов, например МНС, CD2, CD3, CD4, CD7, CD8, CD11a/CD18, CD25, CD27, CD28, CD40, CD45, CD58, CD80, CD86, CD137, ICOS, CD150 (SLAM), ОХ40, 4-1BB, или к их лигандам, например CD 154, или к их антагонистам; с другими иммуномодулирующими соединениями, например, с рекомбинантной связывающей молекулой, содержащей, как минимум, часть внеклеточного домена CTLA4 или его мутанта, например, как минимум, часть внеклеточного домена CTLA4 или его мутанта, связанного с белковой последовательностью не CTLA4, например CTLA4Ig (указано, к примеру, в Американской коллекции типовых культур АТСС 68629), или его мутанта, например LEA29Y; с ингибиторами адгезии молекул, например антагонистами LFA-1, антагонистами ICAM-1 или-3, антагонистами VCAM-4 или антагонистами VLA-4; или с антителами против хемокина, или антителами против хемокиновых рецепторов, или низкомолекулярными антагонистами хемокиновых рецепторов, например антителами против МСР-1.
Когда соединения формулы I вводятся в комбинации с другими иммунодепрессантами/иммуномодуляторами, противовоспалительными или химиотерапевтическими средствами, дозировки совместно вводимого иммунодепрессанта, иммуномодулятора, противовоспалительного или химиотерапевтического соединения будут, конечно, варьироваться в зависимости от типа совместно вводимого лекарственного средства, например, в зависимости от того, является ли оно стероидом или ингибитором кальцинеурина, в зависимости от специфического используемого лекарственного средства, от подвергающегося лечению состояния и так далее. В соответствии с упомянутым выше настоящее изобретение представляется еще в одном аспекте:
5. Способ, как он определен выше, включающий совместное введение, например, сопутствующее или последовательное, терапевтически эффективного нетоксического количества соединения формулы I и, как минимум, второго лекарственного препарата, например иммунодепрессанта, иммуномодулятора, противовоспалительного, противоинфекционного или химиотерапевтического лекарственного средства, например, указанных выше.
6. Фармацевтическая комбинация, например комплект, включающий а) первое средство, являющееся антагонистом CCR5, например соединение формулы I, как здесь раскрывается, в свободной форме или в виде фармацевтически приемлемой соли и б) как минимум, одно сопутствующее средство, например иммунодепрессант, иммуномодулятор, противовоспалительное, антибактериальное или химиотерапевтическое лекарственное средство. Комплект может включать инструкции по применению.
Подразумевается, что термины "совместное введение" или "комбинированное введение" или им подобные, используемые здесь, охватывают введение выбранных терапевтических средств отдельному больному и включают схемы лечения, в которых такие средства необязательно вводятся одинаковым способом или в одно и то же время.
Термин "фармацевтическая комбинация", как он используется в контексте, означает продукт, получаемый в результате смешения или объединения более чем одного активного ингредиента, и включает как определенные, так и не постоянные комбинации активных ингредиентов. Термин "определенная комбинация" означает, что активные ингредиенты, например соединение формулы I и сопутствующее средство, оба вводятся больному одновременно в виде одной порции или дозы. Термин "не постоянная комбинация" означает, что активные ингредиенты, например соединение формулы I и сопутствующее средство, оба вводятся больному в виде отдельных порций или одновременно, совместно, или последовательно без особых временных рамок, при этом такое введение обеспечивает в организме больного терапевтически эффективные уровни двух соединений. Такое введение также используется при терапии с применением смеси, например введение 3 или более активных ингредиентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ЭРГОЛИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛИГАНДОВ ХЕМОКИННОГО РЕЦЕПТОРА | 2006 |
|
RU2416613C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛА КАК ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА | 2005 |
|
RU2470916C2 |
| ИНГИБИТОРЫ АСПАРТАТ-ПРОТЕАЗЫ | 2006 |
|
RU2424231C2 |
| ИНГИБИТОРЫ MAGL | 2017 |
|
RU2754536C1 |
| НОВЫЕ ГИДРОКСИСЛОЖНОЭФИРНЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2016 |
|
RU2734418C2 |
| КОМБИНАЦИИ АКТИВАТОРА (АКТИВАТОРОВ) РЕЦЕПТОРА, АКТИВИРУЕМОГО ПРОЛИФЕРАТОРОМ ПЕРОКСИСОМ (РАПП), И ИНГИБИТОРА (ИНГИБИТОРОВ) ВСАСЫВАНИЯ СТЕРИНА И ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ СОСУДОВ | 2008 |
|
RU2483724C2 |
| МОДУЛЯТОРЫ SHIP1 И ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ | 2014 |
|
RU2679805C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ АРИЛИМИДАЗОЛА, ИХ ПРЕПАРАТЫ И ИХ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2003 |
|
RU2323216C2 |
| FGFR И ЕГО ИНГИБИТОР МУТАЦИЙ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2811207C1 |
| ПРОИЗВОДНОЕ ПИРИМИДИН-4,6-ДИАМИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2022 |
|
RU2834353C2 |
Изобретение относится к новым производным бипиперидина формулы (I)
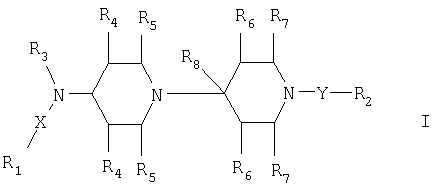
где
X означает прямую связь, -СН2-, -СН2-СН2- или -CHR9-;
R1 означает необязательно R10- и/или R11-замещенный фенил, необязательно R10- и/или R11-замещенный гетероарил, N-окись необязательно R10- и/или R11-замещенного гетероарила или необязательно R10- и/или R11-замещенный нафтил;
R2 имеет одно из значений, приведенных для R1, или означает необязательно R10-замещенный (С1-С6)алкил, необязательно R10-замещенный (С3-С6)циклоалкил, необязательно R10-замещенный адамантил;
R3 имеет одно из значений, приведенных для R1;
каждый из R4, R5, R6 и R7 означает водород;
R8 означает водород или (С1-С6)алкил;
R9 означает (С1-С6)алкил или (С3-С6)циклоалкил;
R10 представляет от 1 до 4 заместителей, независимо выбранных из (С1-С6)алкила, (С1-С6)гидроксиалкила, (С2-С6)алкоксиалкила, (C1-C6) галоидалкила, (С3-С6)-циклоалкила, фенила, гетероарила, N-окиси гетероарила, фтора, хлора, брома, йода, гидроксила, OR9, CONH2, CONHR9, CONR9R9, СООН, CF3, CHF2, CH2F, CN, NH2, NHR9, NR9R9, NHC(O)R9, NR9C(O)R9;
R11 представляет два соседних заместителя, которые образуют аннелированное 4-7-членное неароматическое кольцо, необязательно содержащее до двух гетероатомов, выбранных независимо из азота, кислорода и серы; и
Y означает прямую связь, -С(O)-, -S(O2)-, -СН2-;
в свободной форме или в виде соли.
Соединения формулы (I) и их соли обладают антагонистической активностью в отношении CCR5 рецептора и могут найти применение в медицине. 2 н. и 6 з.п. ф-лы, 6 табл.
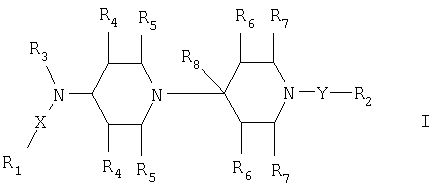
где X означает прямую связь, -CH2-, -СН2-СН2- или -CHR9-;
R1 означает необязательно R10- и/или R11-замещенный фенил, необязательно R10- и/или R11-замещенный гетероарил, N-окись необязательно R10- и/или R11-замещенного гетероарила или необязательно R10- и/или R11-замещенный нафтил;
R2 имеет одно из значений, приведенных для R1, или означает необязательно R10-замещенный (С1-С6)алкил, необязательно R10-замещенный (С3-С6)циклоалкил, необязательно R10-замещенный адамантил;
R3 имеет одно из значений, приведенных для R1;
каждый из R4, R5, R6 и R7 означает водород;
R8 означает водород или (С1-С6)алкил;
R9 означает (С1-С6)алкил или (С3-С6)циклоалкил;
R10 представляет от 1 до 4 заместителей, независимо выбранных из (С1-С6)алкила, (С1-С6)гидроксиалкила, (С2-С6)алкоксиалкила, (C1-С6) галоидалкила, (С3-С6)-циклоалкила, фенила, гетероарила, N-окиси гетероарила, фтора, хлора, брома, йода, гидроксила, OR9, CONH2, CONHR9, CONR9R9, СООН, CF3, CHF2, CH2F, CN, NH2, NHR9, NR9R9, NHC(O)R9, NR9C(O)R9;
R11 представляет два соседних заместителя, которые образуют аннелированное 4-7-членное неароматическое кольцо, необязательно содержащее до двух гетероатомов, выбранных независимо из азота, кислорода и серы; и
Y означает прямую связь, -С(O)-, -S(O2)-, -СН2-,
в свободной форме или в виде соли.
| ПРОИЗВОДНЫЕ N-АЛКИЛЕНПИПЕРИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, ОПТИЧЕСКИ ЧИСТЫЕ ПРОИЗВОДНЫЕ N-АЛКИЛЕНПИПЕРИДИНА | 1992 |
|
RU2089547C1 |
| WO 00/66559 A1, 09.11.2000 | |||
| DE 19643331 A1, 23.04.1998. | |||
Авторы
Даты
2007-04-10—Публикация
2002-04-08—Подача