Ссылка на родственные заявки
[0001] По настоящей заявке испрашивается приоритет в соответствии с предварительной заявкой на патент США №62/423099, поданной 16 ноября 2016 г., которая полностью включена в настоящий документ посредством ссылки.
Предшествующий уровень техники настоящего изобретения
[0002] Моноацилглицерол-липаза (MAGL) представляет собой фермент, ответственный за гидролиз эндоканнабиноидов, таких как 2-AG (2-арахидоноилглицерин), липид на основе арахидоната, в нервной системе.
Краткое раскрытие настоящего изобретения
[0003] В настоящем раскрытии предусмотрены, например, соединения и композиции, которые являются модуляторами MAGL, и их применение в качестве лекарственных средств, способы их получения и фармацевтические композиции, которые содержат раскрытые соединения в качестве по меньшей мере одного активного ингредиента. В настоящем раскрытии также предусмотрено применение раскрытых соединений в качестве лекарственных средств и/или при производстве лекарственных средств для ингибирования активности MAGL у теплокровных животных, таких как люди.
[0004] Согласно одному аспекту предусмотрено соединение формулы (I):
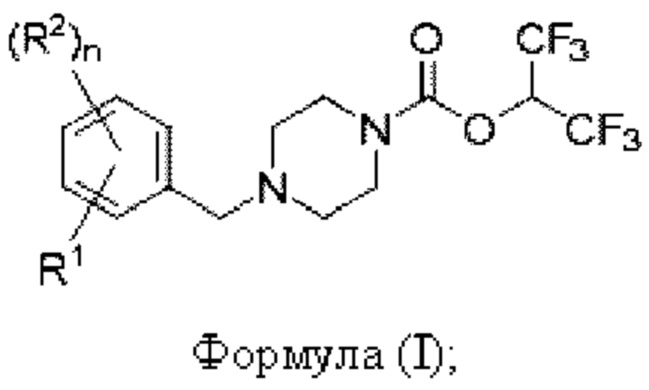
где:
R1 представляет собой -R14, -OR3, -SR4, -S(O)2R4, -N(R4)(R5), -NH(R4’) или -C≡C-(CR6R7)-R8;
каждый R2 независимо выбран из C1-6алкила, галогена, -CN, C1-6галогеналкила, -C1-6алкил(гетероциклоалкила), -OR17 и -C(O)NR18R19;
R3 представляет собой -(CR6R7)m-R8, -(CR6R7)p-Y-(CR6R7)q-R8 или -(CR6R7)t-C3-6циклоалкил-R8;
R4 представляет собой -(CR6R7)m-R8’, -(CR6R7)v-C(O)OH или -(CR6R7)p-Y-(CR6R7)q-R8;
R4’ представляет собой -(CR6R7)m-R8’, -(CR6R7)p-Y-(CR6R7)q-R8, -С4-6алкил-С(O)ОН, -С3-6циклоалкил-С(O)ОН или -С1-6алкил-С3-6циклоалкил-С(O)ОН;
Y представляет собой -О- или -N(R22)-;
R5 представляет собой C1-6алкил или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, С1-6галогеналкила и С1-6алкокси;
каждый R6 и R7 независимо выбран из Н, F и С1-6алкила или R6 и R7, вместе с углеродом, к которому они присоединены, образуют С3-6циклоалкильное кольцо;
R8 представляет собой -C(O)OR9, -C(O)R10 или -C(O)O-(CR12R13)-OC(O)R11;
R8’ представляет собой -C(O)OR9’, -C(O)R10’ или -C(O)O-(CR12R13)-OC(O)R11;
R9 представляет собой Н или С1-6алкил;
R9’ представляет собой С1-6алкил;
R10 представляет собой С1-6алкил или -NHSO2R21;
R10’ представляет собой С2-6алкил или -NHSO2R21;
R11 представляет собой С1-6алкил или С1-6алкокси;
R12 и R13 каждый независимо представляет собой Н или С1-6алкил;
R14 представляет собой -(CR15R16)m-R8 или -(CR6R7)p-Y-(CR6R7)q-R8;
каждый R15 и R16 независимо выбран из Н, F и С1-6алкила;
каждый R17 независимо выбран из Н, С1-6алкила, C1-6галогеналкила и С3-6циклоалкила;
каждый R18 и R19 независимо выбран из Н, C1-6алкила, С3-6циклоалкила, арила и гетероарила или R18 и R19, вместе с азотом, к которому они присоединены, образуют гетероциклоалкильное кольцо, необязательно замещенное одним, двумя или тремя R20;
каждый R20 независимо выбран из галогена, С1-6алкила, С1-6галогеналкила, оксо, -CN и С3-6циклоалкила;
R21 представляет собой С1-6алкил или С3-6циклоалкил;
R22 представляет собой Н, C1-6алкил или -SO2R23;
R23 представляет собой С1-6алкил;
m представляет собой 1, 2, 3 или 4;
n представляет собой 0, 1, 2, 3 или 4;
р представляет собой 2, 3 или 4;
q представляет собой 1, 2 или 3;
t представляет собой 0, 1 или 2 и
v представляет собой 3 или 4;
или его фармацевтически приемлемая соль или сольват.
[0005] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)m-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1, 2 или 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -C≡C-(CR6R7)-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где t представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где t представляет собой 0. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R6 и R7 независимо выбран из Н и C1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R6 и R7, вместе с углеродом, к которому они присоединены, образуют С3-6циклоалкильное кольцо. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5). Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R5 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R5 представляет собой -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -SR4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -S(O)2R4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R4 представляет собой -(CR6R7)v-C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где v представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где v представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R4 представляет собой -(CR6R7)m-R8’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1, 2 или 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R10’ представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R4 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’). Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)m-R8’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1, 2 или 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R10’ представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R6 и R7 независимо выбран из Н и C1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R6 и R7, вместе с углеродом, к которому они присоединены, образуют С3-6циклоалкильное кольцо. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -С4-6алкил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -С3-6циклоалкил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -С1-6алкил-С3-6циклоалкил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8, R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8, R8 представляет собой -C(O)OR9 и R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R2 независимо выбран из С1-6алкила, галогена, -CN и C1-6галогеналкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R2 независимо выбран из C1-6алкила, галогена и C1-6галогеналкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R2 представляет собой -Cl. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где каждый R2 представляет собой -CF3.
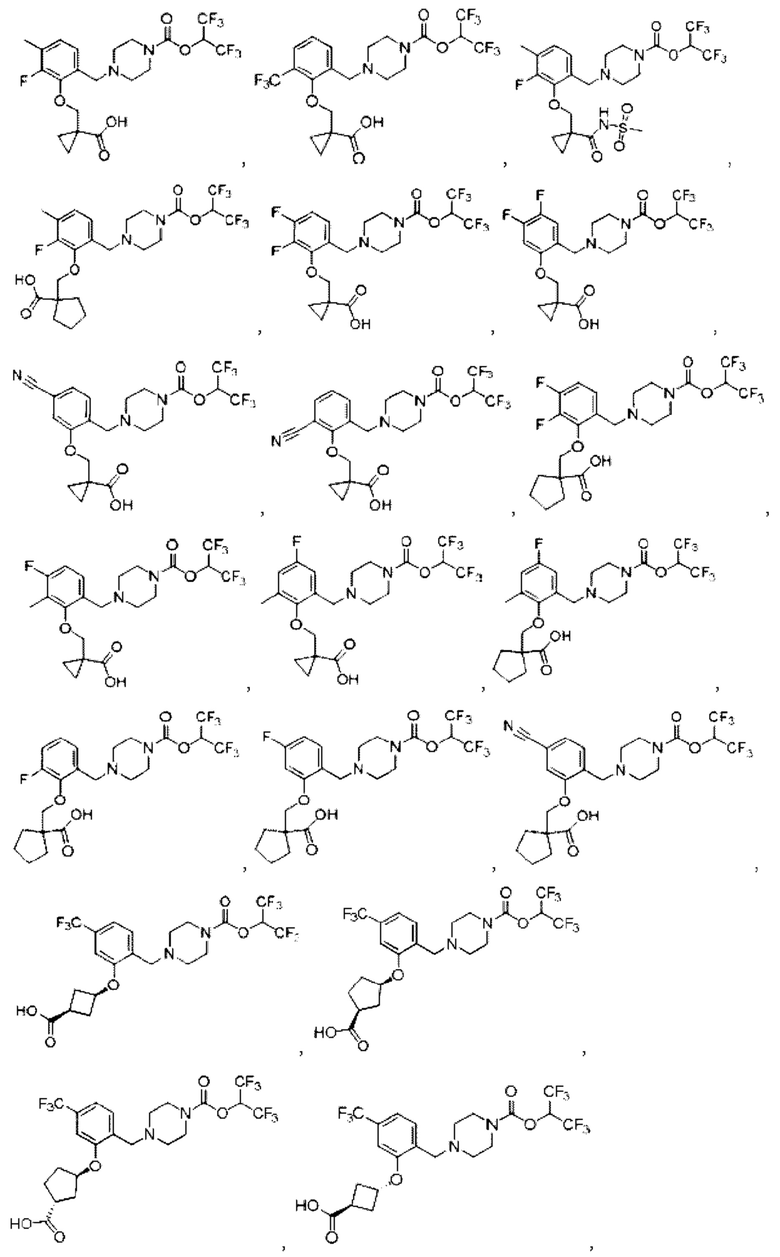
[0006] Согласно другому аспекту предусмотрено соединение, выбранное из:
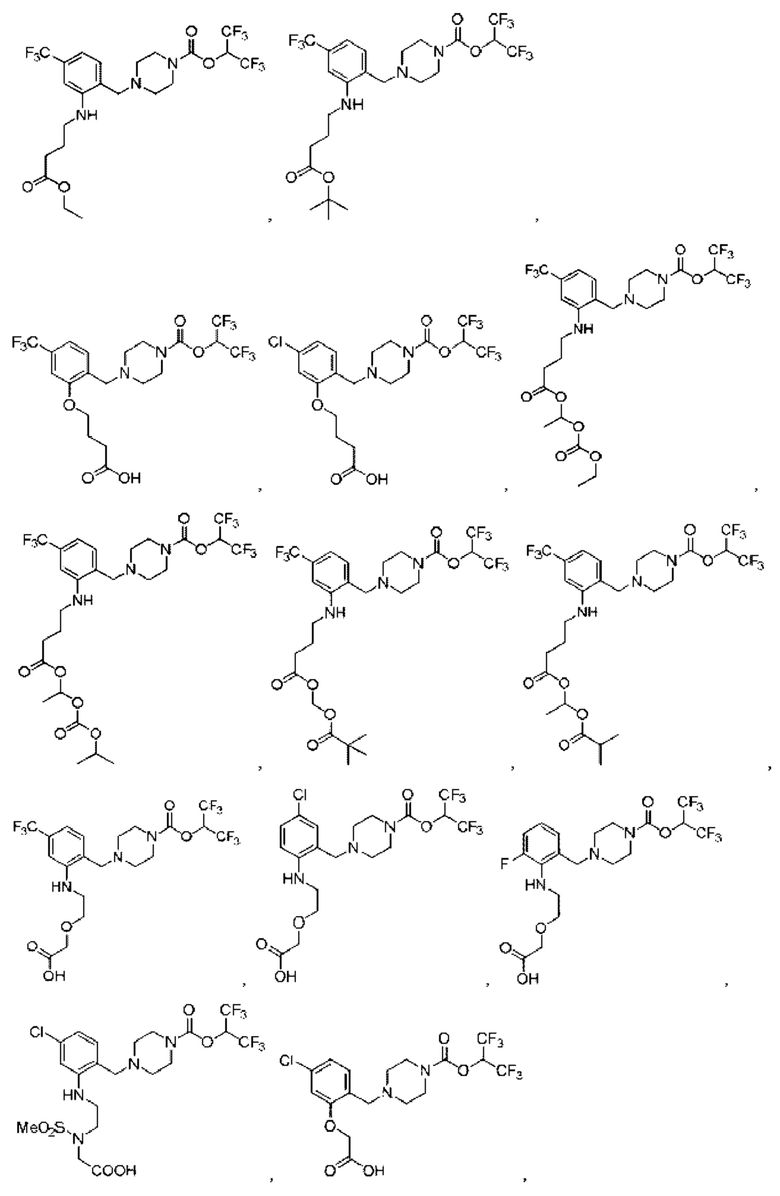
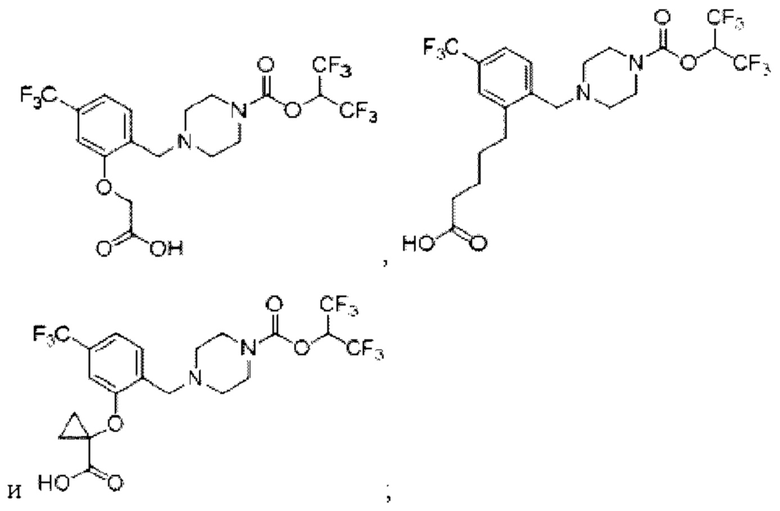
или его фармацевтически приемлемая соль или сольват.
[0007] Согласно другому аспекту предусмотрено соединение, выбранное из:
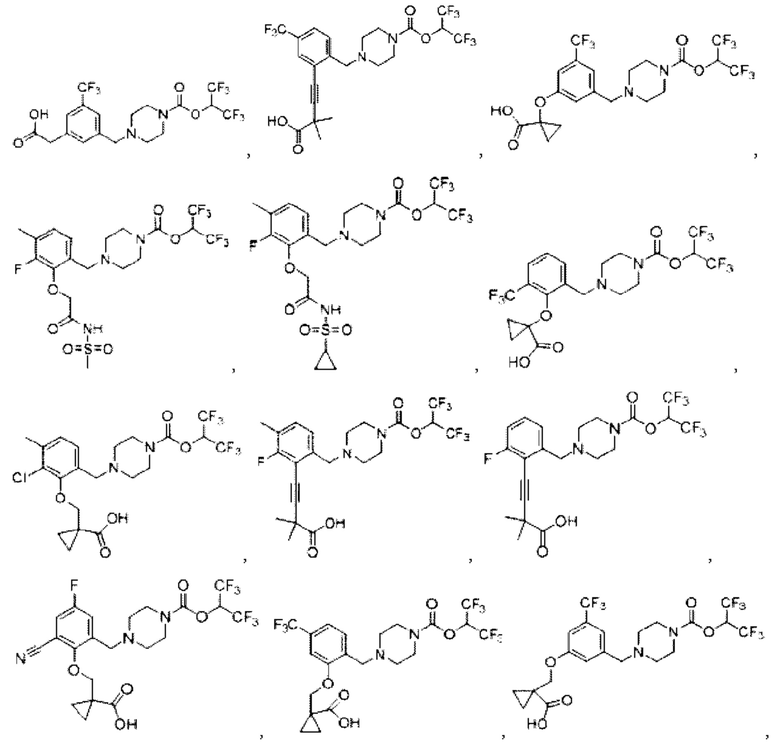
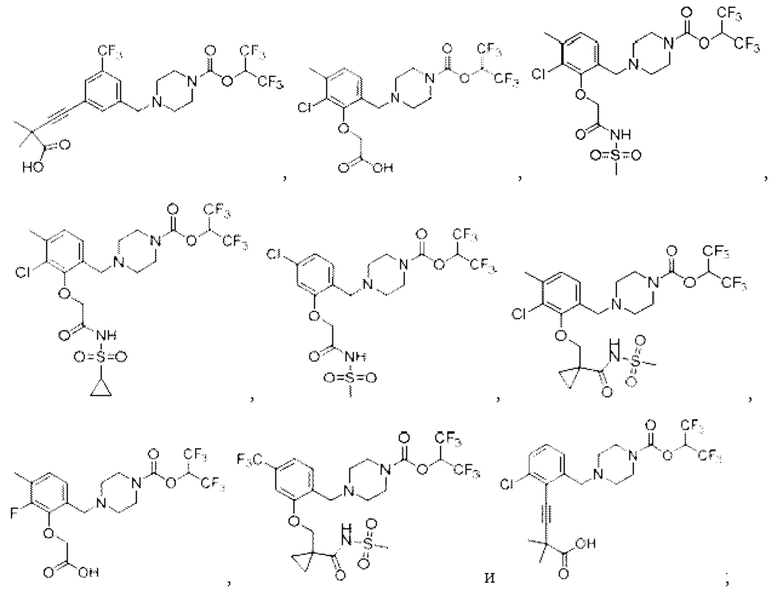
или его фармацевтически приемлемая соль или сольват.
[0008] Согласно другому варианту осуществления предусмотрена фармацевтическая композиция, содержащая описанное в настоящем документе соединение формулы (I) или его фармацевтически приемлемую соль или сольват и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
[0009] Согласно другому варианту осуществления предусмотрен способ лечения боли у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формулы (I) или его фармацевтически приемлемой соли или сольвата. Согласно некоторым вариантам осуществления боль представляет собой невропатическую боль. Согласно некоторым вариантам осуществления боль представляет собой воспалительную боль.
[0010] Согласно другому варианту осуществления предусмотрен способ лечения заболевания или нарушения у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формулы (I) или его фармацевтически приемлемой соли или сольвата, причем заболевание или нарушение представляет собой выбранное из группы, состоящей из эпилепсии/припадочного расстройства, рассеянного склероза, нейромиелита зрительного нерва (NMO), синдрома Туретта, болезни Альцгеймера и боли в животе, связанной с синдромом раздраженного кишечника. Согласно некоторым вариантам осуществления заболевание или нарушение представляет собой эпилепсию/припадочное расстройство. Согласно некоторым вариантам осуществления заболевание или нарушение представляет собой рассеянный склероз. Согласно некоторым вариантам осуществления заболевание или нарушение представляет собой нейромиелит зрительного нерва (NMO). Согласно некоторым вариантам осуществления заболевание или нарушение представляет собой синдрома Туретта. Согласно некоторым вариантам осуществления заболевание или нарушение представляет собой болезнь Альцгеймера. Согласно некоторым вариантам осуществления заболевание или нарушение представляет собой боль в животе, связанную с синдромом раздраженного кишечника.
[0011] Согласно другому варианту осуществления предусмотрен способ лечения синдрома дефицита внимания и гиперактивности (ADHD) у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формулы (I) или его фармацевтически приемлемой соли или сольвата.
Подробное описание настоящего изобретения
[0012] Настоящее изобретение направлено, по меньшей мере частично, на соединения, способные ингибировать MAGL.
[0013] Как используется в настоящем документе и в прилагаемой формуле изобретения, формы единственного числа включают в себя множественные объекты ссылки, если контекст явно не предписывает иное. Таким образом, например, ссылка на «средство» включает в себя множество таких средств, а ссылка на «клетку» включает в себя ссылку на одну или несколько клеток (или на множество клеток) и их эквиваленты. Когда диапазоны используются в настоящем документе для таких физических свойств, как молекулярная масса, или таких химических свойств, как химические формулы, все комбинации и подкомбинации диапазонов и конкретные варианты осуществления в них предназначены для включения. Термин «приблизительно» применительно к числу или числовому диапазону означает, что указанное число или числовой диапазон является приблизительным в пределах экспериментальной изменчивости (или в пределах статистической погрешности эксперимента), и, таким образом, число или числовой диапазон варьирует от 1% до 15% от указанного числа или числового диапазона. Термин «содержащий» (и родственные термины, такие как «содержит» или «имеющий», или «включающий в себя») не предназначен для исключения того, что согласно другим определенным вариантам осуществления, например, согласно варианту осуществления любой композиции вещества, композиции, способа или процесса или т.п., описанного в настоящем документе, может «состоять из» или «состоять по существу из» описанных признаков.
Определения
[0014] Как используется в описании и прилагаемой формуле изобретения, если не указано иное, следующие термины характеризуются значением, указанным ниже.
[0015] Как используется в настоящем документе, C1-Cx включает в себя С1-С2, C1-С3 … C1-Cx. C1-Cx относится к числу атомов углерода, из которых состоит фрагмент, к которому он относится (за исключением необязательных заместителей).
[0016] "Амино" относится к радикалу -NH2.
[0017] "Циано" относится к радикалу -CN.
[0018] "Нитро" относится к радикалу -NO2.
[0019] "Окса" относится к радикалу -О-.
[0020] "Оксо" относится к радикалу =O.
[0021] "Тиоксо" относится к радикалу =S.
[0022] "Имино" относится к радикалу =N-H.
[0023] "Оксимо" относится к радикалу =N-OH.
[0024] "Алкил" или "алкилен" относится к радикалу с неразветвленный или разветвленной углеводородной цепью, состоящему исключительно из атомов углерода и водорода, не содержащему ненасыщенности, содержащему от одного до пятнадцати атомов углерода (например, С1-С15 алкил). Согласно определенным вариантам осуществления алкил содержит от одного до тринадцати атомов углерода (например, C1-С13 алкил). Согласно определенным вариантам осуществления алкил содержит от одного до восьми атомов углерода (например, C1-C8 алкил). Согласно другим вариантам осуществления алкил содержит от одного до шести атомов углерода (например, C1-С6 алкил). Согласно другим вариантам осуществления алкил содержит от одного до пяти атомов углерода (например, С1-С5 алкил). Согласно другим вариантам осуществления алкил содержит от одного до четырех атомов углерода (например, С1-С4 алкил). Согласно другим вариантам осуществления алкил содержит от одного до трех атомов углерода (например, C1-С3 алкил). Согласно другим вариантам осуществления алкил содержит от одного до двух атомов углерода (например, С1-С2 алкил). Согласно другим вариантам осуществления алкил содержит один атом углерода (например, C1 алкил). Согласно другим вариантам осуществления алкил содержит от пяти до пятнадцати атомов углерода (например, С5-С15 алкил). Согласно другим вариантам осуществления алкил содержит от пяти до восьми атомов углерода (например, С5-С8 алкил). Согласно другим вариантам осуществления алкил содержит от двух до пяти атомов углерода (например, С2-С5 алкил). Согласно другим вариантам осуществления алкил содержит от трех до пяти атомов углерода (например, С3-С5 алкил). Согласно другим вариантам осуществления алкильная группа выбрана из метила, этила, 1-пропила (н-пропила), 1-метилэтила (изо-пропила), 1-бутила (н-бутила), 1-метилпропила (втор-бутила), 2-метилпропила (изо-бутила), 1,1-диметилэтила (трет-бутила), 1-пентила (н-пентила). Алкил присоединен к остальной части молекулы одинарной связью. Если специально не указано иное в описании, алкильная группа необязательно замещена одним или несколькими из следующих заместителей: гало, циано, нитро, оксо, тиоксо, имино, оксимо, триметилсиланил, -ORa, -SRa, -OC(O)Ra, -N(Ra)2, -C(O)Ra, -C(O)ORa, -C(O)N(Ra)2, -N(Ra)C(O)ORf, -OC(O)-NRaRf, -N(Ra)C(O)Rf, -N(Ra)S(O)tRf (где t представляет собой 1 или 2), -S(O)tORa (где t представляет собой 1 или 2), -S(O)tRf (где t представляет собой 1 или 2) и -S(O)tN(Ra)2 (где t представляет собой 1 или 2), где каждый Ra представляет собой независимо водород, алкил, фторалкил, циклоалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил и каждый Rf представляет собой независимо алкил, фторалкил, циклоалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил.
[0025] "Алкокси" относится к радикалу, связанному через атом кислорода -О-алкила формулы, где алкил представляет собой алкильную цепь, как определено выше.
[0026] "Алкенил" относится к радикальной группе углеводородной цепи с неразветвленный или разветвленной цепью, состоящей исключительно из атомов углерода и водорода, содержащей по меньшей мере одну двойную связь углерод-углерод и содержащей от двух до двенадцати атомов углерода. Согласно определенным вариантам осуществления алкенил содержит от двух до восьми атомов углерода. Согласно другим вариантам осуществления алкенил содержит от двух до четырех атомов углерода. Алкенил присоединен к остальной части молекулы простой связью, например, этенил (т.е., винил), проп-1-енил (например, аллил), бут-1-енил, пент-1-енил, пента-1,4-диенил и т.п. Если специально не указано иное в описании, алкенильная группа необязательно замещена одним или несколькими из следующих заместителей: галоген, циано, нитро, оксо, тиоксо, имино, оксимо, триметилсиланил, -ORa, -SRa, -OC(O)-Rf, -N(Ra)2, -C(O)Ra, -C(O)ORa, -C(O)N(Ra)2, -N(Ra)C(O)ORf, -OC(O)-NRaRf, -N(Ra)C(O)Rf, -N(Ra)S(O)tRf (где t представляет собой 1 или 2), -S(O)tORa (где t представляет собой 1 или 2), -S(O)tRf (где t представляет собой 1 или 2) и -S(O)tN(Ra)2 (где t представляет собой 1 или 2), где каждый Ra представляет собой независимо водород, алкил, фторалкил, циклоалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил и каждый Rf представляет собой независимо алкил, фторалкил, циклоалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил.
[0027] "Алкинил" относится к радикальной группе углеводородной цепи с неразветвленный или разветвленной цепью, состоящей исключительно из атомов углерода и водорода, содержащей по меньшей мере одну тройную связь углерод-углерод, содержащей от двух до двенадцати атомов углерода. Согласно некоторым вариантам осуществления алкинил содержит от двух до восьми атомов углерода. Согласно другим вариантам осуществления алкинил содержит от двух до четырех атомов углерода. Алкинил присоединен к остальной части молекулы простой связью, например, этинил, пропинил, бутинил, пентинил, гексинил и т.п. Если специально не указано иное в описании, алкинильная группа необязательно замещена одним или несколькими из следующих заместителей: галоген, циано, нитро, оксо, тиоксо, имино, оксимо, триметилсиланил, -ORa, -SRa, -OC(O)Ra, -N(Ra)2, -C(O)Ra, -C(O)ORa, -C(O)N(Ra)2, -N(Ra)C(O)ORf, -OC(O)-NRaRf, -N(Ra)C(O)Rf, -N(Ra)S(O)tRf (где t представляет собой 1 или 2), -S(O)tORa (где t представляет собой 1 или 2), -S(O)tRf (где t представляет собой 1 или 2) и -S(O)tN(Ra)2 (где t представляет собой 1 или 2), где каждый Ra представляет собой независимо водород, алкил, фторалкил, циклоалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил и каждый Rf представляет собой независимо алкил, фторалкил, циклоалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил.
[0028] "Арил" относится к радикалу, полученному из ароматической моноциклической или полициклической углеводородной кольцевой системы путем удаления атома водорода из кольцевого атома углерода. Ароматическая моноциклическая или мультициклическая углеводородная кольцевая система содержит только водород и углерод от шести до восемнадцати атомов углерода, где по меньшей мере одно из колец в кольцевой системе является полностью ненасыщенным, т.е. содержит циклическую делокализованную (4n+2) π-электронную систему в соответствии с теорией Хюккеля. Кольцевая система, из которой получены арильные группы, включает в себя, без ограничения, такие группы, как бензол, флуорен, индан, инден, тетралин и нафталин. Если специально не указано иное в описании, термин "арил" или префикс "ар" (такой как "аралкил") предназначен для включения арильных радикалов, необязательно замещенных одним или несколькими заместителями, независимо выбранными из алкила, алкенила, алкинила, галогена, фторалкила, циано, нитро, арила, аралкила, аралкенила, аралкинила, циклоалкила, гетероциклоалкила, гетероарила, гетероарилалкила, -Rb-ORa, -Rb-OC(O)-Ra, -Rb-OC(O)-ORa, -Rb-OC(O)-N(Ra)2, -Rb-N(Ra)2, -Rb-C(O)Ra, -Rb-C(O)ORa, -Rb-C(O)N(Ra)2, -Rb-O-Rc-C(O)N(Ra)2, -Rb-N(Ra)C(O)ORa, -Rb-N(Ra)C(O)Ra, -Rb-N(Ra)S(O)tRa (где t представляет собой 1 или 2), -Rb-S(O)tORa (где t представляет собой 1 или 2), -Rb-S(O)tRa (где t представляет собой 1 или 2) и -Rb-S(O)tN(Ra)2 (где t представляет собой 1 или 2), где каждый Ra представляет собой независимо водород, алкил, фторалкил, циклоалкил, циклоалкилалкил, арил (необязательно замещенный одной или несколькими гало группами), аралкил, гетероциклоалкил, гетероарил или гетероарилалкил, каждый Rb представляет собой независимо прямую связь или неразветвленную или разветвленную алкиленовую или алкениленовую цепь и Rc представляет собой неразветвленную или разветвленную алкиленовую или алкениленовую цепь.
[0029] "Арилокси" относится к радикалу, связанному через атом кислорода формулы О-арил, где арил является таким, как определено выше.
[0030] "Аралкил" относится к радикалу формулы -Rc-арил, где Rc представляет собой алкиленовую цепь, как определено выше, например, метилен, этилен и т.п. Часть алкиленовой цепи аралкильного радикала необязательно замещена, как описано выше для алкиленовой цепи. Арильная часть аралкильного радикала необязательно замещена, как описано выше для арильной группы.
[0031] "Аралкилокси" относится к радикалу связанному через атом кислорода формулы -О-аралкил, где аралкил является таким, как определено выше.
[0032] "Аралкенил" относится к радикалу формулы -Rd-арил, где Rd представляет собой алкениленовую цепь, как определено выше. Арильная часть аралкенильного радикала необязательно замещена, как описано выше для арильной группы. Часть алкениленовой цепи аралкенильного радикала необязательно замещена, как определено выше для алкениленовой группы.
[0033] "Аралкинил" относится к радикалу формулы -Re-арил, где Re представляет собой алкиниленовую цепь, как определено выше. Арильная часть аралкинильного радикала необязательно замещена, как описано выше для арильной группы. Часть алкиниленовой цепи аралкинильного радикала необязательно замещена, как определено выше для алкиниленовой цепи.
[0034] "Циклоалкил" относится к стабильному неароматическому моноциклическому или полициклическому углеводородному радикалу, состоящему исключительно из атомов углерода и водорода, который включает в себя конденсированные или мостиковые кольцевые системы, содержащие от трех до пятнадцати атомов углерода. Согласно некоторым вариантам осуществления циклоалкил содержит от трех до десяти атомов углерода. Согласно другим вариантам осуществления циклоалкил содержит от пяти до семи атомов углерода. Циклоалкил присоединен к остальной части молекулы одинарной связью. Циклоалкилы являются насыщенными (т.е. содержат только одинарные связи С-С) или частично ненасыщенными (т.е. содержат одну или несколько двойных связей или тройных связей). Примеры моноциклических циклоалкилов включают в себя, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Согласно определенным вариантам осуществления циклоалкил содержит от трех до восьми атомов углерода (например, С3-C8 циклоалкил). Согласно другим вариантам осуществления циклоалкил содержит от трех до семи атомов углерода (например, С3-С7 циклоалкил). Согласно другим вариантам осуществления циклоалкил содержит от трех до шести атомов углерода (например, С3-С6 циклоалкил). Согласно другим вариантам осуществления циклоалкил содержит от трех до пяти атомов углерода (например, С3-С5 циклоалкил). Согласно другим вариантам осуществления циклоалкил содержит от трех до четырех атомов углерода (например, С3-С4 циклоалкил). Частично ненасыщенный циклоалкил также называют "циклоалкенил". Примеры моноциклических циклоалкенилов включают в себя, например, циклопентенил, циклогексенил, циклогептенил и циклооктенил. Полициклические циклоалкильные радикалы включают в себя, например, адамантил, норборнил (например, бицикло[2.2.1]гептанил), норборненил, декалинил, 7,7-диметилбицикло[2.2.1]гептанил и т.п. Если специально не указано иное в описании, термин "циклоалкил" подразумевает включение циклоалкильных радикалов, необязательно замещенных одним или несколькими заместителями, независимо выбранными из алкила, алкенила, алкинила, галогена, фторалкила, циано, нитро, арила, аралкила, аралкенила, аралкинила, циклоалкила, гетероциклоалкила, гетероарила, гетероарилалкила, -Rb-ORa, -Rb-OC(O)-Ra, -Rb-OC(O)-ORa, -Rb-OC(O)-N(Ra)2, -Rb-N(Ra)2, -Rb-C(O)Ra, -Rb-C(O)ORa, -Rb-C(O)N(Ra)2, -Rb-O-Rc-C(O)N(Ra)2, -Rb-N(Ra)C(O)ORa, -Rb-N(Ra)C(O)Ra, -Rb-N(Ra)S(O)tRa (где t представляет собой 1 или 2), -Rb-S(O)tORa (где t представляет собой 1 или 2), -Rb-S(O)tRa (где t представляет собой 1 или 2) и -Rb-S(O)tN(Ra)2 (где t представляет собой 1 или 2), где каждый Ra представляет собой независимо водород, алкил, фторалкил, циклоалкил, циклоалкилалкил, арил (необязательно замещенный одним или несколькими галогеновыми группами), аралкил, гетероциклоалкил, гетероарил или гетероарилалкил, каждый Rb представляет собой независимо прямую связь или неразветвленную или разветвленную алкиленовую или алкениленовую цепь, и Rc представляет собой неразветвленную или разветвленную алкиленовую или алкениленовую цепь.
[0035] "Гало" или "галоген" относится к заместителям, содержащим бром, хлор, фтор или йод.
[0036] "Галогеналкил" относится к алкильному радикалу, как определено выше, который замещен одним или несколькими радикалами галогена, как определено выше.
[0037] "Фторалкил" относится к алкильному радикалу, как определено выше, который замещен одним или несколькими фторрадикалами, как определено выше, например, трифторметил, дифторметил, фторметил, 2,2,2-трифторэтил, 1-фторметил-2-фторэтил и т.п. Алкильная часть фторалкильного радикала необязательно замещена, как определено выше для алкильной группы.
[0038] "Галогеналкокси" относится к алкоксирадикалу, как определено выше, который замещен одним или несколькими радикалами галогена, как определено выше.
[0039] "Гетероциклоалкил" относится к стабильному 3-18-членному неароматическому кольцевому радикалу, который содержит от двух до двенадцати атомов углерода и от одного до шести гетероатомов, выбранных из азота, кислорода и серы. Если специально не указано иное в описании, гетероциклоалкильный радикал представляет собой моноциклическую, бициклическую, трициклическую или тетрациклическую кольцевую систему, которая включает в себя конденсированные, спиро- или мостиковые кольцевые системы. Гетероатомы в гетероциклоалкильном радикале необязательно окисляются. Один или несколько атомов азота, если они присутствуют, необязательно являются кватернизованными. Гетероциклоалкильный радикал частично или полностью насыщен. Согласно некоторым вариантам осуществления гетероциклоалкил присоединен к остальной части молекулы через любой атом кольца (колец). Примеры таких гетероциклоалкильных радикалов включают в себя, без ограничения, диоксоланил, тиенил[1,3]дитианил, декагидроизохинолил, имидазолинил, имидазолидинил, изотиазолидинил, изоксазолидинил, морфолинил, октагидроиндолил, октагидроизоиндолил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, оксазолидинил, пиперидинил, пиперазинил, 4-пиперидонил, пирролидинил, пиразолидинил, хинуклидинил, тиазолидинил, тетрагидрофурил, тритианил, тетрагидропиранил, тиоморфолинил, тиаморфолинил, 1-оксотиоморфолинил и 1,1-диоксотиоморфолинил. Если специально не указано иное в описании, подразумевается, что термин "гетероциклоалкил" включает в себя гетероциклоалкильные радикалы, как определено выше, которые необязательно замещены одним или несколькими заместителями, выбранными из алкила, алкенила, алкинила, галогена, фторалкила, оксо, тиоксо, циано, нитро, арила, аралкила, аралкенила, аралкинила, циклоалкила, гетероциклоалкила, гетероарила, гетероарилалкила, -Rb-ORa, -Rb-OC(O)-Ra, -Rb-OC(O)-ORa, -Rb-OC(O)-N(Ra)2, -Rb-N(Ra)2, -Rb-C(O)Ra, -Rb-C(O)ORa, -Rb-C(O)N(Ra)2, -Rb-O-Rc-C(O)N(Ra)2, -Rb-N(Ra)C(O)ORa, -Rb-N(Ra)C(O)Ra, -Rb-N(Ra)S(O)tRa (где t представляет собой 1 или 2), -Rb-S(O)tORa (где t представляет собой 1 или 2), -Rb-S(O)tRa (где t представляет собой 1 или 2) и -Rb-S(O)tN(Ra)2 (где t представляет собой 1 или 2), где каждый Ra представляет собой независимо водород, алкил, фторалкил, циклоалкил, циклоалкилалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил, каждый Rb представляет собой независимо прямую связь или неразветвленную или разветвленную алкиленовую или алкениленовую цепь, и Rc представляет собой неразветвленный или разветвленный алкилен или алкениленовую цепь.
[0040] "Гетероарил" относится к радикалу, полученному из 5-18-членного ароматического кольцевого радикала, который содержит от одного до семнадцати атомов углерода и от одного до шести гетероатомов, выбранных из азота, кислорода и серы. Используемый в настоящем документе гетероарильный радикал представляет собой моноциклическую, бициклическую, трициклическую или тетрациклическую кольцевую систему, в которой по меньшей мере одно из колец в кольцевой системе является полностью ненасыщенным, т.е. содержит циклическую делокализованную (4n+2) π-электронную систему в соответствии с теорией Хюккеля. Гетероарил включает в себя конденсированные или мостиковые кольцевые системы. Гетероатом(ы) в гетероарильном радикале необязательно окислен. Один или несколько атомов азота, если они присутствуют, необязательно являются кватернизованными. Гетероарил присоединен к остальной части молекулы через любой атом кольца. Если специально не указано иное в описании, подразумевается, что термин "гетероарил" включает в себя гетероарильные радикалы, как определено выше, которые необязательно замещены одним или несколькими заместителями, выбранными из алкила, алкенила, алкинила, галогена, галогеналкила, оксо, тиоксо, циано, нитро, арила, аралкила, аралкенила, аралкинила, циклоалкила, гетероциклоалкила, гетероарила, гетероарилалкила, -Rb-ORa, -Rb-OC(O)-Ra, -Rb-OC(O)-ORa, -Rb-OC(O)-N(Ra)2, -Rb-N(Ra)2, -Rb-C(O)Ra, -Rb-C(O)ORa, -Rb-C(O)N(Ra)2, -Rb-O-Rc-C(O)N(Ra)2, -Rb-N(Ra)C(O)ORa, -Rb-N(Ra)C(O)Ra, -Rb-N(Ra)S(O)tRa (где t представляет собой 1 или 2), -Rb-S(O)tORa (где t представляет собой 1 или 2), -Rb-S(O)tRa (где t представляет собой 1 или 2) и -Rb-S(O)tN(Ra)2 (где t представляет собой 1 или 2), где каждый Ra представляет собой независимо водород, алкил, фторалкил, циклоалкил, циклоалкилалкил, арил, аралкил, гетероциклоалкил, гетероарил или гетероарилалкил, каждый Rb представляет собой независимо прямую связь или неразветвленный или разветвленный алкилен или алкениленовую цепь и Rc представляет собой неразветвленный или разветвленный алкилен или алкениленовую цепь.
[0041] "N-гетероарил" относится к определенному выше гетероарильному радикалу, содержащему по меньшей мере один азот, и причем точка присоединения гетероарильного радикала к остальной части молекулы находится через атом азота в гетероарильном радикале. N-гетероарильный радикал необязательно замещен, как описано выше для гетероарильных радикалов.
[0042] "С-гетероарил" относится к определенному выше гетероарильному радикалу, и причем точка присоединения гетероарильного радикала к остальной части молекулы находится через атом углерода в гетероарильном радикале. С-гетероарильный радикал необязательно замещен, как описано выше для гетероарильных радикалов.
[0043] "Гетероарилокси" относится к радикалу, связанному через атом кислорода формулы -О-гетероарил, где гетероарил является таким, как определено выше.
[0044] "Гетероарилалкил" относится к радикалу формулы -Rc-гетероарил, где Rc представляет собой алкиленовую цепь, как определено выше. Если гетероарил представляет собой азотсодержащий гетероарил, гетероарил необязательно присоединен к алкильному радикалу у атома азота. Алкиленовая цепь гетероарилалкильного радикала необязательно замещена, как определено выше для алкиленовой цепи. Гетероарильная часть гетероарилалкильного радикала необязательно замещена, как определено выше для гетероарильной группы.
[0045] "Гетероарилалкокси" относится к радикалу, связанному через атом кислорода формулы -О-Rc-гетероарил, где Rc представляет собой алкиленовую цепь, как определено выше. Если гетероарил представляет собой азотсодержащий гетероарил, гетероарил необязательно присоединен к алкильному радикалу у атома азота. Алкиленовая цепь гетероарилалкоксирадикала необязательно замещена, как определено выше для алкиленовой цепи. Гетероарильная часть гетероарилалкоксирадикала необязательно замещена, как определено выше для гетероарильной группы.
[0046] Согласно некоторым вариантам осуществления раскрытые в настоящем документе соединения содержат одно или несколько асимметричных центров и, таким образом, дают энантиомеры, диастереомеры и другие стереоизомерные формы, которые определены в терминах абсолютной стереохимии как (R)- или (S)-. Если не указано иное, подразумевается, что все стереоизомерные формы раскрытых в настоящем документе соединений рассматриваются в настоящем изобретении. Когда описанные в настоящем документе соединения содержат алкеновые двойные связи и, если не указано иное, подразумевается, что это раскрытие включает в себя как Е, так и Z геометрические изомеры (например, цис или транс). Аналогично, все возможные изомеры, а также их рацемические и оптически чистые формы и все таутомерные формы также должны быть включены. Термин "геометрический изомер" относится к Е или Z геометрическим изомерам (например, цис или транс) алкеновой двойной связи. Термин "позиционный изомер" относится к структурным изомерам вокруг центрального кольца, таким как орто-, мета- и параизомеры вокруг бензольного кольца.
[0047] "Таутомер" относится к молекуле, в которой возможен сдвиг протона от одного атома молекулы к другому атому той же молекулы. Согласно определенным вариантам осуществления представленные в настоящем документе соединения существуют в виде таутомеров. В условиях, когда таутомеризация возможна, будет существовать химическое равновесие таутомеров. Точное соотношение таутомеров зависит от нескольких факторов, включающих в себя физическое состояние, температуру, растворитель и рН. Некоторые примеры таутомерного равновесия включают в себя:
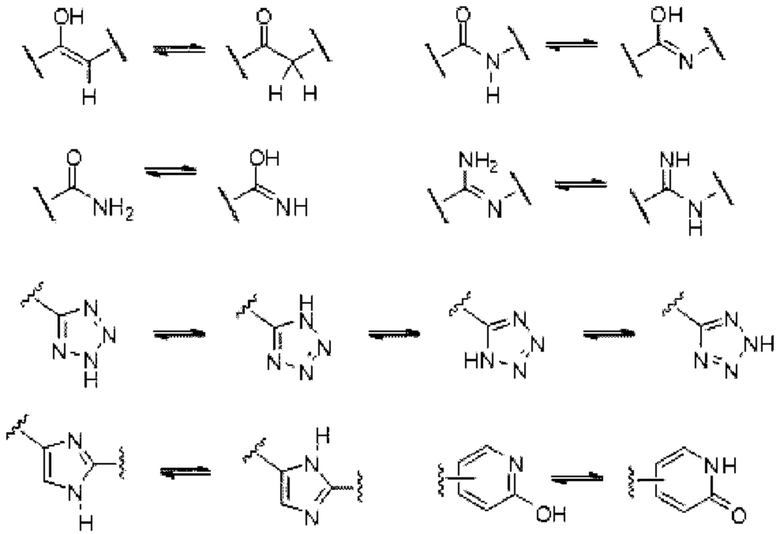
[0048] "Необязательно" означает, что впоследствии описанное событие или обстоятельство может или не может произойти, и что описание включает в себя случаи, когда происходит событие или обстоятельство, и случаи, в которых это не происходит. Например, "необязательно замещенный арил" означает, что арильный радикал является замещенным или нет, и что описание включает в себя как замещенные арильные радикалы, так и арильные радикалы, не содержащие замещения.
[0049] "Фармацевтически приемлемая соль" включает в себя как соли присоединения кислоты, так и соли присоединения основания. Предполагается, что фармацевтически приемлемая соль любого из описанных в настоящем документе пиразольных соединений охватывает любые и все фармацевтически подходящие формы солей. Предпочтительными фармацевтически приемлемыми солями описанных в настоящем документе соединений являются фармацевтически приемлемые соли присоединения кислоты и фармацевтически приемлемые соли присоединения основания.
[0050] "Фармацевтически приемлемая соль присоединения кислоты" относится к тем солям, которые сохраняют биологическую эффективность и свойства свободных оснований, которые не являются биологически или иным образом нежелательными и которые образуются с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота, йодистоводородная кислота, фтористоводородная кислота, фосфорная кислота и т.п. Также включены соли, которые образуются с органическими кислотами, такими как алифатические моно- и дикарбоновые кислоты, фенилзамещенные алкановые кислоты, гидроксиалкановые кислоты, алкандиоевые кислоты, ароматические кислоты, алифатические и ароматические сульфокислоты и т.д. и включают в себя, например, уксусную кислоту, трифторуксусную кислоту, пропионовую кислоту, гликолевую кислоту, пировиноградную кислоту, щавелевую кислоту, малеиновую кислоту, малоновую кислоту, янтарную кислоту, фумаровую кислоту, винную кислоту, лимонную кислоту, бензойную кислоту, коричную кислоту, миндальную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, n-толуолсульфоновую кислоту, салициловую кислоту и т.п. Таким образом, иллюстративные соли включают в себя сульфаты, пиросульфаты, бисульфаты, сульфиты, бисульфиты, нитраты, фосфаты, моногидрофосфаты, дигидрофосфаты, метафосфаты, пирофосфаты, хлориды, бромиды, йодиды, ацетаты, трифторацетаты, пропионаты, каприлаты, изобутатираты, оксалаты, малонаты, сукцинаты, субераты, себацаты, фумараты, малеаты, манделаты, бензоаты, хлорбензоаты, метилбензоаты, динитробензоаты, фталаты, бензолсульфонаты, толуолсульфонаты, фенилацетаты, цитраты, лактаты, малаты, тартраты, метансульфонаты и т.п (смотрите, например, Berge S.M. et al., "Pharmaceutical Salts," Journal of Pharmaceutical Science, 66:1-19 (1997)). Соли присоединения кислоты основных соединений получают контактированием форм свободного основания с достаточным количеством желаемой кислоты для получения соли.
[0051] "Фармацевтически приемлемая соль присоединения основания" относится к тем солям, которые сохраняют биологическую эффективность и свойства свободных кислот, которые не являются биологически или иным образом нежелательными. Эти соли получают из добавления неорганического основания или органического основания к свободной кислоте. Согласно некоторым вариантам осуществления фармацевтически приемлемые соли присоединения основания образуются с металлами или аминами, такими как щелочные и щелочноземельные металлы или органические амины. Соли, полученные из неорганических оснований, включают в себя, без ограничения, соли натрия, калия, лития, аммония, кальция, магния, железа, цинка, меди, марганца, алюминия и т.п. Соли, полученные из органических оснований, включают в себя, без ограничения, соли первичных, вторичных и третичных аминов, замещенных аминов, включая в себя встречающиеся в природе замещенные амины, циклических аминов и основных ионообменных смол, например, изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, диэтаноламин, 2-диметиламиноэтанол, 2-диэтиламиноэтанол, дициклогексиламин, лизин, аргинин, гистидин, кофеин, прокаин, N,N-дибензилэтилендиамин, хлорпрокаин, гидрабамин, холин, бетаин, этилендиамин, этилендианилин, N-метилглюкамин, глюкозамин, метилглюкамин, теобромин, пурины, пиперазин, пиперидин, N-этилпиперидин, полиаминовые смолы и т.п. Смотрите Berge et al., выше.
[0052] Как используется в настоящем документе, "лечение" или "лечить", или "смягчение", или "улучшение" используются в настоящем документе взаимозаменяемо. Эти термины относятся к подходу для получения полезных или желаемых результатов, включая в себя, помимо прочего, терапевтическую пользу и/или профилактическую пользу. Под "терапевтической пользой" понимается искоренение или улучшение основного заболевания, подлежащего лечению. Кроме того, терапевтическая польза достигается за счет устранения или ослабления одного или нескольких физиологических симптомов, связанных с лежащим в основе нарушением, так что у пациента наблюдается улучшение, несмотря на то, что пациент все еще поражен лежащим в основе нарушением. Для профилактической пользы композиции вводят пациенту с риском развития конкретного заболевания или пациенту, сообщающему об одном или нескольких физиологических симптомах заболевания, даже если диагноз этого заболевания не был поставлен.
Соединения
[0053] Описанные в настоящем документе соединения формулы (I), (Ia) или (Ib) являются модуляторами MAGL. Эти соединения и содержащие эти соединения композиции применимы для лечения боли. Согласно некоторым вариантам осуществления описанные в настоящем документе соединения формулы (I), (Ia) или (Ib) применимы для лечения эпилепсии/припадочного расстройства, рассеянного склероза, нейромиелита зрительного нерва (NMO), синдрома Туретта, болезни Альцгеймера или боли в животе, связанной с синдром раздраженного кишечника.
[0054] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I):

где:
R1 представляет собой -R14, -OR3, -SR4, -S(O)2R4, -N(R4)(R5), -NH(R4’) или -C≡C-(CR6R7)-R8;
каждый R2 независимо выбран из C1-6алкила, галогена, -CN, C1-6галогеналкила, -C1-6алкил(гетероциклоалкила), -OR17 и -C(O)NR18R19;
R3 представляет собой -(CR6R7)m-R8, -(CR6R7)p-Y-(CR6R7)q-R8 или -(CR6R7)t-C3-6циклоалкил-R8;
R4 представляет собой -(CR6R7)m-R8’, -(CR6R7)v-C(O)OH или -(CR6R7)p-Y-(CR6R7)q-R8;
R4’ представляет собой -(CR6R7)m-R8’, -(CR6R7)p-Y-(CR6R7)q-R8, -С4-6алкил-С(O)ОН, -C3-6циклоалкил-С(O)ОН или -С1-6алкил-С3-6циклоалкил-С(O)ОН;
Y представляет собой -О- или -N(R22)-;
R5 представляет собой C1-6алкил или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и С1-6алкокси;
каждый R6 и R7 независимо выбран из Н, F и С1-6алкила или R6 и R7, вместе с углеродом, к которому они присоединены, образуют С3-6циклоалкильное кольцо;
R8 представляет собой -C(O)OR9, -C(O)R10 или -C(O)O-(CR12R13)-OC(O)R11;
R8’ представляет собой -C(O)OR9’, -C(O)R10’ или -C(O)O-(CR12R13)-OC(O)R11;
R9 представляет собой Н или С1-6алкил;
R9’ представляет собой C1-6алкил;
R10 представляет собой С1-6алкил или -NHSO2R21;
R10’ представляет собой С2-6алкил или -NHSO2R21;
R11 представляет собой С1-6алкил или С1-6алкокси;
R12 и R13 каждый независимо представляет собой Н или C1-6алкил;
R14 представляет собой -(CR15R16)m-R8 или -(CR6R7)p-Y-(CR6R7)q-R8;
каждый R15 и R16 независимо выбран из Н, F и С1-6алкила;
каждый R17 независимо выбран из Н, С1-6алкила, C1-6галогеналкила и С3-6циклоалкила;
каждый R18 и R19 независимо выбран из Н, C1-6алкила, С3-6циклоалкила, арила и гетероарила или R18 и R19, вместе с азотом, к которому они присоединены, образуют гетероциклоалкильное кольцо, необязательно замещенное одним, двумя или тремя R20;
каждый R20 независимо выбран из галогена, C1-6алкила, C1-6галогеналкила, оксо, -CN и С3-6циклоалкила;
R21 представляет собой С1-6алкил или С3-6циклоалкил;
R22 представляет собой Н, C1-6алкил или -SO2R23;
R23 представляет собой С1-6алкил;
m представляет собой 1, 2, 3 или 4;
n представляет собой 0, 1, 2, 3 или 4;
р представляет собой 2, 3 или 4;
q представляет собой 1, 2 или 3;
t представляет собой 0, 1 или 2; и
v представляет собой 3 или 4;
или его фармацевтически приемлемая соль или сольват.
[0055] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’). Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -(CR6R7)m-R8’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’), R4’ представляет собой -(CR6R7)m-R8’ и каждый R6 и R7 независимо выбран из Н и С1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’), R4’ представляет собой -(CR6R7)m-R8’ и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1, 2 или 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’ и R9’ представляет собой -CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’ и R9’ представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’ и R10’ представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’, R10’ представляет собой -NHSO2R21 и R21 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’, R10’ представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой СН2СН2СН2С(O)ОС(СН3)3.
[0056] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’), R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 независимо выбран из Н и C1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’), R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’), R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’), R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’), R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, Y представляет собой -N(R22)- и R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2ОСН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой CH2CH2N(SO2CH3)CH2C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН(СН3)2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2СН2С(O)OCH2OC(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)СН(СН3)2.
[0057] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -С4-6алкил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -CH2CH2CH2CH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -СН2СН(СН3)СН2С(O)ОН.
[0058] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -С3-6циклоалкил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -NH(R4’) и R4’ представляет собой -С1-6алкил-С3-6циклоалкил-С(O)ОН.
[0059] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5). Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5) и R5 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5) и R5 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5) и R5 представляет собой -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5) и R5 представляет собой -СН2-фенил, необязательно замещенный одной или двумя группами, независимо выбранными из галогена, C1-6алкила, С1-6галогеналкила и C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5) и R5 представляет собой -CH2-фенил, необязательно замещенный одной группой, выбранной из галогена, C1-6алкила, C1-6галогеналкила и С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5) и R4 представляет собой -(CR6R7)m-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R4 представляет собой -(CR6R7)m-R8’ и каждый R6 и R7 независимо выбран из Н и C1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R4 представляет собой -(CR6R7)m-R8’ и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1, 2 или 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где m представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’ и R9’ представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’ и R9’ представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’ и R10’ представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’, R10’ представляет собой -NHSO2R21 и R21 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’, R10’ представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и С1-6алкокси, и R4 представляет собой -CH2CH2CH2C(O)OCH2CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2СН2С(O)ОС(СН3)3.
[0060] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, С1-6галогеналкила и C1-6алкокси, и R4 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, и каждый R6 и R7 независимо выбран из Н и C1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и С1-6алкокси, и R4 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, и Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, С1-6галогеналкила и С1-6алкокси, и R4 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, и Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и С1-6алкокси, и R4 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, Y представляет собой -N(R22)- и R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой Сьеалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и С1-6алкокси, и R4 представляет собой -CH2CH2OCH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -CH2CH2N(SO2CH3)CH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и С1-6алкокси, и R4 представляет собой -CH2CH2CH2C(O)ОСН(CH3)ОС(O)OCH2CH2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и С1-6алкокси, и R4 представляет собой -CH2CH2CH2C(O)ОСН(СН3)ОС(O)ОСН(СН3)2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, С1-6галогеналкила и С1-6алкокси, и R4 представляет собой CH2CH2CH2C(O)OCH2OC(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 или -CH2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)СН(СН3)2.
[0061] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5) и R4 представляет собой -(CR6R7)v-C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 и R4 представляет собой -(CR6R7)v-C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3, R4 представляет собой -(CR6R7)v-C(O)OH и v представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3, R4 представляет собой -(CR6R7)v-C(O)OH и v представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, С1-6галогеналкила и C1-6алкокси, и R4 представляет собой -(CR6R7)v-C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и С1-6алкокси, R4 представляет собой -(CR6R7)v-C(O)OH и v представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и C1-6алкокси, R4 представляет собой -(CR6R7)v-C(O)OH и v представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 и R4 представляет собой -СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 и R4 представляет собой -СН2СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, C1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН3 и R4 представляет собой -СН2СН(СН3)СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -N(R4)(R5), R5 представляет собой -СН2-фенил, необязательно замещенный одной, двумя или тремя группами, независимо выбранными из галогена, С1-6алкила, C1-6галогеналкила и C1-6алкокси, и R4 представляет собой -СН2СН(СН3)СН2С(O)ОН.
[0062] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -(CR6R7)m-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R представляет собой -С(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой 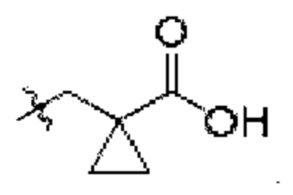 Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой
Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой 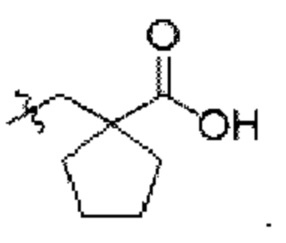 Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН(CH2)СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2С(O)OCH2CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -CH2CH2CH2C(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОС(СН3)3.
Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН(CH2)СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2С(O)OCH2CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -CH2CH2CH2C(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОС(СН3)3.
[0063] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 независимо выбран из Н и С1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, Y представляет собой -N(R22)- и R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -CH2CH2OCH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой OR3 и R3 представляет собой -CH2CH2N(SO2CH3)CH2C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН(СН3)2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОСН2ОС(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)СН(СН3)2.
[0064] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8 и t представляет собой 0. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8 и t представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3, R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8 и t представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -циклопропил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -циклобутил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой -циклопентил-С(O)ОН.
[0065] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -(CR15R16)m-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R14 представляет собой -(CR15R16)m-R8 и m представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -CH2CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН(СН3)СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -CH2CH2CH2C(О)OCH2CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой СН2СН2СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой СН2СН2СН2СН2С(O)ОС(СН3)3.
[0066] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14, R14 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 независимо выбран из Н и С1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14, R14 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14, R14 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14, R14 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14, R14 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, Y представляет собой -N(R22)- и R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -CH2CH2OCH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -CH2CH2N(SO2CH3)CH2C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН(СН3)2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2С(O)ОСН2ОС(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -R14 и R14 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)СН(СН3)2.
[0067] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -C≡C-(CR6R7)-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -C≡C-(CR6R7)-R8 и R6 и R7 независимо выбраны из Н и С1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -C≡C-(CR6R7)-R8 и R6 и R7 каждый независимо представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -С≡С-(CR6R7)-R8 и R6 и R7 представляют собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где представляет собой -С(О)OR9 и R9 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(О)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(О)О-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой 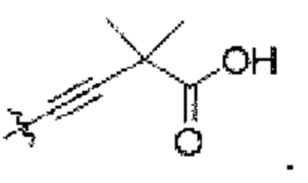
[0068] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 0, 1, 2 или 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (1) или его фармацевтически приемлемая соль или сольват, где n представляет собой 0, 1 или 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 или 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 0 или 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 0. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 4.
[0069] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген, С1-6алкил, C1-6галогеналкил или -OR17. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 независимо выбран из С1-6алкила, галогена, -CN или C1-6галогеналкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген, С1-6алкил или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -Cl. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -F. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой С1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -CF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6галогеналкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -CN.
[0070] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, С1-6алкил, C1-6галогеналкил или -OR17. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил, С1-6галогеналкил, С1-6алкокси, -OCF3 или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил, С1-6галогеналкил, C1-6алкокси или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген или С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо С1-6галогеналкил.
[0071] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси, C1-6галогеналкокси, -ОН или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси, -OCF3 или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, С1-6алкил, С1-6галогеналкил, С1-6алкокси или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, С1-6алкил или С1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген или С1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген или C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо C1-6галогеналкил.
[0072] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль или сольват, где n представляет собой 4 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил и -OR17.
[0073] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia):
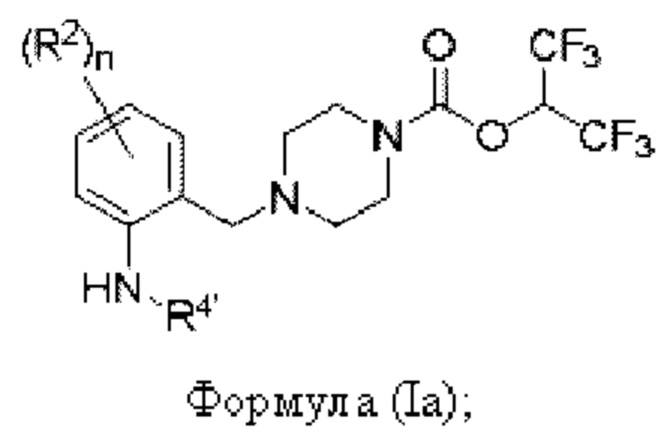
где:
каждый R2 независимо выбран из C1-6алкила, галогена, -CN, C1-6галогеналкила, -C1-6алкил(гетероциклоалкила), -OR17 и -C(O)NR18R19;
R4’ представляет собой -(CR6R7)m-R8’, -(CR6R7)p-Y-(CR6R7)q-R8, -С4-6алкил-С(O)ОН, -С3-6циклоалкил - С(О)ОН ил и -С1-6алкил -С3-6циклоалкил -С(О)ОН,
Y представляет собой -О- или -N(R22)-;
каждый R6 и R7 независимо выбран из Н, F, и C1-6алкила или R6 и R7, вместе с углеродом, к которому они присоединены, образуют С3-6циклоалкильное кольцо;
R8 представляет собой -C(O)OR9, -C(O)R10 или -C(O)O-(CR12R13)-OC(O)R11;
R8’ представляет собой -C(O)OR9’, -C(O)R10’ или -C(O)O-(CR12R13)-OC(O)R11;
R9 представляет собой H или C1-6алкил;
R9’ представляет собой C1-6алкил;
R10 представляет собой С1-6алкил или -NHSO2R21;
R10’ представляет собой С2-6алкил или -NHSO2R21;
R11 представляет собой C1-6алкил или C1-6алкокси,
R12 и R13 каждый независимо представляет собой Н или C1-6алкил;
каждый R17 независимо выбран из Н, С1-6алкила, C1-6галогеналкила и С3-6циклоалкила;
каждый R18 и R19 независимо выбран из Н, C1-6алкила, С3-6циклоалкила, арила и гетероарила или R18 и R19, вместе с азотом, к которому они присоединены, образуют гетероциклоалкильное кольцо, необязательно замещенное одним, двумя или тремя R20;
каждый R20 независимо выбран из галогена, С1-6алкила, C1-6галогеналкила, оксо, -CN, и С3-6циклоалкила;
R21 представляет собой С1-6алкил или С3-6циклоалкил;
R22 представляет собой Н, С1-6алкил или -SO2R23;
R23 представляет собой С1-6алкил;
m представляет собой 1, 2, 3 или 4;
n представляет собой 0, 1, 2, 3 или 4;
р представляет собой 2, 3 или 4 и
q представляет собой 1, 2 или 3;
или его фармацевтически приемлемая соль или сольват.
[0074] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)m-R8’. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)m-R8’ и каждый R6 и R7 независимо выбран из Н и С1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)m-R8’ и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1, 2 или 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где m представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где m представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где m представляет собой 3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где m представляет собой 4. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’.
Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9’ и R9’ представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)OR9’ и R9’ представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’ и R10’ представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10’, R10’ представляет собой -NHSO2R21 и R21 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -С(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8’ представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -CH2CH2CH2C(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2СН2С(O)ОС(СН3)3.
[0075] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 независимо выбран из Н и C1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, Y представляет собой -N(R22)- и R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где р представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (1а) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой С1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -CH2CH2OCH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -CH2CH2N(SO2CH3)CH2C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН(СН3)2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой СН2СН2СН2С(O)OCH2OC(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)СН(СН3)2.
[0076] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -С4-6алкил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -CH2CH2CH2CH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -СН2СН(СН3)СН2С(O)ОН.
[0077] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -С3-6циклоалкил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где R4’ представляет собой -С1-6алкил-С3-6циклоалкил-С(O)ОН.
[0078] Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 0, 1, 2 или 3. Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 0, 1 или 2. Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 1 или 2. Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 0 или 1. Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 0. Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 1. Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 2. Согласно некоторым вариантам осуществления соединения формулы (Ia) или его фармацевтически приемлемой соли или сольвата n представляет собой 3. Согласно некоторым вариантам осуществления соединения формулы (1а) или его фармацевтически приемлемой соли или сольвата n представляет собой 4.
[0079] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген, С1-6алкил, C1-6галогеналкил или -OR17. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 независимо выбран из С1-6алкила, галогена, -CN или C1-6галогеналкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген, C1-6алкил или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -Cl. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -F. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой С1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -CF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6галогеналкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -CN.
[0080] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, С1-6алкил, С1-6галогеналкил или -OR17. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, С1-6алкил, С1-6галогеналкил, С1-6алкокси, -OCF3 или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, С1-6алкил, C1-6галогеналкил, С1-6алкокси или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, С1-6алкил, C1-6галогеналкил или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, С1-6алкил или С1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген или С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо С1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо C1-6галогеналкил.
[0081] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, С1-6алкил, C1-6галогеналкил, С1-6алкокси, С1-6галогеналкокси, -ОН или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси, -OCF3 или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, С1-6алкил, C1-6галогеналкил или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген или C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо C1-6галогеналкил.
[0082] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ia) или его фармацевтически приемлемая соль или сольват, где n представляет собой 4 и каждый R2 представляет собой независимо галоген, С1-6алкил, C1-6галогеналкил и -OR17.
[0083] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib):
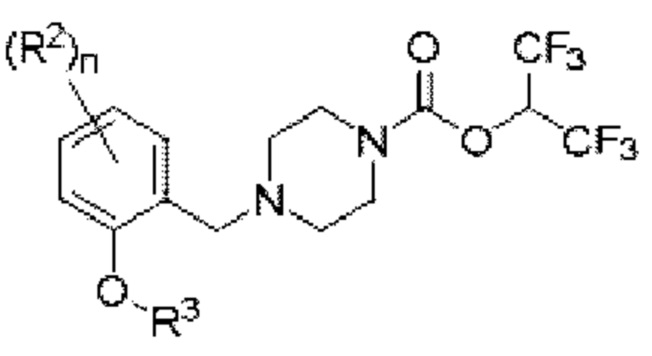
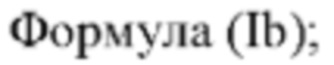
где:
каждый R2 независимо выбран из С1-6алкила, галогена, -CN, C1-6галогеналкила, - C1-6алкил(гетероциклоалкила), -OR17 и -C(O)NR18R19;
R3 представляет собой -(CR6R7)m-R8, -(CR6R7)p-Y-(CR6R7)q-R8 или -(CR6R7)t-C3-6циклоалкил-R8;
Y представляет собой -О- или -N(R22)-;
каждый R6 и R7 независимо выбран из Н, F, и C1-6алкила или R6 и R7, вместе с углеродом, к которому они присоединены, образуют С3-6циклоалкильное кольцо;
R8 представляет собой -C(O)OR9, -C(O)R10 или -C(O)O-(CR12R13)-OC(O)R11;
R9 представляет собой Н или C1-6алкил;
R10 представляет собой C1-6алкил или -NHSO2R21;
R11 представляет собой C1-6алкил или C1-6алкокси;
R12 и R13 каждый независимо представляет собой Н или C1-6алкил;
каждый R17 независимо выбран из Н, C1-6алкила, C1-6галогеналкила и С3-6циклоалкила;
каждый R18 и R19 независимо выбран из Н, C1-6алкила, С3-6циклоалкила, арила и гетероарила или R18 и R19, вместе с азотом, к которому они присоединены, образуют гетерониклоалкильное кольцо, необязательно замещенное одним, двумя или тремя R20;
каждый R20 независимо выбран из галогена, C1-6алкила, C1-6галогеналкила, оксо, -CN и С3-6циклоалкила;
R21 представляет собой C1-6алкил или С3-6циклоалкил;
R22 представляет собой Н, C1-6алкил или -SO2R23;
R23 представляет собой C1-6алкил;
m представляет собой 1, 2, 3 или 4;
n представляет собой 0, 1, 2, 3 или 4;
p представляет собой 2, 3 или 4;
q представляет собой 1, 2 или 3 и
t представляет собой 0, 1 или 2;
или его фармацевтически приемлемая соль или сольват.
[0084] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)m-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой 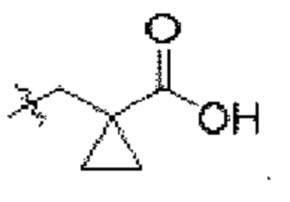 Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой
Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R1 представляет собой -OR3 и R3 представляет собой 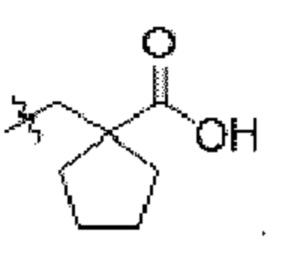 Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -CH2CH(СН3)CH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОС(СН3)3.
Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -CH2CH(СН3)CH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2С(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОСН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОС(СН3)3.
[0085] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 независимо выбран из Н и C1-6алкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и каждый R6 и R7 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -О-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8 и Y представляет собой -N(R22)-. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)p-Y-(CR6R7)q-R8, Y представляет собой -N(R22)- и R22 представляет собой -SO2R23. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где q представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где p представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой Н. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)OR9 и R9 представляет собой -СН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10 и R10 представляет собой -NHSO2R21. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)R10, R10 представляет собой -NHSO2R21 и R21 представляет собой С3-6циклоалкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -С(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R8 представляет собой -C(O)O-(CR12R13)-OC(O)R11 и R11 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -CH2CH2OCH2C(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -CH2CH2N(SO2CH3)CH2C(O)OH. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН2СН3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)ОСН(СН3)2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой СН2СН2СН2С(O)OCH2OC(O)ОС(СН3)3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -СН2СН2СН2С(O)ОСН(СН3)ОС(O)СН(СН3)2.
[0086] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8 и t представляет собой 0. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8 и t представляет собой 1. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -(CR6R7)t-C3-6циклоалкил-R8 и t представляет собой 2. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -циклопропил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -циклобутил-С(O)ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где R3 представляет собой -циклопентил-С(O)ОН.
[0087] Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 0, 1, 2 или 3. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 0, 1 или 2. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 1 или 2. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 0 или 1. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 0. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 1. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 2. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 3. Согласно некоторым вариантам осуществления соединения формулы (Ib) или его фармацевтически приемлемой соли или сольвата n представляет собой 4.
[0088] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген, C1-6алкил, C1-6галогеналкил или -OR17. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 независимо выбран из C1-6алкила, галогена, -CN или C1-6галогеналкила. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген, C1-6алкил или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -Cl. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -F. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -CH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -CF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6алкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -OCH3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой C1-6галогеналкокси. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -ОН. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 1 и R2 представляет собой -CN.
[0089] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил или -OR17. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси, -OCF3 или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген, C1-6алкил или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген или C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 2 и каждый R2 представляет собой независимо C1-6галогеналкил.
[0090] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси, C1-6галогеналкокси, -ОН или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси, -OCF3 или -CN. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил, C1-6алкокси или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил или -OCF3. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген, C1-6алкил или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген или C1-6галогеналкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген или C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо галоген. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо C1-6алкил. Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 3 и каждый R2 представляет собой независимо C1-6галогеналкил.
[0091] Согласно некоторым вариантам осуществления предусмотрено соединение формулы (Ib) или его фармацевтически приемлемая соль или сольват, где n представляет собой 4 и каждый R2 представляет собой независимо галоген, C1-6алкил, C1-6галогеналкил и -OR17.
[0092] Предусмотренные в настоящем документе дополнительные варианты осуществлений включают в себя комбинации одного или нескольких конкретных вариантов осуществлений, изложенных выше.
[0093] Согласно некоторым вариантам осуществления, раскрытое в настоящем документе соединение характеризуется структурой, представленной в таблице 1.
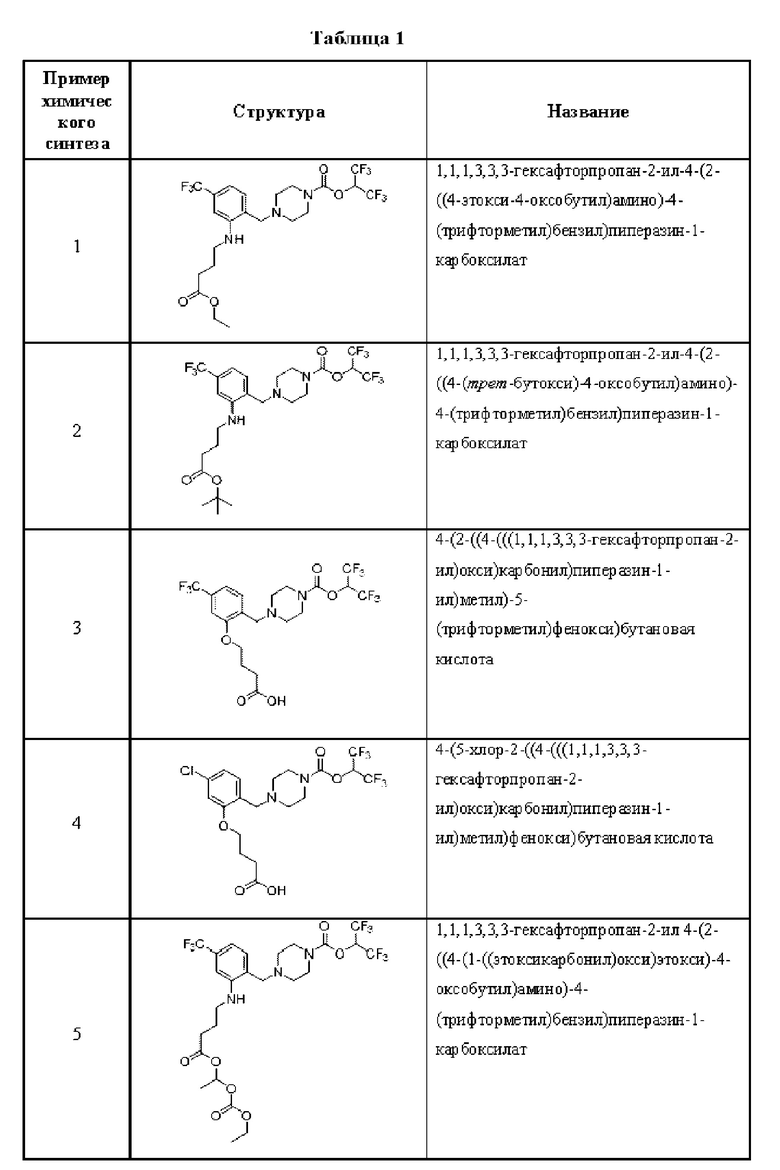
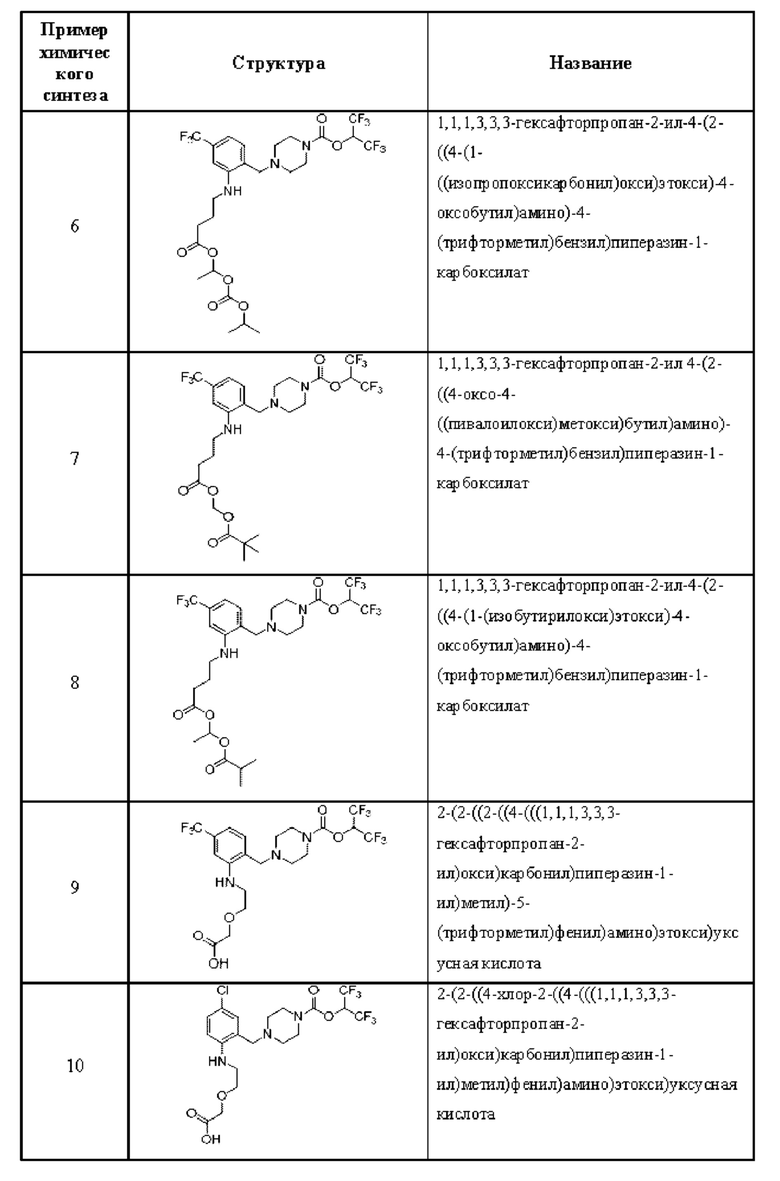
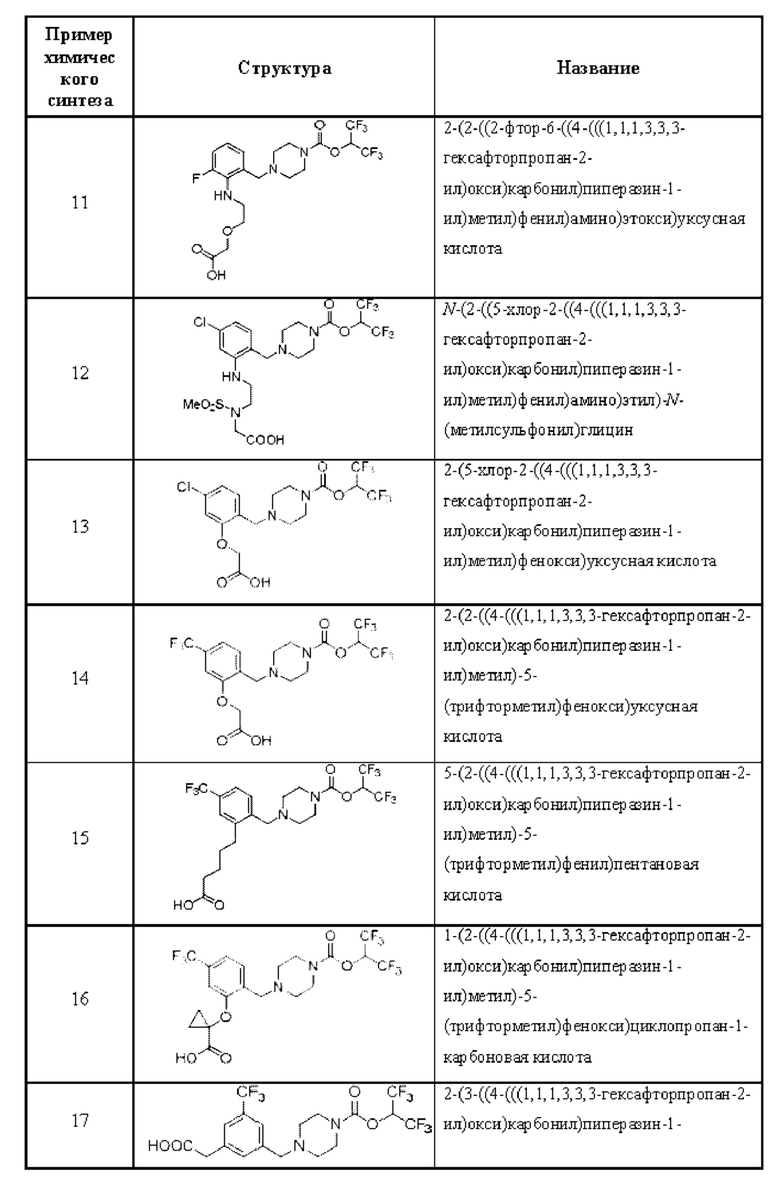
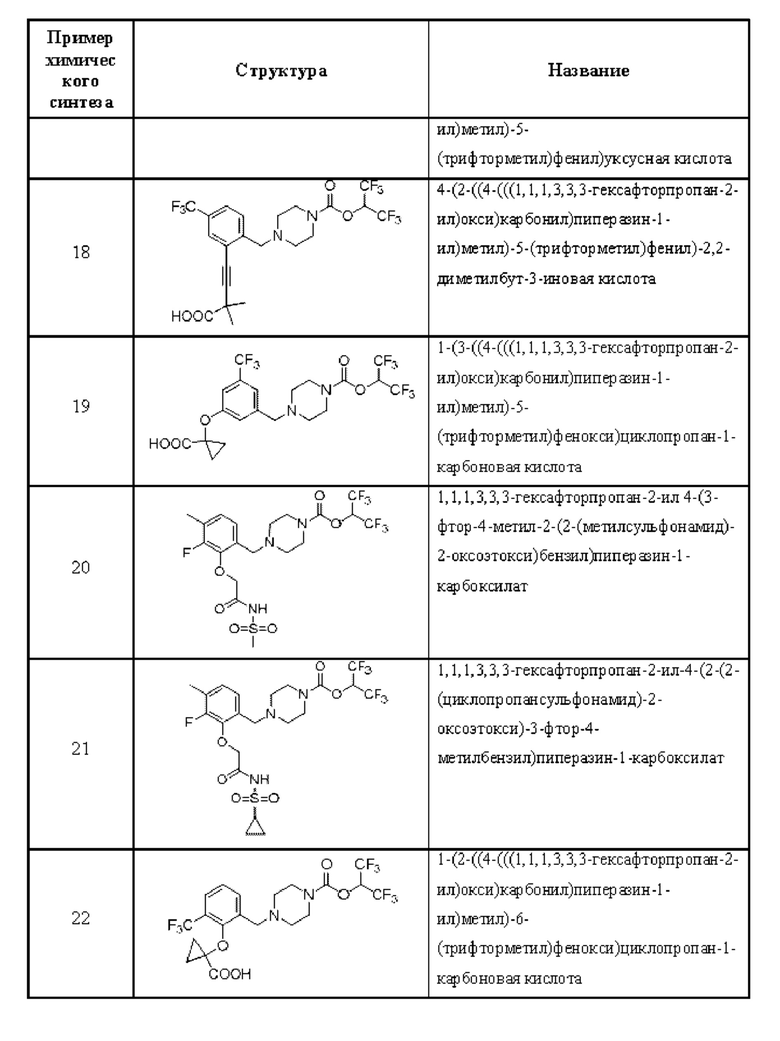
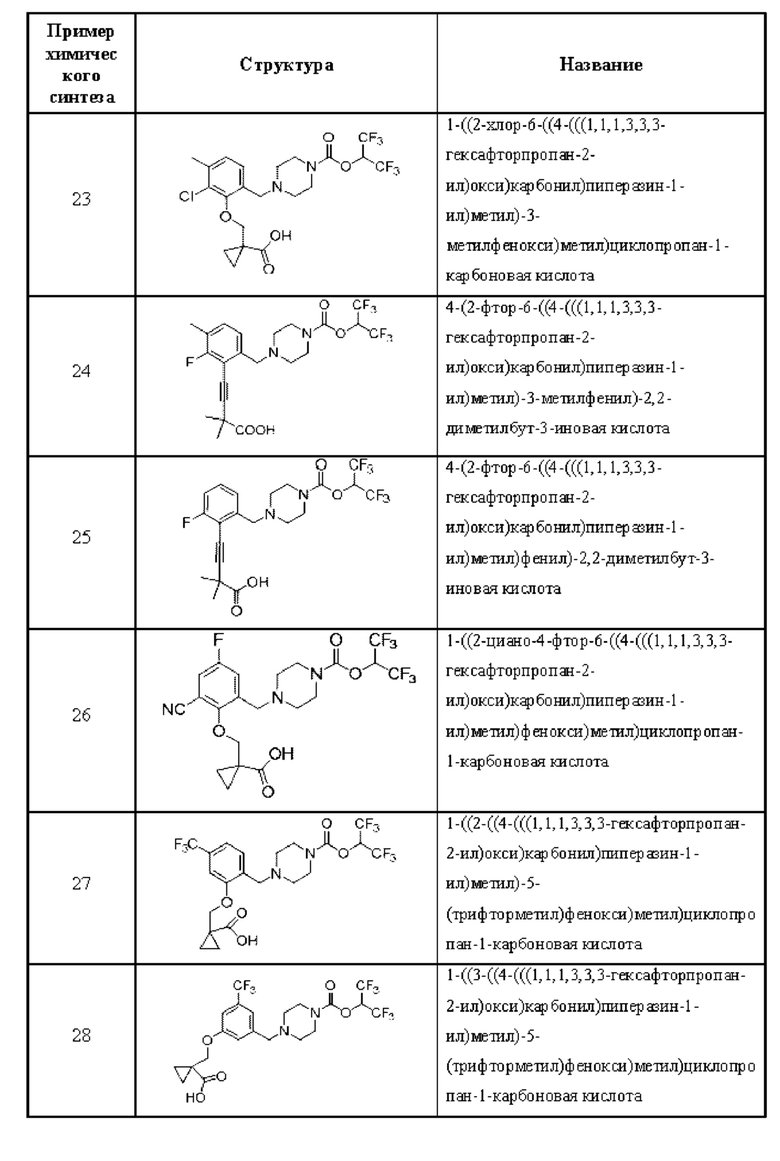
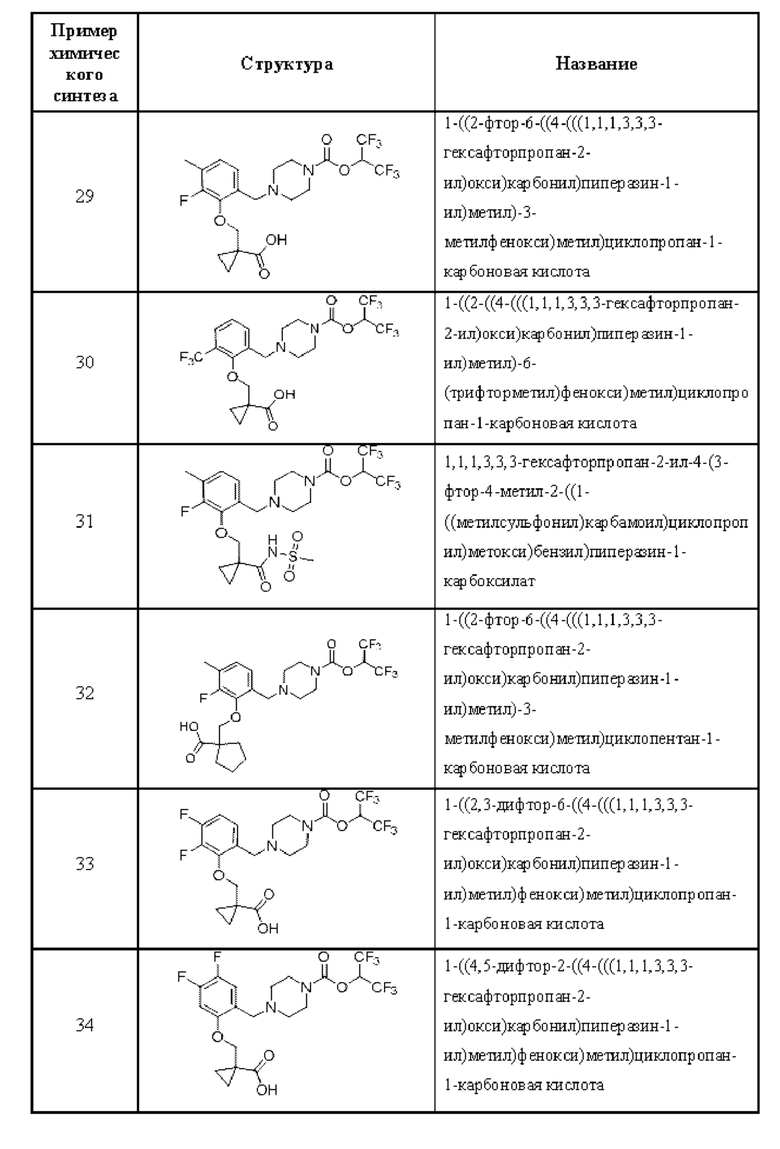
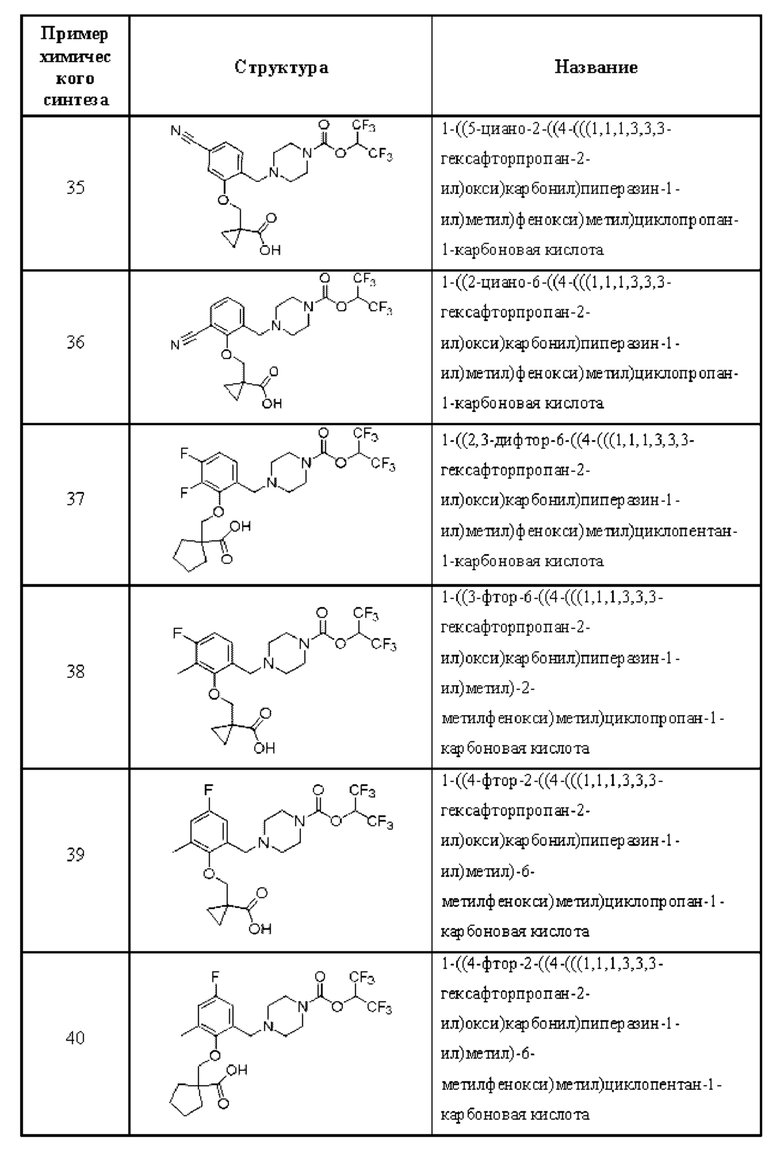
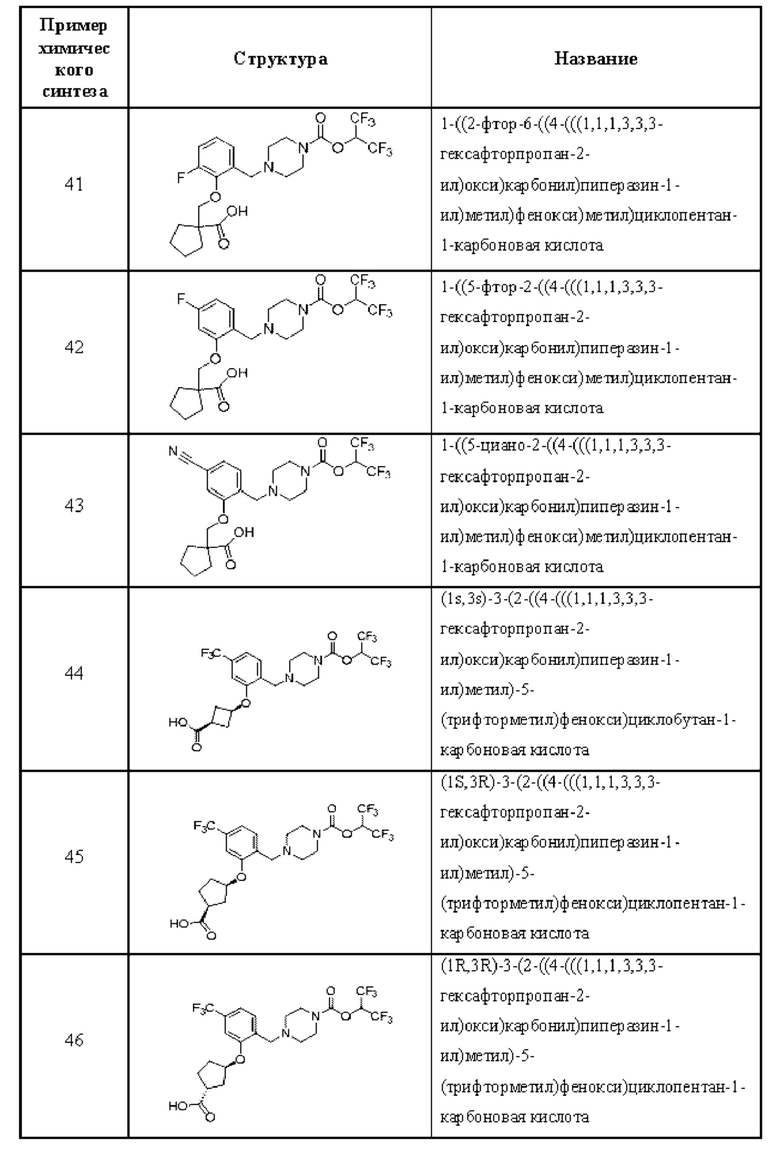
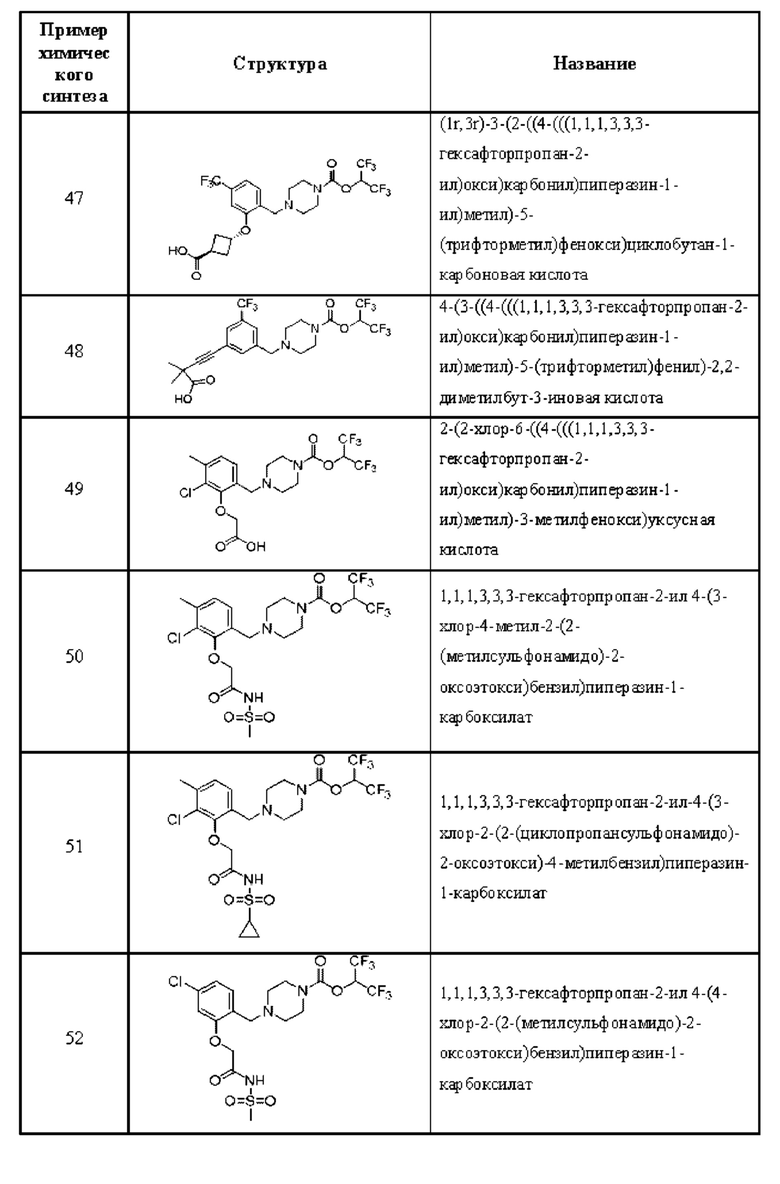
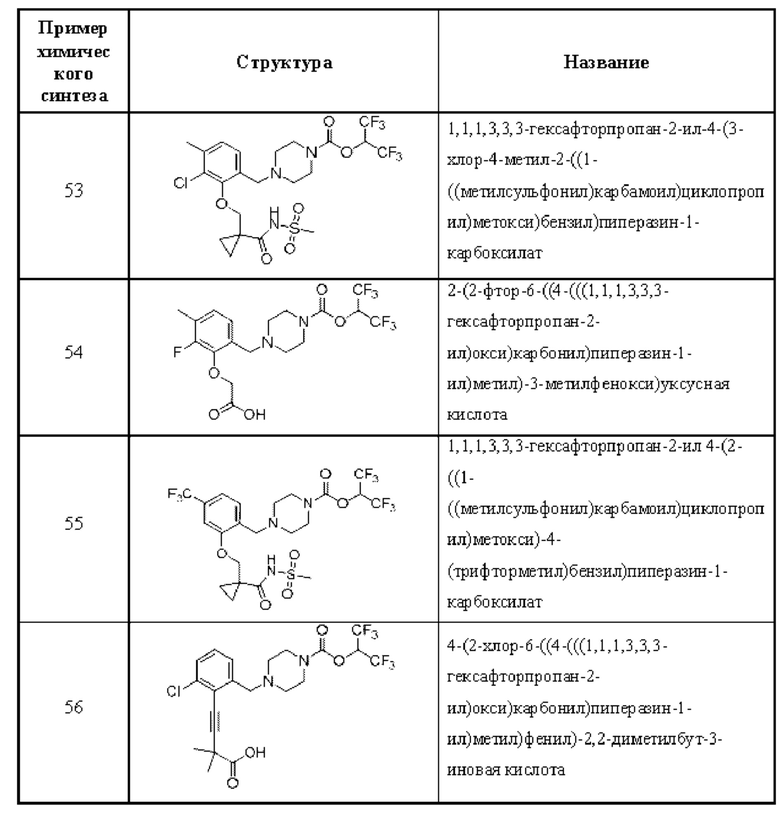
[0094] Согласно некоторым вариантам осуществления раскрытое в настоящем документе соединение выбрано из:
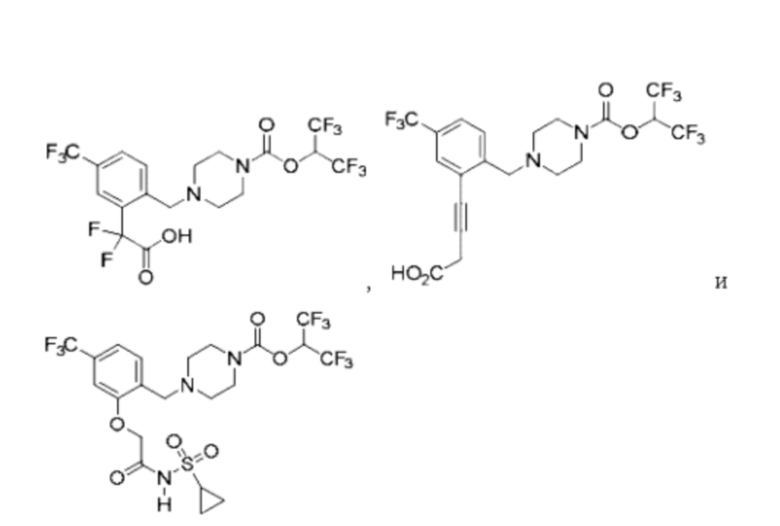
или его фармацевтически приемлемой соли или сольвата.
Получение соединений
[0095] Используемые в реакциях описанные в настоящем документе соединения изготавливают в соответствии с известными способами органического синтеза, исходя из коммерчески доступных химикатов и/или из соединений, описанных в химической литературе. "Коммерчески доступные химикаты" получают из стандартных коммерческих источников, включая в себя Acros Organics (Geel, Belgium), Aldnch Chemical (Milwaukee, WI, включая в себя Sigma Chemical and Fluka), Apin Chemicals Ltd. (Milton Park, UK), Ark Pharrn, Inc. (Libertyville, IL), Avocado Research (Lancashire, U.K.), BDH Inc. (Toronto, Canada), Bionet (Cornwall, U.K), Chemservice Inc. (West Chester, PA), Combi-blocks (San Diego, CA), Crescent Chemical Co. (Hauppauge, NY), eMolecules (San Diego, CA), Fisher Scientific Co. (Pittsburgh, PA), Fisons Chemicals (Leicestershire, UK), Frontier Scientific (Logan, UT), ICN Biomedicals, Inc. (Costa Mesa, CA), Key Organics (Cornwall, U.K.), Lancaster Synthesis (Windham, NH), Matrix Scientific, (Columbia, SC), Maybndge Chemical Co. Ltd. (Cornwall, U.K.), Parish Chemical Co. (Orem, UT), Pfaltz & Bauer, Inc. (Waterbury, CN), Poly organ ix (Houston, TX), Pierce Chemical Co. (Rockford, IL), Riedel de Haen AG (Hanover, Germany), Ryan Scientific, Inc. (Mount Pleasant, SC), Spectrum Chemicals (Gardena, CA), Sundia Meditech, (Shanghai, China), TCI America (Portland, OR), Trans World Chemicals, Inc. (Rockville, MD) и WuXi (Shanghai, China).
[0096] Подходящие справочники и научные труды, которые детализируют синтез реагентов, применимых при получении описанных в настоящем документе соединений или предоставляют ссылки на статьи, которые описывают получение, включают в себя, например, "Synthetic Organic Chemistry", John Wiley & Sons, Inc., New York, S.R. Sandler et al., "Organic Functional Group Preparations," 2nd Ed., Academic Press, New York, 1983, H.O. House, "Modem Synthetic Reactions", 2nd Ed., W.A. Benjamin, Inc. Menlo Park, Calif. 1972, T.L. Gilchrist, "Heterocyclic Chemistry", 2nd Ed., John Wiley & Sons, New York, 1992; J. March, "Advanced Organic Chemistry: Reactions, Mechanisms and Structure", 4th Ed., Wiley-Interscience, New York, 1992 Дополнительные подходящие справочники и научные труды, которые детализируют синтез реагентов, применимых при получении описанных в настоящем документе соединений или предоставляют ссылки на статьи, которые описывают получение, включают в себя, например, Fuhrhop, J. and Penzlin G. "Organic Synthesis: Concepts, Methods, Starting Materials", Second, Revised and Enlarged Edition (1994) John Wiley & Sons ISBN: 3-527-29074-5; Hoffman, R.V. "Organic Chemistry, An Intermediate Text" (1996) Oxford University Press, ISBN 0-19-509618-5; Larock, R.C. "Comprehensive Organic Transformations: A Guide to Functional Group Preparations" 2nd Edition (1999) Wiley-VCH, ISBN: 0-471-19031-4; March, J. "Advanced Organic Chemistry: Reactions, Mechanisms, and Structure" 4th Edition (1992) John Wiley & Sons, ISBN: 0-471-60180-2; Otera, J. (editor) "Modern Carbonyl Chemistry" (2000) Wiley-VCH, ISBN: 3-527-29871-1; Patai, S. "Patai's 1992 Guide to the Chemistry of Functional Groups" (1992) Interscience ISBN: 0-471-93022-9; Solomons, T.W.G. "Organic Chemistry" 7th Edition (2000) John Wiley & Sons, ISBN: 0-471-19095-0; Stowell, J.C., "Intermediate Organic Chemistry" 2nd Edition (1993) Wiley-hiterscience, ISBN: 0-471-57456-2; "Industrial Organic Chemicals: Starting Materials and Intermediates: An Ullmann's Encyclopedia" (1999) John Wiley & Sons, ISBN: 3-527-29645-Х, в 8 томах; "Organic Reactions" (1942-2000) John Wiley & Sons, в более чем 55 томах и "Chemistry of Functional Groups" John Wiley & Sons, в 73 томах.
[0097] Конкретные и аналогичные реагенты также идентифицируются с помощью индексов известных химических веществ, подготовленных Химической реферативной службой Американского химического общества, которые доступны в большинстве публичных и университетских библиотеках, а также через базы данных онлайновые (Американское химическое общество, Вашингтон, округ Колумбия, можно связаться для более подробной информации). Химические вещества, которые известны, но не являются коммерчески доступными в каталогах, могут быть изготовлены по индивидуальному заказу предприятиями химического синтеза, где многие стандартные предприятия по поставке химикатов (например, перечисленные выше) предоставляют услуги по индивидуальному синтезу. Ссылка для получения и выбора фармацевтических солей описанных в настоящем документе карбаматов пиперазина представляет собой P.Н. Stahl & С.G. Wermuth "Handbook of Pharmaceutical Salts", Verlag Helvetica Chimica Acta, Zurich, 2002.
Дополнительные формы раскрытых в настоящем документе соединений
Изомеры
[0098] Кроме того, согласно некоторым вариантам осуществления описанные в настоящем документе соединения существуют в виде геометрических изомеров. Согласно некоторым вариантам осуществления описанные в настоящем документе соединения обладают одной или несколькими двойными связями. Представленные в настоящем документе соединения включают в себя все цис, транс, син, анти, entgegen (Е) и zusammen (Z) изомеры, а также их соответствующие смеси. В некоторых ситуациях соединения существуют в виде таутомеров. Описанные в настоящем документе соединения включают в себя все возможные таутомеры в описанных в настоящем документе формулах. В некоторых ситуациях описанные в настоящем документе соединения обладают одним или несколькими хиральными центрами, и каждый центр существует в R-конфигурации или S-конфигурации. Описанные в настоящем документе соединения включают в себя все диастереомерные, энантиомерные и эпимерные формы, а также их соответствующие смеси. Согласно дополнительным вариантам осуществления представленных в настоящем документе соединений и способов смеси энантиомеров и/или диастереоизомеров, полученные в результате одной препаративной стадии, комбинации или взаимопревращения, применимы для описанных в настоящем документе применений. Согласно некоторым вариантам осуществления описанные в настоящем документе соединения получают в виде оптически чистых энантиомеров путем хирального хроматографического разделения рацемической смеси. Согласно некоторым вариантам осуществления описанные в настоящем документе соединения получают в виде их отдельных стереоизомеров путем взаимодействия рацемической смеси соединения с оптически активным разделяющим средством с образованием пары диастереоизомерных соединений, разделения диастереомеров и извлечения оптически чистых энантиомеров. Согласно некоторым вариантам осуществления предпочтительными являются диссоциируемые комплексы (например, кристаллические диастереомерные соли). Согласно некоторым вариантам осуществления диастереомеры имеют различные физические свойства (например, точки плавления, точки кипения, растворимость, реакционная способность и т.д.) и разделяются с использованием этих различий. Согласно некоторым вариантам осуществления диастереомеры разделяют хиральной хроматографией или, предпочтительно, способами разделения/разрешения, основанными на различиях в растворимости. Согласно некоторым вариантам осуществления оптически чистый энантиомер затем извлекают вместе с разделительным средством любыми практическими средствами, которые не приводят к рацемизации.
Меченные соединения
[0099] Согласно некоторым вариантам осуществления описанные в настоящем документе соединения существуют в их изотопно-меченных формах. Согласно некоторым вариантам осуществления раскрытые в настоящем документе способы включают в себя способы лечения заболеваний путем введения таких изотопно-меченных соединений. Согласно некоторым вариантам осуществления раскрытые в настоящем документе способы включают в себя способы лечения заболеваний путем введения таких изотопно-меченных соединений в качестве фармацевтических композиций. Таким образом, согласно некоторым вариантам осуществления раскрытые в настоящем документе соединения включают в себя изотопно-меченные соединения, которые идентичны тем, которые перечислены в настоящем документе, за исключением того, что один или несколько атомов заменены атомом, имеющим атомную массу или массовое число, отличное от атомной массы или массового числа, как правило, встречающегося в природе. Примеры изотопов, которые включены в соединения по настоящему изобретению, включают в себя изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора и хлорида, такие как 2Н, 3Н, 13С, 14С, 15N, 18O, 17O, 31Р, 32Р, 35S, 18F и 36Cl, соответственно. Описанные в настоящем документе соединения и фармацевтически приемлемые соли, сложные эфиры, сольваты, гидраты или их производные, которые содержат вышеуказанные изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения. Некоторые изотопно-меченные соединения, например, те, в которые включены радиоактивные изотопы, такие как 3Н и 14С, применимы в анализах распределения лекарственного средства и/или субстрата в ткани. Меченные тритием, т.е. 3Н и углерод-14, т.е. 14С, изотопы особенно предпочтительны из-за их простоты получения и обнаружения. Кроме того, замена тяжелыми изотопами, такими как дейтерий, то есть 2Н, дает определенные терапевтические преимущества, обусловленные большей метаболической стабильностью, например, увеличением периода полувыведения in vivo или снижением требований к дозировке. Согласно некоторым вариантам осуществления изотопно-меченные соединения, фармацевтически приемлемые соли, сложные эфиры, сольваты, гидраты или их производные получают любым подходящим способом.
[00100] Согласно некоторым вариантам осуществления описанные в настоящем документе соединения метят другими способами, включающими, без ограничения, применение хромофоров или флуоресцентных фрагментов, биолюминесцентных меток или хемилюминесцентных меток.
Фармацевтически приемлемые соли
[00101] Согласно некоторым вариантам осуществления описанные в настоящем документе соединения существуют в виде их фармацевтически приемлемых солей. Согласно некоторым вариантам осуществления раскрытые в настоящем документе способы включают в себя способы лечения заболеваний путем введения таких фармацевтически приемлемых солей. Согласно некоторым вариантам осуществления раскрытые в настоящем документе способы включают в себя способы лечения заболеваний путем введения таких фармацевтически приемлемых солей в качестве фармацевтических композиций.
[00102] Согласно некоторым вариантам осуществления описанные в настоящем документе соединения содержат кислотные или основные группы и, следовательно, реагируют с любым из ряда неорганических или органических оснований и неорганических и органических кислот с образованием фармацевтически приемлемой соли. Согласно некоторым вариантам осуществления эти соли получают in situ во время окончательного выделения и очистки соединений по настоящему изобретению или путем отдельной реакции очищенного соединения в его свободной форме с подходящей кислотой или основанием и выделения образованной таким образом соли.
Сольваты
[00103] Согласно некоторым вариантам осуществления описанные в настоящем документе соединения существуют в виде сольватов. В настоящем изобретении предусмотрены способы лечения заболеваний путем введения таких сольватов. Настоящее изобретение дополнительно относится к способам лечения заболеваний путем введения таких сольватов в качестве фармацевтических композиций.
[00104] Сольваты содержат либо стехиометрические, либо нестехиометрические количества растворителя и, согласно некоторым вариантам осуществления, образуются в процессе кристаллизации с фармацевтически приемлемыми растворителями, такими как вода, этанол и т.п. Гидраты образуются, когда растворителем является вода, или алкоголяты образуются, когда растворителем является спирт. Сольваты описанных в настоящем документе соединений удобно получать или образовывать в ходе описанных в настоящем документе процессов. Только в качестве примера, гидраты описанных в настоящем документе соединений удобно получать перекристаллизацией из смеси водный/органический растворитель, используя органические растворители, включая в себя, без ограничения, диоксан, тетрагидрофуран или метанол. Кроме того, представленные в настоящем документе соединения существуют как в несольватированной, так и в сольватированной форме. Как правило, сольватированные формы считаются эквивалентными несольватированным формам для целей соединений и способов, представленных в настоящем документе.
Пролекарства
[00105] Согласно некоторым вариантам осуществления описанные в настоящем документе соединения существуют в форме пролекарств. В настоящем изобретении предусмотрены способы лечения заболеваний путем введения таких пролекарств. Настоящее изобретение также относится к способам лечения заболеваний путем введения таких пролекарств в качестве фармацевтических композиций.
[00106] Согласно некоторым вариантам осуществления пролекарства включают в себя соединения, в которых аминокислотный остаток или полипептидная цепь из двух или более (например, двух, трех или четырех) аминокислотных остатков ковалентно связана через амидную или сложноэфирную связь со свободной амино, гидрокси или карбоксильной группой соединений по настоящему изобретению. Аминокислотные остатки включают в себя, без ограничения, 20 встречающихся в природе аминокислот, а также включают в себя 4-гидроксипролин, гидроксилизин, демозин, изодемозин, 3-метилгистидин, нор вал ин, бета-аланин, гамма-аминомасляную кислоту, цитруллин, гомоцистеин, гомосерин, орнитин и метионинсульфон. Согласно другим вариантам осуществления пролекарства включают в себя соединения, в которых остаток нуклеиновой кислоты или олигонуклеотид из двух или более (например, двух, трех или четырех) остатков нуклеиновой кислоты ковалентно связан с соединением по настоящему изобретению.
[00107] Фармацевтически приемлемые пролекарства описанных в настоящем документе соединений также включают в себя, без ограничения, сложные эфиры, карбонаты, тиокарбонаты, N-ацильные производные, N-ацилоксиалкильные производные, четвертичные производные третичных аминов, N-основания Манниха, основания Шиффа, аминокислотные конъюгаты, фосфатные эфиры, соли металлов и сульфонатные эфиры. Согласно некоторым вариантам осуществления соединения, содержащие свободные амино, амидо, гидрокси или карбоксильные группы, превращаются в пролекарства. Например, свободные карбоксильные группы дериватизируются в виде амидов или сложных алкиловых эфиров. В некоторых случаях все эти пролекарственные фрагменты включают в себя группы, включающие в себя, без ограничения, функциональные группы простого эфира, амина и карбоновой кислоты.
[00108] Гидрокси-пролекарства включают в себя сложные эфиры, такие как, без ограничения, ацилоксиалкиловые (например, ацилоксиметиловые, ацилоксиэтиловые) сложные эфиры, алкоксикарбонилоксиалкиловые сложные эфиры, алкиловые сложные эфиры, ариловые сложные эфиры, сложные эфиры фосфорной кислоты, сложные эфиры сульфокислоты, сульфатные эфиры и содержащие дисульфид сложные эфиры; простые эфиры, амиды, карбаматы, полусукцинаты, диметиламиноацетаты и фосфорилоксиметилоксикарбонилы, как указано в Advanced Drug Delivery Reviews 1996, 19, 115.
[00109] Пролекарства, производные амина, включают в себя без ограничения следующие группы и комбинации групп:
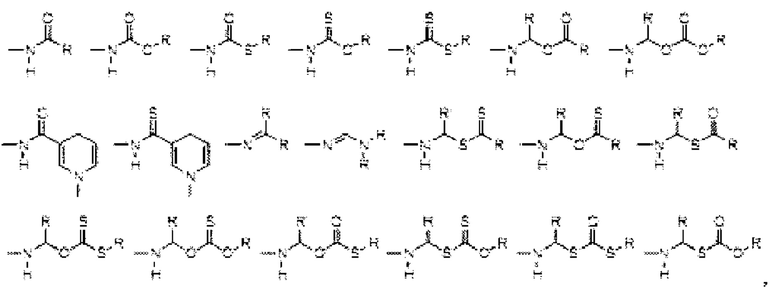
а также сульфонамиды и фосфонамиды.
[00110] В определенных случаях сайты на любых участках ароматического кольца чувствительны к различным метаболическим реакциям, поэтому включение соответствующих заместителей в структуры ароматического кольца уменьшает, минимизирует или устраняет этот метаболический путь.
Фармацевтические композиции
[00111] Согласно определенным вариантам осуществления описанное в настоящем документе соединение формулы (I), (Ia) или (Ib) вводят в виде чистого химического вещества Согласно некоторым вариантам осуществления описанное в настоящем документе соединение формулы (I), (Ia) или (Ib) объединяют с фармацевтически подходящим или приемлемым носителем (также обозначаемым в настоящем документе как фармацевтически подходящее (или приемлемое) вспомогательное вещество, физиологически подходящее (или приемлемое) вспомогательное вещество или физиологически подходящий (или приемлемый) носитель), выбранным на основе выбранного пути введения и стандартной фармацевтической практики, как описано, например, в Remington: The Science и Practice of Pharmacy (Gennaro, 21st Ed. Mack Pub. Co., Easton, PA (2005)).
[00112] Соответственно, в настоящем документе предусмотрена фармацевтическая композиция содержащая по меньшей мере одно описанное в настоящем документе соединение формулы (I), (Ia) или (Ib) или его фармацевтически приемлемая соль или сольват вместе с одним или несколькими фармацевтически приемлемыми носителями. Носитель(и) (или вспомогательное вещество(а)) является приемлемым или подходящим, если носитель совместим с другими ингредиентами композиции и не является вредным для реципиента (т.е. субъекта) композиции.
[00113] Согласно одному варианту осуществления предусмотрена фармацевтическая композиция, содержащая фармацевтически приемлемое вспомогательное вещество и соединение формулы (I) или его фармацевтически приемлемую соль.
[00114] Согласно одному варианту осуществления предусмотрена фармацевтическая композиция, содержащая фармацевтически приемлемое вспомогательное вещество и соединение формулы (Ia) или его фармацевтически приемлемую соль.
[00115] Согласно одному варианту осуществления предусмотрена фармацевтическая композиция, содержащая фармацевтически приемлемое вспомогательное вещество и соединение формулы (Ib) или его фармацевтически приемлемую соль.
[00116] Согласно одному варианту осуществления предусмотрена фармацевтическая композиция, содержащая фармацевтически приемлемое вспомогательное вещество и соединение формулы (II) или его фармацевтически приемлемую соль.
[00117] Согласно другому варианту осуществления предусмотрена фармацевтическая композиция, состоящую по существу из фармацевтически приемлемого вспомогательного вещества и соединения формулы (I) или его фармацевтически приемлемой соли. Согласно другому варианту осуществления предусмотрена фармацевтическая композиция, состоящая по существу из фармацевтически приемлемого вспомогательного вещества и соединения формулы (Ia) или его фармацевтически приемлемой соли. Согласно другому варианту осуществления предусмотрена фармацевтическая композиция, состоящая по существу из фармацевтически приемлемого вспомогательного вещества и соединения формулы (Ib) или его фармацевтически приемлемой соли. Согласно другому варианту осуществления предусмотрена фармацевтическая композиция, состоящая по существу из фармацевтически приемлемого вспомогательного вещества и соединения формулы (II) или его фармацевтически приемлемой соли.
[00118] Согласно определенным вариантам осуществления описанное в настоящем документе соединение формулы (I), (Ia) или (Ib) является по существу чистым, так как оно содержит менее чем приблизительно 5% или менее чем приблизительно 1%, или менее чем приблизительно 0,1% других органических малых молекул, таких как загрязняющие промежуточные продукты или побочные продукты, которые образуются, например, на одной или нескольких стадиях способа синтеза.
[00119] Эти фармацевтические композиции включают в себя композиции, подходящие для перорального, ректального, местного, буккального, парентерального (например, подкожного, внутримышечного, внутрикожного или внутривенного) вагинального, офтальмологического или аэрозольного введения.
[00120] Иллюстративные фармацевтические композиции используются в форме фармацевтического препарата, например, в твердой, полутвердой или жидкой форме, которая включает в себя одно или несколько раскрытых соединений в качестве активного ингредиента в смеси с органическим или неорганическим носителем или вспомогательным веществом, подходящим для наружного, энтерального или парентерального применения. Согласно некоторым вариантам осуществления активный ингредиент смешивают, например, с обычными нетоксичными, фармацевтически приемлемыми носителями для таблеток, пеллет, капсул, суппозиториев, растворов, эмульсий, суспензий и любой другой формы, подходящей для применения. Активное целевое соединение включено в фармацевтическую композицию в количестве, достаточном для оказания желаемого эффекта на процесс или состояние заболевания.
[00121] Согласно некоторым вариантам осуществления для приготовления твердых композиций, таких как таблетки, основной активный ингредиент смешивают с фармацевтическим носителем, например обычными ингредиентами для таблетирования, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, дикальций фосфат или камеди и другими фармацевтическими разбавителями, например водой, для образования твердой композиции для предварительного приготовления, содержащей гомогенную смесь раскрытого соединения или его нетоксичной фармацевтически приемлемой соли. Когда эти композиции до придания им лекарственной формы называются гомогенными, это означает, что активный ингредиент равномерно распределен по всей композиции, так что композицию легко разделить на одинаково эффективные стандартные лекарственные формы, такие как таблетки, пилюли и капсулы.
[00122] В твердых дозированных формах для перорального введения (капсулы, таблетки, пилюли, драже, порошки, гранулы и т.п.) композицию по настоящему изобретению смешивают с одним или несколькими фармацевтически приемлемыми носителями, такими как цитрат натрия или дикальция фосфат и/или любой из следующих: (1) такие наполнители или вспомогательные вещества, как крахмалы, целлюлоза, микрокристаллическая целлюлоза, силиконизированная микрокристаллическая целлюлоза, лактоза, сахароза, глюкоза, маннит и/или кремниевая кислота; (2) такие связующие вещества, как, например, карбоксиметилцеллюлоза, гипромеллоза, альгинаты, желатин, поливинилпирролидон, сахароза и/или камедь; (3) такие увлажнители, как глицерин; (4) такие разрыхлители, как кросповидон, кроскармеллоза натрия, крахмалгликолят натрия, агар-агар, карбонат кальция, крахмал картофельный или тапиока, альгиновая кислота, некоторые силикаты и карбонат натрия; (5) такие замедляющие растворение средства, как парафин; (6) такие ускорители абсорбции, как четвертичные аммониевые соединения; (7) такие смачивающие средства, как, например, докузат натрия, цетиловый спирт и моностеарат глицерина; (8) такие абсорбенты, как каолин и бентонитовая глина; (9) такие смазывающие вещества, как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и их смеси и (10) красители. В случае капсул, таблеток и пилюль согласно некоторым вариантам осуществления композиции содержат буферные средства. Согласно некоторым вариантам осуществления твердые композиции аналогичного типа также используются в качестве наполнителей в мягких и твердых желатиновых капсулах с использованием таких наполнителей, как лактоза или молочные сахара, а также полиэтиленгликоли с высокой молекулярной массой и т.п.
[00123] Согласно некоторым вариантам осуществления таблетку изготавливают прессованием или формовкой, необязательно, с одним или несколькими дополнительными ингредиентами. Согласно некоторым вариантам осуществления прессованные таблетки получают с использованием связующего вещества (например, желатина или гидроксипропилметилцеллюлозы), смазывающего вещества, инертного разбавителя, консерванта, разрыхлителя (например, гликолята крахмала натрия или сшитой натрий карбоксиметилцеллюлозы), поверхностно-активного или диспергирующего средства. Согласно некоторым вариантам осуществления формованные таблетки изготавливают путем формования в подходящей машине смеси композиции по настоящему изобретению, увлажненной инертным жидким разбавителем. Согласно некоторым вариантам осуществления таблетки и другие твердые лекарственные формы, такие как драже, капсулы, пилюли и гранулы, производят с линией разлома или готовят с покрытиями и оболочками, такими как энтеросолюбильные покрытия и другие покрытия.
[00124] Композиции для ингаляции или инсуффляции включают в себя растворы и суспензии в фармацевтически приемлемых водных или органических растворителях или их смесях и порошки. Жидкие лекарственные формы для перорального введения включают в себя фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к рассматриваемой композиции согласно некоторым вариантам осуществления жидкие лекарственные формы содержат инертные разбавители, такие как, например, вода или другие растворители, солюбилизирующие средства и такие эмульгаторы, как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (в частности, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и эфиры жирных кислот и сорбитана, циклодекстрины и их смеси.
[00125] Согласно некоторым вариантам осуществления суспензии, помимо композиции по настоящему изобретению, содержат суспендирующие средства, такие как, например, этоксилированные изостеариловые спирты, сложные эфиры полиоксиэтиленсорбитола и сорбита, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант и их смеси.
[00126] Согласно некоторым вариантам осуществления составы для ректального или вагинального введения представлены в виде суппозитория, который получают путем смешивания рассматриваемой композиции с одним или несколькими подходящими нераздражающими вспомогательными веществами или носителями, содержащими, например, масло какао, полиэтиленгликоль, воск для суппозиториев или салицилат, который является твердым при комнатной температуре, но жидким при температуре тела и, следовательно, будет плавиться в полости тела и высвобождать активное средство.
[00127] Лекарственные формы для трансдермального введения композиции по настоящему изобретению включают в себя порошки, аэрозоли, мази, пасты, кремы, лосьоны, гели, растворы, пластыри и ингаляторы. Согласно некоторым вариантам осуществления активный компонент смешивают в стерильных условиях с фармацевтически приемлемым носителем и с любыми консервантами, буферами или пропеллентами, если требуется.
[00128] Согласно некоторым вариантам осуществления мази, пасты, кремы и гели содержат, в дополнение к композиции субъекта, такие вспомогательные вещества, как животные и растительные жиры, масла, воски, парафины, крахмал, трагакант, производные целлюлозы, полиэтиленгликоли, силиконы, бентониты, кремниевая кислота, тальк и оксид цинка или их смеси.
[00129] Согласно некоторым вариантам осуществления порошки и аэрозоли содержат, помимо рассматриваемой композиции, такие вспомогательные вещества, как лактозу, тальк, кремниевую кислоту, гидроксид алюминия, силикаты кальция и порошок полиамида, или смеси этих веществ. Согласно некоторым вариантам осуществления аэрозоли дополнительно содержат обычные пропелленты, такие как хлорфторуглеводороды, и летучие незамещенные углеводороды, такие как бутан и пропан.
[00130] Согласно некоторым вариантам осуществления описанные в настоящем документе соединения составляют в виде глазных капель для офтальмологического введения.
[00131] Раскрытые в настоящем документе композиции и соединения альтернативно вводят в виде аэрозоля. Это достигается путем приготовления водного аэрозоля, липосомального препарата или твердых частиц, содержащих соединение. Согласно некоторым вариантам осуществления используется неводная (например, фторуглеродный пропеллент) суспензия. Согласно некоторым вариантам осуществления используются ультразвуковые распылители, поскольку они сводят к минимуму воздействие разрушения на средство, что приводит к разложению соединений, содержащихся в композициях по настоящему изобретению. Как правило, водный аэрозоль получают путем приготовления водного раствора или суспензии рассматриваемой композиции вместе с обычными фармацевтически приемлемыми носителями и стабилизаторами. Носители и стабилизаторы варьируют в зависимости от требований к конкретной композиции, но как правило, включают в себя неионогенные поверхностно-активные вещества (твины, плюроники или полиэтиленгликоль), такие безвредные белки, как сывороточный альбумин, сложные эфиры сорбита, олеиновую кислоту, лецитин, такие аминокислоты, как глицин, буферы, соли, сахара или сахарные спирты. Аэрозоли, как правило, получают из изотонических растворов.
[00132] Фармацевтические композиции, подходящие для парентерального введения, содержат предусмотренную композицию в сочетании с одним или несколькими фармацевтически приемлемыми стерильными изотоническими водными или неводными растворами, дисперсиями, суспензиями или эмульсиями или стерильными порошками, которые восстанавливаются в стерильные инъецируемые растворы или дисперсии, просто перед применением, которые согласно некоторым вариантам осуществления содержат антиоксиданты, буферы, бактериостаты, растворенные вещества, которые делают композицию изотонической по отношению к крови предполагаемого реципиента, или суспендирующими средствами или загустителями.
[00133] Примеры подходящих водных и неводных носителей, которые используют в фармацевтических композициях, включают в себя воду, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и т.п.) и их подходящие смеси, растительные масла, такие как оливковое масло и инъецируемые органические сложные эфиры, такие как этилолеат и циклодекстрины. Надлежащая текучесть поддерживается, например, путем использования материалов для покрытия, таких как лецитин, путем поддержания требуемого размера частиц в случае дисперсий и путем использования поверхностно-активных веществ.
[00134] Также рассматриваются энтеральные фармацевтические составы, включающие в себя раскрытое соединение и энтеросолюбильный материал; и фармацевтически приемлемый носитель или вспомогательное вещество. Энтеросолюбильные материалы относятся к полимерам, которые по существу нерастворимы в кислой среде желудка и которые преимущественно растворимы в кишечных жидкостях при определенных значениях рН. Тонкий кишечник представляет собой часть желудочно-кишечного тракта (кишечника) между желудком и толстым кишечником и включает в себя двенадцатиперстную кишку, тощую кишку и подвздошную кишку. рН двенадцатиперстной кишки составляет приблизительно 5,5, рН тощей кишки составляет приблизительно 6,5, а рН дистального отдела подвздошной кишки составляет приблизительно 7,5. Соответственно, энтеросолюбильные материалы не растворимы, например, до рН приблизительно 5,0, приблизительно 5,2, приблизительно 5,4, приблизительно 5,6, приблизительно 5,8, приблизительно 6,0, приблизительно 6,2, приблизительно 6,4, приблизительно 6,6, приблизительно 6,8, приблизительно 7,0, приблизительно 7,2, приблизительно 7,4, приблизительно 7,6, приблизительно 7,8, приблизительно 8,0, приблизительно 8,2, приблизительно 8,4, приблизительно 8,4, приблизительно 8,6, приблизительно 8,8, приблизительно 9,0, приблизительно 9,2, приблизительно 9,4, приблизительно 9,6, приблизительно 9,8 или приблизительно 10,0. Иллюстративные энтеросолюбильные материалы включают в себя ацетат-фталат целлюлозы (САР), фталат гидроксипропилметилцеллюлозы (НРМСР), поливинилацетат фталат (PVAP), ацетат сукцинат гидроксипропилметилцеллюлозы (HPMCAS), ацетат тримеллитат целлюлозы, сукцинат гидроксипропилметилцеллюлозы, ацетат сукцинат целлюлозы, ацетат гексагидрофталат целлюлозы, пропионатфталат целлюлозы, ацетат малеат целлюлозы, ацетилбутират целлюлозы, пропионат ацетат целлюлозы, сополимер метилметакриловой кислоты и метилметакрилата, сополимер метилакрилата, метилметакрилата и метакриловой кислоты, сополимер метилвинилового эфира и малеинового ангидрида (серия Gantrez ES), сополимер этилметилметакрила хлортриметиламмонийэтилакрилата, такие природные смолы, как зеин, шеллак и камедь, канифоль, и несколько коммерчески доступных энтеросолюбильных систем дисперсии (например, Eudragit L30D55, Eudragit FS30D, Eudragit L100, Eudragit S100, Kollicoat EMM30D, Estacryl 30D, Coateric и Aquateric). Растворимость каждого из вышеуказанных материалов либо известна, либо ее легко определить in vitro.
[00135] Доза композиции, содержащей по меньшей мере одно описанное в настоящем документе соединение формулы (I), (Ia) или (Ib), отличается в зависимости от состояния пациента (например, человека), т.е. стадии заболевания, общего состояния здоровья, возраста и других факторов.
[00136] Фармацевтические композиции вводят способом, соответствующим подлежащему лечению (или предотвращению) заболеванию. Подходящая доза и подходящая продолжительность и частота введения будут определяться такими факторами, как состояние пациента, тип и серьезность заболевания пациента, конкретная форма активного ингредиента и способ введения. Как правило, подходящая доза и схема лечения обеспечивают композицию(и) в количестве, достаточном для обеспечения терапевтического и/или профилактического эффекта (например, улучшенного клинического исхода, такого как более частые полные или частичные ремиссии, или более длительное отсутствие заболеваний и/или общая выживаемость, или уменьшение тяжести симптомов. Оптимальные дозы, как правило, определяют с использованием экспериментальных моделей и/или клинических испытаний. Согласно некоторым вариантам осуществления оптимальная доза зависит от массы тела, массы или объема крови пациента.
[00137] Пероральные дозы, как правило, составляют от приблизительно 1,0 до приблизительно 1000 мг, от одного до четырех или более раз в день.
Способы
[00138] В настоящем документе раскрыты способы модулирования активности MAGL. Предполагаемые способы, например, включают воздействие на указанный фермент описанным в настоящем документе соединением. Согласно некоторым вариантам осуществления соединение, используемое одним или несколькими из указанных выше способов, представляет собой одно из описанных в настоящем документе генерических, субгенерических или специфических соединений, таких как соединение формул (I), (Ia) или (Ib) или их фармацевтически приемлемая соль или сольват. Способность описанных в настоящем документе соединений модулировать или ингибировать MAGL, оценивают с помощью процедур, известных в настоящей области техники и/или описанных в настоящем документе. Согласно другому аспекту настоящего раскрытия предусмотрены способы лечения заболевания, связанного с экспрессией или активностью MAGL у пациента.
[00139] Также в настоящем документе раскрыты способы лечения и/или предотвращения у нуждающегося в этом пациента такого нарушения, как одно или несколько из острой или хронической боли и невропатии. Раскрытые способы включают введение фармацевтически эффективного количества описанного в настоящем документе соединения.
[00140] Согласно другому варианту осуществления представлен способ лечения боли у пациента, включающий введение терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата нуждающемуся в этом пациенту для лечения указанной боли. Согласно другому варианту осуществления представлен способ лечения невропатической боли у пациента, включающий введение терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата, нуждающемуся в этом пациенту для лечения указанной невропатической боли. Согласно другому варианту осуществления представлен способ лечения воспалительной боли у пациента, включающий введение терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата нуждающемуся в этом пациенту для лечения указанной воспалительной боли. Согласно другому варианту осуществления представлен способ лечения сложного регионарного болевого синдрома у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00141] Согласно другому варианту осуществления представлен способ лечения заболевания или нарушения у пациента, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата, причем заболевание или нарушение выбрано из группы, состоящей из эпилепсии/припадочного расстройства, рассеянного склероза, нейромиелита зрительного нерва (NMO), синдрома Туретта, болезни Альцгеймера и боли в животе, связанной с синдромом раздраженного кишечника. Согласно другому варианту осуществления представлен способ лечения эпилепсии/припадочного расстройства у пациента, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения рассеянного склероза у пациента, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения нейромиелита зрительного нерва (NMO) у пациента, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения синдрома Туретта у пациента, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения болезни Альцгеймера у пациента, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения боли в животе, связанной с синдромом раздраженного кишечника, у пациента, включающий введение нуждающемуся в этом пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00142] Согласно другому варианту осуществления представлен способ лечения острой боли, воспалительной боли, онкологической боли, боли, вызванной периферической невропатией, центральной боли, фибромиалгии, мигрени, вазоокклюзивных болевых кризов при серповидноклеточной анемии, спастичности или боли, связанной с рассеянным склерозом, функциональной боли в груди, ревматоидного артрита, остеоартрита или функциональной диспепсии у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения острой боли у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения воспалительной боли у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения онкологической боли у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения боли, вызванной периферической невропатией, у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения центральной боли у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения фибромиалгии у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения мигрени у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения вазоокклюзивных болезненных кризов при серповидноклеточной анемии у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения спастичности или боли, связанной с рассеянным склерозом, у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения функциональной боли в груди у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia), (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения ревматоидного артрита у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения остеоартрита у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения функциональной диспепсии у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00143] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения хронического моторного тикозного расстройства у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения хронического моторного тикозного расстройства у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00144] Согласно другому варианту осуществления представлен способ снижения внутриглазного давления в глазах (IOP) у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно другому варианту осуществления представлен способ лечения глаукомы у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00145] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения синдрома дефицита внимания и гиперактивности (ADHD) у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формулы (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения обсессивно-компульсивного расстройства (OCD) у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00146] Согласно другому варианту осуществления представлен способ лечения атопического дерматита у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00147] Согласно другому варианту осуществления представлен способ лечения зуда у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00148] Согласно другому варианту осуществления представлен способ лечения синдрома Дауна у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00149] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ синергетического усиления активности опиоидного анальгетика у пациента, которого подвергают лечению опиоидным анальгетиком, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формулы (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ уменьшения острых побочных эффектов, связанных с опиоидным анальгетиком у пациента, которого подвергают лечению опиоидным анальгетиком, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формулы (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00150] Согласно другому варианту осуществления представлен способ лечения дистонии у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00151] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения амиотрофического латерального склероза (ALS) или связанных с ALS симптомов у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00152] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения возбуждения при аутизме у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00153] Согласно другому варианту осуществления представлен способ лечения нарушения сна или дисфункции мочевого пузыря, связанного с рассеянным склерозом, у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формулы (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00154] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения болезни Хантингтона у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00155] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения болезни Паркинсона у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00156] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ улучшения функционального результата после инсульта у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00157] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения черепно-мозговой травмы у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00158] Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения невралгии тройничного нерва у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата. Согласно некоторым вариантам осуществления в настоящем документе раскрыт способ лечения глоссофарингеальной невралгии у нуждающегося в этом пациента, включающий введение пациенту терапевтически эффективного количества описанного в настоящем документе соединения формул (I), (Ia) или (Ib) или его фармацевтически приемлемой соли или сольвата.
[00159] Согласно определенным вариантам осуществления раскрытое соединение, используемое одним или несколькими из вышеуказанных способов, представляет собой одно из описанных в настоящем документе генерических, субгенерических или специфических соединений, таких как соединение формул (I), (Ia) или (Ib).
[00160] Раскрытые соединения вводят пациентам (животным и людям), нуждающимся в таком лечении, в дозировках, которые обеспечат оптимальную фармацевтическую эффективность. Понятно, что доза, необходимая для применения в любом конкретном применении, будет варьировать от пациента к пациенту не только в зависимости от конкретного выбранного соединения или композиции, но также от путей введения, природы подвергаемого лечению состояния, возраста и состояния пациента, одновременного приема лекарственных средств или специальной диеты, за которыми следит пациент, и других факторов, при этом соответствующая дозировка в конечном итоге остается на усмотрение лечащего врача. Для лечения указанных выше клинических состояний и заболеваний раскрытое в настоящем документе рассматриваемое соединение вводят перорально, подкожно, местно, парентерально, путем ингаляционного спрея или ректально в составах в виде дозированных лекарственных форм, содержащих традиционные нетоксичные фармацевтически приемлемые носители, вспомогательные средства и наполнители. Парентеральное введение включает подкожные инъекции, внутривенные или внутримышечные инъекции или способы инфузии.
[00161] В настоящем документе также рассматриваются комбинированные терапии, например, для совместного введения раскрытого соединения и дополнительного активного средства, как часть конкретной схемы лечения, предназначенной для обеспечения положительного эффекта от совместного действия этих терапевтических средств. Благоприятный эффект комбинации включает в себя, без ограничения, фармакокинетическое или фармакодинамическое взаимодействие, возникающее в результате комбинации терапевтических средств. Введение этих терапевтических средств в комбинации, как правило, осуществляется в течение определенного периода времени (как правило, недели, месяцы или годы в зависимости от выбранной комбинации). Комбинированная терапия предназначена для последовательного введения нескольких терапевтических средств, то есть когда каждое терапевтическое средство вводят в разное время, а также для введения этих терапевтических средств или по меньшей мере двух терапевтических средств по существу одновременным образом.
[00162] Практически одновременное введение осуществляется, например, путем введения субъекту единственного состава или композиции (например, таблетки или капсулы с фиксированным соотношением каждого терапевтического средства) или в нескольких отдельных составах (например, капсулах) для каждого из терапевтических средств. Последовательное или по существу одновременное введение каждого терапевтического средства осуществляется любым подходящим путем, включая в себя, без ограничения, пероральные пути, внутривенные пути, внутримышечные пути и прямую абсорбцию через ткани слизистой оболочки. Терапевтические средства вводят одним и тем же путем или различными путями. Например, первое терапевтическое средство выбранной комбинации вводят внутривенной инъекцией, тогда как другие терапевтические средства комбинации вводят перорально. Альтернативно, например, все терапевтические средства вводят перорально или все терапевтические средства вводятся внутривенно.
[00163] Комбинированная терапия также включает введение терапевтических средств, как описано выше, в дополнительной комбинации с другими биологически активными ингредиентами и немедикаментозной терапией. Если комбинированная терапия дополнительно включает немедикаментозное лечение, немедикаментозное лечение проводится в любое подходящее время, пока достигается положительный эффект от совместного действия комбинации терапевтических средств и немедикаментозного лечения. Например, в соответствующих случаях полезный эффект все еще достигается, когда немедикаментозное лечение временно прекращается от введения терапевтических средств, возможно, на несколько дней или даже недель.
[00164] Компоненты комбинации вводят пациенту одновременно или последовательно. Понятно, что компоненты присутствуют в одном и том же фармацевтически приемлемом носителе и, следовательно, вводятся одновременно. Альтернативно, активные ингредиенты присутствуют в отдельных фармацевтических носителях, таких как обычные пероральные лекарственные формы, которые вводят либо одновременно, либо последовательно.
[00165] Например, для предполагаемого лечения боли раскрытое соединение вводят совместно с другим терапевтическим средством от боли, таким как опиоид, модулятор каннабиноидного рецептора (СВ-1 или СВ-2), ингибитор СОХ-2. ацетаминофен и/или нестероидное противовоспалительное средство. Дополнительные терапевтические средства, например, для лечения боли, которые вводятся совместно, включают в себя морфин, кодеин, гидроморфон, гидрокодон, оксиморфон, фентанил, трамадол и леворфанол.
[00166] Другие предполагаемые терапевтические средства для совместного введения включают в себя аспирин, напроксен, ибупрофен, сальсалат, дифлунизал, дексибупрофен, фенопрофен, кетопрофен, оксапрозин, локсопрофен, индометацин, толметин, сулиндак, этодолак, кеторолак, пироксикам, мелоксикам, теноксикам, дроксикам, лорноксикам, целекоксиб, парекоксиб, римонабант и/или эторикоксиб.
[00167] Следующие примеры приведены только в качестве иллюстрации различных вариантов осуществления и не должны рассматриваться как ограничивающие настоящее изобретение каким-либо образом.
ПРИМЕРЫ
Перечень сокращений
[00168] Как использовано выше и во всем описании настоящего изобретения, следующие сокращения, если не указано иное, следует понимать как характеризующиеся следующими значениями:


I. Химический синтез
[00169] Если не указано иное, реагенты и растворители использовали в том виде, в котором они были получены от коммерческих поставщиков. Безводные растворители и высушенную в печи стеклянную посуду использовали для синтетических превращений, чувствительных к влаге и/или кислороду. Выход не оптимизировали. Время реакции является приблизительным и оно не было оптимизировано. Колоночную хроматографию и тонкослойную хроматографию (ТСХ) проводили на силикагеле, если не указано иное. Спектры приведены в м.д. (δ), а константы взаимодействия (J) приведены в герцах. Для протонных спектров пик растворителя использовали в качестве контрольного пика.
Пример 1: 1,1,1,3,3,3-Гексафторпропан-2-ил-4-(2-((4-этокси-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат
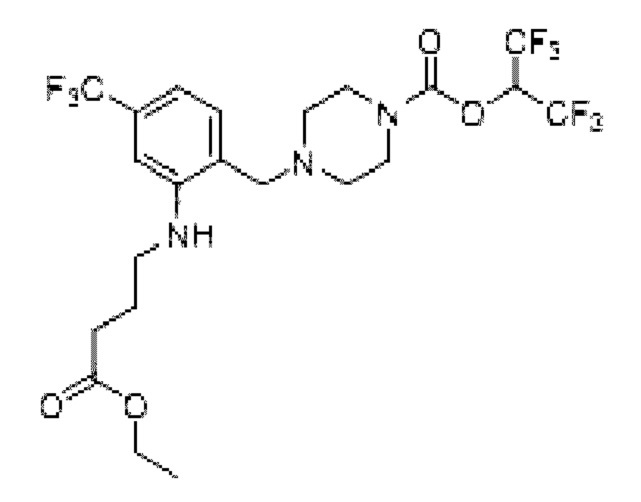
Стадия 1: Получение этил-4-((4-метоксибензил)амино)бутаноата
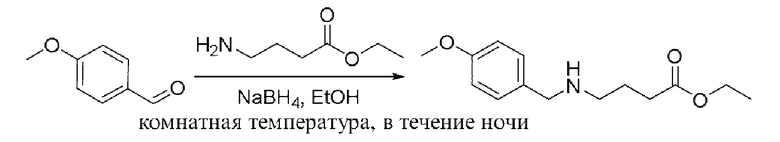
[00170] В колбу загружали этил-4-аминобутаноат (1,00 г, 7,62 ммоль, 1,00 экв.), EtOH (15 мл) и 4-метоксибензальдегид (1,04 мг, 7,62 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение 5 ч при температуре 70°С. Добавляли боргидрид натрия (176 мг, 4,65 ммоль, 0,60 экв.) и полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (3/17), получая 800 мг (выход 42%) этил-4-((4-метоксибензил)амино)бутаноата в виде белого масла. ЖХ/МС (ESI, m/z): 252 [М+Н]+.
Стадия 2: Получение этил-4-((2-формил-5-(трифторметил)фенил)(4-метоксибензил)амино)бутаноата
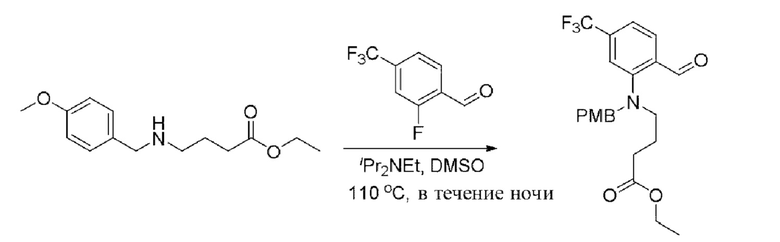
[00171] В колбу загружали этил-4-((4-метоксибензил)амино)бутаноат (400 мг, 1,59 ммоль, 1,00 экв.), 2-фтор-4-(трифторметил)бензальдегид (304 мг, 1,59 ммоль, 1,00 экв.), DMSO (15 мл) и DIPEA (620 мг, 4,77 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при температуре 110°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/4), получая 110 мг (выход 16%) этил-4-((2-формил-5-(трифторметил)фенил)(4-метоксибензил)амино)бутаноата в виде светло-желтого масла. ЖХ/МС (ESL m/z): 424 [М+Н]+
Стадия 3: Получение 1-(трет-бутил)-4-(1,1,1,3,3,3-гексафторпропан-2-ил)пиперазин-1,4-дикарбоксилата
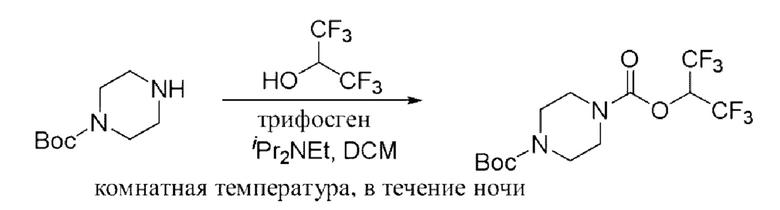
[00172] В колбу загружали трифосген (7,98 г, 26,9 ммоль, 0,50 экв.), DCM (150 мл) и HFIP (18,1 г, 108 ммоль, 2,00 экв.) в атмосфере азота. DIPEA (20,8 г, 161 ммоль, 3,00 экв.) добавляли при температуре 0°С и полученный раствор перемешивали в течение 2 ч при температуре 0°С. Добавляли трет-бутилпиперазин-1-карбоксилат (10,0 г, 53,7 ммоль, 1,00 экв.) и полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (150 мл). Полученный раствор экстрагировали DCM (2×200 мл), а органические слои объединяли, промывали рассолом (2×150 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/4), с получением 15,5 г (выход 76%) 1-(трет-6утил)-4-(1,1,1,3,3,3)-гексафторпропан-2-ил)пиперазин-1,4-дикарбоксилата в виде белого твердого вещества. ЖХ/МС (ESI, m/z): 381 [М+Н]+.
Стадия 4: Получение соли 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат
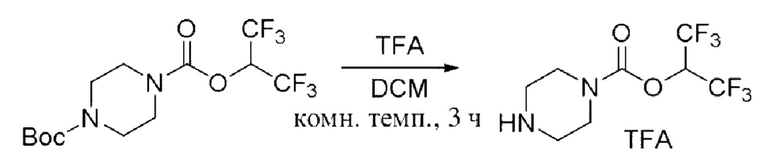
[00173] В колбу загружали 1-(трет-бутил)-4-(1,1,1,3,3,3-гексафторпропан-2-ил)пиперазин-1,4-дикарбоксилат (200 мг, 0,530 ммоль, 1,00 экв.), DCM (10 мл) и TFA (2 мл). Полученный раствор перемешивали в течение 3 ч при комнатной температуре и концентрировали, получая 250 мг соли 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат в виде светло-желтого масла. ЖХ/МС (ESI, m/z): 281 [М+Н]+.
Стадия 5: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-этокси-4-оксобутил)(4-метоксибензил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
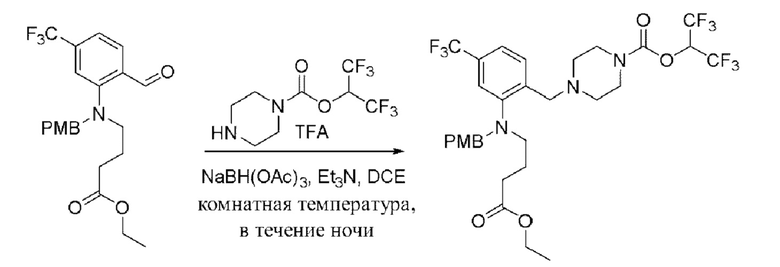
[00174] В колбу загружали этил-4-((2-формил-5-(трифторметил)фенил)-(4-метоксибензил)амино)бутаноат (110 мг, 0,260 ммоль, 1,00 экв), DCE (10 мл), TEA (79,0 мг, 0,780 ммоль, 3,00 экв.) и соль 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат (73,0 мг, 0,260 ммоль, 1,00 экв.). Смесь перемешивали в течение 1 часа при комнатной температуре и добавляли триацетоксиборгидрид натрия (129 мг, 0,780 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (96/4), получая 170 мг (выход 95%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-)((4-этокси-4-оксобутил)-(4-метоксибензил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде светло-желтого масла. ЖХ/МС (ESI, m/z): 688 [М+Н]+.
Стадия 6: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-этокси-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
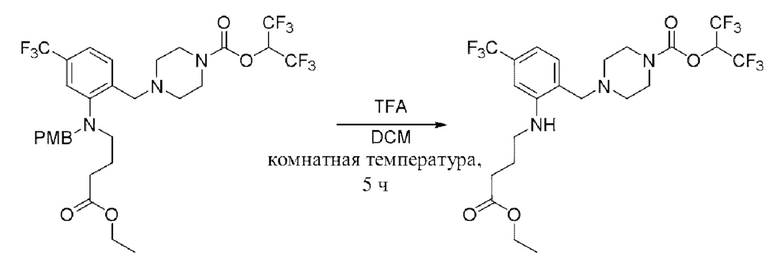
[00175] В колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-этокси-4-оксобутил)-(4-метоксибензил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (170 мг, 0,250 ммоль, 1,00 экв.), DCM (10 мл) и TFA (2 мл). Полученный раствор перемешивали в течение 3 часов при комнатной температуре и концентрировали. Неочищенный продукт (180 мг) очищали препаративной ВЭЖХ с получением 28,9 мг (выход 21%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-этокси-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде светло-желтого масла. 1Н ЯМР (300 МГц, метанол-d4) δ 7,15-7,18 (м, 1H), 6,84-6,87 (м, 2Н), 6,13-6,21 (м, 1H), 4,11-4,18 (м, 2Н), 3,57-3,60 (м, 6Н), 3,24 (т, J=6 Гц, 2Н), 2,46-2,53 (м, 6Н), 1,95-2,04 (м, 2Н), 1,26 (т, J=3 Гц, 3Н). ЖХ/МС (ESI, m/z): 568 [М+Н]+.
Пример 2: 1,1,1,3,3,3-Гексафторпропан-2-ил-4-(2-((4-(трет-бутокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат
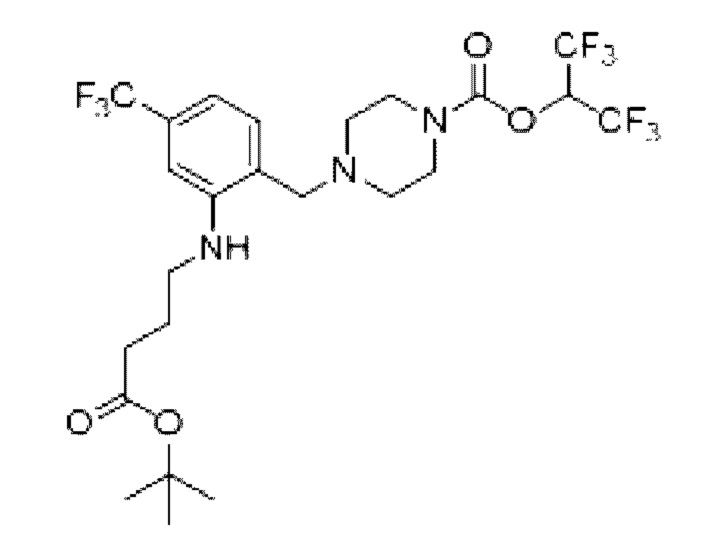
Стадия 1: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(трет-бутокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
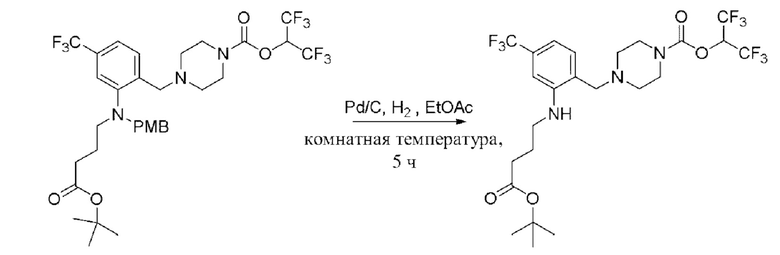
[00176] В колбу загружали EtOAc (10 мл) и 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(трет-бутокси)-4-оксобутил)-(4-метоксибензил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (200 мг, 0,280 ммоль, 1,00 экв., полученный, как описано в примере 1, стадии 1-5, с использованием трет-бутил-4-аминобутаноата на стадии 1). Вводили водород и полученный раствор перемешивали в течение 5 часов при комнатной температуре, затем твердые вещества отфильтровывали и фильтрат концентрировали. Неочищенный продукт очищали препаративной ВЭЖХ с получением 64,6 мг (выход 39%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(трет-бутокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде светло-желтого масла. 1Н ЯМР (400 МГц, хлороформ-d) δ 7,05 (д, J=7,2 Гц, 1Н), 6,86 (д, J=7,6 Гц, 1H), 6,78 (с, 1H), 6,13 (уш. с., 1Н), 5,73-5,76 (м, 1Н), 3,56 (уш. с., 6Н), 3,19 (т, J=6,6 Гц, 2Н), 2,45 (с, 4Н), 2,37 (т, J=7,2 Гц, 2Н), 1,93-1,97 (м, 2Н), 1,45 (с, 9Н). ЖХ/МС (ESI, m/z): 596 [М+Н]+.
Пример 3: 4-(2-((4-(((1,1,1,3,3,3-Гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)бутановая кислота
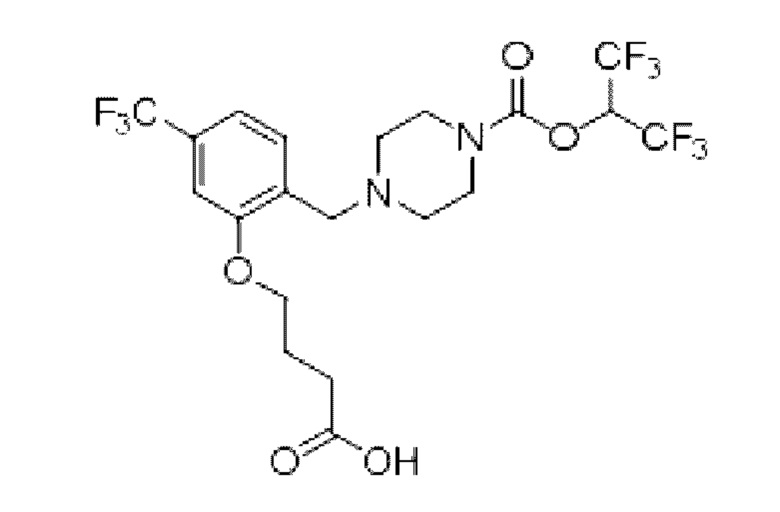
Стадия 1: Получение 2-гидрокси-4-(трифторметил)бензальдегида
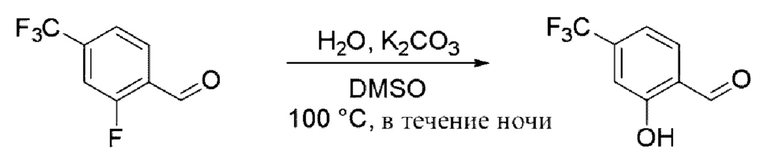
[00177] В колбу загружали 2-фтор-4-(трифторметил)бензальдегид (1,00 г, 5,21 ммоль, 1,00 экв.), воду (2 мл), DMSO (10 мл) и карбонат калия (2,16 г, 15,6 ммоль 3,00 экв.) в атмосфере азота. Полученный раствор перемешивали в течение ночи при температуре 110°С и гасили водой (50 мл). Полученный раствор экстрагировали EtOAc (2×80 мл), а органические слои объединяли, промывали рассолом (2×50 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/19), получая 500 мг (выход 51%) 2-гидрокси-4-(трифторметил)бензальдегида в виде светло-желтого масла.
Стадия 2: Получение трет-бутил-4-(2-формил-5-(трифторметил)фенокси)бутаноата
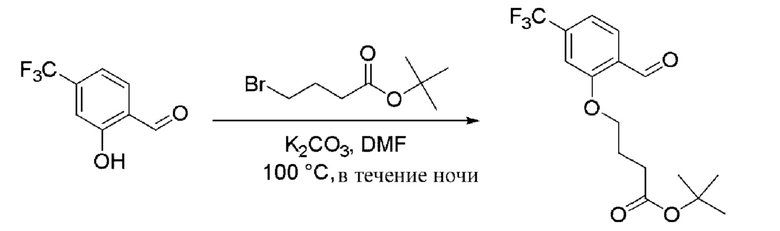
[00178] В колбу загружали 2-гидрокси-4-(трифторметил)бензальдегид (300 мг, 1,58 ммоль, 1,00 экв.), DMF (10 мл), карбонат калия (654 мг, 4,73 ммоль, 3,00 экв.) и трет-бутил-4-бромбутаноат (702 мг, 3,15 ммоль, 2,00 экв.). Полученный раствор перемешивали в течение ночи при температуре 100°С и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/10), с получением 450 мг (выход 86%) трет-бутил-4-(2-формил-5-(трифторметил)фенокси)бутаноата в виде светло-желтого твердого вещества. 1Н ЯМР (300 МГц, хлороформ-d) δ 10,5 (с, 1Н), 7,96 (д, J=7,5 Гц, 1Н), 7,29-7,33 (м, 2Н), 4,22 (т, J=6,0 Гц, 2Н) 2,50 (т, J=6,0 Гц, 2Н), 2,18-2,25 (м, 2Н), 1,49 (с, 9Н).
Стадия 3: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(4-(трет-бутокси)-4-оксобутокси)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
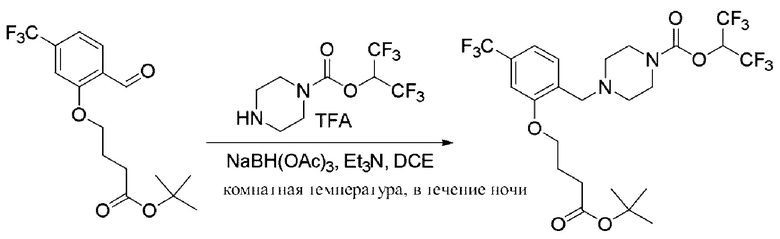
[00179] В колбу загружали соль 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат (202 мг, 0,720 ммоль, 1,20 экв., полученную как описано в примере 1, стадии 3-4), DCE (10 мл), TEA (183 мг, 1,80 ммоль, 3,00 экв.) и трет-бутил-4-(2-формил-5-(трифторметил)фенокси)бутаноат (200 мг, 0,600 ммоль, 1,00 экв.). Смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли триацетоксиборгидрид натрия (382 мг, 1,80 ммоль, 3,00 экв.) и реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (97/3), получая 230 мг (выход 64%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-)(4-(трет-бутокси)-4-оксобутокси)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде светло-желтого масла. ЖХ/МС (ESI, m/z): 597 [М+Н]+.
Стадия 4: Получение 4-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)бутановой кислоты
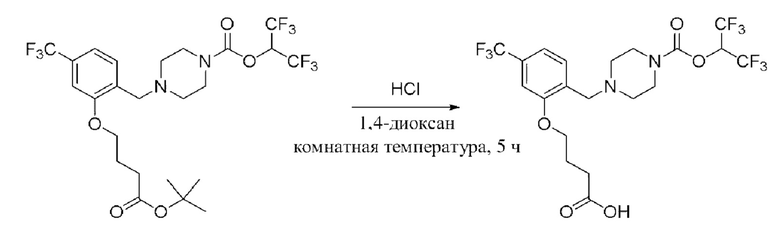
[00180] В колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(4-(трет-бутокси)-4-оксобутокси)-4-(трифторметил)бензилпиперазин-1-карбоксилат (200 мг, 0,340 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и соляную кислоту (3 мл). Полученный раствор перемешивали в течение 3 часов при комнатной температуре и концентрировали. Неочищенный продукт (400 мг) очищали препаративной ВЭЖХ с получением 46,4 мг (26% выход) 4-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-)ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)бутановой кислоты в виде белого твердого вещества. 1Н ЯМР (300 МГц, метанол-d4) δ 7,53 (д, J=7,8 Гц, 1H), 7,19-7,24 (м, 2Н), 6,10-6,18 (м, 1Н), 4,11 (т, J=6,2 Гц, 2H), 3,68 (с, 2Н), 3,56-3,62 (м, 4Н), 2,58-2,61 (м, 4Н), 2,49 (т, J=7,2 Гц, 2Н), 2,08-2,17 (м, 2Н). ЖХ/МС (ESI, m/z): 541 [М+Н]+.
Пример 4: 4-(5-Хлор-2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)бутановая кислота
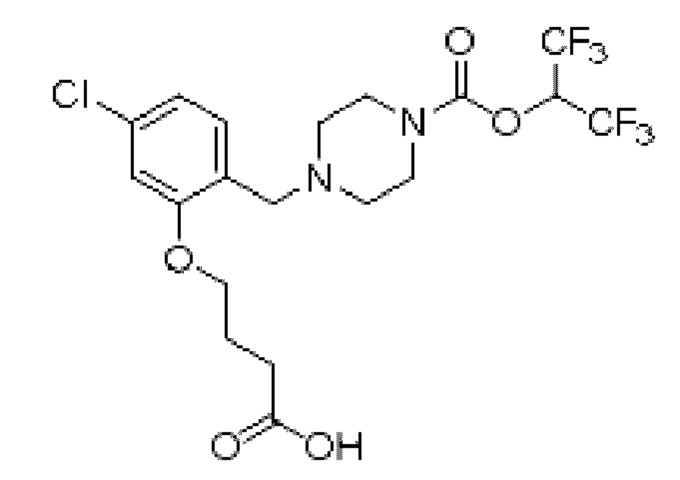
[00181] Указанное в заголовке соединение получали в соответствии с типичной процедурой примера 3, используя коммерчески доступный 4-хлор-2-гидроксибензальдегид на стадии 2, чтобы получить 4-(5-хлор-2-((4-(((1,1)-1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)бутановую кислоту в виде грязно-белого твердого вещества. 1H ЯМР (300 МГц, метанол-d4) 7,29 (д, J=8,1 Гц, 1Н), 7,01 (с, 1Н), 6,92-6,96 (м, 1H), 6,10-6,19 (м, 1Н), 4,07 (t, J=6,0 Гц, 2Н), 3,70 (с, 2Н), 3,63 (уш. с., 4Н), 2,67-2,68 (м, 4Н), 2,48 (т, J=7,0 Гц, 2Н), 2,07-2,16 (м, 2Н). ЖХ/МС (ESI, m/z): 507 [М+Н]+.
Пример 5: 1,1,1,3,3,3-Гексафторпропан-2-ил-4-(2-((4-(1-((этоксикарбонил)окси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат
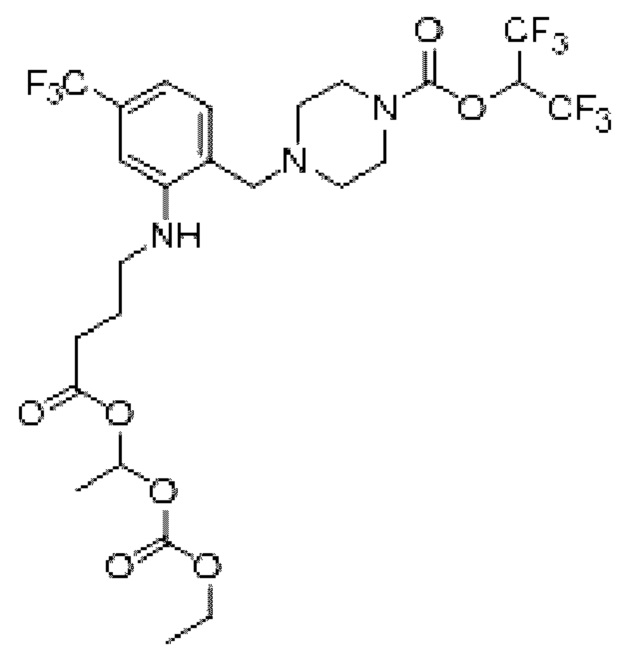
Стадия 1: Получение трет-бутил-4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутаноата
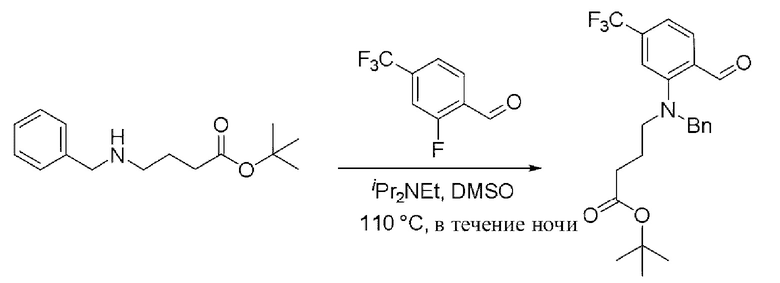
[00182] В колбу загружали трет-бутил-4-(бензиламино)бутаноат (230 мг, 0,920 ммоль, 1,00 экв., полученный, как описано в примере 1, стадия 1, используя бензальдегид и трет-бутил-4-аминобутаноат), 2-фтор-4-(трифторметил)бензальдегид (177 мг, 0,920 ммоль, 1,00 экв.), DMSO (10 мл) и DIPEA (356 мг, 2,75 ммоль, 3,00 экв.). Реакционную смесь перемешивали в течение ночи при температуре 110°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/9), с получением 135 мг (35% выход) трет-бутил-4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутаноата в виде желтого масла. ЖХ/МС (ESI, m/z): 422 [М+Н]+.
Стадия 2: Получение соли 4-(бензил(2-формил-5-(трифторметил)фенил)амино)бутановой кислоты 2,2,2-трифторацетата
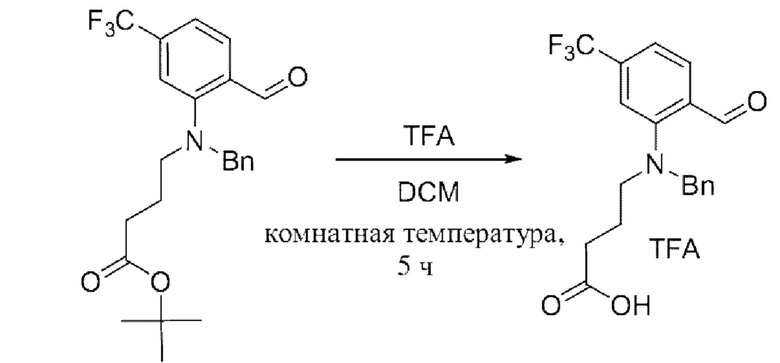
[00183] В колбу загружали трет-бутил-4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутаноат (800 мг, 1,90 ммоль, 1,00 экв.), DCM (2 мл) и TFA (10 мл). Полученный раствор перемешивали в течение 5 часов при комнатной температуре и концентрировали, чтобы получить 830 мг (неочищенной) соли 4-(бензил(2-формил-5-(трифторметил)фенил)амино)бутановой кислоты 2,2,2-трифторацетата в виде желтого масла. ЖХ/МС (ESI, m/z): 366 [М+Н]+.
Стадия 3: Получение 1-((этоксикарбонил)окси)этил-4-(бензил(2-формил-5-(трифторметил)фенил)амино)бутаноата
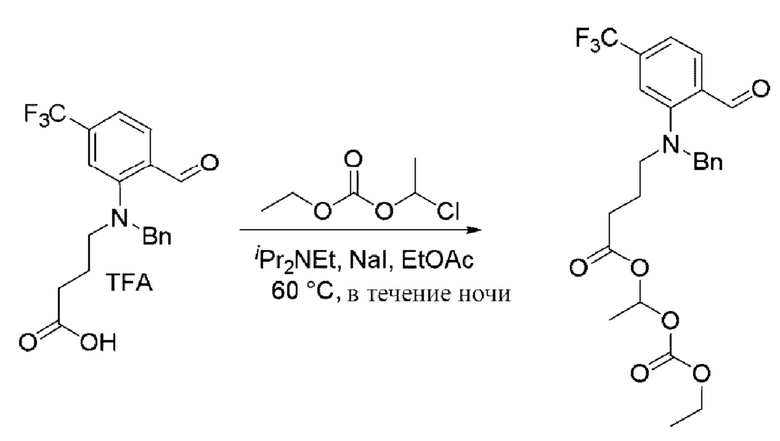
[00184] В колбу загружали соль 4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутановой кислоты 2,2,2-трифторацетат (300 мг, 0,820 ммоль, 1,00 экв.), EtOAc (10 мл), 1-хлорэтилэтилкарбонат (138 мг, 0,900 ммоль, 1,10 экв.), DIPEA (99,0 мг, 0,770 ммоль, 1,20 экв.) и йодид натрия (49,0 мг, 0,328 ммоль, 0,400 экв.) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 60°С и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/4), получая 330 мг (выход 83%) 1-((этоксикарбонил)окси)этил-4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутаноата в виде масла желтого цвета. ЖХ/МС (ESI, m/z): 482 [М+Н]+.
Стадия 4: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(бензил(4-(1-((этоксикарбонил)окси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
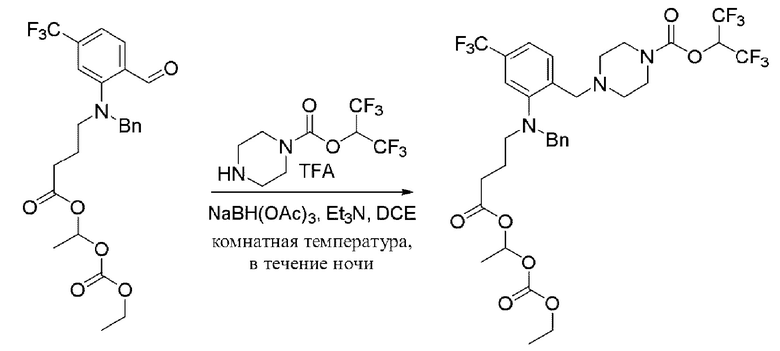
[00185] В колбу загружали 1-((этоксикарбонил)окси)этил-4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутаноат (250 мг, 0,520 ммоль, 1,00 экв.), DCE (10 мл) и соль 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат (145 г, 0,520 ммоль, 1,00 экв., полученной, как описано в примере 1, стадии 3-4). Смесь перемешивали в течение 1 часа при комнатной температуре и затем добавляли триацетоксиборгидрид натрия (330 мг, 1,56 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (97/3), получая 320 мг (выход 83%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-)(бензил-(4-(1-((этоксикарбонил)окси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде желтого масла. ЖХ/МС (ESI, m/z): 746 [М+Н]+.
Стадия 5: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(1-((этоксикарбонил)окси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
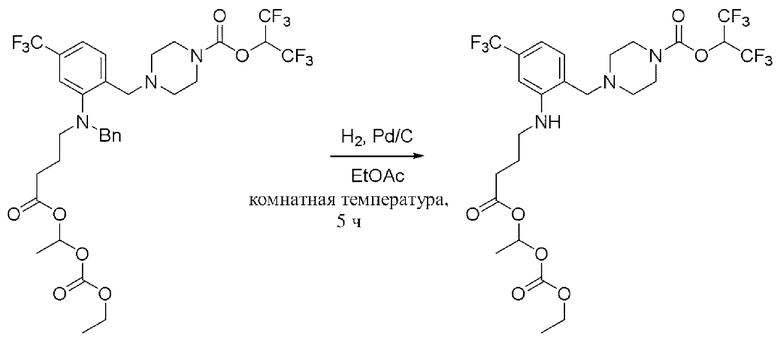
[00186] В колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(бензил-(4-(1-((этоксикарбонил)окси))этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (320 мг, 0,430 ммоль, 1,00 экв.), EtOAc (10 мл) и палладий на угле (107 мг). Водород вводили в реакционную смесь. Через 5 ч при комнатной температуре твердые вещества удаляли фильтрованием. Затем фильтрат концентрировали и очищали препаративной ВЭЖХ с получением 133,6 мг (выход 47%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(1-((этоксикарбонил)окси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде бесцветного масла. 1H ЯМР (300 МГц, хлороформ-d) δ 7,05-7,07 (м, 1Н), 6,86-6,91 (м, 1Н), 6,75-6,80 (м, 2Н), 6,13 (уш. c., 1Н), 5,70-5,79 (м, 1H), 4,15-2,25 (м, 2Н), 3,55 (уш. с., 6Н), 3,19-3,23 (м, 2Н), 2,47-2,52 (м, 6Н), 1,99-2,03 (м, 2Н), 1,51 (д, J=5,4 Гц, 3Н), 1,30 (т, J=7,2 Гц, 3Н). ЖХ/МС (ESI, m/z): 656 [М+Н]+.
Пример 6: 1,1,1,3,3,3-Гексафторпропан-2-ил-4-(2-((4-(1-((изопропоксикарбонил)окси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат
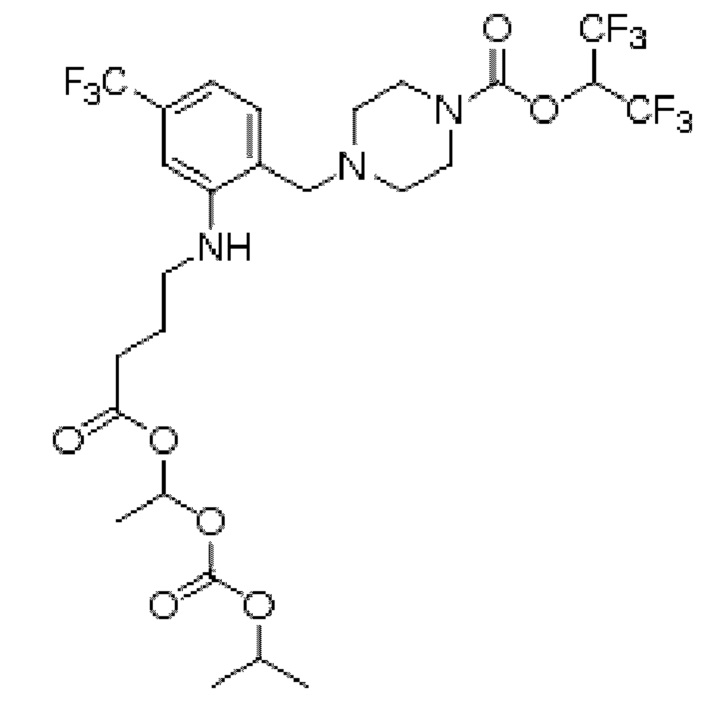
[00187] Указанное в заголовке соединение получали в соответствии с типичной процедурой примера 5 с использованием соляной кислоты и 1,4-диоксана на стадии 2 и 1-хлорэтилизопропилкарбоната на стадии 3 с получением 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(1-((изопропоксикарбонил)окси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде твердого вещества. 1Н ЯМР (300 МГц, хлороформ-d) δ 7,05-7,07 (м, 1H), 6,87 (д, J=6,0 Гц, 1H), 6,77-6,80 (м, 2Н), 6,12 (уш. с., 1Н), 5,70-5,79 (м, 1H), 4,82-4,91 (м, 1H), 3,56 (уш. с., 6Н), 3,19-3,23 (м, 2Н), 2,47-2,52 (м, 6Н), 1,99-2,03 (м, 2Н), 1,51 (д, J=5,7 Гц, 3Н), 1,27-1,31 (м, 6Н). ЖХ/МС (ESI, m/z): 670 [М+Н]+.
Пример 7: 1,1,1,3,3,3-Гексафторпропан-2-ил-4-(2-((4-оксо-4-((пивалоилокси)метокси)бутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат
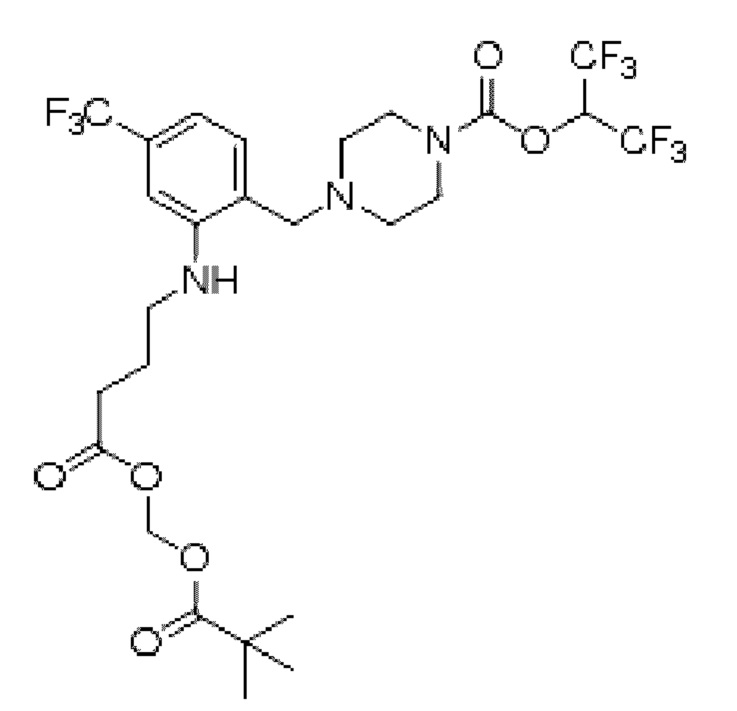
Стадия 1: Получение гидрохлорида 4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутановой кислоты
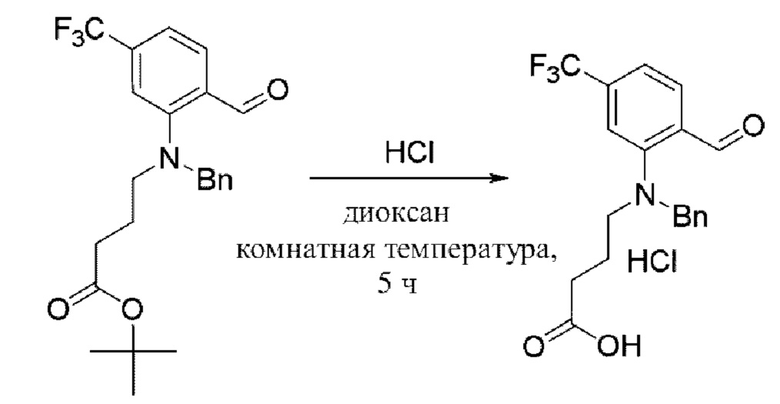
[00188] В колбу загружали гидрохлорид трет-бутил-4-(бензил(2-формил-5-(трифторметил)фенил)амино)бутаноата (350 мг, 0,830 ммоль, 1,00 экв., полученный, как описано в примере 5, стадия 1), 1,4-диоксан (10 мл) и соляную кислоту (2 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре и концентрировали с получением 360 мг (неочищенного) гидрохлорида 4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутановой кислоты в виде светло-желтого масла. ЖХ/МС (ESI, m/z): 366 [М+Н]+.
Стадия 2: Получение 1-(пивалоилокси)метил-4-(бензил(2-формил-5-(трифторметил)фенил)амино)бутаноата
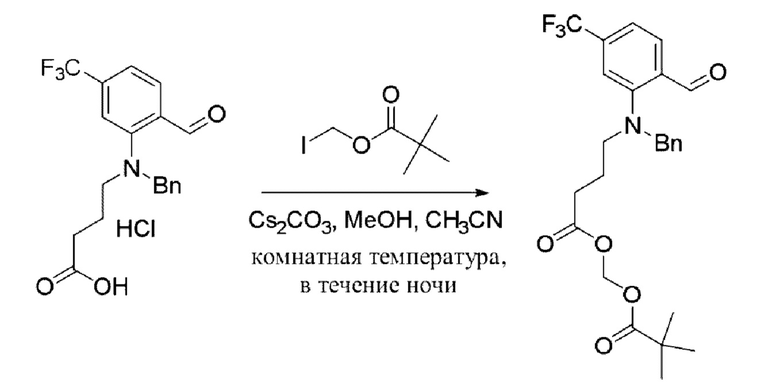
[00189] В колбу загружали гидрохлорид 4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутановой кислоты (303 мг, 0,830 ммоль, 1,00 экв.), МеОН (10 мл) и карбонат цезия (270 мг, 0,830 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение 3 часов при комнатной температуре и концентрировали. Добавляли MeCN (10 мл) и йодометилпивалат (602 мг, 2,49 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/4), получая 300 мг (выход 75%) 1-(пивалоилокси)метил-4-(бензил-(2-формил-5-(трифторметил)фенил))амино)бутаноата в виде желтого масла. ЖХ/МС (ESI, m/z): 480 [М+Н]+.
Стадия 3: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(бензил(4-оксо-4-((пивалоилокси)метокси)бутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
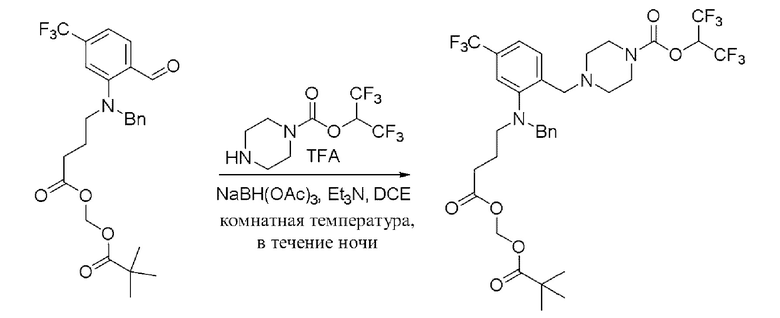
[00190] В колбу загружали 1-(пивалоилокси)метил-4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутаноат (300 мг, 0,630 ммоль, 1,00 экв.), DCE (10 мл), TEA (199 мг, 1,97 ммоль, 3,00 экв.) и соль 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат (175 мг, 0,620 ммоль, 1,00 экв., полученную, как описано в примере 1, стадии 3-4). Смесь перемешивали в течение 1 часа при комнатной температуре и добавляли триацетоксиборгидрид натрия (398 мг, 1,97 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (96/4), получая 200 мг (выход 43%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-)(бензил-(4-оксо-4-((пивалоилокси)метокси)бутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде желтого масла. ЖХ/МС (ESI, m/z): 744 [М+Н]+.
Стадия 4: Получение 1,1,1,3,3,3-гексафторпропан-2-ил 4-(2-((4-оксо-4-((пивалоилокси)метокси)бутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
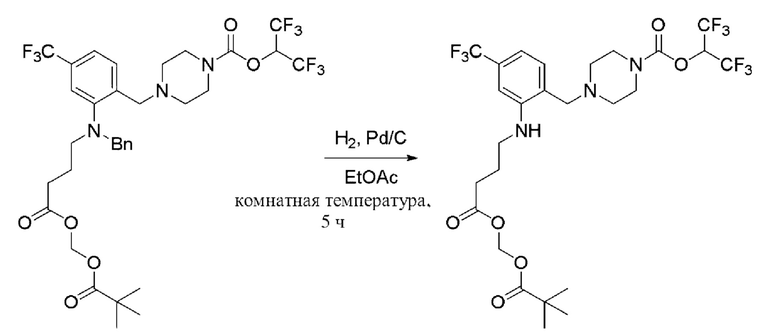
[00191] В колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(бензил-(4-оксо-4-((пивалоилокси)метокси)бутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (200 мг, 0,270 ммоль, 1,00 экв.), EtOAc (10 мл) и 10% палладий на угле (67,0 мг). Водород вводили в реакционную смесь. Через 5 ч при комнатной температуре реакционную смесь фильтровали, а фильтрат концентрировали и очищали препаративной ВЭЖХ с получением 22,4 мг (выход 13%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-оксо-4-((пивалоилокси)метокси)бутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде бесцветного масла. 1Н ЯМР (300 МГц, хлороформ-d) δ 7,06 (д, J=7,5 Гц, 1H), 6,87 (д, J=7,8 Гц, 1H), 6,77 (с, 1H), 6,15 (уш. с., 1H), 5,73-5,77 (м, 3Н), 3,55 (с, 6Н), 3,20 (т, J=6,8 Гц, 2Н), 2,45-2,54 (м, 6Н), 1,99-2,03 (м, 2Н), 1,19 (с, 9Н). ЖХ/МС (ESI, m/z): 654 [М+Н]+.
Пример 8: 1,1,1,3,3,3-Гексафторпропан-2-ил-4-(2-((4-(1-(изобутирилокси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат
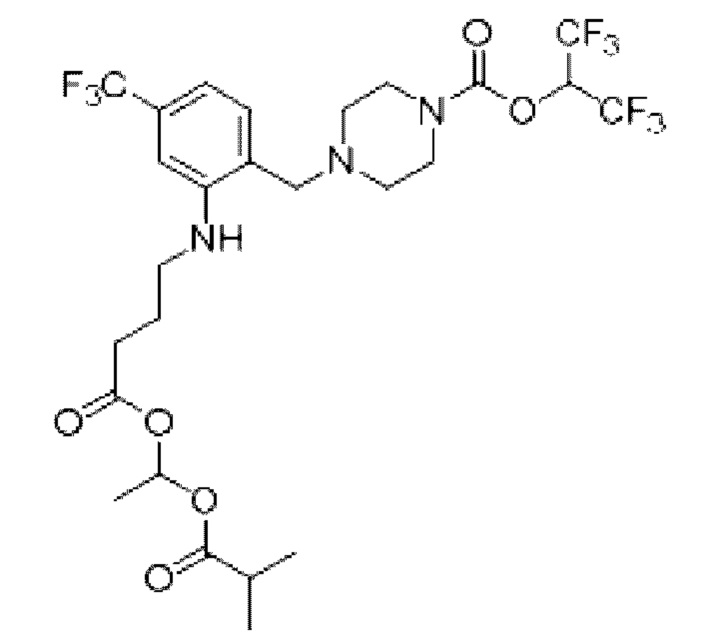
Стадия 1: Получение 1-(изобутирилокси)этил-4-(бензил(2-формил-5-(трифторметил)фенил)амино)бутаноата
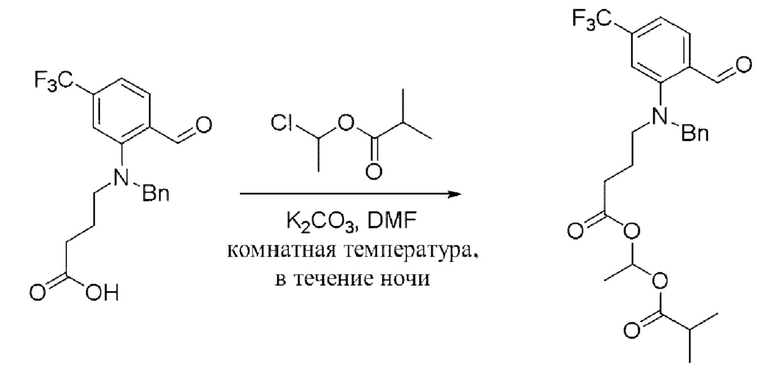
[00192] В колбу загружали 4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутановую кислоту (260 мг, 0,710 ммоль, 1,00 экв., полученную, как описано в примере 7, стадия 1), DMF (10 мл), 1-хлорэтилизобутират (215 мг, 1,43 ммоль, 2,00 экв.) и карбонат калия (295 мг, 2,13 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/9), получая 170 мг (выход 50%) 1-(изобутирилокси)этил-4-(бензил-(2-формил-5-(трифторметил)фенил))амино)бутаноата в виде желтого масла. ЖХ/МС (ESI, m/z): 480 [М+Н]+.
Стадия 2: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(бензил(4-(1-(изобутирилокси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
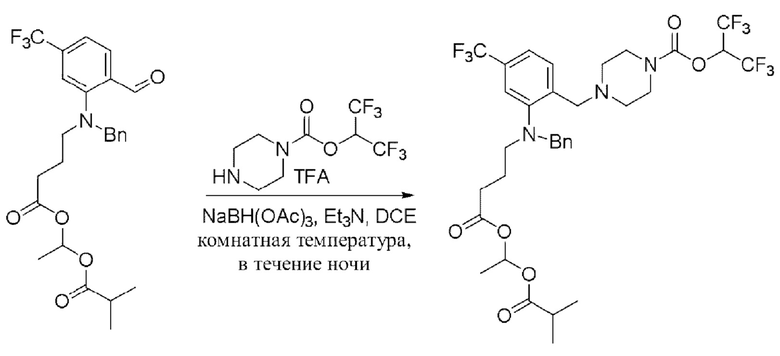
[00193] В колбу загружали 1-(изобутирилокси)этил-4-(бензил-(2-формил-5-(трифторметил)фенил)амино)бутаноат (170 мг, 0,350 ммоль, 1,00 экв.), соль 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат (99,0 мг, 0,350 ммоль, 1,00 экв., полученную, как описано в примере 1, стадии 3-4), DCE (10 мл) и TEA (108 мг, 1,07 ммоль, 3,00 экв.). Смесь перемешивали в течение 1 часа при комнатной температуре, а затем добавляли триацетоксиборгидрид натрия (226 мг, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (97/3), получая 200 мг (выход 76%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-)(бензил-(4-(1-(изобутирилокси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде желтого масла. ЖХ/МС (ESI, m/z): 744 [М+Н]+.
Стадия 3: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(1-(изобутирилокси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
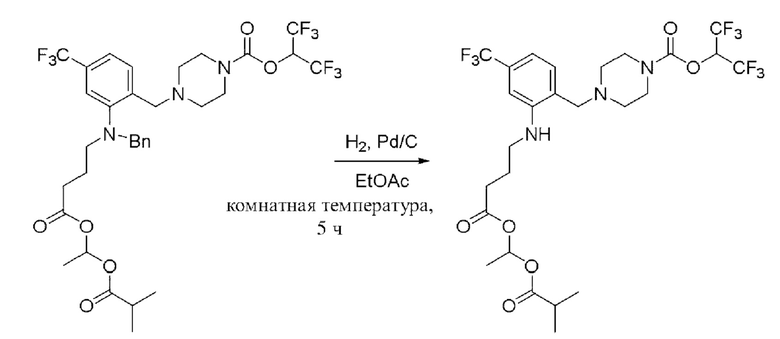
[00194] В колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(бензил-(4-(1-(изобутирилокси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (200 мг, 0,270 ммоль, 1,00 экв.), EtOAc (10 мл) и палладий на угле (100 мг). В реакцию вводили водород и полученную смесь перемешивали в течение 5 часов при комнатной температуре. Твердые вещества отфильтровывали, а фильтрат концентрировали. Сырой продукт (180 мг) очищали препаративной ВЭЖХ, получая 59,9 мг (выход 34%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((4-(1)-(изобутирилокси)этокси)-4-оксобутил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде светло-желтого масла. 1Н ЯМР (300 МГц, метанол-d4) δ 7,05 (д, J=7,5 Гц, 1H), 6,84-6,89 (м, 2Н), 6,77 (с, 1H), 6,13 (уш. с., 1Н), 5,71-5,79 (м, 1H), 3,54 (уш. с., 6Н), 3,20 (т, J=6,6 Гц, 2Н), 2,44-2,60 (м, 7Н), 1,94-2,04 (м, 2Н), 1,46 (д, J=5,4 Гц, 3Н), 1,13-1,16 (м, 6Н). ЖХ/МС (ESI, m/z): 654 [М+Н]+.
Пример 9: 2-(2-((2-((4-(((1,1,1,3,3,3-Гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)амино)этокси)уксусная кислота
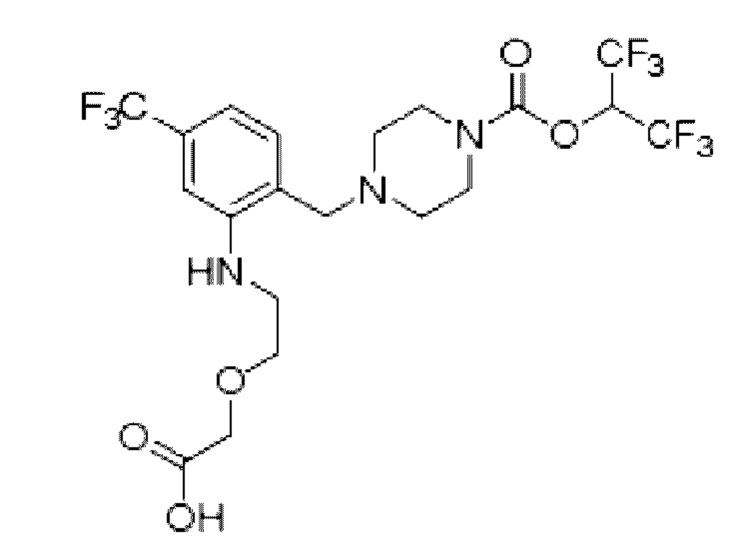
Стадия 1: Получение трет-бутил-2-(2-(((бензилокси)карбонил)амино)этокси)ацетата
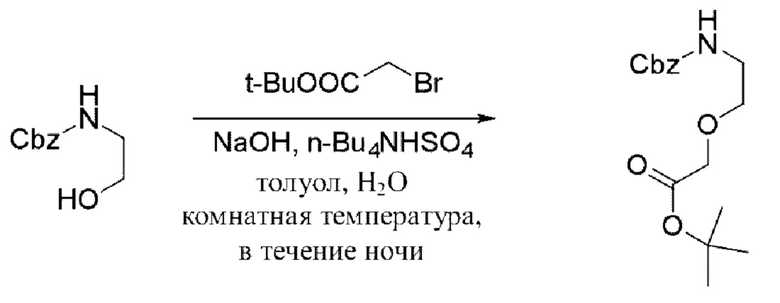
[00195] В колбу загружали трет-бутил-2-бромацетат (6,00 г, 30,8 ммоль, 1,00 экв.), толуол (180 мл), бензил-(2-гидроксиэтил)карбамат (12,0 г, 61,5 ммоль, 2,00 экв.), тетрабутиламмония гидросульфат (5,22 г, 15,40 ммоль, 0,50 экв.) и 30% водный раствор гидроксида натрия (90 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (80 мл). Полученный раствор экстрагировали EtOAc (2×100 мл), а органические слои объединяли, промывали рассолом (2×80 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/3), получая 3,70 г (выход 39%) трет-бутил-2-(2-(((бензилокси)карбонил)амино)этокси)ацетата в виде светло-желтого масла. ЖХ/МС (ESI, m/z): 332 [M+Na]+.
Стадия 2: Получение трет-бутил-2-(2-аминоэтокси)ацетата

[00196] В колбу загружали трет-бутил-2-(2-(((бензилокси)карбонил)амино)этокси)ацетат (3,80 г, 12,3 ммоль, 1,00 экв.), EtOAc (40 мл) и палладий на угле (2,00 г). Вводили водород, и полученный раствор перемешивали в течение ночи при комнатной температуре. Реакционную смесь фильтровали, а фильтрат концентрировали в вакууме, получая 1,80 г (выход 84%) трет-бутил-2-(2-аминоэтокси)ацетата в виде бесцветного масла. ЖХ/МС (ESI, m/z): 176 [М+Н]+.
Стадия 3: Получение трет-бутил-2-(2-((2-формил-5-(трифторметил)фенил)(4-метоксибензил)амино)этокси)ацетата
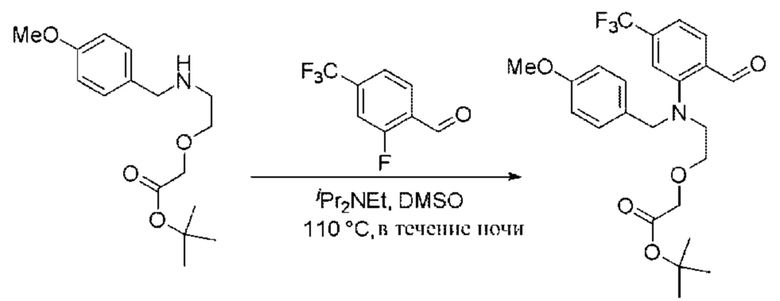
[00197] В колбу загружали трет-бутил-2-(2-((4-метоксибензил)амино)этокси)ацетат (300 мг, 1,02 ммоль, 1,00 экв., полученный, как описано в примере 1, стадия 1, с использованием трет-бутил-2-(2-аминоэтокси)ацетата), DMSO (10 мл), 2-фтор-4-(трифторметил)бензальдегид (235 мг, 1,22 ммоль, 1,20 экв.) и DIPEA (395 мг, 3,06 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при температуре 110°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя этилацетат/петролейный эфир (1/10), получая 160 мг (выход 34%) трет-бутил-2-(2-((2-формил-5-(трифторметил)фенил))(4-метоксибензил)амино)этокси)ацетата в виде масла желтого цвета. ЖХ/МС (ESI, m/z): 468 [М+Н]+.
Стадия 4: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((2-(2-(трет-бутокси)-2-оксоэтокси)этил)(4-метоксибензил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
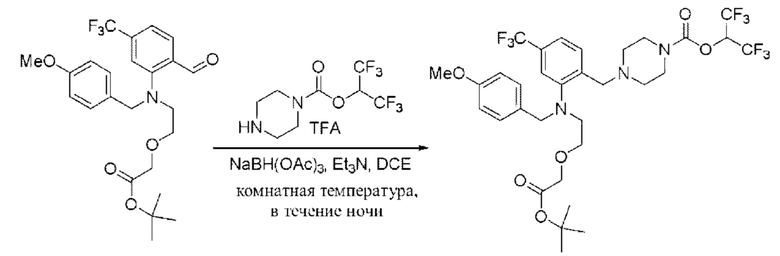
[00198] В колбу загружали соль 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат 2,2,2-трифторацетат (115 мг, 0,410 ммоль, 1,20 экв., полученную, как описано в примере 1, стадии 3-4), DCE (10 мл), TEA (104 мг, 1,03 ммоль, 3,00 экв.) и трет-бутил-2-(2-((2-формил-5-(трифторметил))фенил)-(4-метоксибензил)амино)этокси)ацетат (160 мг, 0,340 ммоль, 1,00 экв.). Смесь перемешивали в течение 1 часа при комнатной температуре, а затем добавляли триацетоксиборгидрид натрия (218 мг, 1,03 ммоль, 3,00 экв.). Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (97/3), получая 160 мг (выход 64%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-)((2-(2-(трет-бутокси)-2-оксоэтокси)этил)-(4-метоксибензил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде желтого масла. ЖХ/МС (ESI, m/z): 732 [М+Н]+.
Стадия 5: Получение 2-(2-((2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)амино)этокси)уксусной кислоты
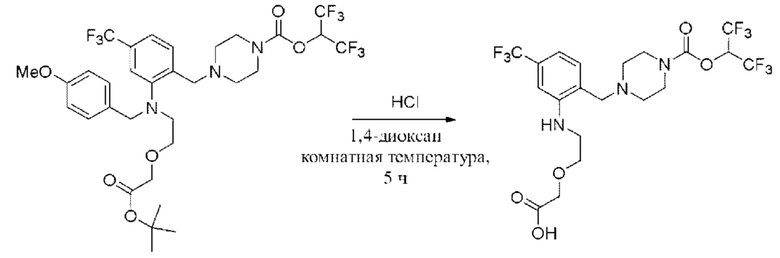
[00199] В колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((2-(2-(трет-бутокси)-2-оксоэтокси)этил)-(4-метоксибензил)амино)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (160 мг, 0,220 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и соляную кислоту (3 мл). Полученный раствор перемешивали в течение 5 часов при комнатной температуре и концентрировали. Неочищенный продукт (300 мг) очищали препаративной ВЭЖХ с получением 17,0 мг (14%) 2-(2-((2-((4-((1,1,1,3,3,3-гексафторпропан))-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)амино)этокси)уксусной кислоты в виде не совсем белого твердого вещества. 1Н ЯМР (400 МГц, метанол-d4) δ 16 7,16 (д, J=7,6 Гц, 1H), 6,84-6,88 (м, 2Н), 6,09-6,18 (м, 1H), 3,94 (с, 2Н), 3,82 (т, J=5,2 Гц, 2Н), 3,60 (уш. с., 6Н), 3,35-3,36 (м, 2Н), 2,45-2,51 (м, 4Н). ЖХ/МС (ESI, m/z): 556 [М+Н]+.
Пример 10: 2-(2-((4-Хлор-2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)амино)этокси)уксусная кислота
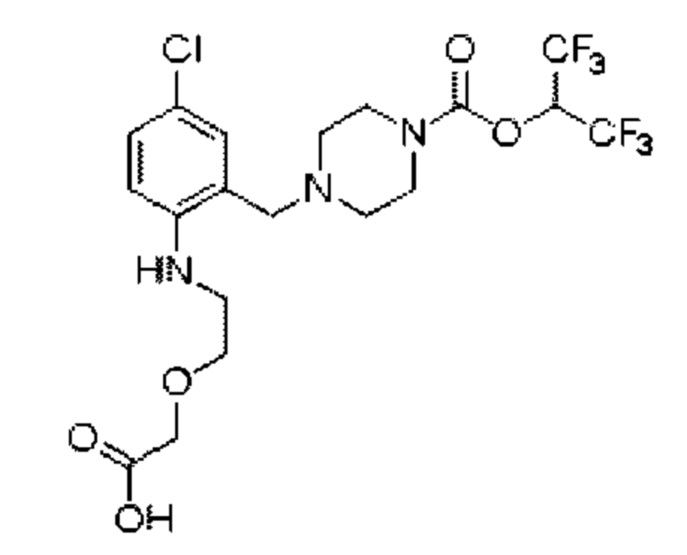
[00200] Указанное в заголовке соединение получали в соответствии с типичной процедурой примера 9 с использованием 5-хлор-2-фторбензальдегида на стадии 3, чтобы получить 2-(2-(4-хлор-2-((4-(((1)-1,1,3,3,3-гексафторпропан-2-ил)окси)кар6онил)пиперазин-1-ил)метил)фенил)амино)этокси)уксусную кислоту в виде желтого твердого вещества. 1Н ЯМР (400 МГц, метанол-d4) δ 7,12-7,14 (м, 1H), 7,02 (с, 1Н), 6,64 (д, J=8,4 Гц, 1Н), 6,11-6,17 (м, 1H), 4,05 (с, 2Н), 3,82 (т, 3=6,8 Гц, 2Н), 3,54-3,66 (м, 6Н), 3,29-3,32 (м, 2Н), 2,46-2,48 (м, 4Н). ЖХ/МС (ESI, m/z): 522 [М+Н]+.
Пример 11: 2-(2-((2-Фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)амино)этокси)уксусная кислота
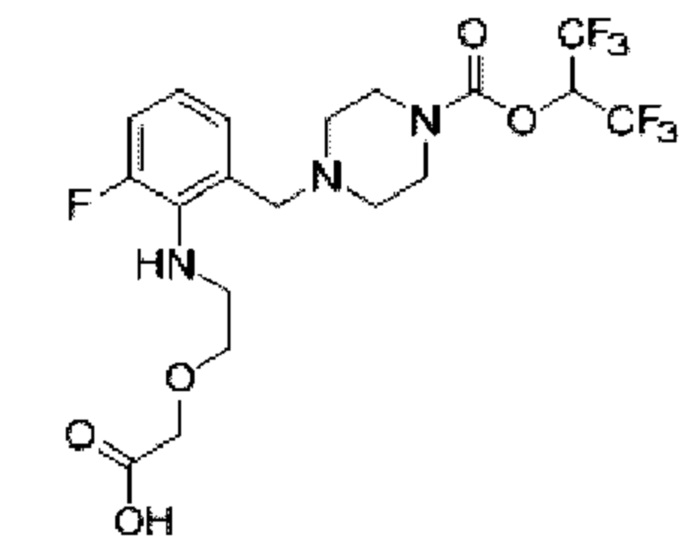
[00201] Указанное в заголовке соединение получали в соответствии с типичной процедурой примера 9 с использованием 2,3-дифторбензальдегида на стадии 3, чтобы получить 2-(2-((2-фтор-6-((4-(((1,1)-1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)амино)этокси)уксусную кислоту в виде светло-желтого масла. 1H ЯМР (300 МГц, метанол-d4) δ 6,86-6,99 (м, 2Н), 6,69-6,78 (м, 1Н), 6,08-6,18 (м, 1H), 3,98 (с, 2Н), 3,62-3,65 (м, 4Н), 3,56 (уш. с., 4Н), 3,45-3,46 (м, 2Н), 2,46 (уш. с., 4Н). ЖХ/МС (ESI, m/z): 506 [М+Н]+.
Пример 12: N-(2-((5-Хлор-2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)амино)этил)-N-(метилсульфонил)глицин
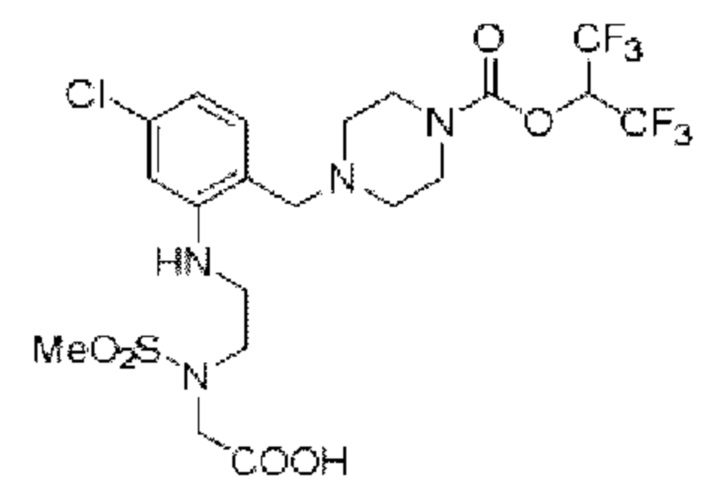
Стадия 1: Получение N-(2-(1,3-диоксогооиндолин-2-ил)этил)метансульфонамида

[00202] В колбу загружали 2-(2-аминоэтил)изоиндолин-1,3-дион (2,00 г, 10,5 ммоль, 1,00 экв.), DCM (20 мл), TEA (2,12 г, 21,0 ммоль, 2,00 экв.) и метансульфонилхлорид (1,44 г, 12,6 ммоль, 1,20 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (80 мл). Полученный раствор экстрагировали EtOAc (2×100 мл), а органические слои объединяли, промывали рассолом (2×80 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали, получая 800 мг (неочищенного) N-(2-(1,3-диоксоизоиндолин-2-ил)этил)метансульфонамида в виде светло-желтого твердого вещества. ЖХ/МС (ESI, m/z): 269 [М+Н]+.
Стадия 2: Получение трет-бутил-N-(2-(1,3-диоксоизоиндолин-2-ил)этил)-N-(метилсульфонил)глицината
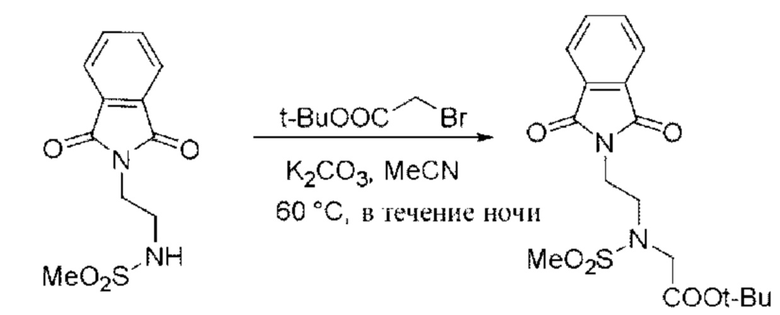
[00203] В колбу загружали N-(2-(1,3-диоксоизоиндолин-2-ил)этил)метансульфонамид (750 мг, 2,80 ммоль, 1,00 экв.), MeCN (10 мл), карбонат калия (1,16 г, 8,40 ммоль, 3,00 экв.) и трет-бутил-2-бромацетат (652 мг, 3,36 ммоль, 1,20 экв.). Полученный раствор перемешивали в течение ночи при температуре 60°С. Твердые вещества отфильтровывали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (3/97), получая 700 мг (выход 65%) трет-бутил-N-(2-(1,3-диоксоизоиндолин-2-ил)этил)-N-(метилсульфонил)глицината в виде грязно-белого твердого вещества. ЖХ/МС (ESI, m/z): 383 [М+Н]+.
Стадия 3: Получение трет-бутил-N-(2-аминоэтил)-N-(метилсульфонил)глицината
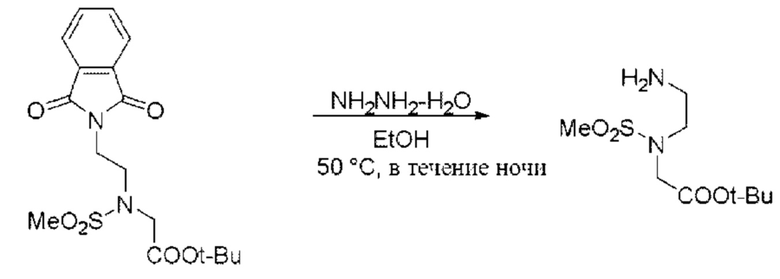
[00204] В колбу загружали трет-бутил-N-(2-(1,3-диоксоизоиндолин-2-ил)этил)-N-(метилсульфонил)глицинат (500 мг, 1,31 ммоль, 1,00 экв.), EtOH (10). мл) и гидразингидрат (328 мг, 6,55 ммоль, 5,00 экв.). Полученный раствор перемешивали в течение ночи при температуре 50°С и концентрировали, получая 300 мг (неочищенного) трет-бутил-N-(2-аминоэтил)-N-(метилсульфонил)глицината в виде светло-желтого твердого вещества. ЖХ/МС (ESI, m/z): 253 [М+Н]+.
Стадия 4: Получение трет-бутил-N-(2-((4-метоксибензил)амино)этил)-N-(метилсульфонил)глицината
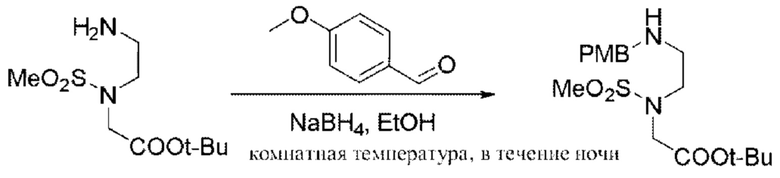
[00205] В колбу загружали трет-бутил-N-(2-аминоэтил)-N-(метилсульфонил)глицинат (300 мг, 1,19 ммоль, 1,00 экв.), EtOH (10 мл) и 4-метоксибензальдегид (162 мг, 1,19 ммоль, 1,00 экв.) Полученный раствор перемешивали в течение 5 часов при температуре 60°С. Добавляли боргидрид натрия (27,0 мг, 0,714 ммоль, 0,60 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (96/4), получая 240 мг (выход 54%) трет-бутил-N-(2-((4-метоксибензил)амино)этил)-N-(метилсульфонил)глицината в виде желтого масла. ЖХ/МС (ESI, m/z): 373 [М+Н]+.
Стадия 5: Получение трет-бутил-N-(2-((5-хлор-2-формилфенил)(4-метоксибензил)амино)этил)-N-(метилсульфонил)глицината
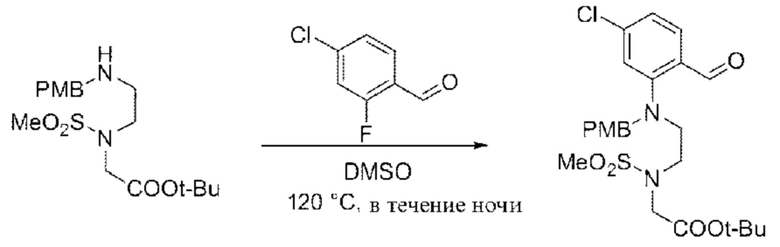
[00206] В колбу загружали трет-бутил-N-(2-((4-метоксибензил)амино)этил)-N-(метилсульфонил)глицинат (200 мг, 0,540 ммоль, 1,00 экв.), DMSO (10 мл) и 4-хлор-2-фторбензальдегид (128 мг, 0,810 ммоль, 1,50 экв.) в атмосфере азота. Полученный раствор перемешивали в течение ночи при температуре 120°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/4), с получением 80,0 мг (выход 29%) трет-бутил-N-(2-((5-хлор-2-формилфенил)(4-)метоксибензил)амино)этил)-N-(метилсульфонил)глицината в виде желтого масла. ЖХ/МС (ESI, m/z): 511 [М+Н]+.
Стадия 6: Получение 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((2-(N-(2-(трет-бутокси)-2-оксоэтил)метилсульфонамидо)этил)(4-метоксибензил)амино)-4-хлорбензил)пиперазин-1-карбоксилата
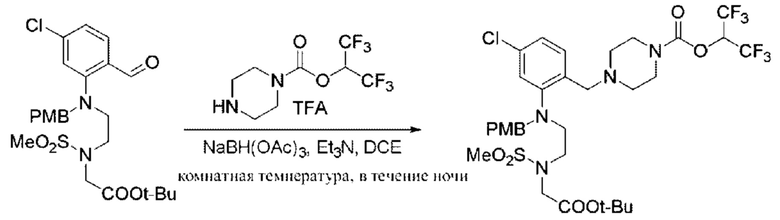
[00207] В колбу загружали соль 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат, 2,2,2-трифторацетат (53,0 мг, 0,190 ммоль, 1,20 экв., полученную как описано в примере 1, стадии 3-4), DCE (10 мл), TEA (48,0 мг, 0,470 ммоль, 3,00 экв.) и трет-бутил-N-(2-((5-хлор-2-формилфенил)(4-метоксибензил)амино)этил)-N-(метилсульфонил)глицинат (80,0 мг, 0,160 ммоль, 1,00 экв.). Смесь перемешивали в течение 1 часа при комнатной температуре и затем добавляли триацетоксиборгидрид натрия (100 мг, 0,470 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (96/4), получая 100 мг (выход 82%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-)((2-(N-(2-(трет-бутокси)-2-оксоэтил)метилсульфонамидо)этил)(4-метоксибензил)амино)-4-хлорбензил)пиперазин-1-карбоксилата в виде желтого масла. ЖХ/МС (ESI, m/z): 175 [М+Н]+.
Стадия 7: Получение N-(2-((5-хлор-2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)амино)этил)-N-(метилсульфонил)глицина
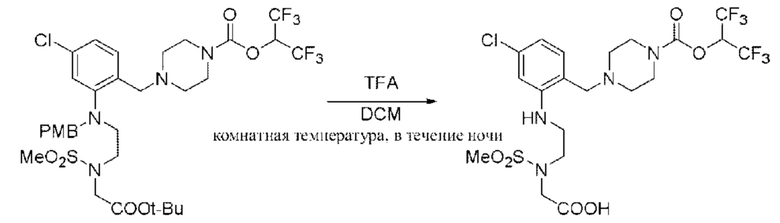
[00208] В колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-((2-(N-(2-(трет-бутокси)-2-оксоэтил)метилсульфонамидо)этил)(4-метоксибензил)амино)-4-хлорбензил)пиперазин-1-карбоксилат (100 мг, 0,130 ммоль, 1,00 экв.), DCM (10 мл) и TFA (5 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре и концентрировали. Неочищенный продукт очищали препаративной ВЭЖХ с получением 6,4 мг (выход 8%) N-(2-((5-хлор-2-((4-(((1,1,1,3,3,3-))гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)амино)этил)-N-(метилсульфонил)глицина в виде белого твердого вещества. 1Н ЯМР (300 МГц, метанол-d4) δ 6,95 (д, J=7,8 Гц, 1H), 6,63 (с, 1H), 6,57-6,58 (м, 1H), 6,17-6,15 (м, 1H), 3,98 (с, 2Н), 3,60-3,64 (м, 4Н), 3,52 (с, 2Н), 3,25-3,30 (м, 4Н), 3,06 (с, 3Н), 2,46-2,48 (м, 4Н). ЖХ/МС (ESI, m/z): 599 [М+Н]+.
Пример 13: 2-(5-Хлор-2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)уксусная кислота
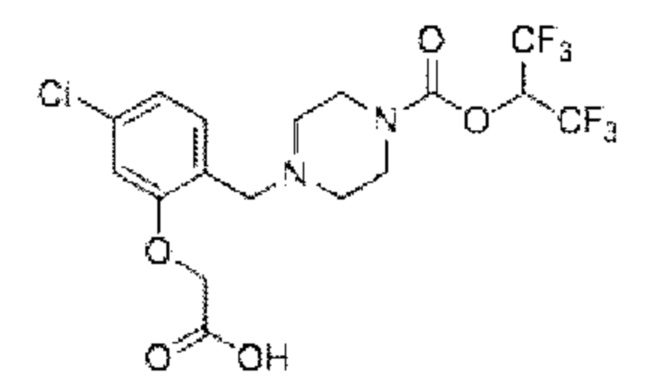
Стадия 1: Получение трет-бутил-4-(4-хлор-2-гидроксибензил)пиперазин-1-карбоксилата
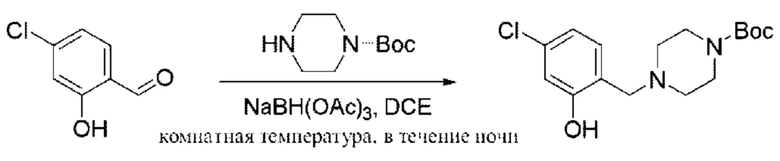
[00209] В колбу загружали 4-хлор-2-гидроксибензальдегид (1,00 г, 6,39 ммоль, 1,00 экв.), DCE (15 мл) и трет-бутилпиперазин-1-карбоксилат (1,43 г, 7,67 ммоль, 1,20 экв.). Смесь перемешивали в течение 1 часа при комнатной температуре и затем добавляли триацетоксиборгидрид натрия (4,08 г, 19,2 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (95/5), получая 1,20 г (выход 57%) трет-бутил-4-(4-хлор-2-гидроксибензил)пиперазин-1-карбоксилата в виде масла желтого цвета. ЖХ/МС (ESI, m/z): 327 [М+Н]+.
Стадия 2: Получение трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-4-хлорбензил)пиперазин-1-карбоксилата
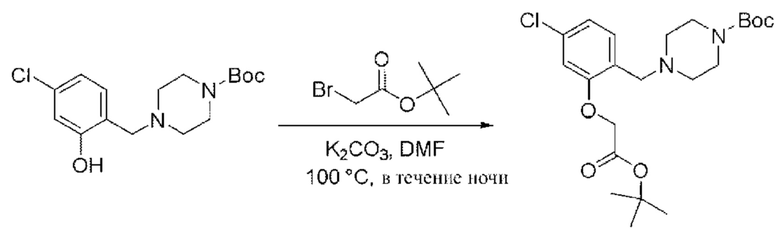
[00210] В колбу загружали трет-бутил-4-(4-хлор-2-гидроксибензил)пиперазин-1-карбоксилат (300 мг, 0,920 ммоль, 1,00 экв.), DMF (10 мл), трет-бутил-2-бромацетат (215 мг, 1,10 ммоль, 1,20 экв.) и карбонат калия (381 мг, 2,76 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при температуре 100°С и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (97/3), получая 200 мг (выход 49%) трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-4-хлорбензил)пиперазин-1-карбоксилат в виде желтого масла. ЖХ/МС (ESI, m/z): 441 [М+Н]+.
Стадия 3: Получение гидрохлорида 2-(5-хлор-2-(пиперазин-1-илметил)фенокси)уксусной кислоты
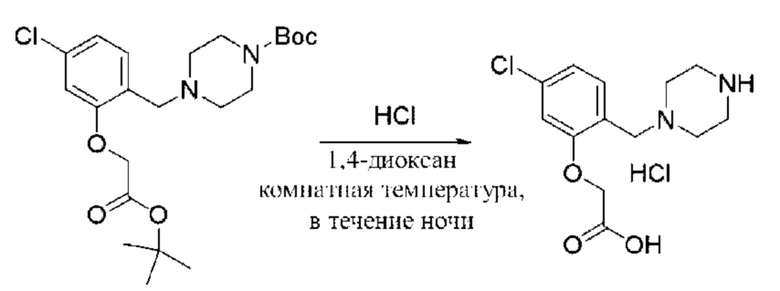
[00211] В колбу загружали трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-4-хлорбензил)пиперазин-1-карбоксилат (200 мг, 0,450 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и соляную кислоту (3 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре и концентрировали с получением 300 мг (неочищенного) гидрохлорида 2-(5-хлор-2-(пиперазин-1-илметил)фенокси)уксусной кислоты в виде желтого полутвердого вещества. ЖХ/МС (ESI, m/z): 285 [М+Н]+.
Стадия 4: Получение 2-(5-хлор-2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)уксусной кислоты
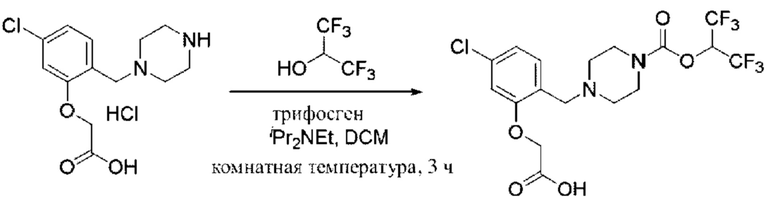
[00212] В колбу загружали трифосген (94,0 мг, 0,315 ммоль, 0,70 экв.), DCM (10 мл) и HFIP (152 мг, 0,900 ммоль, 2,00 экв.) в атмосфере азота. DIPEA (175 мг, 1,35 ммоль, 3,00 экв.) добавляли при температуре 0°С. Смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли гидрохлорид 2-(5-хлор-2-(пиперазин-1-илметил)фенокси)уксусной кислоты (128 мг, 0,450 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение 3 часов при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Неочищенный продукт (300 мг) очищали препаративной ВЭЖХ с получением 145,3 мг (выход 68%) 2-(5-хлор-2-((4-(((1,1,1,3,3,3-)гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)уксусной кислоты в виде белого твердого вещества. 1Н ЯМР (300 МГц, метанол-d4) δ 7,36 (д, J=7,8 Гц, 1Н), 7,25 (с, 1Н), 7,07-7,10 (м, 1Н), 6,17-6,30 (м, 1H), 4,68 (с, 2Н), 4,21 (с, 2Н), 3,86 (уш. с., 4Н), 3,19 (уш. с., 4Н). ЖХ/МС (ESI, m/z): 479 [М+Н]+.
Пример 14: 2-(2-((4-(((1,1,1,3,3,3-Гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)уксусная кислота
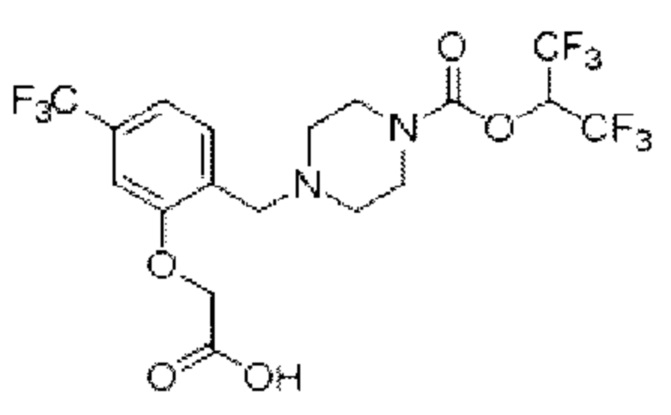
[00213] Указанное в заголовке соединение получали в соответствии с типичной процедурой примера 13 с использованием 2-гидрокси-4-(трифторметил)бензальдегида, полученного, как описано на стадии 1 примера 3, на стадии 1 с получением 2-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)уксусной кислоты в виде белого твердого вещества. 1Н ЯМР (300 МГц, метанол-d4) δ 7,57 (д, J=7,8 Гц, 1H), 7,45 (с, 1Н), 7,35 (д, J=7,8 Гц, 1Н), 6,15-6,28 (м, 1Н), 4,88 (с, 2Н), 4,26 (уш. с., 2Н), 3,83 (уш. с., 4Н), 3,83 (уш. с., 4Н). ЖХ/МС (ESI, m/z): 513 [М+Н]+.
Пример 15: 5-(2-((4-(((1,1,1,3,3,3-Гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)пентановая кислота
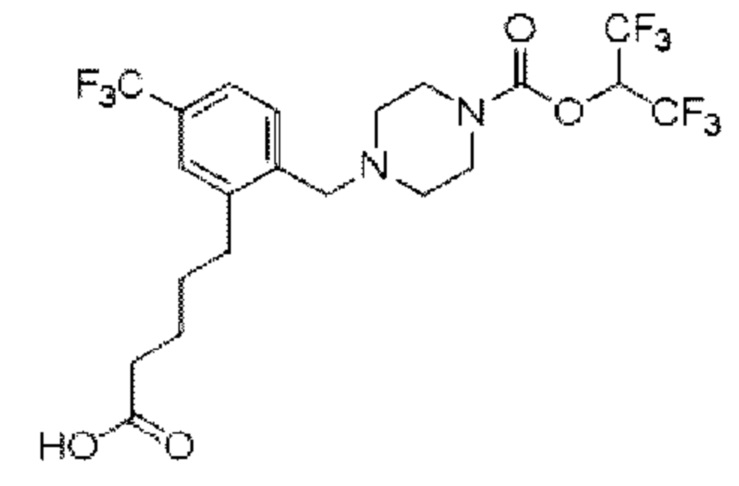
Стадия 1: Получение трет-бутил-4-(2-бром-4-(трифторметил)бензил)пиперазин-1-карбоксилата
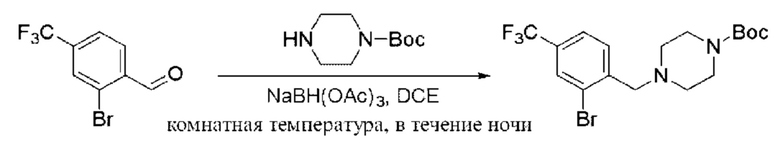
[00214] В колбу загружали 2-бром-4-(трифторметил)бензальдегид (1,00 г, 3,95 ммоль, 1,00 экв.), DCE (15 мл) и трет-бутилпиперазин-1-карбоксилат (813 мг, 4,35 ммоль, 1,10 экв.) Смесь перемешивали в течение 1 часа при комнатной температуре и затем добавляли триацетоксиборгидрид натрия (2,52 г, 11,9 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (98/2), получая 1,50 г (выход 90%) трет-бутил-4-(2-бром-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде светло-желтого масла. ЖХ/МС (ESI, m/z): 423 [М+Н]+.
Стадия 2: Получение трет-бутил-4-(2-формил-4-(трифторметил)бензил)пиперазин-1-карбоксилата
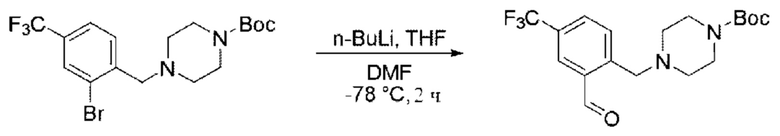
[00215] В колбу загружали итрет-бутил-4-(2-бром-4-(трифторметил)бензил)пиперазин-1-карбоксилат (2,00 г, 4,73 ммоль, 1,00 экв.) и THF (15 мл) в атмосфере азота. Смесь охлаждали до температуры -78°С и в течение 20 минут по каплям добавляли н-бутиллитий (2,5 М в гексане, 2,30 мл, 5,68 ммоль, 1,20 экв.). Через 1 час при температуре -78°С добавляли DMF (1,73 г, 23,7 ммоль, 5,00 экв.). Смесь перемешивали в течение 1 часа при температуре -78°С и концентрировали, получая 1,20 г (выход 68%) трет-бутил-4-(2-формил-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде красного масла. ЖХ/МС (ESI, m/z): 373 [М+Н]+.
Стадия 3: Получение бромистого (4-(трет-бутокси)-4-оксобутил)трифенилфосфония
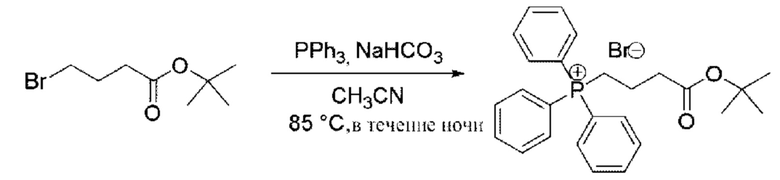
[00216] В колбу загружали трет-бутил-4-бромбутаноат (500 мг, 2,24 ммоль, 1,00 экв.), MeCN (15 мл), трифенилфосфин (590 мг, 2,25 ммоль, 1,00 экв.) и бикарбонат натрия (378 мг, 4,50 ммоль, 2,00 экв.) Полученный раствор перемешивали в течение ночи при температуре 85°С и охлаждали до комнатной температуры. Смесь фильтровали и фильтрат концентрировали. Остаток растирали с диэтиловым эфиром, получая 650 мг (выход 60%) бромистого (4-(трет-бутокси)-4-оксобутил)трифенилфосфония в виде белого твердого вещества. ЖХ/МС (ESI, m/z): 405 [М-Br]+.
Стадия 4: Получение трет-бутил-(Е)-4-(2-(5-(трет-бутокси)-5-оксопент-1-ен-1-ил)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
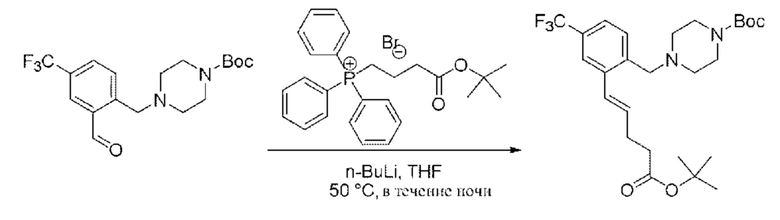
[00217] В колбу загружали бромистый (4-(трет-6утокси)-4-оксобутил)трифенилфосфоний (650 мг, 1,34 ммоль, 1,00 экв.) и THF (15 мл) в атмосфере азота. Смесь охлаждали до температуры -78°С и в течение 10 минут по каплям добавляли н-бутиллитий (2,5 М в гексане, 0,540 мл, 1,34 ммоль, 1,00 экв.). Смесь перемешивали в течение 30 минут при температуре -78°С и добавляли трет-бутил-4-(2-формил-4-(трифторметил)бензил)пиперазин-1-карбоксилат (500 мг, 1,34 ммоль, 1,00 экв.). Реакционную смесь перемешивали в течение ночи при температуре 50°С и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (95/5), получая 210 мг (31% выход) трет-бутил-(Е)-4-(2-(5-(трет-бутокси)-5)-оксопент-1-ен-1-ил)-4-(трифторметил)бензил)пиперазин-1-карбоксилат в виде желтого масла. ЖХ/МС (ESI, m/z): 499 [М+Н]+.
Стадия 5: Получение трет-бутил-4-(2-(5-(трет-бутокси)-5-оксопентил)-4-(трифторметил)бензил)пиперазин-1-карбоксилат
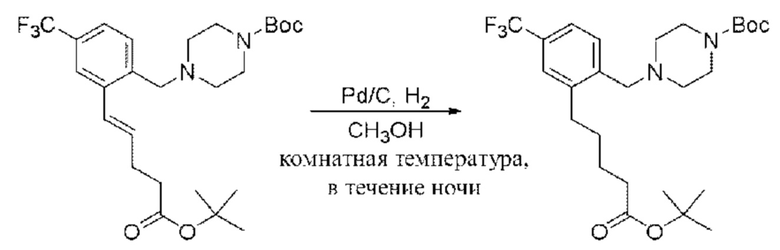
[00218] В колбу загружали трет-бутил-(Е)-4-(2-(5-(трет-бутокси)-5-оксопент-1-ен-1-ил)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (150 мг, 0,300 ммоль, 1,00 экв.), МеОН (10 мл) и палладий на угле (100 мг). В реакцию вводили водород и смесь перемешивали в течение ночи при комнатной температуре, а твердые вещества удаляли фильтрацией. Фильтрат концентрировали, чтобы получить 100 мг (неочищенного) трет-бутил-4-(2-(5-(трет-бутокси)-5-оксопентил)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде масла светло-желтого цвета. ЖХ/МС (ESI, m/z): 501 [М+Н]+.
Стадия 6: Получение гидрохлорида 5-(2-(пиперазин-1-илметил)-5-(трифторметил)фенил)пентановой кислоты
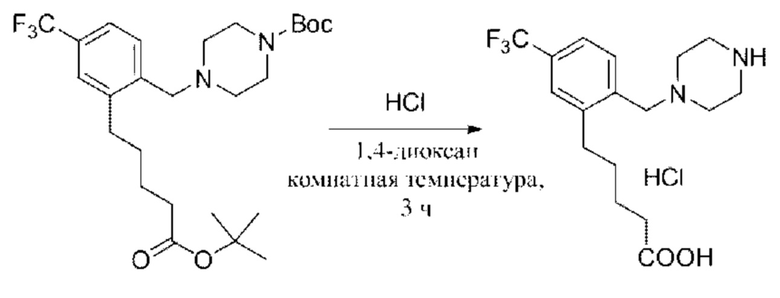
[00219] В колбу загружали трет-бутил-4-(2-(5-(трет-бутокси)-5-оксопентил)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (100 мг, 0,220 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и соляную кислоту (2 мл). Полученный раствор перемешивали в течение 3 ч при комнатной температуре и концентрировали, получая 150 мг (неочищенного) гидрохлорида 5-(2-(пиперазин-1-илметил)-5-(трифторметил)фенил)пентановой кислоты в виде светло-желтого масла. ЖХ/МС (ESI, m/z): 345 [М+Н]+.
Стадия 7: Получение 5-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)пентановой кислоты
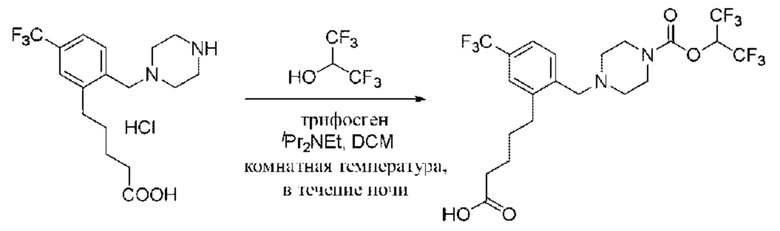
[00220] В колбу загружали трифосген (39,0 мг, 0,130 ммоль, 0,70 экв.), DCM (10 мл) и HFIP (64,0 мг, 0,380 ммоль, 2,00 экв.) в атмосфере азота. DIPEA (73,0 мг, 0,560 ммоль, 3,00 экв.) добавляли при температуре 0°С и смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли гидрохлорид 5-(2-(пиперазин-1-илметил)-5-(трифторметил)фенил)пентановой кислоты (65,0 мг, 0,190 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Неочищенный продукт (300 мг) очищали препаративной ВЭЖХ с получением 21,5 мг (выход 21%) 5-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-)ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)пентановой кислоты в виде бесцветного масла. 1Н ЯМР (300 МГц, метанол-d4) δ 7,41-7,50 (м, 3Н), 6,07-6,19 (м, 1H), 3,60 (с, 2Н), 3,47-3,58 (м, 4Н), 2,79-2,84 (м, 2Н), 2,47-2,49 (м, 4Н), 2,30 (т, J=6,9 Гц, 2Н), 1,64-1,75 (м, 4Н). ЖХ/МС (ESI, m/z): 539 [М+Н]+.
Пример 16: 1-(2-((4-(((1,1,1,3,3,3-Гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновая кислота
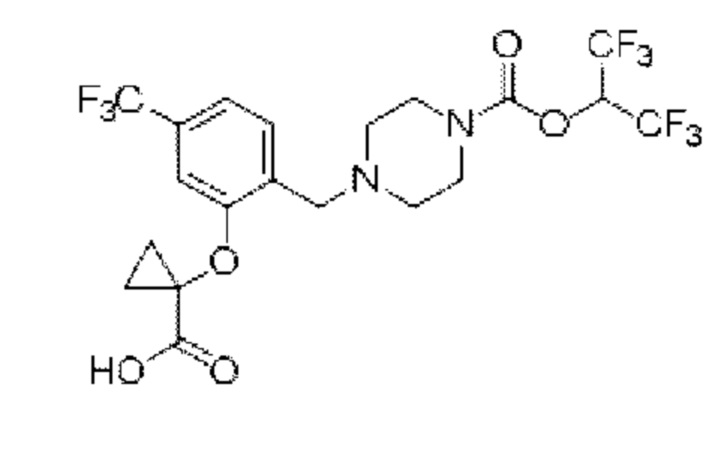
Стадия 1: Получение метил-1-(2-формил-5-(трифторметил)фенокси)циклопропан-1-карбоксилата
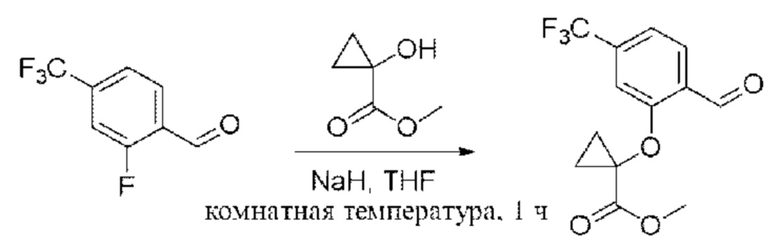
[00221] В колбу загружали метил-1-гидроксициклопропан-1-карбоксилат (362 мг, 3,12 ммоль, 1,50 экв.) и TGF (10 мл). Гидрид натрия (125 мг, 3,12 ммоль, 1,50 экв., 60% в минеральном масле) добавляли при температуре 0°С. Смесь перемешивали в течение 20 минут при комнатной температуре, после чего добавляли 2-фтор-4-(трифторметил)бензальдегид (400 мг, 2,08 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение 1 часа при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем, используя EtOAc/петролейный эфир (1/10), получая 180 мг (выход 29%) метил-1-(2-формил-5-(трифторметил)фенокси)циклопропан-1-карбоксилата в виде светло-желтого масла.
Стадия 2: Получение трет-бутил-4-(2-(1-(метоксикарбонил)циклопропокси)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
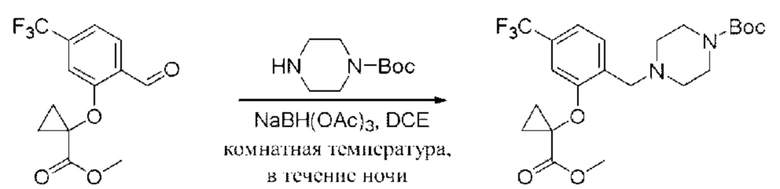
[00222] В колбу загружали метил-1-(2-формил-5-(трифторметил)фенокси)циклопропан-1-карбоксилат (200 мг, 0,690 ммоль, 1,00 экв.), DCE (10 мл) и трет-бутилпиперазин-1-карбоксилат (155 мг, 0,828 ммоль, 1,20 экв.). Смесь перемешивали в течение 1 часа при комнатной температуре и добавляли триацетоксиборгидрид натрия (441 мг, 2,07 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Остаток хроматографировали на колонке с силикагелем с помощью DCM/MeOH (97/3), получая 250 мг (выход 79%) трет-бутил-4-(2-(1-(метоксикарбонил)циклопропокси)-4-(трифторметил)бензил)пиперазин-1-карбоксилата в виде бесцветного масла. ЖХ/МС (ESI, m/z): 459 [М+Н]+.
Стадия 3: Получение 1-(2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты
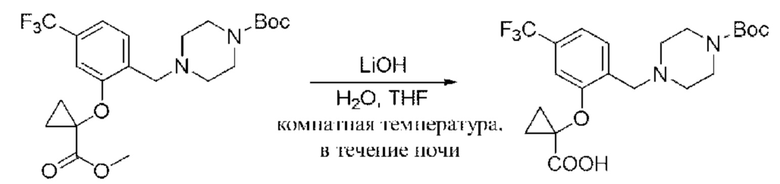
[00223] В колбу загружали трет-бутил-4-(2-(1-(метоксикарбонил)циклопропокси)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (200 мг, 0,440 ммоль, 1,00 экв.), THF (5 мл), воду (5 мл) и гидроксид лития (157 мг, 6,56 ммоль, 15,0 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре, а затем значение рН раствора доводили до 5 с помощью соляной кислоты (1 моль/л). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали, получая 190 мг (неочищенного) 1-(2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты в виде светло-желтого твердого вещества. ЖХ/МС (ESI, m/z): 445 [М+Н]+.
Стадия 4: Получение гидрохлорида 1-(2-(пиперазин-1-илметил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты
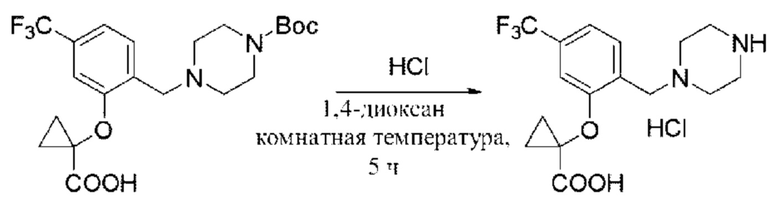
[00224] В колбу загружали 1-(2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновую кислоту (190 мг, 0,430 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и соляную кислоту (3 мл). Полученный раствор перемешивали в течение 5 часов при комнатной температуре и концентрировали, получая 140 мг (неочищенного) гидрохлорида 1-(2-(пиперазин-1-илметил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты в виде светло-желтого твердого вещества. ЖХ/МС (ESI, m/z): 345 [М+Н]+.
Стадия 5: Получение 1-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты
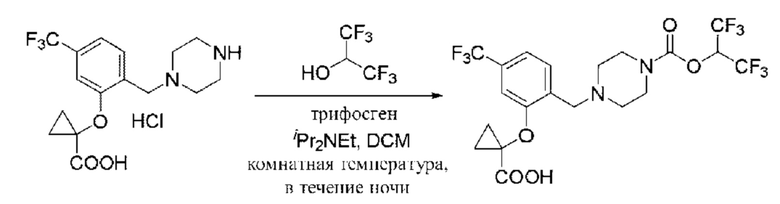
[00225] В колбу загружали трифосген (85,0 мг, 0,290 ммоль, 0,70 экв.), DCM (10 мл), 1,1,1,3,3,3-гексафторпропан-2-ол (137 мг, 0,820 ммоль, 2,00 экв.) в атмосфере азота. DIPEA (158 мг, 1,22 ммоль, 3,00 экв.) добавляли при температуре 0°С. Смесь перемешивали в течение 1 часа при комнатной температуре и добавляли гидрохлорид 1-(2-(пиперазин-1-илметил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты (140 мг, 0,410 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали. Неочищенный продукт (300 мг) очищали препаративной ВЭЖХ с получением 84,9 мг (выход 39%) 1-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-)ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты в виде белого твердого вещества. 1Н ЯМР (300 МГц, метанол-d4) δ 7,55 (д, J=7,8 Гц, 1Н), 7,41 (с, 1Н), 7,30 (д, J=7,8 Гц, 1Н), 6,10-6,19 (м, 1Н) 3,86 (с, 2Н), 3,65-3,66 (м, 4Н), 2,78 (уш. с., 4Н), 1,50-1,54 (м, 2Н), 1,16-1,20 (м, 2Н). ЖХ/МС (ESI, m/z): 539 [М+Н]+.
Пример 17: 2-(3-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)уксусная кислота
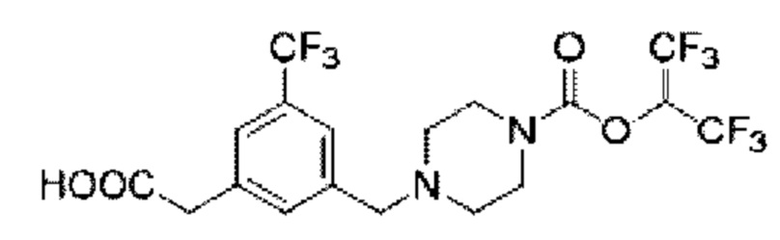
Стадия 1: Синтез трет-бутил-4-(3-бром-5-(трифторметил)бензил)пиперазин-1-карбоксилата
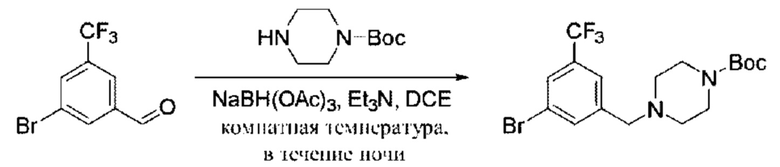
[00226] В колбу загружали 3-бром-5-(трифторметил)бензальдегид (2,53 г, 10,0 ммоль, 1,00 экв.), трет-бутилпиперазин-1-карбоксилат (2,23 г, 12,0 ммоль, 1,20 экв.), DCE (25 мл) и триэтиламин (3,03 г, 29,9 ммоль, 3,00 экв.). Смесь перемешивали в течение 30 минут при комнатной температуре до добавления триацетоксиборгидрида натрия (6,36 г, 30,0 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (25 мл), как описано в примере 1, стадия 5. Остаток хроматографировали на колонке с силикагелем, получая 1,90 г (выход 45%) трет-бутил-4-(3-бром-5-(трифторметил)бензил)пиперазин-1-карбоксилат. ЖХ/МС (ESI, m/z): 423 [М+Н]+.
Стадия 2: Синтез трет-бутил-4-(3-(2-(трет-бутокси)-2-оксоэтил)-5-(трифторметил)бензил)пиперазин-1-карбоксилата
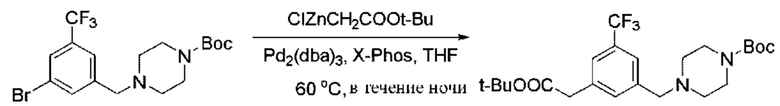
[00227] В колбу загружали трет-бутил-4-(3-бром-5-(трифторметил)бензил)пиперазин-1-карбоксилат (2,00 г, 4,73 ммоль, 1,00 экв.), (2-трет-бутокси-2-оксоэтил)цинка(II) хлорид (28,4 мл, 14,2 ммоль, 3,00 экв., 0,5 М в этиловом эфире), трис(дибензилиденацетон)дипалладий (433 мг, 0,473 ммоль, 0,10 экв.), 2-(дициклогексилфосфино)-2',4',6'-триизопропилбифенил (451 мг, 0,946 ммоль, 0,20 экв.) и THF (30 мл) в атмосфере азота. Полученный раствор перемешивали в течение ночи при температуре 60°С и гасили водой (30 мл). Полученный раствор экстрагировали DCM (3×30 мл), а органические слои объединяли, промывали рассолом (2×10 мл), сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 1,00 г (выход 46%) трет-бутил-4-(3-(2-(трет-бутокси)-2-оксоэтил)-5-(трифторметил)бензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 459 [М+Н]+.
Стадия 3: Синтез 2-(3-(пиперазин-1-илметил)-5-(трифторметил)фенил)уксусной кислоты
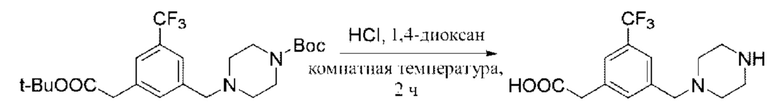
[00228] В колбу загружали трет-бутил-4-(3-(2-(трет-бутокси)-2-оксоэтил)-5-(трифторметил)бензил)пиперазин-1-карбоксилат (200 мг, 0,436 ммоль, 1,00 экв.), 1,4-диоксан (4 мл) и концентрированный хлористый водород (1 мл). Полученный раствор перемешивали в течение 2 ч при комнатной температуре и концентрировали при пониженном давлении, как описано в примере 3, стадия 4, чтобы получить 180 мг (неочищенной) 2-(3-(пиперазин-1-илметил)-5-(трифторметил)фенил)уксусной кислоты. ЖХ/МС (ESI, m/z): 303 [М+Н]+.
Стадия 4: Синтез 2-(3-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)уксусной кислоты
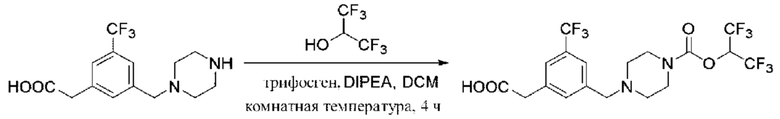
[00229] В колбу загружали трифосген (63,9 мг, 0,215 ммоль, 0,50 экв.), DCM (5 мл) и 1,1,1,3,3,3-гексафторпропан-2-ол (145 мг, 0,861 ммоль, 2,00 экв.). DIPEA (222 мг, 1,72 ммоль, 4,00 экв.) добавляли по каплям при температуре 0°С, и смесь перемешивали в течение 2 часов при комнатной температуре. Добавляли 2-(3-(пиперазин-1-илметил)-5-(трифторметил)фенил)уксусную кислоту (130 мг, 0,430 ммоль, 1,00 экв.) и полученный раствор перемешивали в течение 2 ч при комнатной температуре, а затем гасили насыщенным раствором бикарбоната натрия (20 мл), как описано в примере 1, стадия 1. Неочищенный продукт (200 мг) очищали препаративной ВЭЖХ с получением 54,9 мг (26% выход) 2-(3-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)уксусной кислоты. 1Н ЯМР (300 МГц, метанол-d4) δ 7,58-7,53 (м, 3Н), 6,18-6,08 (м, 1Н), 3,72 (уш. с., 2Н), 3,64-3,56 (м, 6Н), 2,52-2,51 (м, 4Н). ЖХ/МС (ESI, m/z): 497 [М+Н]+.
Пример 18: 4-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)-2,2-диметилбут-3-иновая кислота
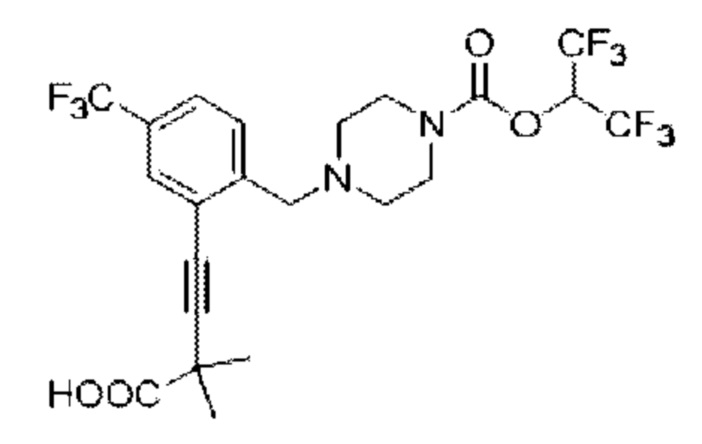
Стадия 1: Синтез трет-бутил-4-(2-йод-4-(трифторметил)бензил)пиперазин-1-карбоксилата
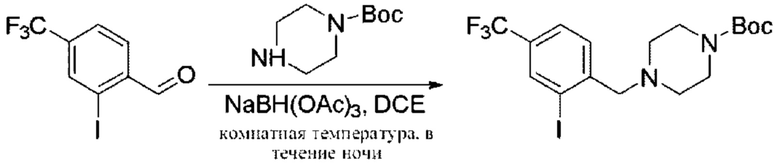
[00230] В колбу загружали 2-йод-4-(трифторметил)бензальдегид (1,00 г, 3,33 ммоль, 1,00 экв.), трет-бутилпиперазин-1-карбоксилат (0,744 г, 3,99 ммоль, 1,20 экв.) и DCE (15 мл). Смесь перемешивали в течение 1 часа при комнатной температуре до добавления триацетоксиборгидрида натрия (2,12 г, 10,0 ммоль, 3,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (20 мл), как описано в примере 15, стадия 1. Остаток хроматографировали на колонке с силикагелем, получая 1,39 г (выход 89%) трет-бутил-4-(2-йод-4-(трифторметил)бензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 471 [М+Н]+.
Стадия 2: Синтез трет-бутил-4-(2-(4-этокси-3,3-диметил-4-оксобут-1-ин-1-ил)-4-(трифторметил)бензил)пиперазин-1-карбоксилата
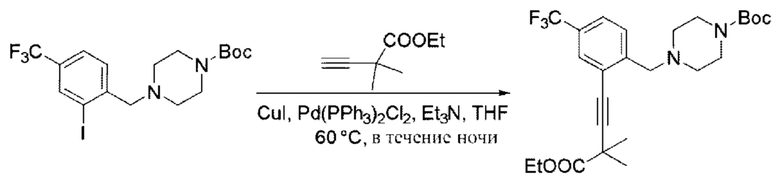
[00231] В колбу загружали трет-бутил-4-(2-йод-4-(трифторметил)бензил)пиперазин-1-карбоксилат (400 мг, 0,851 ммоль, 1,00 экв.), этил 2,2-диметилбут-3-иноат (238 мг, 1,70 ммоль, 2,00 экв.), хлорид бис(трифенилфосфин)палладия(II) (59,6 мг, 0,0851 ммоль, 0,10 экв.), йодид меди(I) (32,3 мг, 0,170 ммоль, 0,20 экв.), триэтиламин (258 мг, 2,55 ммоль, 3,00 экв.) и THF (10 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 60°С и гасили водой (15 мл). Полученный раствор экстрагировали DCM (3×20 мл), а органические слои объединяли, промывали рассолом (1×50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 320 мг (выход 78%) трет-бутил-4-(2-(4-этокси-3,3-диметил-4-оксобут-1-ин-1-ил)-4-(трифторметил)бензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 483 [М+Н]+.
Стадия 3: Синтез 4-(2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)-2,2-диметилбут-3-иновой кислоты
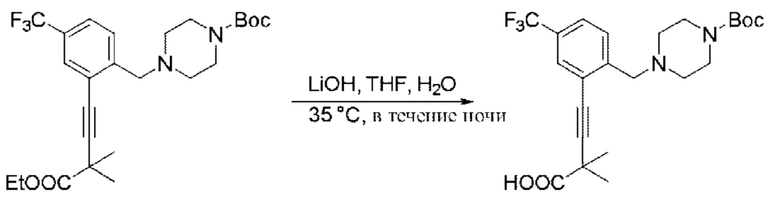
[00232] В колбу загружали трет-бутил-4-(2-(4-этокси-3,3-диметил-4-оксобут-1-ин-1-ил)-4-(трифторметил)бензил)пиперазин-1-карбоксилат (320 мг, 0,660 ммоль, 1,00 экв.), THF (10 мл), гидроксид лития (313 мг, 13,1 ммоль, 20,00 экв.) и воду (2 мл). Полученный раствор перемешивали в течение ночи при температуре 35°С и гасили водой (10 мл). Значение рН раствора доводили до 6 соляной кислотой (1 М), как описано в примере 16, стадия 3, чтобы получить 280 мг (выход 93%) 4-(2-((4-(трет-бутоксикарбонил)пиперазин)-1-ил)метил)-5-(трифторметил)фенил)-2,2-диметилбут-3-иновой кислоты. ЖХ/МС (ESI, m/z): 455 [М+Н]+.
Стадия 4: Синтез 2,2-диметил-4-(2-(пиперазин-1-илметил)-5-(трифторметил)фенил)бут-3-иновой кислоты

[00233] В колбу загружали 4-(2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)-2,2-диметилбут-3-иновую кислоту (280 мг, 0,620 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и концентрированную соляную кислоту (2 мл). Полученный раствор перемешивали в течение 2 ч при комнатной температуре и концентрировали при пониженном давлении, получая 300 мг (неочищенной) 2,2-диметил-4-(2-(пиперазин-1-илметил)-5-(трифторметил)фенил)бут-3-иновой кислоты в виде желтого твердого вещества. ЖХ/МС (ESI, m/z): 355 [М+Н]+.
Стадия 5: Синтез 4-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)-2,2-диметилбут-3-иновой кислоты
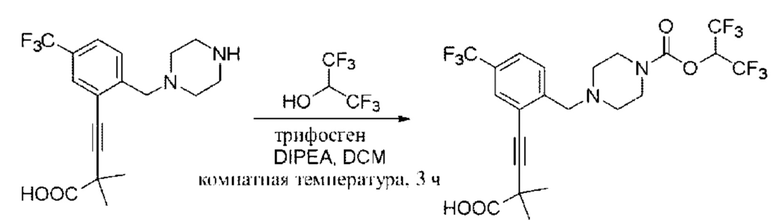
[00234] В колбу загружали трифосген (117 мг, 0,390 ммоль, 0,70 экв.), DCM (10 мл). 1,1,1,3,3,3-гексафторпропан-2-ол (190 мг, 1,13 ммоль, 2,00 экв.) добавляли при температуре 0°С. N,N-DIPEA (292 мг, 2,26 ммоль, 4,00 экв.) добавляли при температуре 0°С. Смесь перемешивали в течение 2 ч при температуре 0°С. Добавляли 2,2-диметил-4-(2-(пиперазин-1-илметил)-5-(трифторметил)фенил)бут-3-иновую кислоту (200 мг, 0,560 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение 1 часа при комнатной температуре и гасили водой (10 мл), как описано в примере 1, стадия 1. Неочищенный продукт (400 мг) очищали препаративной ВЭЖХ с получением 21,1 мг (выход 7%) 4-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенил)-2,2-диметилбут-3-иновой кислоты. 1Н ЯМР (400 МГц, метанол-d4) 7,69-7,68 (м, 2Н), 7,63-7,61 (м, 1H), 6,19-6,13 (м, 1H), 3,84 (с, 2Н), 3,63-3,60 (м, 4Н), 2,63-2,59 (м, 4Н), 1,60 (с, 6Н). ЖХ/МС (ESI, m/z): 549 [М+Н]+.
Пример 19: 1-(3-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновая кислота
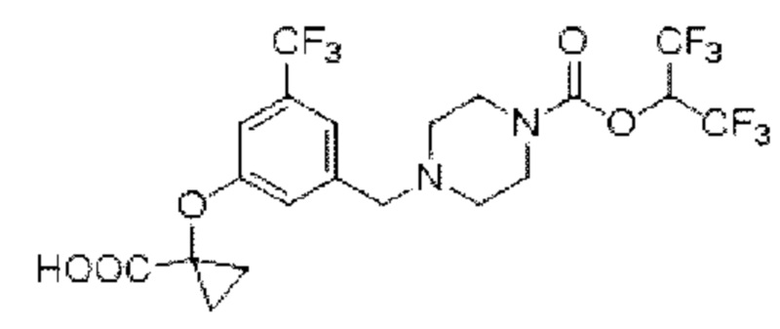
Стадия 1: Синтез трет-бутил-4-(3-гидрокси-5-(трифторметил)бензил)пиперазин-1-карбоксилата
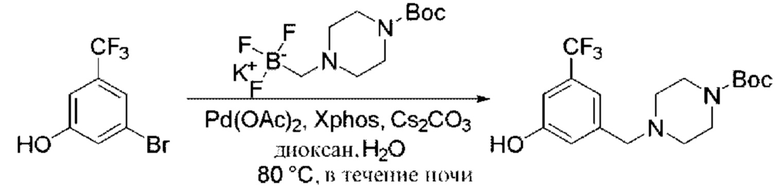
[00235] В колбу загружали 3-бром-5-(трифторметил)фенол (400 мг, 1,66 ммоль, 1,00 экв.), ацетат палладия (18,6 мг, 0,0830 ммоль, 0,05 экв.), 2-(дициклогексилфосфино)-2',4',6'-триизопропилбифенил (79,2 мг, 0,166 ммоль, 0,10 экв.), карбонат цезия (1,62 г, 4,98 ммоль, 3,00 экв.), калий (4-[(трет-бутокси)карбонил]пиперазин-1-илметил)трифторборгидрид (765 мг, 2,50 ммоль, 1,50 экв.), диоксан (10 мл) и воду (2 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 80°С и гасили водой (10 мл). Полученный раствор экстрагировали DCM (3×20 мл), а органические слои объединяли, промывали рассолом (1×20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 580 мг (выход 97%) трет-бутил-4-(3-гидрокси-5-(трифторметил)бензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 361 [М+Н]+.
Стадия 2: Синтез трет-бутил-4-(3-((4-бром-1-метокси-1-оксобутан-2-ил)окси)-5-(трифторметил)бензил)пиперазин-1-карбоксилата
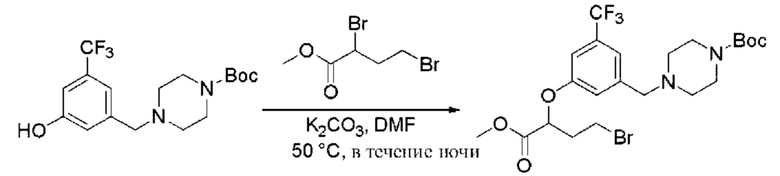
[00236] В колбу загружали трет-бутил-4-(3-гидрокси-5-(трифторметил)бензил)пиперазин-1-карбоксилат (500 мг, 1,39 ммоль, 1,00 экв.), метил-4-бром-2-оксобутаноат (723 мг, 2,78 ммоль, 2,00 экв.), карбонат калия (384 мг, 2,78 ммоль, 2,00 экв.) и DMF (10 мл) в атмосфере азота. Полученный раствор перемешивали в течение ночи при температуре 50°С и гасили водой (10 мл), как описано в примере 3, стадия 4. Остаток хроматографировали на колонке с силикагелем, получая 500 мг (выход 67%) трет-бутил-4-(3-((4-бром-1-метокси-1-оксобутан-2-ил)окси)-5-(трифторметил)бензил)пиперазин-1-карбоксилат. ЖХ/МС (ESI, m/z): 539 [М+Н]+.
Стадия 3: Синтез 1-(3-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты
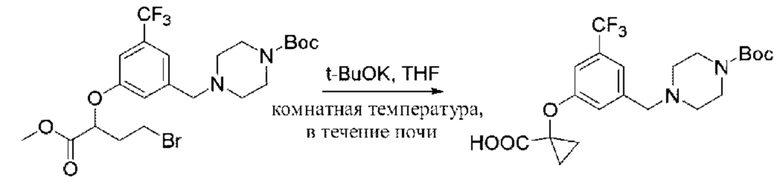
[00237] В колбу загружали трет-бутил-4-(3-((4-бром-1-метокси-1-оксобутан-2-ил)окси)-5-(трифторметил)бензил)пиперазин-1-карбоксилат (500 мг, 0,930 ммоль, 1,00 экв.), трет-бутоксид, калия (208 мг, 1,86 ммоль, 2,00 экв.) и THF (5 мл). Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили водой (10 мл). Полученный раствор экстрагировали DCM (3×30 мл), а органические слои объединяли, промывали рассолом (1×20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 150 мг (выход 36%) 1-(3-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты. ЖХ/МС (ESI, m/z): 445 [М+Н]+.
Стадия 4: Синтез 1-(3-(пиперазин-1-илметил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты
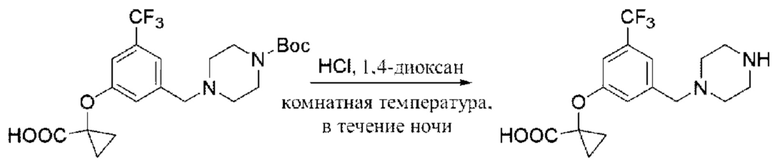
[00238] В колбу загружали 1-(3-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновую кислоту (100 мг, 0,220 ммоль, 1,00 экв.), концентрированную хлористоводородную кислоту (1 мл) и 1,4-диоксан (4 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре и концентрировали при пониженном давлении, чтобы получить 110 мг (неочищенной) 1-(3-(пиперазин-1-илметил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты. ЖХ/МС (ESI, m/z): 345 [М+Н]+.
Стадия 5: Синтез 1-(3-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты
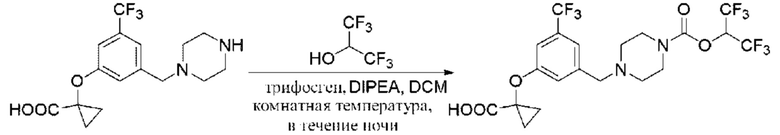
[00239] В колбу загружали трифосген (42,2 мг, 0,142 ммоль, 0,70 экв.) и DCM (5 мл). 1,1,1,3,3,3-гексафторпропан-2-ол (68,2 мг, 0,406 ммоль, 2,00 экв.) добавляли при температуре 0°C с последующим добавлением DIPEA (105 мг, 0,812 ммоль, 4,00 экв.). Смесь перемешивали в течение 2 ч при комнатной температуре перед добавлением 1-(3-(пиперазин-1-илметил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты (70,0 мг, 0,203 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и гасили водой (10 мл), как описано в примере 1, стадия 1. Неочищенный продукт (400 мг) очищали препаративной ВЭЖХ с получением 7,40 мг (выход 7%) 1-(3-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-5-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты. 1Н ЯМР (300 МГц, метанол-d4) δ 7,26 (с, 2Н), 7,08 (с, 1Н), 6,19-6,10 (м, 1H), 3,67-3,59 (м, 6Н), 2,55 (уш. с., 4Н) 1,65-1,61 (м, 2Н), 1,33-1,28 (м, 2Н). ЖХ/МС (ESI, m/z): 539 [М+Н]+.
Пример 20: 1,1,1,3,3,3-гексафторпропан-2-ил-4-(3-фтор-4-метил-2-(2-(метилсульфонамидо)-2-оксоэтокси)бензил)пиперазин-1-карбоксилат
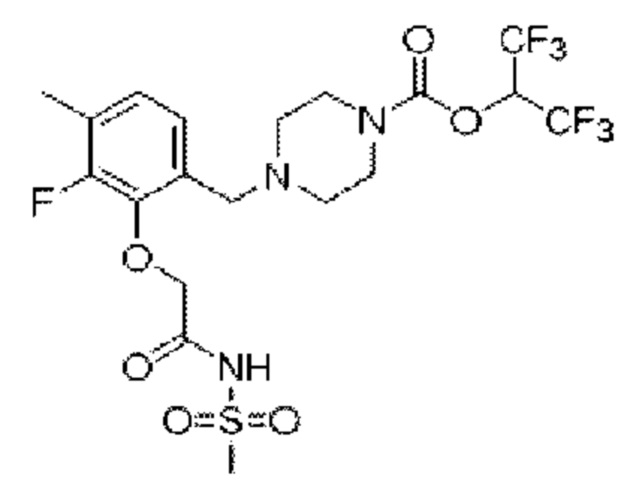
Стадия 1: Синтез трет-бутил-2-(6-бром-2-фтор-3-метилфенокси)ацетата
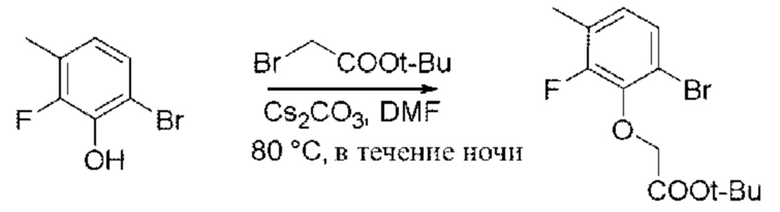
[00240] В колбу загружали 6-бром-2-фтор-3-метилфенол (1,00 г, 4,90 ммоль, 1,00 экв.), DMF (10 мл), карбонат цезия (4,79 г, 14,7 ммоль, 3,00 экв.) и трети-бутил-2-бромацетат (1,43 г, 7,35 ммоль, 1,50 экв.). Реакционную смесь перемешивали в течение ночи при температуре 80°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 0,950 г (выход 61%) трет-бутил-2-(6-бром-2-фтор-3-метилфенокси)ацетата. ЖХ/МС (ESI, m/z): 319 [М+Н]+.
Стадия 2. Синтез трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат
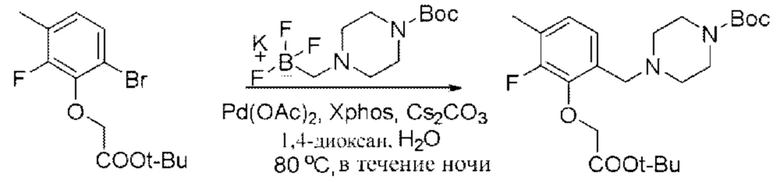
[00241] В колбу загружали трет-бутил-2-(6-бром-2-фтор-3-метилфенокси)ацетат (900 мг, 2,82 ммоль, 1,00 экв.), 1,4-диоксан (10 мл), воду (2 мл), калия ((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)трифторборат (1004 мг, 3,38 ммоль, 1,20 экв.), ацетат палладия (21,0 мг, 0,0850 ммоль, 0,03 экв.), 2-(дициклогексилфосфино)-2',4',6'-триизопропилбифенил (81,0 мг, 0,170 ммоль, 0,06 экв.) и карбонат цезия (2770 мг, 8,50 ммоль, 3,00 экв.) в атмосфере азота. Полученный раствор перемешивали в течение ночи при температуре 80°С и гасили водой (30 мл), как описано в примере 19, стадия 1. Остаток хроматографировали на колонке с силикагелем, получая 1,00 г (выход 81%) трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат. ЖХ/МС (ESI, m/z): 439 [М+Н]+.
Стадия 3: Синтез 2-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенокси)уксусной кислоты

[00242] В колбу загружали трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат (650 мг, 1,48 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и концентрированную соляную кислоту (2 мл), как описано в примере 3, стадия 4. Полученный раствор перемешивали в течение 2 ч при комнатной температуре и концентрировали при пониженном давлении с получением 417 мг (количественно) 2-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенокси)уксусной кислоты. ЖХ/МС (ESI, m/z): 283 [М+Н]+.
Стадия 4: Синтез 2-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)уксусной кислоты
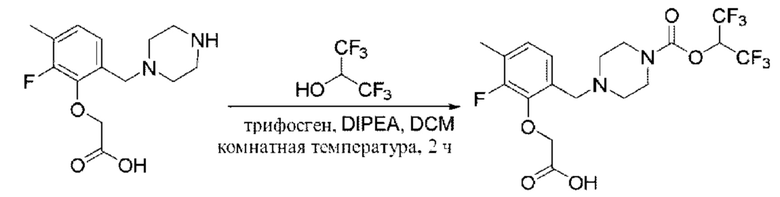
[00243] В колбу загружали трифосген (220 мг, 0,740 ммоль, 0,50 экв.), DCM (10 мл) и 1,1,1,3,3,3-гексафторпропан-2-ол (497 мг, 2,96 ммоль, 2,00 экв.). DIPEA (573 мг, 4,43 ммоль, 3,00 экв.) добавляли при температуре 0°С. Смесь перемешивали в течение 1 часа при комнатной температуре перед добавлением 2-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенокси)уксусной кислоты (417 мг, 1,48 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение 2 ч при комнатной температуре и гасили насыщенным раствором NaHCO3 (30 мл) в атмосфере азота, как описано в примере 1, стадия 1. Неочищенный продукт (300 мг) очищали препаративной ВЭЖХ с получением 400 мг (выход 57%) 2-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)уксусной кислоты. 1Н ЯМР (400 МГц, хлороформ-d) δ 6,89 (д, J=7,2 Гц, 1H), 6,83 (д, J=7,6 Гц, 1H), 5,79-5,73 (м, 1H), 4,92 (с, 2Н) 3,82 (уш. с., 4Н), 3,73 (с, 2Н), 2,78 (уш. с., 4Н), 2,31 (с, 3Н). ЖХ/МС (ESI, m/z): 477 [М+Н]+.
Стадия 5: Синтез 1,1,1,3,3,3-гексафторпропан-2-ил-4-(3-фтор-4-метил-2-(2-(метилсульфонамидо)-2-оксоэтокси)бензил)пиперазин-1-карбоксилата
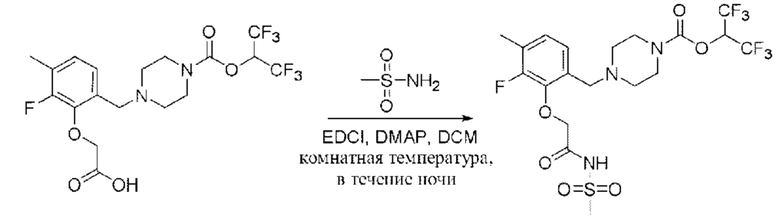
[00244] В колбу загружали 2-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)уксусную кислоту (300 мг, 0,630 ммоль, 1,00 экв.), DCM (10 мл), DMAP (230 мг, 1,89 ммоль, 3,00 экв.), метансульфонамид (180 мг, 1,89 ммоль, 3,00 экв.) и N-(3-диметиламинопропил)-N'-этилкарбодиимида гидрохлорид (242 мг, 1,26 ммоль, 2,00 экв.). Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт (400 мг) очищали препаративной ВЭЖХ с получением 17,3 мг (5% выход) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(3-фтор-4-метил-2-(2-(метилсульфонамидо)-2-оксоэтокси)бензил)пиперазин-1-карбоксилата. 1H ЯМР (300 МГц, хлороформ-d) δ 6,95-6,85 (м, 2Н), 5,75-5,71 (м, 1H), 4,76 (с, 2Н), 3,76-3,72 (м, 6Н), 3,31 (с, 3Н) 2,75 (уш. с., 4Н), 2,29 (с, 3Н). ЖХ/МС (ESI, m/z): 554 [М+Н]+.
Пример 21: 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(2-(циклопропансульфонамидо)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат
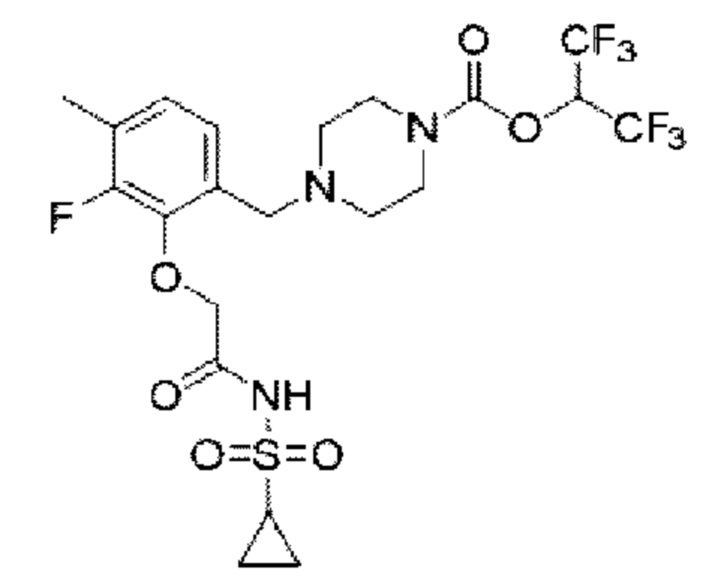
Стадия 1: Синтез трет-бутил-2-(6-бром-2-фтор-3-метилфенокси)ацетата
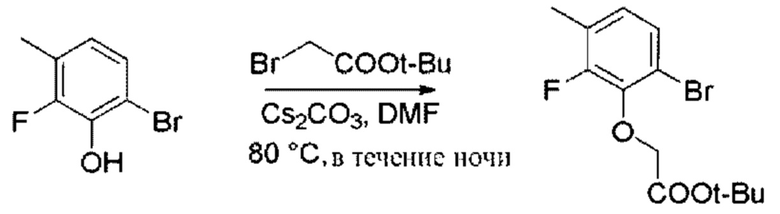
[00245] В колбу загружали 6-бром-2-фтор-3-метилфенол (1,00 г, 4,90 ммоль, 1,00 экв.), DMF (10 мл), карбонат цезия (4,79 г, 14,7 ммоль, 3,00 экв.) и трет-бутил-2-бромацетат (1,43 г, 7,35 ммоль, 1,50 экв.). Полученный раствор перемешивали в течение ночи при температуре 80°С и гасили водой (30 мл), как описано в примере 3, стадия 4. Остаток хроматографировали на колонке с силикагелем, получая 0,950 г (выход 61%) трет-бутил-2-(6-бром-2-фтор-3-метилфенокси)ацетата. ЖХ/МС (ESI, m/z): 319 [М+Н]+.
Стадия 2: Синтез трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат
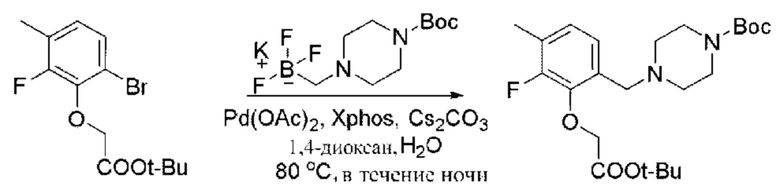
[00246] В колбу загружали трет-бутил-2-(6-бром-2-фтор-3-метилфенокси)ацетат (900 мг, 2,82 ммоль, 1,00 экв.), 1,4-диоксан (10 мл), воду (2 мл), калия ((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)трифторборат (1004 мг, 3,38 ммоль, 1,20 экв.), ацетат палладия (21,0 мг, 0,0850 ммоль, 0,03 экв.), 2-(дициклогексилфосфино)-2',4',6'-триизопропилбифенил (81,0 мг, 0,170 ммоль, 0,06 экв.) и карбонат цезия (2770 мг, 8,50 ммоль, 3,00 экв.) в атмосфере азота. Полученный раствор перемешивали в течение ночи при температуре 80°С и гасили водой (30 мл), как описано в примере 19, стадия 1. Остаток хроматографировали на колонке с силикагелем, получая 1,00 г (выход 81%) трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 439 [М+Н]+.
Стадия 3: Синтез 2-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенокси)уксусной кислоты

[00247] В колбу загружали трет-бутил-4-(2-(2-(трет-бутокси)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат (650 мг, 1,48 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и концентрированную соляную кислоту (2 мл). Полученный раствор перемешивали в течение 2 ч при комнатной температуре и концентрировали при пониженном давлении, как описано в примере 3, стадия 4, чтобы получить 417 мг (количественно) 2-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенокси)уксусной кислоты. ЖХ/МС (ESI, m/z): 283 [М+Н]+
Стадия 4: Синтез 2-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)уксусной кислоты
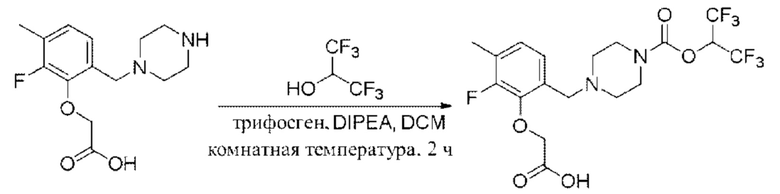
[00248] В колбу загружали трифосген (220 мг, 0,740 ммоль, 0,50 экв.), DCM (10 мл) и 1,1,1,3,3,3-гексафторпропан-2-ол (497 мг, 2,96 ммоль, 2,00 экв.). DIPEA (573 мг, 4,43 ммоль, 3,00 экв.) добавляли при температуре 0°С. Смесь перемешивали в течение 1 часа при комнатной температуре перед добавлением 2-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенокси)уксусной кислоты (417 мг, 1,48 ммоль, 1,00 экв.). Полученный раствор перемешивали в течение 2 ч при комнатной температуре и гасили насыщенным раствором NaHCO3 (30 мл) в атмосфере азота, как описано в примере 1, стадия 1. Неочищенный продукт (300 мг) очищали препаративной ВЭЖХ с получением 400 мг (выход 57%) 2-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)уксусной кислоты. 1Н ЯМР (400 МГц, хлороформ-d) δ 6,89 (д, J=7,2 Гц, 1Н), 6,83 (д, J=7,6 Гц, 1Н), 5,79-5,73 (м, 1Н), 4,92 (с, 2Н) 3,82 (уш. с., 4Н), 3,73 (с, 2Н), 2,78 (уш. с., 4Н), 2,31 (с, 3Н). ЖХ/МС (ESI, m/z): 477 [М+Н]+.
Стадия 5: Синтез 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(2-хлор-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат
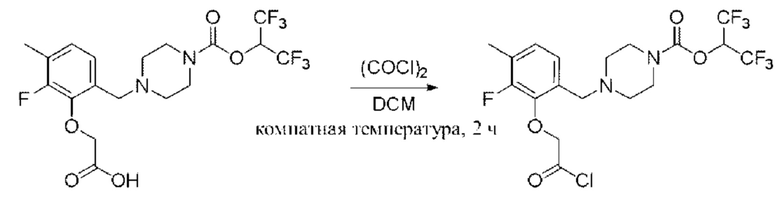
[00249] В колбу загружали 2-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)уксусную кислоту (300 мг, 0,630 ммоль, 1,00 экв.) и DCM (10 мл). Оксалилдихлорид (234 мг, 1,86 ммоль, 3,00 экв.) добавляли при температуре 0°С. Полученный раствор перемешивали в течение 2 ч при комнатной температуре и концентрировали при пониженном давлении, получая 311 мг (неочищенного) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(2-хлор-)2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилата.
Стадия 6: Синтез 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(2-(циклопропансульфонамидо)-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилата
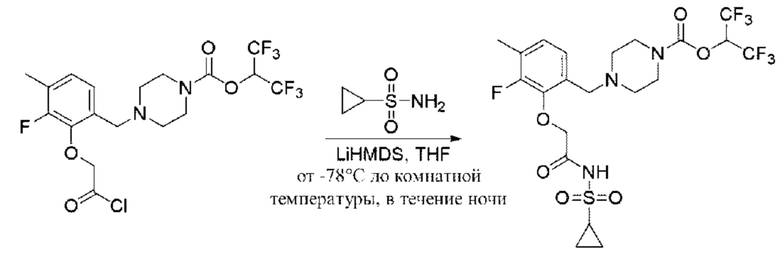
[00250] В колбу загружали циклопропансульфонамид (229 мг, 1,89 ммоль, 3,00 экв.) и THF (10 мл) в атмосфере азота. Смесь охлаждали до температуры -78°С и по каплям добавляли бис(триметилсилил)амид лития (2,52 мл, 2,52 ммоль, 4,00 экв., 1 M в тетрагидрофуране) при температуре -78°С. Смесь перемешивали в течение 30 мин при температуре -78°С до добавления по каплям 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(2-хлор-2-оксоэтокси)-3-фтор-4-метил бензил)пиперазин-1-карбоксилата (311 мг, 0,630 ммоль, 1,00 экв.) в течение 10 минут при температуре -78°С. Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили насыщенным раствором NH4Cl (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт (200 мг) очищали препаративной ВЭЖХ с получением 77,6 мг (выход 21%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(2-(циклопропансульфонамидо))-2-оксоэтокси)-3-фтор-4-метилбензил)пиперазин-1-карбоксилата. 1Н ЯМР (300 МГц, Хлороформ-d) δ 6,94-6,84 (м, 2Н), 5,78-5,69 (м, 1H), 4,72 (с, 2Н), 3,61 (уш. с., 6Н), 3,02-2,96 (м, 1H), 2,56-2,55 (м, 4Н), 2,28 (с, 3Н), 1,39-1,38 (м, 2Н), 1,17-1,10 (м, 2Н). ЖХ/МС (ESI, m/z): 580 [М+Н]+.
Пример 22: 1-(2-((4-(((1,1,1,3,3,3-Гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-6-(трифторметил)фенокси)циклопропан-1-карбоновая кислота
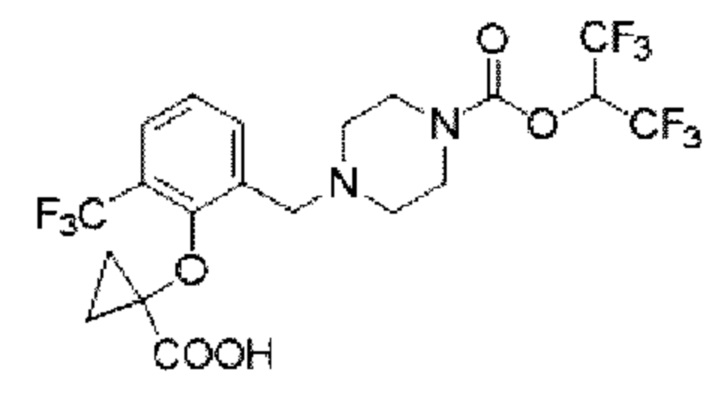
Стадия 1: Синтез трет-бутил-4-бром-2-(2-бром-6-(трифторметил)фенокси)бутаноата
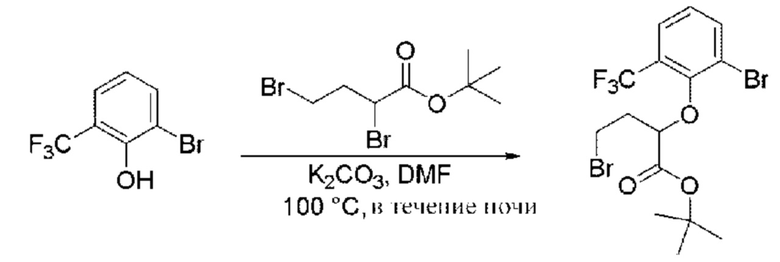
[00251] В круглодонную колбу загружали 2-бром-6-(трифторметил)фенол (0,500 г, 2,07 ммоль, 1,00 экв.), трет-бутил-2,4-дибромбутаноат (1,25 г, 4,14 ммоль, 2,00 экв.), карбонат калия (0,857 г, 6,21 ммоль, 3,00 экв.) и DMF (15 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 100°С и гасили водой (10 мл). Полученный раствор экстрагировали EtOAc (3×20 мл), а органические слои объединяли, промывали рассолом (20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 0,200 г (выход 21%) трет-бутил-4-бром-2-(2-бром-6-(трифторметил)фенокси)бутаноата. ЖХ/МС (ESI, m/z): 461 [М+Н]+.
Стадия 2: Синтез трет-бутил-1-(2-бром-6-(трифторметил)фенокси)циклопропан-1-карбоксилата
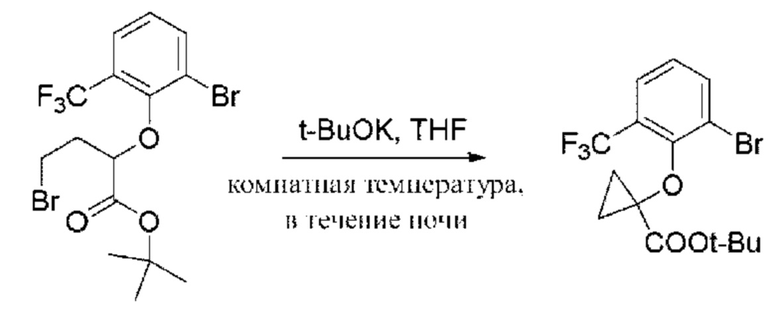
[00252] В круглодонную колбу загружали трет-бутил-4-бром-2-(2-бром-6-(трифторметил)фенокси)бутаноат (1,50 г, 3,26 ммоль, 1,00 экв.), трет-бутоксид калия (0,730 г, 6,52 ммоль, 2,00 экв.) и THF (20 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (3×40 мл), а органические слои объединяли, промывали рассолом (40 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 0,600 г (выход 49%) трет-бутил-1-(2-бром-6-(трифторметил)фенокси)циклопропан-1-карбоксилата. ЖХ/МС (ESI, m/z): 381 [М+Н]-.
Стадия 3: Синтез трифтор((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)бората калия
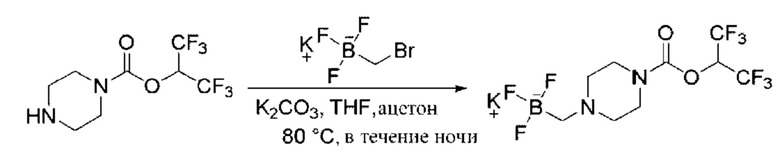
[00253] В круглодонную колбу загружали 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат (7,30 г, 26,1 ммоль, 1,00 экв., пример 1, стадия 2), (бромметил)трифторборанид калия (5,30 г, 26,1 ммоль, 1,00 экв.) и THE (120 мл) в атмосфере азота. Смесь перемешивали в течение ночи при температуре 80°С и концентрировали при пониженном давлении. Добавляли карбонат калия (3,56 г, 26,1 ммоль, 1,00 экв.) и ацетон (150 мл), и полученный раствор перемешивали в течение 2 ч при комнатной температуре до разбавления ацетоном (400 мл). Смесь фильтровали и фильтрат концентрировали при пониженном давлении с получением 10,1 г (выход 97%) трифтор-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси))карбонил)пиперазин-1-ил)метил)бората калия. 1Н ЯМР (300 МГц, хлороформ-d) δ 6,56-6,45 (м, 1Н), 3,38-3,33 (м, 4Н), 2,28-2,22 (м, 4Н), 1,28-1,22 (м, 2Н). ЖХ/МС (ESI, m/z): 361 [М-К]-.
Стадия 4: Синтез 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(1-трет-бутоксикарбонил)циклопропокси)-3-(трифторметил)бензил)пиперазин-1-карбоксилата
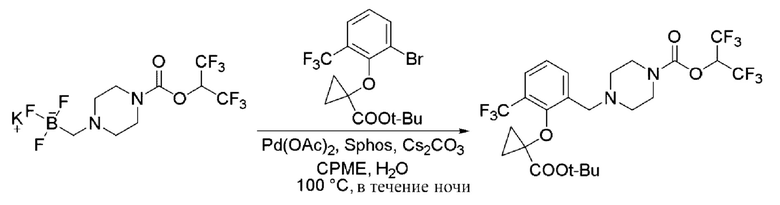
[00254] В круглодонную колбу загружали трет-бутил-1-(2-бром-6-(трифторметил)фенокси)циклопропан-1-карбоксилат (500 мг, 1,31 ммоль, 1,00 экв.), трифтор((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)борат калия (632 мг, 1,58 ммоль, 1,20 экв.), ацетат палладия (20,2 мг, 0,0660 ммоль, 0,05 экв.), 2-дициклогексилфосфино-2',6'-диметоксибифенил (54,3 мг, 0,132 ммоль, 0,10 экв.), карбонат цезия (1,28 г, 3,93 ммоль, 3,00 экв.), циклопентилметиловый эфир (10 мл) и воду (2 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 100°С и гасили водой (10 мл). Полученный раствор экстрагировали дихлорметаном (3×20 мл), а органические слои объединяли, промывали рассолом (20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 90,0 мг (выход 12%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(1-(трет-бутоксикарбонил)циклопропокси)-3-(трифторметил)бензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 595 [М+Н]+.
Стадия 5: Синтез 1-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-6-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты

[00255] В круглодонную колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(1-(трет-бутоксикарбонил)циклопропокси)-3-(трифторметил)бензилпиперазин-1-карбоксилат (90,0 мг, 0,150 ммоль, 1,00 экв.), 1,4-диоксан (5 мл) и концентрированную соляную кислоту (2 мл). Полученный раствор перемешивали в течение 2 часов при комнатной температуре и концентрировали при пониженном давлении. Неочищенный продукт растворяли в насыщенном растворе NaHCO3 (10 мл) и экстрагировали DCM (3×20 мл). Органические слои объединяли, промывали рассолом (30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт (78 мг) очищали препаративной ВЭЖХ с получением 4,7 мг (выход 6%) 1-(2-((4-(((1,1,1,3,3,3-гексафторпропан-2-)ил)окси)карбонил)пиперазин-1-ил)метил)-6-(трифторметил)фенокси)циклопропан-1-карбоновой кислоты. 1H ЯМР (400 МГц, метанол-d4) δ 7,88 (д, J=7,6 Гц, 1Н), 7,50 (д, J=7,6 Гц, 1Н), 7,21 (т, J=7,6 Гц, 1Н), 6,31-6,11 (м, 1Н), 3,82 (с, 2Н), 3,61-3,50 (м, 4Н), 2,62-2,45 (м, 4Н), 1,38 (уш. с., 2Н), 0,98-0,94 (м, 2Н). ЖХ/МС (ESI, m/z): 539 [М+Н]+.
Пример 23: 1-((2-Хлор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)метил)циклопропан-1-карбоновая кислота
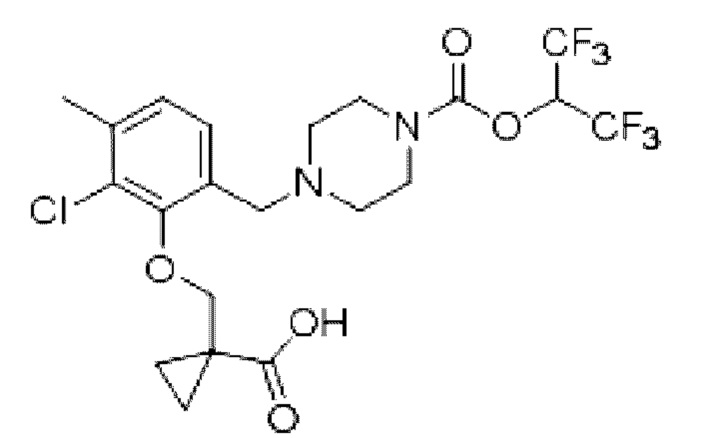
Стадия 1: Синтез этил-1-(((метилсульфонил)окси)метил)циклопропан-1-карбоксилата
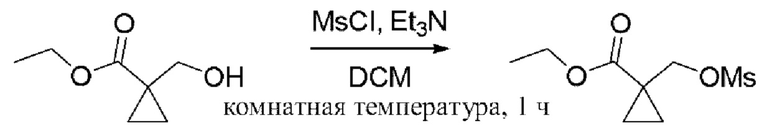
[00256] В круглодонную колбу объемом 100 мл загружали этил-1-(гидроксиметил)циклопропан-1-карбоксилат (1,91 г, 13,3 ммоль, 1,00 экв.), TEA (4,03 г, 39,9 ммоль, 3,00 экв.) и DCM. (40 мл). Метансульфонилхлорид (2,27 г, 20,0 ммоль, 1,50 экв.) добавляли при температуре 0°С и реакционную смесь перемешивали в течение 1 часа при комнатной температуре, а затем гасили насыщенным NH4Cl (30 мл). Полученный раствор экстрагировали дихлорметаном (2×50 мл), а органические слои объединяли, промывали насыщенным NaHCO3 (30 мл) и рассолом (30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении, получая 2,83 г (неочищенного) этил-1-(((метилсульфонил)окси)метил)циклопропан-1-карбоксилата.
Стадия 2: Синтез этил-1-((6-бром-2-хлор-3-метилфенокси)метил)циклопропан-1-карбоксилата
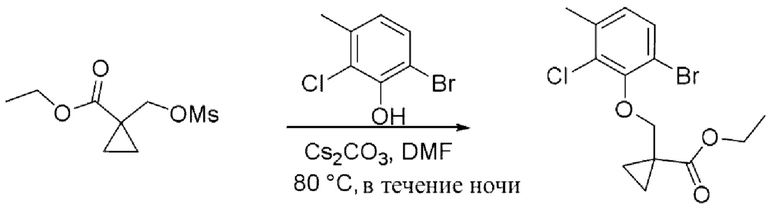
[00257] В круглодонную колбу загружали 6-бром-2-хлор-3-метилфенол (0,900 г, 4,09 ммоль, 1,00 экв.), этил-1-(((метилсульфонил)окси)метил)циклопропан-1-карбоксилат (1,36 г, 6,14 ммоль, 1,50 экв.), карбонат цезия (4,00 г, 12,3 ммоль, 3,00 экв.) и DMF (20 мл). Реакционную смесь перемешивали в течение ночи при температуре 80°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 1,18 г (выход 84%) этил-1-((6-бром-2-хлор-3-метилфенокси)метил)циклопропан-1-карбоксилата. ЖХ/МС (ESI, m/z): 347 [М+Н]+.
Стадия 3: Синтез трет-бутил-4-(3-хлор-2-((1-(этоксикарбонил)циклопропил)метокси)-4-метилбензил)пиперазин-1-карбоксилата
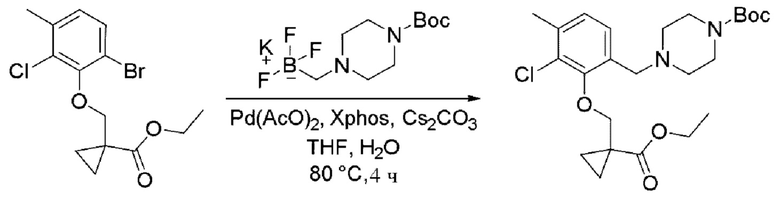
[00258] В круглодонную колбу загружали этил-1-((6-бром-2-хлор-3-метилфенокси)метил)циклопропан-1-карбоксилат (700 мг, 2,02 ммоль, 1,00 экв.), ацетат палладия (90,0 мг, 0,202 ммоль, 0,10 экв.), 2-(дициклогексилфосфино)-2',4',6'-триизопропилбифенил (181 мг, 0,404 ммоль, 0,20 экв., Xphos), карбонат цезия (1980 мг, 6,06 ммоль, 3,00 экв.), ((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)трифторборат калия (927 мг, 3,03 ммоль, 1,50 экв.), THF (8 мл) и воду (2 мл) в атмосфере азота. Реакционную смесь перемешивали в течение 4 ч при температуре 80°С и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 700 мг (выход 74%) трет-бутил-4-(3-хлор-2-((1-(этоксикарбонил)циклопропил)метокси)-4-метилбензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 467 [М+Н]+.
Стадия 4: Синтез 1-((6-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-2-хлор-3-метилфенокси)метил)циклопропан-1-карбоновой кислоты
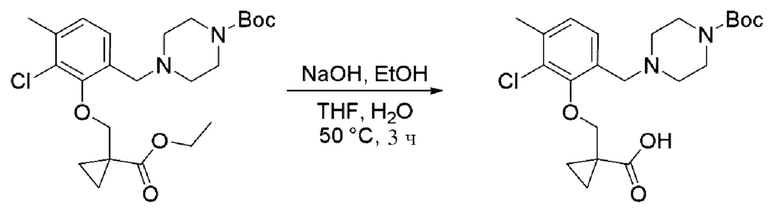
[00259] В круглодонную колбу загружали трет-бутил-4-(3-хлор-2-((1-(этоксикарбонил)циклопропил)метокси)-4-метилбензил)пиперазин-1-карбоксилат (700 мг, 1,50 ммоль, 1,00 экв.), тетрагидрофуран (3 мл), этанол (3 мл), воду (5 мл) и гидроксид натрия (600 мг, 15,0 ммоль, 10,0 экв.). Реакционную смесь перемешивали в течение 3 ч при температуре 50°С. Значение рН раствора доводили до 5 с помощью соляной кислоты (1 моль/л). Полученный раствор экстрагировали дихлорметаном (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении, получая 610 мг (выход 93%) 1-((6-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-2-хлор-3-метилфенокси)метил)циклопропан-1-карбоновой кислоты. ЖХ/МС (ESI, m/z): 439 [М+Н]+.
Стадия 5: Синтез 1-((2-хлор-3-метил-6-(пиперазин-1-илметил)фенокси)метил)циклопропан-1-карбоновой кислоты
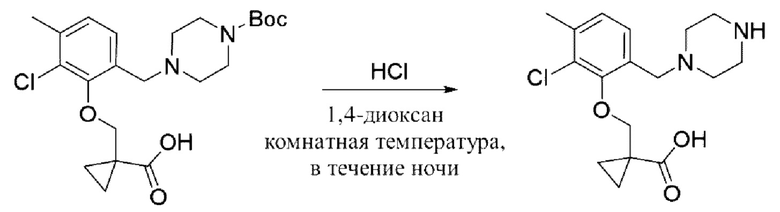
[00260] В круглодонную колбу загружали 1-((6-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-2-хлор-3-метилфенокси)метил)циклопропан-1-карбоновую кислоту (630 мг, 1,44 ммоль, 1,00 экв.), 1,4-диоксан (10 мл) и концентрированную соляную кислоту (3 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре и концентрировали при пониженном давлении, чтобы получить 600 мг (неочищенной) 1-((2-хлор-3-метил-6-(пиперазин-1-илметил)фенокси)метил)циклопропан-1-карбоновой кислоты. ЖХ/МС (ESI, m/z): 339 [М+Н]+.
Стадия 6: Синтез 1-((2-хлор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенокси)метил)циклопропан-1-карбоновой кислоты
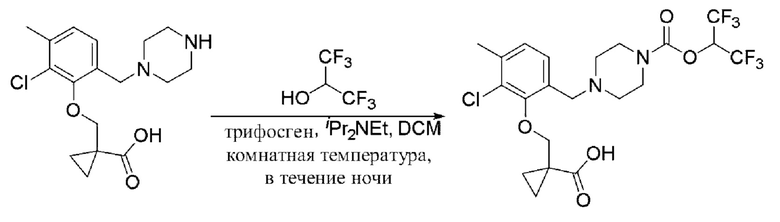
[00261] В круглодонную колбу загружали трифосген (270 мг, 0,910 ммоль, 0,70 эквивалента), дихлорметан (10 мл) и 1,1,1,3,3,3-гексафторпропан-2-ол (437 мг, 2,60 ммоль, 2,00 экв.). N,N-диизопропилэтиламин (503 мг, 3,90 ммоль, 3,00 экв.) добавляли при температуре 0°С и смесь перемешивали в течение 1 часа при комнатной температуре до добавления 1-((2-хлор-3-метил-6-(пиперазин-1-илметил)фенокси)метил)циклопропан-1-карбоновой кислоты (440 мг, 1,30 ммоль, 1,00 экв.). Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили насыщенным NaHCO3 (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт (200 мг) очищали препаративной ВЭЖХ с получением 155 мг (выход 22%) 1-((2-хлор-3-метил-6-(пиперазин-1-илметил)фенокси)метил)циклопропан-1-карбоновой кислоты. 1H ЯМР (300 МГц, метанол-d4) δ 7,21 (д, J=7,8 Гц, 1Н), 7,07 (д, J=8,1 Гц, 1Н), 6,18-6,09 (м, 1Н), 4,11 (с, 2Н) 3,89 (с, 2Н), 3,63-3,54 (м, 4Н), 2,69-2,68 (м, 4Н), 2,35 (с, 3Н), 1,32-1,28 (м, 2Н), 1,11-1,08 (м, 2Н)., ЖХ/МС (ESI, m/z): 533 [М+Н]+.
Пример 24: 4-(2-Фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенил)-2,2-диметилбут-3-иновая кислота
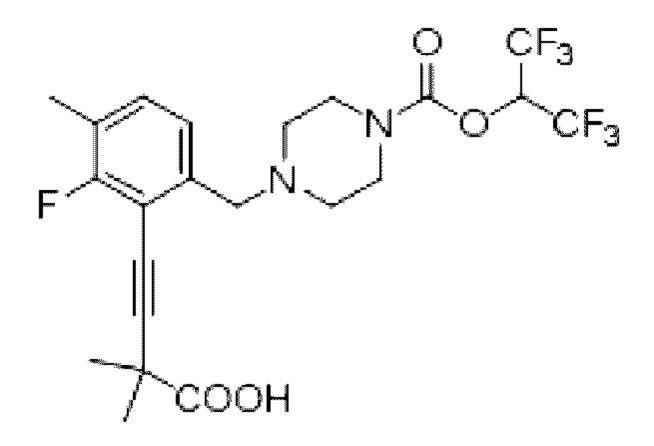
Стадия 1: Синтез трет-бутил-4-(3-фтор-2-гидрокси-4-метилбензил)пиперазин-1-карбоксилат
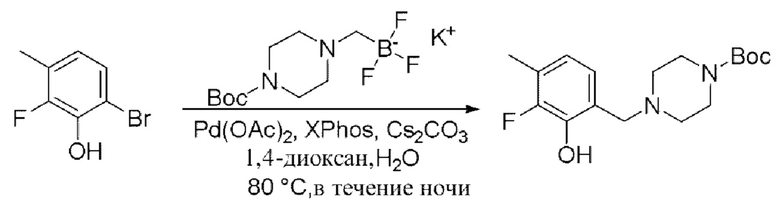
[00262] В круглодонную колбу загружали 6-бром-2-фтор-3-метилфенол (2,00 г, 9,75 ммоль, 1,00 экв.), (4-[(трет-бутокси)карбонил]пиперазин-1-илметил)трифторборанид калия (3,90 г, 12,7 ммоль, 1,30 экв.), ацетат палладия (0,439 г, 1,96 ммоль, 0,20 экв.), 2-(дициклогексилфосфино)-2',4',6'-триизопропилбифенил (1,87 г, 3,93 ммоль, 0,40 экв., Xphos), карбонат цезия (9,59 г, 29,4 ммоль, 3,00 экв.), 1,4-диоксан (20 мл) и воду (4 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 80°С и гасили водой (20 мл). Полученный раствор экстрагировали EtOAc (3×30 мл), а органические слои объединяли, промывали рассолом (1×50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 2,20 г (выход 70%) трет-бутил-4-(3-фтор-2-гидрокси-4-метилбензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 325 [M+H]+.
Стадия 2: Синтез трет-бутил-4-(3-фтор-4-метил-2-(((трифторметил)сульфонил)окси)бензил)пиперазин-1-карбоксилата
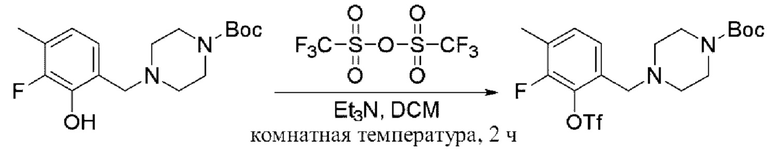
[00263] В круглодонную колбу загружали трет-бутил-4-(3-фтор-2-гидрокси-4-метилбензил)пиперазин-1-карбоксилат (2,00 г, 6,17 ммоль, 1,00 экв.), TEA (1,87 г, 18,5 ммоль, 3,00 экв.) и DCM (40 мл). Трифторметансульфоновый ангидрид (2,61 г, 9,25 ммоль, 1,50 экв.) добавляли при температуре 0°С и реакционную смесь перемешивали в течение 2 ч при комнатной температуре, а затем гасили водой (30 мл). Полученный раствор экстрагировали DCM (3×50 мл), а органические слои объединяли, промывали рассолом (1×50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 1,80 г (выход 64%) трет-бутил-4-(3-фтор-4-метил-2-(((трифторметил)сульфонил)окси)бензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 457 [М+Н]+.
Стадия 3: Синтез трет-бутил-4-(2-(4-этокси-3,3-диметил-4-оксобут-1-ин-1-ил)-3-фтор-4-метилбензил)пиперазин-1-карбоксилата
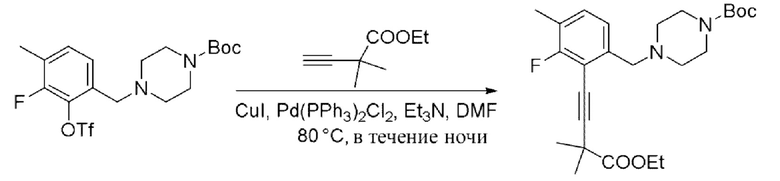
[00264] В круглодонную колбу загружали трет-бутил-4-(3-фтор-4-метил-2-(((трифторметил)сульфонил)окси)бензил)пиперазин-1-карбоксилат (850 мт, 1,86 ммоль, 1,00 экв.), этил-2,2-диметилбут-3-иноат (522 мг, 3,72 ммоль, 2,00 экв.), йодид меди (I) (70,8 мг, 0,370 ммоль, 0,20 экв.), хлорид бис(трифенилфосфин)палладия (II) (130 мг, 0,190 ммоль, 0,10 экв.), TEA (565 мг, 5,58 ммоль, 3,00 экв.) и DMF (10 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 80°С и гасили водой (20 мл). Полученный раствор экстрагировали EtOAc (3×30 мл), а органические слои объединяли, промывали рассолом (1×50 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 100 мг (выход 12%) трет-бутил-4-(2-(4-этокси-3,3-диметил-4-оксобут-1-ин-1-ил)-3-фтор-4-метилбензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 447 [M+H]+.
Стадия 4: Синтез 4-(6-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-2-фтор-3-метилфенил)-2,2-диметилбут-3-иновой кислоты
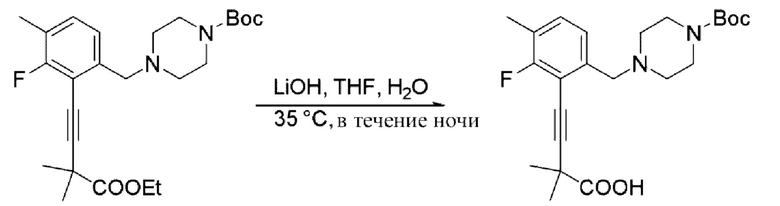
[00265] В круглодонную колбу загружали трет-бутил-4-(2-(4-этокси-3,3-диметил-4-оксобут-1-ин-1-ил)-3-фтор-4-метилбензил)пиперазин-1-карбоксилат (100 мг, 0,224 ммоль, 1,00 экв.), гидроксид лития (322 мг, 13,4 ммоль, 60,00 экв.), тетрагидрофуран (5 мл) и воду (1 мл). Реакционную смесь перемешивали в течение ночи при температуре 35°С и гасили водой (10 мл), прежде чем довести значение рН до рН 6 соляной кислотой (1М). Полученный раствор экстрагировали DCM (3×15 мл), а органические слои объединяли, промывали рассолом (1×20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении, получая 90,0 мг (выход 96%) 4-(6-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-2-фтор-3-метилфенил)-2,2-диметилбут-3-иновой кислоты. ЖХ/МС (ESI, m/z): 419 [М+Н]+.
Стадия 5: Синтез 4-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенил)-2,2-диметилбут-3-иновой кислоты
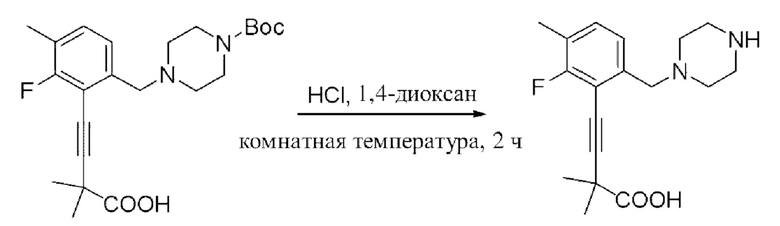
[00266] В круглодонную колбу загружали 4-(6-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-2-фтор-3-метилфенил)-2,2-диметилбут-3-ининовую кислоту (90,0 мг, 0,220 ммоль, 1,00 экв.), 1,4-диоксан (8 мл) и концентрированную соляную кислоту (1 мл). Полученный раствор перемешивали в течение 2 ч при комнатной температуре и концентрировали при пониженном давлении, чтобы получить 100 мг (неочищенной) 4-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенил)-2,2-диметилбут-3-иновой кислоты. ЖХ/МС (ESI, m/z): 319 [М+Н]+.
Стадия 6: Синтез 4-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенил)-2,2-диметилбут-3-иновой кислоты
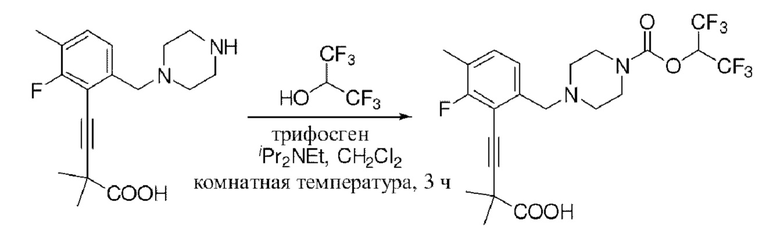
[00267] В круглодонную колбу загружали трифосген (42,5 мг, 0,143 ммоль, 0,70 эквивалента) и DCM (10 мл). 1,1,1,3,3,3-гексафторпропан-2-ол (85,8 мг, 0,510 ммоль, 2,50 экв.) и DIPEA (105 мг, 0,816 ммоль, 4,00 экв.) добавляли последовательно при температуре 0°С. Смесь перемешивали в течение 1 часа при комнатной температуре до добавления 4-(2-фтор-3-метил-6-(пиперазин-1-илметил)фенил)-2,2-диметилбут-3-иновой кислоты (65,0 мг, 0,204 ммоль, 1,00 экв.). Реакционную смесь перемешивали в течение 2 ч при комнатной температуре и гасили водой (10 мл). Полученный раствор экстрагировали DCM (3×15 мл), а органические слои объединяли, промывали рассолом (1×40 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт (200 мг) очищали препаративной ВЭЖХ с получением 34,2 мг (выход 33%) 4-(2-фтор-6-((4-(((1,1,1,3,3,3-)гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)-3-метилфенил)-2,2-диметилбут-3-иновой кислоты. 1H ЯМР (300 МГц, метанол-d4) δ 7,23-7,13 (м, 2Н), 6,20-6,11 (м, 1Н), 3,83 (с, 2Н), 3,63-3,60 (м, 4Н), 2,68-2,67 (м, 4Н), 2,27 (с, 3Н), 1,58 (с, 6Н). ЖХ/МС (ESI, m/z): 513 [М+Н]+.
Пример 25: 4-(2-Фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)-2,2-диметилбут-3-иновая кислота
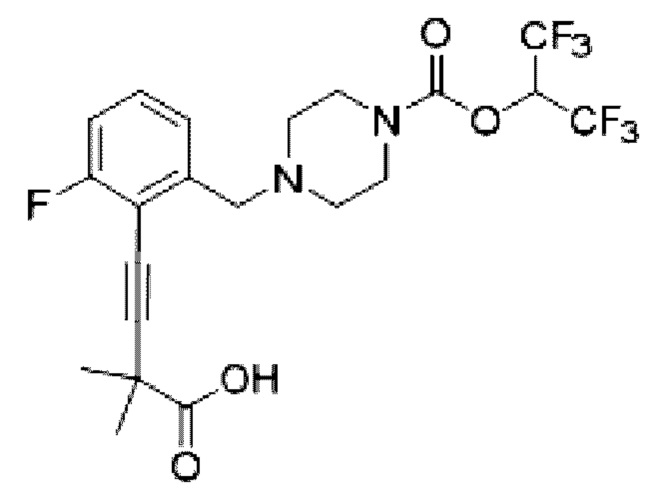
Стадия 1: Синтез 2-(триметилсилил)этил-2,2-диметилбут-3-иноата
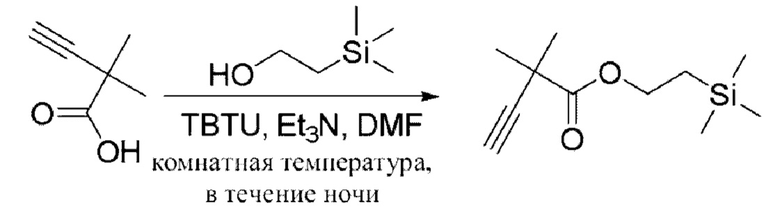
[00268] В круглодонную колбу загружали 2,2-диметилбут-3-иновую кислоту (1,00 г, 8,93 ммоль, 1,00 экв.), 2-(триметилсилил)этан-1-ол (1,05 г, 8,93 ммоль, 1,00 экв.), тетрафторборат 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (3,72 г, 11,6 ммоль, 1,30 экв.), TEA (1,81 г, 17,9 ммоль, 2,00 экв.) и DMF (10 мл). Полученный раствор перемешивали в течение ночи при комнатной температуре. Реакционную смесь разбавляли этиловым эфиром (30 мл) и полученный раствор промывали водой (1×30 мл) и солевым раствором (1×20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем с получением 1,30 г (выход 69%) 2-(триметилсилил)этил-2,2-диметилбут-3-иноата в виде желтого масла. 1H ЯМР (300 МГц, Хлороформ-d) δ 4,28-4,22 (м, 2Н), 2,27 (с, 1Н), 1,50 (с, 6Н), 1,08-1,02 (м, 2Н), 0,07 (с, 9Н).
Стадия 2: Синтез 2-(триметилсилил)этил-4-(2-фтор-6-формилфенил)-2,2-диметилбут-3-иноата
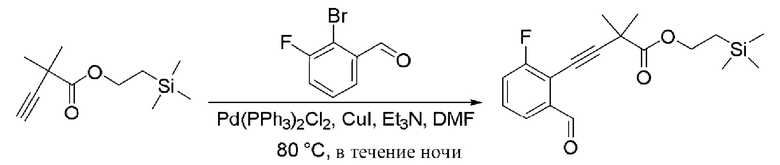
[00269] В круглодонную колбу загружали 2-бром-3-фторбензальдегид (300 мг, 1,49 ммоль, 1,00 экв.), 2-(триметилсилил)этил-2,2-диметилбут-3-иноат (475 мг, 2,24 ммоль, 1,50 экв.), хлорид бис(трифенилфосфин)палладия(II) (52,3 мг, 0,0745 ммоль, 0,05 экв.), йодид меди (I) (28,3 мг, 0,149 ммоль, 0,10 экв.), TEA (451 мг, 4,46 ммоль, 3,00 экв.) и DMF (10 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 80°С и затем гасили водой (10 мл). Полученный раствор экстрагировали DCM (3×15 мл), а органические слои объединяли, промывали рассолом (1×20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 340 мг (выход 72%) 2-(триметилсилил)этил-4-(2-фтор-6-формилфенил)-2,2-диметилбут-3-иноата. ЖХ/МС (ESI, m/z): 357 [M+Na]+.
Стадия 3: Синтез 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(3,3-диметил-4-оксо-4-(2-(триметилсилил)этокси)бут-1-ин-1-ил)-3-фторбензил)пиперазин-1-карбоксилата
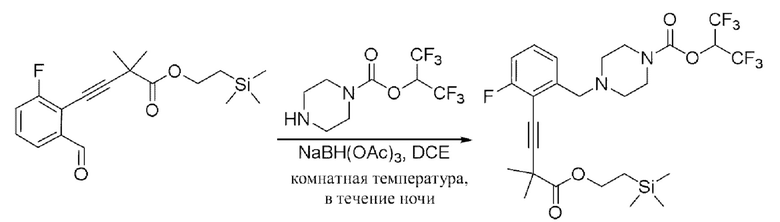
[00270] В круглодонную колбу загружали 2-(триметилсилил)этил-4-(2-фтор-6-формилфенил)-2,2-диметилбут-3-иноат (334 мг, 1,00 ммоль, 1,00 экв.), 1,1,1,3,3,3-гексафторпропан-2-илпиперазин-1-карбоксилат (364 мг, 1,30 ммоль, 1,30 экв.) и DCE (15 мл). Смесь перемешивали в течение 1 часа при комнатной температуре до добавления триацетоксиборгидрида натрия (848 мг, 4,00 ммоль, 4,00 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре и затем гасили водой (10 мл). Смесь экстрагировали DCM (3×15 мл), а органические слои объединяли, промывали рассолом (1×20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 350 мг (выход 59%) 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(3,3-диметил-4-оксо-4-(2-(триметилсилил)этокси)бут-1-ин-1-ил)-3-фторбензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 599 [М+Н]+.
Стадия 4: Синтез 4-(2-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)-2,2-диметилбут-3-иновой кислоты
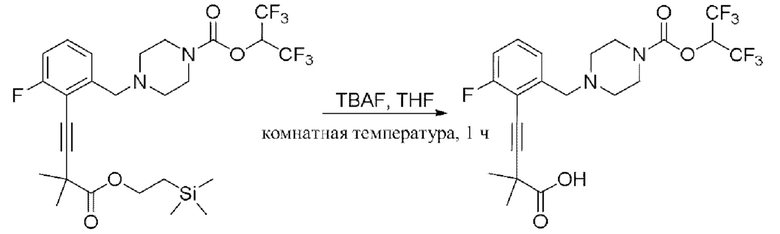
[00271] В круглодонную колбу загружали 1,1,1,3,3,3-гексафторпропан-2-ил-4-(2-(3,3-диметил-4-оксо-4-(2-(триметилсилил)этокси)бут-1-ин-1-ил)-3-фторбензил)пиперазин-1-карбоксилат (350 мг, 0,584 ммоль, 1,00 экв.), фторид тетрабутиламмония (0,9 мл, 1 М в тетрагидрофуране, 0,900 ммоль, 1,50 экв.) и THF (10 мл). Реакционную смесь перемешивали в течение 1 часа при комнатной температуре и гасили водой (10 мл). Полученный раствор экстрагировали DCM (3×15 мл), а органические слои объединяли, промывали рассолом (1×20 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт (280 мг) очищали препаративной ВЭЖХ с получением 107,6 мг (выход 37%) 4-(2-фтор-6-((4-(((1,1,1,3,3,3-)гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенил)-2,2-диметилбут-3-иновой кислоты. 1H ЯМР (400 МГц, метанол-d4) δ 7,34-7,25 (м, 2Н), 7,08-7,04 (м, 1Н), 6,17-6,10 (м, 1Н), 3,81 (с, 2Н), 3,62-3,57 (м, 4Н), 2,62 (уш. с., 4Н), 1,56 (с, 6Н). ЖХ/МС (ESI, m/z): 499 [M+H]+.
Пример 26: 1-((2-Циано-4-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)метил)циклопропан-1-карбоновая кислота
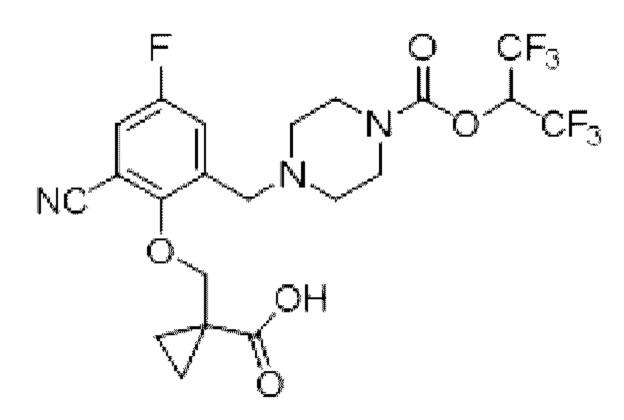
Стадия 1: Синтез этил-1-((2-бром-4-фтор-6-формилфенокси)метил)циклопропан-1-карбоксилата
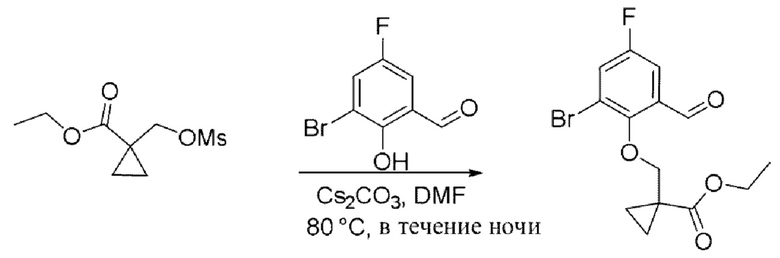
[00272] В круглодонную колбу загружали 3-бром-5-фтор-2-гидроксибензальдегид (1,00 г, 4,59 ммоль, 1,00 экв.), этил-1-[(метансульфонилокси)метил]циклопропан-1-карбоксилат (1,53 г, 6,88 ммоль, 1,50 экв.), карбонат цезия (4,49 г, 13,8 ммоль, 3,00 экв.) и DMF (10 мл). Реакционную смесь перемешивали в течение ночи при температуре 80°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 0,600 г (выход 38%) этил-1-(2-бром-4-фтор-6-формилфеноксиметил)циклопропан-1-карбоксилата. ЖХ/МС (ESI, m/z): 345 [М+Н]+.
Стадия 2: Синтез трет-бутил-4-(3-бром-2-((1-(этоксикарбонил)циклопропил)метокси)-5-фторбензил)пиперазин-1-карбоксилата
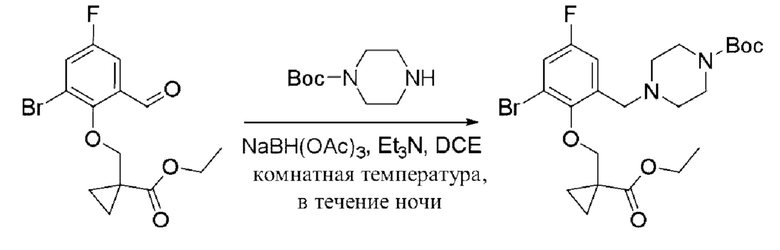
[00273] В круглодонную колбу загружали этил-1-(2-бром-4-фтор-6-формилфеноксиметил)циклопропан-1-карбоксилат (600 мг, 1,74 ммоль, 1,00 экв.), TEA (527 мг, 5,22 ммоль, 3,00 экв.), трет-бутилпиперазин-1-карбоксилат (390 мг, 2,09 ммоль, 1,20 экв.) и DCE (10 мл). Раствор перемешивали в течение 1 часа при комнатной температуре до добавления триацетоксиборгидрида натрия (1110 мг, 5,22 ммоль, 3,00 экв.). Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 540 мг (выход 60%) трет-бутил-4-(3-бром-2-((1-(этоксикарбонил)циклопропил)метокси)-5-фторбензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 515 [М+H]+.
Стадия 3: Синтез трет-бутил-4-(3-циано-2-((1-(этоксикарбонил)циклопропил)метокси)-5-фторбензил)пиперазин-1-карбоксилата
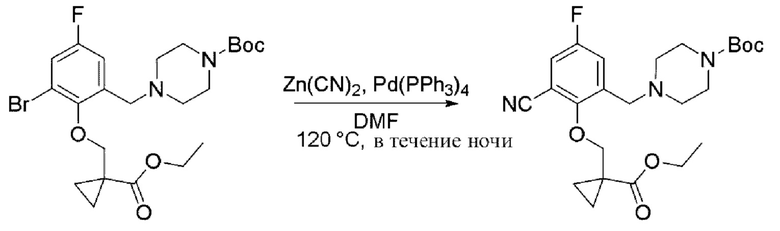
[00274] В круглодонную колбу загружали трет-бутил-4-(3-бром-2-((1-(этоксикарбонил)циклопропил)метокси)-5-фторбензил)пиперазин-1-карбоксилат (240 мг, 0,470 ммоль, 1,00 экв.), цианид цинка (108 мг, 0,940 ммоль, 2,00 экв.), тетракис(трифенилфосфин)палладий (58,0 мг, 0,0500 ммоль, 0,10 экв.) и DMF (10 мл) в атмосфере азота. Реакционную смесь перемешивали в течение ночи при температуре 120°С и гасили водой (30 мл). Полученный раствор экстрагировали EtOAc (2×50 мл) и органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Остаток хроматографировали на колонке с силикагелем, получая 125 мг (выход 58%) трет-бутил-4-(3-циано-2-((1-(этоксикарбонил)циклопропил)метокси)-5-фторбензил)пиперазин-1-карбоксилата. ЖХ/МС (ESI, m/z): 462 [М+Н]+.
Стадия 4: Синтез 1-((2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-6-циано-4-фторфенокси)метил)циклопропан-1-карбоновой кислоты

[00275] В кругло донную колбу загружали трет-бутил-4-(3-циано-2-((1-(этоксикарбонил)циклопропил)метокси)-5-фторбензил)пиперазин-1-карбоксилат (125 мг, 0,270 ммоль, 1,00 экв.), гидроксид лития (130 мг, 5,43 ммоль, 20,0 экв.), THF (5 мл) и воду (5 мл). Реакционную смесь перемешивали в течение ночи при комнатной температуре. Значение рН раствора доводили до 5 с помощью соляной кислоты (1 моль/л). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении, получая 110 мг (выход 94%) 1-((2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-6-циано-4-фторфенокси)метил)циклопропан-1-карбоновой кислоты. ЖХ/МС (ESI, m/z): 434 [М+Н]+.
Стадия 5: Синтез 1-((2-циано-4-фтор-6-(пиперазин-1-илметил)фенокси)метил)циклопропан-1-карбоновой кислоты
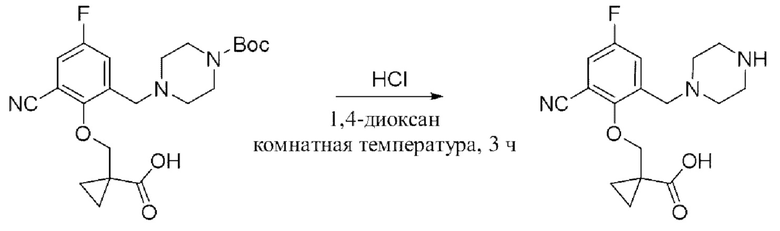
[00276] В круглодонную колбу загружали 1-((2-((4-(трет-бутоксикарбонил)пиперазин-1-ил)метил)-6-циано-4-фторфенокси)метил)циклопропан-1-карбоновую кислоту (160 мг, 0,370 ммоль, 1,00 экв.), концентрированную соляную кислоту (2 мл) и 1,4-диоксан (8 мл). Полученный раствор перемешивали в течение 3 ч при комнатной температуре и концентрировали при пониженном давлении, чтобы получить 123 мг (количественно) 1-((2-циано-4-фтор-6-(пиперазин-1-илметил)фенокси)метил)циклопропан-1-карбоновой кислоты. ЖХ/МС (ESI, m/z): 334 [М+Н]+.
Стадия 6: Синтез 1-((2-циано-4-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)метил)циклопропан-1-карбоновой кислоты
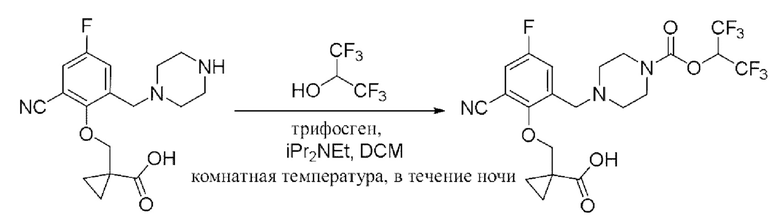
[00277] В круглодонную колбу загружали трифосген (77,0 мг, 0,260 ммоль, 0,700 экв.), 1,1,1,3,3,3-гексафторпропан-2-ол (124 мг, 0,740 ммоль, 2,00 экв.) и DCM (5 мл). N,N-диизопропилэтиламин (143 мг, 1,11 ммоль, 3,00 экв.) добавляли при температуре 0°С и смесь перемешивали в течение 1 часа при комнатной температуре до добавления 1-((2-циано-4-фтор-6-(пиперазин-1-илметил)фенокси)метил)циклопропан-1-карбоновой кислоты (123 мг, 0,370 ммоль, 1,00 экв.). Реакционную смесь перемешивали в течение ночи при комнатной температуре и гасили водой (30 мл). Полученный раствор экстрагировали DCM (2×50 мл), а органические слои объединяли, промывали рассолом (2×30 мл), сушили над безводным Na2SO4, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт (250 мг) очищали препаративной ВЭЖХ с получением 39,9 мг (выход 21%) 1-((2-циано-4-фтор-6-((4-(((1,1,1,3,3,3-гексафторпропан-2-ил)окси)карбонил)пиперазин-1-ил)метил)фенокси)метил)циклопропан-1-карбоновой кислоты. 1Н ЯМР (400 МГц, хлороформ-d) δ 7,46-7,43 (м, 1Н), 7,24-7,22 (м, 1Н), 5,81-5,73 (м, 1Н), 4,22 (с, 2Н), 3,73 (с, 2Н), 3,61-3,60 (м, 4Н), 2,56-2,53 (м, 4Н), 1,57-1,54 (м, 2Н), 1,32-1,29 (м, 2Н). ЖХ/МС (ESI, m/z): 528 [М+Н]+.
Примеры 27-56: Примеры 27-56 получали посредством процедур, аналогичных описанным в примерах 1-26.
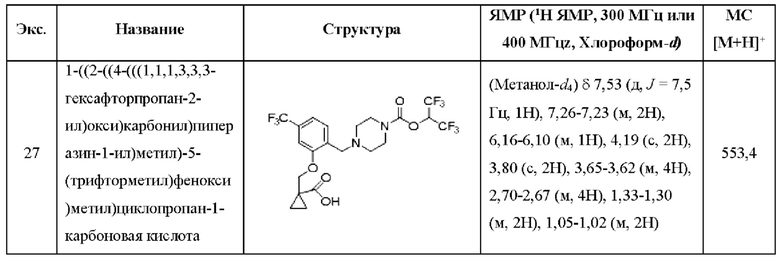
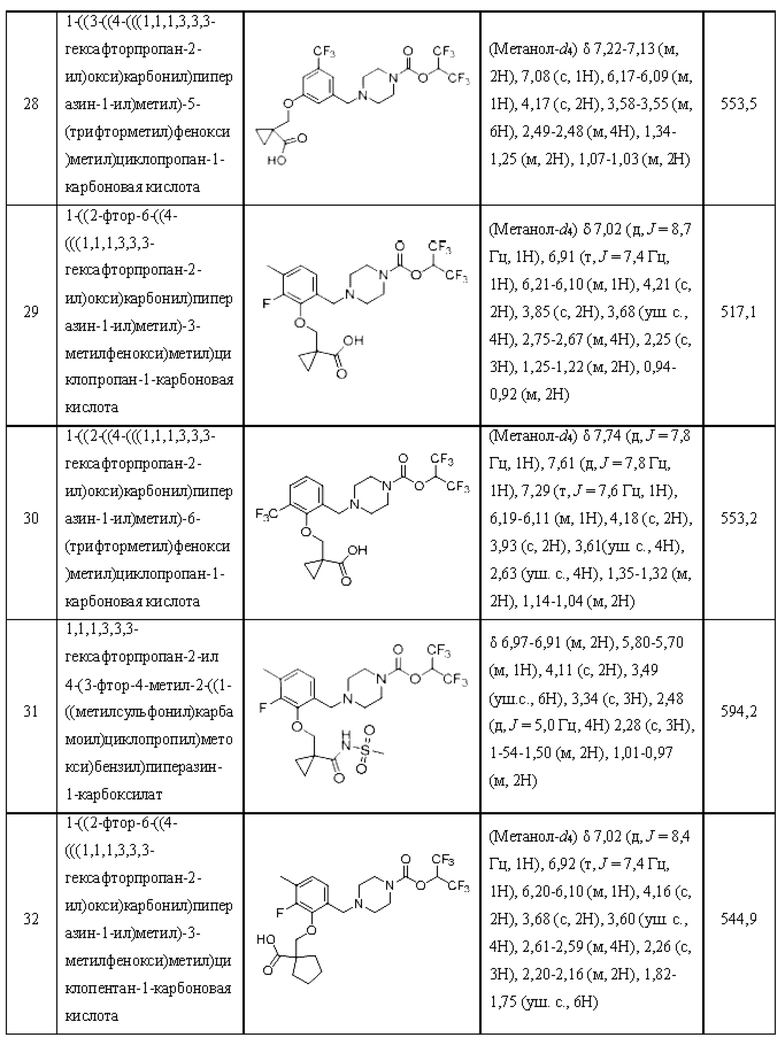
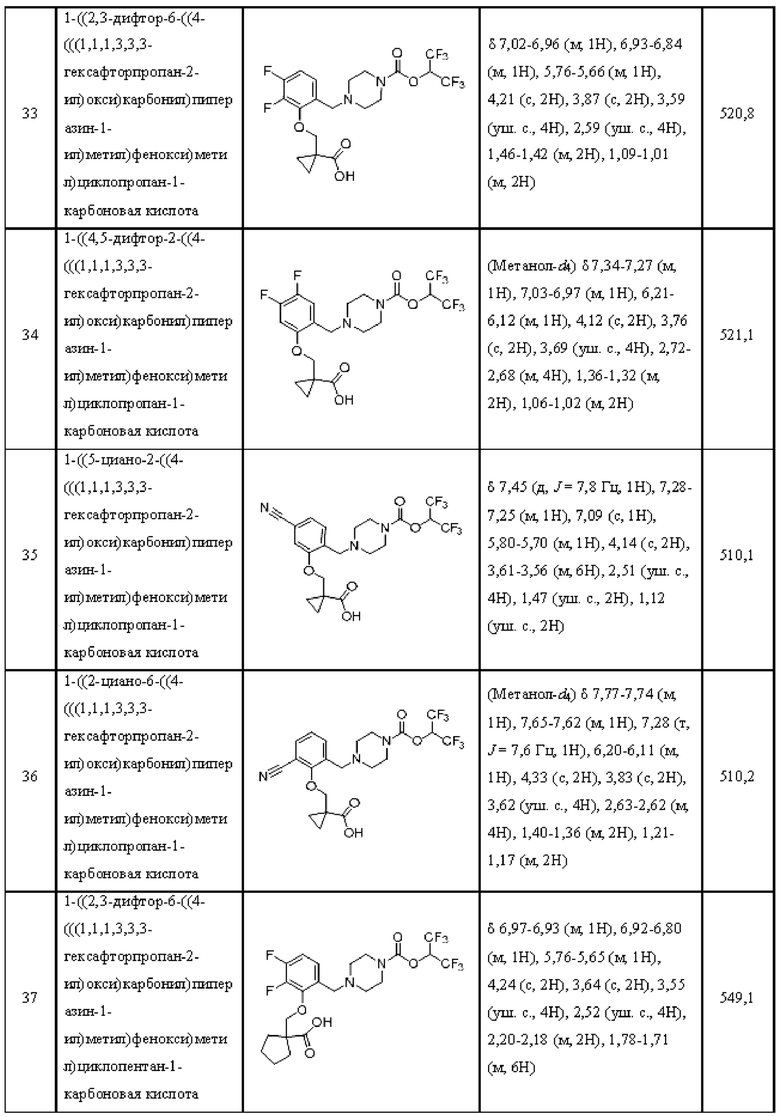
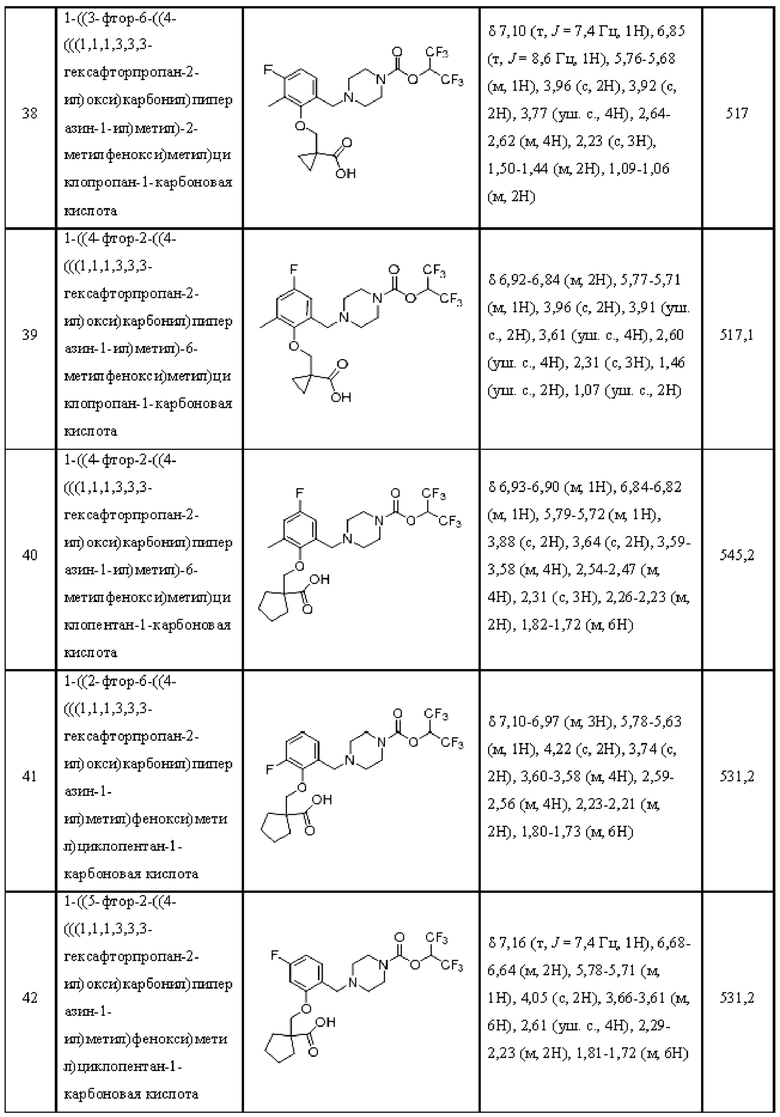
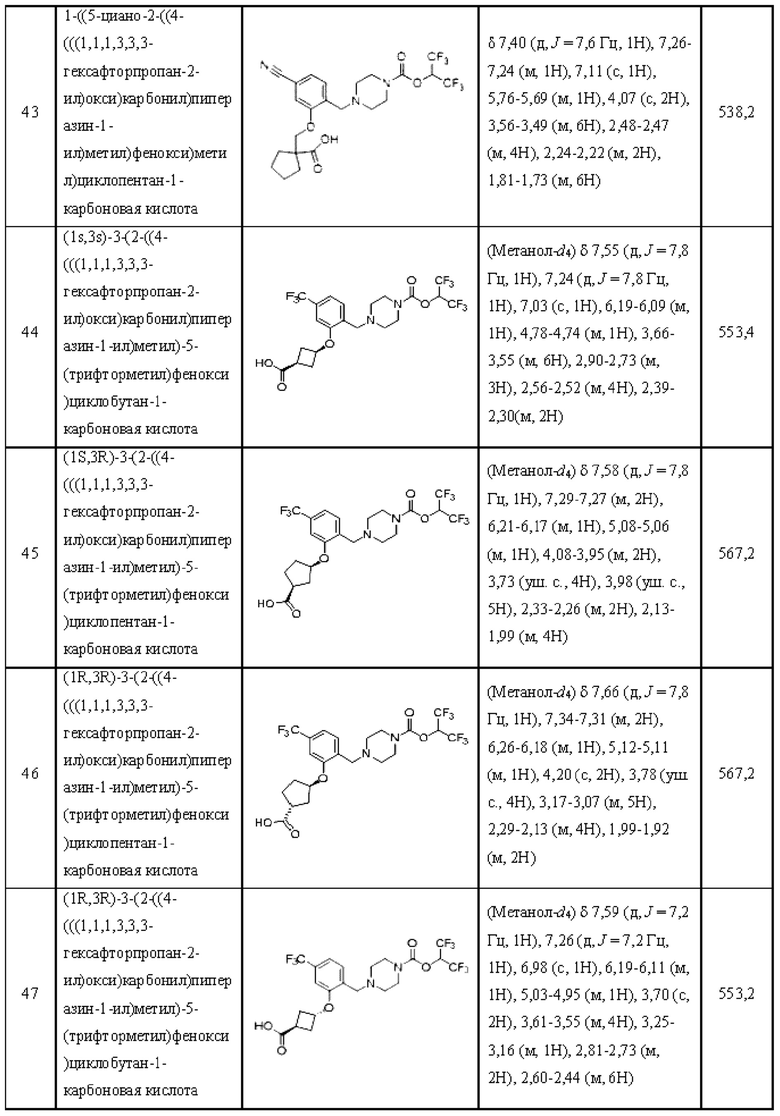
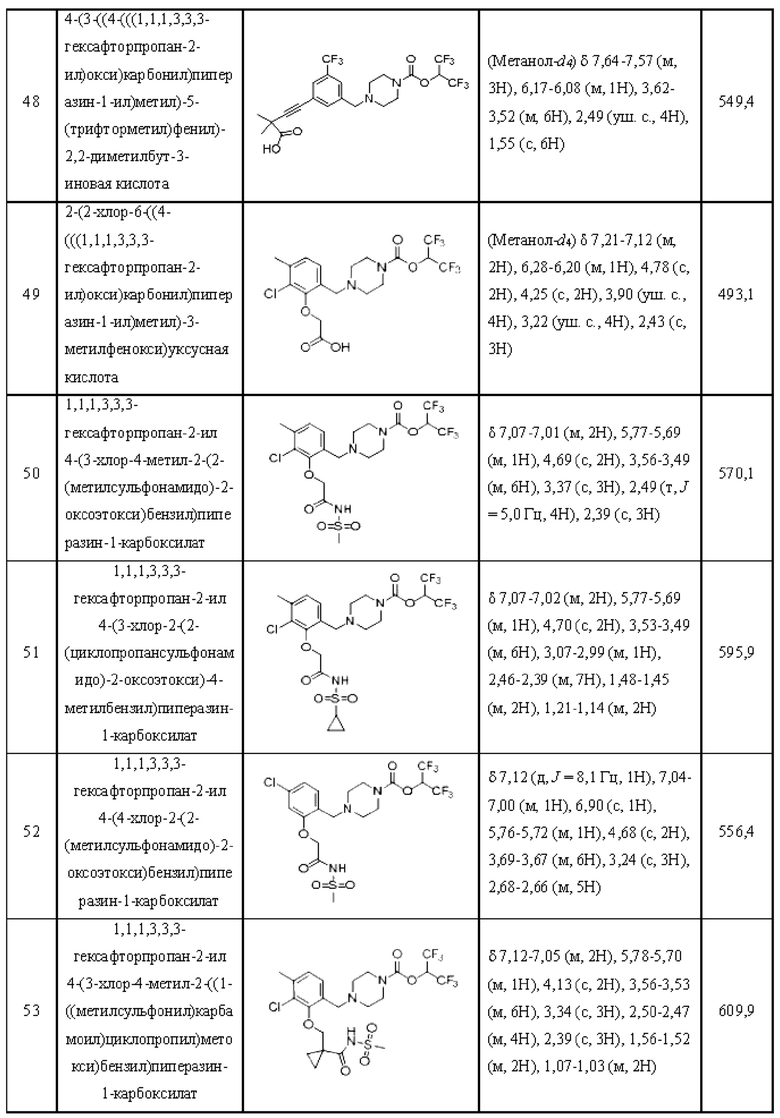
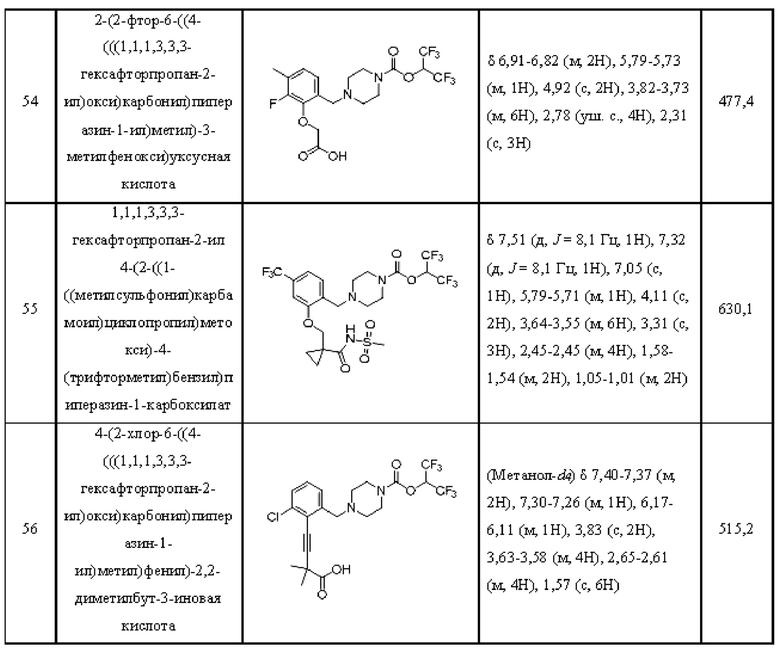
II. Оценка биологического действия
[00278] Соединения исследовали для оценки их активности в отношении MAGL и серин-гидролазы с использованием следующих анализов in vitro и in vivo.
In vitro профилирование белков (человека) на основе конкурентной активности.
[00279] Протеомы (фракции префронтальной коры или клеточной мембраны человека) (50 мкл, концентрация общего белка 1,0-2,0 мг/мл) предварительно инкубировали с различными концентрациями ингибиторов при температуре 37°С. Через 30 минут добавляли FP-Rh или JW912 (1,0 мкл, 50 мкМ в DMSO) и смесь инкубировали еще 30 минут при комнатной температуре. Реакции гасили загрузочным буфером ДСН (15 мкл - 4Х) и прогоняли на ДСН-ПААГ. После визуализации в геле активность серин-гидролазы определяли путем измерения интенсивности флуоресценции полос геля, соответствующих MAGL, с использованием программного обеспечения ImageJ 1.49k. Данные IC50 из этого анализа показаны в таблице 2.
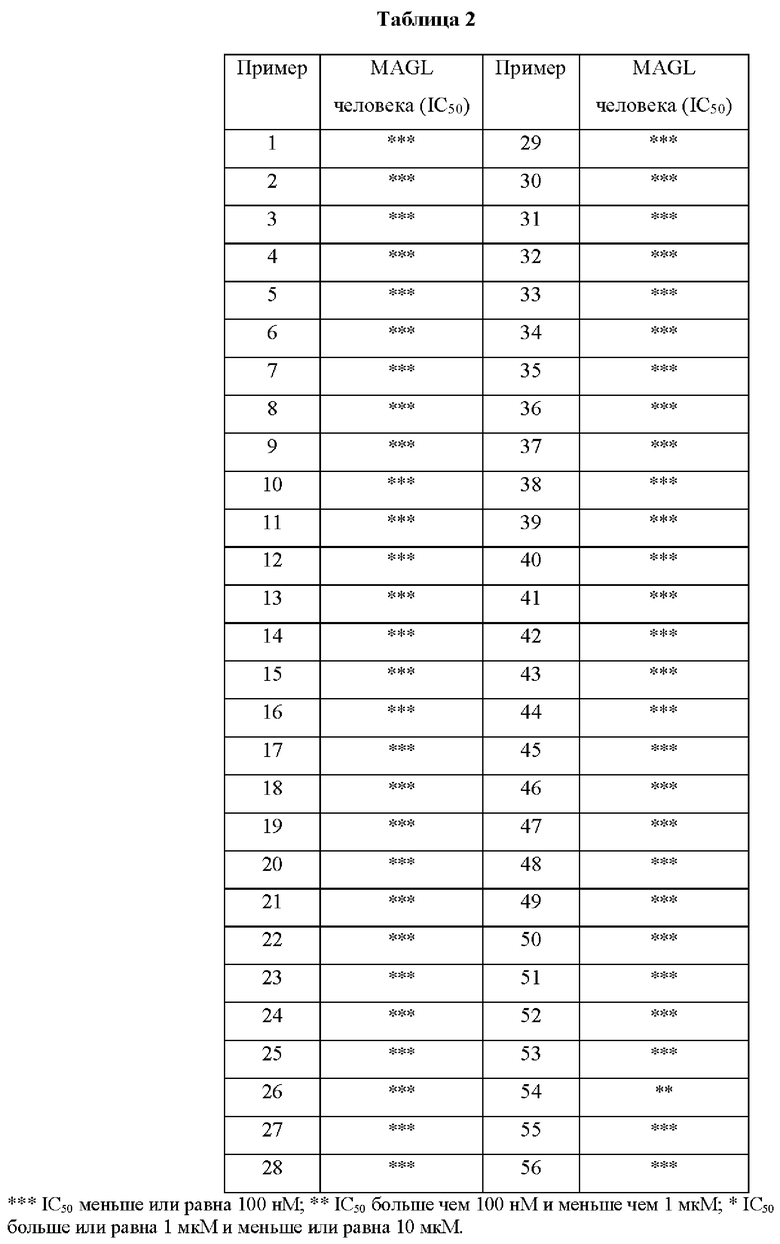
In vitro профилирование белков (мыши) на основе конкурентной активности.
[00280] Протеомы (фракция мембран головного мозга мыши или лизаты клеток) (50 мкл, общая концентрация белка 1,0 мг/мл) предварительно инкубировали с различными концентрациями ингибиторов при температуре 37°С. Через 30 минут добавляли FP-Rh (1,0 мкл; 50 мкМ в DMSO) и смесь инкубировали в течение еще 30 минут при температуре 37°С. Реакции гасили загрузочным буфером ДСН (50 мкл - 4Х) и прогоняли на ДСН-ПААГ. После визуализации в геле активность серин-гидролазы определяли путем измерения интенсивности флуоресценции полос геля, соответствующих MAGL, с использованием программного обеспечения ImageJ 1.49k.
Получение протеом головного мозга мышей от получавших ингибитор мышей.
[00281] Ингибиторы вводили C57B1/6J дикого типа перорально через желудочный зонд в наполнителе из полиэтиленгликоля. Каждое животное умерщвляли через 4 ч после введения, и протеомы головного мозга готовили и анализировали в соответствии с ранее установленными способами (смотрите Niphakis, M.J., et al. (2011) ACS Chem. Neurosci. и Long, J.Z., et al. Nat. Chem. Biol. 5:37-44). Данные по ингибированию в процентах приведены в таблице 3.
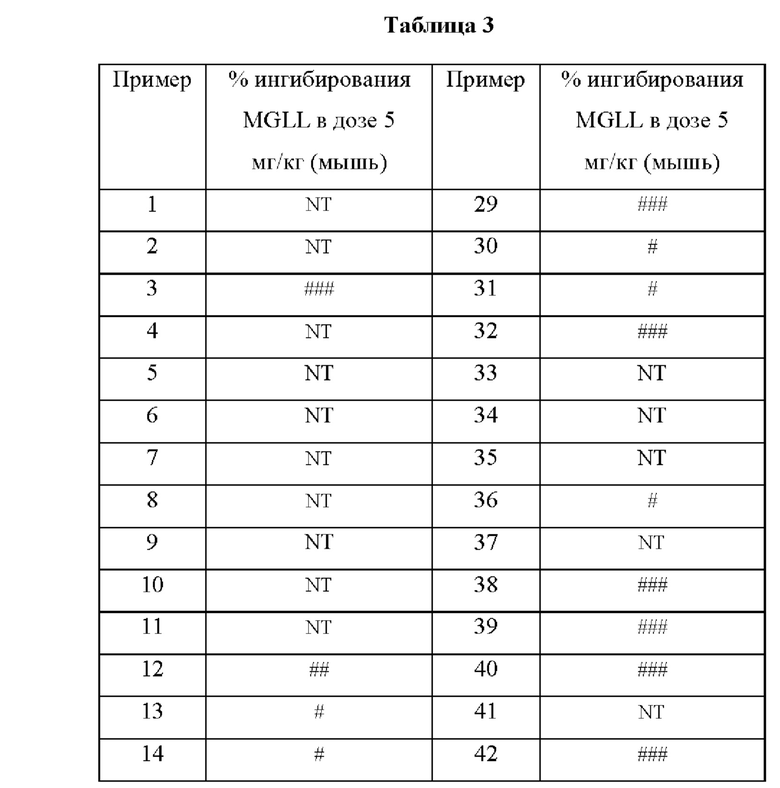
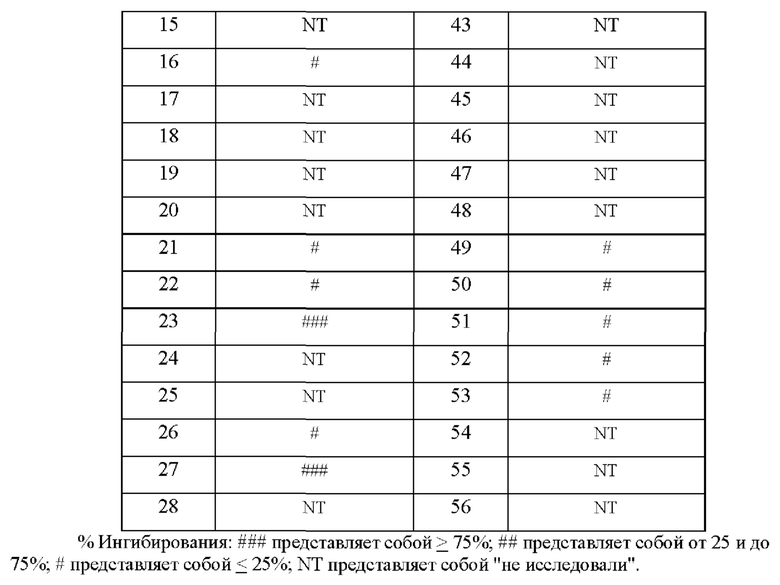
| название | год | авторы | номер документа |
|---|---|---|---|
| СПИРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2018 |
|
RU2781639C2 |
| ИНГИБИТОРЫ MAGL НА ОСНОВЕ ПИРАЗОЛА | 2018 |
|
RU2789157C2 |
| ИНГИБИТОРЫ ТРАНСГЛУТАМИНАЗЫ 2 (TG2) | 2019 |
|
RU2781370C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СПИРОСОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ MAGL | 2018 |
|
RU2726631C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ИММУНОМОДУЛЯТОРЫ В КАЧЕСТВЕ ИНГИБИТОРА КОНТРОЛЬНЫХ ТОЧЕК ИММУННОГО ОТВЕТА PDL1 | 2020 |
|
RU2824127C2 |
| АНТАГОНИСТ ЭСТРОГЕНОВОГО РЕЦЕПТОРА | 2019 |
|
RU2832735C2 |
| 11,13-МОДИФИЦИРОВАННЫЕ САКСИТОКСИНЫ ДЛЯ ЛЕЧЕНИЯ БОЛИ | 2018 |
|
RU2778455C2 |
| ПУТИ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ | 2020 |
|
RU2795503C2 |
| МАКРОЦИКЛИЧЕСКИЕ ФЕНИЛКАРБАМАТЫ, ИНГИБИРУЮЩИЕ HCV | 2008 |
|
RU2490261C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ИНГИБИТОРА MAGL | 2017 |
|
RU2799564C2 |
Изобретение относится к соединениям пиперазина формулы (I). Технический результат: получены новые соединения формулы (I), которые могут быть применимы в качестве модуляторов MAGL. 5 з.п. ф-лы.
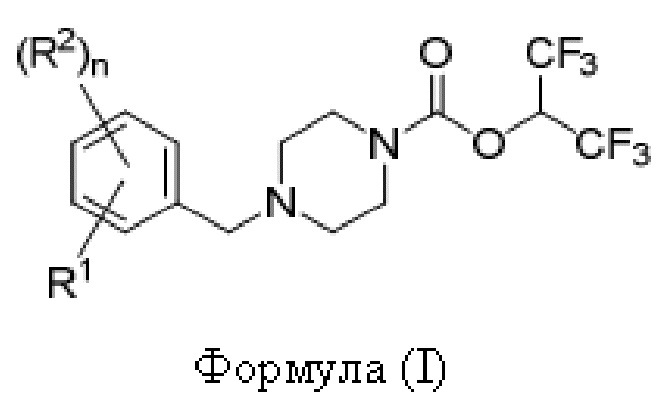
1. Соединение, характеризующееся структурой формулы (I):
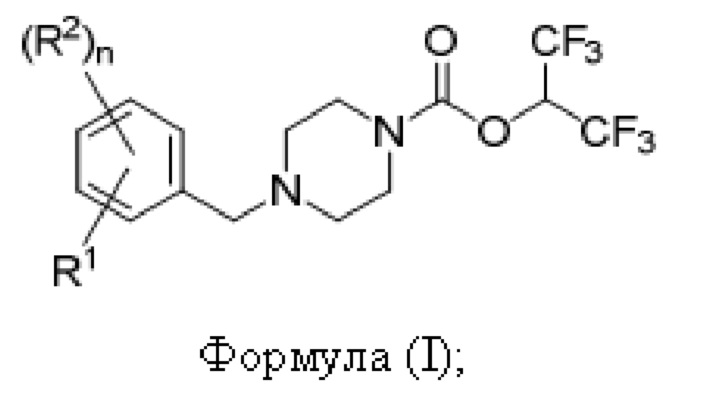
где:
R1 представляет собой -OR3;
каждый R2 независимо выбран из C1-6алкила, галогена и C1-6галогеналкила;
R3 представляет собой -(CR6R7)m-R8;
каждый R6 и R7 независимо выбран из Н; или R6 и R7 вместе с углеродом, к которому они присоединены, образуют С4-5циклоалкильное кольцо;
R8 представляет собой -C(O)OR9;
R9 представляет собой Н;
m представляет собой 1, 2, 3 или 4; и
n представляет собой 1 или 2;
или его фармацевтически приемлемая соль.
2. Соединение по п. 1 или его фармацевтически приемлемая соль, где m представляет собой 1, 2 или 3.
3. Соединение по любому из пп. 1, 2 или его фармацевтически приемлемая соль, где R6 и R7 вместе с углеродом, к которому они присоединены, образуют С4-5циклоалкильное кольцо.
4. Соединение по любому из пп. 1-3 или его фармацевтически приемлемая соль, где n представляет собой 1.
5. Соединение по любому из пп. 1-4 или его фармацевтически приемлемая соль, где R2 представляет собой -CF3.
6. Соединение по п. 1, характеризующееся структурой, выбранной из:

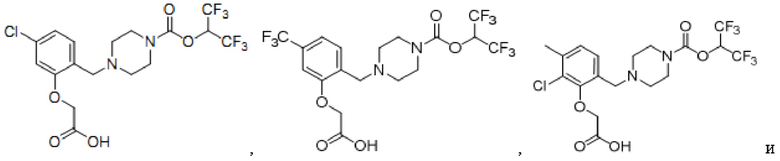
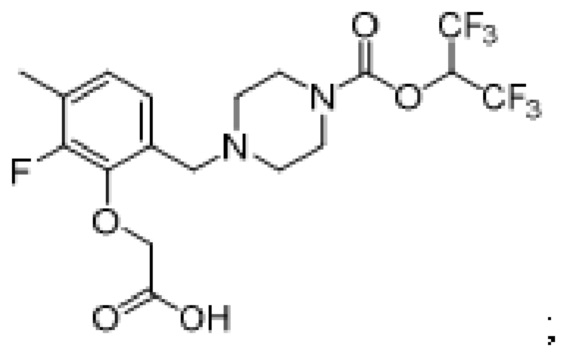
или его фармацевтически приемлемая соль.
| WO 2016149401 A2, 22.09.2016 | |||
| US 2015148330 A1, 28.05.2015 | |||
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ МОДУЛЯТОРОВ ПУТИ HEDGEHOG | 2007 |
|
RU2413718C2 |
Авторы
Даты
2021-09-03—Публикация
2017-11-15—Подача