Настоящее изобретение относится к антраниламидпиридинамидам избирательного действия в качестве ингибиторов VEGFR-2 и VEGFR-3, к их получению и применению в качестве лекарственных средств для лечения заболеваний, обусловленных персистирующим ангиогенезом.
Персистирующий ангиогенез (развитие кровеносных сосудов) может являться причиной различных заболеваний, таких как псориаз, артрит, например ревматоидный артрит, гемангиома, эндометриоз, ангиофиброма, глазные болезни, например диабетическая ретинопатия, неоваскулярная глаукома, заболевания почек, например гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбомикроангиопатия, отторжение трансплантата и гломерулопатия, фиброзные заболевания, например цирроз печени, заболевания, связанные с пролиферацией мезангиальных клеток, и артериосклероз, или может привести к прогрессированию этих заболеваний.
Персистирующий ангиогенез индуцируется фактором VEGF (васкулярный эндотелиальный фактор роста) через его рецептор. Для проявления фактором VEGF этого действия необходимо, чтобы VEGF связывался с рецептором и инициировал фосфорилирование тирозина.
Прямое или косвенное ингибирование VEGF-рецептора может использоваться для лечения подобных заболеваний и другого индуцируемого VEGF патологического ангиогенеза, а также расстройств, связанных с нарушением проницаемости сосудов, таких как васкуляризация опухолей. Так, например, известно, что с помощью растворимых рецепторов и антител к VEGF удается подавить рост опухолей.
Из заявки WO 00/27819 известны амиды антраниловой кислоты, которые применяются в качестве лекарственных средств для лечения псориаза, артрита, такого как ревматоидный артрит, гемангиомы, ангиофибромы, глазных болезней, таких как диабетическая ретинопатия, неоваскулярная глаукома, заболеваний почек, таких как гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбомикроангиопатия, отторжение трансплантата и гломерулопатия, фиброзных заболеваний, таких как цирроз печени, заболеваний, связанных с пролиферацией мезангиальных клеток, артериосклероза, повреждений нервной ткани, а также для ингибирования повторной окклюзии сосудов после лечения с использованием баллонных катетеров, при протезировании сосудов или после применения механических приспособлений, таких как стенты, для сохранения просвета (проходимости) сосудов.
Интенсивный ангиогенез является предпосылкой избыточного роста (разрастания) внематочного эндометрия при эндометриозе. Благодаря этому подавление ангиогенеза можно использовать также для терапии данной формы болезни, обусловливающей болезненные состояния и приводящей часто к бесплодию.
Известные соединения хотя, как правило, и эффективные при вышеназванных показаниях, тем не менее эта их эффективность сопровождается токсичностью и ухудшает переносимость медикамента. С учетом этого остается актуальной потребность, с одной стороны, в более эффективных, а с другой стороны, токсикологически более безвредных соединений, которые к тому же должны отличаться лучшей переносимостью.
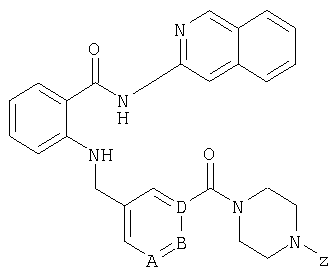
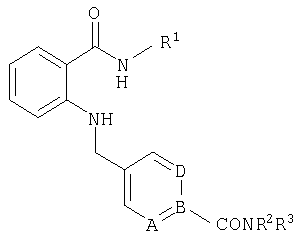
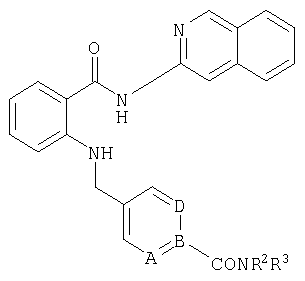
При создании изобретения было установлено, что указанные выше недостатки удается устранить благодаря соединениям общей формулы I
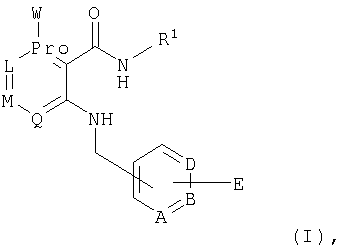
в которой
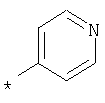
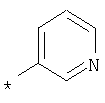
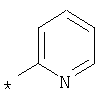
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, C1-С6алкоксигруппой, гало-C1-С6алкилом либо группой -OR5, -SR4, -SOR4 или -SO2R4 арил либо гетарил, или представляет собой группу -COOR8, -CONR2R3, -SR4, -SOR4, -SO2R4, -SCN, -PO(OR12)(OR13), -CH-CH-COR9 или -C≡C-R9,
G представляет собой атом азота или группу -С-Х,
L представляет собой атом азота или группу -С-Х,
М представляет собой атом азота или группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
при этом в кольце расположен максимум один атом азота,
Х представляет собой водород, галоген или незамещенный либо необязательно одно- или многозамещенный галогеном C1-С6алкил, C1-С6алкилоксигруппу или C1-С6-карбоксиалкил,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, аралкилоксигруппой, C1-С6алкилом и/или группой -NR2R3 разветвленный либо неразветвленный C1-С12алкил или C2-С12алкенил, или представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, C1-С6алкилом и/или группой -NR2R3 C3-С10циклоалкил либо C3-С10пиклоалкенил, или представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, гидроксигруппой, C1-С6алкилоксигруппой, C2-С6алкенилом, арил-C1-С6-алкилоксигруппой, аралкилоксигруппой, C1-С6алкилом, гало-C1-С6-алкилом либо группой =О, -SO2R4, -OR5, -R5 или -PO(OR12)(OR13) арил либо гетарил,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-C1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-ОР3, -SR4, -SOR4 или -SO2R4 C1-С6алкил, C3-С6циклоалкил, C3-С6циклоалкенил, арил либо гетарил или
R2 и R3 вместе с атомом азота образуют C3-С8кольцо, которое необязательно может содержать еще один атом азота, серы либо кислорода или может содержать группу -N(R10) и которое необязательно может быть идентично либо различно одно- или многозамещенным галогеном, цианогруппой, C1-С6алкилом, гало-C1-С6алкилом, арилом либо группой -OR5, -SR4, -SOR4 или -SO2R4,
R4 представляет собой гидроксигруппу, C1-С6алкил, арил, гетароарил или группу -NR2R3,
R5 представляет собой водород, C1-С12алкил, гало-C1-С6алкил, C3-С6циклоалкил либо гало-C3-С6циклоалкил или представляет собой C1-С12алкил, который может быть одно- либо многократно разорван кислородом, или
представляет собой группу -(CH2)2NR2R3, -CH2CN либо -CH2CF3,
R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил или
R6 и R7 вместе образуют 5-7-членное кольцо, которое может содержать атом кислорода либо серы или группу -N(R10)-,
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил, C1-С6алкоксигруппу, бензил, арил или гетарил,
R9 представляет собой водород, C1-С6алкил, три-C1-С6алкилсилил, арил, гетарил или группу -COR11,
R10 представляет собой водород, C1-С6алкил или арил,
R11 представляет собой водород, C1-С6алкил или группу -NR2R3, и
R12 и R13 независимо друг от друга представляют собой водород или C1-С6алкил, а также благодаря их изомерам, энантиомерам и солям.
Предлагаемые в изобретении соединения препятствуют фосфорилированию тирозина, соответственно подавляют персистирующий ангиогенез и тем самым останавливают рост и распространение опухолей, причем в первую очередь они отличаются меньшей степенью ингибирования изоформ цитохрома Р 450 (2С9 и 2С19).
Многие лекарственные средства расщепляются под действием этих изоформ. При ингибировании данных изоформ повышается уровень содержания указанных лекарственных средств в плазме, что может привести к нежелательным побочным эффектам.
Под алкилом имеется в виду соответственно прямоцепочечный либо разветвленный алкильный остаток, такой, например, как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, пентил, изопентил или гексил, гептил, октил, нонил, децил, ундецил и додецил.
Под алкоксигруппой имеется в виду соответственно прямоцепочечная либо разветвленная алкоксигруппа, такая, например, как метилокси, этилокси, пропилокси, изопропилокси, бутилокси, изобутилокси, втор-бутилокси, пентилокси, изопентилокси, гексилокси, гептилокси, октилокси, нонилокси, децилокси, ундецилокси или додецилокси.
Под циклоалкилом имеются в виду моноциклические алкильные кольца, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил или циклодецил, а также бициклические или трициклические кольца, такие, например, как адамантанил.
Под циклоалкенилом имеются в виду соответственно циклобутенил, циклопентенил, циклогексенил, циклогептенил, циклооктенил, циклононенил или циклодеценил, причем присоединение может происходить как по двойной, так и по простым (одинарным) связям.
Под галогеном имеется в виду соответственно фтор, хлор, бром или иод.
Под алкенилом имеется в виду соответственно прямоцепочечный либо разветвленный алкенильный остаток, содержащий 2-6, предпочтительно 2-4, С-атомов. В качестве примеров можно назвать следующие алкенильные остатки: винил, пропен-1-ил, пропен-2-ил, бут-1-ен-1-ил, бут-1-ен-2-ил, бут-2-ен-1-ил, бут-2-ен-2-ил, 2-метилпроп-2-ен-1-ил, 2-метилпроп-1-ен-1-ил, бут-1-ен-3-ил, бут-3-ен-1-ил и аллил.
Арильный остаток содержит соответственно 6-12 атомов углерода, и в качестве примеров можно назвать нафтил, бифенил и прежде всего фенил.
Гетероарильный остаток включает от 3 до 16 кольцевых атомов и вместо углерода может содержать в кольце один или более идентичных либо разных гетероатомов, таких как кислород, азот или сера, и может быть моно-, би- или трициклическим и дополнительно может быть соответственно сконденсирован с бензольным ядром.
В качестве примеров можно назвать тиенил, фуранил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, оксадиазолил, тиазолил, тиадиазолил и др. и их бензопроизводные, такие, например, как бензофуранил, бензотиенил, бензоксазолил, бензимидазолил, индазолил, индолил, изоиндолил и др., или пиридил, пиридазинил, пиримидинил, пиразинил, триазинил и др. и их бензопроизводные, такие, например, как хинолил, изохинолил и др., или азоцинил, индолизинил, пуринил и др. и их бензопроизводные, или циннолинил, фталазинил, хиназолинил, хиноксалинил, нафтиридинил, птеридинил, карбазолил, акридинил, феназинил, фенотиазинил, феноксазинил, ксантенил, оксепинил и др.
Арильный и гетероарильный остаток может быть соответственно идентично либо различно одно-, дву- или тризамещенным гидроксигруппой, галогеном, С1-С4алкоксигруппой, С1-С4алкилом или С1-С4алкилом, одно- либо многозамещенным в свою очередь галогеном.
При наличии кислотной функциональной группы в качестве солей пригодны физиологически совместимые соли органических и неорганических оснований, такие, например, как обладающие хорошей растворимостью соли щелочных и щелочноземельных металлов, а также N-метилглюкамин, диметилглюкамин, этилглюкамин, лизин, 1,6-гексадиамин, этаноламин, глюкозамин, саркозин, серинол, трисгидроксиметиламинометан, аминопропандиол, основание Совака (Sovak) и 1-амино-2,3,4-бутантриол.
При наличии же основной функциональной группы пригодными являются физиологически совместимые соли таких органических и неорганических кислот, как соляная кислота, серная кислота, фосфорная кислота, лимонная кислота, винная кислота, фумаровая кислота и др.
Предлагаемые в изобретении соединения общей формулы I могут быть представлены также в таутомерных формах и включают Е- либо Z-изомеры или, при наличии хирального центра, также рацематы и энантиомеры.
В качестве особенно эффективных зарекомендовали себя такие соединения общей формулы I, в которой
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, C1-С6алкоксигруппой, гало-C1-С6алкилом либо группой -OR5, -SR4, -SOR4 или -SO2R4 арил либо гетарил, или представляет собой группу -COOR8, -CONR2R3, -SR4, -SOR4, -SO2R4, -SCN, -PO(OR12)(OR13), -CH=CH-COR9 или -C≡C-R9,
G представляет собой атом азота или группу -С-Х,
L представляет собой атом азота или группу -С-Х,
М представляет собой атом азота или группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
при этом в кольце расположен максимум один атом азота,
Х представляет собой водород, галоген или незамещенный либо необязательно одно- или многозамещенный галогеном C1-С6алкил, C1-С6алкилоксигруппу или C1-С6-карбоксиалкил,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, гидроксигруппой, C1-С6алкилоксигруппой, C2-С6алкенилом, арил-C1-С6алкилоксигруппой, аралкилоксигруппой, C1-С6алкилом, гало-C1-С6алкилом либо группой =O, -SO2R4, -OR5, -R5 или -PO(OR12)(OR13) арил либо гетарил,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-C1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR5, -SR4, -SOR4 или -SO2R4 C1-С6алкил, C3-С6циклоалкил, C3-С6циклоалкенил, арил либо гетарил или
R2 и R3 вместе с атомом азота образуют C3-С8кольцо, которое необязательно может содержать еще один атом азота, серы либо кислорода или может содержать группу -N(R10) и которое необязательно может быть идентично либо различно одно- или многозамещенным галогеном, цианогруппой, C1-С6алкилом, гало-C1-С6алкилом, арилом либо группой -OR5, -SR4, -SOR4 или -SO2R4,
R4 представляет собой гидроксигруппу, C1-С6алкил, арил, гетароарил или группу -NR2R3,
R5 представляет собой водород, C1-С12алкил, гало-C1-С6алкил, C3-С6циклоалкил либо гало-C3-С6циклоалкил или представляет собой C1-С12алкил, который может быть одно- либо многократно разорван кислородом, или
представляет собой группу -(CH2)2NR2R3, -CH2CN либо -CH2CF3,
R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил или
R6 и R7 вместе образуют 5-7-членное кольцо, которое может содержать атом кислорода либо серы или группу -N(R10)-,
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил, C1-С6алкоксигруппу, бензил, арил или гетарил,
R9 представляет собой водород, C1-С6алкил, три-C1-С6алкилсилил, арил, гетарил или группу -COR11,
R10 представляет собой водород, C1-С6алкил или арил,
R11 представляет собой водород, C1-С6алкил или группу -NR2R3 и
R12 и R13 независимо друг от друга представляют собой водород или C1-С6алкил, а также их изомеры, энантиомеры и соли.
К особенно эффективным относятся далее такие соединения общей формулы I, в которой
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, C1-С6алкоксигруппой, гало-C1-С6алкилом либо группой -OR5, -SR4, -SOR4 или -SO2R4 арил либо гетарил, или представляет собой группу -COOR8, -CONR2R3, -SR4, -SOR4, -SO2R4, -SCN, -PO(OR12)(OR13), -CH=CH-COR9 или -C≡C-R9,
G представляет собой атом азота или группу -С-Х,
L представляет собой атом азота или группу -С-Х,
М представляет собой атом азота или группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
при этом в кольце расположен максимум один атом азота,
Х представляет собой водород или галоген,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, аралкилоксигруппой, C1-С6алкилом, гало-C1-С6алкилом либо группой -SO2R4, -OR5, -R5 или -PO(OR12)(OR13) арил либо гетарил,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-C1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR3, -SR4, -SOR4 или -SO2R4 C1-С6алкил, C3-С6циклоалкил, C3-С6циклоалкенил, арил либо гетарил или
R2 и R3 вместе с атомом азота образуют C3-С8кольцо, которое необязательно может содержать еще один атом азота, серы либо кислорода или может содержать группу -N(R10) и которое необязательно может быть идентично либо различно одно- или многозамещенным галогеном, цианогруппой, C1-С6алкилом, гало-C1-С6алкилом, арилом либо группой -OR5, -SR4, -SOR4 или -SO2R4,
R4 представляет собой гидроксигруппу или группу -NR2R3,
R5 представляет собой водород, C1-С12алкил или C1-С12алкил, который может быть одно- либо многократно разорван кислородом, или представляет собой группу -(CH2)2NR2R3, -CH2CN либо -СН2CF3,
R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил или
R6 и R7 вместе образуют 5-7-членное кольцо, которое может содержать атом кислорода либо серы или группу -N(R10)-,
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил, C1-С6алкоксигруппу, бензил, арил или гетарил,
R9 представляет собой водород, C1-С6алкил, три-C1-С6алкилсилил, арил, гетарил или группу -COR11,
R10 представляет собой водород, C1-С6алкил или арил,
R11 представляет собой водород, C1-С6алкил или группу -NR2R3 и
R12 и R13 независимо друг от друга представляют собой водород или C1-С6алкил, а также их изомеры, энантиомеры и соли.
Эффективными свойствами обладают также соединения общей формулы I, в которой
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, C1-С6алкоксигруппой, гало-C1-С6алкилом либо группой -OR5, -SR4, -SOR4 или -SO2R4 гетарил, или представляет собой группу -COOR8, -CONR2R3, -SR4, -SOR4, -SO2R4, -SCN, -PO(OR12)(OR13), -CH=CH-COR9 или -C≡C-R9,
G представляет собой группу -С-Х,
L представляет собой группу -С-Х,
М представляет собой группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
Х представляет собой водород или галоген,
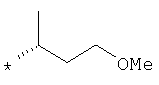
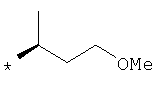
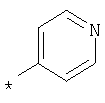
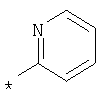
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, аралкилоксигруппой, C1-С6алкилом, гало-C1-С6алкилом либо группой -SO2R4, -OR5, -R5 или -PO(OR12)(OR13) фенил, тиофен, фуран, оксазол, тиазол, имидазол, пиразол, пиридин, пиримидин, триазин, хинолин, изохинолин или замещен по группе
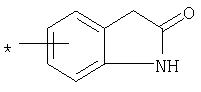 ,
, 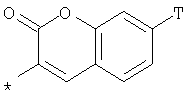 ,
,
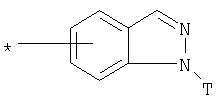 или
или 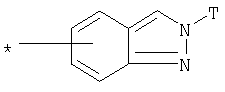
в которой Т обозначает водород, C1-С6алкил или C1-С6алкоксигруппу,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-C1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR5, -SR4, -SOR4 или -SO2R4 C1-С6алкил, C3-С6циклоалкил, C3-С6циклоалкенил, арил либо гетарил или
R2 и R3 вместе с атомом азота образуют C3-С8кольцо, которое необязательно может содержать еще один атом азота, серы либо кислорода или может содержать группу -N(R10) и которое необязательно может быть идентично либо различно одно- или многозамещенным галогеном, цианогруппой, C1-С6алкилом, гало-C1-С6алкилом, арилом либо группой -OR5, -SR4, -SOR4 или -SO2R4,
R4 представляет собой гидроксигруппу или группу -NR2R3,
R5 представляет собой водород, C1-С12алкил, гало-C1-С6алкил, C3-С6циклоалкил либо гало-C3-С6циклоалкил или представляет собой C1-С12алкил, который может быть одно- либо многократно разорван кислородом, или представляет собой группу -(CH2)2NR2R3, -CH2CN либо -СН2CF3,
R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил или
R6 и R7 вместе образуют 5-7-членное кольцо, которое может содержать атом кислорода либо серы или группу -N(R10)-,
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил, C1-С6алкоксигруппу, бензил, арил или гетарил,
R9 представляет собой водород, C1-С6алкил или три-C1-С6алкилсилил и
R12 и R13 независимо друг от друга представляют собой водород или C1-С6алкил, а также их изомеры, энантиомеры и соли.
Исключительными по своей эффективности свойствами отличаются такие соединения общей формулы I, в которой
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой тиенил, пиридил либо группу -COOR8, -CONR2R3 или -C≡C-R9
G представляет собой группу -С-Х,
L представляет собой группу -С-Х,
М представляет собой группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
Х представляет собой водород или галоген,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, аралкилоксигруппой, C1-С6алкилом, гало-C1-С6алкилом либо группой -SO2R4, -OR5, -R5 или -PO(OR12)(OR13) фенил, тиофен, фуран, оксазол, тиазол, имидазол, пиразол, пиридин, пиримидин, триазин, хинолин, изохинолин или замещен по группе
 ,
,  ,
,
 или
или 
в которой Т обозначает водород, C1-С6алкил или C1-С6алкоксигруппу,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, C1-С6алкилом, фенилом либо группой -NR6R7, -OR5 или C1-С6алкил-OR5 C1-С6алкил, C3-С6циклоалкил, фенил либо пиридил или
R2 и R3 вместе с атомом азота образуют C3-С8кольцо, которое необязательно может содержать еще один атом азота либо кислорода и которое необязательно может быть идентично либо различно одно- или многозамещенным C1-С6алкилом,
R4 представляет собой гидроксигруппу или группу -NR2R3,
R5, R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил или
R6 и R7 вместе образуют 5-7-членное кольцо, которое может содержать атом кислорода или серы,
R8 представляет собой водород, C1-С6алкил или бензил,
R9 представляет собой водород, C1-С6алкил или три-C1-С6алкилсилил и
R12 и R13 независимо друг от друга представляют собой водород или C1-С6алкил, а также их изомеры и соли.
Предлагаемые в изобретении соединения, равно как и их физиологически совместимые соли препятствуют фосфорилированию тирозина, соответственно подавляют персистирующий ангиогенез и тем самым останавливают рост и распространение опухолей, причем в первую очередь они отличаются меньшей степенью ингибирования изоформ цитохрома Р 450 (2С9 и 2С19). Поэтому лечение с использованием соединений по изобретению можно проводить без риска и в тех случаях, когда одновременно применяются дополнительные ("сопровождающие") лекарственные средства, расщепляемые под действием указанных изоформ.
Соединения формулы I равно как и их физиологически совместимые соли благодаря их ингибирующей активности по отношению к фосфорилированию VEGF-рецептора могут применяться в качестве лекарственных средств. Профиль их действия позволяет применять предлагаемые в изобретении соединения для лечения заболеваний, обусловленных или стимулируемых персистирующим ангиогенезом.
Поскольку соединения формулы I идентифицируются как ингибиторы тирозинкиназ VEGFR-1 и VEGFR-2, они пригодны прежде всего для лечения таких болезней, которые обусловлены или развитию которых способствует инициированный через VEGF-рецептор персистирующий ангиогенез или повышение проницаемости сосудов.
Объектом настоящего изобретения является также применение предлагаемых в нем соединений в качестве ингибиторов тирозинкиназ VEGFR-1 и VEGFR-2, соответственно KDR и FLT.
Объектом настоящего изобретения в соответствии с этим являются также лекарственные средства для лечения опухолей и применение таких средств.
Предлагаемые в изобретении соединения могут применяться либо индивидуально, либо в составе соответствующей композиции в качестве лекарственных средств для лечения псориаза, саркомы Капоши, рестеноза, такого, например, как рестеноз, индуцированный стентами, эндометриоза, болезни Крона, болезни Ходжкина, лейкемии, артрита, такого как ревматоидный артрит, гемангиомы, ангиофибромы, глазных болезней, таких как диабетическая ретинопатия, неоваскулярная глаукома, заболеваний почек, таких как гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбоангиопатия, отторжение трансплантата и гломерулопатия, фиброзных заболеваний, таких как цирроз печени, заболеваний, связанных с пролиферацией мезангиальных клеток, артериосклероза, повреждений нервной ткани и для торможения повторной окклюзии сосудов после лечения с использованием баллонных катетеров, при протезировании сосудов или после применения механических приспособлений, таких, например, как стенты, для сохранения проходимости (просвета) сосудов, в качестве иммуносупрессоров, в качестве вспомогательных средств, способствующих безрубцовому заживлению ран, при старческих пятнах и при контактном дерматите.
При лечении повреждений нервной ткани с использованием соединений по изобретению удается предотвратить быстрое рубцевание в поврежденных местах, т.е. рубцевание удается предотвратить до того момента, когда аксоны восстановят взаимосвязь друг с другом. Это, как очевидно, облегчает восстановление нервных путей и связей.
С помощью предлагаемых в изобретении соединений можно подавить, кроме того, образование асцита у пациентов. В равной степени с их помощью удается подавить отеки, обусловленные фактором VEGF.
Лимфоангиогенез играет важную роль при лимфогенном метастазировании (см. Т.Karpanen и др., Cancere Res. за 1 марта 2001, 61 (5), cc.1786-1790, Т.Veikkola и др., EMBO J. за 15 марта 2001, 20 (6), cc.1223-1231).
Предлагаемые в изобретении соединения также исключительно высокоэффективны в качестве ингибиторов VEGFR-киназы 3 и благодаря этому могут успешно применяться в качестве активных ингибиторов лимфоангиогенеза. Лечение с использованием соединений по изобретению позволяет не только снизить разрастание метастаз, но и уменьшить их число.
Предлагаемые в изобретении соединения проявляют свою эффективность и при заболеваниях, которые связаны с чрезмерным лимфоангиогенезом и которые относят по этой причине к синдрому лимфоангиогиперплазии и -дисплазии.
Лекарственные средства такого типа, содержащие их композиции и их применение также являются объектом настоящего изобретения.
В соответствии с этим изобретение относится далее к применению соединений общей формулы I для получения лекарственного средства, соответственно к применению этого лекарственного средства для лечения псориаза, саркомы Капоши, рестеноза, такого, например, как рестеноз, индуцированный стентами, эндометриоза, болезни Крона, болезни Ходжкина, лейкемии, артрита, такого как ревматоидный артрит, гемангиомы, ангиофибромы, глазных болезней, таких как диабетическая ретинопатия, неоваскулярная глаукома, заболеваний почек, таких как гломерулонефрит, диабетическая нефропатия, злокачественный нефросклероз, тромбоангиопатия, отторжение трансплантата и гломерулопатия, фиброзных заболеваний, таких как цирроз печени, заболеваний, связанных с пролиферацией мезангиальных клеток, артериосклероза, повреждений нервной ткани и для торможения повторной окклюзии сосудов после лечения с использованием баллонных катетеров, при протезировании сосудов или после применения механических приспособлений, таких, например, как стенты, для сохранения проходимости (просвета) сосудов, в качестве иммуносупрессоров, в качестве вспомогательных средств, способствующих безрубцовому заживлению ран, при старческих пятнах и при контактном дерматите.
Кроме того, с помощью предлагаемых в изобретении соединений можно, как указывалось выше, подавить образование асцита у пациентов. В равной мере с их помощью удается подавить отеки, обусловленные фактором VEGF.
Для применения соединений формулы I в качестве лекарственного средства их переводят в соответствующую лекарственную форму, т.е. изготавливают фармацевтический препарат, содержащий наряду с действующим веществом для энтерального или парентерального применения пригодные для таких целей фармацевтические органические или неорганические инертные наполнители, такие, например, как вода, желатин, гуммиарабик, лактоза, крахмал, стеарат магния, тальк, масла растительного происхождения, полиалкиленгликоли и т.п. Фармацевтические препараты могут выпускаться в твердой форме, например в виде таблеток, драже, суппозиториев, капсул, либо в жидкой форме, например в виде растворов, суспензий или эмульсий. При необходимости в их состав могут включаться, кроме того, вспомогательные вещества, такие как консерванты, стабилизаторы, смачиватели или эмульгаторы, соли для изменения осмотического давления или буферы.
Для парентерального применения пригодны прежде всего растворы для инъекции или суспензии, в первую очередь водные растворы активных соединений в полигидроксиэтоксилированном касторовом масле.
В качестве систем-носителей могут использоваться также поверхностно-активные вспомогательные вещества, такие как соли желчных кислот или фосфолипиды животного либо растительного происхождения, равно как и их смеси, а также липосомы или их компоненты.
Для перорального применения пригодны прежде всего таблетки, драже или капсулы с тальком и/или углеводородным наполнителем либо связующим, таким, например, как лактоза, кукурузный или картофельный крахмал. Возможно также применение и жидких лекарственных форм, таких, например, как микстура, к которой при необходимости добавляют подслащивающее вещество или одно либо несколько вкусовых веществ.
Дозировку действующих веществ можно варьировать в зависимости от методики введения лекарственных средств, возраста и веса пациента, типа и степени тяжести конкретного заболевания и тому подобных факторов. Суточная доза составляет от 0,5 до 1000 мг, предпочтительно от 50 до 200 мг, причем эта доза может назначаться для одноразового приема или ее можно разделять на две и более суточных дозы.
Вышеописанные композиции и лекарственные формы также являются объектом настоящего изобретения.
Предлагаемые в изобретении соединения получают в принципе по известным методам. Так, например, для получения соединений общей формулы I соединение общей формулы II
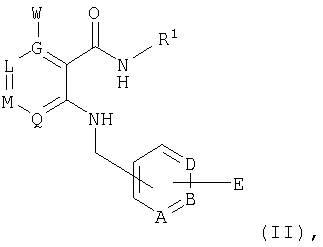
в которой А, В, D, G, L, M, Q, W и R1 имеют значения, указанные для общей формулы I, a E представляет собой СООН-группу карбоновой кислоты, подвергают по известным из литературы методам в соответствующем растворителе и соответствующем органическом основании взаимодействию с амином общей формулы III
 ,
,
где R8 и R9 имеют значения, указанные в общей формулы I, либо, если Е представляет собой нитрильную группу, нитрил омыляют с образованием амида, или соединение общей формулы IV
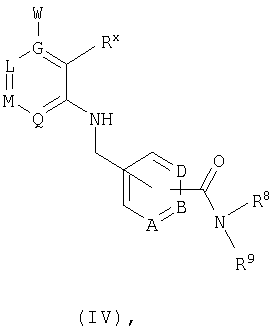
в которой А, В, D, G, L, M, Q, W, R8 и R9 имеют значения, указанные для общей формулы I, a Rx обозначает сложноэфирную либо кислотную группу, переводят в соответствующий амид.
Процесс образования амида проводят по методам, известным из литературы. Так, например, для образования амида можно исходить из соответствующего сложного эфира. Этот сложный эфир согласно описанной в Journ. Org. Chem. (1995), с.8414, методике подвергают взаимодействию с алюминийтриметилом и соответствующим амином в растворителях, таких как толуол, при температурах в интервале от 0°С до температуры кипения используемого растворителя. При наличии в молекуле двух сложноэфирных групп обе эти группы переводят в один и тот же амид. Вместо алюминийтриметила может использоваться также гексаметилдисилазид натрия.
Для образования амида, кроме вышеназванных, могут использоваться все методы, известные из химии пептидов. Так, в частности, соответствующую кислоту в апротонных полярных растворителях, таких как диметилформамид, через активированное производное кислоты, получаемое, например, с помощью гидроксибензотриазола и карбодиимида, такого как диизопропилкарбодиимид, или же с помощью предварительно образованных реагентов, таких как ГАТУ (Chem. Comm. (1994), с.201) или БТУ, при температурах в интервале от 0°С до температуры кипения используемого растворителя, предпочтительно при 80°С, подвергают взаимодействию с амином. Для образования амида пригоден также метод с использованием смешанного ангидрида кислоты, имидазолида или азида.
Нитрилы с помощью известных из литературы методов можно омылять с получением в результате амидов. Высокоэффективной является обменная реакция, описанная в Synthesis (1989), с.949, с использованием карбоната калия и пероксида водорода в апротонном полярном растворителе, таком как диметилсульфоксид, предпочтительно при комнатной температуре.
Еще одна возможность получать предлагаемые в изобретении соединения общей формулы I состоит в том, что соединение общей формулы IIa
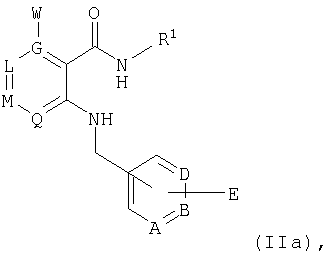
в которой А, В, D, G, L, М, Q, W и R1 имеют значения, указанные для общей формулы I, a E представляет собой галоген или O-сульфонат, такой, например, как атом хлора, брома либо иода, O-трифторметансульфонат или O-метилсульфонат,
а) подвергают взаимодействию с соответствующим образом замещенными концевыми алкенами по реакции Хекка (см. "Palladium Reagents in Organic Syntheses", изд-во Academic Press (1985), New York, c.179 и далее) или с винилбороновыми кислотами либо эфирами винилбороновых кислот по реакции Сузуки (см. Tetrahedron Lett. 39 (1983), cc.3271 и далее) или с винилстаннанами по реакции Штилле (см. Pure & Appl. Chem. 57 (1985), с.1771), или
б) подвергают реакции сочетания с любым образом замещенными концевыми алкинами, например по методу Стефена-Кастро (см. Journ. Org. Chem. 28 (1963), cc.3313 и далее) либо при катализе палладием по методу Соногашира (см. "Comprehensive Organic Synthesis: Carbon-Carbon σ-Bond Formation", изд-во Pergamon Press (1991), Oxford UK, том 3, cc.551 и далее), или
в) подвергают реакции сочетания с арил- и гетарилборными кислотами либо их эфирами по методу Сузуки (см. Acc.Chem.Res. 63 (1991), cc.419 и далее, или Journ. Am. Soc. 122 (2000), cc.4020 и далее), либо с арил- и гетарилстаннанами по методу Штилле (см. Angew. Chem. 98 (1986), cc.504 и далее, или Angew. Chem. Int. Ed. (международное издание) 38 (1999), cc.2411 и далее), либо с арильными и гетарильными соединениями Гриньяра или аналогичными цинкорганическими производными по методу Негиши (см. "Metal-catalyzed Cross-coupling Reaction", под ред. Diederich/Stang, изд-во Wiley-VCH (1998), New York, глава 1, или Journ. Am. Soc. 123 (2001), cc.2719 и далее), или
г) переводят путем катализированного палладием карбонилирования в атмосфере моноксида углерода при давлении от 1 до 20 бар в диметилформамиде в присутствии соответствующего спирта (см. "Palladium Reagents in Organic Syntheses", изд-во Academic Press (1985), New York, cc.352 и далее или Synth. Comm. 27 (1997), cc.515 и далее) в соответствующий эфир карбоновой кислоты, или
д) переводят путем катализированного палладием карбонилирования в атмосфере моноксида углерода при давлении от 1 до 20 бар в смесях диметилформамида и воды в соответствующую карбоновую кислоту (см. Journ. Org. Chem. 46 (1981), cc.4614 и далее); карбоновые кислоты можно также получать омылением соответствующих эфиров карбоновых кислот, или
е) подвергают катализированному палладием карбонилированию в атмосфере моноксида углерода при давлении от 1 до 20 бар в диметилформамиде в присутствии аминов с получением соответствующих амидов карбоновых кислот (см. "Palladium Reagents in Organic Syntheses", изд-во Academic Press (1985), New York, cc.352 и далее, Tetrahedron Lett. 23 (1982), cc.3383 и далее); синтез амидов карбоновых кислот можно также осуществлять исходя из эфиров карбоновых кислот, особенно эффективным в этих целях зарекомендовал себя метод Вайнреба (Weinreb) (см. Tetrahedron Lett. 17 (1977), cc.4171 и далее, Journ. Org., Chem. 60 (1995), cc.8414 и далее); амиды карбоновых кислот можно также синтезировать из получаемых в разделе д) карбоновых кислот, используя с этой целью в принципе все методы, известные из химии пептидов (см. Synthesis (1972), cc.453-463, или "Comprehensive Organic Transformations", изд-во Wiley-VCH (1989), New York, cc.972-976); так, например, соответствующую карбоновую кислоту можно подвергать в апротонных полярных растворителях, таких как диметилформамид, через активированное производное карбоновой кислоты, получаемое, например, за счет добавления карбонилдиимидазола, при температурах в интервале от 0 до 120°С, предпочтительно при комнатной температуре, взаимодействию с аминами, такими, в частности, как ГАТУ (см. Chem. Comm. (1994), с.201), или
ж) взаимодействием с тиоалкилами, -арилами и -гетарилами непосредственно, в присутствии оснований, таких, например, как гидрид калия либо трет-бутанолят калия, или переходных металлов, например медной стружки, хлорида либо бромида меди, или дихлорида палладия, в апротонных растворителях, таких, например, как диметилформамид, N-метилпирролидон, диметилсульфоксид или ксилол, при температурах в интервале от 20 до 200°С переводят в соответствующий сульфид; при этом может оказаться целесообразным проводить данную реакцию в микроволновой печи (см. Tetrahedron 39 (1983), cc.4153 и далее); 2-тиозамещенные пиридильные производные можно также без проблем получать из 2-пиридонового производного после тионилирования пентасульфидом фосфора (см. Bull. Soc. Chim. Fr. (1953), cc.1001 и далее) либо реагентом Лоуссона (см. Tetrahedron 40 (1984), cc.2047 и далее) и последующим алкилированием алкилгалогенидами, предпочтительно алкилиодидами (см. Journ. Org. Chem. 64 (1999), cc.7935-7939) либо алкилсульфонатами, предпочтительно алкилтрифторметилсульфонатами.
Далее возможны следующие варианты реакции:
з) оксидированием сульфидов обычными окислителями, такими, например, как пероксид водорода, периодат натрия, трет-бутоксигипохлорит, хлорит натрия, метахлорпербензойная кислота, трифторперуксусная кислота, диметилдиоксиран, аммонийнитрат церия или азотная кислота (см. "Oxidations in Organic Chemistry", изд-во ACS Washington (1990), cc.252-263), в растворителях, таких, например, как дихлорметан, дихлорэтан, хлороформ, тетрагидрофуран, ацетонитрил, диметилформамид, N-метилпирролидон, диметилсульфоксид, диметоксиэтан, диглим, тетраглим или вода, при температурах в интервале от 20°С до температуры кипения используемого растворителя могут быть получены соответствующие сульфоксиды. Полученные таким путем сульфоксиды можно далее оксидировать до соответствующих сульфонов; эта операция осуществляется, например, с помощью окислителей, таких как пероксид водорода, перманганат калия, перборат натрия или гидроперсульфат калия (см. Tetrahedron Lett. 22 (1981), cc.1287 и далее), в растворителях, таких, например, как дихлорметан, дихлорэтан, хлороформ, тетрагидрофуран, ацетонитрил, диметилформамид, N,N-диметилацетамид, диметилсульфоксид или вода, при температурах в интервале от 20°С до температуры кипения используемого растворителя. Обработка сульфидов избытком вышеназванных окислителей приводит непосредственно к соответствующим сульфонам (см. "The chemistry of sulphones and sulfoxides" в Patai, изд-во Wiley, New York (1988), cc.165-231).
и) оксидированием полученных в разделе ж) тиолов могут быть получены хлорсульфонаты, особенно эффективным при этом зарекомендовало себя оксидирование хлором в водной соляной кислоте (см. Journ. Org. Chem. 64 (1999), cc.5896-5903), либо тетрахлорметаном (см. Journ. Med. Chem. 43)2000), cc.843-858), либо гипохлоритом натрия в серной кислоте (см. Tetrahedron Asymm. 8 (1997), cc.3559-3562).
к) взаимодействием со смесью из роданида меди и роданида калия в полярно апротонных растворителях, таких, например, как ацетонитрил, диметилформамид, N,N-диметилацетамид, диметилсульфоксид, диглим, тетраглим или N-метилпирролидон, могут быть получены соответствующие тиоцианаты (см. Journ. Chem. Soc. Chem. Comm. (1989), cc.81 и далее). Из этих тиоцианатов в свою очередь путем оксидирования гипохлоритом можно получать соответствующие хлорангидриды сульфокислот.
л) взаимодействием указанных в разделе и) хлорсульфонатов с аминами в растворителях, таких, например, как дихлорметан, дихлорэтан, хлороформ, тетрагидрофуран, этилацетат, ацетонитрил, диметилформамид, N-метилпирролидон, N,N-диметилацетамид, диметоксиэтан или вода, при температурах в интервале от 0°С до температуры кипения используемого растворителя могут быть получены соответствующие сульфамиды (см. Tetrahedron 56 (2000), cc.8253-8262).
м) путем гидролиза полученных в разделе и) хлорсульфонатов в воде либо в водном щелоке при температурах в интервале от 5 до 100°С получают соответствующие сульфокислоты.
н) катализированным палладием взаимодействием с О,О-диалкилфосфитами в апротонных растворителях, таких, например, как диметилформамид, N-метилпирролидон, N,N-диметилацетамид, диметилсульфоксид или толуол, в присутствии основания, такого, например, как триэтиламин или диизопропилэтиламин, при температурах в интервале от 0°С до температуры кипения используемого растворителя, предпочтительно при 80°С, могут быть получены соответствующие фосфонаты (см. Bull. Chem. Soc. Jpn. 55 (1982), cc.909 и далее).
о) путем металлирования, например с помощью н-бутиллития, втор-бутиллития, трет-бутиллития, метиллития, диизопропиламида лития или этилмагнийбромида, в апротонных растворителях, таких как диэтиловый эфир, тетрагидрофуран или диоксан, при температурах в интервале от -100°С до 0°С, предпочтительно при -78°С в тетрагидрофуране, и реакцией с изоцианатами могут быть получены соответствующие амиды карбоновых кислот.
п) по реакции, аналогично описанной в разделе о), и улавливанием металлированных промежуточных продуктов эфиром хлормуравьиной кислоты могут быть получены соответствующие эфиры карбоновых кислот.
р) по реакции, аналогично описанной в разделе о), и улавливанием металлированных промежуточных продуктов диметилформамидом, этилформиатом либо N-формилморфолином могут быть получены соответствующие альдегиды.
с) по реакции, аналогично описанной в разделе о), и улавливанием металлированных промежуточных продуктов алкилгалогенидами либо алкилсульфонатами, предпочтительно алкилиодидами либо алкилтрифторметансульфонатами, могут быть получены соответствующие пиридилалкильные производные.
т) путем восстановления водородом в присутствии каталитических количеств палладия, никеля либо родия или солей этих металлов, например палладия на активированном угле, в полярно-протонных растворителей либо в смесях растворителей, таких, например, как метанол - ледяная уксусная кислота, полученные в разделе а) пиридилалкены и полученные в разделе б) пиридилалкины можно переводить в соответствующие пиридилалканы.
Последовательность проведения описанных стадий способа может во всех случаях варьироваться.
Получение предлагаемых в изобретении соединений
Ниже получение соединений по изобретению более подробно поясняется на примерах, которые не ограничивают его объем.
Пример 1
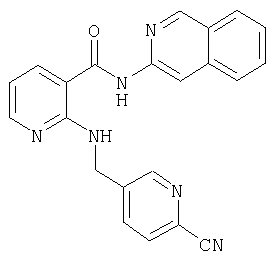
Получение пропиламида 5-{[2-(изохинолин-3-илкарбамоил)фенил-амино]метил}пиридин-2-карбоновой кислоты
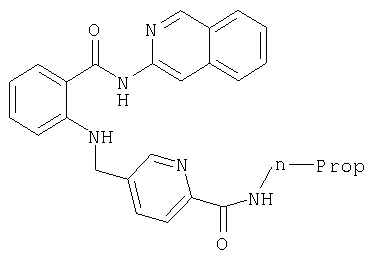
В 2,5 мл диметилформамида в атмосфере аргона и исключая доступ влаги вводят 50 мг (0,13 ммоля) 5-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты и 42 мг (0,26 ммоля) карбонилдиимидазола и в течение 30 мин перемешивают при комнатной температуре. Затем к этой смеси добавляют 15 мг (0,26 ммоля) н-пропиламина и в течение 12 ч продолжают перемешивание при комнатной температуре. После этого разбавляют водой до объема порядка 30 мл и трижды экстрагируют встряхиванием с этиловым эфиром уксусной кислоты его порциями по 20 мл. Собранную органическую фазу сушат, фильтруют и концентрируют, а остаток хроматографируют на колонке для экспресс-хроматографии (5 г материала Isolute flash silica, фирма Separtis) путем градиентного элюирования, начиная со 100%-ного гексана и заканчивая смесью гексана и этилового эфира уксусной кислоты в соотношении 50%:50%. В результате получают 45 мг (79% от теории) пропиламида 5-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты с молярным пиком в МС (масс-спектроскопии) m/e=439.
По аналогичной методике получают также соединения в представленных ниже примерах:
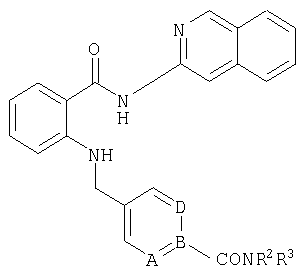
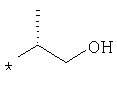
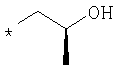
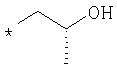
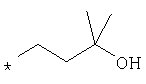
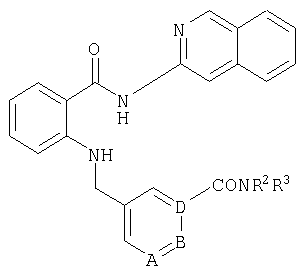
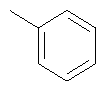
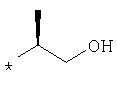



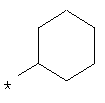
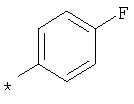
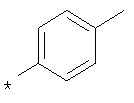
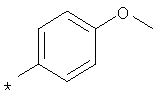
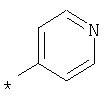
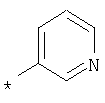

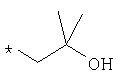
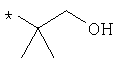
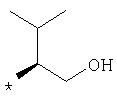
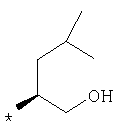
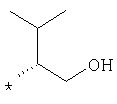
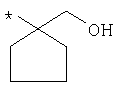
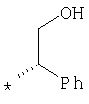
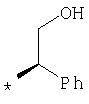
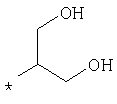
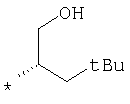
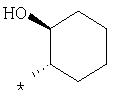
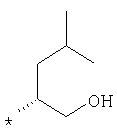
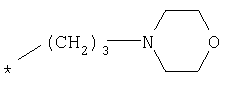
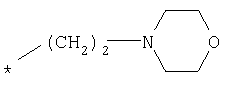
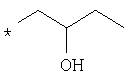
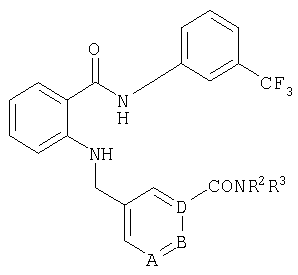




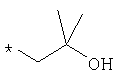
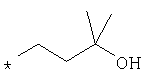
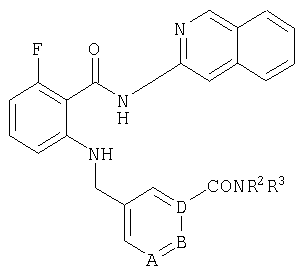




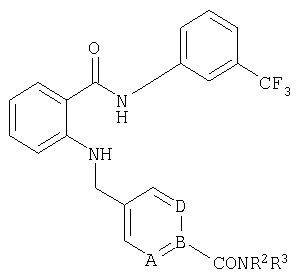
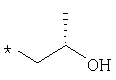
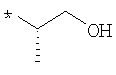
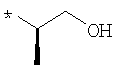





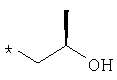
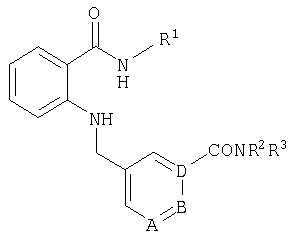
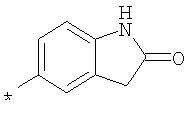













пик в МС (m/e)



































Пример 2.0
Получение пиридин-3-иламида 5-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
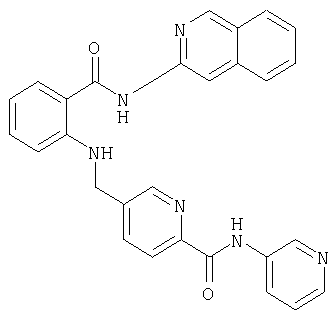
120 мг (0,3 ммоля) 5-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты растворяют в атмосфере аргона в 5 мл абсолютного диметилформамида, смешивают с 56 мг (0,6 ммоля) 3-аминопиридина, 76 мг (0,75 ммоля) N-метилморфолина и 136 мг (0,36 ммоля) гексафторфосфата O-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония (ГАТУ) и в течение 48 ч перемешивают при комнатной температуре. Затем концентрируют в вакууме и остаток хроматографируют на колонке для экспресс-хроматографии (5 г материала Isolute flash silica, фирма Sepostis) путем градиентного элюирования, используя в качестве элюента метиленхлорид:этанол в соотношении 100:0-95:5. В результате получают пиридин-3-иламида 5-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты.
МС (m/е 474).
По аналогичной методике получают также следующие соединения:
Пример 3.0
Получение амида 5-{[2-(2-оксо-2,3-дигидро-1Н-индол-5-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
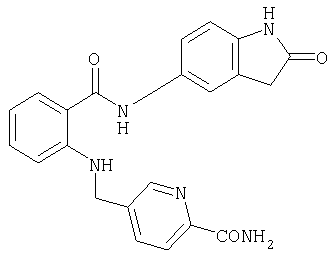
36 мг (0,09 ммоля) 2-[(6-цианопиридин-3-илметил)амино]-N-(2-оксо-2,3-дигидро-1Н-индол-5-ил)бензамида смешивают в 1 мл диметилсульфоксида с 30 мг (0,22 ммоля) карбоната калия и 0,05 мл (0,42 ммоля) пероксида водорода (30%-ного) и в течение 3,5 ч перемешивают при комнатной температуре. Затем разбавляют водой и экстрагируют этиловым эфиром уксусной кислоты.
Органическую фазу промывают, сушат, фильтруют и концентрируют. Остаток разделяют путем перемешивания с теплым метанолом. В результате получают 5 мг (11% от теории) амида 5-{[2-(2-оксо-2,3-дигидро-1Н-индол-5-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты.
По аналогичной методике получают также следующие соединения:
Пример 3.1
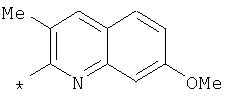
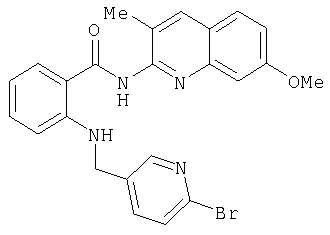
Амид 4-{[2-(7-метокси-3-метилхинолин-2-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
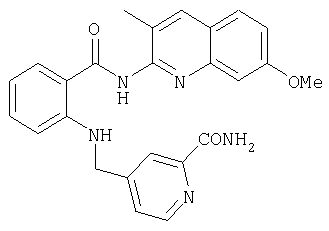
Пример 3.2
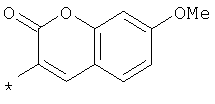
Амид 4-{[2-(7-метокси-2-оксо-2Н-хромен-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
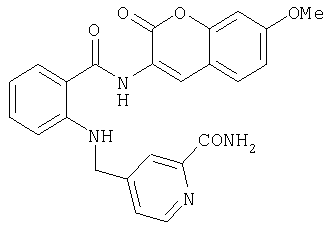
Пример 3.3
Амид 5-{[2-(7-метокси-2-оксо-2Н-хромен-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
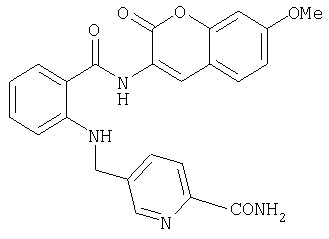
Пример 3.4
Амид 5-{[2-(7-метокси-3-метилхинолин-2-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
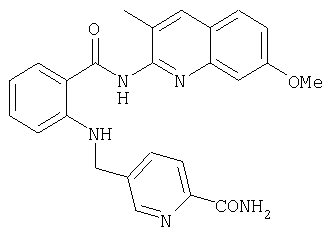
Пример 3.5
Амид 4-{[2-(изохинолин-3-илкарбамоил)-6-азафениламино]метил}пиридин-2-карбоновой кислоты
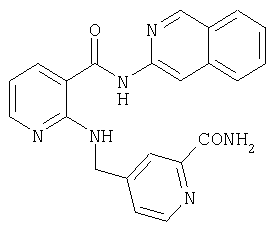
Пример 3.6
Амид 5-{[2-(2-оксо-2,3-дигидро-1Н-индол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
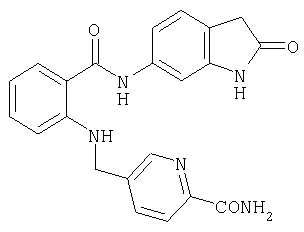
Пример 3.7
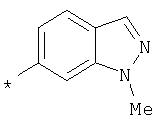
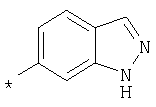
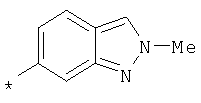
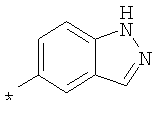
Амид 4-{[2-(2-метил-2Н-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
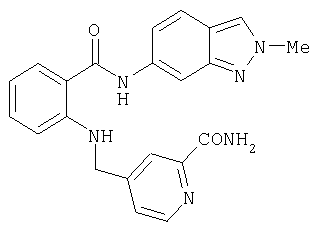
Пример 3.8
Амид 4-{[2-(1Н-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
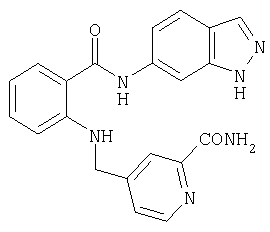
Пример 3.9
Амид 4-{[2-(1-метил-1Н-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
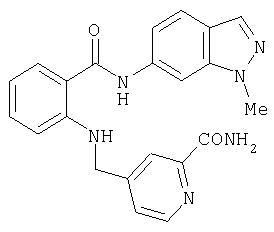
Пример 3.10
Амид 5-{[2-(изохинолин-3-илкарбамоил)-6-азафениламино]метил}пиридин-2-карбоновой кислоты
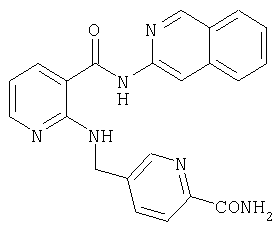
Пример 3.11
Амид 4-{[2-(2-оксо-2,3-дигидро-1Н-индол-5-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
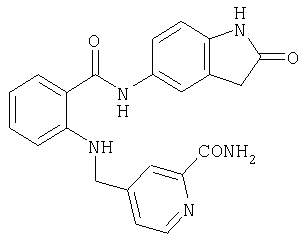
Пример 4.0
Получение N-трет-бутиламида 4-{[2-(изохинолин-3-илкарбамоил)-6-азафениламино]метил}пиридин-2-карбоновой кислоты
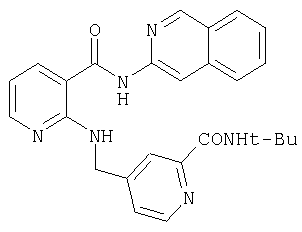
В 5 мл толуола в атмосфере защитного газа и исключая доступ влаги 72 мг (0,5 ммоля) 3-аминоизохинолина смешивают с 0,25 мл триметилалюминия (0,5 ммоля, 2-молярного в толуоле) и в течение 30 мин перемешивают при комнатной температуре. Затем добавляют 120 мг (0,45 ммоля) метилового эфира 2-[(2-трет-бутилкарбамоилпиридин-4-илметил)амино]никотиновой кислоты и в течение 2 ч нагревают до 120°С. После охлаждения смешивают с 30 мл разбавленного раствора гидрокарбоната натрия и трижды экстрагируют этиловым эфиром уксусной кислоты его порциями по 30 мл. Собранную уксусноэфирную фазу промывают водой, сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле, используя в качестве элюента метиленхлорид: этанол в соотношении 95:5. После повторной хроматографии на силикагеле, используя в качестве элюента гексан: этиловый эфир уксусной кислоты в соотношении 1:1, получают 70 мг (30% от теории) N-трет-бутиламида 4-{[2-(изохинолин-3-илкарбамоил)-6-азафениламино]метил}пиридин-2-карбоновой кислоты с температурой плавления 201°С.
Пример 5.0
Получение (2-гидроксипропил)амида 4-{[2-(изохинолин-3-илкарбамоил)-6-азафениламино]метил}пиридин-2-карбоновой кислоты
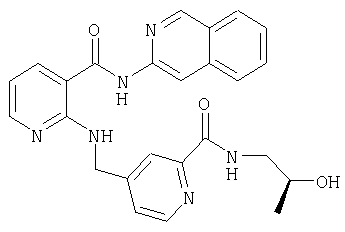
283 мг (1 ммоль) 2-хлор-N-изохинолин-3-илникотинамида смешивают в 5 мл пиридина с примерно 1,66 ммоля (2-гидроксипропил)амида 4-аминометилпиридин-2-карбоновой кислоты и в течение 2 ч нагревают до 100°С. После концентрирования растворяют в воде и трижды экстрагируют встряхиванием с этиловым эфиром уксусной кислоты его порциями по 30 мл. Собранную органическую фазу промывают водой, сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле, используя в качестве элюента метиленхлорид: ацетон в соотношении 1:1. В результате получают 40 мг (9% от теории) (2-гидроксипропил)амида 4-{[2-(изохинолин-3-илкарбамоил)-6-азафениламино]метил}пиридин-2-карбоновой кислоты в виде смолы.
Пример 6.0
Получение амида N-(изохинолин-3-ил)-2-[3-(пиридин-3-ил)пиридин-4-илметиламино]бензойной кислоты
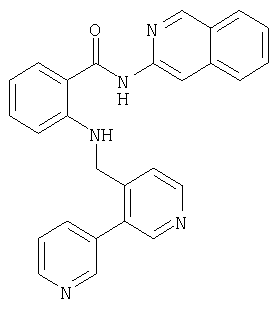
94 мг (0,22 ммоля) амида N-(изохинолин-3-ил)-2-[3-бромпиридин-4-илметиламино]бензойной кислоты последовательно смешивают в 3,7 мл толуола с 0,73 мл этанола, 0,36 мл 2-молярного раствора карбоната натрия, 6 мг палладий(0)тетракистрифенилфосфина и 32 мг пиридин-3-бороновой кислоты и в течение 6,5 ч нагревают до температуры бани 120°С. Затем водой разбавляют до объема 25 мл и трижды экстрагируют этиловым эфиром уксусной кислоты его порциями по 25 мл. Собранную уксусноэфирную фазу сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле с использованием в качестве элюента метиленхлорида и этанола в соотношении 10:1. В результате получают 45 мг (47% от теории) амида N-(изохинолин-3-ил)-2-[3-(пиридин-3-ил)пиридин-4-илметиламино]бензойной кислоты в виде смолы.
1H-ЯМР (d6-ДМСО): 10,68 (s, 1Н), 9,21 (s, 1H), 8,72 (s, 1H), 8,64 (d, J=3,8, 1H), 8,57 (d, J=5,1, 1H), 8,54 (s, 1H), 8,48 (s, 1H), 8,11-7,94 (m, 4H), 7,85 (d, J=7,6, 1H), 7,74 (t, J≈7,3, 1H), 7,59-7,47 (m, 3H), 7,23 (t, J≈7,5, 1H), 6,63 (t, J=7,5, 1H), 6,39 (d, J=8,3, 1H), 4,45 (d, J=5,0, 2H).
MC (CI-NH3): 432 (80%, [M+H]+).
Пример 6.1
Получение амида N-(изохинолин-3-ил)-2-[3-(тиен-3-ил)пиридин-4-илметиламино]бензойной кислоты
По аналогичной методике получают также амид N-(изохинолин-3-ил)-2-[3-(тиен-3-ил)пиридин-4-илметиламино]бензойной кислоты
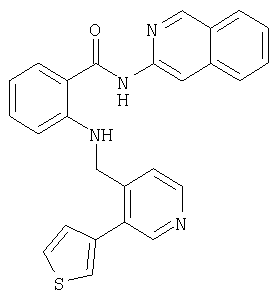
MC (CI-NH3): 437 (100%, [M+H]+).
Пример 6.2
Получение амида N-(изохинолин-3-ил)-2-[2-аминокарбонилпиридин-4-илметиламино]бензойной кислоты
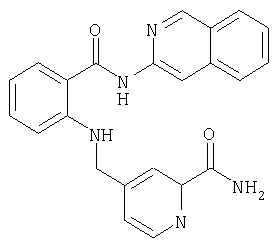
130 мг (0,34 ммоля) амида N-(изохинолин-3-ил)-2-[2-цианопиридин-4-илметиламино]бензойной кислоты смешивают в 2,5 мл диметилсульфоксида со 126 мг карбоната калия и 0,25 мл пероксида водорода (30%-ного) и в течение 1 ч перемешивают при комнатной температуре. Затем смешивают с водой и выпавший в осадок продукт отделяют вакуум-фильтрацией. Остаток размешивают в смеси из метиленхлорида и этанола и отделяют вакуум-фильтрацией. В результате получают 96 мг (71% от теории) амида N-(изохинолин-3-ил)-2-[2-аминокарбонилпиридин-4-илметиламино]бензойной кислоты с температурой плавления 200°С.
1H-ЯМР (d6-ДМСО): 10,73 (s, 1Н), 9,22 (s, 1H), 8,60 (s, 1H), 8,56 (d, J=4,7, 1H), 8,25 (шир.s, 1H), 8,10-8,04 (m, 3H), 7,95 (d, J=8,0, 1H), 7,88 (d, J=6,9, 1H), 7,74 (t, J≈7,4, 1H), 7,63-7,57 (m, 3H), 7,25 (t, J≈7,0, 1H), 6,64 (t, J≈7,5, 1H), 6,54 (d, J=8,4, 1H), 4,62 (шир.d, J=5,5, 2H).
MC (EI): 397 (38%, [M]+).
Пример 6.3
Получение амида N-(изохинолин-3-ил)-2-[(2-аминокарбонилпиридин-5-ил)метиламино]бензойной кислоты
По аналогичной методике получают также амид N-(изохинолин-3-ил)-2-[(2-аминокарбонилпиридин-5-ил)метиламино]бензойной кислоты
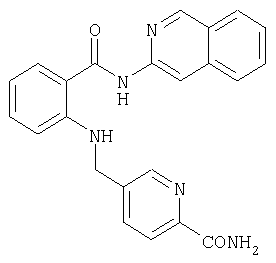
MC (ESI): 398 (78%, [М+Н]+).
Пример 6.4
Получение амида N-(изохинолин-3-ил)-2-[(2-метоксикарбонилпиридин-4-ил)метиламино]бензойной кислоты
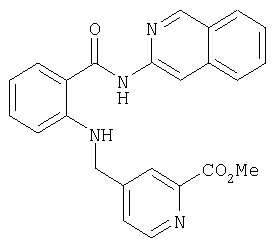
20 мг (0,05 ммоля) амида N-(изохинолин-3-ил)-2-[2-бромпиридин-4-илметиламино]бензойной кислоты, 1,6 мг (0,003 ммоля) бис(дифенилфосфин)ферроцена (ДФФФ), 0,35 мг (0,0015 ммоля) ацетата палладия(II), 14 мкл (0,1 ммоля) триэтиламина суспендируют в смеси из 1 мл метанола и 1 мл диметилформамида и в течение 5 ч перемешивают в автоклаве в атмосфере СО (3 бара) при 50°С. Затем реакционную смесь фильтруют через мембранный фильтр, концентрируют и в завершение хроматографируют на силикагеле, используя в качестве элюента гексан: EtOAc в соотношении 3:7. В результате получают 12 мг (58% от теории) амида N-(изохинолин-3-ил)-2-[(2-метоксикарбонилпиридин-4-ил)метиламино]бензойной кислоты.
1H-ЯМР (CDCl3): 9,12 (шир.s, 1H), 8,94 (s, 1Н), 8,67 (s, 1H), 8,61 (d, J=5,1, 1H), 8,36 (шир.s, 1H), 8,09 (s, 1H), 7,87 (d, J=8,5, 1H), 7,81 (d, J=8,5, 1H), 7,71 (d, J=7,7, 1H), 7,64 (t, J≈7,8, 1H), 7,49-7,44 (m, 2H), 7,24-7,19 (m, 1H), 6,68 (t, J≈7,8, 1H), 6,42 (d, J=8,0, 1H), 4,50 (шир.s, 2H), 3,93 (s, 3H).
MC (ESI): 413 (100%, [M+H]+).
Пример 6.5
Получение амида N-(изохинолин-3-ил)-2-[(2-бензилоксикарбонилпиридин-4-ил)метиламино]бензойной кислоты
По аналогичной методике получают также амид N-(изохинолин-3-ил)-2-[(2-бензилоксикарбонилпиридин-4-ил)метиламино]бензойной кислоты
1H-ЯМР (CDCl3): 9,00 (s, 1H), 8,76 (шир.s, 1H), 8,68 (d, J=5,0, 1H), 8,66 (s, 1H), 8,39 (t, J≈6,1, 1H), 8,14 (s, 1H), 7,91 (d, J=7,9, 1H), 7,85 (d, J=8,0, 1H), 7,69-7,62 (m, 2H), 7,53-7,46 (m, 4H), 7,38-7,25 (m, 4H), 6,73 (t, J≈7,2, 1H), 6,48 (d, J=7,8, 1H), 5,44 (s, 2H), 4,56 (d, J=6,0, 2H).
MC (CI-NH3): 489 (85%, [M+H]+).
Пример 6.6
Получение амида N-(изохинолин-3-ил)-2-[(2-гидроксикарбонилпиридин-4-ил)метиламино]бензойной кислоты
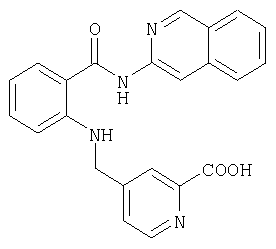
а) 20 мг (0,05 ммоля) амида N-(изохинолин-3-ил)-2-[(2-метоксикарбонилпиридин-4-ил)метиламино]бензойной кислоты смешивают в смеси из 1 мл тетрагидрофурана и 1 мл метанола с 10,2 мг (0,25 ммоля) гидроксида лития в воде и в течение 4 ч перемешивают при 22°С. Затем реакционную смесь фильтруют через мембранный фильтр, концентрируют и хроматографируют на силикагеле, используя в качестве элюента толуол, уксусную кислоту и воду в соотношении 10:10:1. В результате получают 14 мг (69% от теории) амида N-(изохинолин-3-ил)-2-[(2-гидроксикарбонилпиридин-4-ил)метиламино]бензойной кислоты.
б) 433 мг (1 ммоль) амида N-(изохинолин-3-ил)-2-[(2-бромпиридин-4-ил)метиламино]бензойной кислоты, 50 мг (0,09 ммоля) бис(дифенилфосфин)ферроцена (ДФФФ), 10 мг (0,045 ммоля) ацетата палладия(II), 280 мкл (2 ммоля) триэтиламина суспендируют в смеси из 5 мл воды и 10 мл диметилформамида и в течение 5 ч перемешивают в автоклаве в атмосфере СО (3 бара) при 50°С. Затем реакционную смесь фильтруют через мембранный фильтр, концентрируют, растворяют в дихлорметане, смешивают с активированным углем, нагревают, фильтруют и концентрируют. Полученное твердое вещество перекристаллизовывают из дихлорметана. В результате получают 283 мг (71% от теории) амида N-(изохинолин-3-ил)-2-[(2-гидроксикарбонилпиридин-4-ил)метиламино]бензойной кислоты.
1H-ЯМР (d6-DMSO): 10,73 (s, 1H), 9,22 (s, 1H), 8,63 (d, J=4,9, 1H), 8,60 (s, 1H), 8,22 (шир.t, J≈6,0, 1H), 8,10 (d, J=8,0, 1H), 8,04 (s, 1H), 7,94 (d, J=8,1, 1H), 7,87 (d, J=6,8, 1H), 7,74 (t, J≈7,5, 1H), 7,60-7,54 (m, 2H), 7,25 (t, J≈7,0, 1H), 6,65 (t, J≈7,6, 1H), 6,54 (d, J=8,4, 1H), 4,62 (шир.d, J=5,5, 2H). Протон не наблюдается или закрыт.
МС (CI-NH3): 399 (75%, [М+Н]+).
Температура плавления: 185°С.
Пример 6.7
Получение амида N-(изохинолин-3-ил)-2-[(2-морфолинокарбонилпиридин-4-ил)метиламино]бензойной кислоты
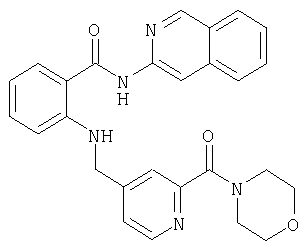
Смесь из 40 мг (0,1 ммоля) амида N-(изохинолин-3-ил)-2-[(2-гидроксикарбонилпиридин-4-ил)метиламино]бензойной кислоты и 9 мкл (0,1 ммоля) морфолина в 1 мл диметилформамида порциями смешивают с 34 мг (0,2 ммоля) карбонилдиимидазола. После 4-часового перемешивания при 22°С смесь концентрируют, остаток растворяют в 5 мл дихлорметана, промывают 1-молярным водным раствором карбоната калия (2 мл), сушат над MgSO4, фильтруют и концентрируют. В результате получают бесцветную смолу (38 мг, 81% от теории).
1Н-ЯМР (CDCl3): 9,02 (s, 1H), 8,71 (шир.s, 1H), 8,64 (s, 1H), 8,51 (d, J=5,1, 1H), 8,36 (t, J≈6,0, 1H), 8,01 (s, 1H), 7,93-7,82 (m, 2H), 7,69-7,64 (m, 2H), 7,50 (t, J≈7,8, 1H), 7,39 (d, J=6,1, 1H), 7,28-7,20 (m, 1H), 6,73 (t, J≈7,8, 1H), 6,52 (d, J=8,1, 1H), 4,55 (d, J=6,0, 2H), 3,79-3,62 (m, 8H).
MC (EI): 467 (15%, [M+H]+).
Пример 6.8
Получение амида N-(изохинолин-3-ил)-2-[(3-триметилсилилэтинилпиридин-4-ил)метиламино]бензойной кислоты
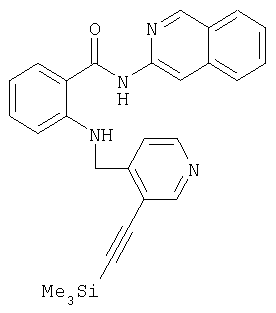
108 мг (0,25 ммоля) амида N-(изохинолин-3-ил)-2-[(3-бромпиридин-4-ил)метиламино]бензойной кислоты смешивают в 1 мл диметилформамида с 1 мл триэтиламина, 5 мг (0,026 ммоля) иодида меди(I), 9 мг (0,008 ммоля) палладийтетракистрифенилфосфина и 0,07 мл триметилсилилацетилена и затем в атмосфере аргона, исключая при этом доступ влаги, нагревают в течение 3,5 ч до температуры бани 70°С. Далее примешивают 40 мл воды и трижды экстрагируют этиловым эфиром уксусной кислоты его порциями по 25 мл. Уксусноэфирную фазу промывают водой, сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле, используя в качестве элюента этиловый эфир уксусной кислоты:гексан в соотношении 1:1. В результате получают 38 мг (33,6% от теории) амида N-(изохинолин-3-ил)-2-[(3-триметилсилилэтинилпиридин-4-ил)метиламино]бензойной кислоты в виде аморфного твердого вещества.
1H-ЯМР (d6-ДМСО): 10,71 (s, 1H), 9,22 (s, 1H), 8,62 (s, 1H), 8,58 (s, 1H), 8,49 (d, J=4,9, 1H), 8,21 (шир.t, J≈6,1, 1H), 8,09 (d, J=8,2, 1H), 7,92 (d, J=8,0, 1H), 7,88 (d, J=7,9, 1H), 7,74 (t, J≈8,0, 1H), 7,57 (t, J≈7,7, 1H), 7,40 (d, J=5,1, 1H), 7,28 (t, J≈7,5, 1H), 6,65 (t, J≈7,7, 1H), 6,54 (d, J=8,1, 1H), 4,58 (d, J=6,0, 2H), 0,27 (s, 3H).
MC (EI): 450 (105%, [M]+).
Пример 6.9
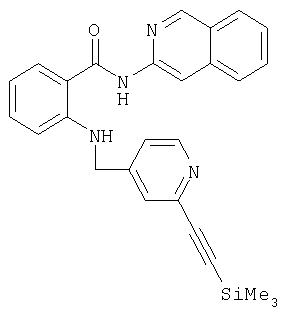
Получение амида N-(изохинолин-3-ил)-2-[(2-триметилсилилэтинилпиридин-4-ил)метиламино]бензойной кислоты
По методике, аналогично описанной в примере 9, получают также амид N-(изохинолин-3-ил)-2-[(2-триметилсилилэтинилпиридин-4-ил)метиламино]бензойной кислоты
Получение исходных и промежуточных соединений
Если получение промежуточных соединений не описывается, то подразумевается, что эти соединения известны либо их можно получать аналогично известным соединениям или с помощью описанных в настоящей заявке способов.
Пример А
Стадия 1 способа
А-1) Получение 2-бромпиридин-5-карбальдегида
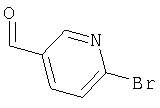
2-бромпиридин-5-карбальдегид получают по методу, описанному F.J.Romero-Salguerra и др. в THL 40 (1999), с.859.
А-2) Получение 2-бромизоникотиновой кислоты
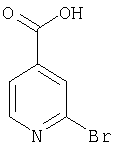
160 г (0,93 моля) 2-бром-4-метилпиридина по каплям добавляют к 152 г (0,96 моля) перманганата калия в 4 л воды. Затем после одночасового перемешивания с обратным холодильником повторно добавляют 152 г (0,96 моля) перманганата калия. После дальнейшего 2-часового перемешивания с обратным холодильником фильтруют в горячем состоянии через целит и промывают водой. Водную фазу трижды экстрагируют встряхиванием с дихлорметаном. Затем водную фазу концентрируют до половины ее объема и с помощью концентрированной соляной кислоты рН устанавливают на значение 2. Выпавшее в осадок твердое вещество отделяют вакуум-фильтрацией и при 70°С сушат в вакууме. В результате получают 56,5 г (28% от теории) 2-бромизоникотиновой кислоты в виде твердого продукта белого цвета.
А-3) Получение 2-бром-4-гидроксиметилпиридина
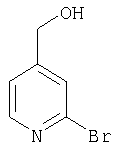
К 56,5 г (280 ммолей) 2-бромизоникотиновой кислоты в 1,2 л тетрагидрофурана (ТГФ) добавляют 30,2 мл (295 ммолей) триэтиламина. Затем охлаждают до -10°С и по каплям смешивают с 38,2 мл (295 ммолей) изобутилового эфира хлормуравьиной кислоты. После одночасового перемешивания при -10°С смесь охлаждают до -70°С и по каплям смешивают с 590 мл (590 ммолей) раствора алюмогидрида лития (LiAlH4) (1-молярного в ТГФ). После одночасового перемешивания при -70°С температуре дают повыситься до -40°С. Далее добавляют 600 мл 50%-ной уксусной кислоты. В течение ночи перемешивают при комнатной температуре. Нерастворимые компоненты отделяют вакуум-фильтрацией и фильтрат концентрируют. Остаток очищают на силикагеле гексаном и гексаном/этиловым эфиром уксусной кислоты в соотношении 1:1. В результате получают 28,0 г (55% от теории) 2-бром-4-гидроксиметилпиридина в виде затвердевающегося масла белого цвета.
А-4) Получение 2-бром-4-формилпиридина
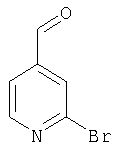
К 28,0 г (148,9 ммоля) 2-бром-4-гидроксиметилпиридина в 500 мл дихлорметана добавляют в течение 6 ч 149 г (1714 ммолей) пиролюзита. Затем в течение 48 ч перемешивают при комнатной температуре. Далее отделяют вакуум-фильтрацией через целит и концентрируют. В результате получают 16,4 г (60% от теории) 2-бром-4-формилпиридина в виде затвердевающегося масла белого цвета.
Стадия 2 способа
А-5) Получение 2-[(6-бромпиридин-3-илметил)амино]-N-изохинолин-3-илбензамида
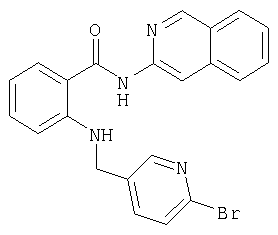
3,46 г (13,17 ммоля) 2-амино-N-изохинолин-3-илбензамида предварительно помещают в 50 мл метанола, затем смешивают с 1,5 мл ледяной уксусной кислоты и 2,45 г (13,17 ммоля) 2-бромпиридин-5-карбальдегида, после чего в течение 24 ч перемешивают при комнатной температуре в атмосфере аргона, исключая при этом доступ влаги. Далее примешивают 828 мг (13,17 ммоля) цианборогидрида натрия и продолжают перемешивание при комнатной температуре в течение последующих 24 ч. После концентрирования под вакуумом остаток растворяют в разбавленном растворе гидрокарбоната натрия и отделяют вакуум-фильтрацией. Полученный остаток размешивают в небольшом количестве этилового эфира уксусной кислоты и повторно отделяют вакуум-фильтрацией. Полученный таким путем остаток хроматографируют на силикагеле, используя в качестве элюента гексан и этиловый эфир уксусной кислоты в соотношении 1:1. В результате получают 3,27 г (57% от теории) 2-[(6-бромпиридин-3-илметил)амино]-N-изохинолин-3-илбензамида.
А-6) Получение амида N-(изохинолин-3-ил)-2-[3-бромпиридин-4-илметиламино]бензойной кислоты
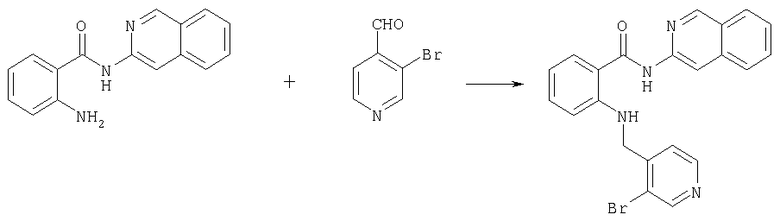
263 мг (1 ммоль) амида N-(изохинолин-3-ил)-2-аминобензойной кислоты последовательно смешивают в 6 мл МеОН с 0,06 мл ледяной уксусной кислоты, 298 мг (1,6 ммоля) 3-бромпиридин-4-карбальдегида (получение согласно Tetrahedron 2000, с.347) и в течение 24 ч перемешивают при комнатной температуре. Затем добавляют 100 мг (1,6 ммоля) цианборогидрида натрия и продолжают перемешивание в течение последующих 24 ч. Далее примешивают 50 мл разбавленного раствора гидрокарбоната натрия и выпавший в осадок продукт отделяют вакуум-фильтрацией. Остаток хроматографируют на силикагеле с использованием в качестве элюента смеси метиленхлорида и этанола в соотношении 95:5. В результате получают амид ЧМ-(изохинолин-3-ил)-2-[3-бромпиридин-4-илметиламино]бензойной кислоты в виде смолы. Используемый в реакции 3-бромпиридин-4-карбальдегид получают по методу, описанному в Chem. Pharm. Bull., 38 (1970), с.2446.
По аналогичной методике получают также следующие соединения:
А-7) 2-[(2-бромпиридин-4-илметил)амино]-N-изохинолин-3-илбензамид
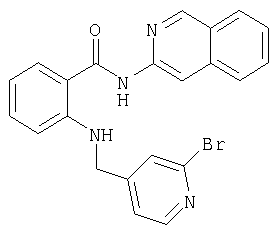
1H-ЯМР (CDCl3): 9,00 (s, 1H), 8,78 (s, 1H), 8,66 (s, 1H), 8,35 (t, J≈5,7, 1H), 8,30 (d, J=5,1, 1H), 7,92 (d, J=8,1, 1H), 7,86 (d, J=8,5, 1H), 7,70-7,65 (m, 2H), 7,53-7,48 (m, 2H), 7,33-7,26 (m, 2H), 6,75 (t, J≈7,8, 1H), 6,48 (d, J=8,5, 1H), 4,48 (d, J=5,9, 2H).
МС (Cl, NH3): 435 (100%), 433 (100%).
А-8) 2-[(2-бромпиридин-4-илметил)амино]-N-(2-оксо-2,3-дигидро-1Н-индол-6-ил)бензамид
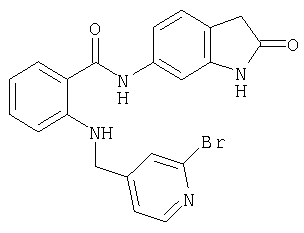
A-9) 2-[(2-бромпиридин-4-илметил)амино]-N-(2-оксо-2,3-дигидро-1Н-индол-5-ил)бензамид
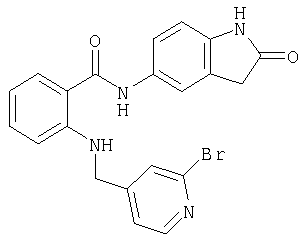
A-10) 2-[(6-бромпиридин-3-илметил)амино]-N-(2-оксо-2,3-дигидро-1Н-индол-6-ил)бензамид
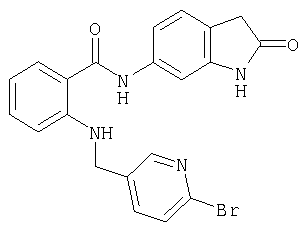
A-11) 2-[(6-бромпиридин-3-илметил)амино]-N-(2-оксо-2,3-дигидро-1Н-индол-5-ил)бензамид
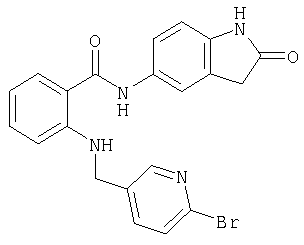
А-12) 2-[(6-бромпиридин-3-илметил)амино]-N-(7-метокси-2-оксо-2H-хромен-3-ил)бензамид
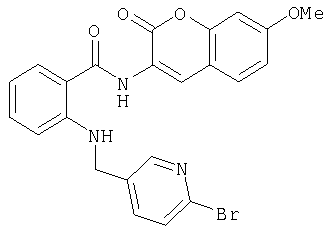
А-13) 2-[(2-бромпиридин-4-илметил)амино]-N-(7-метокси-2-оксо-2Н-хромен-3-ил)бензамид
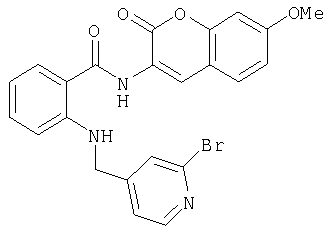
А-14а) 2-[(2-бромпиридин-4-илметил)амино]-N-(3-трифторметилфенил)бензамид
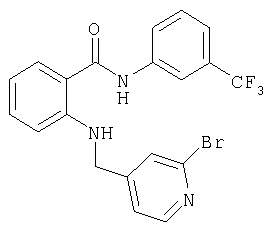
А-14б) 2-[(6-бромпиридин-3-илметил)амино]-N-(7-метокси-3-метилхинолин-2-ил)бензамид
Стадия 3 способа
А-15) Получение 5-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты
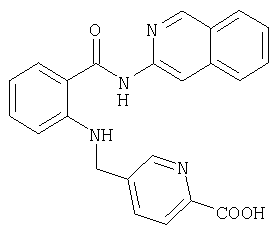
3,27 г (7,55 ммоля) 2-[(6-бромпиридин-3-илметил)амино]-N-изохинолин-3-илбензамида смешивают в 75 мл диметилформамида с 2,2 мл триэтиламина, 36 мл воды, 362 мг (0,65 ммоля) бисдифенилфосфинферроцена и 75 мг (0,33 ммоля) ацетата палладия(II) и встряхивают в автоклаве в атмосфере моноксида углерода при давлении 3 бара и температуре 50°С в течение 3 ч. После охлаждения проводят на силикагеле вакуум-фильтрацию и фильтрат концентрируют. Остаток растворяют в воде, с помощью ледяной уксусной кислоты рН устанавливают на значение 5-6, отделяют вакуум-фильтрацией и осадок на фильтре промывают гексаном. В результате получают 3,35 г 5-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновой кислоты, которую без дальнейшей очистки используют в последующей обменной реакции.
По аналогичной методике получают также следующие соединения:
А-16) 4-{[2-(изохинолин-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
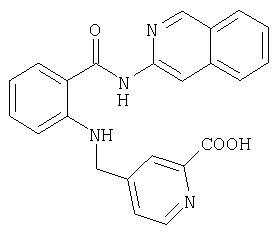
A-17) 4-{[2-(2-оксо-2,3-дигидро-1H-индол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
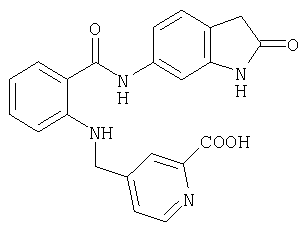
А-18) 5-{[2-(2-оксо-2,3-дигидро-1H-индол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
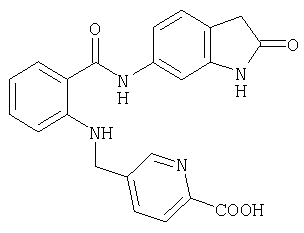
А-19) 4-{[2-(2-оксо-2,3-дигидро-1H-индол-5-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
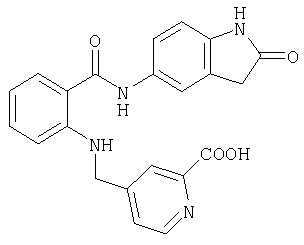
А-20) 5-{[2-(2-оксо-2,3-дигидро-1H-индол-5-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
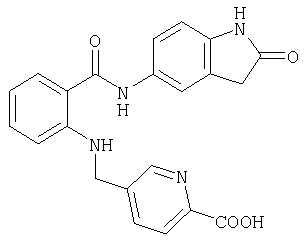
A-21) 5-{[2-(7-метокси-2-оксо-2H-хромен-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
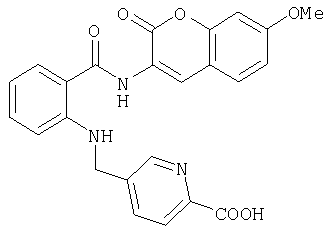
А-22) 4-{[2-(7-метокси-2-оксо-2H-хромен-3-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
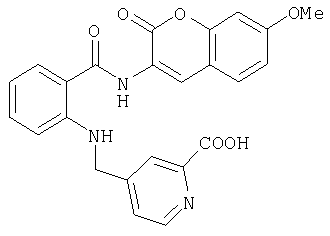
А-23) 4-{[2-(7-метокси-3-метилхинолин-2-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
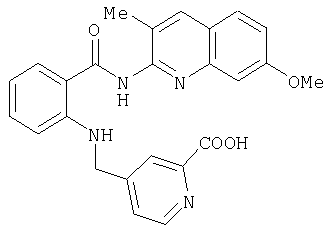
А-24) 5-{[2-(7-метокси-3-метилхинолин-2-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
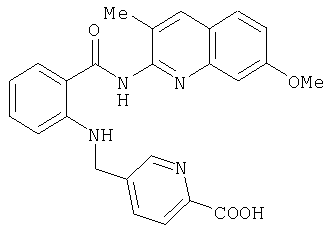
А-25) 5-{[2-(1-метил-1H-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
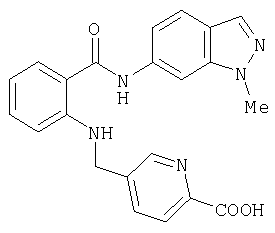
A-26) 4-{[2-(1-метил-1H-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
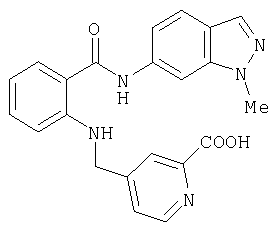
А-27) 4-{[2-(2-метил-2H-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
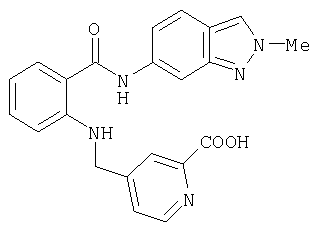
А-28) 5-{[2-(2-метил-2H-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
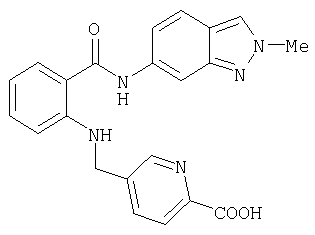
А-29) 4-{[2-(3-трифторметилфенилкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
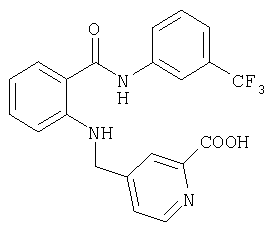
температура плавления 151°С;
А-30) 4-{[2-(1H-индазол-6-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
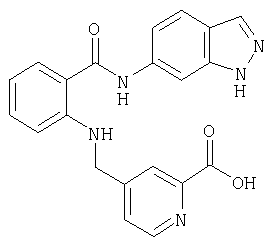
А-31) 4-{[2-(1H-индазол-5-илкарбамоил)фениламино]метил}пиридин-2-карбоновую кислоту
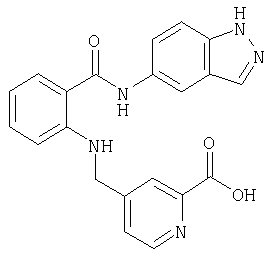
Пример Б
Стадия 1 способа
Б-1) Получение 5-нитро-1,3-дигидроиндол-2-она
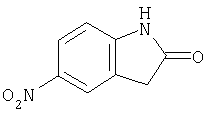
5-нитро-1,3-дигидроиндол-2-он получают по методу R.T.Courts, описанному в Journ. Org. Chem. 48 (1970), с.3747.
Б-2) Получение метилового эфира динитрофенилуксусной кислоты
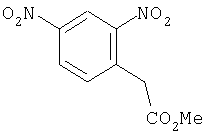
22,6 г (100 ммолей) 2,4-динитрофенилуксусной кислоты растворяют в смеси из 200 мл метанола и 830 мл толуола и при комнатной температуре смешивают с 83 мл триметилсилилдиазометана (2-молярном в толуоле, 166 ммолей) и затем в течение 3 ч перемешивают при комнатной температуре. После концентрирования досуха и сушки при 70°С под вакуумом получают 24 г (100% от теории) метилового эфира 2,4-динитрофенилуксусной кислоты.
Б-3) Получение 6-нитро-1,3-дигидроиндол-2-она
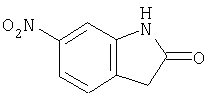
20 г (83 ммоля) метилового эфира 2,4-динитрофенилуксусной кислоты гидрируют в 400 мл ледяной уксусной кислоты с помощью 2,1 г палладия на угле (10%-ного) при давлении водорода 20 бар в течение 1,5 ч при комнатной температуре. После отфильтровывания катализатора концентрируют и интенсивно сушат над твердым гидроксидом калия под вакуумом. Остаток хроматографируют на силикагеле градиентным элюированием с использованием в качестве элюента смеси метиленхлорида и этанола в соотношении от 97,5:2,5 до 90:10. После перекристаллизации из этилового эфира уксусной кислоты получают 4 г (30% от теории) 6-нитро-1,3-дигидроиндол-2-она с температурой плавления 206°С.
Стадия 2 способа
Б-4) Получение 5-амино-1,3-дигидроиндол-2-она
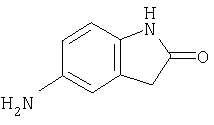
356 мг 5-нитро-1,3-дигидроиндол-2-она гидрируют в 30 мл смеси тетрагидрофурана и этанола (соотношение 1:1) с помощью 400 мг палладия на угле (10%-ного) при комнатной температуре и нормальном давлении в течение 1 ч. После удаления катализатора вакуум-фильтрацией на кизельгуре и концентрирования получают 320 мг (100% от теории) 5-амино-1,3-дигидроиндол-2-она.
Б-5) Получение 6-амино-1,3-дигидроиндол-2-она
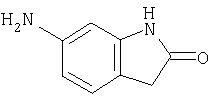
Аналогичным путем, исходя из соответствующего нитросоединения, получают 6-амино-1,3-дигидроиндол-2-он.
Стадия 3 способа
Б-6) 2-нитро-N-(2-оксо-2,3-дигидро-1H-индол-5-ил)бензамид
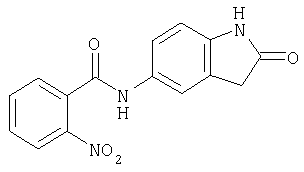
В 1 мл диметилацетамида растворяют 320 мг 5-амино-1,3-дигидроиндол-2-она и по каплям смешивают с 371 мг (2 ммоля) 2-нитробензоилхлорида, при этом происходит небольшое повышение температуры. После перемешивания в течение ночи при комнатной температуре концентрируют под вакуумом и остаток растворяют в этиловом эфире уксусной кислоты и воде. После удаления вакуум-фильтрацией нерастворимых твердых веществ получают 130 мг (21,9% от теории) 2-нитро-N-(2-оксо-2,3-дигидро-1H-индол-5-ил)бензамида. После экстракции встряхиванием органическую фазу промывают, фильтруют и концентрируют и в результате повторно получают 400 мг (67% от теории) 2-нитро-N-(2-оксо-2,3-дигидро-1H-индол-5-ил)бензамида с температурой плавления 265°С.
Б-7) Получение 2-нитро-N-(2-оксо-2,3-дигидро-1H-индол-6-ил)бензамида
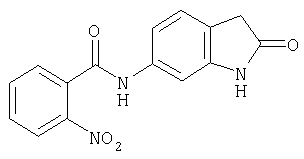
По методике, аналогичной стадии 1 способа, получают 2-нитро-N-(2-оксо-2,3-дигидро-1H-индол-6-ил)бензамида с температурой плавления >300°С.
Стадия 4 способа
Б-8) Получение амида 2-амино-N-(индол-2-он-5-ил)бензойной кислоты
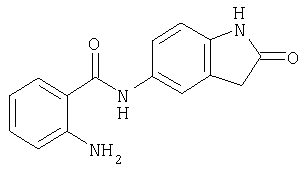
По методике, аналогичной стадии 2 способа, получают также амид 2-амино-N-(индол-2-он-5-ил)бензойной кислоты с температурой плавления 219°С.
Б-9) Получение амида 2-амино-N-(индол-2-он-6-ил)бензойной кислоты
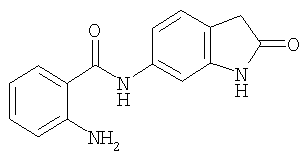
По методике, аналогичной стадии 2, получают также амид 2-амино-N-(индол-2-он-6-ил)бензойной кислоты с температурой плавления 230°С.
Пример В
В-1) Получение 2-амино-N-(7-метокси-2-оксо-2H-хромен-3-ил)бензамида
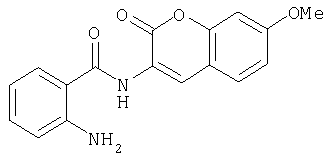
Стадия 1 способа
В-2) Получение 3-нитро-7-метоксихромен-2-она
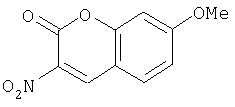
13 г (85,4 ммоля) 2-гидрокси-4-метоксибензальдегида в течение 15 ч нагревают в 300 мл толуола с использованием водоотделителя вместе с 9,8 г (102,5 ммоля) н-пропиламингидрохлорида и 11,5 мл (102,5 ммоля) этилового эфира нитроуксусной кислоты и кипятят далее в течение 5 ч с использованием водоотделителя. После охлаждения разбавляют этиловым эфиром уксусной кислоты и экстрагируют встряхиванием с водой. Уксусноэфирную фазу сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле с помощью метиленхлорида в качестве элюента. В результате получают 6,14 г (33% от теории) 3-нитро-7-метоксихромен-2-она.
Стадия 2 способа
В-3) Получение 3-амино-7-метоксихромен-2-она
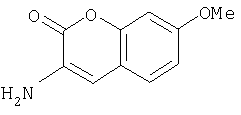
По методике, аналогичной стадии 2 способа из примера Б, исходя из 3-нитро-7-метоксихромен-2-она в этаноле получают 3-амино-7-метоксихромен-2-он.
Стадия 3 способа
В-4) Получение амида 2-нитро-N-(7-метоксибензопиран-2-он-3-ил)бензойной кислоты
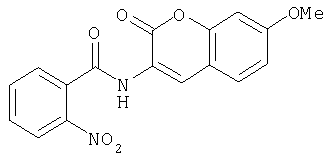
По методике, аналогичной стадии 3 способа из примера Б, исходя из 2-нитробензоилхлорида и 3-амино-7-метоксихромен-2-она, а также 2-нитро-N-(7-метокси-2-оксо-2H-хромен-3-ил)бензамида получают амид 2-нитро-N-(7-метоксибензопиран-2-он-3-ил)бензойной кислоты.
Стадия 4 способа
В-5) Получение 2-амино-N-(7-метокси-2-оксо-2H-хромен-3-ил)бензамида

По методике, аналогичной стадии 2 способа из примера Б, исходя из 2-нитро-N-(7-метокси-2-оксо-2H-хромен-3-ил)бензамида в толуоле/тетрагидрофуране (соотношение 5:2) получают 2-амино-N-(7-метокси-2-оксо-2H-хромен-3-ил)бензамид.
Пример Г
Г-1) Получение 2-[(6-цианопиридин-3-илметил)амино]-N-(2-оксо-2,3-дигидро-1H-индол-5-ил)бензамида
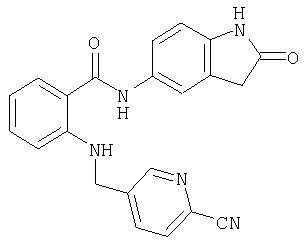
219 мг (0,5 ммоля) 2-[(6-бромпиридин-3-илметил)амино]-N-(2-оксо-2,3-дигидро-1H-индол-5-ил)бензамида помещают в 7 мл диметилацетамида, добавляя 59 мг (0,5 ммоля) цианида цинка(II), 12 мг (0,013 ммоля) трис(дибензилиденацетон)дипалладия, 10 мг (0,018 ммоля) бис(дифенилфосфино)ферроцена и 4 мг (0,06 ммоля) цинкового порошка, и в атмосфере аргона, исключая при этом доступ влаги, перемешивают в течение 7,5 ч при температуре бани 150°С. После охлаждения смесь разбавляют водой, экстрагируют встряхиванием с этиловым эфиром уксусной кислоты и органическую фазу сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле путем градиентного элюирования с использованием в качестве элюента смеси метиленхлорид/этанол в соотношении от 97,5:2,5 до 90:10. В результате получают 65 мг (30% от теории) 2-[(6-цианопиридин-3-илметил)амино]-N-(2-оксо-2,3-дигидро-1H-индол-5-ил)бензамида.
По аналогичной методике получают также следующее соединение:
Г-2) 2-[(6-цианопиридин-3-илметил)амино]-N-(7-метокси-2-оксо-2H-хромен-3-ил)бензамид
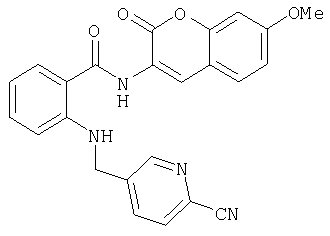
Пример Д
Стадия 1 способа
Д-1) Получение метилового эфира 2-хлорникотиновой кислоты
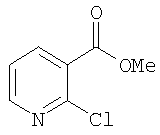
5,6 г 2-хлорникотиновой кислоты растворяют в 280 мл толуола и 80 мл метанола, смешивают с 37,4 мл (74,8 ммоля) триметилсилилдиазометана (2-молярного в гексане) и в течение 3 ч перемешивают при комнатной температуре. После концентрирования смеси получают 7 г (100% от теории) метилового эфира 2-хлорникотиновой кислоты.
Стадия 2 способа
Д-2) Получение метилового эфира 2-[(пиридин-4-илметил)амино]никотиновой кислоты
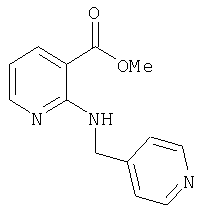
4,0 г (23,3 ммоля) метилового эфира 2-хлорникотиновой кислоты в течение 1,5 ч нагревают с 2,52 г (23,3 ммоля) 4-аминометилпиридина до температуры бани 100°С. После охлаждения разбавляют 100 мл разбавленного раствора гидрокарбоната натрия и трижды экстрагируют встряхиванием с этиловым эфиром уксусной кислоты его порциями по 50 мл. Объединенную органическую фазу промывают, сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле, используя в качестве элюента смесь метиленхлорид/этанол в соотношении 10:1. В результате получают 1,36 г (24% от теории) метилового эфира 2-[(пиридин-4-илметил)амино]никотиновой кислоты.
По аналогичной методике получают также следующее соединение:
Д-3) метиловый эфир 2-[(пиридин-3-илметил)амино]никотиновой кислоты
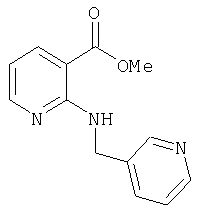
Стадия 3 способа
Д-4) Получение метилового эфира 2-[(1-оксипиридин-4-илметил)амино]никотиновой кислоты
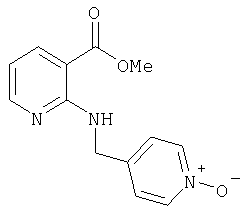
2,09 г (8,59 ммоля) метилового эфира 2-[(пиридин-4-илметил)амино]никотиновой кислоты смешивают в 150 мл метиленхлорида с 2,21 г (9,98 ммоля) м-хлорпербензойной кислоты и в течение 24 ч перемешивают при комнатной температуре. Затем примешивают 50 мл разбавленного раствора гидрокарбоната натрия, встряхивают, органическую фазу отделяют и трижды экстрагируют метиленхлоридом его порциями по 50 мл. Объединенную органическую фазу промывают, сушат, фильтруют и концентрируют. В результате получают 2,7 г (100% от теории) метилового эфира 2-[(1-оксипиридин-4-илметил)амино]никотиновой кислоты в виде масла.
По аналогичной методике получают также следующее соединение:
Д-5) метиловый эфир 2-[(1-оксипиридин-3-илметил)амино]никотиновой кислоты
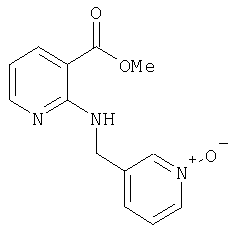
Стадия 4 способа
Д-6) Получение метилового эфира 2-[(2-цианопиридин-4-илметил)амино]никотиновой кислоты
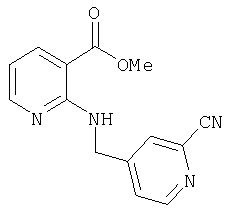
2,7 г (10,4 ммоля) метилового эфира 2-[(1-оксипиридин-4-илметил)амино] никотиновой кислоты в течение 8 ч нагревают в 52 мл диметилформамида в сосуде под давлением вместе с 3,15 г (31,2 ммоля) триэтиламина и 9,19 г (62,4 ммоля) триметилсилилцианида до температуры бани 110°С. После концентрирования под вакуумом остаток растворяют в 100 мл разбавленного раствора гидрокарбоната натрия и трижды экстрагируют этиловым эфиром уксусной кислоты его порциями по 100 мл. Объединенную органическую фазу промывают, сушат, фильтруют и концентрируют. Остаток хроматографируют на колонке для экспресс-хроматографии (50 г, материал Isoplute flash silica; фирма Separtis) путем градиентного элюирования с использованием в качестве элюента смеси метиленхлорид/этанол в соотношении от 100:0 до 95:5. В результате получают 1,31 г (47% от теории) метилового эфира 2-[(2-цианопиридин-4-илметил)амино]никотиновой кислоты.
По аналогичной методике получают также следующее соединение:
Д-7) Получение метилового эфира 2-[(6-цианопиридин-3-илметил)амино]никотиновой кислоты
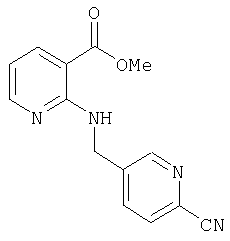
При получении указанного соединения одновременно в небольшом количестве образуется также метиловый эфир 2-[(2-цианопиридин-3-илметил)амино]никотиновой кислоты.
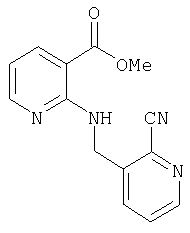
Стадия 5 способа
Д-8) Получение 2-[(2-цианопиридин-4-илметил)амино]-N-изохинолин-3-илникотинамида
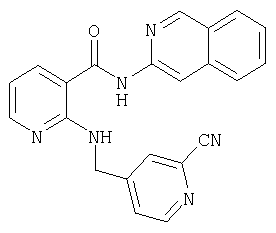
В 10 мл толуола в атмосфере аргона и исключая доступ влаги перемешивают в течение 30 мин при 4°С 277 мг (1,92 ммоля) 3-аминоизохинолина и 0,86 мл триметилалюминия (2-молярный раствор в толуоле). Затем добавляют 468 мг (1,74 ммоля) метилового эфира 2-[(2-цианопиридин-4-илметил)амино]никотиновой кислоты, после чего в течение 2 ч нагревают с обратным холодильником. Далее примешивают 30 мл разбавленного раствора гидрокарбоната натрия и трижды экстрагируют встряхиванием с этиловым эфиром уксусной кислоты его порциями по 30 мл. Объединенную органическую фазу промывают, сушат, фильтруют и концентрируют. Остаток хроматографируют на колонке для экспресс-хроматографии (20 г, материал Isolute flash silica, фирма Separtis) путем градиентного элюирования с использованием в качестве элюента смеси метиленхлорид/этанол в соотношении от 100:0 до 95:5. В результате получают 400 мг (60% от теории) 2-[(2-цианопиридин-4-илметил)амино]-N-изохинолин-3-илникотинамида.
Д-9) Получение амида N-(изохинолин-3-ил)-2-[2-цианопиридин-4-илметиламино]бензойной кислоты
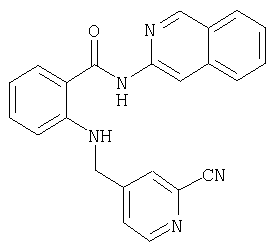
920 г (2,5 ммоля) N-оксида амида N-(изохинолин-3-ил)-2-(4-пиридилметил)аминобензойной кислоты последовательно смешивают в стеклянном сосуде под давлением, куда предварительно помещают 20 мл диметилформамида, с 760 мг (7,5 ммоля) триэтиламина и 1,24 г (12,5 ммоля) триметилсилилцианида, после чего в течение 10 ч нагревают до температуры бани 110°С. Затем смесь разбавляют водой до объема порядка 200 мл и трижды экстрагируют встряхиванием с этиловым эфиром уксусной кислоты его порциями по 50 мл. Собранную органическую фазу промывают 50 мл воды, сушат, фильтруют и концентрируют. Остаток хроматографируют сначала на силикагеле, используя в качестве элюента смесь этиловый эфир/гексан в соотношении 1:1, а затем повторно на силикагеле, но используя в качестве элюента смесь дихлорметан/этанол в соотношении 100:2. В результате получают 132 мг (14% от теории) амида N-(изохинолин-3-ил)-2-[2-цианопиридин-4-илметиламино]бензойной кислоты в виде смолы.
Если получение промежуточных соединений не описывается, то, как указывалось выше, подразумевается, что эти соединения известны либо их можно получать аналогично известным соединениям или с помощью описанных в настоящей заявке способов.
По аналогичной методике получают также следующие соединения:
Д-10) 2-[(2-цианопиридин-3-илметил)амино]-N-изохинолин-3-илникотинамид
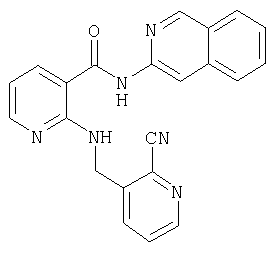
Д-11) 2-[(6-цианопиридин-3-илметил)амино]-N-изохинолин-3-илникотинамид
Пример Е
Стадия 1 способа
Е-1) Получение метилового эфира 2-[(2-бромпиридин-4-илметил)амино]бензойной кислоты
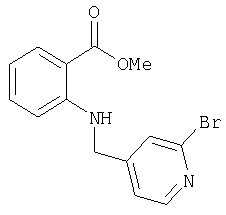
6,04 г (40 ммолей) метилового эфира антраниловой кислоты в 600 мл метанола смешивают с 3,2 мл уксусной кислоты и 7,4 г (40 ммолей) 2-бромпиридин-4-карбальдегида и в течение ночи перемешивают при 40°С. После добавления 3,8 г (60 ммолей) цианборогидрида натрия продолжают перемешивание в течение ночи при 40°С. Затем повторно добавляют 3,8 г (60 ммолей) цианборогидрида натрия и в течение выходных дней перемешивают при 40°С. Далее примешивают воду и концентрируют практически досуха. Водную фазу экстрагируют этиловым эфиром уксусной кислоты, объединенные органические фазы сушат, фильтруют и концентрируют. Сырой продукт хроматографируют на силикагеле путем градиентного элюирования с использованием в качестве элюента гексана и смеси гексан/этиловый эфир уксусной кислоты в соотношении 1:3 и смеси гексан/этиловый эфир уксусной кислоты в соотношении 1:1. В результате получают 10,0 г (78% от теории) метилового эфира 2-[(2-бромпиридин-4-илметил)амино]бензойной кислоты в виде бесцветного масла.
Стадия 2 способа
Е-2) Получение метилового эфира 2-[(2-пианопиридин-4-илметил)амино]бензойной кислоты
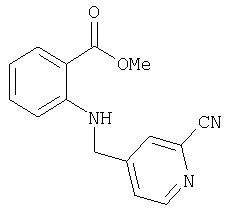
1,28 г (4,0 ммоля) метилового эфира 2-[(2-бромпиридин-4-илметил)амино]бензойной кислоты в 140 мл диметилацетамида смешивают с 0,532 г (4,56 ммоля) цианида цинка(II), 0,072 г (0,08 ммоля) трис(дибензилиденацетон)дипалладия, 0,088 г (0,16 ммоля) бис(дифенилфосфино)ферроцена и 0,029 г (0,46 ммоля) цинкового порошка. Далее перемешивают в течение 6 ч при 150°С. После охлаждения реакционную смесь сливают на воду. Затем трижды экстрагируют этиловым эфиром уксусной кислоты, объединенные органические фазы сушат над сульфатом натрия и концентрируют. Полученный продукт хроматографируют на силикагеле путем градиентного элюирования с использованием в качестве элюента смеси гексан/этиловый эфир уксусной кислоты в соотношении от 100:0 до 50:50. В результате получают 0,887 г (83% от теории) метилового эфира 2-[(2-цианопиридин-4-илметил)амино]бензойной кислоты в виде твердого вещества желтого цвета.
Стадия 3 способа
Е-3) Получение 2-[(2-цианопиридин-4-илметил)амино]-N-(7-метокси-3-метилхинолин-2-ил)бензамида
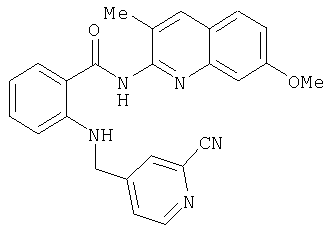
При 0°С 0,25 г триметилалюминия (2-молярного в толуоле) по каплям добавляют к 0,094 г (0,5 ммоля) 7-метокси-3-метилхинолин-2-иламина в 4 мл толуола. После 10-минутного перемешивания при 0°С по каплям добавляют 0,133 г (0,5 ммоля) метилового эфира 2-[(2-цианопиридин-4-илметил)амино]бензойной кислоты в 2 мл толуола. Затем в течение 2 ч перемешивают с обратным холодильником и в течение ночи при комнатной температуре. Осадок отделяют вакуум-фильтрацией и суспендируют в насыщенном растворе гидрокарбоната натрия. Затем добавляют этилендиаминтетрауксусную кислоту. Далее экстрагируют встряхиванием с этиловым эфиром уксусной кислоты, сушат над сульфатом натрия и концентрируют. После очистки колоночной хроматографией на силикагеле путем градиентного элюирования с использованием смеси гексан/ацетон в соотношении от 100:0 до 50:50 получают 0,113 г (54% от теории) 2-[(2-цианопиридин-4-илметил)амино]-N-(7-метокси-3-метилхинолин-2-ил)бензамида в виде пенистого вещества желтого цвета.
Пример Ж
Стадия 1 способа
Ж-1) Получение 2-[(2-бромпиридин-4-илметил)амино]бензойной кислоты
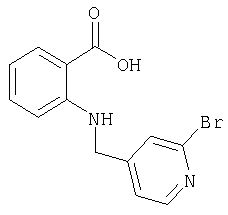
10,0 г (31,2 ммоля) метилового эфира 2-[(2-бромпиридин-4-илметил)амино]бензойной кислоты растворяют в 290 мл этанола и смешивают с 31,2 мл 2-молярного едкого натра. После перемешивания в течение ночи при комнатной температуре этанол удаляют, а водную фазу экстрагируют встряхиванием с этиловым эфиром уксусной кислоты. Водную фазу подкисляют концентрированной соляной кислотой. Образовавшийся осадок отделяют вакуум-фильтрацией и сушат. В результате получают 5,93 г (62% от теории) 2-[(2-бромпиридин-4-илметил)амино]бензойной кислоты в виде твердого вещества белого цвета.
Стадия 2 способа
Ж-2) Получение 2-[(2-бромпиридин-4-илметил)амино]-N-(2-метил-2H-индазол-6-ил)бензамида
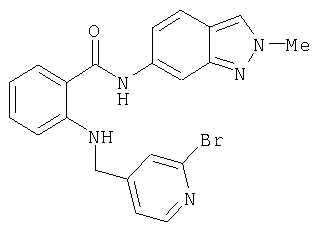
0,500 г (1,6 ммоля) 2-[(2-бромпиридин-4-илметил)амино]бензойной кислоты, 0,471 г (3,2 ммоля) 2-метил-2H-индазол-6-иламина, 0,4 мл (3,68 ммоля) N-метилморфолина и 0,729 г (1,92 ммоля) гексафторфосфата О-(7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония (ГАТУ) в 25 мл диметилформамида перемешивают в течение 16 ч при комнатной температуре. Затем диметилформамид удаляют в вакууме, создаваемом масляным насосом. Образующийся остаток растворяют в насыщенном растворе гидрокарбоната натрия. Затем трижды экстрагируют этиловым эфиром уксусной кислоты и объединенные органические фазы сушат, фильтруют и концентрируют. Остаток хроматографируют на силикагеле путем градиентного элюирования с использованием в качестве элюента смеси гексан/ацетон в соотношении от 100:0 до 50:50. В результате получают 0,669 г (96% от теории) 2-[(2-бромпиридин-4-илметил)амино]-N-(2-метил-2H-индазол-6-ил)бензамида в виде пенистого вещества бежевого цвета.
По аналогичной методике получают также следующие соединения:
Ж-3) 2-[(2-бромпиридин-4-илметил)амино]-N-(1-метил-1H-индазол-6-ил)бензамид
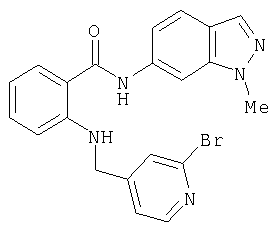
Ж-4) 2-[(2-бромпиридин-4-илметил)амино]-N-(1Н-индазол-6-ил)бензамид
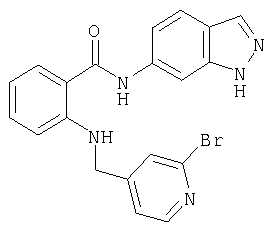
Ж-5) 2-[(2-бромпиридин-4-илметил)амино]-N-(1Н-индазол-5-ил)бензамид
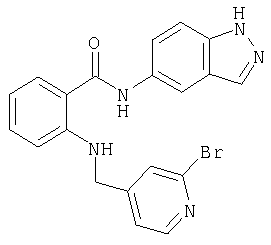
Ж-6) 2-[(2-бромпиридин-4-илметил)амино]-N-(2-оксо-2,3-дигидро-1H-индол-6-ил)бензамид
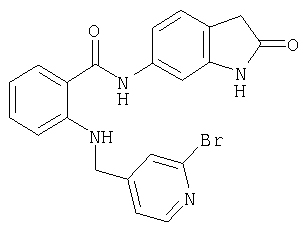
Ж-7) 2-[(2-бромпиридин-4-илметил)амино]-N-(2-оксо-2,3-дигидро-1H-индол-5-ил)бензамид
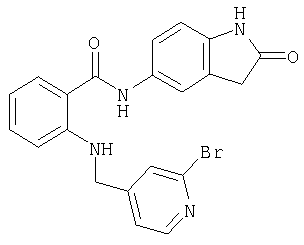
З-1) 4-(трет-бутоксикарбониламинометил)пиридин-2-карбоновая кислота
4-(трет-бутоксикарбониламинометил)пиридин-2-карбоновую кислоту получают согласно Chem Eur. J. 2 (2000), с.216, исходя из трет-бутилового эфира (2-цианопиридин-4-илметил)карбаминовой кислоты.
З-2) Оптически активный трет-бутиловый эфир [2-(2-гидроксипропилкарбамоил)пиридин-4-илметил]карбаминовой кислоты
Оптически активный трет-бутиловый эфир [2-(2-гидроксипропилкарбамоил)пиридин-4-илметил]карбаминовой кислоты получают по способу, указанному в примере 2.0, исходя из 4-(трет-бутоксикарбониламинометил)пиридин-2-карбоновой кислоты и S-(+)-1-амино-2-пропанола с выходом 91%.
З-3) Оптически активный (2-гидроксипропил)амид 4-аминометилпиридин-2-карбоновой кислоты
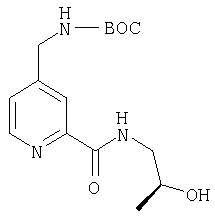
480 мг (1,7 ммоля) трет-бутилового эфира [2-(2-гидроксипропилкарбамоил)пиридин-4-илметил]карбаминовой кислоты смешивают в 30 мл этанола с 17 мл 1 н. соляной кислоты и при пропускании потока азота в течение 3 ч нагревают до температуры бани 110°С. Затем смесь концентрируют под вакуумом, сушат и без дальнейшей очистки используют аналогично примеру 5.0.
З-4) 2-хлор-N-изохинолин-3-илникотинамид
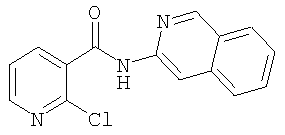
2,9 г (20 ммолей) 3-аминоизохинолина суспендируют в 45 мл тетрагидрофурана и по каплям смешивают с раствором из 3,5 г (20 ммолей) 2-хлорникотиноилхлорида в 45 мл тетрагидрофурана. После перемешивания в течение ночи при комнатной температуре смесь отделяют вакуум-фильтрацией и остаток промывают тетрагидрофураном. Затем остаток взмучивают в воде и повторно отделяют вакуум-фильтрацией и сушат. В результате получают 3,14 г (55% от теории) 2-хлор-N-изохинолин-3-илникотинамида.
Ниже на примерах по применению, которые не ограничивают объем изобретения, более подробно поясняются биологическое действие предлагаемых соединений и их применение.
Использовавшиеся в опытах растворы
Исходные растворы:
исходный раствор А: 3 мМ АТФ в воде, рН 7,0 (-70°С),
исходный раствор Б: g-33 Р-АТФ 1 мКи/100 мкл,
исходный раствор В: поли(Glu4Тyr) 10 мг/мл в воде.
Раствор для разведений:
растворители субстратов: 10 мМ ДТТ, 10 мМ хлорид марганца, 100 мМ хлорид магния,
раствор фермента: 120 мМ трис/HCl, рН 7,5, 10 мкМ оксид натрийванадия.
Пример по применению 1
Подавление активности киназы KDR и FLT-1 в присутствии соединений по изобретению
В сужающийся по концам титрационный микропланшет (без связывания протеина) добавляют 10 мкл питательной смеси (исходный раствор А объемом 10 мкл АТФ +25 мкКи γ-33Р-АТФ (примерно 2,5 мкл исходного раствора Б) + исходный раствор В: 30 мкл поли(Glu4Тyr) +1,21 мл растворителя субстратов), 10 мкл раствора ингибитора (соединения в соответствии с разведениями, в качестве контроля служит 3%-ный раствор ДМСО в растворителе субстратов) и 10 мкл раствора фермента (11,25 мкг исходного раствора фермента (киназы KDR или FLT-1), разведенного при 4°С в 1,25 мл раствора фермента). Указанные ингредиенты тщательно перемешивают и в течение 10 мин инкубируют при комнатной температуре. Затем добавляют 10 мкл стоп-раствора (250 мМ ЭДТК, рН 7,0), перемешивают и 10 мкл раствора переносят на фосфоцеллюлозный фильтр типа Р 81, после чего несколько раз промывают в 0,1-молярной фосфорной кислоте. Фильтровальную бумагу сушат, покрывают слоем Meltilex и с помощью микросчетчика бета-частиц измеряют радиоактивность.
IC50-значения представляют собой величины, определяемые по концентрации ингибитора, необходимой для подавления встраивания фосфата на 50% от его встраивания в отсутствие ингибитора, за вычетом контрольного значения, полученного в результате слепого опыта (реакция, прекращенная с помощью ЭДТК).
Результаты ингибирования киназы (IC50-значения в нМ) представлены в нижеследующей таблице 1.
Пример по применению 2
Ингибирование цитохрома Р450
Ингибирование цитохрома Р450 проводили в соответствии с публикацией авторов Crespi и др. (Anal. Biochem. 248 (1997), cc.188-190) с использованием экспрессируемых бакуловирусом/клетками насекомых изоферментов цитохрома Р450 (1А2, 2С9, 2С19, 3А4) человека.
Результаты представлены в нижеследующей таблице 2.
Ингибирование изоферментов цитохрома Р450 (IC50, мкМ)
Приведенные результаты однозначно подтверждают, что предлагаемые в изобретении соединения по своим свойствам превосходят известные соединения, т.е. предлагаемые в изобретении соединения проявляют в существенно меньшей степени ингибирующее действие детоксифицирующей системы цитохрома Р450 по сравнению с известными соединениями, что приводит к заметно ослабленному взаимодействию с другими действующими веществами.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТРАНИЛАМИДЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2001 |
|
RU2263664C2 |
| НОВЫЕ АНТРАНИЛАМИДОПИРИДИНМОЧЕВИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ РЕЦЕПТОРА VEGF | 2005 |
|
RU2415850C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ МОДУЛЯЦИИ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ, СПОСОБ ПОЛУЧЕНИЯ ЭТИХ СОЕДИНЕНИЙ | 2000 |
|
RU2255937C2 |
| АЗАИНДОЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Xa | 2004 |
|
RU2330853C2 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха | 2004 |
|
RU2346944C2 |
| Новые соединения | 2016 |
|
RU2734256C2 |
| ЗАМЕЩЕННЫЕ АМИДЫ БЕНЗОЙНОЙ КИСЛОТЫ И ИХ СОДЕРЖАЩИЙ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 2001 |
|
RU2353618C2 |
| ИНДОЛ-2-КАРБОКСАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА Ха И/ИЛИ VIIa, ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2299881C2 |
| ИЗОСЕРИНОВЫЕ ПРОИЗВОДНЫЕ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА СВЕРТЫВАНИЯ КРОВИ IXA | 2007 |
|
RU2446157C2 |
| КАРБОКСАМИДНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КАЛЬПАИНА | 2010 |
|
RU2540856C2 |
Настоящее изобретение относится к антраниламидпиридинамидам избирательного действия в качестве ингибиторов VEGFR-2 и VEGFR-3. Описываются соединения общей формулы I
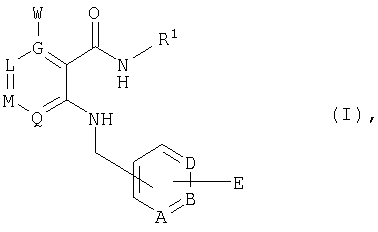
в которой А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце, Е представляет собой арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий 5 или 6 кольцевых атомов и вместо углерода содержащий в кольце идентичные либо разные гетероатомы, выбранные из атомов азота или серы, или представляет собой группу -COOR8, -CONR2R3 или 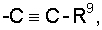 G представляет собой атом азота или группу -С-Х, L представляет собой атом азота или группу -С-Х, М представляет собой атом азота или группу -С-Х, Q представляет собой атом азота или группу -С-Х, при этом в кольце расположен максимум один атом азота, Х представляет собой водород, W представляет собой водород или галоген, R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, C1-С6алкилом или группой =O арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 16 кольцевых атомов и вместо углерода содержащий в кольце один или более идентичных либо разных гетероатомов, таких как кислород, азот или сера, который может быть моно-, би- или трициклическим и дополнительно может быть сконденсирован с бензольным ядром, R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-C1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR5 C1-С6алкил, C3-С6циклоалкил, C3-С6циклоалкенил арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 6 кольцевых атомов и вместо углерода содержащий в кольце один или более гетероатомов, таких как азот или сера, или R2 и R3 вместе с атомом азота образуют С3-С8кольцо, которое необязательно может содержать еще один атом азота или кислорода, либо может содержать группу -N(R10), R5 представляет собой водород, R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил, R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил или бензил, R9 представляет собой водород или три-C1-С6алкилсилил, R10 представляет собой водород или C1-С6алкил, а также их изомеры, энантиомеры и соли. Также описывается лекарственное средство на основе соединений формулы I. Технический результат - получены новые соединения, обладающие полезными биологическими свойствами. 2 н. и 6 з.п. ф-лы, 2 табл.
G представляет собой атом азота или группу -С-Х, L представляет собой атом азота или группу -С-Х, М представляет собой атом азота или группу -С-Х, Q представляет собой атом азота или группу -С-Х, при этом в кольце расположен максимум один атом азота, Х представляет собой водород, W представляет собой водород или галоген, R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, C1-С6алкилом или группой =O арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 16 кольцевых атомов и вместо углерода содержащий в кольце один или более идентичных либо разных гетероатомов, таких как кислород, азот или сера, который может быть моно-, би- или трициклическим и дополнительно может быть сконденсирован с бензольным ядром, R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-C1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR5 C1-С6алкил, C3-С6циклоалкил, C3-С6циклоалкенил арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 6 кольцевых атомов и вместо углерода содержащий в кольце один или более гетероатомов, таких как азот или сера, или R2 и R3 вместе с атомом азота образуют С3-С8кольцо, которое необязательно может содержать еще один атом азота или кислорода, либо может содержать группу -N(R10), R5 представляет собой водород, R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил, R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил или бензил, R9 представляет собой водород или три-C1-С6алкилсилил, R10 представляет собой водород или C1-С6алкил, а также их изомеры, энантиомеры и соли. Также описывается лекарственное средство на основе соединений формулы I. Технический результат - получены новые соединения, обладающие полезными биологическими свойствами. 2 н. и 6 з.п. ф-лы, 2 табл.
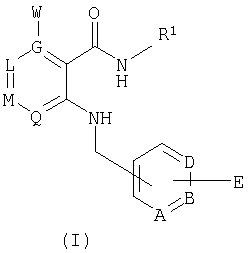
в которой
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий 5 или 6 кольцевых атомов и вместо углерода содержащий в кольце идентичные либо разные гетероатомы, выбранные из атомов азота или серы, или представляет собой группу -COOR8, -CONR2R3 или -C≡C-R9,
G представляет собой атом азота или группу -С-Х,
L представляет собой атом азота или группу -С-Х,
М представляет собой атом азота или группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
при этом в кольце расположен максимум один атом азота,
Х представляет собой водород,
W представляет собой водород или галоген,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, C1-С6алкилом или группой =O арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 16 кольцевых атомов и вместо углерода содержащий в кольце один или более идентичных либо разных гетероатомов, таких как кислород, азот или сера, который может быть моно-, би- или трициклическим и дополнительно может быть сконденсирован с бензольным ядром,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, цианогруппой, С1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-С1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR5 C1-С6алкил, С3-С6циклоалкил, С3-С6циклоалкенил арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 6 кольцевых атомов и вместо углерода содержащий в кольце один или более гетероатомов, таких как азот или сера, или
R2 и R3 вместе с атомом азота образуют С3-С8кольцо, которое необязательно может содержать еще один атом азота или кислорода, либо может содержать группу -N(R10),
R5 представляет собой водород,
R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил или бензил,
R9 представляет собой водород или три-C1-С6алкилсилил,
R10 представляет собой водород или С1-С6алкил,
а также их изомеры, энантиомеры и соли.
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий 5 или 6 кольцевых атомов и вместо углерода содержащий в кольце идентичные либо разные гетероатомы, выбранные из атомов азота и серы, или представляет собой группу -COOR8, -CONR2R3 или -C≡C-R9,
G представляет собой атом азота или группу -С-Х,
L представляет собой атом азота или группу -С-Х,
М представляет собой атом азота или группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
при этом в кольце расположен максимум один атом азота,
Х представляет собой водород,
W представляет собой водород или галоген,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, C1-С6алкилом или группой =O арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 16 кольцевых атомов и вместо углерода содержащий в кольце один или более идентичных либо разных гетероатомов, таких как кислород, азот или сера, который может быть моно-, би- или трициклическим и дополнительно может быть сконденсирован с бензольным ядром,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-С1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR5 C1-С6алкил, С3-С6циклоалкил, С3-С6циклоалкенил арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 6 кольцевых атомов и вместо углерода содержащий в кольце один или более гетероатомов, таких как азот или сера, или
R2 и R3 вместе с атомом азота образуют С3-С8кольцо, которое необязательно может содержать еще один атом азота, либо кислорода или может содержать группу -N(R10),
R5 представляет собой водород,
R6 и R7 независимо друг от друга представляют собой водород или С1-С6алкил,
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил или бензил,
R9 представляет собой водород или три-C1-С6алкилсилил,
а также их изомеры, энантиомеры и соли.
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий 5 или 6 кольцевых атомов и вместо углерода содержащий в кольце идентичные либо разные гетероатомы, выбранные из атомов азота или серы, или представляет собой группу -COOR8, -CONR2R3 или -C≡C-R9,
G представляет собой атом азота или группу -С-Х,
L представляет собой атом азота или группу -С-Х,
М представляет собой атом азота или группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
при этом в кольце расположен максимум один атом азота,
Х представляет собой водород,
W представляет собой водород или галоген,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, С1-С6алкилом арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 16 кольцевых атомов и вместо углерода содержащий в кольце один или более идентичных либо разных гетероатомов, таких как кислород, азот или сера, который может быть моно-, би- или трициклическим и дополнительно может быть сконденсирован с бензольным ядром,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, C1-С6алкилом, фенилом, гидрокси-С1-С6алкилом, гало-С1-С6алкилом либо группой -NR6R7, -OR5, C1-С6алкил-OR5 C1-С6алкил, С3-С6циклоалкил, С3-С6циклоалкенил арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 6 кольцевых атомов и вместо углерода содержащий в кольце один или более гетероатомов, таких как азот или сера, или
R2 и R3 вместе с атомом азота образуют С3-С8кольцо, которое необязательно может содержать еще один атом азота, либо кислорода или может содержать группу -N(R10),
R5 представляет собой водород,
R6 и R7 независимо друг от друга представляют собой водород или C1-С6алкил,
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном С1-С6алкил или бензил,
R9 представляет собой водород или три-С1-С6алкилсилил,
R10 представляет собой водород, С1-С6алкил,
а также их изомеры, энантиомеры и соли.
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой гетероарил, включающий 5 или 6 кольцевых атомов и вместо углерода содержащий в кольце идентичные либо разные гетероатомы, выбранные из атомов азота или серы, или представляет собой группу -COOR8, -CONR2R3 или -C≡C-R9,
G представляет собой группу -С-Х,
L представляет собой группу -С-Х,
М представляет собой группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
Х представляет собой водород,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, С1-С6алкилом фенил, тиофен, фуран, оксазол, тиазол, имидазол, пиразол, пиридин, пиримидин, триазин, хинолин, изохинолин или замещен по группе
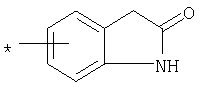 ,
, 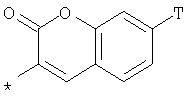 ,
,
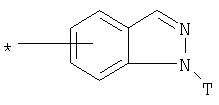 или
или 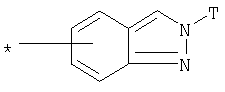
в которой Т обозначает водород, C1-С6алкил или C1-С6алкоксигруппу,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, C1-С6алкилом, фенилом, гидрокси-C1-С6алкилом, гало-C1-С6алкилом либо группой -NR6R7, -OR5, С1-С6алкил-OR5 C1-С6алкил, С3-С6циклоалкил, С3-С6циклоалкенил арил, содержащий 6-12 кольцевых атомов углерода, либо гетероарил, включающий от 3 до 6 кольцевых атомов и вместо углерода содержащий в кольце один или более гетероатомов, таких как азот или сера, или
R2 и R3 вместе с атомом азота образуют С3-С8кольцо, которое необязательно может содержать еще один атом азота либо кислорода или может содержать группу -N(R10),
R5 представляет собой водород,
R6 и R7 независимо друг от друга представляют собой водород или С1-С6алкил,
R8 представляет собой водород или необязательно одно- либо многозамещенный галогеном C1-С6алкил или бензил,
R9 представляет собой водород или три-С1-С6алкилсилил,
а также их изомеры, энантиомеры и соли.
А, В и D независимо друг от друга представляют собой атом азота или атом углерода, при этом по меньшей мере один атом азота содержится в кольце,
Е представляет собой тиенил, пиридил либо группу -COOR8, -CONR2R3 или -C≡C-R9,
G представляет собой группу -С-Х,
L представляет собой группу -С-Х,
М представляет собой группу -С-Х,
Q представляет собой атом азота или группу -С-Х,
Х представляет собой водород,
R1 представляет собой необязательно идентично либо различно одно- или многозамещенный галогеном, гидроксигруппой, C1-С6алкилоксигруппой, С1-С6алкилом фенил, тиофен, фуран, оксазол, тиазол, имидазол, пиразол, пиридин, пиримидин, триазин, хинолин, изохинолин или замещен по группе
 ,
,  ,
,
 или
или 
или в которой Т обозначает водород, С1-С6алкил или C1-С6алкоксигруппу,
R2 и R3 независимо друг от друга представляют собой водород или необязательно идентично либо различно одно- или многозамещенный галогеном, C1-С6алкилом, фенилом либо группой -NR6R7, -OR5 или С1-С6алкил-OR5 C1-С6алкил, С3-С6циклоалкил, фенил либо пиридил или
R2 и R3 вместе с атомом азота образуют С3-С8кольцо, которое необязательно может содержать еще один атом азота либо кислорода,
R5 представляет собой водород,
R6 и R7 независимо друг от друга представляют собой водород или С1-С6алкил,
R8 представляет собой водород, С1-С6алкил или бензил,
R9 представляет собой водород или три-C1-С6алкилсилил,
а также их изомеры и соли.
| WO 00/27819 А, 18.05.2000 | |||
| WO 00/27820 A, 18.05.2000 | |||
| ПРОИЗВОДНЫЕ АНТРАНИЛОВОЙ КИСЛОТЫ ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ НА ИХ ОСНОВЕ | 1994 |
|
RU2128644C1 |
Авторы
Даты
2007-05-20—Публикация
2002-05-03—Подача