Настоящее изобретение относится к новому бензамидному производному и его фармацевтически приемлемым кислотно-аддитивным солям, фармацевтическим композициям, содержащим указанное новое соединение, способам получения указанных соединений и композиций и их применению в качестве лекарственного средства при лечении нарушений моторики желудочно-кишечного тракта.
ЕР-0445862-А, опубликованная 11 сентября 1991 года, раскрывает N-(4-пиперидинил)(дигидробензофуран или дигидро-2Н-бензопиран)карбоксамидные производные, обладающие свойствами стимуляции моторики желудочно-кишечного тракта.
WO-96/16060, опубликованная 30 мая 1996 года, конкретно раскрывает соединение 4-амино-5-хлор-2,3-дигидро-N-[1-(3-метоксипропил)-4-пиперидинил]-7-бензофуранкарбоксамида, которое общеизвестно как "прукалоприд".
Соединения по настоящему изобретению отличаются от указанных тем, что они неизменно содержат 1-пиперидиноксидную группу, а также улучшенными фармакологическими свойствами.
Настоящее изобретение относится к соединениям формулы (I)
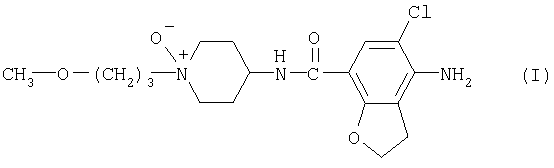
и их стереохимически изомерным формам и фармацевтически приемлемым кислотно-аддитивным солям.
Термин "стереохимически изомерные формы", как он использован выше, означает все возможные изомерные формы, которые могут иметь соединения формулы (I). Если не отмечено или не указано иное, химическое обозначение соединений означает смесь всех возможных стереохимически изомерных форм, при этом указанные смеси включают все диастереомеры и энантиомеры основной молекулярной структуры. Более конкретно, заместители в пиперидиновой группе имеют либо цис-, либо трансконфигурацию. Очевидно, что стереохимически изомерные формы соединений формулы (I) предназначены для охвата объемом данного изобретения.
Фармацевтически приемлемые кислотно-аддитивные соли, как указано выше, включают терапевтически активные нетоксичные формы кислотно-аддитивных солей, которые могут образовывать соединения формулы (I). Фармацевтически приемлемые кислотно-аддитивные соли можно удобным образом получать путем обработки основной формы такой подходящей кислотой. Подходящие кислоты включают, например, неорганические кислоты, такие как галогенводородные кислоты, например хлористоводородную или бромистоводородную кислоту, серную, азотную, фосфорную и подобные кислоты; или органические кислоты, такие как, например, уксусная, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая (т.е. этандиовая), малоновая, янтарная (т.е. бутандиовая кислота), малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламиновая, салициловая, п-аминосалициловая, памовая и подобные кислоты.
Наоборот, указанные формы солей можно преобразовать в форму свободного основания путем обработки подходящим основанием.
Термин "аддитивная соль", как он использован выше, также включает сольваты, которые могут образовывать соединения формулы (I), а также их соли. Такие сольваты, например, представляют собой гидраты, алкоголяты и т.п.
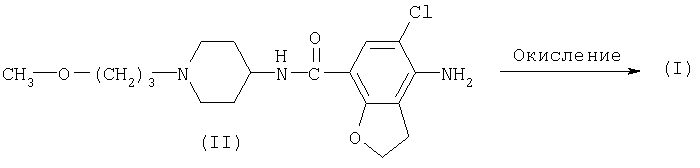
Соединения формулы (I) можно получать, следуя известным в данной области техники процедурам для преобразования трехвалентного азота в его N-оксидную форму. Указанную реакцию N-окисления, как правило, можно осуществлять путем взаимодействия соединения формулы (II) с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды включают, например, перекись водорода, перекиси щелочных или щелочноземельных металлов, например пероксид натрия, пероксид калия; подходящие органические пероксиды могут включать пероксикислоты, такие как, например, бензолкарбопероксокислота или галогензамещенная бензолкарбопероксокислота, например 3-хлорбензолкарбопероксокислота, пероксоалкановые кислоты, например пероксоуксусная кислота, алкилгидропероксиды, например трет-бутилгидропероксид. Подходящими растворителями, например, являются вода, низшие спирты, например этанол и т.п., углеводороды, например толуол, кетоны, например 2-бутанон, галогенированные углеводороды, например дихлорметан, и смеси таких растворителей.
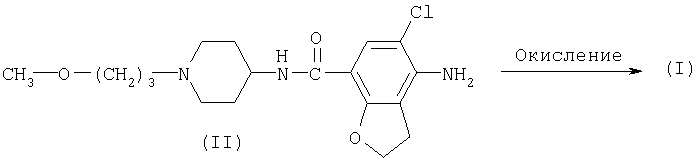
Соединения формулы (I), как получены указанным выше способом, можно синтезировать в форме смеси цис- и транс-стереоизомеров, которые можно разделить известными из уровня техники методами разделения. Альтернативно, в зависимости от реакционных условий реакции окисления, продуктом указанной реакции окисления может быть либо цис-стереоизомер, либо трансстереоизомер.
Соединения формулы (II) являются известными соединениями и могут быть получены в соответствии с процедурой, описанной в WO-96/16060.
При пероральном введении N-оксидные соединения формулы (I) по настоящему изобретению преобразуются в соединения формулы (II) в результате бактериального или ферментного восстановления. Кроме того, было обнаружено, что системное воздействие соединений формулы (II), неожиданно, было ниже при пероральном введении N-оксидного соединения формулы (I) в сравнении с пероральным введением эквимолярного количества соединения формулы (II), тогда как эффект улучшения моторики сохранялся. Более низкое системное воздействие может быть выгодным для снижения потенциальных неблагоприятных эффектов.
Соединения формулы (II), имеющие родовое название "прукалоприд", способствуют как холинергической, так и нехолинергической неадренергической (NANC) стимулирующей нейротрансмиссии и стимулируют моторику толстого кишечника и дефекацию у животных. Эти соединения не обладают сродством к 5-НТ2А и 5-НТ3А рецепторам, но являются сильными и селективными агонистами 5-НТ4А рецепторов. Прукалоприд индуцирует сокращения мегаколона в толстой кишке, которые распространяются по всей длине толстой кишки как волна перистальтики, и поэтому обладает значительным эффектом усиления моторики в толстом кишечнике. Кроме того, считают, что прукалоприд также полезен для лечения нарушений моторики верхнего отдела желудочно-кишечного тракта, таких как гастроэзофагеальный рефлюкс.
Учитывая его энтерокинетические свойства, прукалоприд является полезным при лечении нарушений моторики системы кишечника, таких как гастропарез, диспепсия, запор, псевдонепроходимость, отсутствие тонуса кишечника, послеоперационное отсутствие тонуса кишечника, синдром раздраженной толстой кишки (IBS) и индуцированное лекарственными средствами замедленное прохождение через желудочно-кишечный тракт. Эти соединения также можно использовать для облегчения очищения толстого кишечника или для облегчения интубации и/или эндоскопии. Указанный способ включает системное введение эффективного для стимуляции моторики количества прукалоприда теплокровным животным, включая человека.
В свете применимости соединений формулы (I) следует то, что настоящее изобретение также обеспечивает способ лечения теплокровных животных, включая человека (далее будет использовано общее название "пациенты"), страдающих нарушениями моторики кишечной системы. Следовательно, обеспечивается способ лечения для облегчения симптомов у пациентов, страдающих от таких состояний, как, например, запор, псевдонепроходимость, отсутствие тонуса кишечника, послеоперационное отсутствие тонуса кишечника, синдром раздраженной толстой кишки (IBS) и индуцированное лекарственными средствами замедленное прохождение через желудочно-кишечный тракт, и для очистки толстого кишечника.
Следовательно, предлагается применение соединения формулы (I) в качестве лекарственного средства и, в частности, применение соединения формулы (I) для изготовления лекарственного средства для лечения состояний, связанных с нарушенной моторикой или проходимостью верхнего и нижнего отдела желудочно-кишечного тракта.
Для получения фармацевтических композиций по настоящему изобретению эффективное количество конкретного соединения, в форме основания или кислотно-аддитивной соли, в качестве активного ингредиента объединяют с получением однородной смеси с фармацевтически приемлемым носителем, при этом такой носитель может принимать самые различные формы в зависимости от формы препарата, предназначенного для введения. Такие фармацевтические композиции желательны в унитарной дозированной форме, подходящей предпочтительно для перорального введения, ректального введения или введения путем парентеральной инъекции. Например, при получении композиций в дозированной форме для перорального введения можно использовать любую обычную фармацевтическую среду, такую как, например, воду, гликоли, масла, спирты и т.п. для жидких препаратов для перорального введения, таких как суспензии, сиропы, эликсиры и растворы; или твердые носители, такие как крахмалы, сахара, каолин, лубриканты, связующие, дезинтегранты и т.п. для получения порошков, пилюль, капсул и таблеток. Из-за простоты введения таблетки и капсулы представляют наиболее выгодную единичную дозированную форму для перорального введения, в этом случае, очевидно используются твердые фармацевтические носители. Для парентеральных композиций носитель обычно включает стерильную воду, по меньшей мере, большей частью, хотя могут быть включены и другие ингредиенты, такие как вещества, способствующие растворению. Растворы для инъекций, например, можно получать, используя носитель, который включает физиологический раствор, раствор глюкозы или смеси физиологического раствора и раствора глюкозы. Суспензии для инъекций, можно также получать, используя соответствующие жидкие носители, суспендирующие вещества и т.п. В композициях, подходящих для чрескожного введения, носитель необязательно включает вещества, улучшающие проникновение, и/или подходящие смачивающие вещества, необязательно объединенные с подходящими добавками любой природы, которые используют в небольших пропорциях, при этом такие добавки не вызывают значительного вредного воздействия на кожу. Такие добавки могут способствовать введению при нанесении на кожу и/или могут быть полезными для получения желаемых композиций. Такие композиции можно вводить различными путями, например, в виде чрескожного пластыря, в виде пятна, в форме мази. Кислотно-аддитивные соли соединений формулы (I) из-за их повышенной растворимости в воде по сравнению с соответствующей формой основания, очевидно, являются более подходящими для получения жидких композиций.
Особенно выгодно составлять (готовить) указанные выше фармацевтические композиции в единичной дозированной форме для простоты введения и равномерного дозирования. Единичная дозированная форма, как этот термин используется в описании изобретения и в формуле изобретения, относится к физически дискретным единицам, подходящим в качестве единиц дозирования, при этом каждая единица содержит предварительно определенное количество активного ингредиента, рассчитанное для получения желаемого терапевтического эффекта, в сочетании с необходимым фармацевтическим носителем. Примеры таких единичных дозированных форм представляют собой таблетки (включая таблетки с насечками или с покрытием), капсулы, пилюли, пакетики с порошком, облатки, растворы или суспензии для инъекций, мерные чайные ложечки, мерные столовые ложечки и т.п., и их множественные сегрегированные формы.
Для перорального введения фармацевтические композиции могут иметь форму твердых дозированных форм, например, таблетки (как только для глотания, так и жевательные формы), капсулы или гелевые капсулы, полученные традиционными способами с фармацевтически приемлемыми эксципиентами, такими как связующие (например, предварительно желатинизированный кукурузный крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например, лактоза, микрокристаллическая целлюлоза или фосфат кальция); лубриканты (например, стеарат магния, тальк или диоксид кремния); дезинтегранты (например, картофельный крахмал или натрий крахмалгликолят); или смачивающие вещества (например, лаурилсульфат натрия). На таблетки можно наносить покрытие известными из уровня техники методами.
Жидкие препараты для перорального введения могут иметь форму, например, растворов, сиропов или суспензий, или они могут иметь форму сухого продукта для восстановления водой или другим подходящим носителем перед использованием. Такие жидкие препараты можно получать обычными способами, необязательно с фармацевтически приемлемыми добавками, такими как суспендирующие вещества (например, сироп сорбита, метилцеллюлоза, гидроксипропилметилцеллюлоза или гидрированные пищевые жиры); эмульгирующие вещества (например, лецитин или аравийская камедь); неводные носители (например, миндальное масло, жирные сложные эфиры или этиловый спирт); и консерванты (например, метил- или пропил п-гидроксибензоаты или сорбиновая кислота).
Фармацевтически приемлемые подсластители предпочтительно включают, по меньшей мере, один сильный подсластитель, такой как сахарин, натриевый или кальциевый сахарин, аспартам, ацесульфам кальция, цикламат натрия, алитам, дигидрохальконовый подсластитель, монеллин, стевиозид или сахароза (4,1',6'-трихлор-4,1',6'-тридезоксигалактосахароза), предпочтительно сахарин, натриевый или кальциевый сахарин, и, необязательно, объемный подсластитель, такой как сорбит, маннит, фруктоза, сахароза, мальтоза, изомальт, глюкоза, гидрированный сироп глюкозы, ксилит, карамель или мед.
Сильные подсластители обычно используют в низких концентрациях. Например, в случае натриевого сахарина концентрация может находиться в пределах от 0,04% до 0,1% (мас./об.) в расчете на общий объем готового препарата и предпочтительно составляет около 0,06% в препаратах низкого дозирования и около 0,08% в препаратах высокого дозирования. Объемный подсластитель можно эффективно использовать в более высоких количествах, от около 10% до около 35%, предпочтительно от около 10% до 15% (мас./об.).
Фармацевтически приемлемые отдушки, которые могут маскировать горький вкус ингредиентов, в препаратах низкого дозирования предпочтительно представляют собой фруктовые отдушки, такие как вишневую, малиновую, черносмородиновую или клубничную отдушку. Комбинация двух отдушек может дать очень хорошие результаты. В препаратах высокого дозирования могут потребоваться более сильные отдушки, такие как карамельно-шоколадная отдушка, мятно-охлаждающая отдушка, отдушка с фантазийным вкусом и подобные фармацевтически приемлемые сильные отдушки. Каждая отдушка может присутствовать в готовой композиции в концентрации от 0,05% до 1% (мас./об.). Выгодно использовать комбинации указанных сильных отдушек. Предпочтительно, используют отдушку, которая не претерпевает никаких изменений или не утрачивает свой вкус и цвет в кислотных условиях композиции.
Соединения по настоящему изобретению также можно составлять в виде депо препаратов. Такие долго действующие композиции можно вводить путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Так, например, соединения можно составлять (готовить) с подходящими полимерными или гидрофобными веществами (например, в виде эмульсий в подходящем масле) или ионообменными смолами, или в виде производных с умеренным растворением, например в виде умеренно растворимых солей.
Соединения по настоящему изобретению можно составлять для парентерального введения путем инъекции, удобно внутривенной, внутримышечной или подкожной инъекции, например, путем болюсной инъекции или непрерывной внутривенной инфузии. Препараты для инъекций могут быть представлены в виде единичных дозированных форм, например в ампулах, или многодозовых контейнерах, с добавлением консервантов. Композиции можно получать в таких формах, как суспензии, растворы или эмульсии в масляных или водных носителях, и они могут содержать вещества, способствующие изготовлению лекарственных форм, такие как изотонические, суспендирующие, стабилизирующие и/или диспергирующие вещества. Альтернативно, активный ингредиент может быть в форме порошка для восстановления перед применением с использованием подходящего носителя, например, стерильной апирогенной воды.
Соединения по настоящему изобретению также можно представить в композиции для ректального введения, такой как суппозитории или удерживаемые клизмы, например, содержащие традиционные основы для суппозиториев, такие как масло какао или другие глицериды.
Композиции по настоящему изобретению могут, необязательно, включать вещество против газообразования, такое как симетикон, альфа-D-галактозидаза и т.п. Кроме того, композиции могут, необязательно, включать другие активные ингредиенты, например, антагонисты δ-опиата, такие как нальтриндол и т.п.
Предполагается, что терапевтически эффективное количество будет, как правило, составлять от около 0,001 мг/кг до около 2 мг/кг веса тела, предпочтительно от около 0,02 мг/кг до около 0,5 мг/кг веса тела. Способ лечения может также включать введение активного ингредиента по схеме от двух до четырех приемов в день или как требуется.
Количество прукалоприд-N-оксида или его фармацевтически приемлемой кислотно-аддитивной соли, необходимое как суточная доза при лечении, будет варьироваться в зависимости от пути введения, природы состояния, подлежащего лечению, и возраста, веса и состояния пациента, и, в конечном счете, будет определяться лечащим врачом. Однако, как правило, подходящая суточная доза находится в пределах от около 0,05 до около 200 мг в день, в частности, от около 0,1 до 20 мг в день, и более конкретно, от около 0,5 до 10 мг в день. Подходящая суточная доза для применения в профилактических целях обычно находится в этих же пределах. Может быть подходящим введение необходимой дозы в виде двух, трех, четырех или более субдоз с подходящими интервалами в течение суток. Введение можно осуществлять до или после приема пищи (например, до обеда или после обеда).
Экспериментальная часть
А. Получение
Для некоторых химических веществ используется химическая формула, например, CH3CN - для ацетонитрила, CH2Cl2 - для дихлорметана, NH4OAc - для ацетата аммония и СН3ОН - для метанола.
Пример А.1
4-Амино-5-хлор-2,3-дигидро-N-[1-(3-метоксипропил)-4-пиперидинил]-7-бензофуранкарбоксамид (0,012 моль) растворяли в дихлорметане (200 мл) и добавляли 3-хлорбензолкарбопероксокислоту (0,015 моль). Смесь перемешивали в течение 3 часов при комнатной температуре. Смесь разбавляли водным раствором аммиака и полученный осадок отфильтровывали и перекристаллизовывали из CH3CN/2-пропанола. Осадок отфильтровывали и сушили с получением 2,15 г цис-4-амино-5-хлор-2,3-дигидро-N-[1-(3-метоксипропил)-4-пиперидинил]-7-бензофуранкарбоксамида, N-оксид моногидрата (соединение (1), т.пл. 179,8оС).
Пример А.2
4-Амино-5-хлор-2,3-дигидро-N-[1-(3-метоксипропил)-4-пиперидинил]-7-бензофуранкарбоксамид (0,05 моль) растворяли в дихлорметане (500 мл) и добавляли 3-фенил-2-(фенилсульфонил)оксазиридин (реагент Davis) (0,055 моль). Полученную смесь перемешивали в течение 4 часов при комнатной температуре. Смесь концентрировали до объема около 200 мл и полученный осадок отфильтровывали, сушили и очищали колоночной хроматографией на силикагеле (элюент: CH2Cl2/CH3ОН 95/5). Чистые фракции собирали и растворитель выпаривали. Остаток растирали в DIPE, отфильтровывали, сушили и очищали при помощи высокоэффективной жидкостной хроматографии над RP-18 (элюент: (0,5% NH4ОАс в Н2О)/CH3CN 85/15 об./об.). Чистые фракции собирали и растворитель выпаривали. Остаток растирали в DIPE, отфильтровывали и сушили с получением 1,26 г транс-4-амино-5-хлор-2,3-дигидро-N-[1-(3-метоксипропил)-4-пиперидинил]-7-бензофуранкарбоксамида, N-оксид моногидрата (соединение (2), т.пл. 230оС).
В. Фармакологические примеры
Пример В.1
Двум самцам собак породы Beagle перорально вводили 1 мл испытываемой композиции, включающей 2,5 мг/кг 4-амино-5-хлор-2,3-дигидро-N-[1-(3-метоксипропил)-4-пиперидинил]-7-бензофуранкарбоксамида ("прукалоприд").
После периода вымывания в течение четырех недель тем же двум собакам перорально вводили 1 мл испытываемой композиции, включающей 2,61 мг/кг соединения (1).
Образцы крови брали через яремную вену сразу после дозирования (контрольный образец) и на 0,25 ч, 0,5 ч, 1 ч, 1,5 ч, 2 ч, 4 ч, 6 ч, 8 ч и 24 ч после дозирования. Аликвоты 10 мл собирали в пробирки, содержащие EDTA. Сразу после взятия проб крови получали образцы плазмы путем центрифугирования при примерно 1700g в течение примерно 10 минут.
Концентрации прукалоприда в образцах плазмы определяли методом ЖХ/MS/MS. Количественный предел для прукалоприда составил 5,0 нг/мл.
На основании данных концентрации в плазме для каждого отдельного времени, используя фактические временные точки взятия проб, определяли следующие фармакокинетические параметры для прукалоприда после перорального введения прукалоприда и соединения (1), которые обобщены в таблице.
Сmax = пик концентрации в плазме, определенный путем визуального изучения данных,
Тmax = время достижения пика концентрации в плазме, определенное путем визуального изучения данных,
AUC0-∞ - площадь под кривой концентрации в плазме в зависимости от времени, которая экстраполирована до бесконечности.
после одноразового перорального введения
прукалоприда и соединения (1)
Как можно видеть из таблицы, пероральное введение соединения (1) дает более низкий пик концентрации в плазме Сmax прукалоприда и большее время Тmax для достижения указанного Сmax. Следовательно, системное воздействие прукалоприда после перорального введения соединения (1) значительно ниже, чем после перорального введения самого прукалоприда.
Настоящее изобретение относится к новому бензамидному производному формулы 1, его стереохимически изомерным формам и его фармацевтически приемлемым кислотно-аддитивным солям, фармацевтическим композициям, содержащим указанное новое соединение, способам получения указанных соединений и композиций и их применению в качестве лекарственного средства при лечении нарушений моторики желудочно-кишечного тракта. 4 н. и 4 з.п. ф-лы, 1 табл.
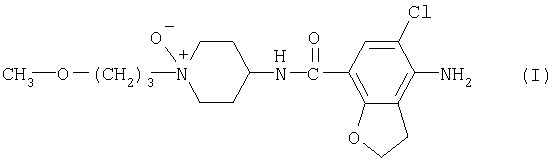
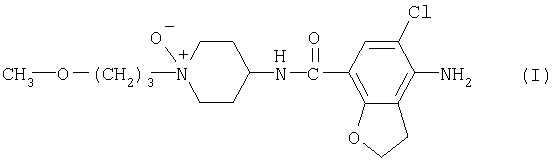
и его стереохимически изомерные формы и фармацевтически приемлемые кислотно-аддитивные соли.
| WO 9616060 A1, 30.05.1996 | |||
| Устройство для измерения момента | 1972 |
|
SU445862A1 |
| Горизонтальный ветряный двигатель | 1932 |
|
SU30640A1 |
| 4-АМИНО-5-ХЛОР-2,3-ДИГИДРО-N-[1-(3-МЕТОКСИПРОПИЛ)-4-ПИПЕРИДИНИЛ]-7-БЕНЗОФУРАНКАРБОКСАМИД ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ КИСЛОТНО-АДДИТИВНАЯ СОЛЬ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1995 |
|
RU2154643C2 |
| RU 2070884 C1, 27.12.1996. | |||
Авторы
Даты
2007-06-27—Публикация
2003-01-13—Подача