Изобретение относится к замещенным тетрациклическим производным оксазепина и тиазепина, имеющим антипсихотическую, сердечно-сосудистую и гастрокинетическую активность, и способу их получения. Кроме того, изобретение относится к композициям, содержащим их, так же как их применению в качестве лекарственного средства.
Соединения подобной структуры описываются в патенте США 4039558, который раскрывает производные пирролидинодибензоазепина, -оксазепина, -тиазепина и -диазепина, имеющие антигистаминовые, седативные и антидепрессивные свойства. ЕР-А-0421823 описывает подобные производные дибензопиразино- или бензопиридопиразиноазепина, обладающие противоаллергической и противоастматической активностью. Данные соединения отличаются от них присутствием изоксалидинового кольца и их фармакологическими свойствами.
Изобретение относится к соединениям формулы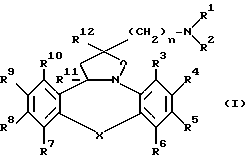
их фармацевтически приемлемым кислотно- или основно-аддитивным солям и стереохимически изомерным формам, а также их N-оксидным формам, где:
R1 и R2 каждый независимо представляет водород; C1-6-алкил; C1-6-алкилкарбонил; тригалогенметилкарбонил; C1-6-алкил, замещенный гидрокси, C1-6-алкилокси, карбоксилом, C1-6-алкилкарбонилокси, C1-6-алкилоксикарбонилом или арилом; или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, могут образовать кольцо морфолинила или радикал формулы: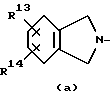
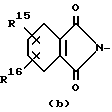
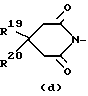
где R13, R14, R15, и R16 каждый независимо представляет водород, галоген, трифторметил или C1-6-алкил;
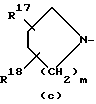
m представляет 1, 2 или 3;
R17, R18, R19 и R20 каждый независимо представляет водород или C1-6-алкил; или R19 и R20 , взятые вместе, могут образовать двухвалентный радикал C4-5-алкандиил;
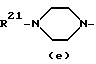
R21 представляет водород; C1-6-алкил; C1-6-алкилкарбонил; тригалогенметилкарбонил; C1-6-алкилоксикарбонил; арил; ди(арил)метил; C1-6-алкил, замещенный гидрокси, C1-6-алкилокси, карбоксилом, C1-6-алкилкарбонилокси, C1-6-алкилоксикарбонилом или арилом;
R3, R4, R5, R6, R7, R8, R9 и R10 каждый независимо представляют водород, галоген, циано, гидрокси, трифторметил, трифторметокси, карбоксил, нитро, амино, моно- или ди(С1-6-алкил)амино, С1-6-алкилкарбониламино, аминосульфонил, моно- или ди(С1-6-алкил)аминосульфонил, C1-6-алкил, C1-6-алкилокси, C1-6-алкилкарбонил, C1-6-алкилоксикарбонил;
R11 представляет водород, C1-6-алкил или трифторметил;
R12 представляет водород: C1-6-алкил, циано или трифторметил;
n представляет 0, 1, 2, 3, 4, 5 или 6;
X представляет O, S, S(= О) или S(= О)2;
арил представляет фенил или фенил, замещенный 1, 2 или 3 заместителями, выбранными из галогена, гидрокси, C1-6-алкила и трифторметила.
В предшествующих определениях C1-6алкил определяет насыщенные углеводородные радикалы с нормальной или разветвленной цепью, имеющие от 1 до 6 атомов углерода, такие, как, например, метил, этил, пропил, бутил, 1-метилпропил, 1,1-диметилэтил, пентил, гексил; C4-5-алкандиил определяет двухвалентные насыщенные углеводородные радикалы с нормальной или разветвленной цепью, имеющие 4 или 5 атомов углерода, такие, как, например, 1,4-бутандиил, 1,5-пентандиил; галоген представляет собой фтор, хлор, бром и иод.
Подразумевается, что фармацевтически приемлемые кислотно-аддитивные соли, упоминаемые здесь выше, содержат терапевтически активные нетоксичные кислотно-аддитивные солевые формы, которые способны образовать соединения формулы (I). Эти соли можно получить обработкой соединений формулы (I) в виде оснований подходящими кислотами, такими как неорганические кислоты, например, галогенводородной кислотой, например, хлористоводородной или бромистоводородной кислотой, серной, азотной, фосфорной и подобными кислотами; или органические кислоты, например, уксусной, гидроксиуксусной, пропановой, молочной, пировиноградной, щавелевой, малоновой, янтарной, малеиновой, фумаровой, яблочной, винной, лимонной, метансульфокислотой, этансульфокислотой, бензослульфокислотой, п-толуолсульфокислотой, цикламиновой, салициловой, п-аминосалициловой, памоевой и подобными кислотами.
Соединения формулы (I), содержащие кислотные части, могут быть также превращены в их формы терапевтически активных нетоксичных солей металлов или аддитивных солей с амином обработкой подходящими органическими или неорганическими основаниями. Формы подходящих солей оснований содержат, например, аммониевые соли, соли щелочных и щелочноземельных металлов, например, литиевые, натриевые, калиевые, магниевые, кальциевые соли и тому подобные, соли с органическими основаниями, например, соли с бензатином, N-метил-D-глюкамином, гидрабамином и соли с аминокислотами, такими, как, например, аргинин, лизин и тому подобные.
Наоборот, эти солевые формы можно превратить в свободные формы обработкой подходящим основанием или кислотой.
Термин аддитивная соль, используемый здесь выше, содержит также сольваты, которые способны образовать соединения формулы (I), также как их соли. Такими сольватами являются, например, гидраты, алкоголяты и тому подобные.
Подразумевается, что N-оксидные формы соединений формулы (I) содержат те соединения формулы (I), где один или несколько атомов азота окисляются в так называемый N-оксид, в частности те N-оксиды, где азот, несущий заместители R1 и R2, N-окислен.
Термин "стереохимически изомерные формы", используемый здесь ранее и в дальнейшем, обозначает все возможные изомерные формы, в которых соединения формулы (I) могут иметь место. Если не упоминается или не указывается особо, химические названия соединений означают смесь, в частности рацемическую смесь, всех возможных стереохимически изомерных форм, причем эти смеси содержат все диастереомеры и энантиомеры базовой молекулярной структуры. Ясно подразумевается, что формула (I) заключает в себя стереохимически изомерные формы соединений формулы (I) и смеси таких форм.
Нумерация тетрациклической системы, присутствующей в соединениях формулы (I), как определяется Кемикал Абстрактс, показывается в формуле (I')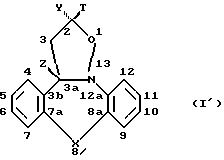
Соединения формулы (I) находятся в виде "цис" и "транс"-изомеров. Такие термины относятся к положению заместителей на оксазолидиновом кольце и находятся в соответствии с номенклатурой Кемикал Абстрактс. Номенклатура необычна в том, что атом углерода 3b, являющийся частью циклической системы, не рассматривается в качестве соответствующего заместителя атома углерода 3а. Когда устанавливают конфигурацию, рассматривают заместитель на атоме углерода 3а (*то есть "Z") и заместитель с наибольшим приоритетом на атоме углерода 2 (то есть либо "Т", либо "Y"). Когда "Z" и заместитель с наибольшим приоритетом на атоме углерода 2 находятся на одной и той же стороне средней плоскости, определяемой кольцом изоксазолидина, то конфигурацию обозначают "цис", если нет, конфигурацию обозначают как "транс".
Соединения формулы (I) имеют, по меньшей мере, два асимметрических центра, а именно, атом углерода 3а, несущий заместитель R11, и атом углерода 2, несущий заместитель R12. Эти асимметрические центры и любой другой асимметрический центр, который может присутствовать, обозначаются символами R и S.
Всякий раз при использовании здесь в дальнейшем подразумевается, что термин соединения формулы (I) включает в себя также фармацевтически приемлемые кислотно-аддитивные соли, основно-аддитивные соли и все стереоизомерные формы и также N-оксидные формы.
Особые группы соединений формулы (I) составляют соединения, где применяют одно или несколько следующих ограничений:
a) R1 и R2 каждый независимо представляет водород, C1-6-алкил, тригалогенметилкарбонил, C1-6-алкил, замещенный карбоксилом или C1-6-алкилоксикарбонилом, или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют кольцо морфолинила или радикал формулы (b), (с), (d), (е);
b) R15 и R16 представляют водород;
с) R17 и R18 представляют водород и m представляет 1 или 2;
d) R19 и R20 берут вместе для образования двухвалентного радикала C4-5-алкандиила;
е) R21 представляет водород, С1-6-алкил, ди(арил)метил, C1-6-алкилоксикарбонил, тригалогенметилкарбонил, C1-6-алкил, замещенный гидрокси, карбоксилом, C1-6-алкилоксикарбонилом;
f) R3, R4, R5, R6 каждый независимо представляет водород, галоген, трифторметил, C1-6-алкилоксикарбонил, C1-6-алкиламиносульфонил, карбоксил;
g) R7, R8, R9, R10 каждый независимо представляет водород, галоген, трифторметил, C1-6-алкилоксикарбонил, C1-6-алкиламиносульфонил, карбоксил;
h) R11 и R12 представляют водород;
i) Х представляет О, S или S(= О).
Интересными соединениями являются те соединения формулы (I) или подгрупп, как определено выше, где R3, R5, R6, R7, R10 , R11 и R12 представляют водород; и в частности, R4, R8, и R9 каждый независимо выбирают из C1-6-алкилоксикарбонила и карбоксила, предпочтительно R4, R8 и R9 каждый независимо выбирают из водорода, галогена, трифторметила и С1-6-алкиламиносульфонила.
Интересными соединениями являются также те соединения формулы (I) или подгрупп, как определено выше, где n представляет 1, 2 или 3, и X представляет О.
Далее интересными соединениями являются те соединения формулы (I) или подгрупп, как определено выше, где n представляет 1, и X представляет S или S(= О).
Более интересными соединениями являются те интересные соединения, у которых R1 и R2 каждый независимо выбирают из водорода, метила, C1-6-алкила, замещенного карбоксилом или C1-6-алкилоксикарбонилом, или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют кольцо морфолинила или радикал формулы (b), (с) или (е).
Предпочтительными соединениями являются те соединения формулы (I), где X представляет О, n представляет 1, 2 или 3; R1 и R2 оба представляют метил или вместе атомом азота, к которому они присоединены, образуют радикал формулы (b), в котором R15 и R16 оба представляют водород, или формулы (е), в которой R21 представляет водород, C1-6-алкил или трифторметилкарбонил, R4 и R9 каждый независимо выбирают из водорода, галогена, трифторметила, C1-6-алкиламиносульфонила, R3, R5-R8 и R10-R12 представляют водород.
Наиболее предпочтительными соединениями являются:
цис-2-[(диметиламино)метил]-3,3а-дигидро-N-метил-2Н-ди-бенз[b,f]изоксазоло[2,3-d] [1,4]оксазепин-11-сульфамид;
цис-11-хлор-3,3а-дигидро-2-(1-пиперазинилметил)-2Н-ди-бенз[b, f] изоксазоло[2,3-d] [1,4]оксазепин;
цис-2-[[3,3а-дигидро-11-(трифторметил)-2Н-дибенз[b,f] изоксазоло-[2,3-d] [1,4]оксазепин-2-ил]метил]-1Н-изоиндол-1,3-(2Н)-дион и
цис-11-хлор-3,3a-дигидpo-N, N-диметил-2H-дибенз[b, f]-изоксазоло [2,3-d] [1,4]оксазепин-2-пропанамин,
их стереохимически изомерные формы и фармацевтически приемлемые кислотно-аддитивные соли, а также их N-оксидные формы.
Интересно, что соединения формулы (1) довольно просто синтезировать. Вообще их можно получить 1,3-диполярным циклоприсоединением диенофила формулы (III) и промежуточного соединения формулы (II). В промежуточных соединениях (II) и (III) и в любом другом промежуточном соединении, упоминаемом здесь в дальнейшем, R1-R12 и X такие, как определено здесь ранее, если не оговорено особо. Это 1,3-диполярное циклоприсоединение можно стандартно проводить смешиванием реагентов, необязательно в инертном растворителе таком, как, например, ароматический растворитель, например, толуол, простой эфир, например, тетрагидрофуран, или смесь таких растворителей. Перемешивание и повышенные температуры или повышенное давление могут повысить скорость реакции. Реакция промежуточного соединения (II) с промежуточным соединением (III) на практике региоселективно (селективно по положению) дает соединения формулы (I)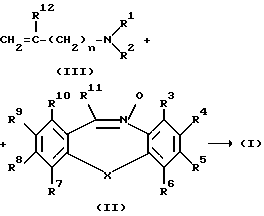
В этом и следующих способах получения продукты реакции можно выделить из реакционной смеси и, если необходимо, далее очистить в соответствии с методиками, обычно известными в данной области, такими, как, например, экстракция, кристаллизация, растирание и хроматография.
Соединения формулы (I) можно также превратить друг в друга известными в данной области методиками. Например:
а) соединение формулы (I), где R1 и R2, взятые вместе с атомом азота, к которому они присоединены, образуют радикал формулы (b), можно превратить в соответствующий первичный амин обработкой гидразином или щелочью;
b) соединение формулы (1), где R1 или R2 представляет трифторметилкарбонил, можно превратить в соответствующий первичный или вторичный амин гидролизом водной щелочью;
с) соединение формулы (I), где R1 или R2 представляет C1-6-алкил, замещенный C1-6-алкилкарбонилокси, можно гидролизовать в соединение формулы (I), где R1 или R2 представляет C1-6-алкил, замещенный гидрокси;
d) соединение формулы (I), где R1 и R2 оба представляют водород, можно моно- или ди-N-алкилировать в соответствующий амин;
е) соединение формулы (I), где R1 и R2 оба представляют водород, можно N-ацилировать в соответствующий амид;
f) соединение формулы (I), содержащее C1-6-алкилоксикарбонильную группу, можно гидролизовать в соответствующую карбоновую кислоту.
Соединения формулы (I), где X не является S, можно превратить в соответствующие N-оксидные формы известными в данной области способами для превращения трехвалентного азота в его N-оксидную форму. Эту реакцию N-окисления можно проводить обычно путем реакции исходного материала формулы (I) с 3-фенил-2-(фенилсульфонил)оксазиридином или с подходящим органическим или неорганическим пероксидом. Подходящие неорганические пероксиды содержат, например, пероксид водорода, пероксиды щелочных или щелочноземельных металлов, например, пероксид натрия, пероксид калия, подходящие органические пероксиды могут содержать надкислоты, такие, как, например, бензолнадкарбоновая кислота или галогензамещенная бензолнадкарбоновая кислота, например, 3-хлорбензолнадкарбоновая кислота, надалкановые кислоты, например, надуксусная кислота, алкилгидропероксиды, например, трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие алканолы, например, этанол и тому подобные, углеводороды, например, толуол, кетоны, например, 2-бутанон, галогенированные углеводороды, например, дихлорметан, и смеси таких растворителей.
Промежуточные соединения формулы (II), где X представляет 0, S(= О) или S ( = О)2, причем эти промежуточные соединения представляются формулой (11-а), можно получить окислением промежуточного соединения формулы (IV) подходящим окислителем, таким, как, например, 2-бензолсульфонил-3-фенилоксазиридин, пероксид водорода, трет-бутилгидропероксид или метахлорнадбензойная кислота.
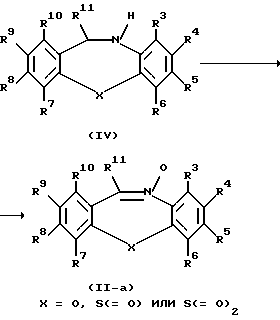
Это окисление проводят в инертном растворителе при температурах в диапазоне между -20oC и 50oC, предпочтительно между 0oC и комнатной температурой. Подходящими растворителями являются, например, вода, хлорированные углеводороды, например, хлороформ, ароматические углеводороды, например, толуол, спирты, например, метанол, кетоны, например, 4-метил-2-пентанон, или смесь таких растворителей. Когда используют пероксидные окислители, скорость реакции можно повысить путем использования металлических катализаторов, таких, как, например, Na2WO4, VO(ацетилацетонат)2, Ti(OBu)4 и MoO2(ацетилацетонат)2, необязательно в инертной атмосфере реакции, такой, как, например, аргон.
Альтернативно, промежуточные соединения формулы (II), где R11 представляет водород и R3-R10 такие, как они были определены здесь выше, но другие, чем нитрогруппа, причем эти промежуточные соединения представляются формулой (11-b), можно получить восстановлением нитрогруппы промежуточного соединения формулы (V) в присутствии воды и подходящего восстановителя, такого, как, например, цинк или железо, с последующей in situ внутримолекулярной циклизацией в присутствии слабой кислоты, такой, как, например, хлорид аммония или уксусная кислота. Эту восстановительную циклизацию проводят в инертном растворителе, таком, как, например, 1,4-диоксан. Перемешивание и повышенные температуры могут повысить скорость реакции. В промежуточном соединении (V) R3-R10 такие, как они были определены в промежуточных соединениях формулы (II-b).
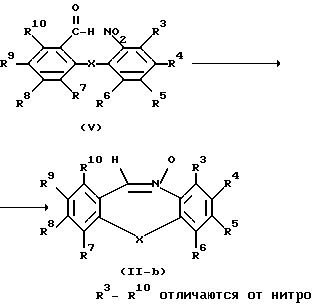
Чистые стереохимически изомерные формы соединений формулы (I) можно получить известными в данной области способами. Диастереомеры можно разделить физическими способами, такими, как селективная кристаллизация и хроматографические методы, например, противоточное распределение, жидкостная хроматография и тому подобные.
Соединения формулы (I), получаемые здесь ранее описанными способами, обычно являются рацемическими смесями энантиомеров, которые можно разделить известными в данной области способами расщепления. Рацемические соединения формулы (I), которые достаточно основные или кислотные, можно превратить в соответствующие диастереомерные солевые формы реакцией с подходящей хиральной кислотой или, соответственно, хиральным основанием. Эти диастереомерные солевые формы затем разделяют, например, селективной или фракционной кристаллизацией и энантиомеры выделяют из них при помощи щелочи или кислоты. Альтернативный способ разделения энантиомерных форм соединений формулы (I) включают жидкостную хроматографию, использующую хиральную стационарную фазу. Эти чистые стереохимически изомерные формы можно также получить из соответствующих чистых стереохимически изомерных форм подходящих исходных материалов при условии, что реакция протекает стереоспецифически. Предпочтительно, если необходим определенный стереоизомер, чтобы это соединение синтезировали стереоспецифическими способами получения. Эти способы должны выгодно использовать энантиомерно чистые исходные материалы.
Фармакологическую активность соединений согласно изобретению оценивают одним или несколькими следующими испытаниями, испытаниями на связывание in vitro 5-НТ2-рецепторов, испытанием на комбинированные апоморфин, триптамин и норэфедрин на крысах, который описывается в Arch. Int. Pharmacodyn., 227, 238 - 253 (1977); "мХФП-испытанием на крысах"; и "Испытанием с приподнятым и освещенным плюс-лабиринтом на крысах". Последние два испытания оба описываются здесь в дальнейшем. Дополнительно, данные соединения демонстрируют интересную фармакологическую активность в "Tail Suspension Test" и также в "Испытании на LSD-лекарственную дискриминацию", которое описывается в Drug Dev. Res. , 18, 119 - 144 (1989). Другим интересным свойством соединений формулы (I) является то, что они подавляют индуцированное амфетамином стереотипическое поведение у крыс.
С точки зрения их фармакологических свойств, соединения формулы (I) полезны в качестве терапевтических средств при лечении или предупреждении нарушений центральной нервной системы, подобных тревоге, депрессии и легкой степени депрессии, биполярным нарушениям, нарушениям сна, сексуальным расстройствам, психозам, пограничным случаям психоза, шизофрении, мигрени, изменению личности или навязчивым компульсивным нарушениям, социальным фобиям или паническим приступам, органическим психическим расстройствам, психическим расстройствам у детей, агрессии, нарушениям памяти и нарушениям позы у старых людей, аддикции, ожирению, булимии и аналогичным нарушениям. В частности, данные соединения можно использовать в качестве анксиолитиков, антидепрессантов и в качестве средств, имеющих способность перевешивать аддиктивные свойства лекарственных средств при злоупотреблении ими.
Соединения формулы (I) можно также использовать в качестве терапевтических средств при лечении двигательных нарушений. Может быть выгодным использование данных соединений в комбинации с классическими терапевтическими средствами для таких нарушений.
Соединения этого изобретения могут также служить в качестве терапевтических средств для лечения или предупреждения повреждения нервной системы, вызванного травмой, ударом, нейродегенеративными болезнями и тому подобными; сердечно- сосудистых болезней, подобных высокому кровяному давлению, тромбозу, удару и тому подобных; желудочно-кишечных нарушений, подобных дисфункции перистальтики желудочно-кишечного тракта и тому подобных. Данные соединения могут быть также полезными в качестве противосудорожных средств.
В виду указанных выше применений соединений формулы (I) следует, что данное изобретение относится также к способу лечения теплокровных животных, страдающих от таких болезней, причем этот способ содержит системное введение терапевтического количества соединения формулы (I), эффективного при лечении описанных выше нарушений.
Данное изобретение поэтому относится также к соединениям формулы (I), определяемым здесь ранее, для использования в качестве лекарственного средства, в частности для использования в качестве лекарственного средства для лечения описанных выше нарушений.
Специалисты в области лечения таких заболеваний могли определить эффективное терапевтическое суточное количество из результатов испытаний, представленных здесь далее. Эффективное терапевтическое суточное количество должно быть от около 0,001 мг/кг до около 10 мг/кг массы тела, более предпочтительно от около 0,005 мг/кг до около 1 мг/кг массы тела.
Для облегчения введения соединения согласно изобретению можно получить в виде различных фармацевтических форм в зависимости от пути введения. Для приготовления фармацевтических композиций данного изобретения терапевтически эффективное количество конкретного соединения, необязательно в форме аддитивной соли, в качестве активного ингредиента тщательно смешивают с фармацевтически приемлемым носителем, который может принимать разнообразные формы в зависимости от формы препарата, необходимого для введения. Эти фармацевтические композиции желательны в унифицированной лекарственной форме, подходящей, предпочтительно, для введения перорально, ректально, чрескожно или парентеральной инъекцией. Например, при получении композиции в пероральной лекарственной форме можно использовать любую обычную фармацевтическую среду, такую, как, например, вода, гликоли, масла, спирты и тому подобные в случае пероральных жидких препаратов, таких, как суспензии, сиропы, эликсиры и растворы; или твердые носители, такие как крахмалы, сахара, каолин, смазочные вещества, связующие, дезинтегрирующие средства и тому подобные в случае порошков, пилюль, капсул и таблеток. Вследствие легкости их введения таблетки и капсулы представляют наиболее выгодную пероральную унифицированную лекарственную форму, очевидно, что в этом случае используют твердые фармацевтические носители. Для парентеральных композиций носитель будет обычно содержать стерильную воду, по меньшей мере большей частью, хотя могут быть включены другие ингредиенты, например, улучшающие растворимость. Можно, например, приготовить инъецируемые растворы, в которых носитель содержит солевой раствор, раствор глюкозы или смесь солевого раствора и раствора глюкозы. Инъецируемые растворы, содержащие соединения формулы (I), можно приготовить в масле для пролонгированного действия. Подходящими маслами для этой цели являются, например, арахисовое масло, кунжутное масло, хлопковое масло, кукурузное масло, соевое масло, синтетические эфиры глицерина и жирных кислот с длинной цепью и смеси этих и других масел. Можно также приготовить инъецируемые суспензии, в этом случае можно использовать подходящие жидкие носители, суспендирующие агенты и тому подобные. В композициях, подходящих для чрескожного введения, носитель необязательно содержит повышающее проникновение внутрь средство и/или подходящее увлажняющее средство, необязательно комбинированное с подходящими добавками любой природы в небольшой пропорции, эти добавки не должны оказывать никакого вредного действия на кожу. Эти добавки могут облегчить введение в кожу и/или могут быть полезными для приготовления необходимых композиций. Эти композиции можно вводить разными путями, например, в виде чрескожных пластырей, в виде наносимого пятна или в виде мази. Кислотно- или основно-аддитивные соли соединений формулы (I) благодаря их повышенной водорастворимости относительно соответствующей формы основания или кислоты, явно более подходящие при получении водных композиций.
Чтобы повысить растворимость и/или стабильность соединений формулы (I) в фармацевтических композициях, может быть выгодным использование α-, β-, γ-циклодекстринов или их производных, в частности гидроксиалкилзамещенных циклодекстринов, например, 2-гидроксипропил- β -циклодекстрина. Сорастворители, например, спирты также могут улучшить растворимость и/или стабильность соединений формулы (I) в фармацевтических композициях.
В особенности выгодно готовить вышеупомянутые фармацевтические композиции в унифицированной лекарственной форме для облегчения введения и однородности дозы. Термин унифицированная лекарственная форма, используемый здесь в описании и формуле изобретения, относится к физически дискретным единицам, подходящим в качестве унифицированных доз, причем каждая единица содержит заданное количество активного ингредиента, рассчитанное для достижения желаемого терапевтического действия, вместе с требуемым фармацевтическим носителем. Примерами таких унифицированных лекарственных форм являются таблетки (включая таблетки с бороздкой или покрытием), капсулы, пилюли, пакетики с порошком, облатки, инъецируемые растворы или суспензии, наполненные чайные ложки, наполненные столовые ложки и тому подобное, и разделенные многократные дозы их.
Следующие примеры предназначены для иллюстрации, а не ограничения объема данного изобретения.
Экспериментальная часть
А. Получение промежуточных соединений
Приведенное ниже сокращение "EtOAc" (ЭА) означает этилацетат, "DMF" (ДМФ) означает диметилформамид и "RT" (КТ) означает комнатную температуру.
Пример 1
а) Смесь 1-(2-пропенил)пиперазина (6,6 г) и этил-2-пропеноата (11,3 мл) в этаноле (100 мл) перемешивают и кипятят с обратным холодильником в течение 1 часа 30 минут. Растворитель выпаривают, получая 9,6 г (80%) этил-4-(2-пропенил)- 1-пиперазинпропаноата (промежуточное соединение 1).
b) Смесь промежуточного соединения 1 (7,5 г) в растворе соляной кислоты (35%) (20 мл), уксусной кислоты (20 мл) и воды (10 мл) перемешивают и кипятят с обратным холодильником в течение 4 часов. Смесь охлаждают на ледяной бане и добавляют NaOH (50%) до pH смеси около 6, и растворитель выпаривают. Остаток обрабатывают ЭА, осадок отделяют фильтрованием и фильтрат выпаривают. Масляный остаток растворяют в толуоле и растворитель выпаривают. Остаток очищают хроматографией в короткой колонке с силикагелем (элюент: CH2Cl2/(CH3OH/NH3), 8/2). Чистые фракции собирают и выпаривают, получая 5,3 г (81%) 4-(2-пропенил)-1- пиперазинпропановой кислоты (промежуточное соединение 2).
Пример 2
Смесь 2-гидроксибензальдегида (16,7 г) и Al2O3/KF (65,5 г) в ДМФ нагревают до 120oC в атмосфере N2 и добавляют 4-бром-1-фтор-2-нитробензол (30 г) в ДМФ- Смесь перемешивают при 120oC в течение 3 часов. Осадок отделяют фильтрованием и фильтрат выпаривают. Остаток очищают хроматографией на колонке с силикагелем (элюент 1: гексан/CH2Cl2/АцОЭт, 8/1/1; элюент 2: CH2Cl2/2-пропанон, 9/1) и чистые фракции собирают, получая 26 г (59%) 2-(4-бром-2-нитрофенокси)бензальдегида (промежуточное соединение 3). Аналогично получают 5-хлор-(2-нитрофенокси)бензальдегид (промежуточное соединение 4).
Пример 3
a) 1,4-Дихлор-2-нитробензол (31,6 г) добавляют к смеси 2,2'-дитиодибензальдегида (41 г) и карбоната калия (41,3 г) в метаноле (820 г) и реакционную смесь перемешивают и кипятят с обратным холодильником в течение 2 часов. Добавляют еще 1,4-дихлор-2-нитробензол (31,6 г) и реакционную смесь перемешивают и кипятят с обратным холодильником в течение 2 часов. Добавляют воду и смесь экстрагируют CH2Cl2. Отделенный органический слой выпаривают и остаток очищают хроматографией на колонке с силикагелем (элюент: гексан/ЭтОАс, 97,5/2,5). Чистые фракции собирают и выпаривают растворитель, получая 37 г (84%) 2-[(4- хлор-2-нитрофенил)тио]бензальдегида (промежуточное соединение 5). Аналогично получают 2- [[2-нитро-4-(трифторметил)фенил] тио] бензальдегид (промежуточное соединение 6).
b) Смесь пероксимонофосфата калия (35,6 г) в воде (120 мл) добавляют по каплям в смесь промежуточного соединения 5 (8,5 г) в метаноле (120 мл), охлажденную на ледяной бане, и смесь перемешивают при КТ в течение 7 часов. Растворитель выпаривают, добавляют воду и осадок отделяют фильтрованием. Остаток очищают флэш-хроматографией на силикагеле (элюент: CH2Cl2/CH3OH, 98/2). Чистые фракции собирают и выпаривают, получая 4.8 г (51%) 2-[(4-хлор-2- нитрофенил)сульфинил]бензальдегида (промежуточное соединение 7).
Пример 4
a) LiAlH4 (1 М) в тетрагидрофуране (100 мл) добавляют по каплям в смесь 3-хлордибенз[b, f] оксазепин-11(11OH)-она (12,3 г) (получен, как описано в Indian J. Chem. , 1974, 12(3), 227-35) в 1,4-диоксане (400 мл) в атмосфере азота. Смесь перемешивают и кипятят с обратным холодильником в течение 1 часа 30 минут, охлаждают и по каплям добавляют воду. Смесь подкисляют и экстрагируют ЭА. Органический слой сушат над Na2SO4, фильтруют и выпаривают. Остаток очищают хроматографией на колонке с силикагелем (элюент: CH2Cl2). Чистые фракции собирают и выпаривают, получая 9,74 г (84%) 3-хлор-10,11-дигидродибенз[b,f] [1,4]оксазепина (промежуточное соединение 8).
b) 3-Фенил-2-(фенилсульфонил)оксазиридин (36,4 г) добавляют в смесь промежуточного соединения 8 (15,4 г) в трихлорметане (700 мл) и смесь перемешивают при КТ в течение 1 часа. Растворитель выпаривают и остаток очищают хроматографией на колонке с силикагелем (элюент: CH2Cl2). Чистые фракции собирают и выпаривают, получая 8,6 г (34%) 10-оксид 3-хлордибенз[b,f] [1,4] оксазепина (промежуточное соединение 9).
Пример 5
Смесь промежуточного соединения 3 (10 г) и цинка (10,3 г) в 1,4-диоксане (200 мл) и воде (15 мл) перемешивают при КТ. По каплям при температуре ниже 25oC добавляют хлорид аммония (4,3 г) в воде (17 мл) и смесь перемешивают при КТ в течение 1 часа. Осадок отделяют фильтрованием и фильтрат выпаривают. Остаток обрабатывают водой и экстрагируют CH2Cl2/CH3OH, 9/1. Органический слой сушат, фильтруют и выпаривают. Остаток очищают хроматографией на колонке на силикагеле (элюент 1: CH2Cl2/гексан/ЭтОАц, 5/4/1; элюент 2: CH2Cl2/2-пропанон, 9/1). Чистые фракции собирают и выпаривают, получая 2,2 г (24%) 10-оксида 8-бромдибенз[b,f][1,4]оксазепина (промежуточное соединение 10).
Аналогично получают:
В. Получение соединений формулы (I)
Пример 6
Смесь промежуточного соединения 15 (2,6 г) и N,N-диметил-2-пропен-1-амина (2,9 мл) в толуоле (40 мл) перемешивают при 80oC в течение 2 часов. Растворитель выпаривают и остаток очищают колоночной хроматографией на силикагеле (элюент: гексан/CH2Cl2/CH3OH, 3,5/6/0,5). Чистые фракции собирают и выпаривают. Остаток превращают в соль щавелевой кислоты (1:1) в C2H5OH при КТ, получая 1 г (63%) этандиоата (±)-3,3а-дигидро-N,N-диметил-2Н-дибенз[b,f] изоксазоло [2,3-d] -[1,4] оксазепин-2-метанамина (1: 1), т. пл. 179,6oC (соединение 1).
Пример 7
По такой же методике, как в примере 6, но с использованием тетрагидрофурана в качестве растворителя, получают также этандиоат (±)-цис-11-хлор-3,3а-дигидро-N, N-диметил-2Н-дибенз [b, f] изоксазоло [2,3-d]-[1,4]оксазепин-2-метанамина (1:1), т. пл. 154,4oC (соединение 2).
Пример 8
Смесь (±)-цис-1-[(11-хлор-3,3а-дигидро-2Н-дибенз [b, f] изоксазоло [2,3-d] -[1,4] оксазепин-2-ил)метил] -4-(трифторацетил) пиперазина (7,1 г), полученного по способу примера 7, и карбоната калия (4,2 г) в метаноле (300 мл) и воде (43 мл) перемешивают при комнатной температуре в течение 2 часов. Растворитель выпаривают. Остаток обрабатывают водой, экстрагируют CH2Cl2 и отделенный органический слой выпаривают. Остаток (5,1 г) очищают флэш-хроматографией на силикагеле (элюент: CH2Cl2/CH3OH, 9/1, 8/2 до 7/3) и чистые фракции собирают и выпаривают. Остаток (4,2 г) превращают в соль щавелевой кислоты (2: 3) в C2H5OH при комнатной температуре, получая 3,9 г (47%) этандиоата (±)-цис-11-хлор-3,3а-дигидро-2- (1-пиперазинилметил)-2Н-дибенз[b, f]изоксазоло[2,3-d]-[1,4] оксазепина (2:3), т.пл. > 250,0oC (соединение 3).
Пример 9
Этандиоат (±)-метил-цис-2-[(диметиламино)метил] -3,3а-дигидро-2Н-дибенз[b, f] изоксазоло[2,3-d] [1,4]оксазепин-11- карбоксилата (1:1) (1,53 г), полученный по способу примера 7, в этаноле (60 мл) добавляют по каплям в смесь гидрооксида натрия (0,3 г) в воде (7,5 мл) и смесь перемешивают и кипятят с обратным холодильником в течение 2 часов. Растворитель выпаривают в вакууме и остаток подкисляют НС1 (4 Н) до pH 3,6. Остаток отделяют фильтрованием, сушат над P2O5 и очищают хроматографией на короткой колонке с силикагелем (элюент: CH2Cl2/(CH3OH/NH3), 7/3). Чистые фракции собирают и выпаривают и остаток (1 г) обрабатывают CH2Cl2/C2H5OH/H2O, 25 мл/5 мл/5 мл. Осадок отделяют фильтрованием и сушат, получая 0,5 г (38%) полугидрата (±)-цис-2-[(диметиламино)метил]-3,3а-дигидро-2Н-дибенз[b,f]изоксазоло[2,3-d] -[1,4] оксазепин-11-карбоновой кислоты; т. пл. 229,8oC (соединение 4).
Пример 10
Смесь (±)-цис-2-[[3,3а-дигидро-11-(трифторметил)-2Н-дибенз[b, f]изоксазоло[2,3-d] -[1,4] оксазепин-2-ил]метил]-1H-изоиндол-1,3(2Н)-диона (2,53 г), полученного по способу примера 7, и гидразингидрата (0,28 мл) в этаноле (30 мл) перемешивают при 80oC в течение 5 часов. Остаток отделяют фильтрованием и фильтрат выпаривают. Масляный остаток (3,3 г) очищают флэш-хроматографией на силикагеле (элюент: CH2Cl2/CH3OH, 9,5/0,5). Чистые фракции собирают и выпаривают и масляный остаток (0,7 г) превращают в соль щавелевой кислоты (1: 1) в C2H5OH при КТ, получая 0,8 г (35%) этандиоата (±)-цис-3,3а-дигидро-11-(трифторметил)-2H-дибенз[b, f] изоксазоло[2,3-d]-[1,4]оксазепин-2-метанамина (1:1); т.пл. 250oC (соединение 5).
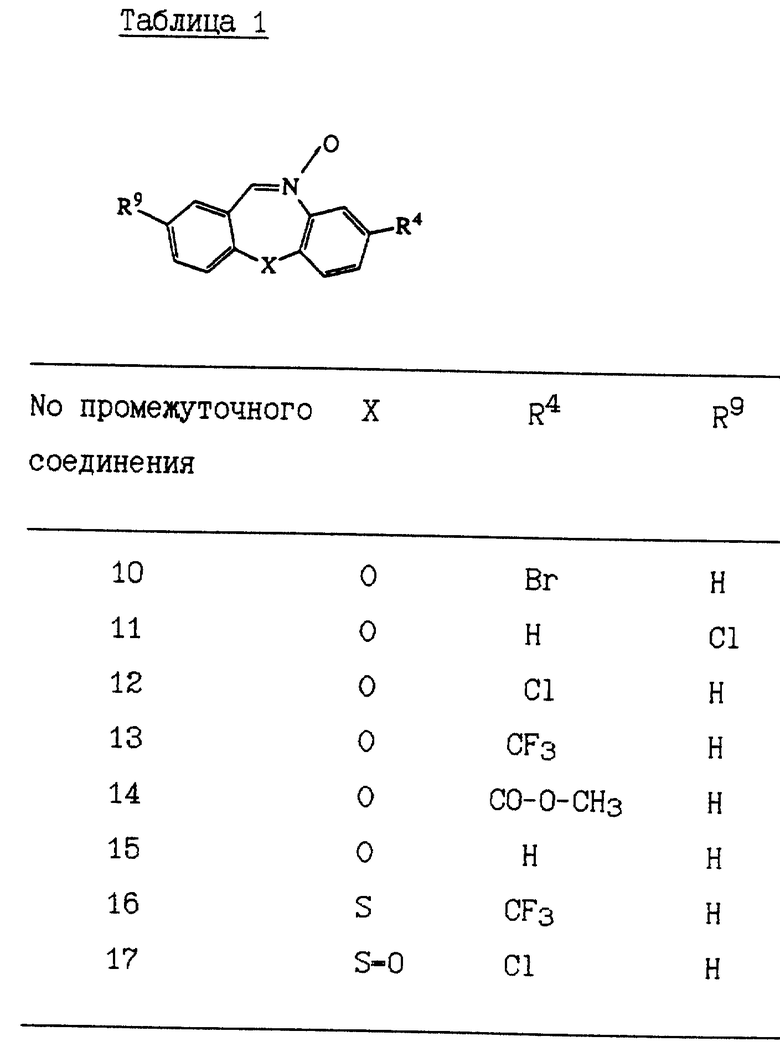
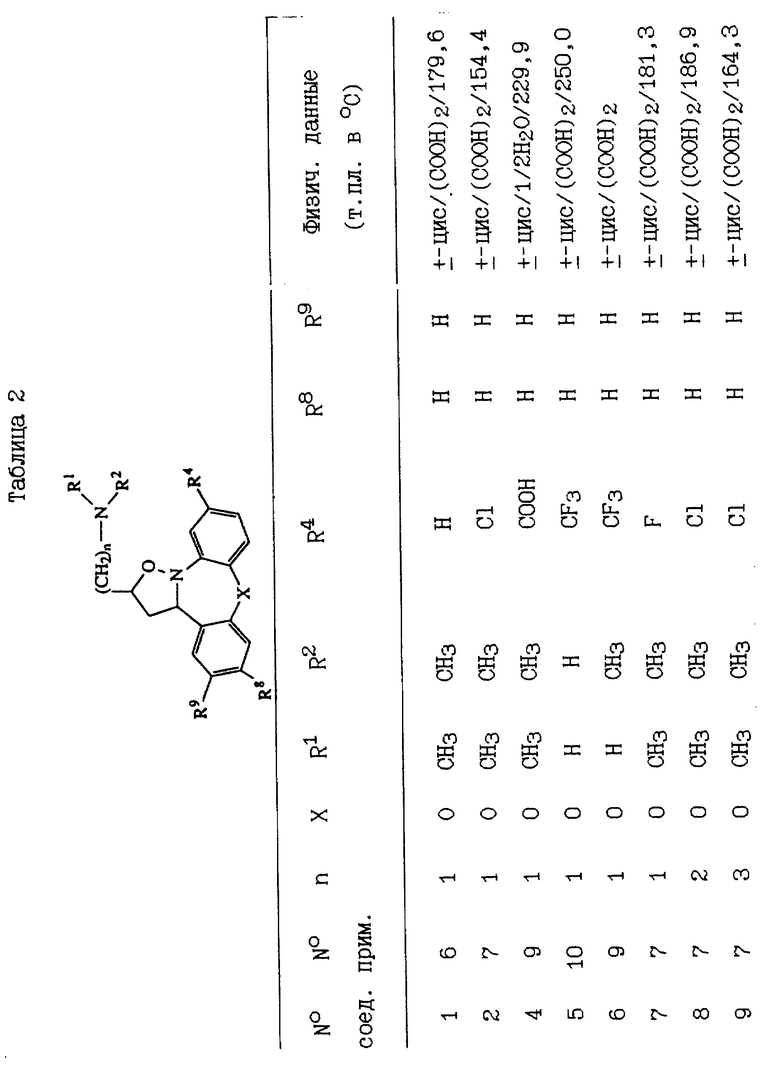
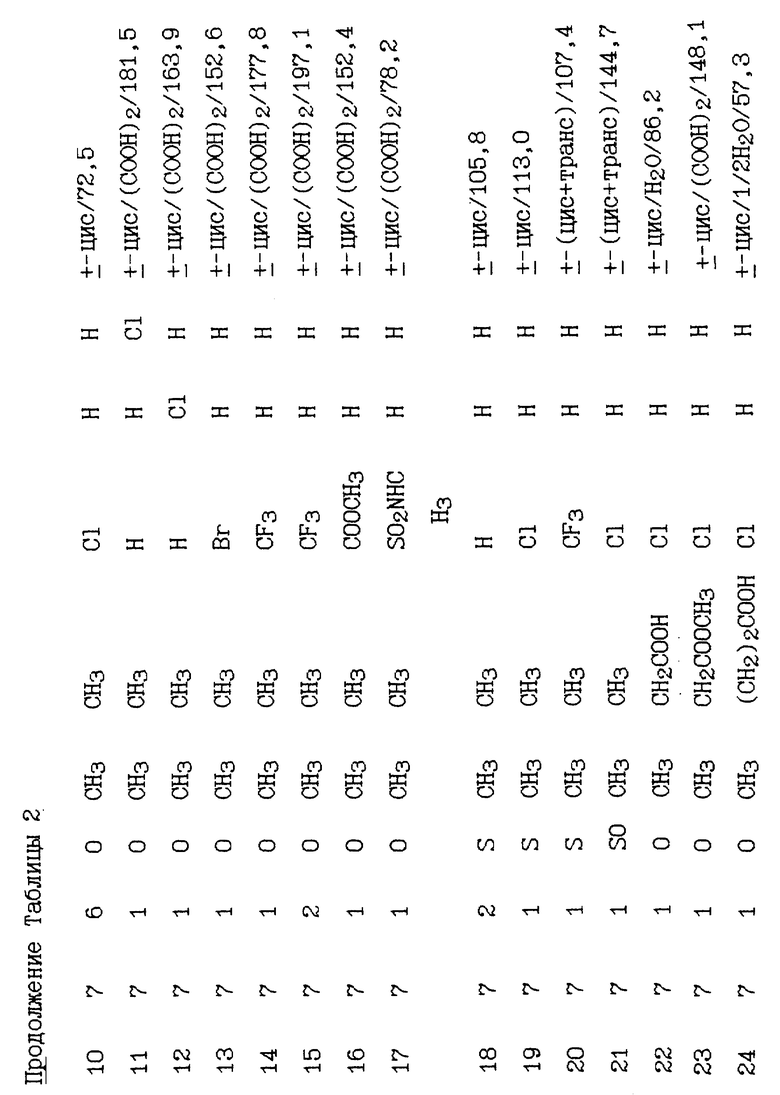
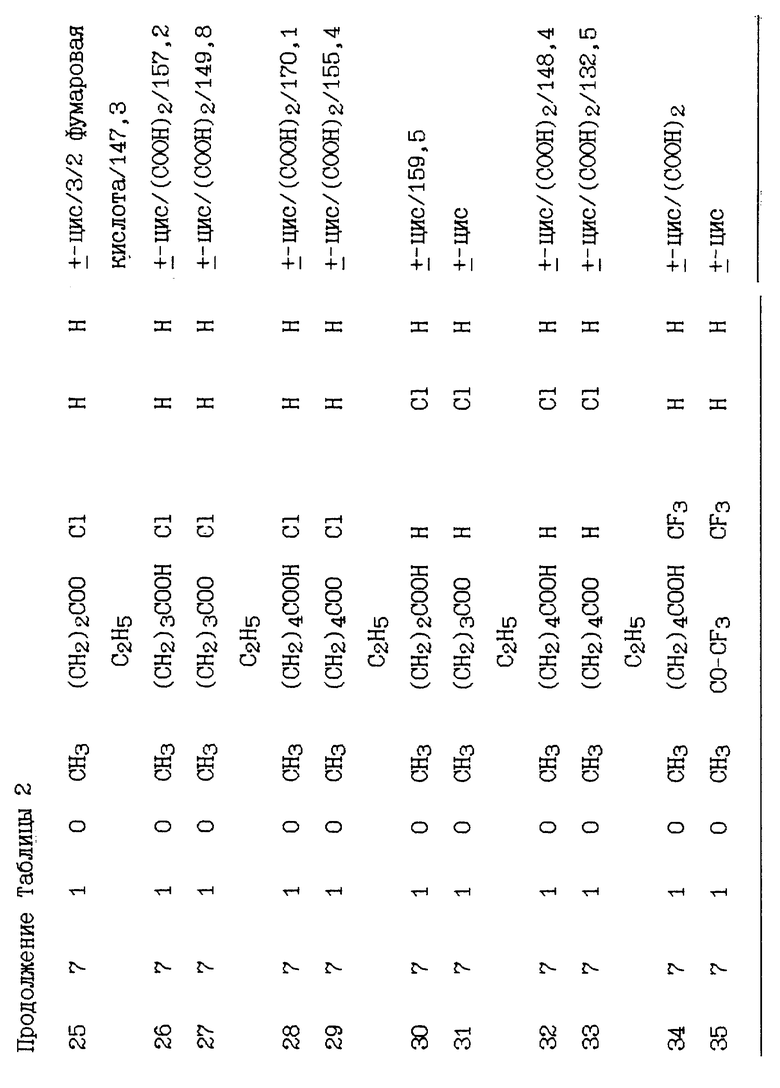
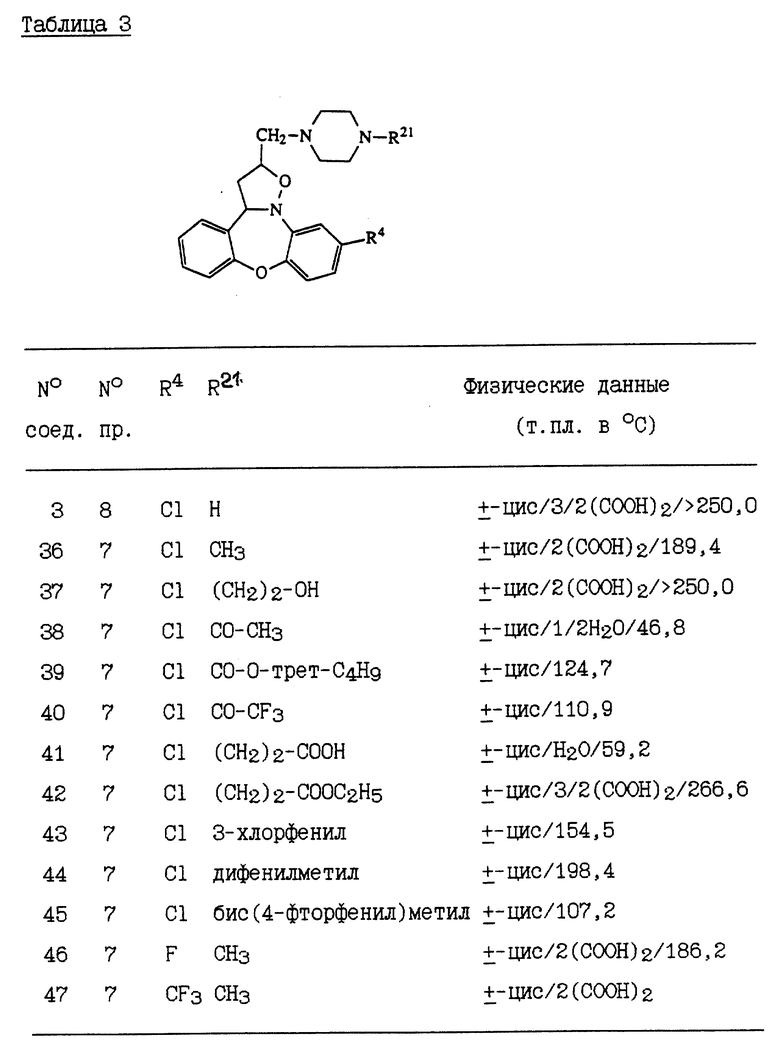
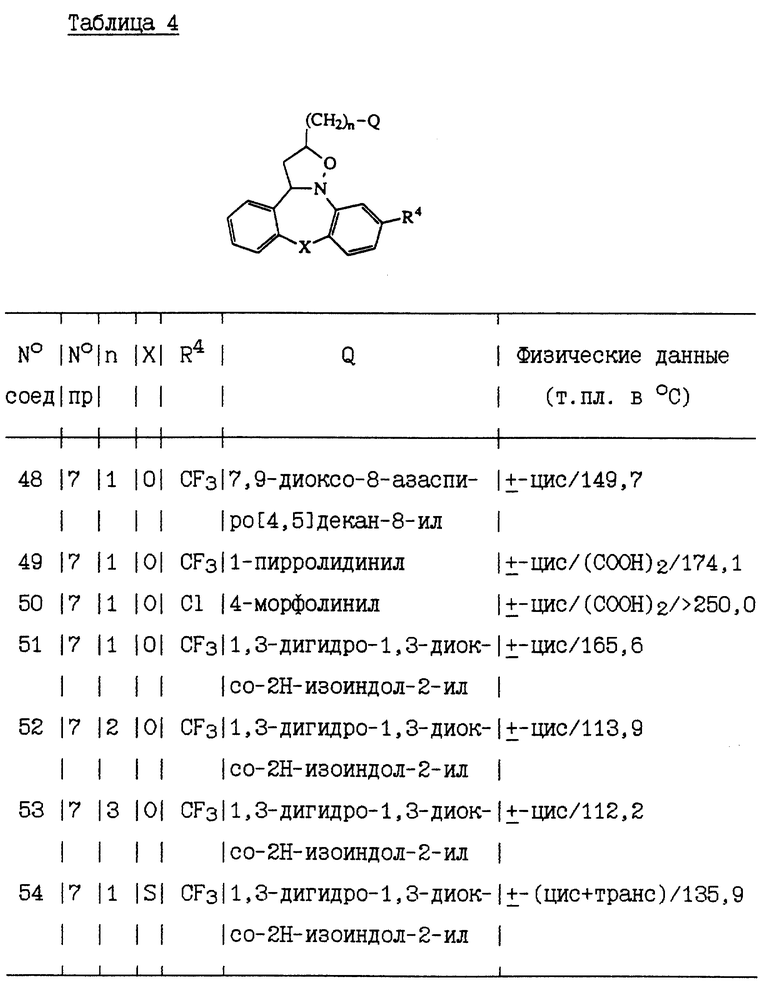
В таблицах 2-5 перечисляются соединения, которые получают способом, аналогичным способу одного из вышеупомянутых здесь примеров.
С. Фармакологический пример
Пример 11: "Испытание с мХФП на крысах"
Крыс обрабатывали испытуемым соединением в дозе, изменяющейся между 0,0025 мг/кг и 40 мг/кг массы тела, при предварительном времени испытания Т, изменяющемся между 5 и 480 минутами, и 1 мг/кг мХФП (метахлорфенилпиперазина), введенном внутривенно за 15 минут до испытания. По истечении предварительного времени испытания Т обработанных крыс подвергали "Тесту открытого поля на крысах", описываемому в Drug Dev. Res. 18, 119 - 144 (1989), но используя источник инфракрасного излучения вместо источника излучения Kleverlux ® (12 В/20 Вт). Дозу, при которой 40% испытуемых крыс показали подавление мХФП-индуцированных эффектов, то есть мХФП-антагонизм, определяли как активную дозу. Диапазон активности испытуемого соединения измеряли отношением НБАД (наиболее активная доза) к НМАД (наименее активная доза). Соединения с номерами 9 и 11 имели отношение (НБАД к НМАД) 4 или выше. Соединения с номером 2, 3, 5 - 7, 10, 13, 14, 16, 18 - 21, 26, 28, 33, 38, 44, 48, 50 и 52 показывали мХФП-антагонизм, по меньшей мере при одной испытуемой дозе.
Пример 12: "Тест с приподнятым и освещенным плюс-лабиринтом на крысах"
"Тест с приподнятым и освещенным плюс-лабиринтом на крысах" описывается в Drug Dev. Res. 18, 119 - 144 (1989). Активную дозу испытуемого соединения в этом испытании определяли как дозу, при которой 40% испытуемых крыс обследовали освещенные проходы лабиринта. Диапазон активности измеряли аналогично диапазону примера 11. Соединения с номером 3, 8, 17, 19, 21, 40, 51, 53 и 54 имели отношение (НБАД к НМАД) 4 или выше. Соединения с номером 1, 2, 4 - 6, 9 - 13, 16, 18, 22, 26 - 30, 32, 33, 36, 39, 41, 43, 44, 46, 47, 49, 50 и 52 показывали активность, по меньшей мере, при одной испытуемой дозе у одной или нескольких испытуемых крыс.
D. Примеры композиций
Термин "активный ингредиент" (А.И.), используемый во всех этих примерах, относится к соединению формулы (I), его фармацевтически приемлемой кислотно-аддитивной соли, его стереохимически изомерной форме или его N-оксидной форме.
Пример 13: Пероральные капли
500 г А.И. растворяли в 0,5 л 2-гидроксипропановой кислоты и 1,5 л полиэтиленгликоля при 60 - 80oC. После охлаждения до 30 - 40oC добавляли 35 л полиэтиленгликоля и смесь хорошо перемешивали. Затем добавляли раствор 1750 г натриевой соли сахарина в 2,5 л очищенной воды и при перемешивании добавляли 2,5 л в качестве вкусовой добавки какао и, сколько нужно до общего объема 50 л, полиэтиленгликоля, получая пероральные капли (раствор), содержащие 10 мг/мл А.И. Подходящие контейнеры заполняли получаемым раствором.
Пример 14: Пероральный раствор
Метил-4-гидроксибензоата (9 г) и 1 г пропил-4-гидроксибензоата растворяли в 4 л кипящей очищенной воды. В 3 л этого раствора растворяли сначала 10 г 2,3-дигидроксибутандиовой кислоты и затем 20 г А.И. Последний раствор смешивали с оставшейся частью первого раствора и добавляли в смесь 12 л 1,2,3-пропантриола и 3 л 70% раствора сорбита. 40 г натриевой соли сахарина растворяли в 0,5 л воды и добавляли 2 мл эссенции малины и 2 мл эссенции крыжовника. Последний раствор смешивали с первым, добавляли, сколько нужно до общего объема 20 л, воду, получая пероральный раствор, содержащий 5 мг активного ингредиента на полную чайную ложку (5 мл). Подходящие контейнеры заполняли получаемым раствором.
Пример 15: Таблетки, покрытые пленкой
Получение сердцевины таблетки
Смесь 100 г А. И. , 570 г лактозы и 200 г крахмала хорошо смешивали и затем увлажняли раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона приблизительно в 200 мл воды. Смесь в виде влажного порошка просеивали, сушили и просеивали снова. Затем добавляли 100 г микрокристаллической целлюлозы и 15 г гидрогенизированного растительного масла. Все хорошо перемешивали и прессовали в таблетки, получая 10000 таблеток, содержащих каждая 10 мг активного ингредиента.
Покрытие
В раствор 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляли раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляли 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. 10 г полиэтиленгликоля расплавляли и растворяли в 75 мл дихлорметана. Последний раствор добавляли в первый и затем добавляли 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной суспензии красителя и все гомогенизировали. Сердцевины таблеток покрывали полученной таким образом смесью в устройстве нанесения покрытия.
Пример 16: Инъецируемый раствор
1,8 г Метил-4-гидроксибензоата и 0,2 г пропил-4-гидроксибензоата растворяли приблизительно в 0,5 л кипящей воды для инъекций. После охлаждения до около 50oС добавляли при перемешивании 4 г молочной кислоты, 0,05 г пропиленгликоля и 4 г А.И. Раствор охлаждали до комнатной температуры и дополняли водой для инъекции, сколько необходимо, до объема 1 л, получая раствор, содержащий 4 мг/мл А.И. Раствор стерилизовали фильтрованием и стерильные контейнеры заполняли этим раствором.
Изобретение относится к соединениям формулы I, их фармацевтически приемлемым солям и стереоизомерным формам, где R - водород или С1-6-алкил; R2 - водород; С1-6-алкил; тригалогенметилкарбонил; С1-6-алкил, замещенный карбоксилом, С1-6-алкилкарбонилокси, С1-6-алкилоксикарбонилом, или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, могут образовывать кольцо морфолинила или необязательно замещенный гетероциклический радикал; R3 - R10 каждый независимо представляет водород; R8, R9 независимо представляют собой водород или галоген; R11 и R12 - водород; n = 1, 2, 3, 4, 5 или 6; Х - О, S, S(=O). Соединения формулы I можно использовать в качестве терапевтических средств при лечении или предупреждении нарушений ЦНС, сердечно-сосудистых нарушений и желудочно-кишечных нарушений. Описывается также способ их получения, композиция, обладающая антипсихотической активностью. 4 с. и 3 з.п. ф-лы, 4 табл.
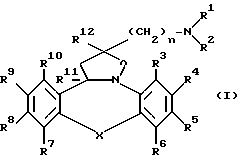
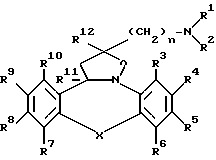
его фармацевтически приемлемые кислотно- или основно-аддитивные соли и стереохимически изомерные формы,
где R1 представляет собой водород или С1-6алкил;
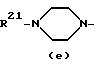
R2 представляет водород; С1-6алкил; тригалогенметилкарбонил; С1-6алкил, замещенный карбоксилом, С1-6алкилоксикарбонилом, или R1 и R2, взятые вместе с атомом азота, к которому они присоединены, могут образовать кольцо морфолинила или радикал формулы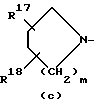
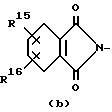
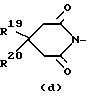
где R15 и R16 представляют водород;
m = 1;
R17, R18 представляет водород или R19 и R20, взятые вместе, могут образовать двухвалентный радикал С4-5алкандиил;
R21 представляет водород, С1-6алкил, С1-6алкилкарбонил, тригалоидметилкарбонил, С1-6алкил-оксикарбонил, фенил, замещенный одним галогеном, дифенилметил, С1-6алкил, замещенный гидроксилом, карбоксилом, С1-6алкилоксикарбонилом, бисфенилом, в котором каждая фенильная группа замещена одним заместителем-галогеном;
R4 представляет собой водород, галоген, трифторметил, карбоксил, моно (С1-6алкил)аминосульфонил, С1-6алкилоксикарбонил;
R3, R5, R6, R7 и R10 все представляют водород;
R8, R9 независимо представляют собой водород или галоген;
R11 представляет водород;
R12 представляет водород;
n = 1,2,3,4,5 или 6;
Х представляет О, S, S(=O).
цис-2-[(диметиламино)метил] -3, 3а-дигидро-N-метил-2Н-дибенз [b,f]изоксазоло[2,3-d][1,4]оксазепин-11-сульфамид;
цис-11-хлор-3, 3а-дигидро-2-(1-пиперазинилметил)-2Н-дибенз [b,f]-изоксазоло[2,3-d][1,4]оксазепин;
цис-2[(3,3a-дигидро-11-(трифторметил)-2Н-биденз[b,f], изоксазоло [2,3-d] [1,4]оксазепин-2ил]метил]-1Н-изоиндол-1,3-(2Н)-дион и
цис-11-хлор-3, 3а-дигидро-N, N-диметил-2Н-дибенз [b,f]изоксазоло [2,3-d] [1,4]оксазепин-2-пропанамин,
их стереохимически изомерные формы и фармацевтически приемлемые кислотно-аддитивные соли.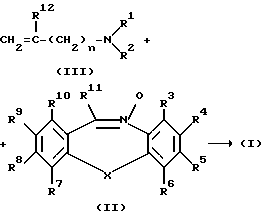
где в промежуточных продуктах II и III R1 -R12, Х и n определяются как в п.1,
с последующим, если необходимо, превращением соединения формулы I в терапевтически активную нетоксичную кислотно-аддитивную соль обработкой кислотой или в терапевтически активную нетоксичную основно-аддитивную соль обработкой основанием или, наоборот, превращением кислотно-аддитивной соли в свободное основание обработкой щелочью или превращением основно-аддитивной соли в свободную кислоту обработкой кислотой и, если необходимо, получают их стереохимически изомерные формы.
| Способ получения производных бензодиазепина | 1969 |
|
SU496733A3 |
| DE 2947773 A1, 04.06.1980 | |||
| ПЛТЕЯТНО-ШННЧЕСНД1 БИ5ЛИОТЕКА | 0 |
|
SU321812A1 |
| Способ приготовления сернистого красителя защитного цвета | 1921 |
|
SU84A1 |
| US 4039558, 02.08.1977 | |||
| US 4723007, 02.02.1988. | |||
Авторы
Даты
2000-12-27—Публикация
1995-10-25—Подача