Изобретение относится к медицине, а именно к кардиологии, в частности к способам прогнозирования развития наджелудочковых нарушений сердечного ритма (НСР), в частности пароксизмов мерцания и трепетания предсердий (МП и ТП) у больных с наджелудочковой экстрасистолией (НЖЭ).
Аналогом предлагаемого решения является способ прогнозирования развития пароксизмов МП и ТП у больных с НЖЭ, заключающийся в определении ширины и амплитуды зубца Р электрокардиограммы (ЭКГ), причем при выявлении зубца Р шириной более 0,12 с и (или) амплитудой более 2,5 мм прогнозируется развитие пароксизмов этих аритмий в течение нескольких лет после первого обследования (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993).
По наиболее близкой технической сущности в качестве прототипа нами выбран способ прогнозирования развития пароксизмов МП и ТП у больных с НЖЭ, заключающийся в определении размера или объема правого и (или) левого предсердий, причем при дилатации предсердий более 4,0 см прогнозируется развитие (в течение 1-3 лет) пароксизмов МП и ТП (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993).
Недостатком аналога и прототипа является недостаточная точность прогнозирования развития пароксизмов МП и ТП.
Задачей изобретения является повышение точности прогнозирования развития пароксизмов МП и ТП у больных с НЖЭ.
Техническое решение поставленной задачи заключается в том, что больному с НЖЭ проводят ЭКГ-исследование, затем определяют начало турбулентности ритма сердца (ТРС), наклон ТРС и при выявлении начала ТРС<0% и наклона ТРС>2,5 мс/R-Rcp. после усреднения этих показателей как минимум в 10 экстрасистолических комплексах проводят с помощью чреспищеводной электрокардиостимуляции (ЧПЭКС) индуцирование как минимум 10 наджелудочковых экстрасистол с одинаковым предэктопическим интервалом, составляющим на 10% больше, чем эффективный рефракторный период атриовентрикулярного соединения так, чтобы до и после индуцированной экстрасистолы было не менее 20 синусовых комплексов, и при выявлении начала ТРС>0% и наклона ТРС<2,5 мс/R-Rcp. до или после стимуляции как минимум в 10 экстрасистолических комплексах прогнозируют развитие пароксизмов МП и ТП в течение месяца после обследования.
Существенными отличительными признаками заявляемого способа являются следующие - при выявлении начала ТРС<0% и наклона ТРС>2,5 мс/R-Rcp. после усреднения этих показателей как минимум в 10 экстрасистолических комплексах проводят с помощью ЧПЭКС индуцирование как минимум 10 наджелудочковых экстрасистол с одинаковым предэктопическим интервалом, составляющим на 10% больше, чем эффективный рефракторный период атриовентрикулярного соединения так, чтобы до и после индуцированной экстрасистолы было не менее 20 синусовых комплексов, и при выявлении начала ТРС>0% и наклона ТРС<2,5 мс/R-Rcp. до или после стимуляции как минимум в 10 экстрасистолических комплексах прогнозируют развитие пароксизмов МП и ТП в течение месяца после обследования.
Способ осуществляется следующим образом. Больному с НЖЭ проводят ЭКГ-исследование, затем определяют начало ТРС, наклон ТРС и при выявлении начала ТРС<0% и наклона ТРС>2,5 мс/R-Rcp. после усреднения этих показателей как минимум в 10 экстрасистолических комплексах проводят с помощью ЧПЭКС индуцирование как минимум 10 наджелудочковых экстрасистол с одинаковым предэктопическим интервалом, составляющим на 10% больше, чем эффективный рефракторный период атриовентрикулярного соединения так, чтобы до и после индуцированной экстрасистолы было не менее 20 синусовых комплексов, и при выявлении начала ТРС>0% и наклона ТРС<2,5 мс/R-Rcp. до или после стимуляции как минимум в 10 экстрасистолических комплексах прогнозируют развитие пароксизмов МП и ТП в течение месяца после обследования.
В настоящее время известно, что при регистрации возбуждения по миокарду предсердий или желудочков проведение возбуждения (ПВ) подчиняется закону "стока" от одного кардиомиоцита к другому (Физиология и патофизиология сердца. Т.1.: пер. с англ. - Под. ред. Н. Сперелаксиса. - М.: Медицина, 1990, Olshansky В., Okumura К., Hess P.G., Waldo A.L. Demonstration of the area of slow conduction in human atrial flutter. // J. Amer. Coll. Cardiol. - 1991. - Vol.16, N.6. - P.1639-1648, Shimisu A., Nosaki A., Rudy Y., Waldo A.L. Multiplexing studies of effects of rapid atrial pacing on the area of slow conduction during atrial flutter in canine pericarditis model. // Circulation. - 1991. - Vol.83, N.3. - P.983-994). Поэтому путем прямого наложения электродов на миокард регистрируют характер и направление ПВ по сердечной мышце. Кроме того, миокард предсердий является тканью с быстрым ответом, т.е. для мембранного потенциала сократительных волокон предсердий характерна быстрая деполяризация (Физиология и патофизиология сердца. Т.1.: пер. с англ. - Под. ред. Н. Сперелаксиса. - М.: Медицина, 1990). Начало деполяризации соответствует электрическому возбуждению миокарда и регистрируется на ЭКГ как начало зубца Р или комплекса QRS, а вход кальциевого тока через мембрану кардиомиоцитов - развитию механического сокращения миокарда (Физиология и патофизиология сердца. Т.1.: пер. с англ. - Под. ред. Н. Сперелаксиса. - М.: Медицина, 1990). Следует отметить, что интервал от начала электрического возбуждения миокарда до начала его механического сокращения как в клинических, так и в экспериментальных исследованиях обозначают как время асинхронного сокращения (Физиология и патофизиология сердца. Т.1.: пер. с англ. - Под. ред. Н. Сперелаксиса. - М.: Медицина, 1990).
Наличие наджелудочковых аритмий, в том числе НЖЭ, у больных ИБС обусловлено тем, что отмечается замедление и неравномерное ПВ в верхних и средних отделах предсердий, что отражает дисперсию возбудимости миокарда предсердий (Бокерия Л.А. Тахиаритмии: Диагностика и хирургическое лечение. - Л.: Медицина, 1989, Olshansky В., Okumura К., Hess P.G., Waldo A.L. Demonstration of the area of slow conduction in human atrial flutter. // J. Amer. Coll. Cardiol. - 1991. - Vol.16, N.6. - P.1639-1648, Shimisu A., Nosaki A., Rudy Y., Waldo A.L. Multiplexing studies of effects of rapid atrial pacing on the area of slow conduction during atrial flutter in canine pericarditis model. // Circulation. -1991. - Vol.83, N.3. - P.983-994, Zipes D.P. Genesis of cardiac arrhythmias: electrophysiological consideration // Heart Disease / Ed. E. Braunwald, 1984. - P.605-647), причем у этих больных нарушение предсердной проводимости отмечается задолго до увеличения предсердий и других предикторов развития МП и ТП (Шабров А.В., Олесин А.И., Голуб Я.В., Голуб В.И. Клиническая оценка использования неинвазивного метода определения внутри и межпредсердной проводимости у больных ишемической болезнью сердца. // Тер. архив. - 1999. - №1. - С.34-39). При сопоставлении локализации участков замедления распространения возбуждения и ретроградным ПВ по предсердиям с зонами гипокинезии была выявлена положительная корреляция между ними, составившая в среднем r=0,89 и r=91 соответственно (Шабров А.В., Олесин А.И., Голуб Я.В., Голуб В.И. Клиническая оценка использования неинвазивного метода определения внутри и межпредсердной проводимости у больных ишемической болезнью сердца. // Тер. архив. - 1999. - №1. - С.34-39).
Дисбаланс вегетативной нервной системы занимает одно из первых мест в ряде других предикторов неблагоприятного течения МП и ТП (Coumel P., Thomas О., Leenhardt A. Drug therapy for prevention of atrial fibrillation. // Amer. J. Cardiol. - 1996. - Vol.77, N.3. - P.3А-9A) в результате усугубления неравномерной рефрактерности миокарда предсердий и нарушения ПВ по миокарду. В результате повышенного вагусного тонуса эти аритмии могут возникать в ночное время или после приема пищи у людей без органической патологии сердца, которая расценивается многими авторами как "вагусная" форма МП и ТП, в то время как у части пациентов эта аритмия может развиваться на фоне физической нагрузки, эмоциональных реакций, инфузии изопротеренола и обозначается как "катехоламиновая" форма МП и ТП (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993).
Согласно современным представлениям ТРС - это физиологическая двухфазная реакция синусового узла на преждевременное сокращение. Механизм ТРС заключается в барорефлекторном ответе на преждевременное сокращение и кратковременным снижением артериального давления в экстрасистолическом комплексе и высокой амплитудой в последующем синусовом комплексе с соответствующими изменениями частоты сердечных сокращений, которые и определяются при анализе ТРС (Schmidt G., Malik М., Barthel P. et al. Heat-rate turbulence after ventricular premature beats as a predictor of mortality after acute myocardial infarction. // Lancet. - 1999. - Vol.353, N6. - P.1390-1396). Феномен начала ТРС связан с тем, что многочисленные ионные каналы кардиомиоцитов к моменту преждевременного эктопического сокращения еще полностью не восстановлены, что приводит к укорочению потенциала действия. При преждевременном эктопическом сокращении снижается ударный объем, что, в свою очередь, обуславливает уменьшение уровня артериального давления, приводя к активизации аортальных, каротидных барорецепторов и к увеличению через барорефлекторную дугу частоты сердечных сокращений. Феномен наклона ТРС объясняется тем, что с момента компенсаторной паузы ионные каналы кардиомиоцитов полностью восстанавливаются, это приводит к увеличению ударного объема, повышению артериального давления и через барорефлекс снижает частоту сердечных сокращений. Сходные результаты ТРС были получены при НЖЭ (Savelieva I., Wichterle D., Berkowitsch A. et al. Different effect atrial and ventricular premature on heart rate turbulence: relation to left ventricular function. // PACE. - 2002. - Vol.25, Part II. - P.608). Наличие патологических значений ТРС при преждевременном эктопическом сокращении отражает дисбаланс вегетативной нервной системы (Schmidt G., Malik М., Barthel P. et al. Heat-rate turbulence after ventricular premature beats as a predictor of mortality after acute myocardial infarction. // Lancet. - 1999. - Vol.353, N6. - P.1390-1396), что является независимым предиктором внезапной смерти у больных желудочковой экстрасистолией.
В предлагаемом нами способе предполагается, что при наличии НЖЭ, обусловленной неравномерным ПВ по миокарду предсердий (Шабров А.В., Олесин А.И., Голуб Я.В., Голуб В.И. Клиническая оценка использования неинвазивного метода определения внутри и межпредсердной проводимости у больных ишемической болезнью сердца. // Тер. архив. - 1999. - №1. - С.34-39), в сочетании с дисбалансом вегетативной нервной системы возможно прогнозировать развитие пароксизмов МП и ТП. Следует отметить, что выбор индуцирования НЖЭ с помощью ЧПЭКС с одинаковым предэктопическим интервалом, составляющим на 10% больше, чем эффективный рефракторный период атриовентрикулярного соединения с помощью ЧПЭКС, обусловлен тем, что при этих условиях максимальный индекс преждевременности индуцированной экстрасистолы составляет в среднем 20%, а постэкстрасистолическая пауза - на 20% и более длиннее нормального интервала R-R, что является одним из условий расчета ТРС (Schmidt G., Malik М., Barthel P. et al. Heat-rate turbulence after ventricular premature beats as a predictor of mortality after acute myocardial infarction. // Lancet. - 1999. - Vol.353, N6. - P.1390-1396, Savelieva I., Wichterle D., Berkowitsch A. et al. Different effect atrial and ventricular premature on heart rate turbulence: relation to left ventricular function. // PACE. - 2002. - Vol.25, Part II. - P.608).
Пример конкретного выполнения.
Пример 1.
ИБ №457. Больной А., 65 лет, поступил в дневной стационар 16.01.2004 г. по направлению участкового врача по поводу ИБС: стенокардии, периодических приступов сердцебиения. Из анамнеза известно, что больной страдает ИБС: стенокардией II функционального класса в течение последних 4-5 лет. Постоянно принимает нитронг, аспирин в дозе 300-400 мг в сутки, метопролол в дозе 25-50 мг в сутки. В последние 3-4 месяца стал отмечать появление перебоев в работе сердца. При суточном мониторировании ЭКГ, выполненном амбулаторно 10.12.2004 г., была выявлена одиночная и парная предсердная экстрасистолия (ПЭ) с частотой до 15-35 экстрасистол в час.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: стабильная стенокардия напряжения II функционального класса, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была продолжена терапия нитронгом в дозе 6,4 мг в сутки, аспирином в дозе 300 мг в сутки, эналаприлом (эднит) в дозе 5 мг в сутки.
На второй день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 30 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г. Иваново). На ЭКГ было выявлено 3-5 ПЭ в минуту. Затем было рассчитано начало ТРС ПЭ по формуле:
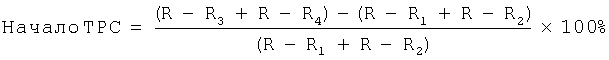 ,
,
где начало ТРС - начало турбулентности ритма сердца в %, (R-R3+R-R4) - два интервала R-R после ПЭ в мс, (R-R1+R-R2) - два интервала R-R перед ПЭ в мс.
Затем был рассчитан наклон ТРС как максимальное значение позитивного наклона линии линейной регрессии, рассчитанное между значениями интервала R-R (в мс) и последовательным номером интервала R-R в любых 5 циклах из 20 интервалов R-R, следующих за ПЭ (единица измерения наклона ТРС в мс/R-R). Результаты исследования нескольких экстрасистол больного усреднялись.
Для иллюстрации представляем расчет наклона ТРС у больного А., 65 лет. У него 2 интервала R-R после ПЭ составили 757 мс и 743 мс, а перед ПЭ - 728 мс и 727 мс. Затем был проведен расчет начала ТРС по вышеуказанной формуле:
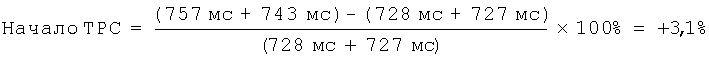
Таким образом, у данного больного начало ТРС для одной ПЭ составило +3,1%.
Начало и наклон ТРС были рассчитаны в 32 ПЭ. Результаты исследования у больного А., 65 лет, представлены в таблице 1.
У больного А., 65 лет, прогнозировалось развитие МП и ТП. Больному было индуцировано МП методом залповой сверхчастой стимуляции с помощью ЧПЭКС, причем порог индуцирования аритмии (ПИА) составил 350 имп./мин. Аритмия купировалась самостоятельно через 5 минут. Следует отметить, что при ЧПЭКС показатели, отражающие функцию синусового узла, такие как время восстановления функции синусового узла, корригированное время восстановления функции синусового узла, время синоатриального проведения, определенные по общепринятой методике (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993), не выходили за пределы колебаний нормальных величин. В последующем больному была проведена терапия нитратами, аспирином, ренитеком (эналаприлом) в дозах, указанных выше. Противоаритмические препараты не назначались. Спонтанные приступы МП и ТП длительностью от 3-6 секунд до 10-15 минут были выявлены при суточном мониторировании ЭКГ, проведенным на следующий день после вышеуказанного обследования.
Таблица 1. Результаты исследования начала и наклона ТРС у больного А., 65 лет.
Данный пример показал, что при регистрации ПЭ началом ТРС>0% и наклоном ТРС<2,5 мс/R-R можно прогнозировать пароксизмы МП и ТП в течение 1 суток после обследования.
Пример 2.
ИБ №21138. Больной С., 58 лет, поступил в стационар 19.06.2002 г. по направлению врача скорой помощи по поводу ИБС: прогрессирующей стенокардии. Из анамнеза известно, что больной страдает ИБС: стенокардией II функционального класса в течение последних 3 лет. Постоянно принимает нитросорбид, антиагреганты. За два дня до госпитализации у больного усилились ангинозные боли по частоте, длительности, интенсивности, а также изменился характер болевого синдрома. Госпитализация в стационар.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: прогрессирующая стенокардия, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была продолжена терапия нитросорбидом в дозе 30 мг в сутки, аспирином в дозе 300 мг в сутки, ренитеком в дозе 5 мг в сутки, поляризующей смесью с нитроглицерином.
На третий день пребывания больного в стационаре характер ангинозных болей стабилизировался.
На третий день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 40 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г. Иваново). На ЭКГ было выявлено 2-3 ПЭ в минуту. Затем были рассчитаны начало и наклон ТРС в 35 ПЭ.
Данные начала и наклона ТРС у больного С., 58 лет, представлены в таблице 2.
Результаты начала и наклона ТРС у больного С., 58 лет
Как видно из таблицы, начало ТРС составило -3,7% (норма <0%), наклон ТРС 22,5 мс/R-R (норма >2,5 мс/R-R) (см. таблицу 2, исходные данные). Средняя частота сердечного ритма составила 70 уд. в мин. Затем больному была проведена ЧПЭКС и индуцирована ПЭ с одинаковым предэктопическим интервалом, составившим 330 мс (что на 10% больше эффективного рефракторного периода атриовентрикулярного соединения, составившего 300 мс), так, чтобы до и после индуцированной ПЭ было 20 синусовых интервалов R-R. Данные начала и наклона ТРС у больного С., 58 лет, при индуцировании ПЭ с помощью ЧПЭКС представлены в таблице 2. Как видно из таблицы, начало ТРС составило 6,9% (норма <0%), наклон ТРС 1,1 мс/R-R (норма >2,5 мс/R-R) (см. таблицу 2, после ЧПЭКС).
У больного С., 58 лет, прогнозировалось развитие МП и ТП. Больному было индуцировано МП методом залповой сверхчастой стимуляции с помощью ЧПЭКС, причем ПИА составил 420 имп./мин. Аритмия купировалась самостоятельно через 5 минут. Следует отметить, что при ЧПЭКС показатели, отражающие функцию синусового узла, такие как время восстановления функции синусового узла, корригированное время восстановления функции синусового узла, время синоатриального проведения, определенные по общепринятой методике (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993), не выходили за пределы колебаний нормальных величин. В последующем больному была проведена терапия нитратами, аспирином в дозах, указанных выше. Противоаритмические препараты не назначались.
Спонтанные приступы МП и ТП длительностью от 15 секунд до 10-15 минут были выявлены при суточном мониторировании ЭКГ через 3 недели после вышеуказанного обследования, причем при проведении ЧПЭКС в этот же период (через 3 недели после первой стимуляции) ПИА составил 260 имп./мин.
Данный пример показал, что при регистрации ПЭ с началом ТРС<0% и наклоном ТРС>2,5 мс/R-R можно прогнозировать пароксизмы МП и ТП путем определения вышеуказанных показателей при индуцировании ПЭ (с одинаковым предэктопическим интервалом, составляющим на 10% больше эффективного рефракторного периода атриовентрикулярного соединения) с помощью ЧПЭКС, причем при значениях начала ТРС>0% и наклона ТРС<2,5 мс/R-R индуцированных НЖЭ прогнозируются пароксизмы МП и ТП в течение 3 недель после обследования.
Пример 3.
ИБ №2698. Больной О., 60 лет, поступил в стационар 21.04.2002 г. по направлению врача поликлиники по поводу ИБС: впервые возникшей стенокардии. Из анамнеза известно, что больной ранее считал себя практически здоровым.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: впервые возникшая стенокардия, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была начата терапия эринитом в 40 мг в сутки, аспирином в дозе 300 мг в сутки, зоокором 20 мг в сутки, поляризующей смесью с нитроглицерином.
На третий день пребывания больного в стационаре ангинозные боли купировались и в дальнейшем не рецидивировали.
На третий день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 35 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г. Иваново). На ЭКГ было выявлено 2 ПЭ в минуту. Затем были рассчитаны начало и наклон ТРС в 37 ПЭ.
Данные начала и наклона ТРС у больного О., 60 лет, представлены в таблице 3.
Результаты начала и наклона ТРС у больного О., 60 лет
Как видно из таблицы, начало ТРС составило -3,4% (норма <0%), наклон ТРС 26,7 мс/R-R (норма >2,5 мс/R-R) (см. таблицу 3, исходные данные). Средняя частота сердечного ритма составила 78 уд. в мин. Затем больному была проведена ЧПЭКС и индуцирована ПЭ с одинаковым предэктопическим интервалом, составившим 374 мс (что на 10% больше эффективного рефракторного периода атриовентрикулярного соединения, составившего 340 мс), так, чтобы до и после индуцированной ПЭ было 20 синусовых интервалов R-R. Данные начала и наклона ТРС у больного О., 60 лет, при индуцировании ПЭ с помощью ЧПЭКС представлены в таблице 3. Как видно из таблицы, начало ТРС составило -5,3% (норма <0%), наклон ТРС 24,1 мс/R-R (норма >2,5 мс/R-R) (см. таблицу 3, после ЧПЭКС).
У больного О., 68 лет, развитие МП и ТП не прогнозировалось. Больному была проведена попытка индуцирования МП методом залповой сверхчастой стимуляции с помощью ЧПЭКС, однако аритмия не была индуцировна. Следует отметить, что при ЧПЭКС показатели, отражающие функцию синусового узла, такие как время восстановления функции синусового узла, корригированное время восстановления функции синусового узла, время синоатриального проведения, определенные по общепринятой методике (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993), не выходили за пределы колебаний нормальных величин. В последующем больному была проведена терапия нитратами, аспирином, зоокором в дозах, указанных выше. Противоаритмические препараты не назначались.
При последующем наблюдении в течение года, включающем проведение суточного мониторирования ЭКГ и ЧПЭКС один раз в 3 месяца, пароксизмов МП и ТП не наблюдалось.
Данный пример показал, что при регистрации ПЭ с началом ТРС<0% и наклоном ТРС>2,5 мс/R-R пароксизмы МП и ТП не прогнозируются, а также при определении вышеуказанных показателей при индуцировании ПЭ (с одинаковым предэктопическим интервалом, составляющим на 10% больше эффективного рефракторного периода атриовентрикулярного соединения) с помощью ЧПЭКС, причем при значениях начала ТРС<0% и наклона ТРС>2,5 мс/R-R индуцированных НЖЭ пароксизмы МП и ТП не прогнозируются.
Пример 4.
ИБ №1056. Больной К., 68 лет, поступил в стационар 21.02.2002 г. по направлению участкового врача по поводу ИБС: стенокардии, периодических приступов сердцебиения. Из анамнеза известно, что больной страдает ИБС: стенокардией II функционального класса в течение последних 6 лет. Постоянно принимает моночинкве в дозе 50 мг в сутки, аспирин в дозе 300-400 мг в сутки, эналаприл (ренитек) в дозе 20 мг в сутки. В последние 3-4 месяца стал отмечать появление перебоев в работе сердца. При суточном мониторировании ЭКГ, выполненном амбулаторно 10.12.2001 г., была выявлена одиночная ПЭ с частотой до 26 экстрасистол в час.
В стационаре по данным клинико-инструментального обследования состояние больного было расценено как ИБС: стабильная стенокардия напряжения II функционального класса, данных за наличие "свежих" очаговых изменений миокарда выявлено не было. Больному была продолжена терапия моночинкве в дозе 50 мг в сутки, аспирином в дозе 300-400 мг в сутки, эналаприлом (ренитек) в дозе 20 мг в сутки.
На второй день пребывания больного в стационаре была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 25 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г. Иваново). На ЭКГ было выявлено 3-4 ПЭ в минуту. Затем были рассчитаны начало и наклон ТРС в 37 ПЭ.
Данные начала и наклона ТРС у больного К., 68 лет, представлены в таблице 4.
Результаты начала и наклона ТРС у больного К., 68 лет
Как видно из таблицы, начало ТРС составило -4,8% (норма <0%), наклон ТРС 18,6 мс/R-R (норма >2,5 мс/R-R) (см. таблицу 4, исходные данные). Средняя частота сердечного ритма составила 72 уд. в мин. Затем больному была проведена ЧПЭКС и индуцирована ПЭ с одинаковым предэктопическим интервалом, составившим 385 мс (что на 10% больше эффективного рефракторного периода атриовентрикулярного соединения, составившего 350 мс), так, чтобы до и после индуцированной ПЭ было 20 синусовых интервалов R-R. Данные начала и наклона ТРС у больного К., 68 лет, при индуцировании ПЭ с помощью ЧПЭКС представлены в таблице 4. Как видно из таблицы, начало ТРС составило +7,6% (норма <0%), наклон ТРС 1,6 мс/R-R (норма >2,5 мс/R-R) (см. таблицу 4, после ЧПЭКС).
У больного К., 68 лет, прогнозировалось развитие МП и ТП. В последующем больному была проведена терапия нитратами, аспирином, ренитеком (эналаприлом) в дозах, указанных выше. Противоаритмические препараты не назначались. Спонтанный приступ МП и ТП развился через 3,5 недели после обследования, купированный внутривенным введением новокаинамида в дозе 1000 мг. В качестве противорецидивной терапии пароксизмов МП и ТП больному дополнительно к проводимой терапии был назначен соталол в дозе 160 мг в сутки. Аритмия не рецидивировала на протяжении 2 лет.
Данный пример показал, что при регистрации ПЭ с началом ТРС<0% и наклоном ТРС>2,5 мс/R-R можно прогнозировать пароксизмы МП и ТП путем определения вышеуказанных показателей при индуцировании ПЭ (с одинаковым предэктопическим интервалом, составляющим на 10% больше эффективного рефракторного периода атриовентрикулярного соединения) с помощью ЧПЭКС, причем при значениях начала ТРС>0% и наклона ТРС<2,5 мс/R-R индуцированных НЖЭ прогнозируются пароксизмы МП и ТП в течение 3,5 недель после обследования.
Наблюдалось 119 больных ИБС, осложненной ПЭ. Всем больным проводилась терапия нитратами пролонгированного действия, антиагрегантами, ингибиторами ангиотензинпревращающего фермента (ренитек, эналаприл, энап). Антиаритмические препараты не назначались. У всех больных прогнозирование пароксизмов МП и ТП проводилось по предлагаемому способу и согласно прототипу - прогнозирование развития пароксизмов МП и ТП в зависимости от размера или объема правого и (или) левого предсердий, причем при дилатации одного или обоих предсердий более 4,0 см прогнозируются пароксизмы МП и ТП (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993).
Статистический анализ полученных результатов проведен на ЭВМ.
У 87 (73,11%) из всех обследованных пациентов согласно прототипу (Кушаковский М.С. Аритмии сердца. - Л.: Медицина, 1993) было выявлено увеличение левого предсердия более 4,0 см. У этих больных согласно прототипу прогнозировалось развитие пароксизмов МП и ТП в течение 1-3 лет после обследования. Всем больным согласно предлагаемому способу была проведена регистрация ЭКГ одновременно в 12 стандартных отведениях на протяжении 25-40 минут с помощью компьютерного комплекса «Полиспектр-ритм» (фирма «Нейрософт», г. Иваново). На ЭКГ было выявлено 2-6 ПЭ в минуту (в среднем 4±1 ПЭ в минуту). Затем были рассчитаны начало и наклон ТРС в 25-35 ПЭ у каждого больного.
У 40 (33,61%) из 119 обследованных больных наблюдались патологические значения ТРС ПЭ с началом ТРС>0% и наклоном ТРС<2,5 мс/R-R, в среднем составившие 7,4±0,3% и 1,2±0,1 мс/R-R соответственно, а у остальных значения ТРС ПЭ были в пределах нормы - с началом ТРС<0% и наклоном ТРС>2,5 мс/R-R, в среднем составившие -4,1±0,2% и 22,5±0,6 мс/R-R соответственно. Всем пациентам с нормальными значениями ТРС (при значениях начала ТРС<0% и наклона ТРС>2,5 мс/R-R) была индуцирована ПЭ (с одинаковым предэктопическим интервалом, составляющим на 10% больше эффективного рефракторного периода атриовентрикулярного соединения) с помощью ЧПЭКС, и на индуцированных ПЭ были рассчитаны начало и наклон ТРС.
Результаты исследования показали, что у 21 (26,58%) из 79 больных значения начала и наклона ТРС на индуцированных ПЭ с помощью ЧПЭКС оказались в пределах нормы и в среднем составили -7,5±0,3% и 23,4±0,4 мс/R-R соответственно, а у остальных были выявлены патологические значения ТРС индуцируемых ПЭ: значения этих показателей в среднем составили 6,3±0,2% и 1,1±0,1 мс/R-R соответственно.
У всех больных с нормальными значениями ТРС ПЭ (со значениями начала ТРС<0% и наклоном ТРС>2,5 мс/R-R), так и индуцированных ПЭ с помощью ЧПЭКС, у которых согласно предлагаемому способу не прогнозировались пароксизмы МП и ТП, развитие этих НСР не наблюдалось на протяжении 6 лет наблюдения, в то время как у остальных 96 (97,96%) из 98 больных, у которых по предлагаемому способу прогнозировались пароксизмы МП и ТП в течение 1 месяца после первого обследования, отмечалось развитие этих НСР в течение месяца (в среднем через 1,5±1,1 недели) после первого обследования, а у остальных - в течение 3 месяцев после первого обследования, в то время как только у 2 (2,30%) из 87 больных с дилатацией предсердий, у которых согласно прототипу прогнозировалось развитие пароксизмов МП и ТП в течение 1-3 лет после первого обследования, наблюдалось развитие пароксизмов этих НСР в течение месяца после первого обследования и у 7 (8,05%) из этих 87 больных - в течение года после первого обследования (Р<0,001).
Поэтому наиболее точно (в среднем в 42,6 раза) можно прогнозировать развитие пароксизмов МП и ТП в течение 1 месяца после первого обследования с помощью предлагаемого способа в сравнении с прототипом (см. таблицу 5).
Таким образом, более точно (в среднем в 42,6 раза) можно прогнозировать развитие пароксизмов МП и ТП с помощью предлагаемого способа в сравнении с прототипом, что обеспечит назначение адекватной терапии для предупреждения пароксизмов этих аритмий.
Сопоставление точности прогнозирования пароксизмов МП и ТМ предлагаемого способа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ У БОЛЬНЫХ С НАДЖЕЛУДОЧКОВОЙ ЭКСТРАСИСТОЛИЕЙ | 2005 |
|
RU2294137C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ У БОЛЬНЫХ С НАДЖЕЛУДОЧКОВОЙ ЭКСТРАСИСТОЛИЕЙ | 2006 |
|
RU2312592C1 |
| Способ прогнозирования наджелудочковых нарушений ритма сердца у пациентов, находящихся на хроническом гемодиализе | 2024 |
|
RU2838480C1 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ РАЗВИТИЯ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ, РЕФРАКТЕРНЫХ К ФАРМАКОЛОГИЧЕСКОЙ АНТИАРИТМИЧЕСКОЙ ТЕРАПИИ | 2004 |
|
RU2268079C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ ПАРОКСИЗМА ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ | 2013 |
|
RU2519758C1 |
| СПОСОБ ДИАГНОСТИКИ МЕХАНИЗМОВ ЖЕЛУДОЧКОВОЙ ЭКСТРАСИСТОЛИИ | 2005 |
|
RU2294138C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА РАЗВИТИЯ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У БОЛЬНЫХ С ПРЕДСЕРДНОЙ ЭКСТРАСИСТОЛИЕЙ | 2014 |
|
RU2556602C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ | 2000 |
|
RU2181257C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ФАРМАКОЛОГИЧЕСКОЙ АНТИАРИТМИЧЕСКОЙ ТЕРАПИИ В КАЧЕСТВЕ ПЕРВИЧНОЙ ПРОФИЛАКТИКИ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ У БОЛЬНЫХ С ПРЕДСЕРДНОЙ ЭКСТРАСИСТОЛИЕЙ | 2018 |
|
RU2688394C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РЕЦИДИВИРОВАНИЯ ВПЕРВЫЕ ВОЗНИКШИХ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ | 1999 |
|
RU2192775C2 |
Изобретение относится к медицине, к кардиологии. У больных с наджелудочковой экстрасистолией (НЖЭ) определяют начало турбулентности ритма сердца (ТРС) и наклон ТРС. При этом при выявлении начала ТРС<0% и наклона ТРС>2,5 мс/R-Rcp. после усреднения этих показателей как минимум в 10 экстрасистолических комплексах проводят с помощью чреспищеводной электрокардиостимуляции индуцирование как минимум 10 наджелудочковых экстрасистол с одинаковым предэктопическим интервалом, составляющим на 10% больше, чем эффективный рефракторный период атриовентрикулярного соединения так, чтобы до и после индуцированной экстрасистолы было не менее 20 синусовых комплексов. При выявлении начала ТРС>0% и наклона ТРС<2,5 мс/R-Rcp. до или после стимуляции как минимум в 10 экстрасистолических комплексах прогнозируют развитие пароксизмов мерцания и трепетания предсердий в течение месяца после обследования. Способ позволяет более точно прогнозировать развитие пароксизмов мерцания и трепетания предсердий. 5 табл.
Способ прогнозирования развития пароксизмов мерцания и трепетания предсердий у больных с наджелудочковой экстрасистолией (НЖЭ) путем определения начала турбулентности ритма сердца (ТРС) и наклона ТРС, отличающийся тем, что при выявлении начала ТРС<0% и наклона ТРС>2,5 мс/R-Rcp. после усреднения этих показателей как минимум в 10 экстрасистолических комплексах проводят, с помощью чреспищеводной электрокардиостимуляции, индуцирование как минимум 10 наджелудочковых экстрасистол с одинаковым предэктопическим интервалом, составляющим на 10% больше, чем эффективный рефракторный период атриовентрикулярного соединения так, чтобы до и после индуцированной экстрасистолы было не менее 20 синусовых комплексов и при выявлении начала ТРС>0% и наклона ТРС<2,5 мс/R-Rcp. до или после стимуляции как минимум в 10 экстрасистолических комплексах прогнозируют развитие пароксизмов мерцания и трепетания предсердий в течение месяца после обследования.
| КУШАКОВСКИЙ М.С | |||
| Аритмии сердца | |||
| - Л.: Медицина, 1993, с.231 | |||
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ | 2000 |
|
RU2181257C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ | 2000 |
|
RU2195872C2 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ РАЗВИТИЯ ПАРОКСИЗМОВ МЕРЦАНИЯ И ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ | 2002 |
|
RU2219975C2 |
| МАКАРОВ Л.М | |||
| и др | |||
| "Турбулентность ритма сердца" у больных с некоронарогенными тахиаритмиями | |||
| - Вестник аритмологии, 28.05.2004, №35, с.232-238 | |||
| CYGANKIEWICZ I | |||
| et al | |||
| Circadian changes in heart rate | |||
Авторы
Даты
2007-07-27—Публикация
2006-01-10—Подача