Область изобретения
Область данного изобретения относится к хромопротеинам и флуоресцентным белкам.
Предпосылки изобретения
Мечение представляет собой приспособление для маркировки интересующих белков, клетки или организма, и оно играет заметную роль во многих биохимических, молекулярно-биологических и медико-диагностических применениях. Разработано множество различных меток, включая радиоактивные метки, цветовые метки, флуоресцентные метки, хемилюминесцентные метки и т.д. Однако сохраняется интерес к разработке новых меток. Особенно интересной является разработка новых белковых меток, включая цветовые и/или флуоресцентные белковые метки.
Связанная литература
Интересующие патенты США включают: 6066476; 6020192; 5985577; 5976796; 5968750; 5968738; 5958713; 5919445; 5874304; и 5491084. Интересующие публикации Международных патентов включают: WO 00/46233; WO 99/49019; и DE 19718640 A. Также в круг интересов входят: Anderluh et al., Biochemical and Biophysical Research Communications (1996) 220:437-442; Dove et al., Biological Bulletin (1995) 189: 288-297; Fradkov et al., FEBS Lett. (2000) 479(3):127-30; Gurskaya et al., FEBS Lett., (2001) 507(1):16-20; Gurskaya et al., BMC Biochem. (2001) 2:6; Lukyanov, K., et al (2000) J Biol Chemistry 275 (34):25879-25882; Macek et al., Eur. J. Biochem. (1995) 234:329-335; Martynov et al., J Biol Chem. (2001) 276:21012-6; Matz, M. V., et al. (1999) Nature Biotechnol., 17:969-973; Terskikh et al., Science (2000) 290:1585-8; Tsien, Annual Rev. of Biochemistry (1998) 67:509-544; Tsien, Nat. Biotech. (1999) 17:956-957; Ward et al., J.Biol. Chem. (1979) 254:781-788; Wiedermann et al., Jarhrestagung der Deutschen Gesellschact fur Tropenokologie-gto. Ulm. 17-19.02.1999. Poster P-4.20; Yarbrough et al., Proc Natl Acad Sci U S A (2001) 98:462-7.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Раскрыты композиции нуклеиновых кислот, кодирующих новые хромопротеины/флуоресцентные белки и их мутанты, а также кодирующие то же самое белки. Интересующие белки являются белками, которые окрашены и/или флуоресцируют, причем данное свойство возникает вследствие взаимодействия двух или большего количества остатков данного белка. Указанные белки, кроме того, характеризуются тем, что их получают от не обладающих биолюминесценцией видов кишечнополостных (Cnidaria), например, коралловых полипов (Anthozoa), или от видов коралловых полипов, не относящихся к морским перьям (Pennatulacea). Конкретные интересующие белки включают в себя следующие конкретные белки: (1) зеленый флуоресцентный белок из Heteractis crispa (hcriGFP); (2) зеленый флуоресцентный белок из Dendronephthya sp. (dendGFP); (3) красный флуоресцентный белок от Zoanthus sp. (zoanRFP); (4) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP1); (5) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP2); (6) красный флуоресцентный белок из Ricordea florida (rfloRFP); (7) зеленый флуоресцентный белок из Ricordea florida (rfloGFP); (8) красный флуоресцентный белок из Montastraea cavernosa (mcavRFP); (9) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP); (10) зеленый флуоресцентный белок из Condylactis gigantea (cgigGFP); (11) зеленый флуоресцентный белок из Agaricia fragilis (afraGFP); (12) зеленый флуоресцентный белок из Ricordea florida (rfloGFP2); (13) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP2); и (14) гомолог зеленого флуоресцентного белка из Montastraea annularis (mannFP). Также в область интересов входят белки, по существу сходные с указанными выше белками или являющиеся их мутантами. Также раскрыты фрагменты нуклеиновой кислоты и кодируемые ими пептиды, а также антитела к указанным белкам, и трансгенные клетки и организмы. Указанные композиции нуклеиновых кислот и белков находят множество различных способов применения. Наконец, предоставляются наборы для использования в таких применениях, например, те, что включают указанные композиции нуклеиновой кислоты.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фигура 1. Изменение спектров эмиссии во время созревания новых красных люминофоров: zoan2RFP (A, B), mcavRFP (C, D) и rfloRFP (E, F). Возбуждающая длина волны дана на каждом графике. Горизонтальная ось представляет собой длину волны в нанометрах, вертикальная ось представляет собой интенсивность флуоресценции. Стадии созревания: А, С, E - ранние; B, D, F - поздние (для подробностей см. методы). Все три белка демонстрировали фенотип "таймер" (зеленая эмиссия вначале и красная эмиссия, возникающая позднее). Заметьте, что zoan2RFP созревает значительно быстрее, чем mcavRFP и rfloRFP: даже на "ранней" стадии пик красной эмиссии очень выражен, а на "поздней" стадии белок полностью превращается в красный. mcavRFP и rfloRFP, наоборот, не претерпевают такого полного созревания.
Фигура 2. Подробности спектров возбуждения mcavRFP (A, B) и rfloRFP (C, D). Длины волн, при которых отслеживали эмиссию, даны на графиках. A, C: спектры возбуждения полосы зеленой эмиссии в незрелом белке, неспособном к красной эмиссии. B, D: спектры возбуждения полосы красной эмиссии в более зрелой формы. Горизонтальная ось представляет собой длину волны в нанометрах, вертикальная ось представляет собой интенсивность флуоресценции. Заметьте, что в обоих белках основные пики возбуждения для незрелой зеленой и зрелой красной форм фактически идентичны друг другу.
Фигура 3. Филогенетическое древо максимальной вероятности для имеющегося в настоящее время набора данных GFP-подобных белков коралловых полипов. Числа в узлах означают четырежды усложненные поддерживающие значения (1000 попыток усложнения). Белки из подкласса Alcyonaria, которые сочли лежащими вне групп, помечены белым на черном. "Ствол" дерева (жирная серая линия), объединяющий две корневые группы, по-видимому, отражает разнообразие GFP-подобных белков до разделения подклассов Alcyonaria и Zoantharia. Серые полосы, маркированные A, B, C и D, четыре различные эволюционные группы GFP-подобных белков, обнаруженных в Zoantharia. Линейка масштаба: 0,1 замены/участок.
Фигура 4. Краткое изложение спектральных характеристик и структур хромофора семейства GFP-подобных белков. Заметьте, что в данной публикации используются названия для GFP-подобных белков, отличные от тех, что предлагаются в оригинальных публикациях (оригинальные названия, если доступны, даны в скобках в первом столбце; для подробностей номенклатуры см. текст).
Фигура 5. Краткое изложение главных эволюционных групп GFP-подобных белков из подкласса Zoantharia.
Фигура 6. Спектры возбуждения (сплошные линии) и эмиссии (пунктирные линии) для GFP-подобных белков, описанных в данной публикации. Длины волн, при которых были сняты кривые возбуждения или эмиссии, даны в легенде каждого графика. Горизонтальная ось представляет собой длину волны в нанометрах, вертикальная ось представляет собой интенсивность флуоресценции. Графики для двух новых оранжево-красных белков обрамлены.
Фигура 7А-7С. Выравнивание клонированных в настоящее время и спектроскопически охарактеризованных GFP-подобных белков. Нумерация над выравниванием приведена согласно GFP из Aequorea victoria.
На фигуре 8 предоставлена нуклеотидная и аминокислотная последовательность hcriGFP Heteractis crispa дикого типа.(SEQ ID NO: 01 & 02).
На фигуре 9 предоставлена нуклеотидная и аминокислотная последовательность dendGFP Dendronephthya sp. дикого типа.(SEQ ID NO: 03 & 04)
На фигуре 10 предоставлена нуклеотидная и аминокислотная последовательность zoanRFP Zoanthus sp. дикого типа.(SEQ ID NO: 05 & 06).
На фигуре 11 предоставлена нуклеотидная и аминокислотная последовательность scubGFP1 Scolymia cubensis дикого типа. (SEQ ID NO: 07 & 08).
На фигуре 12 предоставлена нуклеотидная и аминокислотная последовательность scubGFP2 Scolymia cubensis дикого типа.(SEQ ID NO: 09 & 10).
На фигуре 13 предоставлена нуклеотидная и аминокислотная последовательность rfloRFP Ricordea florida дикого типа. (SEQ ID NO: 11 & 12).
На фигуре 14 предоставлена нуклеотидная и аминокислотная последовательность rfloGFP Ricordea florida дикого типа (SEQ ID NO: 13 & 14).
На фигуре 15 предоставлена нуклеотидная и аминокислотная последовательность mcavRFP Montastraea cavernosa дикого типа (SEQ ID NO: 15 & 16).
На фигуре 16 предоставлена нуклеотидная и аминокислотная последовательность mcavGFP Montastraea cavernosa дикого типа (SEQ ID NO: 17 & 18).
На фигуре 17 предоставлена нуклеотидная и аминокислотная последовательность cgigGFP Condylactis gigantea дикого типа (SEQ ID NO: 19 & 20).
На фигуре 18 предоставлена нуклеотидная и аминокислотная последовательность afraGFP Agaricia fragilis дикого типа (SEQ ID NO: 21 & 22).
На фигуре 19 предоставлена нуклеотидная и аминокислотная последовательность rfloGFP2 Ricordea florida дикого типа (SEQ ID NO: 23 & 24).
На фигуре 20 предоставлена нуклеотидная и аминокислотная последовательность mcavGFP2 Montastraea cavernosa дикого типа (SEQ ID NO: 25 & 26).
На фигуре 21 предоставлена нуклеотидная и аминокислотная последовательность mannFP Montastraea annularis дикого типа (SEQ ID NO: 27 & 28).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к нуклеиновой кислоте, находящейся не в своем природном окружении, где нуклеиновая кислота кодирует хромофорный или флуоресцентный белок и происходит из не способных к биолюминесценции видов кишечнополостных. В некоторых осуществлениях не способные к биолюминесценции виды кишечнополостных представляют собой виды коралловых полипов. В некоторых осуществлениях нуклеиновую кислоту является выделенной. В некоторых осуществлениях нуклеиновая кислота находится не в своем природном окружении, где нуклеиновая кислота кодирует хромофорный или флуоресцентный белок коралловых полипов и происходит из не относящихся к морским перьям видов коралловых полипов. В некоторых осуществлениях нуклеиновая кислота характеризуется последовательностью остатков, которая по существу совпадает или идентична нуклеотидной последовательности длиной по крайней мере 10 остатков из SEQ ID NO: 01; 03; 05; 07; 09; 11; 13; 15; 17; 19; 21; 23; 25 и 27. В некоторых осуществлениях нуклеиновая кислота обладает сходством последовательности по крайней мере примерно на 60% с последовательностью длиной по крайней мере 10 остатков, выбранной из группы, состоящей из SEQ ID NO: 01; 03; 05; 07; 09; 11; 13; 15; 17; 19; 21; 23; 25 и 27. В некоторых осуществлениях нуклеиновая кислота кодирует хромофорный и/или флуоресцентный белок, который происходит: (a) из не способных к биолюминесценции видов кишечнополостных; или (b) из не относящихся к морским перьям видов коралловых полипов. В некоторых осуществлениях нуклеиновая кислота кодирует белок, который характеризуется аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 02; 04; 06; 08; 10; 12; 14; 16; 18; 20; 22; 24; 26; и 28. В некоторых осуществлениях нуклеиновая кислота кодирует мутантный белок хромофорного и/или флуоресцентного белка, который происходит: (a) из не способных к биолюминесценции видов кишечнополостных; или (b) из не относящихся к морским перьям видов коралловых полипов; где в некоторых осуществлениях мутантный белок содержит по крайней мере одну точечную мутацию по сравнению с соответствующим ему белком дикого типа; и в другом осуществлении мутантный белок содержит по крайней мере одну делеционную мутацию по сравнению с соответствующим ему белком дикого типа.
Также предоставлены фрагменты предоставленных нуклеиновых кислот. Также раскрыты выделенные нуклеиновые кислоты или их миметики, которые в жестких условиях гибридизуются с предоставленными нуклеиновыми кислотами. Также предоставлены конструкции, в состав которых входит вектор и нуклеиновая кислота по настоящему изобретению. Также предоставляются экспрессирующие кассеты, которые содержат: (a) область инициации транскрипции, функциональную в экспрессирующем хозяине; (b) нуклеиновую кислоту по настоящему изобретению; и (c) область терминации транскрипции, функциональную в указанном экспрессирующем хозяине. Также раскрыты клетки или их потомки, содержащие экспрессирующую кассету по настоящему изобретению как часть внехромосомного элемента или интегрированной в геном клетки хозяина в результате введения указанной экспрессирующей кассеты в указанную клетку хозяина.
Также раскрыты способы получения хромофорного и/или флуоресцентного белка, которые охватывают: выращивание клетки по настоящему изобретению, где экспрессирован указанный белок; и выделение указанного белка в значительной степени очищенным от других белков.
Также раскрыты белки или их фрагменты, кодируемые нуклеиновой кислотой по настоящему изобретению.
Также раскрыты антитела, специфично связывающиеся с белком по настоящему изобретению.
Также раскрыты трансгенные клетки или их потомки, которые содержат трансген, выбранный таким образом, что он содержит нуклеиновую кислоту по настоящему изобретению.
Также раскрыты трансгенные организмы, которые содержат трансген, который включает в себя нуклеиновую кислоту по настоящему изобретению.
Также предоставляются применения, в которых используется хромофорный или флуоресцентный белок по настоящему изобретению.
Также предоставляются применения, в которых используется нуклеиновая кислота, кодирующая хромофорный или флуоресцентный белок по настоящему изобретению.
Также предоставлены наборы, которые включают в свой состав нуклеиновую кислоту по настоящему изобретению и инструкции для применения указанной нуклеиновой кислоты.
ОПРЕДЕЛЕНИЯ
По настоящему изобретению могут использоваться общепринятые способы молекулярной биологии, микробиологии и рекомбинантной ДНК, находящиеся в пределах данной области знания. Такие способы полно раскрыты в литературе.
См., например, Maniatis, Fritsch & Sambrook, "Molecular Cloning: A Laboratory Manual (1982); "DNA Cloning: A Practical Approach," Volumes I and II (D.N. Glover ed., 1985); "Oligonucleotide Synthesis" (M.J. Gait ed. 1984); "Nucleic Acid Hybridization" (B.D. Hames & S.J. Higgins eds. (1985)); "Transcription and Translation" (B.D. Hames & S.J. Higgins eds. (1984)); "Animal Cell Culture" (R.I. Freshney, ed. (1986)); "Immobilized Cells and Enzymes" (IRL Press, (1986)); B. Perbal,"A Practical Guide To Molecular Cloning" (1984).
"Вектор" представляет собой репликон, такой как плазмида, фаг или космида, к которому может быть присоединен другой сегмент ДНК, что приводит к репликации присоединенного сегмента.
"Молекула ДНК" относится к полимерной форме дезоксирибонуклеотидов (аденин, гуанин, тимин или цитозин) в одноцепочной форме или в виде двухцепочечной спирали. Данный термин относится только к первичной или вторичной структуре молекулы, и не ограничивает ее какими-либо конкретными третичными формами. Таким образом, данный термин охватывает двухцепочечную ДНК, обнаруживаемую, между прочим, в линейных молекулах ДНК (например, во фрагментах рестрикции), вирусах, плазмидах и хромосомах.
"Кодирующая последовательность" ДНК представляет собой последовательность ДНК, которая транскрибируется и транслируется в полипептид in vivo при ее помещении под контроль подходящих регуляторных последовательностей. Границы кодирующей последовательности определяются стартовым кодоном с 5' (N-) конца и стоп-кодоном трансляции с 3' (С-) конца. Кодирующая последовательность может включать в себя в качестве неограничивающих примеров прокариотические последовательности, кДНК из эукариотической кДНК, геномные ДНК-последовательности из эукариотической ДНК (например, из млекопитающих), и синтетические последовательности ДНК. Сигнал полиаденилирования и последовательность терминации транскрипции могут локализоваться в 3'-направлении от кодирующей последовательности.
Применяемый здесь термин "гибридизация" относится к процессу ассоциации двух цепей нуклеиновой кислоты с образованием антипараллельного дуплекса, стабилизируемого посредством водородных связей между остатками противоположных цепей нуклеиновой кислоты.
Термин "олигонуклеотид" относится к короткой (менее 100 оснований в длину) молекуле нуклеиновой кислоты.
Применяемый здесь термин "регуляторные последовательности ДНК" относится к последовательностям контроля транскрипции и трансляции, таким как промоторы, энхансеры, сигналы полиаденилирования, терминаторы, и тому подобное, которые обеспечивают и/или регулируют экспрессию кодирующей последовательности в клетке хозяина.
"Промоторная последовательность" представляет собой регуляторную область ДНК, способную связывать в клетке РНК-полимеразу и инициировать транскрипцию кодирующей последовательности по ходу цепи (в 3'-направлении). Для целей определения настоящего изобретения промоторная последовательность связана со своего 3'-конца с сайтом инициации транскрипции и продлевается выше (в 5'-направлении), включая минимальное количество оснований или элементов, необходимых для инициации транскрипции на уровне, который можно выявить по сравнению с фоновым уровнем. В пределах промоторной последовательности находится сайт инициации транскрипции, а также связывающие белок домены, ответственные за связывание РНК-полимеразы.
Эукариотические промоторы часто, но не всегда содержат "TATA"-боксы и "CAT"-боксы. Различные промоторы, включая индуцируемые промоторы, могут использоваться для управления различными векторами по настоящему изобретению.
Применяемые здесь термины "рестрикционные эндонуклеазы" и "ферменты рестрикции" относятся к бактериальным ферментам, каждый из которых разрезает двухцепочечную ДНК по специфичной нуклеотидной последовательности или около нее.
Клетка "трансформирована" или "трансфицирована" экзогенной или гетерологичной ДНК, когда такая ДНК введена внутрь клетки. Трансформирующая ДНК может быть или не быть интегрированной в геном клетки (ковалентно связанной). Например, в прокариотах, дрожжах, и клетках млекопитающих трансформирующая ДНК может поддерживаться в эписомном элементе, таком как плазмида.
В отношении эукариотических клеток стабильно трансформированная клетка является той, в которой ДНК интегрировалась в хромосому, так что она наследуется дочерней клеткой путем репликации хромосомы. Данная стабильность демонстрируется способностью эукариотической клетки поддерживать клеточные линии или клоны, состоящие из популяции дочерних клеток, содержащих трансформирующую ДНК. "Клон" представляет собой популяцию клеток, происходящих из единственной клетки или общего предка путем митоза. "Клеточная линия" представляет собой клон первичной клетки, который способен к стабильному росту in vitro в течение многих поколений.
"Гетерологичная" область ДНК-конструкции представляет опознаваемый сегмент ДНК внутри более крупной молекулы ДНК, причем он не обнаруживается в ассоциации с данной более крупной молекулой в природе. Таким образом, когда гетерологичная область кодирует ген млекопитающего, данный ген обычно фланкирован ДНК, которая не фланкирует геномную ДНК млекопитающего в геноме исходного организма. В другом примере гетерологичная ДНК включает кодирующую последовательность в конструкции, где части генов из двух разных источников собраны вместе, так что получается продукт в виде белка слияния. Аллельные вариации встречающихся в природе мутационных событий не приводят к образованию гетерологичной области ДНК, как определено здесь.
Используемый здесь термин "репортерный ген" относится к кодирующей последовательности, присоединенной к гетерологичному промоторному или энхансерному элементу, и продукт которой может легко и количественно анализироваться при введении конструкции в ткани или клетки.
Описанные здесь аминокислоты предпочтительно находятся в "L"-изомерной форме. Аминокислотные последовательности даны в однобуквенном коде (A: аланин; C: цистеин; D: аспарагиновая кислота; E: глутаминовая кислота; F: фенилаланин; G: глицин; H: гистидин; I: изолейцин; K: лизин; L: лейцин; M: метионин; N: аспарагин; P: пролин; Q: глутамин; R: аргинин; S: серин; T: треонин; V: валин; W: триптофан; Y: тирозин; X: любой остаток). NH2 относится к свободной аминогруппе, присутствующей на N-конце полипептида. COOH относится к свободной карбоксигруппе, присутствующей на С-конца полипептида. Применяется стандартная полипептидная номенклатура по J. Biol. Chem., 243 (1969), 3552-59.
Термин "иммунологически активный" означает способность природного, рекомбинантного или синтетического хромофорного/флуоресцентного белка или его любого олигопептида индуцировать специфический иммунный ответ в подходящих животных или клетках и связываться со специфическими антителами. Применяемый здесь термин "антигенная аминокислотная последовательность" означает аминокислотную последовательность, каковая сама по себе или в ассоциации с молекулой носителя может вызывать у млекопитающего ответ антител. Термин "специфичное связывание" в контексте связывания антитела с антигеном, является термином, хорошо понятным в данной области и относится к связыванию антитела с антигеном, против которого получено антитело, но не с другими, неродственными антигенами.
Используемый здесь термин "выделенный" применяется для описания полинуклеотида, полипептида, антитела или клетки хозяина, которая находится в окружении, отличающемся от того, в котором данный полинуклеотид, полипептид, антитело или клетка хозяина встречается в природе.
Биолюминесценция (BL) определяется как испускание света живыми организмами, которое хорошо видно в темноте и влияет на зрительное поведение животных (См., например, Harvey, E. N. (1952). Bioluminescence. New York: Academic Press; Hastings, J. W. (1995). Bioluminescence. In: Cell Physiology (ed. by N. Speralakis). pp. 651-681. New York: Academic Press; Wilson, T. and Hastings, J. W. (1998). Bioluminescence. Annu Rev Cell Dev Biol 14, 197-230.). Биолюминесценция не включает так называемое сверхслабое испускание света, которое может детектироваться по существу во всех живущих структурах с использованием чувствительного люминометрического оборудования (Murphy, M. E. and Sies, H. (1990). Visible-range low-level chemiluminescence in biological systems. Meth. Enzymol. 186,595-610; Radotic, K, Radenovic, C., Jeremic, M. (1998) Spontaneous ultra-weak bioluminescence in plants: origin, mechanisms and properties. Gen Physiol Biophys 17, 289-308), и слабое испускание света, которое, по всей вероятности, не играет какой-либо экологической роли, такое как свечение конуса роста бамбука (Totsune, H., Nakano, M., Inaba, H. (1993). Chemiluminescence from bamboo shoot cut. Biochem. Biophys. Res Comm. 194, 1025-1029) или испускание света во время оплодотворения яйцеклеток животного (Klebanoff, S. J., Froeder, C. A., Eddy, E. M., Shapiro, B. M. (1979). Metabolic similarities between fertilization and phagocytosis. Conservation of peroxidatic mechanism. J. Exp. Med. 149, 938-953; Schomer, B. and Epel, D. (1998). Redox changes during fertilization and maturation of marine invertebrate eggs. Dev Biol 203, 1-11).
ОПИСАНИЕ КОНКРЕТНЫХ ОСУЩЕСТВЛЕНИЙ
Раскрыты композиции нуклеиновых кислот, кодирующих новые хромопротеины/флуоресцентные белки и их мутанты, а также кодирующие то же самое белки. Интересующие белки являются белками, которые окрашены и/или флуоресцируют, причем данное свойство возникает вследствие взаимодействия двух или большего количества остатков данного белка. Указанные белки, кроме того, характеризуются тем, что их получают от не обладающих биолюминесценцией видов кишечнополостных (Cnidaria), например, коралловых полипов (Anthozoa), или от видов коралловых полипов, не относящихся к морским перьям (Pennatulacea). Конкретные интересующие белки включают следующие конкретные белки: (1) зеленый флуоресцентный белок из Heteractis crispa (hcriGFP); (2) зеленый флуоресцентный белок из Dendronephthya sp. (dendGFP); (3) красный флуоресцентный белок от Zoanthus sp. (zoanRFP); (4) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP1); (5) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP2); (6) красный флуоресцентный белок из Ricordea florida (rfloRFP); (7) зеленый флуоресцентный белок из Ricordea florida (rfloGFP); (8) красный флуоресцентный белок из Montastraea cavernosa (mcavRFP); (9) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP); (10) зеленый флуоресцентный белок из Condylactis gigantea (cgigGFP); (11) зеленый флуоресцентный белок из Agaricia fragilis (afraGFP); (12) зеленый флуоресцентный белок из Ricordea florida (rfloGFP2); (13) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP2); и (14) гомолог зеленого флуоресцентного белка из Montastraea annularis (mannFP). Также в область интересов входят белки, по существу сходные с указанными выше белками или являющиеся их мутантами. Также раскрыты фрагменты нуклеиновой кислоты и кодируемые ими пептиды, а также антитела к указанным белкам и трансгенные клетки и организмы, которые включают указанные композиции нуклеиновой кислоты/белка. Указанные композиции нуклеиновых кислот и белков находят множество различных способов применения. Наконец, предоставляются наборы для использования в таких применениях, например, те, что включают указанные композиции нуклеиновой кислоты.
Перед дальнейшим описанием настоящего изобретения следует понять, что данное изобретение не ограничено конкретными осуществлениями изобретения, описанными ниже, так как могут быть осуществлены вариации конкретных изобретений, и тем не менее, они войдут в объем прилагаемой формулы изобретения. Также следует понимать, что использованная терминология предназначена для целей описания конкретных осуществлений и не подразумевается как ограничивающая. Вместо этого объем настоящего изобретения устанавливается прилагаемой формулой изобретения.
В данной спецификации и прилагаемой формуле изобретения единственное число включает также ссылки на множественное число, кроме тех случаев, когда контекст четко не определяет иного. Если не определено иначе, все используемые здесь технические и научные термины имеют то же значение, которое обычно подразумевается рядовым специалистом в области, к которой относится изобретение.
Там, где предоставляются интервал значений, подразумевается, что изобретение относится к каждому промежуточному между верхним и нижним пределом данного интервала значению до десятой доли нижнего предела, кроме случаев, где контекст четко определяется иное, и к каждому другому установленному или промежуточному значению в установленном интервале. Верхнее и нижнее предельное значение данных меньших интервалов могут независимо входить в состав меньших интервалов, и также относятся к изобретению, при этом подчиняясь тому, что каждое предельное значение может конкретно исключаться из установленного интервала. В случае когда установленный интервал включает в себя один или оба предельных значения, интервалы, исключающие один или оба данных включенных предельных значения, также относятся к изобретению.
Если не определено иначе, все используемые здесь технические и научные термины имеют то же значение, которое обычно подразумевается рядовым специалистом в области, к которой относится изобретение. Хотя в воплощении или тестировании данного изобретения могут использоваться любые способы, устройства и материалы, сходные или эквивалентные тем что здесь описаны, в настоящее время описываются предпочтительные способы, устройства и материалы.
Все упомянутые здесь публикации включены сюда в качестве ссылки с целью описания и раскрытия описанных в данных публикациях клеточных линий, векторов, методологий и других компонентов по изобретению, которые могут использоваться в связи с описанным здесь изобретением.
В дальнейшем описании настоящего изобретения вначале будут описаны указанные композиции нуклеиновой кислоты с последующим обсуждением указанных белковых композиций, композиций антител и трансгенных клеток/организмов. Затем предоставляется обзор репрезентативных способов, в которых находят применение указанные белки.
КОМПОЗИЦИИ НУКЛЕИНОВОЙ КИСЛОТЫ
Как резюмировалось выше, настоящее изобретение относится к композициям нуклеиновой кислоты, кодирующим хромофорные и флуоресцентные белки и их мутанты, а также гомологи и фрагменты данных белков. Под хромофорным и/или флуоресцентным белком подразумевается белок, который окрашен, т.е. пигментирован, причем белок может быть или не быть флуоресцентным, например он может характеризоваться слабой, средней или высокой степенью флуоресценции после облучения светом с возбуждающей длиной волны. В любом случае указанные интересующие белки являются теми, в которых цветовая характеристика, т.е. хромофорная и/или флуоресцентная характеристика, возникает вследствие взаимодействия двух или большего количества остатков белка, но не из-за одного остатка, более конкретно одной боковой цепи одного остатка белка. Как таковое флуоресцентные белки по настоящему изобретению не охватывают белки, которые характеризуются флуоресценцией только из остатков, которые действуют сами по себе как внутренние флуоресцирующие агенты, т.е., триптофан, тирозин и фенилаланин. Как таковые флуоресцентные белки по настоящему изобретению представляют собой флуоресцентные белки, флуоресценция которых возникает от некоторой структуры в белке, которая отличается от указанных ранее единичных остатков, например, она возникает вследствие взаимодействия двух или большего количества остатков.
Под композицией нуклеиновых кислот подразумевается композиция, содержащая последовательность ДНК, характеризующуюся открытой рамкой считывания, которая кодирует хромофорный/флуоресцентный полипептид по настоящему изобретению, т.е. хромофорным/флуоресцентным геном, и способна в подходящих условиях экспрессироваться в виде хромофорного/флуоресцентного белка по настоящему изобретению. Также в данный термин входят нуклеиновые кислоты, которые гомологичны, по существу сходны или идентичны нуклеиновым кислотам по настоящему изобретению. Таким образом, настоящее изобретение предоставляет гены и их кодирующие последовательности, кодирующие белки по настоящему изобретению, а также их гомологи. Указанные нуклеиновые кислоты находятся не в своем природном окружении, например, они выделены, присутствуют в обогащенных количествах, и т.д., из их встречающегося в природе окружения, например, организма, из которого они получены.
Нуклеиновые кислоты далее характеризуются тем, что они кодируют белки, происходящие из: (1) не характеризующихся биолюминесценцией видов, часто из не характеризующихся биолюминесценцией видов кишечнополостных, например, не характеризующихся биолюминесценцией видов коралловых полипов; или (2) из видов коралловых полипов, которые не относятся к видам Pennatulacea, т.е. не являются морскими перьями.
Как таковые нуклеиновые кислоты могут кодировать белки из биолюминесцентных видов коралловых полипов, если они не относятся к видам Pennatulacea, например не являются видами Renilla или Ptilosarca. Конкретные интересующие нуклеиновые кислоты являются теми, что кодируют следующие конкретные белки: (1) зеленый флуоресцентный белок из Heteractis crispa (hcriGFP) (инвентарный № Генбанка AF420592); (2) зеленый флуоресцентный белок из Dendronephthya sp. (dendGFP) (инвентарный № Генбанка AF420591); (3) красный флуоресцентный белок из Zoanthus sp. (zoanRFP) (инвентарный № Генбанка AY059642); (4) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP1) (инвентарный № Генбанка AY037767); (5) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP2) (инвентарный № Генбанка AY037771); (6) красный флуоресцентный белок из Ricordea florida (rfloRFP) (инвентарный № Генбанка AY037773); (7) зеленый флуоресцентный белок из Ricordea florida (rfloGFP) (инвентарный № Генбанка AY037772); (8) красный флуоресцентный белок из Montastraea cavernosa (mcavRFP) (инвентарный № Генбанка AY037770); (9) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP) (инвентарный № Генбанка AY037769); (10) зеленый флуоресцентный белок из Condylactis gigantea (cgigGFP) (инвентарный № Генбанка AY03776); (11) зеленый флуоресцентный белок из Agaricia fragilis (afraGFP); (12) зеленый флуоресцентный белок из Ricordea florida (rfloGFP2); (13) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP2); и (14) гомолог зеленого флуоресцентного белка из Montastraea annularis (mannFP). Также в сферу интересов входят производные формы или мутанты, гомологи указанных выше нуклеиновых кислот.
В дополнение к описанным выше конкретным композициям нуклеиновой кислоты в круг интересов входят гомологи указанных выше последовательностей. В отношении гомологов указанных нуклеиновых кислот источником гомологичных генов может быть любой вид растения или животного, или последовательность может быть полностью или частично синтетической. В конкретных осуществлениях сходство последовательности между гомологами составляет, по крайней мере, примерно 20%, иногда, по крайней мере, примерно 25%, и может составлять 30%, 35%, 40%, 50%, 60%, 70% или выше, включая 75%, 80%, 85%, 90% и 95% или выше. Сходство последовательности вычисляют на основе последовательности сравнения, которая может представлять собой отрезок большей последовательности, такой как консервативный мотив, кодирующий участок, фланкирующий участок, и т.д. Последовательность сравнения обычно составляет, по крайней мере, 18 нуклеотидов длиной, обычно, по крайней мере, 30 нуклеотидов длиной, и может простираться до длины полной последовательности, с которой происходит сравнение. Алгоритмы для анализа последовательности, такие как BLAST, описанный Altschul et al. (1990), J. Mol.Biol. 215: 403-10 (с использованием установок по умолчанию, т.е. параметры w=4 и T=17) известны в данной области. Предоставленные здесь последовательности являются существенными для распознавания родственных и гомологичных нуклеиновых кислот при поиске в базах данных. Особенно интересными в некоторых осуществлениях являются нуклеиновые кислоты по существу той же длины, что нуклеиновая кислота, установленная как SEQ ID NO: 01, 03, 05, 07, 09, 11, 13, 15, 17, 19, 21, 23, 25 или 27, где по существу та же длина означает, что любое различие по длине не превышает примерно 20 числовых %, обычно не превышает примерно 10 числовых %, и чаще не превышает примерно 5 числовых %; и они характеризуются идентичностью по последовательности в отношении любой из данных последовательностей, равной, по крайней мере, примерно 90%, обычно, по крайней мере, примерно 95% и, чаще, по крайней мере, примерно 99%, по всей длине нуклеиновой кислоты. Во многих осуществлениях нуклеиновые кислоты характеризуются последовательностью, которая по существу сходна (то есть такая же) или идентична последовательностям SEQ ID NO: 01, 03, 05, 07, 09, 11, 13, 15, 17, 21, 23, 25, 27. Под по существу сходными подразумевается, что идентичность последовательности в основном составляет, по крайней мере, примерно 60%, обычно, по крайней мере, примерно 75% и часто, по крайней мере, примерно 80, 85, 90, или даже 95%.
Также раскрыты нуклеиновые кислоты, которые кодируют белки, кодируемые описанными выше нуклеиновыми кислотами, но отличаются по последовательности от описанных выше нуклеиновых кислот вследствие вырожденности генетического кода.
Также раскрыты нуклеиновые кислоты, которые гибридизуются с описанными выше нуклеиновыми кислотами в жестких условиях. Примером жестких условий гибридизации является гибридизация при 50°C или выше и 0,1·SSC (15 мМ хлорид натрия /1,5 мМ цитрат натрия). Другим примером условий жесткой гибридизации является инкубация в течение ночи при 42°C в растворе: 50% формамид, 5·SSC (150 мМ NaCl, 15 мМ трехзамещенный цитрат натрия), 50 мМ фосфат натрия (pH 7,6), 5× раствор Denhardt, 10% декстрансульфат, и 20 мкг/мл денатурированной расщепленной ДНК спермы лосося, с последующей промывкой фильтров в 0,1·SSC примерно при 65°C.
Жесткие условия гибридизации представляют собой условия гибридизации, которые являются по крайней мере такими же жесткими, как представленные выше условия, где условия считаются по крайней мере такими же жесткими, если они по крайней мере на 80%, обычно по крайней мере на 90% столь же жесткие, как конкретные условия жесткости, приведенные выше. В данной области известны другие жесткие условия гибридизации и также могут использоваться для идентификации нуклеиновых кислот по данному конкретному осуществлению изобретения.
Также раскрыты нуклеиновые кислоты, кодирующие мутантные формы белков по изобретению. Мутантные нуклеиновые кислоты могут быть получены путем случайного мутагенеза или нацеленного мутагенеза с использованием хорошо известных способов, которые являются рутинными в данной области. В некоторых осуществлениях хромофорные или флуоресцентные белки, кодируемые нуклеиновыми кислотами, кодирующих гомологи или мутанты, обладают такими же флуоресцентными свойствами, как флуоресцентный белок дикого типа. В других осуществлениях нуклеиновые кислоты гомолога или мутанта кодируют хромофорные или флуоресцентные белки с измененными спектральными свойствами, что описано здесь боле подробно.
Одной из категорий мутантов, которая особенно интересна, является неагрегирующий мутант. Во многих осуществлениях неагрегирующий мутант отличается от последовательности дикого типа мутацией N-конца, которая модулирует заряды, имеющие место на боковых группах N-концевых остатков, например, с изменением на противоположный или нейтрализацией данного заряда, способом, достаточным для получения неагрегирующего мутанта встречающегося в природе белка или мутанта, где конкретный белок считается неагрегирующим, если он определен как неагрегирующий с использованием анализа, описанного в заявке на выдачу патента США № 60/270983, описание которого включено сюда полностью в качестве ссылки.
Другой особенно интересующей категорией мутанта является мутант с модулированной олигомеризацией. Мутант считается мутантом с модулированной олигомеризацией, если свойства его олигомеризации отличаются по сравнению с таковыми белка дикого типа. Например, если конкретный мутант олигомеризуется в большей или меньшей степени по сравнению с диким типом, считается, что он является мутантом олигомеризации. Особенно интересными являются мутанты олигомеризации, которые не олигомеризуются, т.е. представляют собой мономеры в физиологических (например, внутриклеточных) условиях, или олигомеризуются в меньшей степени, чем дикий тип, т.е. представляют собой димеры или тримеры во внутриклеточных условиях.
Нуклеиновые кислоты по настоящему изобретению могут представлять собой кДНК или геномную ДНК или их фрагмент. В конкретных осуществлениях нуклеиновые кислоты по настоящему изобретению включают в себя одну или несколько открытых рамок считывания, кодирующих конкретные флуоресцентные белки и полипептиды, и интроны, а также прилегающие 5'- и 3'-некодирующие нуклеотидные последовательности, участвующие в регуляции экспрессии, продлевающиеся примерно до расстояния 20 тыс. н.п. от кодирующей области, но, возможно, и дальше в каждом направлении. Указанные нуклеиновые кислоты могут быть введены в подходящий вектор для внехромосомного поддержания или для интеграции в геном хозяина, как более подробно описано ниже.
Подразумевается, что используемый здесь термин "кДНК" охватывает все нуклеиновые кислоты, которые имеют набор элементов последовательности, находящихся в нативных молекулах зрелой мРНК, где элементы последовательности представляют собой экзоны и 5'- и 3'-некодирующие области.
Обычно молекулы мРНК содержат следующие друг за другом экзоны, тогда как лежащие между ними интроны, если они имеются, удаляются путем сплайсинга РНК в ядре с образованием протяженной открытой рамки считывания, кодирующей белок.
Интересующая геномная последовательность включает в себя нуклеиновую кислоту между инициаторным кодоном и стоп-кодоном, что определено перечисленными последовательностями, включая все интроны, которые обычно присутствуют в нативной хромосоме. Она может, кроме того, включать в себя 5'- или 3'-нетранслируемые области, находящиеся в зрелой мРНК. Она может, кроме того, включать в себя специфичные последовательности регуляции транскрипции и трансляции, такие как промоторы, энхансеры, и т.д., охватывая около 1 тыс. н.п., но, возможно, больше фланкирующей геномной ДНК с 5'- или 3'-конца транскрибируемой области. Геномная ДНК может быть выделена в виде фрагмента длиной 100 тыс. н.п. или менее; и может быть по существу лишенной фланкирующей хромосомной последовательности. Геномная ДНК, фланкирующая кодирующую область с 3' или с 5'-конца, или внутренние регуляторные последовательности, которые иногда находятся в интронах, содержат последовательности, требуемые для надлежащей экспрессии, специфичной для ткани и стадии.
Композиции нуклеиновой кислоты по настоящему изобретению может кодировать указанные белки целиком или частями. Двух- или одноцепочечные фрагменты могут быть получены из последовательности ДНК путем химического синтеза олигонуклеотидов общепринятыми способами, путем расщепления ферментами рестрикции, путем ПЦР-амплификации, и т.д. По большей части фрагменты ДНК составляют, по крайней мере, примерно 15 нуклеотидов, обычно, по крайней мере, примерно 18 нуклеотидов или примерно 25 нуклеотидов и может составлять по крайней мере, примерно 50 нуклеотидов.
В некоторых осуществлениях указанные молекулы нуклеиновой кислоты могут составлять примерно 100 нуклеотидов, примерно 200 нуклеотидов, примерно 300 нуклеотидов, примерно 400 нуклеотидов, примерно 500 нуклеотидов, примерно 600 нуклеотидов, примерно 700 нуклеотидов, или 720 нуклеотидов в длину. Указанные нуклеиновые кислоты могут кодировать фрагменты указанных белков или полноразмерные белки, например, указанные нуклеиновые кислоты могут кодировать полипептиды, равные примерно 25 а.к., примерно 50 а.к., примерно 75 а.к., примерно 100 а.к., примерно 125 а.к., примерно 150 а.к., примерно 200 а.к., примерно 210 а.к., примерно 220 а.к., примерно 230 а.к. или примерно 240 а.к, до размера целого белка.
Указанные нуклеиновые кислоты выделяют и получают по существу очищенными, в основном в ином виде, чем в интактной хромосоме. Обычно данную ДНК получают по существу очищенной от других последовательностей нуклеиновой кислоты, которые не включают в себя нуклеиновую кислоту по настоящему изобретению или ее фрагментов, и она в основном очищена, по крайней мере, примерно до 50%, обычно, по крайней мере, примерно до 90%, и, как правило, обычно является "рекомбинантной", т.е., фланкированной одним или несколькими нуклеотидами, с которыми она обычно не ассоциирована во встречающейся в природе хромосоме.
Раскрыты указанные полинуклеотиды (например, полинуклеотид, характеризующийся последовательностью SEQ ID NO: 01, 03, 05, 07, 09, 11, 13, 15, 17, 19, 21, 23, 25, 27, и т.д.), соответствующая кДНК, полноразмерный ген и конструкции указанных полинуклеотидов. Данные молекулы могут генерироваться синтетически с использованием некоторого количества протоколов, известных специалистам в данной области. Подходящие полинуклеотидные конструкции очищены с использованием стандартных способов рекомбинантной ДНК, как, например, описано в Sambrook et al., Molecular Cloning: A Laboratory Manual, 2nd Ed., (1989) Cold Spring Harbor Press, Cold Spring Harbor, NY, и по действующим предписаниям, описанным в United States Dept. of HHS, National Institute of Health (NIH) Guidelines for Recombinant DNA Research.
Также раскрыты нуклеиновые кислоты, которые кодируют белки слияния указанных белков или их фрагментов, которые объединены со вторым белком, например, последовательностью деградации, сигнальным пептидом, и т.д. Белки слияния могут содержать указанный полипептид или его фрагменты и полипептид, не относящийся к коралловым полипам, ("партнер слияния"), присоединенный в рамку с N-конца и/или C-конца указанного полипептида. Партнеры слияния включают в себя в качестве неограничивающих примеров полипептиды, которые могут связываться с антителом, специфичным к партнеру слияния (например, эпитопные метки); антитела или их связывающие фрагменты; полипептиды, которые предоставляют каталитическую функцию или индуцируют клеточный ответ; лиганды или рецепторы или их миметики и тому подобное. В таких белках слияния партнер слияния в основном в природе не ассоциирован с указанной частью белка слияния, относящейся к коралловому полипу, и обычно не является белком кораллового полипа или его производным/фрагментом, например, он не обнаружен в видах коралловых полипов.
Также раскрыты конструкции, содержащие указанные нуклеиновые кислоты, встроенные в вектор, где такие конструкции могут использоваться для некоторого числа различных применений, включая воспроизводство, продукцию белка, и т.д. Могут быть получены и использоваться вирусные и невирусные векторы, включая плазмиды. Выбор вектора зависит от типа клетки, в которых требуется воспроизводство и цели воспроизводства. Некоторые векторы могут использоваться для амплификации и получения большого количества требуемой последовательности ДНК. Другие векторы могут использоваться для экспрессии в клетках в культуре. Еще одни векторы могут использоваться для переноса и экспрессии в клетках целого животного или субъекта. Выбор подходящего вектора известен специалисту в данной области. Многие такие векторы доступны коммерчески. Для получения конструкций частичный или полноразмерный полинуклеотид встраивают в вектор, обычно посредством присоединения ДНК-лигазой в участке расщепления ферментом рестрикции в векторе. Альтернативно требуемая нуклеотидная последовательность может встраиваться путем гомологичной рекомбинации in vivo. Обычно это осуществляется путем присоединения областей гомологии в вектор по краям требуемой нуклеотидной последовательности. Области гомологии добавляют путем лигирования олигонуклеотидов или путем полимеразной цепной реакции с использованием праймеров, содержащих область гомологии и часть требуемой нуклеотидной последовательности, например.
Также предоставляются экспрессирующие кассеты или системы, которые среди прочих применений используются при синтезе указанных белков. Для экспрессии генный продукт, кодируемый полинуклеотидом по изобретению, экспрессируют в любой подходящей системе экспрессии, включая, например, системы, относящиеся к бактериям, дрожжам, насекомым, амфибиям и млекопитающим. Подходящие векторы и клетки хозяина описаны в патенте США № 5654173. В данном экспрессирующем векторе указанный полинуклеотид, установленный в SEQ ID NO: 01; 03; 05; 07; 09; 11; 13; 15; 17; 19; 21; 23; 25 или 27, связывают с регуляторной последовательностью, как следует для получения требуемых свойств экспрессии. Данные регуляторные последовательности могут включать в себя промоторы (присоединенные с 5'-конца смысловой цепи или с 3'-конца антисмысловой цепи), энхансеры, терминаторы, операторы, репрессоры и индукторы. Промоторы могут быть регулируемыми или конститутивными. В некоторых ситуациях может требоваться применение промоторов, активных в определенных условиях, таких как тканеспецифические или специфичные для определенных стадия развития промоторы. Их связывают с требуемой нуклеотидной последовательностью с использованием способов, описанных выше для связывания с векторами. Могут использоваться любые способы, известные в данной области. Иными словами, экспрессирующий вектор предоставляет область инициации транскрипции и трансляции, которая может быть индуцируемым или конститутивным, где кодирующая область функционально связана для транскрипционного контроля с областью инициации транскрипции, и областью терминации трансляции и транскрипции. Данные области контроля могут быть природными, относящимися к указанному виду, от которого получают указанную нуклеиновую кислоту, или может быть получена из экзогенных источников.
Экспрессирующие векторы в основном содержат подходящие сайты рестрикции, расположенные вблизи промоторной последовательности для обеспечения вставки последовательностей нуклеиновой кислоты, кодирующих гетерологичные белки. Может присутствовать подлежащий селекции маркер, функциональный в экспрессирующем хозяине. Экспрессирующие векторы могут применяться, среди прочего, для продукции белков слияния, как описано выше.
Могут быть получены экспрессирующие кассеты, содержащие область инициации транскрипции, ген или его фрагмент, и область терминации транскрипции. Особенно интересным является применение последовательностей, которые обеспечивают экспрессию функциональных эпитопов или доменов, длиной обычно примерно 8 аминокислот, чаще, по крайней мере, примерно 15 аминокислот длиной, до 25 аминокислот и вплоть до длины полной открытой рамки считывания гена. После введения ДНК клетки, содержащие конструкцию, могут подвергаться селекции посредством селектируемого маркера; клетки размножают и затем используют для экспрессии.
Описанные выше экспрессирующие системы могут использоваться с прокариотами или эукариотами по общепринятым способам в зависимости от цели экспрессии. Для полномасштабной продукции белка в качестве экспрессирующих клеток хозяина может использоваться одноклеточный организм, такой как E. coli, B. subtilis, S. cerevisiae, клетки насекомых в комбинации с бакуловирусными векторами, или клетки высшего организма, такого как позвоночные, например клетки COS 7, HEK 293, CHO, ооциты Xenopus и т.д. В некоторых ситуациях требуется экспрессировать гены в эукариотических клетках, где экспрессированный белок будет иметь преимущество из-за нативного фолдинга и посттрансляционных модификаций. Малые пептиды также могут быть синтезированы в лаборатории. Полипептиды, представляющие собой участки целой белковой последовательности, могут использоваться для идентификации и исследования частей белка, значимых в плане функции.
Конкретные интересующие экспрессирующие системы включают экспрессирующие системы на основе клеток бактерий, дрожжей, насекомых и млекопитающих. Представители таких систем из каждой данной категории представлены ниже.
Бактерии. Системы экспрессии в бактериях включают в себя те, что описаны в Chang et al., Nature (1978) 275: 615; Goeddel et al., Nature (1979) 281:544; Goeddel et al., Nucleic Acids Res. (1980) 8: 4057; Европейском патенте 0036776; патенте США № 4551433; DeBoer et al., Proc. Natl. Acad. Sci. (USA) (1983) 80: 21-25; и Siebenlist et al., Cell (1980) 20: 269.
Дрожжи. Экспрессирующие системы в дрожжах включают в себя те, описаны в Hinnen et al., Proc. Natl. Acad. Sci. (USA) (1978) 75:1929; Ito et al., J. Bacteriol. (1983) 153:163; Kurtz et al., Mol. Cell. Biol. (1986) 6: 142; Kunze et al., J. Basic Microbiol. (1985) 25: 141; Gleeson et al., J. Gen. Microbiol. (1986) 132:3459; Roggenkamp et al., Mol. Gen. Genet. (1986) 202: 302; Das et al., J. Bacteriol. (1984) 158:1165; De Louvencourt et al., J. Bacteriol. (1983) 154:737; Van den Berg et al., Bio/Technology (1990) 8:135; Kunze et al., J. Basic Microbiol. (1985) 25:141; Cregg et al., Mol. Cell. Biol. (1985) 5:3376; в патентах США № 4837148 и 4929555; Beach and Nurse, Nature (1981) 300:706; Davidow et al., Curr. Genet. (1985) 10:380; Gaillardin et al., Curr. Genet. (1985) 10:49; Ballance et al., Biochem. Biophys. Res. Commun. (1983) 112:284-289; Tilburn et al., Gene (1983) 26:205-221; Yelton et al., Proc. Natl. Acad. Sci. (USA) (1984) 81:1470-1474; Kelly and Hynes, EMBO J. (1985) 4:475479; EP 0244234; и WO 91/00357.
Клетки насекомых. Экспрессию гетерологичных генов в насекомых проводят, как описано в патенте США № 4745051; Friesen et al., "The Regulation of Baculovirus Gene Expression", in:The Molecular Biology Of Baculoviruses (1986) (W. Doerfler, ed. ); EP 0127839; EP 0155476; and Vlak et al., J. Gen. Virol. (1988) 69:765-776; Miller et al., Ann. Rev. Microbiol. (1988) 42:177; Carbonell et al., Gene (1988) 73:409; Maeda et al., Nature (1985) 315:592-594; Lebacq-Verheyden et al., Mol. Cell. Biol. (1988) 8:3129; Smith et al., Proc. Natl. Acad. Sci. (USA) (1985) 82:8844; Miyajima et al., Gene (1987) 58:273; и Martin et al., DNA (1988) 7:99. Многие бакуловирусные штаммы и варианты и соответствующие чувствительные клетки хозяина из насекомых описаны в Luckow et al., Bio/Technology (1988) 6:47-55, Miller et al., Generic Engineering (1986) 8:277-279, и Maeda et al., Nature (1985) 315:592-594.
Клетки млекопитающих. Экспрессию в млекопитающих проводят, как описано Dijkema et al., EMBO J. (1985) 4:761, Gorman et al., Proc. Natl. Acad. Sci. (USA) (1982) 79:6777, Boshart et al., Cell (1985) 41:521 и в патенте США № 4399216. Другие свойства экспрессии в млекопитающих используют, как описано в Ham and Wallace, Meth. Enz. (1979) 58:44, Barnes and Sato, Anal. Biochem. (1980) 102:255, в патентах США № 4767704, 4657866, 4927762, 4560655, WO 90/103430, WO 87/00195, и U. S. RE 30985.
При использовании любых из указанных выше клеток хозяина или других подходящих клеток или организмов хозяина для репликации и/или экспрессии полинуклеотидов или нуклеиновых кислот по изобретению полученная в результате реплицированная нуклеиновая кислота, РНК, экспрессированный белок или полипептид находится в объеме изобретения как продукт клетки или организма хозяина. Данный продукт получают любым подходящим способом, известным в данной области.
Если идентифицирован ген, соответствующий выбранному полинуклеотиду, его экспрессия может регулироваться в клетке, по отношению которой ген является нативным. Например, эндогенный для клетки ген может регулироваться экзогенной регуляторной последовательностью, встроенной в геном клетки в позиции, достаточной, по крайней мере, для усиления экспрессии гена в данной клетке. Регуляторная последовательность может быть сконструирована для интеграции в геном путем гомологичной рекомбинации, как описано в патентах США № 5641670 и 5733761, описания которых включены сюда в качестве ссылки, или она может быть сконструирована для интеграции в геном путем негомологичной рекомбинации, как описано в WO 99/15650, описание которых включены сюда в качестве ссылки. По существу настоящее изобретение также относится к продукции указанного белка без манипуляций с самой кодирующей нуклеиновой кислотой, но вместо этого с интеграцией регуляторной последовательности в геном клетки, которая уже включает ген, кодирующий требуемый белок, как описано во включенных выше патентных документах.
Также раскрыты гомологи указанных нуклеиновых кислот. Гомологи идентифицируются любым числом способов. Фрагмент предоставленной кДНК может использоваться в качестве зонда для гибридизации с библиотекой кДНК целевого интересующего организма, где используют условия низкой жесткости. Данный зонд может представлять собой большой фрагмент, или один или несколько коротких вырожденных праймеров. Нуклеиновые кислоты, обладающие сходством по последовательности, детектируют путем гибридизации при условиях низкой жесткости, например, при 50°C и 6·SSC (0,9 M хлорид натрия /0,09 M цитрат натрия) и остаются связанными, когда подвергаются отмывке при 55°C в 1·SSC (0,15 M хлорид натрия /0,015 M цитрат натрия). Идентичность по последовательности может определяться путем гибридизации в жестких условиях, например, при 50°C или выше и 0,1·SSC (15 мМ хлорид натрия /1,5 мМ цитрат натрия). Нуклеиновые кислоты, характеризующиеся областью с существенной идентичностью в отношении предоставленных последовательностей, например, аллельные варианты, генетически измененные версии гена, и т.д., связываются с предоставленными последовательностями в жестких условиях гибридизации. Путем использования зондов, особенно меченых зондов последовательностей ДНК, можно выделять гомологичные или родственные гены.
Также в круг интересов входят промоторные элементы указанных геномных последовательностей, где последовательность 5'-фланкирующей области может использоваться для промоторных элементов, включая участки связывания энхансера, которые, например, обеспечивают регуляцию экспрессии в клетках/тканях, где экспрессируется ген указанных белков.
Также раскрыты малые фрагменты ДНК указанных нуклеиновых кислот, причем данные фрагменты могут использоваться в качестве праймеров для ПЦР, скрининговых зондов для гибридизации, и т.д. Более крупные фрагменты ДНК, т.е. размером более 100 нуклеотидов, могут использоваться для продукции кодируемого белка, как описано в предыдущем разделе. Для применения в реакциях геометрической амплификации, таких как геометрическая ПЦР, используют пару праймеров. Точная композиция последовательностей праймеров не является критичной для данного изобретения, но в большинстве применений праймеры гибридизуются с указанной последовательностью в жестких условиях, как это известно в данной области. Предпочтительным является выбор пары праймеров, которые будут генерировать продукт амплификации длиной по крайней мере 50 нуклеотидов, предпочтительно, по крайней мере, около 100 нуклеотидов. Алгоритмы для выбора последовательностей праймеров в основном известны и доступны в виде пакетов коммерческого программного обеспечения. Праймеры для амплификации гибридизуются с комплементарными цепями ДНК и осуществляют затравку реакции в направлении один к другому.
Данная ДНК также может использоваться для идентификации экспрессии гена в биологическом образце. Способ, которым клетки тестируют на наличие конкретных нуклеотидных последовательностей, таких как геномная ДНК или РНК, хорошо описан в литературе. В кратком изложении ДНК или мРНК выделяют из образца клеток. мРНК можно амплифицировать путем ОТ-ПЦР с использованием обратной транскриптазы, с образованием комплементарной цепи ДНК с последующей амплификацией путем полимеразной цепной реакции с использованием праймеров, специфичных для указанных последовательностей ДНК. Альтернативно образец мРНК разделяют путем гель-электрофореза, переносят на подходящую подложку, например нитроцеллюлозу, нейлон, и т.д., и затем тестируют фрагментом указанной ДНК в качестве зонда. Другие способы, такие как анализ лигирования олигонуклеотидов, гибридизация in situ и гибридизация с ДНК-зондами, размещенными на твердом чипе, также могут найти применение. Детекция гибридизации мРНК с указанной последовательностью указывает на экспрессию гена белка коралловых полипов в данном образце.
Указанные нуклеиновые кислоты, включающие фланкирующие промоторные области и кодирующие области, могут подвергаться мутации различными способами, известными в данной области, с целью получения направленных изменений силы промотора, последовательности кодируемого белка, свойств кодируемого белка, включая флуоресцентные характеристики кодируемого белка и т.д. Последовательность ДНК или белковый продукт такой мутации обычно по существу сходен с предоставленными здесь последовательностями, например, отличается по крайней мере одним нуклеотидом или аминокислотой соответственно и может отличаться, по крайней мере, двумя, но не более чем десятью нуклеотидами или аминокислотами. Изменения последовательности могут представлять собой замены, вставки, делеции, или их комбинацию. Делеции могут далее включать большие изменения, такие как делеции домена или экзона, например, делеции участков длиной 10, 20, 50, 75, 100, 150 или большего числа аминокислотных остатков. Известны способы мутагенеза клонированных генов in vitro. Примеры протоколов сайт-специфического мутагенеза можно найти в Gustin et al. (1993), Biotechniques 14:22; Barany (1985), Gene 37:111-23; Colicelli et al. (1985), Mol. Gen. Genet. 199:537-9; и Prentki et al (1984), Gene 29:303-13. Способы сайт-специфического мутагенеза можно найти в Sambrook et al., Molecular Cloning: A Laboratory Manual, CSH Press 1989, pp. 15.3-15. 108; Weiner et al. (1993), Gene 126:35-41; Sayers et al (1992), Biotechniques 13:592-6; Jones and Winistorfer (1992), Biotechniques 12:528-30; Barton et al. (1990), Nucleic Acids Res 18:7349-55; Marotti and Tomich (1989), Gene Anal. Tech. 6:67-70; и Zhu (1989), Anal Biochem 177:120-4. Такие мутированные производные нуклеиновой кислоты могут использоваться для исследования структурно-функциональных взаимоотношений конкретного хромофорного/флуоресцентного белка или для изменения свойств белка, которые воздействуют на его функцию или регуляцию.
Особенный интерес для многих осуществлений представляет следующий протокол специфического мутагенеза, причем данный протокол находит применение для мутирования хромопротеинов (например, окрашенные белки, которые, если и флуоресцируют, то слабо) с получением флуоресцентных мутантов. По данному протоколу последовательность белка-кандидата выравнивают с аминокислотной последовательностью GFP Aequorea victoria дикого типа по протоколу, приведенному в Matz et al.,"Fluorescent proteins from non-bioluminescent Anthozoa species," Nature Biotechnology (October 1999) 17:969-973. Идентифицируют остаток 148 выровненного хромопротеина и затем заменяют его на Ser, например, путем сайт-специфического мутагенеза, что приводит к продукции флуоресцентного мутанта хромопротеина дикого типа. См., например, описанный ниже NFP-7, белок дикого типа которого представляет собой хромопротеин, который мутируют в флуоресцентный белок путем замены на Ser нативного остатка Ala в позиции 148.
Также в круг интересов входят гуманизированные версии указанных нуклеиновых кислот. Используемый здесь термин "гуманизированный" относится к изменениям, внесенным в последовательность нуклеиновой кислоты для оптимизации кодонов для экспрессии белка в человеческих клетках (Yang et al., Nucleic Acids Research 24 (1996), 4592-4593). См. также патент США № 5795737, в котором описана гуманизация белков, раскрытие которого внесено сюда в качестве ссылки.
БЕЛКОВЫЕ/ПОЛИПЕПТИДНЫЕ КОМПОЗИЦИИ
Также настоящее изобретение относится к хромофорным и/или флуоресцентным белкам и их мутантам, а также к относящимся к ним полипептидным композициям.
Поскольку указанные белки представляют собой хромопротеины, они являются окрашенными белкам, которые могут быть флуоресцентными, слабо флуоресцентными или нефлуоресцентными. Используемые здесь термины хромопротеин и флуоресцентный белок не охватывают люциферазы, такие как люцифераза Renilla, и относятся к любому белку, который пигментирован или окрашен, и/или флуоресцирует при облучении светом, например, белым светом или светом со специфической длиной волны (или узкой полосой длин волн, такой как длина волны возбуждения). Используемый здесь термин "полипептидная композиция" относится к обоим полноразмерным белкам, а также к их частям или фрагментам. Также к данному термину относятся вариации встречающегося в природе белка, где такие вариации являются гомологичными или по существу сходными с встречающимся в природе белком, и мутанты встречающихся в природе белков, что описано ниже более подробно. Указанные полипептиды присутствуют в другом окружении, нежели их природное окружение.
Во многих осуществлениях указанные белки характеризуются максимумом поглощения, варьирующим примерно от 300 до 700, обычно примерно от 350 до 650 и чаще примерно от 400 до 600 нм. Когда указанные белки являются флуоресцентными белками, под которыми подразумевается, что они могут быть возбуждены при одной длине волны, после чего они будут испускать свет на другой длине волны, спектр возбуждения указанных белков обычно варьирует примерно от 300 до 700, обычно примерно от 350 до 650 и чаще примерно от 400 до 600 нм, в то время как спектр эмиссии указанных белков обычно варьирует примерно от 400 до 800, обычно примерно от 425 до 775 и чаще примерно от 450 до 750 нм. Указанные белки в основном характеризуются максимальным коэффициентом экстинкции, который варьирует примерно от 10000 до 50000; а обычно примерно от 15000 до 45000. Указанные белки обычно варьируют по длине примерно от 150 до 300 и обычно примерно от 200 до 300 аминокислотных остатков; и в основном имеют молекулярную массу, варьирующую примерно от 15 до 35 кДа, обычно примерно от 17,5 до 32,5 кДа.
В некоторых осуществлениях указанные белки являются яркими, где под ярким подразумевают, что данные хромопротеины и их флуоресцентные мутанты могут детектироваться обычными способами (например, визуальным скринингом, спектрофотометрией, спектрофлуорометрией, флуоресцентной микроскопией, при помощи приборов FACS, и т.д.). Яркость флуоресценции конкретного флуоресцентного белка определяется его квантовым выходом, умноженным на максимальный коэффициент экстинкции. Яркость хромопротеина может выражаться его максимальным коэффициентом экстинкции.
В некоторых осуществлениях указанные белки подвергаются быстрому фолдингу во время экспрессии в клетках хозяина. Под быстрым фолдингом подразумевают, что белки за короткий период достигают своей третичной структуры, которая обеспечивает их хромофорное или флуоресцентное свойство. В данных осуществлениях белки сворачиваются за период, который в основном не превышает примерно 3 суток, обычно не превышает примерно 2 суток и чаще не превышает примерно 1 сутки.
Конкретные интересующие белки включают в себя следующие конкретные белки: (1) зеленый флуоресцентный белок из Heteractis crispa (hcriGFP); (2) зеленый флуоресцентный белок из Dendronephthya sp. (dendGFP); (3) красный флуоресцентный белок от Zoanthus sp. (zoanRFP); (4) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP1); (5) зеленый флуоресцентный белок из Scolymia cubensis (scubGFP2); (6) красный флуоресцентный белок из Ricordea florida (rfloRFP); (7) зеленый флуоресцентный белок из Ricordea florida (rfloGFP); (8) красный флуоресцентный белок из Montastraea cavernosa (mcavRFP); (9) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP); (10) зеленый флуоресцентный белок из Condylactis gigantea (cgigGFP); (11) зеленый флуоресцентный белок из Agaricia fragilis (afraGFP); (12) зеленый флуоресцентный белок из Ricordea florida (rfloGFP2); (13) зеленый флуоресцентный белок из Montastraea cavernosa (mcavGFP2); и (14) гомолог зеленого флуоресцентного белка из Montastraea annularis (mannFP).
Также раскрыты гомологи или белки (или их фрагменты), которые отличаются по последовательности от предоставленных выше конкретных аминокислотных последовательностей по настоящему изобретению, т.е. SEQ ID NO: 02; 04; 06; 08; 10;. 12; 14; 16; 18; 20; 22; 24; 26 или 28. Под гомологом подразумевается белок, характеризующийся идентичностью аминокислотной последовательности, равной, по крайней мере, примерно 10%, обычно, по крайней мере, примерно 20% и чаще, по крайней мере, примерно 30%, и во многих осуществлениях, по крайней мере, примерно 35%, обычно, по крайней мере, примерно 40%, и чаще, по крайней мере, примерно 60%, в отношении белка по настоящему изобретению, что определяется с использованием кластерного алгоритма MegAlign, DNAstar (1998), как описано в D. G. Higgins and P. M. Sharp, "Fast and Sensitive multiple Sequence Alignments on a Microcomputer," (1989) CABIOS, 5:151-153. (Использованные параметры представляют собой ktuple 1, штраф за вставку 3, окно 5 и сохраненных диагоналей 5). Во многих осуществлениях интересующие гомологи характеризуются гораздо более высокой идентичностью последовательности, например 65%, 70%, 75%, 80%, 85%, 90% или выше.
Также предоставлены белки, которые по существу идентичны белку дикого типа, где под по существу идентичным подразумевается, что белок характеризуется идентичностью аминокислотной последовательности в отношении последовательности белка дикого типа, равной, по крайней мере, примерно 60%, обычно, по крайней мере, примерно 65% и чаще, по крайней мере, примерно 70%, где в некоторых случаях идентичность может быть гораздо выше, например 75%, 80%, 85%, 90%, 95% или выше.
Во многих осуществлениях указанные гомологи имеют структурные характеристики, обнаруженные в предоставленных выше конкретных последовательностях, где такие структурные характеристики включают в себя структуру фолдинга β-бочонка.
Также раскрыты белки, которые являются мутантами описанных выше встречающихся в природе белков. Мутанты могут сохранять биологические свойства белков дикого типа (например, встречающихся в природе), или могут обладать биологическими свойствами, которые отличаются от белков дикого типа. Термин "биологические характеристики" указанных белков включает в качестве неограничивающих примеров спектральные свойства, такие как максимум поглощения, максимум эмиссии, максимальный коэффициент экстинкции, яркость (например, по сравнению с белком дикого типа или другим белком сравнения, таким как зеленым флуоресцентным белком от A. victoria), и тому подобное; стабильность in vivo и/или in vitro (например, период полужизни); и т.д. Мутанты включают единичные аминокислотные замены, делеции одной или нескольких аминокислот, N-концевых усечений, C-концевых усечений, вставок, и т.д.
Мутанты можно генерировать с использованием стандартных способов молекулярной биологии, например случайного мутагенеза и направленного мутагенеза. Здесь описаны некоторые мутанты. С помощью руководства, предоставленного в примерах и с использованием стандартных способов, специалисты в данной области могут легко получить большое разнообразие дополнительных мутантов и протестировать, изменились ли у них биологические характеристики. Например, интенсивность флуоресценции может быть измерена с использованием спектрофотометра с различными длинами волн возбуждающего света.
Те белки по настоящему изобретению, которые являются встречающимися в природе, присутствуют в окружении, не присущим им в природе, например, выделены из присущего им в природе окружения. В некоторых осуществлениях указанные белки присутствуют в композиции, которая обогащена указанным белком по сравнению с его природным окружением. Например, предоставляется очищенный белок, где под очищенным подразумевается, что белок присутствует в композиции, которая по существу не содержит белков, не являющихся интересующими хромофорными/флуоресцентными белками, где "по существу не содержит" означает, что менее чем 90%, обычно менее чем 60% и чаще менее 50% композиции состоит из белков, не являющихся интересующими хромофорными белками. Белки по настоящему изобретению может также присутствовать в выделенном виде, под чем подразумевается, что белок по существу свободен от других белков и других встречающихся в природе биологических молекул, таких как олигосахариды, полинуклеотиды и их фрагменты, и тому подобного, где термин "по существу свободный" в данном случае означает, что менее 70%, обычно менее 60% и чаще менее 50% от композиции, содержащей выделенный белок, составляют какую-либо другую встречающуюся в природе биологическую молекулу. В некоторых осуществлениях белки присутствуют по существу в чистом виде, где под "по существу чистым видом" подразумевается, по крайней мере, 95%, обычно, по крайней мере, 97% и чаще, по крайней мере, 99% чистоты.
В дополнение к встречающимся в природе белкам, также предоставлены полипептиды, которые отличаются от встречающихся в природе белков, например, описанных выше мутантных белков. В основном такие полипептиды включают аминокислотную последовательность, кодируемую открытой рамкой считывания (ORF) гена, кодируемого указанным белком дикого типа, включая полноразмерный белок и его фрагменты, особенно биологически активные фрагменты и/или фрагменты, соответствующие функциональным доменам, и тому подобное; и включая продукты слияния указанных полипептидов с другими белками или их частями. Интересующие фрагменты обычно составляют, по крайней мере, примерно 10 а.к. длиной, обычно, по крайней мере, примерно 50 а.к., и может быть длиной 300 а.к. или длиннее, но обычно не превышает примерно 1000 а.к. в длину, где фрагмент имеет участок аминокислот, идентичный указанному белку, по крайней мере, примерно на 10 а.к. и обычно, по крайней мере, примерно на 15 а.к. и во многих осуществлениях по крайней мере, примерно на 50 а.к. В некоторых осуществлениях указанные полипептиды составляют примерно 25 а.к., примерно 50 а.к., примерно 75 а.к., примерно 100 а.к., примерно 125 а.к., примерно 150 а.к., примерно 200 а.к., примерно 210 а.к., примерно 220 а.к., примерно 230 а.к. или примерно 240 а.к. в длину вплоть до целого белка. В некоторых осуществлениях фрагмент белка сохраняет все или по существу все биологические характеристики белка дикого типа.
Указанные белки и полипептиды могут быть получены из встречающихся в природе источников или продуцированы синтетически. Например, белки дикого типа могут происходить из биологических источников, которые экспрессируют белок, например не способных к биолюминесценции кишечнополостных, например видов коралловых полипов, таких как конкретные виды, перечисленные выше. Указанные белки также могут быть получены синтетическими средствами, например, путем экспрессии рекомбинантного гена или нуклеиновой кислоты, содержащей последовательность, кодирующую интересующий белок, в подходящем хозяине, как описано выше. Могут использоваться любые процедуры очистки белка, где подходящие методологии очистки белка описаны в Guide to Protein Purification, (Deuthser ed.) (Academic Press, 1990). Например, лизат может быть получен из природного источника и очищен с использованием ВЭЖХ, гель-фильтрации, гель-электрофореза, аффинной хроматографии и тому подобного.
КОМПОЗИЦИИ АНТИТЕЛ
Также раскрыты антитела, которые специфично связываются с указанными флуоресцентными белками. Подходящие антитела получают иммунизацией животного-хозяина пептидами, включающими в себя весь указанный белок или его часть. Подходящие животные-хозяева включают в себя мышь, крысу, овцу, козу, хомяка, кролика, и т.д. Белок-иммуноген в основном происходит из видов кишечнополостных, конкретно видов коралловых полипов или видов коралловых полипов, не относящихся к морским перьям. Животное-хозяин в основном является видом, отличным от давшего иммуноген, например представляет собой мышь, и т.д.
Иммуноген может включать в себя целый белок или его фрагменты и производные. Предпочтительные иммуногены включают в себя весь указанный белок или его часть, где данные остатки содержат посттрансляционные модификации, обнаруженные в природном целевом белке. Иммуногены получают различными способами, известными в данной области, например экспрессией клонированных генов с использованием принятых способов рекомбинации, выделением от коралловых полипов исходных видов, и т.д.
Для получения поликлональных антител первой стадией является иммунизация животного-хозяина целевым белком, где данный целевой белок предпочтительно находится по существу в чистом виде, включая менее 1% контаминантов. Иммуноген может содержать полноразмерный целевой белок, его фрагмент или производные. Для усиления иммунного ответа животного-хозяина целевой белок может комбинироваться с адъювантом, где подходящие адъюванты включают в себя алюминиевые квасцы, декстрансульфат, высокомолекулярные полимерные анионы, эмульсии масла и воды, например адъювант Фрейнда, полный адъювант Фрейнда, и тому подобное. Целевой белок может также конъюгироваться с синтетическими белками-носителями или синтетическими антигенами. Многих хозяев можно иммунизировать для получения поликлональных антител. Такие хозяева включают в себя кроликов, морских свинок, грызунов, например мышей, крыс, овец, коз, и тому подобное. Целевой белок вводят хозяину обычно внутрикожно, причем после начальной дозы следуют одна или несколько, обычно, по крайней мере, две дополнительных загрузочных дозы. После иммунизации у хозяина отбирают кровь с последующим отделением от кровяных клеток сыворотки. Ig, присутствующий от полученной в результате антисыворотки, может далее фракционироваться с использованием известных способов, таких как разделение солями аммония, хроматография на DEAE, и тому подобное.
Моноклональные антитела продуцируют общепринятыми способами. В основном источником плазматических клеток являются селезенка и/или лимфатические узлы иммунизированного животного-хозяина. Плазматические клетки иммортализуют путем слияния с миеломными клетками с получением гибридомных клеток. Культуральные надосадочные жидкости от индивидуальных гибридом подвергают скринингу с использованием стандартных способов для идентификации тех, которые продуцируют антитела с требуемой специфичности. Подходящие животные для продукции моноклональных антител к человеческому белку включают в себя мышь, крысу, хомяка и т.д. Для получения антител против мышиного белка животное в основном представляет собой хомяка, морскую свинку, кролика, и т.д.
Антитело может быть очищено из надосадочных жидкостей гибридомные клеток или асцитных жидкостей общепринятыми способами, например, путем аффинной хроматографии с использованием белка, связанного на нерастворимой подложке, сефарозы с белком A, и т.д.
Антитело может продуцироваться в виде единственной цепи вместо обычной структуры из нескольких субъединиц. Одноцепочечные антитела описаны в Jost et al. (1994) J. B. G. 269:26267-73 и в других источниках. Последовательности ДНК, кодирующие вариабельную область тяжелой цепи и вариабельную область легкой цепи, лигируют со спейсером, кодирующим, по крайней мере, примерно 4 аминокислоты, представляющих собой малые нейтральные аминокислоты, включая глицин и/или серин. Белок, кодируемый данной слитой конструкцией, обеспечивает сборку функциональной вариабельной области, которая сохраняет специфичность и аффинность первоначального антитела.
Также в область интересов некоторых осуществлений входят гуманизированные антитела. Способы гуманизации антител хорошо известны в данной области. Гуманизированное антитело может представлять собой продукт от животного, содержащего гены константной области трансгенного человеческого иммуноглобулина (см., например, заявки на выдачу Международного патента WO 90/10077 и WO 90/04036). Альтернативно интересующее антитело может конструироваться с использованием способов рекомбинантной ДНК с заменой CH1-, CH2-, CH3-, шарнирных доменов, и/или доменов каркаса на соответствующую последовательность человека (см. WO 92/02190).
Применение кДНК Ig для конструирования генов химерного иммуноглобулина известно в данной области (Liu et al. (1987) P. N. A. S. 84:3439 и (1987) J. Immunol. 139:3521). мРНК выделяют из гибридомы или другой клетки, продуцирующей антитело, и используют для получения кДНК. Интересующую кДНК можно амплифицировать путем полимеразной цепной реакции с использованием специфических праймеров (патент США № 4683195 и 4683202). Альтернативно получают библиотеку и подвергают ее скринингу для выделения интересующей последовательности. Последовательность ДНК, кодирующую вариабельную область антитела, затем объединяют с последовательностями человеческой константной области. Последовательности генов человеческих константных областей можно найти в Kabat et al. (1991) Sequences of Proteins of Immunoloqical Interest, N. I. H. publication no. 91-3242. Гены человеческих C-областей легко доступны от известных клонов. Выбор изотипа направляется требуемыми эффекторными функциями, такими как связывание комплемента или активность антителозависимой клеточной цитоксичности. Предпочтительными изотипами являются IgG1, IgG3 и IgG4. Или могут использоваться константные области человеческой легкой цепи. Затем общепринятыми способами экспрессируют химерное, гуманизированное антитело.
Фрагменты антитела, такие как Fv, F(ab')2 и Fab, могут быть получены путем расщепления интактного белка, например протеазой, или химическим расщеплением. Альтернативно конструируют укороченный ген. Например, химерный ген, кодирующий часть фрагмента F(ab')2, охватывает последовательности ДНК, кодирующие CH1-домен и шарнирную область H-цепи, за которыми следуют стоп-кодон трансляции с получением укороченной молекулы.
Консенсусные последовательности H- и L J-областей могут использоваться при конструировании олигонуклеотидов для использования в качестве праймеров для введения подходящих сайтов рестрикции в J-область для последующего связывания с сегментов V-области с сегментами человеческой C-области. кДНК C-области может модифицироваться путем сайт-специфического мутагенеза для размещения сайта рестрикции в аналогичной позиции в человеческой последовательности.
Экспрессирующие последовательности включают плазмиды, ретровирусы, YAC, происходящие из EBV эписомы, и тому подобное. Подходящим вектором является тот, который кодирует функционально полноценную человеческую иммуноглобулиновую последовательность CH или CL с подходящими сайтами рестрикции, сконструированную таким образом, что в нее может легко быть встроена и экспрессирована любая последовательность VH или VL. В таких векторах обычно происходит сплайсинг последовательности между донорным участком сплайсинга во встроенной J-области и акцепторным участком сплайсинга, предшествующим человеческой C-области, и также в областях сплайсинга, которые имеют место между экзонами человеческого CH. В нативных хромосомных участках ниже кодирующей последовательности происходят полиаденилирование и терминация транскрипции. Полученное в результате химерное антитело может быть соединено с любым сильным промотором, включая ретровирусные LTRs, например, ранний промотор SV-40 (Okayama et al. (1983) Mol. Cell. Bio. 3:280), LTR вируса саркомы Рауша (Gorman et al. (1982) P. N. A. S. 79:6777), и LTR вируса мышиного лейкоза Молони (Grosschedl et al. (1985) Cell 41:885); нативные промоторы Ig, т.д.
ТРАНСГЕННЫЕ ОРГАНИЗМЫ
Указанные нуклеиновые кислоты могут использоваться для получения трансгенных, не относящихся к человеку растений или животных или сайт-специфических модификаций в клеточных линиях. Трансгенные клетки по настоящему изобретению содержат одну или несколько нуклеиновых кислот по настоящему изобретению, присутствующих в качестве трансгена, где данное определение охватывает родительские клетки, трансформированные так, чтобы они включали трансген, и их потомство. Во многих осуществлениях трансгенные клетки представляют собой клетки, которые в норме не несут или не содержат нуклеиновую кислоту по настоящему изобретению. В тех осуществлениях, где трансгенные клетки в природе содержат указанные нуклеиновые кислоты, данные нуклеиновые кислоты присутствуют в клетке в позиции, отличной от их природного расположения, т.е. интегрированы в геномный материал клетки в неприродной локализации. Трансгенные клетки могут быть получены посредством гомологичной рекомбинации, где изменяют эндогенный локус. Альтернативно конструкцию нуклеиновой кислоты случайно интегрируют в геном. Векторы для стабильной интеграции включают плазмиды, ретровирусы и другие вирусы животных, YAC, и тому подобное.
Трансгенные организмы по настоящему изобретению включают клетки и многоклеточные организмы, например растения и животные, которые являются нокаут-организмами по эндогенному гену, в которых экспрессия последнего по крайней мере снижена, если вообще не элиминирована. Интересующие трансгенные организмы также включают клетки и многоклеточные организмы, например, растения и животные, в которых белок или его варианты экспрессируются в клетках или тканях, где он в норме не экспрессируется, и/или в концентрациях, в норме в данных клетках или тканях не присутствующих.
ДНК-конструкции для гомологичной рекомбинации включают, по крайней мере, часть гена по настоящему изобретению, где данный ген содержит требуемую(ые) генетическую(ие) модификацию(и), и охватывает области гомологии с целевым локусом. ДНК-конструкции для случайной интеграции не должны включать в себя области гомологии, способствующие рекомбинации. Обычно включают маркеры для положительной и отрицательной селекции. Способы получения клеток, имеющих направленные генные модификации, путем гомологичной рекомбинации известны в данной области. Для различных способов трансфекции клеток млекопитающих см. Keown et al. (1990), Meth. Enzymol. 185:527-537.
Для эмбриональных стволовых (ES) клеток может быть получена линия ES-клеток, или эмбриональные клетки могут быть получены свежими из организма хозяина, например из мыши, крысы, морской свинки, и т.д. Такие клетки выращивают на подходящем слое питающих фибробластов или выращивают в присутствии фактора ингибирования лейкоза (LIF). После трансформации ES- или эмбриональных клеток их можно использовать для получения трансгенных животных. После трансформации клетки помещают на питательный слой в подходящей среде. Клетки, содержащие конструкцию, могут детектироваться путем использования селективной среды. По прошествии времени, достаточного для роста колоний, их изымают и анализируют наличие гомологичной рекомбинации или интеграции конструкции. Те колонии, которые являются позитивными, затем могут использоваться для манипуляций с эмбрионом и инъекции бластоцисты. Бластоцисты получают самок в возрасте 4-6 недель с избыточной овуляцией. ES-клетки трипсинизируют и модифицированные клетки вводят инъекцией в бластоцель бластоцисты. После инъекции бластоцисты возвращают в каждую маточную трубу ложно беременных самок. Самок доводят до конца беременности и подвергают скринингу полученное в результате потомство на наличие конструкции. За счет обеспечения у бластоцисты иного фенотипа и генетических измененных клеток и можно легко обнаружить химерное потомство.
Химерных животных подвергают скринингу на наличие модифицированного гена, и самцов и самок, содержащих модификацию, скрещивают с получением гомозиготного потомства. Если генные изменения вызывают летальность на некотором этапе развития, ткани или органы могут быть оставлены в качестве аллогенных или конгенных трансплантатов или в культуре in vitro. Трансгенные животные могут представлять собой млекопитающее, не относящееся к человеку, такое как лабораторные животные, домашние животные, и т.д. Трансгенные животные могут использоваться в функциональных исследованиях, скрининге лекарств, и т.д. Репрезентативные примеры применения трансгенных животных включают те, что описаны ниже.
Трансгенные растения могут быть получены сходным образом. Способы получения трансгенных растительных клеток и растений описаны в патенте США № 5767367; 5750870; 5739409; 5689049; 5689045; 5674731; 5656466; 5633155; 5629470; 5595896; 5576198; 5538879; 5484956; описания которых включены сюда в качестве ссылки. Способы получения трансгенных растений также описаны в Plant Biochemistry and Molecular Biology (eds Lea & Leegood, John Wiley & Sons) (1993) pp 275-295. В кратком изложении, собирают подходящую растительную клетку или ткань в зависимости от природы вида растения. В некоторых случаях выделяют протопласты как таковые, где такие протопласты могут выделяться из разнообразных растительных тканей, например листа, гипокотиля, корня, и т.д. Для выделения протопласта собранные клетки инкубируют в присутствии целлюлаз для удаления клеточной стенки, где точные условия инкубации варьируют в зависимости от типа растения и/или ткани, из которой выделена клетка. Полученные в результате протопласты затем отделяют от полученного в результате клеточного дебриса путем просеивания и центрифугирования. Вместо использования протопластов для получения трансгенного хозяина могут использоваться эмбриогенные эксплантаты, содержащие соматические клетки. После сбора клеток или ткани в растительные клетки вводят интересующую экзогенную ДНК, причем для такого введения доступно много различных способов. Выделение протопластов дает возможность для введения путем протоколов ДНК-опосредованного переноса генов, включая инкубацию протопластов со свободной ДНК, например, с плазмидами, содержащими интересующие экзогенную кодирующую последовательность в присутствии поливалентных катионов, например, PEG или PLO; и электропорацию протопластов в присутствии свободной ДНК, содержащей интересующие экзогенную кодирующую последовательность. Затем отбирают протопласты, которые успешно захватили экзогенную ДНК, выращивают из них каллус и, наконец, трансгенное растение путем контакта с соответствующими количествами и соотношениями факторов стимуляции, например, ауксинов и цитокининов. В случае эмбриогенных эксплантатов подходящий способ введения экзогенной ДНК в целевые соматические клетки осуществляется путем использования ускорения частиц или протоколов "генной пушки". Полученным в результате эксплантатам затем дают возможность вырасти в химерные растения, скрещивают и получают трансгенное потомство. Вместо подходов со свободной ДНК, описанных выше, другим подходящим способом получения трансгенных растений является трансформация, опосредованная Agrobacterium. При трансформации, опосредованной Agrobacterium, получают совместно интегрирующиеся или бинарные векторы, содержащие экзогенную ДНК, и затем вводят их в подходящий штамм Agrobacterium, например, A. tumefaciens. Полученные в результате бактерии затем инкубируют с полученными протопластами или тканевыми эксплантатами, например листовыми пластинками, и продуцируют каллус. Затем каллус выращивают в условиях селекции, подвергают селекции и подвергают воздействию сред роста для индукции роста корня и стебля и окончательного получения трансгенного растения.
ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ
Указанные хромопротеины и их флуоресцентные мутанты используются в многих разнообразных применениях, где применения неизбежно меняются в зависимости от того, является данный белок хромопротеином или флуоресцентным белком. Репрезентативные применения для каждого из данных типов белком будут описаны ниже, где описанные далее применения являются сугубо репрезентативными и никоим образом не ограничивают применение указанных белков так, как описано.
Хромопротеины
Указанные хропротеины по настоящему изобретению используются в многих разнообразных применениях. Одним из интересующих применений является применение в качестве красителей, которые способны придавать окраску или пигментировать конкретную композицию вещества. Особый интерес в некоторых осуществлениях вызывают нетоксичные хромопротеины. Указанные хромопротеины могут входить в состав многих различных композиций вещества, где репрезентативные композиции вещества включают в себя пищевые композиции, фармацевтические препараты, косметические препараты, живые организмы, например, животные и растения, и тому подобное. При использовании в качестве красителя или пигмента достаточное количество хромопротеина включают в состав композиции вещества для придания ей требуемой окраски или пигментации. Хромопротеин может вводиться в состав композиции вещества с использованием любого подходящего протокола, где конкретный используемый протокол обязательно будет зависеть, по крайней мере частично, от природы композиции вещества, подлежащей окрашиванию. Протоколы, которые могут использоваться, включают в себя в качестве неограничивающих примеров смешивание, диффузию, растирание, распыление, инъекцию, татуировку и тому подобное.
Хромопротеины также могут найти применение в качестве меток при анализах по детекции вещества, например анализов на интересующее биологическое вещество. Например, хромопротеины могут вводиться в аддукты с специфичными в отношении анализируемого вещества антителами или их связывающими фрагментами и впоследствии использоваться в иммунологических анализах на предмет интересующих веществ в комплексном образце, как описано в патенте США № 4302536; описание которого включено сюда в качестве ссылки. Вместо антител или их связывающих фрагментов указанные хромопротеины или их хромогенные фрагменты могут конъюгироваться с лигандами, которые специфично связывают интересующее анализируемое вещество, или с другими группами, факторами роста, гормонами и тому подобным, что хорошо понятно специалистам в данной области.
В дополнительных осуществлениях указанные хромопротеины могут использоваться в качестве маркеров для селекции в применениях рекомбинантной ДНК, например при продукции трансгенных клеток и организмов, как описано выше. По существу можно сконструировать конкретный протокол трансгенной продукции с использованием экспрессии указанных хромопротеинов в качестве маркеров для селекции успешного или неуспешного осуществления протокола. Таким образом, появление окраски указанного хромопротеина в фенотипе трансгенного организма, полученного конкретным способом, может использоваться для индикации того, что конкретный организм успешно несет интересующий трансген, часто интегрированный так, что обеспечивается его экспрессия в организме. При использовании в качестве маркера для селекции нуклеиновая кислота, кодирующая указанный хромопротеин, может использоваться в процессе получения трансгенного организма, причем данный процесс более подробно описан выше. Конкретные интересующие трансгенные организмы, где указанные белки могут использоваться в качестве маркеров для селекции, включают в себя трансгенные растения, животных, бактерии, грибы, и тому подобное.
В дополнительных осуществлениях хромопротеины (и флуоресцентные белки) по настоящему изобретению находят применение в солнцезащитных кремах в качестве селективных фильтров, и т.д., способом, сходным с применениями белков, описанных в WO 00/46233.
Флуоресцентные белки
Указанные флуоресцентные белки по настоящему изобретению (а также другие компоненты по настоящему изобретению, описанные выше) используются в многих различных применениях, где такие применения в качестве неограничивающих примеров охватывают следующее. Первым интересующим применением является использованием указанных белков в применениях переноса резонансной энергии флуоресценции (FRET). В данных применениях указанные белки служат в качестве доноров и/или акцепторов в комбинации со вторым флуоресцентным белком или красителем, например, с флуоресцентным белком, описанным в Matz et al., Nature Biotechnology (October 1999) 17:969-973, с зеленым флуоресцентным белком из Aequoria victoria или его флуоресцентным мутантом, например, как описано в патенте США № 6066476; 6020192; 5985577; 5976796; 5968750; 5968738; 5958713; 5919445; 5874304, описания которых включены сюда в качестве ссылки, с другими флуоресцентными красителями, например кумарином и его производными, например, с 7-амино-4-метилкумарином, аминокумарином, красителями bodipy, такими как Bodipy FL, cascade blue, с флуоресцеином и его производными, например флуоресцеинтиоцианатом, Oregon green, родаминовыми красителями, например Texas red, тетраметилродамином, эозинами и эритрозинами, цианиновыми красителями, например Cy3 и Cy5, с макроциклическими хелатами ионов лантанидов, например, красителем quantum, и т.д., с хемилюминесцентными красителями, например люциферазами, включая те, что описаны в патенте США № 5843746; 5700673; 5674713; 5618722; 5418155; 5330906; 5229285; 5221623; 5182202; описания которых включены сюда в качестве ссылки. Конкретные примеры того, где могут использоваться анализы FRET, задействующие указанные флуоресцентные белки, охватывают в качестве неограничивающих примеров: детекцию белок-белковых взаимодействий, например, двухгибридную систему млекопитающих, димеризацию факторов транскрипции, мультимеризацию мембранных белков; образование комплексов многих белков, и т.д., в качестве биосенсора некоторого количества различных событий, где пептид или белок ковалентно связывают с флуоресцентной комбинацией FRET, включающей указанные флуоресцентные белки, и связывающий пептид или белок, например, представляет собой субстрат, специфический для протеазы, например, для расщепления, опосредованного каспазой; линкер, который претерпевает конформационное изменение по получении сигнала, который увеличивает или снижает FRET, например, регуляторный домен PKA (сенсор цАМФ); фосфорилирование, например, где в линкере имеет место участок фосфорилирования, или линкер характеризуется специфичностью связывания с фосфорилированным/дефосфорилированным доменом другого белка, или линкер имеет связывающий Ca2+ домен. Репрезентативные применения переноса резонансной энергии флуоресценции или применения FRET, в которых используются указанные белки, охватывают в качестве неограничивающих примеров те, что описаны в патенте США № 6008373; 5998146; 5981200; 5945526; 5945283; 5911952; 5869255; 5866336; 5863727; 5728528; 5707804; 5688648; 5439797; описания которых включены сюда в качестве ссылки.
Указанные флуоресцентные белки также находят применение в качестве биосенсоров в прокариотических и эукариотических клетках, например в качестве индикатора иона Ca2+; в качестве индикатора pH, в качестве индикатора фосфорилирования, в качестве индикатора других ионов, например магния, натрия, калия, хлорида и галогенидов. Например, для детекции иона Ca, известно, что белки, содержащие мотив EF-руки, переносятся из цитозоля на мембраны после связывания Ca2+. Данные белки содержат группу миристиловой кислоты, которая скрыта внутри молекулы гидрофобными взаимодействиями с другими областями белка. Связывание Ca2+ индуцирует конформационное изменение, приводящее к экспонированию группы миристиловой кислоты, которая затем становится доступной для встраивания в липидный бислой (что называется "переключение Ca2+-миристил"). Слияние такого содержащего EF-руку белка с флуоресцентным белком (ФБ) может делать его индикатором внутриклеточного Ca2+ за счет мониторинга перемещения из цитозоля на плазматическую мембрану путем конфокальной микроскопии. Белки EF-руки, подходящие для применения в данной системе, включают в себя в качестве неограничивающих примеров: рековерин (1-3), кальциневрин B, тропонин C, визинин, нейрокальцин, кальмодулин, парвальбумин и тому подобные. Для индикации pH может использоваться система, основанная на гисактофилинах. Гисактофилины представляют собой миристилированные богатые гистидином белки, которые, как показано, существуют в Dictyostelium. Их связывание с актином и кислыми липидами является строго pH-зависимым в пределах вариаций pH в цитоплазме. В живых клетках связывание с мембраной, как предполагается, преобладает над взаимодействием гисактофилинов с актиновыми филаментами. При pH ≤6,5 они локализуются на плазматической мембране и в ядре. При рН 7,5 они, наоборот, равномерно распределяются по цитоплазматическому пространству. Данное изменение распределения обратимо и происходит благодаря гистидиновым кластерам, экспонированным в виде петель на поверхности молекулы. Обращение внутриклеточного распределения в интервале вариации цитоплазматического pH соотносится с pK гистидиновых остатков, равным 6,5. Клеточное распределение не зависит от миристилирования белка. Путем слияния ФБ (флуоресцентных белков) с гисактофилином можно следить за внутриклеточным распределением белка слияния путем лазерного сканирования, конфокальной микроскопии или стандартной флуоресцентной микроскопии. Количественный анализ флуоресценции может выполняться путем проведения линейных сканирований сквозь клетки (лазерная сканирующая конфокальная микроскопия) или другого анализа электронных данных (например, с использованием программного обеспечения metamorph (Universal Imaging Corp) и усреднения данных, полученных в популяции клеток. Существенное рН-зависимое перераспределение гисактофилина-ФБ из цитозоля на плазматическую мембрану происходит в пределах 1-2 мин и достигает уровня стабильного состояния через 5-10 мин. Обратная реакция имеет место в сходной временной шкале. По существу белок слияния гисактофилина и флуоресцентного белка, который действует сходным образом, можно использовать для мониторинга изменений рН в цитозоле в реальном времени в живых клетках млекопитающих. Такие способы используются в высокопроизводительных приложениях, например при измерении значений pH как следствия активации рецепторов факторов роста (например, эпителиального или происходящего из тромбоцитов фактора роста), хемотактической стимуляции/клеточной локомоции, при детекции внутриклеточных изменений рН в качестве вторичного мессенджера, при мониторинге внутриклеточного рН в экспериментах по манипуляции рН, и тому подобное. Для детекции активности PKC в репортерной системе использован тот факт, что молекула, называемая MARCKS (миристилированный богатый аланином субстрат киназы C) является субстратом PKC. Он заякорен в плазматической мембране путем миристилирования к участку положительно заряженных аминокислот (ED-домен), который связывается с отрицательно заряженной плазматической мембраной путем электростатических взаимодействий. После активации PKC ED-домен становится фосфорилированным посредством PKC, становясь, таким образом, отрицательно заряженным, и вследствие электростатического отталкивания MARCKS перемещается с плазматической мембраны в цитоплазму (что называется "миристил-электростатическое переключение"). Слияние N-конца MARCKS в интервале от мотива миристилирования до ED-домена MARCKS с флуоресцентным белком по настоящему изобретению обеспечивает указанную выше систему детекции активности PKC. При фосфорилировании PKC белок слияния переходит с плазматической мембраны в цитозоль. За данным перемещением можно следить при помощи стандартной флуоресцентной микроскопии или конфокальной микроскопии, например, с использованием технологии Cellomics или других систем скрининга с высоким разрешением (High Content Screening) (например, Universal Imaging Corp./Becton Dickinson). Указанная выше репортерная система имеет применение при скрининге с высоким разрешением, например скрининге ингибиторов PKC, и в качестве индикатора активности PKC при многих сценариях скрининга на выявление потенциальных реагентов, препятствующих реализации данного пути передачи сигнала. Способы применения флуоресцентных белков в качестве биосенсоров также включает те, что описаны в патенте США № 972638; 5824485 и 5650135 (а также в цитируемых здесь ссылках), раскрытия которых включены сюда в качестве ссылки.
Указанные флуоресцентные белки также используются в применениях, относящихся к автоматическому скринингу полей клеток, экспрессирующих флуоресцентные репортерные группы путем использования анализа изображения и электронного анализа. Скрининг может использоваться для обнаружения лекарств и в области функциональной геномики: например, где указанные белки используются в качестве маркеров целых клеток для детекции изменений реорганизации и миграции многих клеток, например, образования многоклеточных трубок (образование кровеносных сосудов) эндотелиальными клетками, миграции клеток через Fluoroblok Insert System (Becton Dickinson Co. ), заживления ран, разрастания нейрита, и т.д.; где данные белки используют в качестве маркеров, объединенных с пептидами (например, направленными последовательностями) и белками, что обеспечивает детекцию изменения внутриклеточной локализации в качестве индикатора клеточной активности, примером чего является: передача сигнала, такого как перемещение после стимуляции киназ и транскрипционных факторов, таких как протеинкиназа C, протеинкиназа A, транскрипционный фактор NFkB и NFAT; для изучения белков клеточного цикла, таких как циклин A, циклин B1 и циклин E; для изучения расщепления протеазами с последующим перемещением расщепленного субстрата; для изучения фосфолипидов; в качестве маркеров внутриклеточных структур, таких как эндоплазматический ретикулум, аппарат Гольджи, митохондрии, пероксисомы, ядро, ядрышки, плазматическая мембрана, гистоны, эндосомы, лизосомы, микротрубочки, актин; в качестве инструментов для скрининга с высоким разрешением: совместная локализация других флуоресцентных белков слияния с данными маркерами локализации в качестве индикатора перемещения внутриклеточных флуоресцентных белков/пептидов слияния или в качестве единичного маркера; и тому подобное. Примеры применений, задействующих автоматический скрининг полей клеток, в которых используются указанные флуоресцентные белки, охватывают: патент США № 5989835; а также WO/0017624; WO 00/26408; WO 00/17643; и WO 00/03246; описания которых включены сюда в качестве ссылок.
Указанные флуоресцентные белки также находят применение в высокопроизводительных скрининговых анализах. Указанные флуоресцентные белки являются стабильными белками с периодами полужизни, превышающими 24 ч. Также предоставляются дестабилизированные версии указанных флуоресцентных белков с меньшими периодами полужизни, которые могут использоваться в качестве репортеров транскрипции при обнаружении лекарств. Например, белок по настоящему изобретению может объединяться с предполагаемой сигнальной последовательностью, происходящей из белка с более коротким периодом полужизни, например, с последовательностью PEST, из мышиного гена орнитиндекарбоксилазы, боксом разрушения мышиного циклина B1 и убиквитином, и т.д. Для описания дестабилизированных белков и векторов, которые могут использоваться для их продукции, см., например, патент США № 6130313; описание которых включено сюда в качестве ссылки. Для скрининга лекарственных средств с использованием дестабилизированных версий указанных флуоресцентных белков могут детектироваться промоторы путей передачи сигнала, например, AP1, NFAT, NFkB, Smad, STAT, p53, E2F, Rb, myc, CRE, ER, GR и TRE, и тому подобное.
Указанные белки могут использоваться в качестве детекторов вторичных мессенджеров, например, путем слияния указанных белков с конкретными доменами: например, с Ca-связывающим доменом PKC-гамма, DAG-связывающим доменом PKC-гамма, SH2-доменом и SH3-доменом, и т.д.
Могут быть получены секретируемые формы указанных белков, например, путем слияния секретируемых лидерных последовательностей с указанными белками для конструирования секретируемых форм указанных белков, которые, в свою очередь, могут использоваться для множества различных применений.
Указанные белки также используются в применениях активируемой флуоресценции клеточной сортировки. В таких применениях указанный флуоресцентный белок используют в качестве метки для маркировки популяции клеток и полученную в результате популяцию меченых клеток сортируют на устройстве активируемой флуоресценции клеточной сортировки, как известно в данной области. Способы FACS описаны в патенте США № 5968738 и 5804387; раскрытия которых включены сюда в качестве ссылки.
Указанные белки также находят применение в качестве маркеров животных in vivo (например, трансгенных животных). Например, экспрессия указанного белка может управляться тканеспецифическими промоторами, где такие способы находят применения в исследованиях по генной терапии, например, по тестированию эффективности трансгенной экспрессии среди прочих применений. Репрезентативное применение флуоресцентных белков в трансгенных животных, которое иллюстрирует данный класс применений, находится в WO 00/02997, описание которого включено сюда в качестве ссылки.
Дополнительные применения указанных белков охватывают использование в качестве маркеров после инъекции в клетки или животным, и при калибровке количественных измерений (флуоресценции и белка); в качестве маркеров или репортеров в кислородных биосенсорных устройствах для мониторинга жизнеспособности клеток; в качестве маркеров или меток для животных, домашних животных, игрушек, пищевых продуктов и тому подобного.
Указанные флуоресцентные белки также находят применение в анализах протеолитического расщепления. Например, анализы инактивируемой расщеплением флуоресценции могут разрабатываться с использованием указанных белков, где указанные белки конструируют так, чтобы они включали последовательность расщепления конкретной протеазы без нарушения флуоресцентного характера белка. После расщепления флуоресцентного белка активированной протеазой флуоресценция резко снижается вследствие разрушения функционального хромофора. Альтернативно с использованием указанных белков может разрабатываться активируемая расщеплением флуоресценция, где указанные белки конструируют так, чтобы они содержали дополнительную спейсерную последовательность в близком соседстве или внутри хромофора. Данный вариант характеризуется значительно сниженной флуоресцентной активностью, поскольку части функционального хромофора разделяются спейсером. Спейсер обрамляется двумя идентичными участками расщепления конкретной протеазой. После расщепления активированной протеазой спейсер вырезается, и две оставшиеся "субъединицы" флуоресцентного белка смогут снова объединиться с получением функционального флуоресцентного белка. Оба описанных типа применений могут быть разработаны для анализов на различные типы протеаз, например каспаз, и т.д.
Указанные белки также могут использоваться в анализах определения фосфолипидной композиции в биологических мембранах. Например, с указанными белками могут быть выполнены белки слияния указанных белков (или любой другой вид ковалентной или нековалентной модификации указанных белков), которые обеспечивают связывание с конкретными фосфолипидами для локализации/визуализации профилей распределения фосфолипидов в биологических мембранах, что также обеспечивает анализ совместной локализации мембранных белков в конкретных фосфолипидных участках. Например, PH-домен GRP1 обладает высоким сродством к фосфатидилинозитолтрифосфату (PIP3), но не к PIP2. По существу, белок слияния PH-домена GRP1 и указанных белков может конструироваться для специфичного мечения богатых PIP3 областей в биологических мембранах.
Еще одно применение указанных белков представляет собой флуоресцентный таймер, в котором переключение одного цвета флуоресценции на другой (например, зеленого на красный), сопутствующее старению флуоресцентного белка, используется для определения активации/деактивации генной экспрессии, например, генной экспрессии при развитии, зависимой от клеточного цикла генной экспрессии, специфичной для циркадных ритмов генной экспрессии, и тому подобного.
Описанные выше антитела по настоящему изобретению также используются в некоторых применениях, включая дифференцировку указанных белков из других флуоресцентных белков.
НАБОРЫ
Также настоящее изобретение относится к наборам для использования при воплощении одного или нескольких из описанных выше применений, где указанные наборы обычно содержат элементы для получения указанных белков, например, конструкцию, содержащую вектор, который охватывает кодирующую указанный белок область. Компоненты указанного набора обычно присутствуют в подходящей среде для хранения, например, в буферном растворе, обычно в подходящем контейнере. Также в настоящих наборах могут присутствовать антитела к предоставленному белку. В некоторых осуществлениях набор содержит множество различных векторов, каждый из которых кодирует указанный белок, где векторы сконструированы для экспрессии в различных окружениях и/или при различных условиях, например, для конститутивной экспрессии, где вектор охватывает сильный промотор для экспрессии клеток млекопитающих, при наличии лишенного промотора вектора с множеством клонирующих участков для индивидуального встраивания промотора и заданной экспрессией, и т.д.
В дополнение к описанным выше компонентам указанные наборы далее включают инструкции для воплощения указанных способов. Данные инструкции могут присутствовать в указанных наборах в разнообразных формах, одна или несколько из которых может находиться в наборе. Одной из форм, в которой могут присутствовать данные инструкции, является печатная информация на подходящей среде или субстрате, например, на листе или листах бумаги, на которых напечатана данная информация, на упаковке набора, на вкладыше в упаковку, и т.д. Другим средством может являться средство, считываемое с компьютера, например, дискета, CD, и т.д., на которое записана данная информация. Еще одним средством, которое может иметь место, является адрес веб-сайта, который может использоваться через Интернет для получения информации на удаленном сайте. В наборах могут присутствовать любые подходящие средства.
Следующие примеры предлагаются вниманию с целью иллюстрации, а не с целью ограничения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
I. Введение
В следующем экспериментальном разделе авторы изобретения представляют одиннадцать новых GFP-подобных белков.
II. Материалы и методы
A. Сбор образцов
Образцы (100-500 мг ткани) Montastraea cavernosa, Condylactis gigantea, Scolumia cubensis и Ricordea florida собирали в морском заповеднике Florida Keys (Long Key) по санкции National Marine Sanctuary FKNMS-2000-009. Образцы собирали во время ночных погружений, образцы-кандидаты собирали, основываясь на их видимости в свете ультрафиолетовой лампы. Другие образцы (Dendronephthya sp., Heteractis crispa, Discosoma sp. 3, Zoanthus sp. 2) забирали из частных аквариумов с морской водой.
B. Клонирование и экспрессия GFP-подобных белков
Общую РНК выделяли из образцов ткани, следуя протоколу, описанному Chomczynski, P. & Sacchi, N. (1987) Anal Biochem 162, 156-9. Общую кДНК амплифицировали с использовали набора для амплификации кДНК SMARTT™ (Clontech). Данные амплифицированные образцы кДНК использовали для амплификации 3'-фрагментов кДНК, кодирующих GFP-подобные белки и дальнейшего получения потерянных 5'-флангов, точно как описано в Matz, M. V., Fradkov, A. F., Labas, Y. A., Savitsky, A. P., Zaraisky, A. G., Markelov, M. L. & Lukyanov, S. A. (1999) Nat Biotechnol 17, 969-73. После определения полной последовательности кДНК кодирующие области амплифицировали с использованием тех же образцов ДНК, что были использованы для клонирования 3'- и 5'-флангов в качестве матриц. Лежащий выше ("N-концевой") праймер содержал 5'-концевую "пятку" (5'- tTGAtTGAtTGAAGGAGAaatatc), несущую стоп-кодоны (выделены жирным) во всех рамках и участок связывания бактериальной рибосомы (подчеркнуто), за которой следовала целевая последовательность кДНК (20-22 оснований), начиная с инициирующего кодона ORF. Лежащий ниже ("C-концевой") праймер составлял 22-25 оснований длиной и соответствовал антисмысловой последовательности кДНК вокруг стоп-кодона ORF. Полученные в результате фрагменты клонировали с использованием набора с вектором pGEM-T (Promega) по протоколу производителя с использованием штамма Escherichia coli JM109 в качестве хозяина. Колонии выращивали на чашках с LB/агаром/карбенициллином, дополненными 0,3 мМ IPTG, в течение 16-20 часов при 37°C, и затем инкубировали в течение двух суток при 4°C. Флуоресцентные колонии выбирали с использованием флуоресцентного микроскопа, и высевали широкими полосами на новые чашки. Те же колонии использовали для инокуляции культуры в течение ночи с последующим выделением и секвенированием плазмиды, для подтверждения идентичности клона. Бактерии собирали с чашек, суспендировали в 1 мл PBS и разрушали обработкой ультразвуком. Лизат осветляли центрифугированием и их флуоресцентные характеристики определяли с использованием спектрофлуориметра LS-50B (Perkin Elmer Instruments). Для mcavRFP и rfloGFP "ранние" образцы собирали через 24 часа при 37°C, "поздние" образцы - через 24 часа при 37°C, после которых следовали четверо суток при 4°C.
C. Филогенетический анализ
Выравнивание GFP-подобных белков (см. добавочные данные) конструировали по Matz, M. V., Fradkov, A. F., Labas, Y. A., Savitsky, A. P., Zaraisky, A. G., Markelov, M. L. & Lukyanov, S. A. (1999) Nat Biotechnol 17, 969-73, учитывая соображения структуры белка. Когда после выравнивания белка проводили выравнивание ДНК, исключали слабо выравниваемые N- и C-концевые области. Филогенетическое древо конструировали с использованием программного обеспечения Tree-Puzzle (Strimmer, K. & von Haeseler, A. (1996) Mol. Biol. Evol. 13,964-969) по модели HKY эволюции ДНК (Hasegawa, M., Kishino, H. & Yano, K. (1985) J. Mol. Evol. 22, 160-174), принимая во внимание то, что вариабельность участков подчиняется гамма-распределению с альфа-параметром, оцененным по набору данных. Подтверждали, что древо является древом максимальной вероятности с помощью программного обеспечения PAML (Yang, Z. (2000) (University College (http://abacus.gene.ucl.ac.uk /software/paml.html), London;. England)) по модели REV (Yang, Z. H., Goldman, N. & Friday, A. (1994) Molecular Biology and Evolution 11, 316-324). Древо, построенное с помощью Tree-Puzzle по выравниванию белков (JTT model, (Jones, D. T., Taylor, W. R. & Thornton, J. M. (1992) CABIOS 8,275-282) обладает той же топологией, но более низкими значениями поддержки вследствие меньшего числа информативных участков в выравнивании белков.
III. Результаты и обсуждение
A. Номенклатура
Для ясности представления филогенетического анализа в данной работе авторы изобретения использовали новую номенклатуру GFP-подобных белков. Идентификационные обозначения, данные авторами изобретения, включают в себя четырехбуквенную начальную часть, составленную из первой буквы родового названия и трех начальных букв видового названия с последующим определением цветового типа: GFP - зеленый, RFP - красный, YFP - желтый, CP - хромопротеин (не флуоресцентный). Когда вид не определен, начальная часть представляет собой четыре начальные буквы родового названия. В случае множественных неидентифицированных видов в одном роде, к начальной части добавляется число (как в dis3GFP или zoan2RFP); в случае нескольких белков одного цветового типа, обнаруженных у одного вида, число добавляется к определению цвета (как в scubGFP1 и scubGFP2). Для GFP Aequorea victoria и drFP583 из Discosoma sp. сохранены широко распространенные обычные названия: GFP и DsRed.
B. Новые GFP-подобные белки
Клонировали всего четырнадцать новых GFP-подобных белков и получали их спектральные характеристики. Спектральные свойства 11 из данных белков суммированы в таблице 1, находящейся в фигурах, а также на других фигурах данной заявки.
Данная группа из 11 белков охватывает представителей, проявляющих свойства, которые ранее не наблюдались в GFP-подобных белках коралловых полипов. Два зеленых белка из Condylactis gigantea (cgigGFP) и Heteractis crispa (hcriGFP) обладают спектрами возбуждения с двумя пиками, очень сходными с таковым для GFP дикого типа, и это указывает на то, что их хромофоры претерпевают фотоконверсию между нейтральным и ионизированным состояниями (Brejc, K., Sixma, T. K., Kitts, P. A., Kain, S. R., Tsien, R. Y., Ormo, M. & Remington, S. J. (1997) Proc Natl Acad Sci U S A 94, 2306-11; Palm,; G. J., Zdanov, A., Gaitanaris, G. A., Stauber, R., Pavlakis, G. N. & Wlodawer, A (1997). Nat Struct Biol 4, 361-5). Белок zoan2RFP с красной эмиссией, хотя и очень схожий с DsRed по форме кривых возбуждения эмиссии, ведет себя как "таймер": он вначале становится зеленым, а потом созревает в красный (фиг. 1, A и B), подобно одному из мутантных вариантов DsRed (Terskikh, A., Fradkov, A., Ermakova, G., Zaraisky, A., Tan, P., Kajava, A. V., Zhao, X., Lukyanov, S., Matz, M., Kim, S., Weissman, I. & Siebert, P. (2000) Science 290,1585-8.). Два новых белка с красной эмиссией из большого звездчатого коралла Montastraea cavernosa (mcavRFP) и флоридского кораллиморфа Ricordea florida (rfloRFP) также проявляют фенотип "таймера" (фиг. 1, C-F). В отличие от zoan2RFP они не могут полностью дозревать в красные в экспериментах настоящих заявителей по экспрессии в бактериях, результатом чего является спектры эмиссии с двумя пиками, показанные на фигуре 1 (D и F). Замечательно, что для обоих данных белков полоса красной эмиссии в более зрелой форме имела основной пик возбуждения, по сути идентичный таковому незрелой зеленой формы, при том что желто-оранжевый пик возбуждения был значительно меньше (фиг. 2). Это сильно отличает данные белки от остальных оранжево-красных белков, в которых красная эмиссия наилучшим образом возбуждается в желто-оранжевой области (фигура 4, таблица 1, спектр E). Эта необычная форма спектров возбуждения может быть следствием фотоконверсии состояний ионизации хромофора (по аналогии с зелеными белками), или даже более глубоких различий в структуре хромофора. В пользу последнего говорит тот факт, что форма пиков красной эмиссии mcavRFP и rfloRFP заметно отличается от других оранжево-красных белков: они гораздо уже и почти симметричные в отличие от широких и скошенных пиков эмиссии других белков (сравните спектры E и F в таблице 1, фигура 4). Между тем, в GFP из Aequorea Victoria наличие или отсутствие фотоконверсии не имеет большого влияния на форму спектра эмиссии (Heim, R., Cubitt, A. B. & Tsien, R. Y. (1995) Nature 373, 663-4). Сильное сходство основных пиков возбуждения зрелого и незрелого белков позволяет сделать заманчивое предположение, что в mcavRFP и rfloRFP основным механизмом, обеспечивающим красную эмиссию, является "встроенный" перенос резонансной энергии флуоресценции (FRET) от незрелой зеленой формы белка к зрелой красной форме.
C. Структурные/спектральные типы GFP-подобных белков
По мнению авторов изобретения наилучшим способом классификации GFP-подобных белов является классификация по их цвету, как он предстает человеческому глазу. Авторы изобретения различают четыре цветовых типа GFP-подобных белков: зеленый, желтый, оранжево-красный и фиолетово-синий, или хромопротеины (таблица 1, фигура 14). Все они характеризуется одним и тем же фолдом полипептидной цепи, называемым "бета-бочонок" (Ormo, M., Cubitt, A. B., Kallio, K., Gross, L. A., Tsien, R. Y. & Remington, S. J (1996) Science 273,1392-5.; Yang, F., Moss, L. G. & Philips, G. N., Jr. (1996) Nat Biotechnol 14, 1246-51). Однако имеются существенные различия между данными цветовыми типами, поскольку затрагивается структура хромофора (см. таблицу 1).
В GFP (зеленый цвет) хромофор образуется остатками 65-67 (Ser-Tyr-Gly) в результате конденсации между углеродом карбонила Ser-65 и азотом аминогруппы Gly-67, что образует пятичленный цикл, с последующим дегидрированием метиленового мостика Tyr-66. Все зеленые белки явственно обладают таким хромофором, и различия в формах спектров объясняются модификациями их окружения. Следует заметить, что зеленые белки, имеющие спектры возбуждения/эмиссии, как на панели A таблицы 1, иногда называются голубыми или даже синими, но для человеческого глаза цвет данных белков после очистки пока остается ярко зеленым. В красном белке DsRed синтез хромофора включает в себя конъюгированную пи-систему хромофорного дегидрирования связи между альфа-углеродом и азотом аминогруппы первого образующего хромофор остатка. Между тем, у представителя хромопротеинов asulCP циклизация ведет к образованию шестичленного, а не пятичленного кольца, и критической стадией возникновения расширенной конъюгированной пи-системы является разрыв полипептидной цепи непосредственно перед хромофором. Замечательно, что ни один другой хромопротеин не содержит такого разрыва цепи, что демонстрируется путем денатурирующего электрофореза продуктов экспрессии в бактериях (данные не показаны). Это означает, что хромофорная структура asulCP является исключением, а не правилом для данного цветового типа. Исследования биохимии и мутагенеза желтого zoanYFP показали, что данный белок характеризуется еще одной структурой хромофора. Так, следует сделать вывод, что хотя выраженное цветовое отличие между GFP-подобными белками означает различие в структуре хромофора (что дает повод для использования цвета при классификации), различные хромофоры могут быть обнаружены даже в белках одного цвета, что случается в группе хромопротеинов и, вероятно, в группе оранжево-красных белков.
Молекулярные основы изменения цвета
Поскольку путь синтеза хромофора в DsRed является расширенной формой пути GFP, можно легко представить, что любая мутация, повреждающая дополнительный автокаталитический участок в DsRed, будет преобразовывать его в зеленый белок. Действительно, во время случайного и сайт-специфического мутагенеза было обнаружено по крайней мере семь различных вариантов DsRed, излучающих в зеленой области. Сходные соображения следует применять к двум новым красным белкам, поскольку их красное излучение также является результатом дальнейшей модификации хромофора с зеленой эмиссией.
Было показано, что единичная аминокислотная замена может превращать хромопротеин в DsRed-подобный флуоресцентный белок. Особенно неожиданным это было для asulCP из Anemonia sulcata, который, как было непосредственно показано, содержит очень несходный хромофор; и кажется маловероятным, что его красный флуоресцентный мутантный вариант действительно переключается на синтез хромофора типа DsRed вместо первоначального. Однако случайные мутации в данном мутантном варианте приводили к появлению форм с зеленой эмиссией. Поскольку в изначальном автокаталитическом пути asulCP не присутствовало стадии промежуточного продукта с зеленой эмиссией, образование структуры с зеленой эмиссией в данных мутантах указывает на значительное отклонение, наиболее вероятно, в направлении образования последовательности хромофора типа GFP/DsRed, судя по форме спектров возбуждения эмиссии в зеленых мутантах asulCP.
Наконец, желтый белок zoanYFP также может преобразовываться в состояние с зеленой эмиссией по крайней мере двумя различными аминокислотными заменами.
Учитывая эти данные, правдоподобным кажется следующее объяснение наблюдаемого филогенетического профиля: различные структуры хромофора, даже наиболее несходные, являются альтернативными продуктами, синтезируемыми с помощью сходного в своей основе автокаталитического окружения, а не происходят при длительной эволюции различных каталитических механизмов. Очевидно, что лишь малое число аминокислотных изменений в белке могут действовать как переключатель между альтернативными путями, примером чего являются результаты мутагенеза хромопротеина asulCP.
Все цитируемые в данной спецификации публикации и патентные заявки включены сюда в качестве ссылки, как если бы каждая отдельная публикация или патентная заявка была бы конкретно и индивидуально указана как включенная в качестве ссылки. Цитирование любой публикации осуществляется для ее описания до даты подачи и не должно рассматриваться как допущение того, что настоящее изобретение не наделено правом предшествовать такой публикации на основании более раннего изобретения.
Хотя описанное выше изобретение описано в некоторых подробностях для иллюстрации и примеров с целью ясности понимания, в свете учения настоящего изобретения обычным специалистам в данной области очевидно, что могут быть сделаны некоторые изменения и модификации изобретения без уклонения от сущности или объема прилагаемой формулы изобретения.















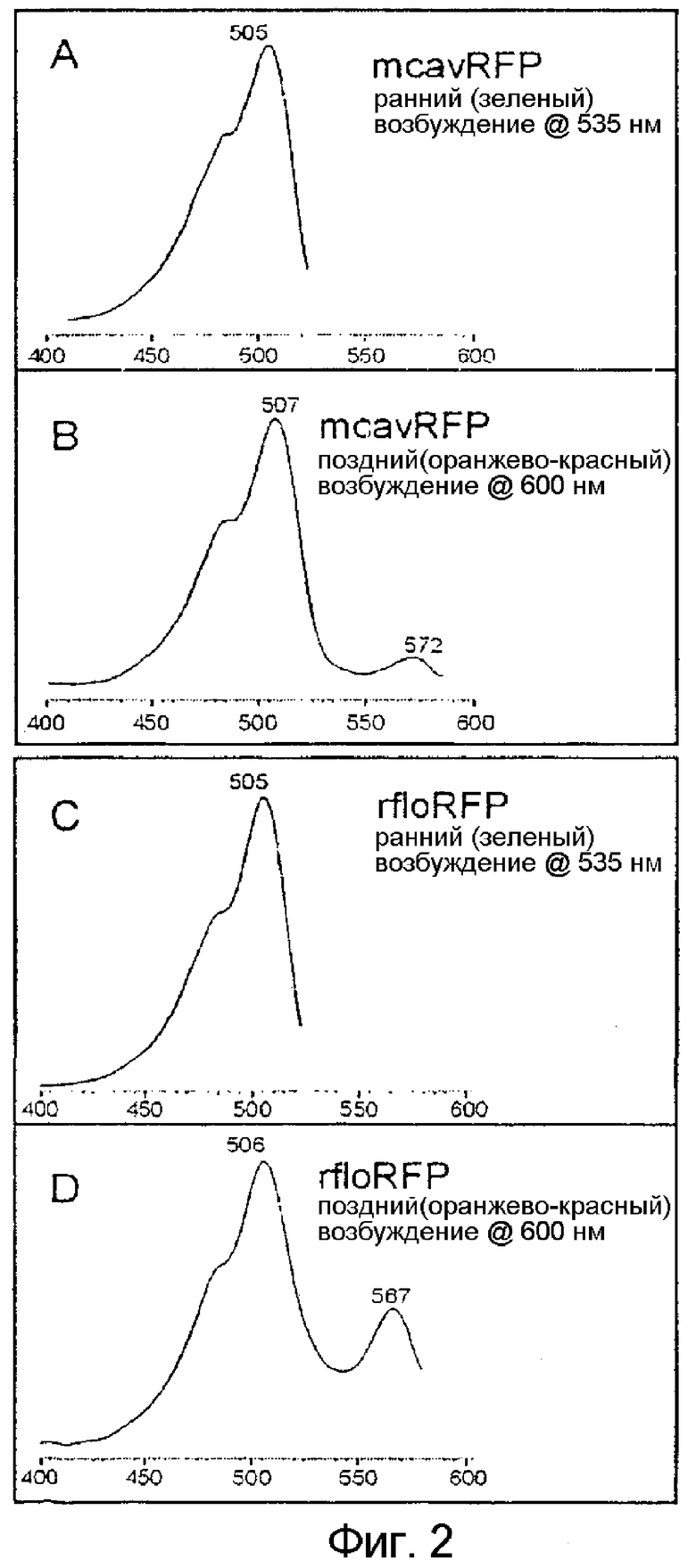
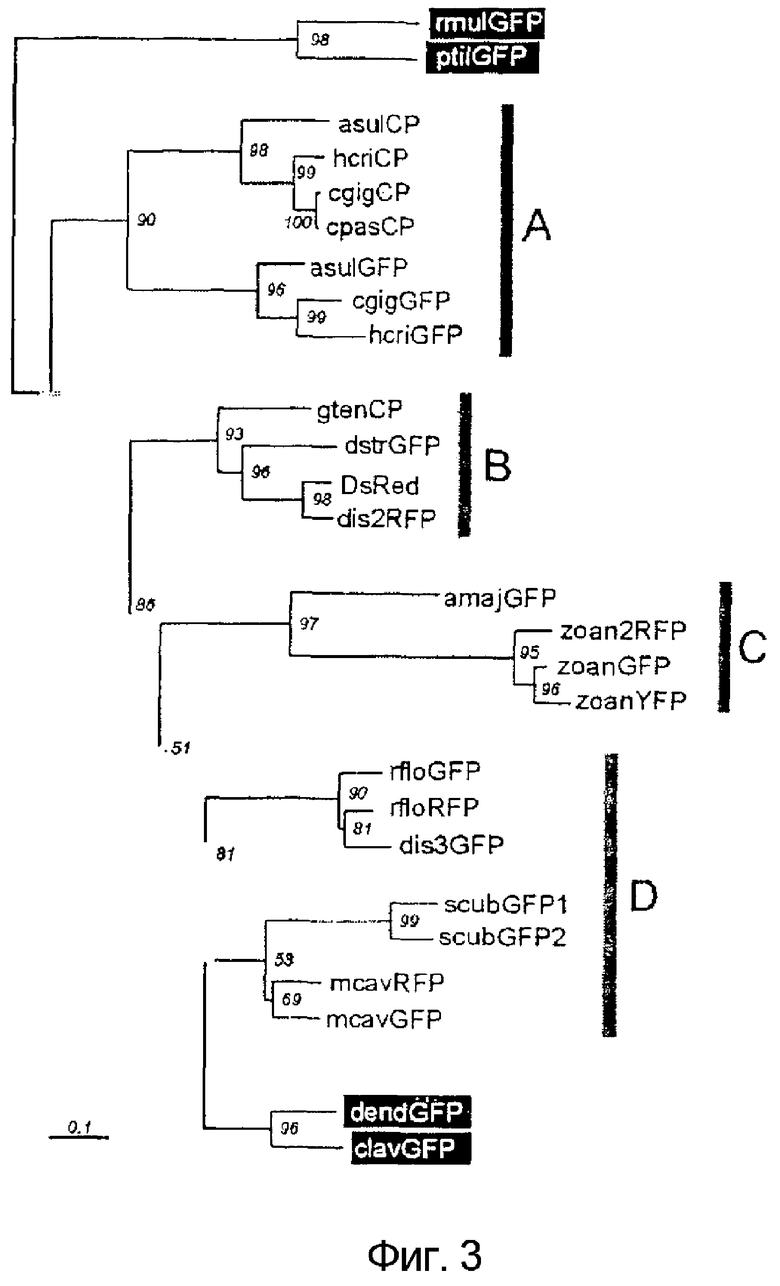
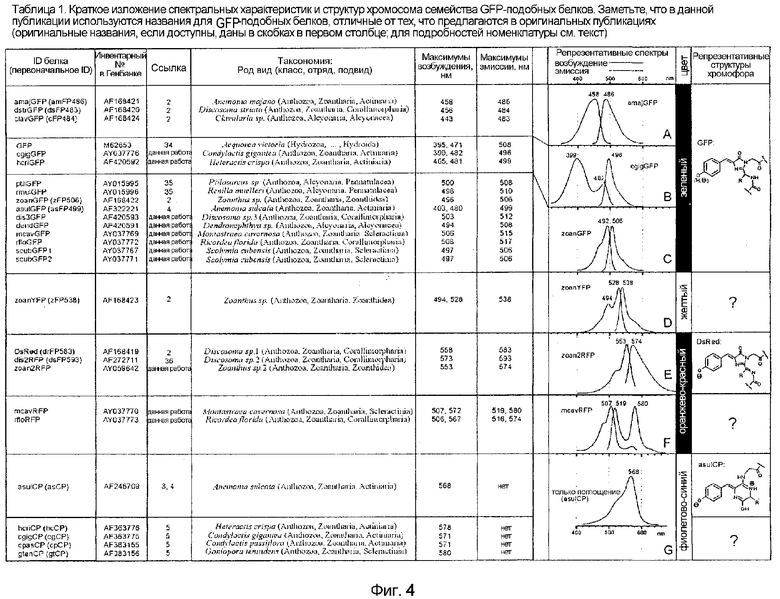
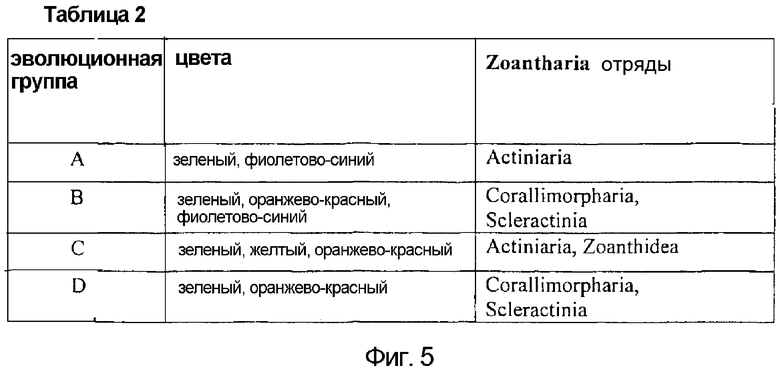
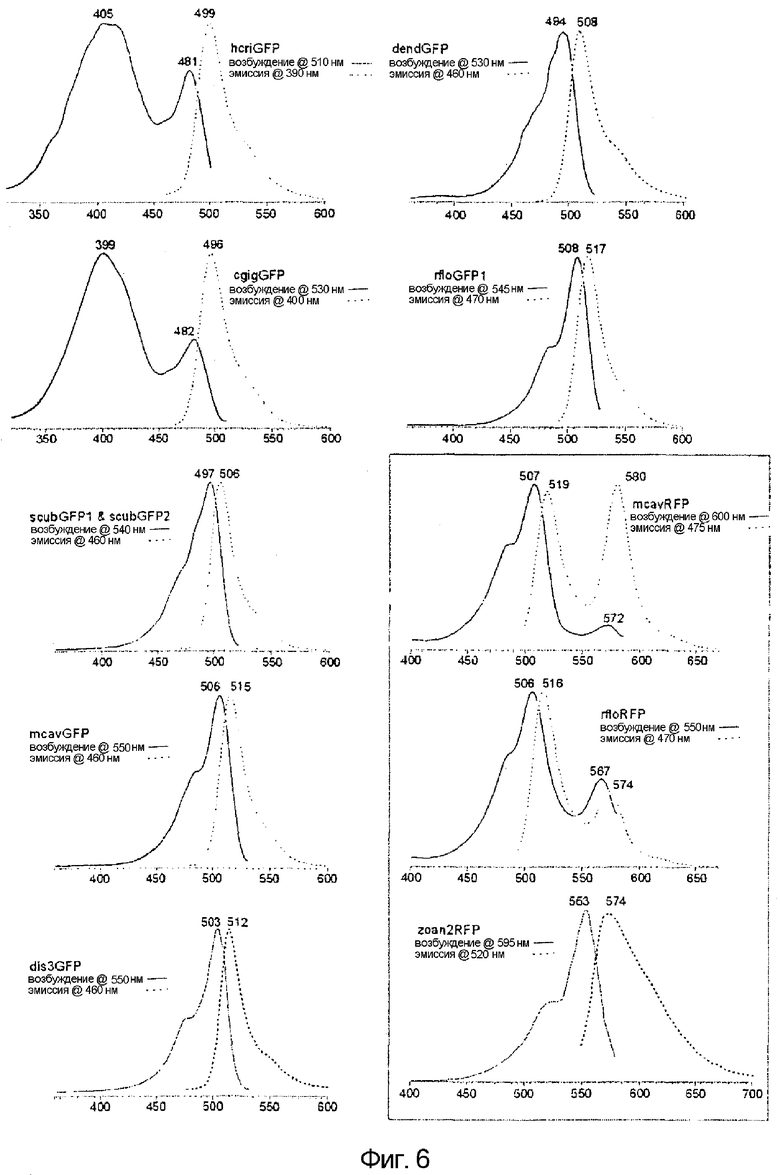
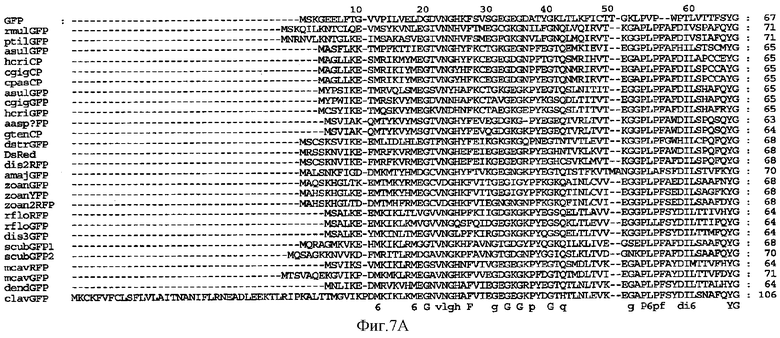





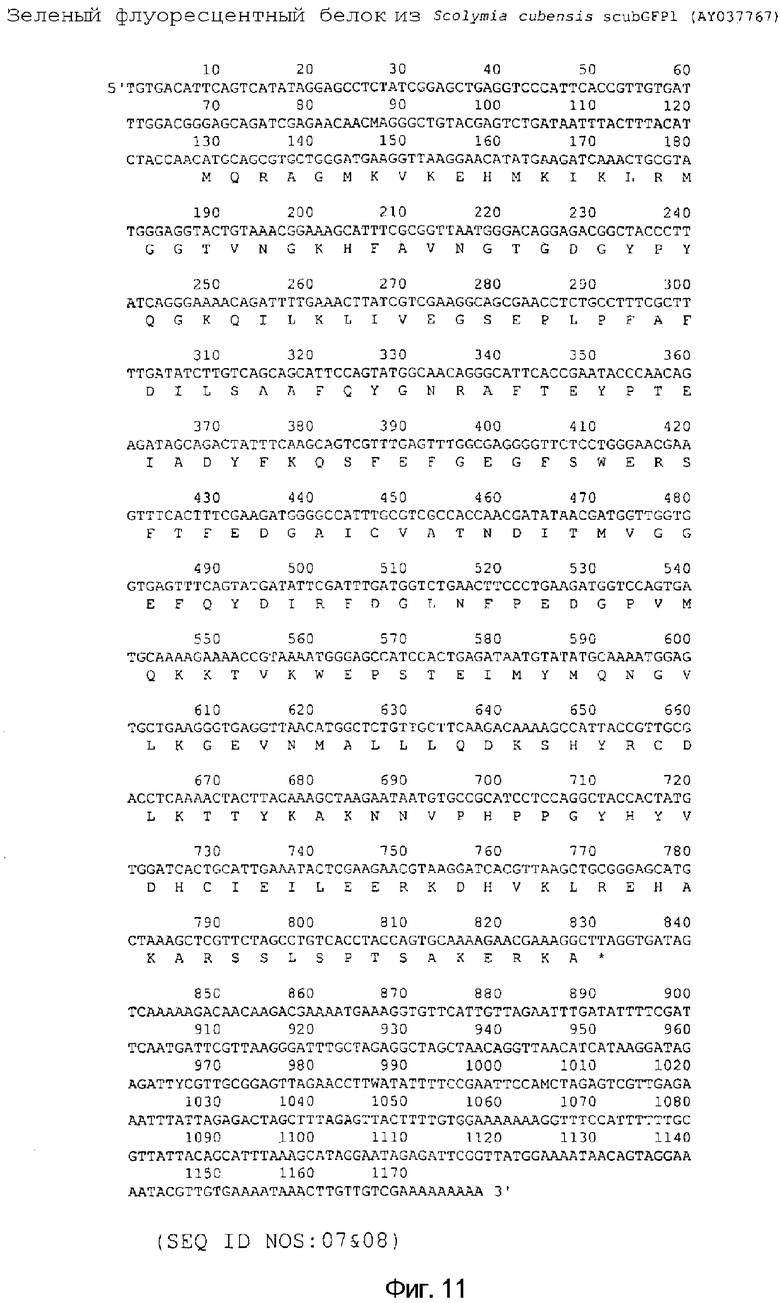

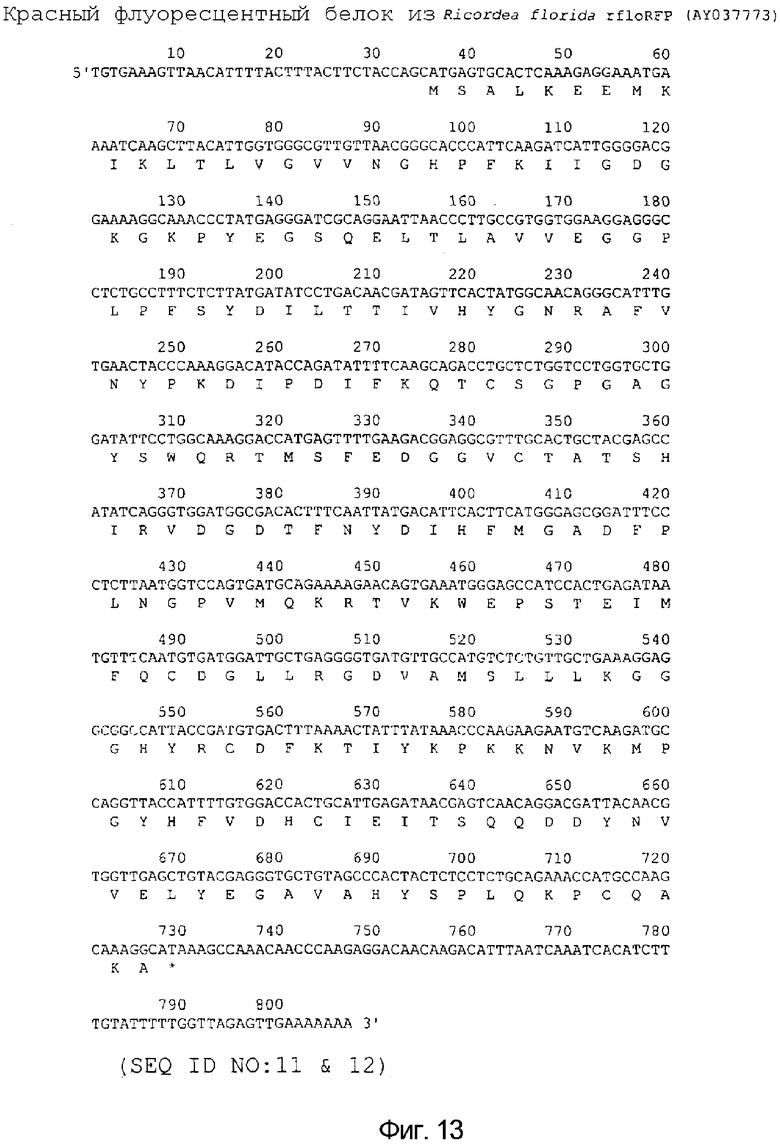
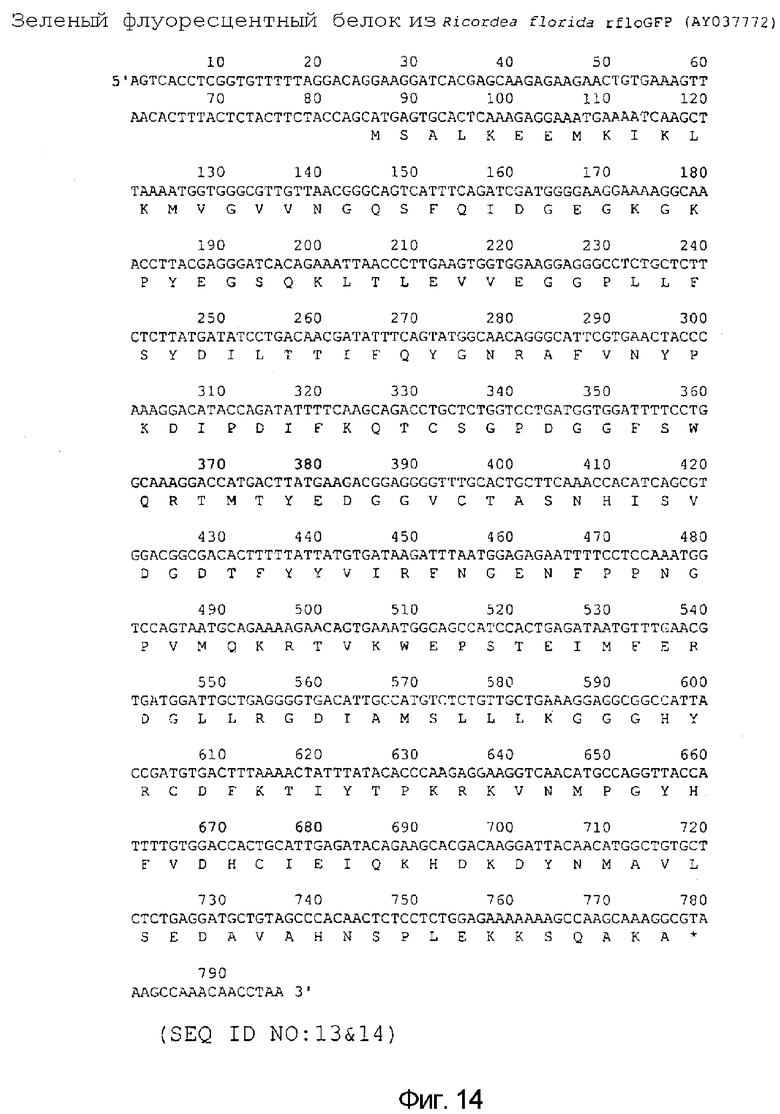
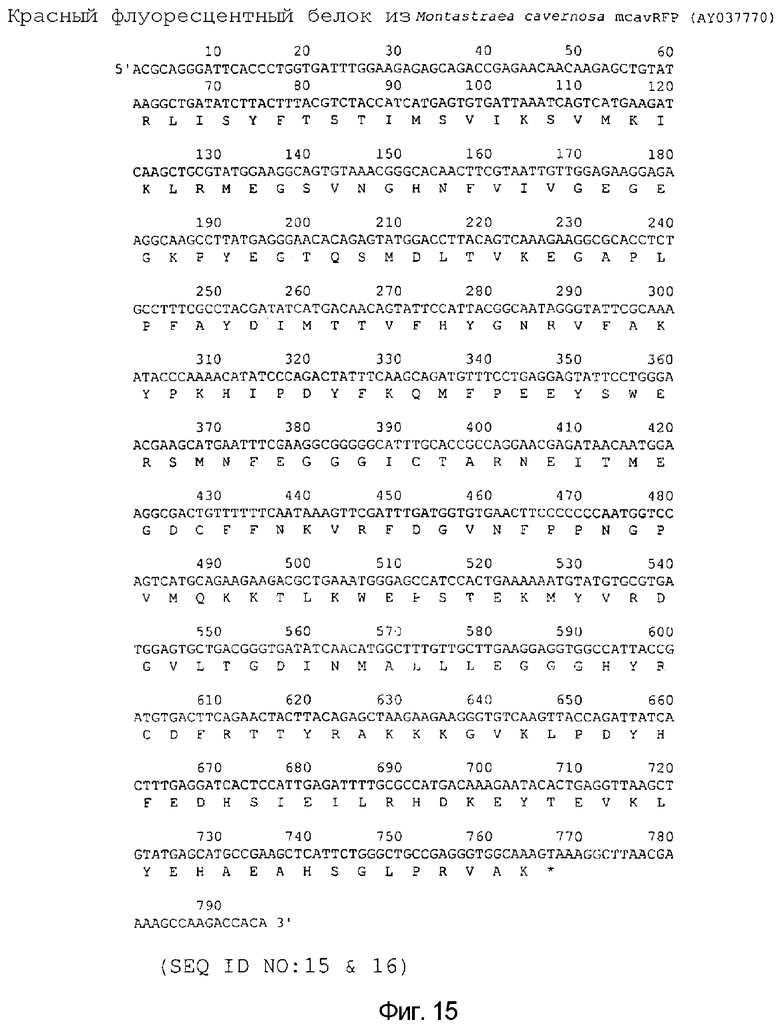



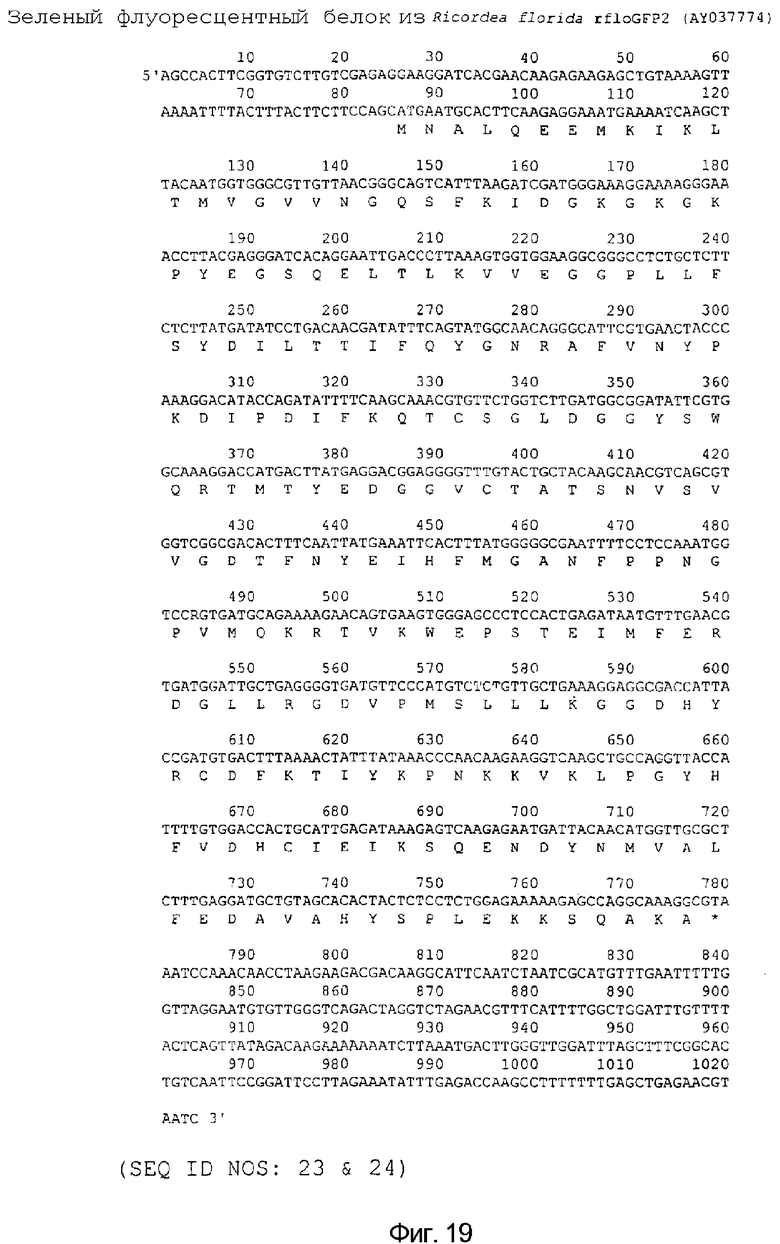

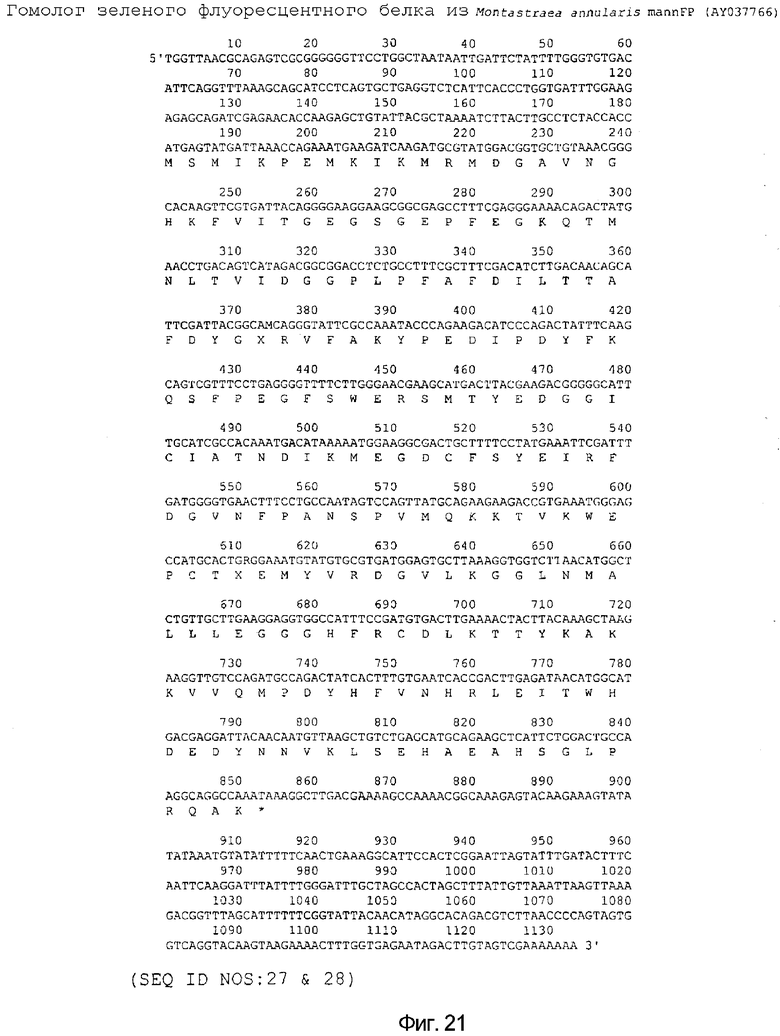
Изобретение относится к нуклеиновой кислоте, кодирующей хромофорный и/или флуоресцентный белок, обладающий сходством аминокислотной последовательности, составляющим, по меньшей мере, приблизительно 80%, с SEQ ID NO: 02, 04, 06, 08, 10, 12, 14, 16, 18, 20, 22, 24, 26 или 28, или комплементарной нуклеиновой кислоте, гибридизующейся в жестких условиях с указанной нуклеиновой кислотой. Также изобретение относится к нуклеиновой кислоте, кодирующей белок, характеризующийся аминокислотной последовательностью SEQ ID NO: 02, 04, 06, 08, 10, 12, 14, 16, 18, 20, 22, 24, 26 или 28, и к набору для получения белка. 3 н. и 4 з.п. ф-лы, 21 ил.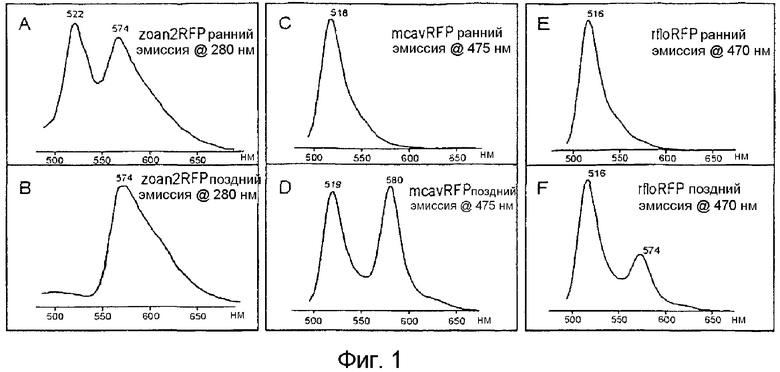
| УСТРОЙСТВО ДЛЯ ПОЛУЧЕНИЯ ТОЛЧКООБРАЗНОГО ЗАДАЮЩЕГО СИГНАЛА В ГИДРАВЛИЧЕСКИХ СЛЕДЯЩИХСИСТЕМАХ | 0 |
|
SU322221A1 |
| WIEDENMANN J | |||
| ET AL | |||
| Cracks in the beta-can: fluorescent proteins from Anemonia sulcata | |||
| Proct | |||
| Natl | |||
| Acad | |||
| Sci | |||
| U.S.A., 2000, 97 (26), pp.14091-14096 Database GenBank Accession № AF 420592, 19 September 2001, № AY 037776, 30 May 2001 | |||
| LABAS Y.A | |||
| ET AL | |||
| Diversity and evolution of the green | |||
Авторы
Даты
2007-07-27—Публикация
2002-11-12—Подача