Изобретение относится к области медицины и может использоваться в способах получения препаратов для мезотерапии, применяющихся для коррекции возрастных изменений кожи лица при старении.
Стремление как можно дольше сохранить привлекательность и внешнюю молодость побуждает людей применять разнообразные косметологические средства, прибегать к помощи косметологов и пластических хирургов. По статистическим данным, каждая шестая женщина старше 40 лет прибегает к услугам косметологов и пластических хирургов. А 60% всех операций в хирургических отделениях Института пластической хирургии и косметологии МЗ и СР РФ направлено на коррекцию возрастных изменений лица.
Известно, что возрастной процесс снижения тургора и эластичности кожи связан с уменьшением числа юных и зрелых фибробластов. В молодой коже благодаря значительному числу фибробластов коллагеновые волокна и гликозаминогликановый гель постоянно обновляются. С возрастом обновление межклеточного вещества дермы и синтез коллагена идет все медленнее, накапливаются поврежденные коллагеновые волокна, а количество гликозаминогликанов неуклонно снижается. В результате кожа теряет влагу, истончается ее дермальный слой, что приводит к снижению ее упругости и эластичности - кожа стареет.
Все кремы, содержащие коллаген, эластин и гликозаминогликаны, дают временный незначительный эффект, так как эти субстанции редко проникают глубже эпидермиса и только частично сглаживают морщины и складки.
В настоящее время разрабатываются различные подходы к коррекции возрастных изменений мягких тканей лица: оперативная косметология - различные варианты фейслифтинга, аппаратная косметология, фотоомоложение, мезотерапия. Последняя является наиболее перспективной, так как путем микроинъекций обеспечивается доставка препарата в более глубокие слои дермы и осуществляется длительное воздействие на ткани-мишени.
Мезотерапия как метод воздействия известен уже более 150 лет. Но идеи и принципы мезотерапии в современном ее применении сформулировал основатель методики Мишель Пистор в 1952 г. Основа метода мезотерапии - внутрикожные микроинъекции различных препаратов на уровень средней части дермы - мезодермы. Осуществляется либо обкалывание всей проблемной зоны либо отдельного анатомического участка, либо введение препарата в определенные точки. Применяется папульная, туннельная техники.
Однако часто приходится сталкиваться с отсутствием ожидаемого эффекта от введения препарата или использования многокомпонентного коктейля. Длительность эффекта после проведения курса инъекций препаратами коллагена, эластина, гиалуроновой кислоты достигает 2-3-х месяцев. До сих пор не найден препарат, отвечающий всем требованиям эстетической медицины. Одной из попыток решения данной проблемы является применение клеточных технологий или органопрепаратов.
В научной литературе известны методы коррекции возрастных изменений кожи с помощью органопрепаратов. Наиболее известным производителем органопрепаратов на фармацевтическом рынке является НПК Вит Орган. Остальные органопрепараты НПК Вит Орган из клеточного содержимого (от стволовых до зрелых клеток телят) широко применяются за рубежом и в России с целью коррекции возрастных изменений. Однако отрицательным моментом использования фетальных органопрепаратов является сенсибилизация человеческого организма чужеродным животным белком, ряд ученых считают, что подобные инъекции вредны - из-за разницы генокода животного и человека.
Основной принцип омоложения кожи аутологичными фибробластами заключается в простой, эффективной идее: доставить в стареющую кожу эффективные более молодые клетки, которые способны выполнять специализированную функцию по синтезу коллагена и гликозаминогликанов.
В работе Г.Келлера с соавторами пациентам в возрасте 37-61 года вводили аутологичные фибробласты, выделенные из кожи пациентов, с получением стойкого клинического эффекта. В опытах на животных было доказано отсутствие онкогенных и туморогенных свойств аутологичных фибробластов (Бюллетень экспериментальной биологической медицины 2000 г., 130 (8), стр.203-206). А.А.Згурский и Э.А.Крихели применяли культуру аутогенных фибробластов кожи для коррекции возрастных изменений кожи лица и области шеи пациенткам в возрасте 40-60 лет ("Применение аутогенных фибробластов в косметологии", опубл. в журнале "Эстетическая медицина", т.3 №4, с.336-342, 2004 г.). При наблюдении за пациентками в течение 12 месяцев отмечен стойкий положительный эффект, проявлявшийся в исчезновении мелких и уменьшении крупных морщин, а также в общем улучшении состояния кожи.
Наиболее близким является способ получения препарата для мезотерапии, включающий выделение аутологичных фибробластов человека для интрадермального введения их пациенту, запатентованный американской компанией "ISOLAGEN TECHNOLOGIES Inc." (Патент США №5660850, опубл. 26.08.1997, "Use of autologous dermal fibroblasts for the repair of skin and soft tissue defects).
Из указанного патента известен также препарат для мезотерапии, включающий аутологичные фибробласты человека для интрадермального введения их пациенту.
Работы были начаты в 1995 году. К 1999 г. были проведены многоцентровые двойные слепые плацебоконтролируемые клинические испытания, доказавшие эффективность и безопасность метода. Эффективность доказывалась значительным уменьшением рельефности кожи (измерялась методом лазерной профилометрии), утолщением дермального слоя, увеличением в нем числа фибробластов и плотности коллагена, а также субъективной оценкой пациентов. По гистологическим показателям эффект остается заметным спустя 3 года после лечения, по другим - до 7 лет. В известном способе аутологичные фибробласты, полученные из кожи доноров, сразу после их получения интрадермально вводятся пациенту.
Однако недостатком введения аутологичных фибробластов является невысокий пролиферативный потенциал, особенно у культуры, выделенной из кожи пожилых доноров, с этой точки зрения, для достижения оптимального омолаживающего эффекта необходимо использование "молодых" клеток, которые имеют больший пролиферативный потенциал по сравнению с культурами, полученными от взрослых доноров. Кроме того, при введении аутологичных фибробластов от доноров возможна экспрессия антигенов гистосовместимости.
Наилучшие результаты клеточной терапии достигаются при использовании культур эмбриональных фибробластов, однако применение эмбриональных клеток в России запрещено законом о "клонировании" и не используется по этическим мотивам.
Решаемая изобретением задача - улучшение качества получаемого препарата и усиление омолаживающего эффекта.
Технический результат, который может быть получен при осуществлении заявленного способа, - улучшение качественных показателей получаемых препаратов, таких как стойкость клинического эффекта при мезотерапии, ускорение проявления эффекта эластичности кожи.
Технический результат, который может быть получен при изготовлении препарата, - повышение его пролиферативного потенциала и уменьшение экспрессии антигенов гистосовместимости, увеличение объемного капиллярного кровотока кожи, ускорение проявления эффекта эластичности кожи и сокращение курса мезотерапии при применении заявленных препаратов.
Дополнительный технический результат, который может быть достигнут, - увеличение срока хранения препарата до проведения сеанса мезотерапии.
Для решения поставленной задачи с достижением указанного технического результата по первому варианту в известном способе получения препарата для мезотерапии, включающем выделение культуры фибробластов человека для интрадермального введения их пациенту, согласно изобретению выделение аллогенных фибробластов производят из пуповины новорожденного после нормальных родов.
Возможны дополнительные варианты осуществления способа, в которых целесообразно, чтобы:
- выделение аллогенных фибробластов производили из пуповины новорожденного после нормальных родов на 39-40 недели гестации;
- при выделении аллогенных фибробластов из пуповины новорожденного вены канюлировали с обеих сторон и промывали сначала раствором Хенкса, а затем 0,1% раствором коллагеназы 1 типа, приготовленным на среде DMEM, свободной от сыворотки, и инкубируют при 37°С в течение 30 минут, затем осуществляют механическое воздействие на ткани пуповины, собирают отделившиеся клетки, промывая их раствором Хенкса, полученную после механического воздействия и промывания суспензию клеток центрифугируют при 1000 об/мин в течение 5 минут, получая осадок клеток, который ресуспензируют в ростовой среде DMEM, содержащей 10% фетальной сыворотки крупного рогатого скота, 100 ед./мл пенициллина, 100 ед./мл стрептомицина, 2 мМ глютамина, 1 мМ пирувата натрия, 10 нг/мл базального фактора роста фибробластов bFGF, ресуспензированный осадок клеток в ростовой среде DMEM переносят в культуральные чашки и культивируют до формирования монослоя, сменяя ростовую среду DMEM 2 раза в неделю, и при достижении монослоя клетки пересевают в соотношении 1:3;
- перед проведением сеанса мезотерапии монослой переводили в суспензию путем обработки смесью раствора Версена и 0,25% раствора трипсина в соотношении 1:1 в течение 20 мин при 37°С, которую затем трижды промывают физиологическим раствором с рН 7,2, затем суспензию осаждают центрифугированием в течение 5 мин при 1000 об/мин, осадок клеток ресуспензируют в стерильном биологическом растворе NCTF-135, получая аллогенные фибробласты человека для интрадермального введения пациенту в количестве 1-5 млн клеток в 5 мл.
Для решения поставленной задачи с достижением указанного технического результата по второму варианту в известном способе получения препарата для мезотерапии, включающем выделение культуры фибробластов человека для интрадермального введения их пациенту, согласно изобретению выделение аллогенных фибробластов производят из пуповины новорожденного после нормальных родов, производят выделение аутологичных фибробластов собственно пациента, которые смешивают с аллогенными фибробластами из пуповины новорожденного.
Возможны дополнительные варианты осуществления способа по второму варианту, в котором целесообразно, чтобы:
- при выделении аллогенных фибробластов из пуповины новорожденного вены канюлировали с обеих сторон и промывали сначала раствором Хенкса, а затем 0,1% раствором коллагеназы 1 типа, приготовленным на среде DMEM, свободной от сыворотки, и инкубируют при 37°С в течение 30 минут, затем осуществляют механическое воздействие на ткани пуповины, собирают отделившиеся клетки, промывая их раствором Хенкса, полученную после механического воздействия и промывания суспензию клеток центрифугируют при 1000 об/мин в течение 5 минут, получая осадок клеток, который ресуспензируют в ростовой среде DMEM, содержащей 10% фетальной сыворотки крупного рогатого скота, 100 ед./мл пенициллина, 100 ед./мл стрептомицина, 2 мМ глютамина, 1 мМ пирувата натрия, 10 нг/мл базального фактора роста фибробластов bFGF, ресуспензированный осадок клеток в ростовой среде DMEM переносят в культуральные чашки и культивируют до формирования монослоя, сменяя ростовую среду DMEM 2 раза в неделю, и при достижении монослоя клетки пересевают в соотношении 1:3;
- перед проведением сеанса мезотерапии монослой переводили в суспензию путем обработки смесью раствора Версена и 0,25% раствора трипсина в соотношении 1:1 в течение 20 мин при 37°С, которую затем трижды промывают физиологическим раствором с рН 7,2, затем суспензию осаждают центрифугированием в течение 5 мин при 1000 об/мин, осадок клеток ресуспензируют в стерильном биологическом растворе NCTF-135, получая аллогенные фибробласты пуповины человека в количестве 1-5 млн клеток в 2,5 мл - первый полуфабрикат;
- при выделении аутологичных фибробластов собственно пациента использовали его фрагмент кожи, который промывают раствором Версена с добавлением антибиотиков 100 ед./мл пенициллина, 100 ед./мл стрептомицина, 100 ед./мл амфотерицина в течение 1 часа при комнатной температуре при встряхивании на шейкере, затем фрагмент кожи измельчают, получая гомогенат, к которому добавляют 0,1% раствор коллагеназы 1 типа, приготовленной на среде DMEM, свободной от сыворотки, и инкубируют в нем при 37°С в течение 2 часов, получая суспензию, которую центрифугируют при 1000 об/мин в течение 5 минут, получая осадок клеток, который ресуспензируют в ростовой среде DMEM, содержащей 10% фетальной сыворотки крупного рогатого скота, 100 ед./мл пенициллина, 100 ед./мл стрептомицина, 2 мМ глютамина, 1 мМ пирувата натрия, 10 нг/мл базального фактора роста фибробластов bFGF, ресуспензированный осадок клеток в ростовой среде DMEM переносят в культуральные чашки и культивируют до формирования монослоя, сменяя среду 2 раза в неделю, при достижении монослоя клетки пересевают в соотношении 1:3;
- перед проведением сеанса мезотерапии монослой клеток собственно пациента переводили в суспензию путем обработки смесью раствора Версена и 0,25% раствора трипсина в соотношении 1:1 в течение 20 мин при 37°С, которую затем трижды промывают физиологическим раствором с рН 7,2, затем суспензию осаждают центрифугированием в течение 5 мин при 1000 об/мин, осадок клеток ресуспензируют в стерильном биологическом растворе NCTF-135, получая аутологичные фибробласты человека в количестве 1-5 млн клеток в 2,5 мл - второй полуфабрикат;
- аллогенные фибробласты из пуповины новорожденного - первый полуфабрикат и аутологичные фибробласты собственно пациента - второй полуфабрикат смешивали между собой в соотношении 1:1, получая готовый препарат в количестве 1-5 млн клеток в 5 мл.
Соответственно полученный по первому варианту реализации способа известный препарат для мезотерапии, включающий культуру фибробластов человека для интрадермального введения их пациенту, согласно изобретению в нем в качестве культуры фибробластов человека использованы аллогенные фибробласты, полученные из пуповины новорожденного.
Соответственно полученный по второму варианту реализации способа препарат для мезотерапии, включающий культуру фибробластов человека для интрадермального введения их пациенту, согласно изобретению в нем в качестве культуры фибробластов человека использована смесь аллогенных фибробластов, полученных из пуповины новорожденного, и аутологичных фибробластов, полученных из кожи собственно пациента.
Указанные преимущества, а также особенности настоящего изобретения поясняются лучшим вариантом его выполнения со ссылками на прилагаемые чертежи.
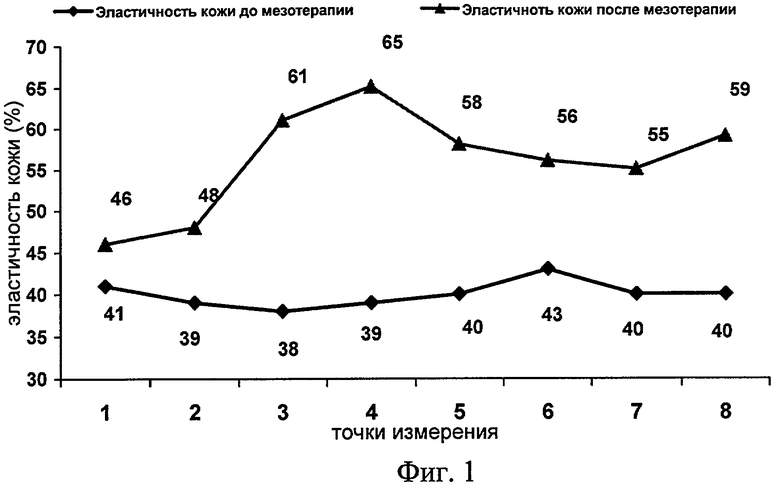
Фиг.1 изображает усредненный для различных пациентов график изменения эластичности кожи до и через 14 дней после сеанса мезотерапии аллогенными фибробластами из пуповины.
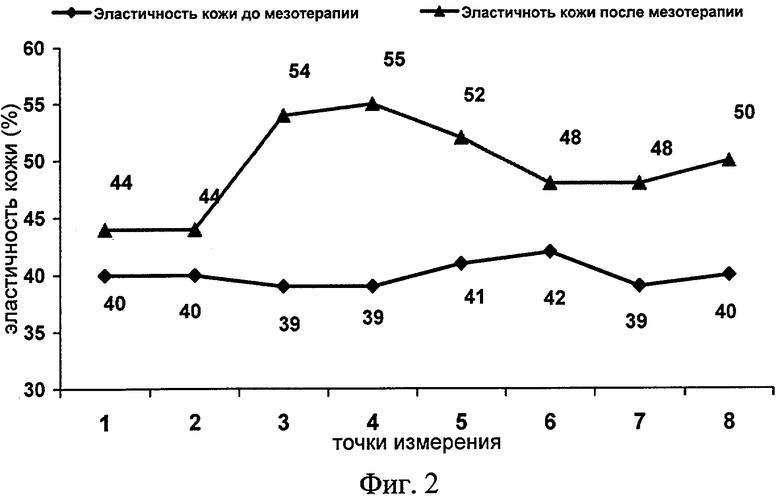
Фиг.2 - то же, что фиг.1, после сеанса мезотерапии смесью аллогенных фибробластов из пуповины и аутологичных фибробластов собственно пациента.
Фиг.3 - фотография лица пациентки до (слева) и после (справа) проведения мезотерапии аллогенными фибробластами из пуповины.
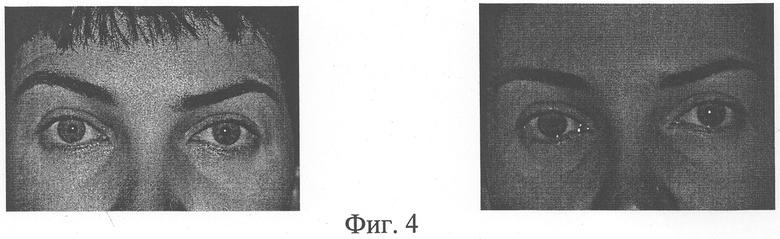
Фиг.4 - фотография лица пациентки до (слева) и после (справа) проведения мезотерапии смесью аллогенных фибробластов, полученных из пуповины новорожденного, и аутологичных фибробластов, полученных из кожи собственно пациента.
Способ получения препарата для мезотерапии реализуется следующим образом.
Сначала производится тестирование донора (собственно пациента) перед забором биологического материала - кожи.
Образцы крови доноров исследуются на наличие маркеров следующих инфекционных агентов:
вирусов гепатита В и С,
вируса иммунодефицита человека (ВИЧ) 1 и 2 типов,
вируса герпеса простого 1, 2 и 6 типов,
вируса Эпштейна-Барр,
цитомегаловируса и Toxoplasma Gondi,
сифилиса.
При заборе пуповины для получения аллогенных фибробластов дополнительно к вышеперечисленным анализам образцов крови, донорам (матерям) проводится исследование соскоба цервикального канала на наличие маркеров уреоплазмы, хламидии и микоплазмы.
Выявление таких инфекций, как ВИЧ, сифилис, а также острых форм гепатитов В и С, являлось абсолютным противопоказанием для культивирования биологического материала и введения полученных клеток - аутологичных фибробластов реципиенту.
В случае выявления других инфекционных агентов у донора либо при наличии антител к ним решение о культивировании биологического материала и возможности введения клеточного препарата реципиенту принимает врач. В нашем исследовании выявление любых инфекционных агентов или антител к ним являлось абсолютным противопоказанием для культивирования биологического материала.
Получение и культивирование аллогенных фибробластов пуповины осуществляют следующим образом.
Образцы пуповины человека собирают после нормальных родов на 38-40 недели гестации для получения аллогенных фибробластов после нормальных родов. После перевязки и перерезания пуповину помещают в стерильный контейнер, содержащий раствор Хенкса с добавлением пенициллина 100 мг/мл, стрептомицина 100 мг/мл и амфотерицина 100 мг/мл и на льду перевозят в лабораторию. Пуповину освобождают от остатков крови и тщательно промывают в растворе Версена с добавлением антибиотиков 100 ед./мл пенициллина, 100 ед./мл стрептомицина, 100 ед./мл амфотерицина) в течение 1 часа при комнатной температуре на шейкере. Вены канюлируют с обеих сторон и промывают сначала раствором Хенкса, а затем 0,1% раствором коллагеназы 1 типа, приготовленным на среде DMEM (Dulbecco's modified Eagle medium), свободной от сыворотки, и инкубируют при 37°С в течение 30 минут, затем осуществляют механическое воздействие на ткани пуповины, собирают отделившиеся клетки, промывая их раствором Хенкса. Полученную после механического воздействия и промывания суспензию клеток центрифугируют при 1000 об/мин в течение 5 минут, получая осадок, который ресуспензируют в ростовой среде: DMEM (Dulbecco's modified Eagle medium), содержащей 10% фетальной сыворотки крупного рогатого скота, 100 ед./мл пенициллина, 100 ед./мл стрептомицина, 2 мМ глютамина, 1 мМ пирувата натрия, 10 нг/мл базального фактора роста фибробластов bFGF (FGF - Fibroblast Growth Factore) (bFGF - Basic Fibroblast Growth Factore/). Ресуспензированный осадок клеток в ростовой среде переносят в культуральные чашки и культивируют до формирования монослоя, сменяя ростовую среду 2 раза в неделю. При достижении монослоя клетки пересевают в соотношении 1:3.
Перед проведением сеанса мезотерапии монослой клеток обрабатывают смесью раствора Версена и 0,25% раствора трипсина (1:1) в течение 20 мин при 37°С, получая клеточную суспензию, которую затем трижды промывают физиологическим раствором с рН 7,2. Затем клетки осаждают центрифугированием 5 мин при 1000 об/мин. Осадок клеток ресуспензируют в стерильном биологическом растворе NCTF-135 в количестве 1-5 млн клеток в 5 мл, получая первый вариант готового препарата для мезотерапии.
NCTF-135 'коктейль мгновенной красоты' 2865 Б (Препарат Laboratories FILORGA). Состав: витамины (16), нуклиевые кислоты (5), минералы (4), аминокислоты (23), коэнзимы (коферменты), антиоксиданты, а именно витамины: С, А, К, В2, В5, В7, В9, В12, Е, В1, В3, РР, Вв, В8, Н, В10, аминокислоты: аминомасляная, аспарагиновая, глютаминовая, аланин, аргинин, аспарагин, сирин, цистин, глютамин, гликоль, гидроксипролин, гистидин, изолейцин, лейцин, лизин, метионин, орнитин, фенилаланин, пролин, таурин, трионин, триптофан, тирозин, валин, коферменты: коэнзим А, НАД, НАДФ, кокарбоксилаза, ФАД, АТФ, антиоксиданты: аскорбиновая кислота, глютатион, нуклеиновые кислоты - дезоксигуанозин, дезоксиаденозин, дезоксицистидин, тимидин, метилцитозин, минералы: кальций, магний, калий, натрий.
Готовый препарат хранится до 72 часов после его приготовления при температуре от +4°С до +10°С.
Получение аутологичных фибробластов из биологического материала собственно пациента осуществляют следующими образом.
С помощью хирургического лезвия одноразового использования берут кусочек кожи 3×3 мм с внутренней поверхности предплечья или с ягодицы. Другой вариант забора первичного материла для выделения аутологичных фибробластов - с помощью одноразовой биопсийной иглы малого диаметра. Фрагмент кожи промывают раствором Версена с добавлением антибиотиков (100 ед./мл пенициллина, 100 ед./мл стрептомицина 100 ед./мл, 100 ед./мл амфотерицина) 1 час при комнатной температуре при встряхивании на шейкере. Затем фрагмент кожи измельчают ножницами. К гомогенату добавляют 0,1% раствор коллагеназы 1 типа, приготовленной на среде DMEM, и инкубируют в нем в течение 2 часов. Затем центрифугируют при 1000 об/мин 5 минут. Осадок клеток ресуспензируют в ростовой среде: DMEM, содержащей 10% фетальной сыворотки крупного рогатого скота, 100 ед./мл пенициллина, 100 ед./мл стрептомицина, 2 мМ глютамина, 1 мМ пирувата натрия, 10 нг/мл базального фактора роста фибробластов bFGF. Суспензию клеток в ростовой среде переносят в культуральные чашки. Проводят культивирование до формирования монослоя, сменяя ростовую среду 2 раза в неделю. При достижении монослоя клетки пересевают в соотношении 1:3.
Перед проведением сеанса мезотерапии монослой клеток обрабатывают смесью раствора Версена и 0,25% раствора трипсина (1:1) в течение 20 мин при 37°С, получая клеточную суспензию, которую затем трижды промывают физиологическим раствором с рН 7,2. Затем клетки осаждают центрифугированием 5 мин при 1000 об/мин. Осадок ресуспензируют в стерильном биологическом растворе NCTF-135 в количестве 1-5 млн клеток в 2,5 мл, получая второй полуфабрикат.
Для получения препарата по второму варианту первый полуфабрикат, полученный из пуповины, и второй полуфабрикат, полученный из кожи собственно пациента, смешивают между собой в соотношении 1:1, получая второй вариант готового препарата для мезотерапии.
Таким образом, при смешивании культур клеток, полученных из пуповины и из кожи собственно пациента, в соотношении, например, 1:1 получают препарат для мезотерапии (коктейль), включающий аутологичные фибробласты человека для интрадермального введения их пациенту, в котором в качестве аутологичных фибробластов человека использована смесь аутологичных фибробластов, полученных из пуповины новорожденного и из кожи собственно пациента.
Как показали исследования, полученные препараты можно хранить в отличие от известных аналогов в течение 72 часов при температуре от +4°С до +10°С.
За счет использования в этих препаратах аллогенных фибробластов из пуповины удается повысить их пролиферативный потенциал и уменьшить экспрессию антигенов гистосовместимости, увеличить объемный капиллярный кровоток кожи, ускорить проявления эффекта эластичности кожи. За счет применения во втором препарате аутологичных фибробластов, полученных из кожи собственно пациента, удается дополнительно уменьшить экспрессию антигенов гистосовместимости. Поскольку использование культур эмбриональных фибробластов запрещено, то наиболее оптимальными для получения омолаживающего эффекта являются аллогенные фибробласты, полученные из пуповины. Они относятся к "молодым" клеткам, не онкогенны, имеют ограниченную продолжительность жизни и низкую экспрессию антигенов гистосовместимости.
Полученные препараты проходили следующие испытания.
Вирусологические исследования на наличие маркеров вирусов гепатитов В и С, вируса иммунодефицита человека (ВИЧ) 1 и 2 типов, вируса герпеса простого 1,2 и 6 типов, вируса Эпштена-Барр, цитомегаловируса, Toxoplasma Gondi.
Бактериологическое исследование на наличие аэробной и анаэробной микрофлоры, а также микроскопических грибов.
На каждый препарат выдается паспорт соответствия с указанием результатов обследования культуры, объема препарата, концентрации клеток, а также срока годности препарата. На доклиническом этапе клеточные препараты проходили исследования на острую токсичность и пирогенность на животных.
Все операции по подготовке клеточных препаратов для мезотералии проводят в стерильных условиях культурального бокса.
Готовая суспензия вводится с помощью множественных внутрикожных инъекций (методика мезотерапии). Сеанс мезотерапии проводится в процедурном кабинете в положении пациентки лежа или сидя без предварительной анестезии. Введение препарата производится с помощью шприцов объемом от 5,0 до 20,0 мл со специальными иглами для внутридермальных инъекций (27-30G). Препарат вводится в кожу на глубину 2-4 мм маленькими дозами. Объем вводимого раствора в одну инъекцию должен составлять 0,02-0,05 мл. При введении препарата целесообразно использовать технику микропапул или трассирующую технику, так как только при использовании этих методик возможно создать необходимое депо препарата в тканях.
При использовании техники микропапул готовая суспензия вводится интрадермально отдельными уколами с образованием папул. Инъекции проводятся по всей поверхности лица, шеи и декольте на расстоянии 10-15 мм друг от друга. Шприц и игла располагаются по касательной к коже, срез иглы направлен вверх. Давление на поршень осуществляется большим пальцем рабочей руки. Препарат вводится в папиллярный слой дермы на глубину 2-4 мм.
При использовании трассирующей техники используется контролируемое интрадермальное линейное введение как под морщины, так и в область проблемных зон. Игла длиной 13 мм вводится по касательной к коже, срезом вверх. Препарат вводится на выходе иглы (ретроградно) на глубину 2 мм.
Количество клеток в готовой суспензии - 1-2-5 млн клеток в 5 мл стерильного биологического раствора NCTF-135.
Курс мезотерапии с использованием клеточного материала рассчитан на 3 процедуры с интервалом введения 1 месяц. Эффект от введения препарата начинает проявляться через 1-2 недели и постепенно нарастает, достигая стойкого клинического эффекта через 1 месяц от первой инъекции. У пациенток с выраженными инволюционными изменениями и отсутствием стойкого клинического эффекта от 1-й инъекции в течение 1 месяца рекомендуется увеличивать дозу препарата при второй инъекции до 5,0×106 клеток в 5 мл раствора.
Результаты использования препаратов оценены у 98 пациенток с инволюционными изменениями кожи лица.
Для объективизации оценки таких параметров, как тургор и эластичность, микроциркуляция, плотность и однородность кожи лица до и после проведения мезотерапии аутологичными фибробластами, использовались современные инструментальные методы исследования:
- эластометрия, ElastometrR ЕМ 25 фирмы "Courage + Khazaka electronic GmbH" (Германия),
- лазерная доплеровская флоуметрия, одноканальный лазерный доплеровский флоуметр фирмы "Transonic System Inc" (США).
Изменения эластичности кожи пациенток после проведения мезотерапии с использованием аутологичных фибробластов представлены на фиг.1 и 2, где на фиг.1 показан усредненный для различных пациентов график изменения эластичности кожи до и через 14 дней после сеанса мезотерапии аутологичными (аллогенными) фибробластами из пуповины, а на фиг.2 - после сеанса мезотерапии смесью аутологичных фибробластов из пуповины и собственно пациента. Как видно из фиг.1 и 2, показатели эластичности кожи для обоих препаратов практически одинаковы. Эластичность кожи через 14 дней после введения препаратов увеличивалась на 18-27% в разных точках лица, эффект повышения эластичности сохранялся в течение 3-8-12 месяцев после проведения курса клеточной терапии. Дальнейшие исследования стойкости действия в настоящее время не завершены, поскольку исследования этих новых препаратов проводились в течение одного 2005 года.
Показатели объемного капиллярного кровотока кожи оценены с помощью лазерной доплеровской флоуметрии в сроки 14 дней и 3 месяца после выполнения мезолифтинга с использованием препаратов и представлены в таблице.
↑
↑
При контрольном осмотре пациенток через 14 дней после сеанса мезотерапии с использованием клеточного материала было отмечено увеличение объемного капиллярного кровотока кожи лица во всех точках исследования (р<0,1). При контрольном осмотре через 6 месяцев сохранялось увеличение объемного капиллярного кровотока по всем точкам (р=0,1). Р - критерий Стьюдента достоверности полученных результатов. В данном случае смысл р<0,1: с вероятностью более 90% отличия достоверны или вероятность недостоверности отличий составляет менее 10%.
Степень и быстрота наступления клинического эффекта зависели от исходного состояния кожи пациентки. Слабый и кратковременный клинический эффект наблюдался у пациенток, тонус кожи которых был существенно снижен и наблюдалась выраженная деформация овала лица. В этом случае следует увеличивать дозу готовой суспензии до 5,0×106 в 5 мл физиологического раствора при повторной инъекции через 1 месяц. Результаты, полученные методами субъективной и объективной оценки, совпали.
Пример 1. Пациентка А. 64 лет (фиг.3) с выраженными возрастными изменениями кожи лица. Проведен курс мезотерапии аллогенными фибробластами пуповины в дозе 3,0 млн клеток в 5,0 мл физиологического раствора готовой суспензии.
После проведения курса мезотерапии отмечено повышение показателей эластичности кожи на 15-21% и улучшение микроциркуляции, исчезли мелкие морщинки в области угла глаза, сгладились носогубные складки, нарастание эффекта было отмечено через 6 и 12 месяцев исследования.
Пример 2. Пациентка В. 36 лет (фиг.4) с возрастными изменениями кожи 2 степени, витилиго. Проведен курс мезотерапии смесью аллогенных фибробластов из пуповины новорожденного и аутологичных фибробластов и собственно пациентки в дозе 1,0 млн клеток в 5,0 мл физиологического раствора, через 1 и 3 месяца отмечено повышение эластичности кожи на 28-34%, улучшение микроциркуляции, исчезли пигментации, улучшился цвет лица, исчезли мелкие морщинки в параорбитальной области и области лба, мешки под глазами.
Таким образом, предложенные способы получения препаратов и полученные этими способами препараты для мезотерапии позволяют осуществить коррекцию возрастных изменений кожи лица с использованием только аллогенных фибробластов или с использованием аутологичных или аллогенных фибробластов, санкционируют запускание процессов саморегуляции кожи. По данным объективных инструментальных исследований улучшается структура кожи, восстанавливается ее эластичность, повышается микроциркуляция, что субъективно приводит к улучшению цвета и укреплению овала лица.
Наиболее успешны заявленные способы получения препаратов для мезотерапии и эти препараты промышленно применимы в оперативной косметологии.

Заявленная группа изобретений относится к области медицины и может использоваться в способах получения препарата для мезотерапии, применяющегося для коррекции возрастных изменений кожи лица при старении. Предложен способ выделения аллогенных фибробластов человека для интрадермального введения их пациенту. Выделение аллогенных фибробластов производят из пуповины новорожденного. Предложен способ выделения аутологичных фибробластов собственно пациента, которые смешивают с аллогенными фибробластами из пуповины новорожденного. Предложен препарат для мезотерапии, который содержит аллогенные фибробласты, полученные из пуповины новорожденного. Предложен препарат для мезотерапии, который содержит смесь аллогенных фибробластов, полученных из пуповины новорожденного, и аутологичных фибробластов из кожи собственно пациента. Изобретение позволяет улучшить качество получаемого препарата и обеспечивает усиление омолаживающего эффекта. 4 н. и 1 з.п. ф-лы, 4 ил., 1 табл.
| JP 4187614 А1, 06.07.1992 | |||
| Дифференциальный усилитель | 1985 |
|
SU1314440A1 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| RU 2004118437 A, 20.11.2005 | |||
| US 5660850 A 26.08.1997 | |||
| WO 9704720 A1, 13.02.1997 | |||
| WO 2005065269 A1, 21.07.2005. | |||
Авторы
Даты
2007-10-27—Публикация
2006-03-24—Подача