По данной заявке испрошен приоритет по предварительной заявке на патент США №60/272676, поданной 1 марта 2001 г., которая включена сюда в качестве ссылки.
Область техники
Данное изобретение относится к соединениям и композициям для доставки бисфосфонатов к цели. Эти соединения хорошо подходят для получения нековалентных смесей с бисфосфонатами для перорального введения животным. Также описаны способы получения, введения и лечения.
Уровень техники
Обычные средства доставки активных агентов часто сильно ограничены биологическими, химическими и физическими барьерами. Обычно такие барьеры создаются окружающей средой, через которую происходит доставка, окружающей средой цели доставки и/или самой целью. Биологически и химически активные агенты особенно чувствительны к таким барьерам.
При доставке животным биологически активных и химически активных фармакологических и терапевтических агентов, барьеры создаются телом. Примерами физических барьеров являются кожа, жировые би-слои и мембраны различных органов, которые относительно непроницаемы для определенных активных агентов, но должны быть пересечены перед достижением цели, такой как сердечно-сосудистая система. Химические барьеры включают, но не ограничены ими, различие рН желудочно-кишечного (ЖК) тракта и расщепляющие ферменты.
Эти барьеры имеют особенное значение при разработке пероральных систем доставки. Пероральная доставка многих биологически или химически активных агентов была бы преимущественным путем введения животным, если бы не биологические, химические и физические барьеры, которые препятствуют, ограничивают или снижают проходимость активных агентов. Одними из многочисленных агентов этой категории являются бисфосфонаты. Бисфосфонаты обычно прописывают для лечения и/или профилактики остеопороза (См. Drug Delivery Today, Yates, A. John and Rodan, Gideon "Alendronate and Osteoporosis", vol.3, №; 2, pgs.69-78, February 1998). Хотя некоторые бисфосфонаты в настоящее время доступны в виде пероральных таблетированных лекарственных форм, средняя пероральная биодоступность относительно внутривенной (ВВ) ссылочной дозы довольно низка; например, алендронат имеет фиксированную среднюю биодоступность 0,7% для доз в интервале от 5 до 40 мг при введении после голодания в течение ночи. Ранние способы перорального введения чувствительных фармакологических агентов основаны на совместном введении адъювантов (например, резорцинолами и неионными поверхностно-активными веществами, такими как полиоксиэтиленолеиловый эфир и н-гексадецилполиэтиленовый эфир) для искусственного повышения проницаемости стенок кишечника, а также совместном введении ферментных ингибиторов (например, ингибиторов панкреатического трипсина, диизопропилфторфосфата (ДФФ) и трасилола) для ингибирования ферментного разложения. Липосомы также описаны в качестве системы доставки лекарственных средств для инсулина и гепарина. Однако широкое применение таких систем доставки лекарственных средств невозможно из-за того, что: (1) системы требуют токсических количеств адъювантов или ингибиторов; (2) недоступны подходящие низкомолекулярные «грузы», например, активные агенты; (3) системы обладают плохой стабильностью и имеют недостаточный срок годности; (4) системы трудно производить; (5) системы не защищают активный агент («груз»); (6) системы отрицательно изменяют активные агенты; или (7) системы не способствуют абсорбции активного агента.
Определенные модифицированные аминокислоты были использованы для доставки фармацевтических агентов. См., например, патенты США 5629020; 5643957; 5650386; 5766633; 5776888 и 5866536 и заявку РСТ WO 00/06534.
Существует необходимость в простой недорогой системе доставки, которую легко получить, для доставки бисфосфонатов.
Краткое описание изобретения
Данное изобретение относится к композициям, содержащим, по крайней мере, одно из соединений-агентов доставки следующих формул и, по крайней мере, один бисфосфонат. Такие композиции способствуют доставке бисфосфонатов к выбранным биологическим системам и повышают или улучшают биодоступность бисфосфонатов по сравнению с введением без соединения-агента доставки. Соединения-агенты доставки в соответствии с данным изобретением включают соединения, имеющие следующие формулы или их соли:
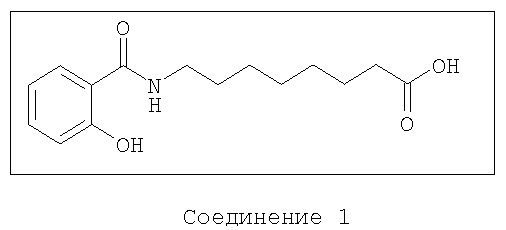
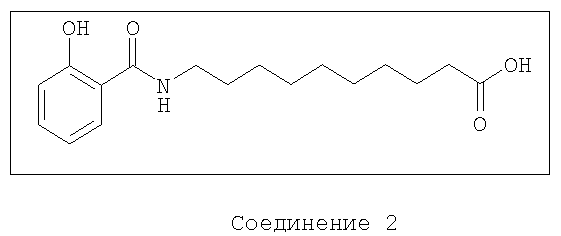
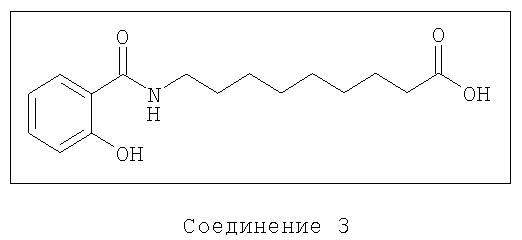
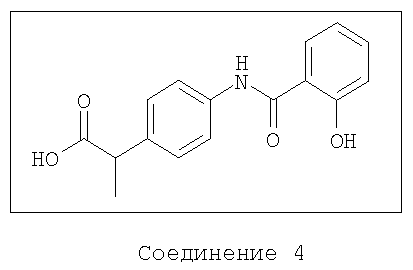
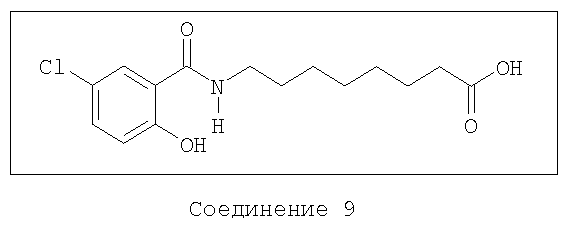
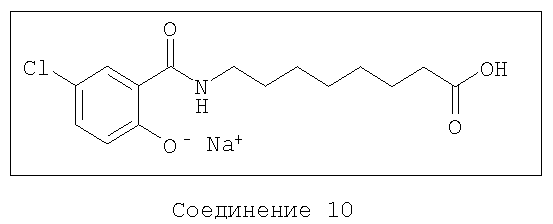
В другом предпочтительном варианте, композиция содержит бисфосфонат и агент доставки следующей формулы и его соли:
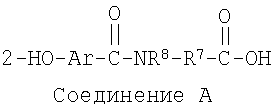
где Ar является фенилом или нафтилом; необязательно замещенным ОН, галогеном, С1-С4алкилом, С1-С4алкенилом, С1-С4алкокси или С1-С4галоалкокси;
R7 выбирают из группы, включающей С4-С20алкил, С4-С20алкенил, фенил, нафтил, (С1-С10алкил)фенил, (С1-С10алкенил)фенил, (С1-С10алкил)нафтил, (С1-С10алкенил)нафтил, фенил(С1-С10алкил), фенил(С1-С10алкенил), нафтил(С1-С10алкил) или нафтил(С1-С10алкенил);
R8 выбирают из группы, включающей водород, С1-С4алкил, С2-С4алкенил, С1-С4алкокси, С1-С4 и галоалкокси;
R7 необязательно замещен С1-С4алкилом, С2-С4алкенилом, С1-С4алкокси, С1-С4 галоалкокси, -ОН, -SH и -CO2R9 или любым их сочетанием;
R9 является водородом, С1-С4алкилом или С2-С4алкенилом.
R7 необязательно прерван кислородом, азотом, серой или любым их сочетанием;
при условии, что соединения не замещены аминогруппой в положении альфа по отношению к кислотной группе или их соли.
Согласно одному предпочтительному варианту, Ar замещен ОН. Согласно другому предпочтительному варианту, Ar замещен ОН и галогеном.
Предпочтительно, R7 является С4-С20алкилом или фенил(С1-С10алкилом). Более предпочтительно, R7 является С5-С10алкилом или фенил(С2алкилом). Наиболее предпочтительно, R7 является С7-С9алкилом или фенил(С2алкилом).
Предпочтительные соединения-носители включают соединения формул 1, 2, 3, 4 или их соли.
В другом варианте композиция включает бисфосфонат и агент доставки следующей структуры и его соли:
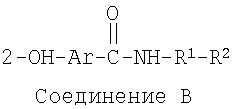
где
Ar является фенилом или нафтилом;
Ar необязательно замещен С1-С4алкилом, С1-С4алкокси, С2-С4алкенилом, С2-С4алкинилом, арилом, арилокси, гетероциклическим кольцом, С5-С7карбоциклическим кольцом, галогеном, -ОН, -SH, CO2R6, -NR7R8 или -N+R7R8R9Y-;
(а) R1 является С1-С16алкиленом, С2-С4алкениленом, С2-С16алкиниленом, С6-С16ариленом, (С1-С16алкил)ариленом или арил(С1-С16алкиленом);
R2 является -NR3R4 или -N+R7R8R9Y-;
R3 и R4 независимо являются водородом; кислородом; гидрокси; замещенным или незамещенным С1-С16алкилом; замещенным или незамещенным С2-С16алкенилом; замещенным или незамещенным С2-С16алкинилом; замещенным или незамещенным арилом; замещенным или незамещенным алкилкарбонилом; замещенным или незамещенным арилкарбонилом; замещенным или незамещенным алкансульфинилом; замещенным или незамещенным арилсульфинилом; замещенным или незамещенным алкансульфонилом; замещенным или незамещенным арилсульфонилом; замещенным или незамещенным алкоксикарбонилом; замещенным или незамещенным арилоксикарбонилом;
R5 независимо является водородом; замещенным или незамещенным С1-С16алкилом; замещенным или незамещенным С2-С16алкенилом; замещенным или незамещенным С2-С16алкинилом; замещенным или незамещенным арилом; замещенным или незамещенным алкилкарбонилом; замещенным или незамещенным арилкарбонилом; замещенным или незамещенным алкансульфинилом; замещенным или незамещенным арилсульфинилом; замещенным или незамещенным алкансульфонилом; замещенным или незамещенным арилсульфонилом; замещенным или незамещенным алкоксикарбонилом; замещенным или незамещенным арилоксикарбонилом;
(b) R1, R2 и R5 такие, как определены выше; и
R3 и R4 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца; или 5-, 6- или 7-членного гетероциклического кольца, замещенного С1-С6алкилом, С1-С6алкокси, арилом, арилокси, оксогруппой или карбоциклическим кольцом; или
(с) R2 и R5 такие, как определены выше; и
R1 и R3 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца; или 5-, 6- или 7-членного гетероциклического кольца, замещенного С1-С6алкилом, алкокси, арилом, арилокси или оксогруппой или карбоциклического кольца;
R4 является водородом; кислородом; гидрокси; замещенным или незамещенным С1-С16алкилом; замещенным или незамещенным С2-С16алкенилом; замещенным или незамещенным С2-С16алкинилом; замещенным или незамещенным арилом; замещенным или незамещенным алкилкарбонилом; замещенным или незамещенным арилкарбонилом; замещенным или незамещенным алкансульфинилом; замещенным или незамещенным арилсульфинилом; замещенным или незамещенным алкансульфонилом; замещенным или незамещенным арилсульфонилом; замещенным или незамещенным алкоксикарбонилом; замещенным или незамещенным арилоксикарбонилом;
R6 является водородом; С1-С4алкилом; С1-С4алкилом, замещенным галогеном или -ОН; С2-С4алкенилом; или С2-С4алкенилом, замещенным галогеном или -ОН;
R7, R8 и R9 независимо являются водородом; кислородом; С1-С4алкилом; С1-С4алкилом, замещенным галогеном или -ОН; С2-С4алкенилом; или С2-С4алкенилом, замещенным галогеном или -ОН; и
Y является галогеном, гидрокси, сульфатом, нитратом, фосфатом, алкокси, перхлоратом, тетрафторборатом или карбоксилатом. Не ограничивающим примером подходящего карбоксилата является ацетат.
Термин «замещенный» в данном описании, относящийся к соединению В, включает, но не ограничен ими, следующие заместители: галоген и -ОН.
В одном предпочтительном варианте Ar является незамещенным фенилом или фенилом, замещенным одним или более С1-С4алкилом, С1-С4алкокси или галогеном; более предпочтительно, фенилом, замещенным метокси, Cl, F или Br; более предпочтительно заместителем является Cl.
В другом предпочтительном варианте R1 является С1-С12алкилом, более предпочтительно, С2-С8алкилом, более предпочтительно, С2-С6алкилом и более предпочтительно С6алкилом.
В другом предпочтительном варианте R3 и R4 независимо являются Н или С1-С2алкилом; более предпочтительно, R3 и R4 оба не являются Н; более предпочтительно, R3 и R4 независимо являются метилом или этилом; и более предпочтительно, R3 и R4 оба являются метилом.
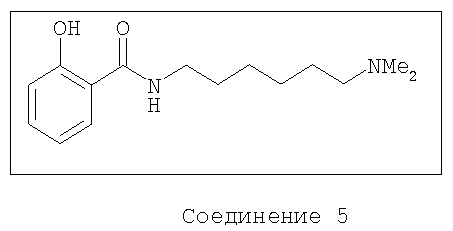
В другом предпочтительном варианте соединение является соединением формулы 5 или его солями.
Также представлены стандартные лекарственные формы, содержащие композиции. Стандартные лекарственные формы могут быть в виде жидкостей или твердых веществ, таких как таблетки, капсулы или частицы, включая порошки или саше.
В другом варианте представлен способ введения бисфосфонатов животным, при необходимости такого введения, введением композиции в соответствии с данным изобретением животному. Предпочтительным способом введения является пероральный.
Еще одним вариантом является способ лечения и/или профилактики заболеваний костей животных введением композиции в соответствии с данным изобретением животному. Обычно эффективное количество композиции вводят для лечения и/или профилактики заболеваний костей.
Еще одним вариантом является способ получения композиции в соответствии с данным изобретением смешиванием, по крайней мере, одного соединения-агента доставки и, по крайней мере, одного бисфосфоната.
Подробное описание данного изобретения
Соединения-агенты доставки
Термины «алкил» и «алкенил» в данном описании включают линейные и разветвленные алкильные и алкенильные заместители, соответственно.
Соединения-агенты доставки, изображенные в виде карбоновых кислот, могут быть в форме карбоновой кислоты или ее соли. Подходящие соли включают, но не ограничены ими, органические и неорганические соли, например, соли щелочных металлов, таких как натрий (например, мононатриевые и динатриевые соли, такие как мононатриевые и динатриевые соли соединений 1-4 и 7-9), калий и литий; соли щелочноземельных металлов, таких как магний, кальций или барий; аммониевые соли; основные аминокислоты, такие как лизин или аргинин; и органические амины, такие как диметиламин или пиридин. Предпочтительно, солями являются натриевые соли. Соли могут быть одно- или поливалентными солями, такими как мононатриевые соли и динатриевые соли. Соли также могут быть сольватами, включая сольваты этанола, и гидратами.
Соединения-агенты доставки, изображенные в виде аминов, могут быть в форме свободных аминов или их солей. Подходящие соли включают, но не ограничены ими, органические и неорганические соли, например, гидрохлорид, ацетат или цитрат.
Соли соединений-агентов доставки в соответствии с данным изобретением могут быть получены методами, известными в данной области техники. Например, натриевые соли могут быть получены растворением соединения-агента доставки в этаноле и добавлением водного гидроксида натрия.
Если агент доставки имеет аминогруппу и группу карбоновой кислоты, могут применяться полиаминокислоты и пептиды, содержащие одно или более из этих соединений. Аминокислота представляет собой любую карбоновую кислоту, имеющую, по крайней мере, одну свободную аминогруппу, и включает природные и синтетические аминокислоты. Полиаминокислоты являются либо пептидами (которые представляют собой две или более аминокислоты, соединенные пептидной связью) либо представляют собой две или более аминокислоты, связанные связью, образованной другими группами, которые могут быть связаны, например, сложной эфирной или ангидридной связью. Пептиды могут изменяться по длине от дипептидов с двумя аминокислотами до полипептидов с несколькими сотнями аминокислот. Одна или более из аминокислот или пептид могут быть ацилированы или сульфонированы.
Описанные здесь соединения являются производными аминокислот, и они могут быть легко получены из аминокислот методами, известными специалистам в данной области техники, такими как описаны в WO 96/30036, WO 97/36480, WO 00/06534, WO 00/46812, WO 00/50386, WO 00/59863, WO 01/32596, WO 00/07979, патенте США №5643957, патенте США №5650386 и патенте США №5866536, которые включены сюда в качестве ссылок. Например, соединения могут быть получены взаимодействием одной аминокислоты с соответствующим ацилирующим или аминмодифицирующим агентом, которые взаимодействуют со свободной аминогруппой, присутствующей в аминокислоте, с получением амидов. Могут применяться защитные группы для избежания нежелательных побочных реакций, что известно специалистам в данной области техники. Защитные группы раскрыты в T.W.Green, Protecting Groups in Organic Synthesis, Wiley, New York (1981), содержание которой включено сюда в качестве ссылки.
Соединение-агент доставки может быть очищен перекристаллизацией или фракционированием на одной или более твердых хроматографических подложках, отдельно или вместе. Подходящие системы растворителей для перекристаллизации включают, но не ограничены ими, ацетонитрил, метанол, этанол, этилацетат, гептан, воду, тетрагидрофуран и их сочетания. Фракционирование может проводиться на подходящей хроматографической подложке, такой как окись алюминия, с применением смесей метанола/н-пропанола в качестве подвижной фазы; хроматографией с обращенной фазой с применением смесей трифторуксусной кислоты/ацетонитрила в качестве подвижной фазы; и ионообменной хроматографией с применением воды или подходящего буфера в качестве подвижной фазы. Если проводят анионообменную хроматографию, предпочтительно применяют градиент 0-500 мМ хлорида натрия.
Бисфосфонаты
Термин «бисфосфонаты» относится к пирофосфантым аналогам, в которых центральный атом кислорода группы фосфор-кислород-фосфор молекулы замещен атомом углерода с получением группы фосфор-углерод-фосфор. Примеры бисфосфонатов включают, но не ограничены ими, алендронат, клодронат, этидронат, ибандронат, инкадронат, минодронат, неридронат, олпадронат, памидронат, ризедронат, тилудронат, золедронат, ЕВ1053, YH529 и любые их аналоги, миметики и полиэтиленгликоль-модифицированные производные.
Системы доставки
Композиция в соответствии с данным изобретением содержит одно или более соединений-агентов доставки и один или более бисфосфонат. В одном варианте, одно или более соединение-агент доставки смешивают с одним или более бисфосфонатом до введения с получением композиции для введения.
Композиции для введения могут быть в виде жидкости. Средой для раствора может быть вода. Дозируемые растворы могут быть получены смешиванием раствора соединения-агента доставки с раствором бисфосфоната, непосредственно перед введением. Альтернативно, раствор соединения-агента доставки (или бисфосфоната) может быть смешан с твердой формой бисфосфоната (или соединения-агента доставки). Соединение-агент доставки и бисфосфонат также могут быть смешаны в виде сухих порошков. Соединение-агент доставки и бисфосфонат также могут быть смешаны во время процесса производства.
Дозируемые растворы могут необязательно содержать добавки, такие как соли фосфатного буфера, лимонная кислота, гликоли или другие диспергирующие агенты. Стабилизирующие добавки могут быть введены в раствор, предпочтительно в концентрации от около 0,1 до 20% (масс./объем).
Композиции для введения альтернативно могут быть в виде твердого вещества, такого как таблетки, капсулы или частицы, или порошки или саше. Твердые дозированные формы могут быть получены смешиванием твердой формы соединения с твердой формой бисфосфоната. Альтернативно, твердое вещество может быть получено из раствора соединения-агента доставки и бисфосфоната методами, известными в данной области техники, такими как сушка вымораживанием (лиофилизация), осаждение, кристаллизация и твердые дисперсии.
Композиции для введения в соответствии с данным изобретением также могут включать один или более ферментных ингибиторов. Такие ферментные ингибиторы включают, но не ограничены ими, соединения, такие как актинонин или эпиактинонин и их производные. Другие ферментные ингибиторы включают, но не ограничены ими, апротинин (тразилол) и ингибитор Боумана-Бирка.
Количество бисфосфоната, применяемое в композиции для введения в соответствии с данным изобретением, представляет собой количество, эффективное для достижения цели введения бисфосфоната. Количество бисфосфоната в композициях обычно является фармакологически, биологически, терапевтически или химически эффективным количеством. Однако количество может быть меньше, чем количество, применяемое в композиции в виде стандартной лекарственной формы, так как стандартная лекарственная форма может содержать множество композиций соединений-агентов доставки/бисфосфонатов, или может содержать раздельное фармакологически, биологически, терапевтически или химически эффективное количество. Общее эффективное количество может вводиться суммарным количеством единичных доз, содержащих, в общем, эффективное количество бисфосфоната.
Общее применяемое количество бисфосфоната может быть определено методами, известными специалистам в данной области техники. Однако, так как композиции в соответствии с данным изобретением могут доставлять бисфосфонат более эффективно, чем композиции, содержащие только бисфосфонат, пациенту может вводиться более низкое количество бисфосфоната по сравнению с количеством, используемым в стандартных лекарственных формах известного уровня техники, или система доставки может быть введена субъекту, при этом достигая того же уровня бисфосфоната в крови и/или терапевтического эффекта.
Описанные здесь соединения-агенты доставки способствуют доставке бисфосфоната, особенно в пероральной форме, но также могут применяться в интраназальных, подъязычных, интрадуоденальных, подкожных, буккальных, внутрикишечных, ректальных, вагинальных, слизистых, легочных, чрезкожных, внутрикожных, парентеральных, внутривенных, внутримышечных и глазных системах.
Стандартные лекарственные формы также могут включать один или смеси наполнителей, разбавителей, разрыхлителей, смазывающих агентов, пластификаторов, красителей, вкусовых добавок, агентов, маскирующих вкус, сахаров, подсластителей, солей и дозирующих носителей, включая, но не ограничиваясь ими, воду, 1,2-пропандиол, этанол, оливковое масло, или любые их сочетания.
Соединения и композиции в соответствии с данным изобретением применяют для введения бисфосфонатов животным, включая, но не ограничиваясь ими, птиц, таких как куры; и млекопитающих, таких как грызуны, коровы, свиньи, собаки, кошки, приматы и, особенно, человек.
Система особенно полезна для доставки бисфосфонатов, которые, иначе, были бы разрушены или оказались менее эффективными под влиянием условий, с которыми бисфосфонаты сталкиваются до достижения цели (например, области, в которой бисфосфонаты должны выделяться) и внутри тела животного, которому они введены. Особенно соединения и композиции в соответствии с данным изобретением полезны для перорального введения бисфосфонатов, особенно тех, которые обычно не могут быть доставлены перорально, или тех, для которых желательно улучшение доставки.
Композиции в соответствии с данным изобретением применяются для доставки бисфосфонатов в выбранные биологические системы и для повышения и/или улучшения биодоступности бисфосфонатов по сравнению с введением бисфосфонатов в чистом виде. Доставки и/или биодоступность может быть повышена и/или улучшена доставкой большего количества бисфосфоната в определенный период времени, или доставкой большего количества бисфосфоната в течение определенного времени, или доставкой бисфосфоната в определенный момент времени (эффект быстрой или замедленной доставки) или доставкой бисфосфонатов в течение определенного периода времени (замедленное выделение).
Композиции в соответствии с данным изобретением могут вводиться для лечения и/или профилактики любых заболеваний, для которых бисфосфонаты являются известными агентами для лечения и/или профилактики. Обычно эффективное количество композиции вводят для лечения и/или профилактики желаемого заболевания.
Другим вариантом данного изобретения является способ лечения и/или профилактики заболеваний костей у животных введением композиции в соответствии с данным изобретением животному. Обычно эффективное количество композиции вводят для лечения и/или профилактики желаемого заболевания костей. Заболевания костей включают, но не ограничены ими, заболевания костей и болезненные состояния и включают, но не ограничены ими, остеопороз, дегенерацию костей, болезнь Педжета и/или функцию остеокласта (например, ингибирующие остеокласты).
Определенные показания для бисфосфонатов могут быть найдены в Physicians' Desk Reference (54th Ed., 2000, Medical Economics Company, Inc., Montvale, NJ), которая включена сюда в качестве ссылки.
Подходящее количество бисфосфоната и агента доставки может быть определено методами, известными в данной области техники.
После введения бисфосфонат попадает в кровеносную систему. Биодоступность бисфосфонатов рассчитывают исходя из их экскреции в моче или их поглощения костной тканью, согласно методам, применяемым в данной области техники.
Описание предпочтительных вариантов
Представленные ниже примеры иллюстрируют данное изобретение без ограничений. Все части даны как части масс., если не указано иначе.
Протонный ядерный магнитный резонанс (1Н ЯМР) анализ для перечисленных ниже соединений проводят на 300 МГц спектрометре Брукера с применением диметилсульфоксида (ДМСО-d6) в качестве растворителя, если не указано иначе.
Пример 1 - получение соединения
Получение соединения 1
Натрий N-салицилоил-8-аминокаприлат
Натриевая соль соединения 1 может быть получена способами, описанными в US 5650386, WO 00/46182 или WO 00/59863.
Получение соединения 2
10-(N-салицилоиламино)декановая кислота
Соединение 2 может быть получено способами, описанными в US 5866536, WO 00/46182 или WO 00/59863.
Получение соединения 3
9-(салицилоиламино)нонановая кислота
Соединение 3 может быть получено способами, описанными в US 5866536, WO 00/46182 или WO 00/59863 с применением соответствующих исходных материалов.
Получение соединения 4
Получение 2-(4-(N-салицилоил)аминофенил)пропионовой кислоты
Соединение 4 может быть получено следующим способом.
Суспензию 58,6 г (0,355 моль) 2-(4-аминофенил)пропионовой кислоты и 500 мл метиленхлорида обрабатывают 90,11 мл (77,13 г, 0,710 моль) триметилсилилхлорида и кипятят с обратным холодильником в течение 120 мин. Реакционную смесь охлаждают до температуры 0°С и обрабатывают 184,44 мл (107,77 г, 1,065 моль) триэтиламина. После перемешивания в течение 5 минут эту смесь обрабатывают раствором 70,45 г (0,355 моль) хлоридом О-ацетилсалицилоила и 150 мл метиленхлорида. Реакционную смесь нагревают до 25°С и перемешивают в течение 64 часов. Летучие вещества удаляют в вакууме. Остаток перемешивают в 2н водном гидроксиде натрия в течение 1 часа и подкисляют 2М водной серной кислотой. Твердое вещество дважды перекристаллизовывают из этанола/воды с получением рыжевато-коричневого твердого вещества. Выделение фильтрацией дает 53,05 г (52% выход) 2-(4-(N-салицилоил)аминофенил)пропионовой кислоты. Растворимость: 200 мг/мл (200 мг + 350 мкл 2н NaOH + 650 мкл Н2О, рН 7,67).
Элементный анализ: Рассчитано: С=67,36, Н=5,3, N=4,91.
Найдено: С=67,05, Н=5,25, N=4,72.
Получение натриевой соли соединения 4
Получение 2-(4-(N-салицилоил)аминофенил)пропионата натрия
Натриевая соль соединения 4 может быть получена следующим способом.
Раствор 53,05 г (0,186 моль) 2-(4-(N-салицилоил)аминофенил)пропионовой кислоты и 300 мл этанола обрабатывают 7,59 г (0,190 моль) NaOH, растворенного в 22 мл воды. Реакционную смесь перемешивают в течение 30 минут при температуре 25°С и в течение 30 минут при температуре 0°С. Полученное бледно-желтое твердое вещество выделяют фильтрацией с получением 52,61 г 2-(4-(N-салицилоил)аминофенил)пропионата натрия. Растворимость: 200 мг/мл, прозрачный раствор, рН 6,85.
Элементный анализ: Рассчитано: С=60,45, Н=5,45, N=3,92, Na=6.43.
Найдено: С=60,84, Н=5,87, N=3,85, Na=6.43.
Температура плавления 236-238°С.
Получение соединения 5
N-(6-Диметиламиногексил)салициламид
Соединение 5 может быть получено следующим способом.
Суспензию 18,02 г (110 ммоль) карсалама, 18,0 мл (15,84 г, 109 ммоль) 6-диметиламино-1-гексанола, 29,12 г (111 ммоль) трифенилфосфина и 150 мл тетрагидрофурана обрабатывают раствором 21,8 мл (22,39 г, 111 ммоль) диизопропилазодикарбоксилата и 40 мл тетрагидрофурана, добавляя по каплям в течение 20 минут, при этом температура суспензии возрастает до около 67°С. Реакционную смесь охлаждают до около 25°С и перемешивают в течение около 20 часов. Раствор обрабатывают 150 мл (300 ммоль) водного 2н гидроксида натрия и нагревают до температуры около 60°С в течение около 90 минут. Реакционную смесь промывают этилацетатом (2×60 мл). Водную фазу подкисляют 4% водной хлористоводородной кислотой до рН немного меньше, чем около 0, и промывают этилацетатом (2×60 мл). рН водной фазы повышают до около 4,5 50% водным карбонатом калия и промывают этилацетатом (2×60 мл). Водную фазу обрабатывают твердым бикарбонатом натрия и экстрагируют этилацетатом (14×60 мл). Объединенные 14 экстрактов этилацетата сушат над сульфатом натрия и концентрируют до вязкой жидкости. Жидкость помещают в минимальное количество этилацетата, разбавляют 100 мл гексана и обрабатывают на ледяной бане 150 мл гексана с образованием белого твердого вещества. 13,65 г N-(6-диметиламиногексил)салициламида выделяют фильтрацией.
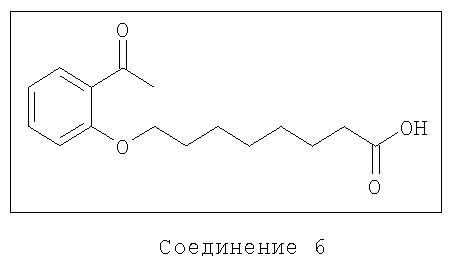
Получение соединения 6
8-(2-Ацетилфенокси)октановая кислота
Соединение 6 может быть получено следующим способом.
Гидроксид калия (10,72 г, 191,1 ммоль) измельчают в ступке до порошка, затем добавляют в 250 мл круглодонную колбу, содержащую 80 мл диметилсульфоксида. Полученную смесь перемешивают в течение 5 минут, затем добавляют 6,47 г (47,5 ммоль) 2-гидроксиацетофенона и сразу же добавляют 24,04 г (95,7 ммоль) этил 8-бромоктаноата. Реакционную смесь перемешивают при комнатной температуре в течение 1 часа. Оранжевую реакционную смесь выливают в 200 мл дистиллированной воды, затем пять раз экстрагируют 300 мл (всего) метиленхлорида. Органические слои промывают двумя порциями воды по 50 мл, затем концентрируют с получением ярко-желтой жидкости.
Жидкость растворяют в 25 мл диоксана. Добавляют водный гидроксид натрия (1н, 20 мл) и полученную жидкость перемешивают и нагревают (65°С) в течение 2 часов. Реакционную смесь охлаждают до 0°С, подкисляют до рН 1 концентрированной водной хлористоводородной кислотой, затем экстрагируют двумя порциями по 100 мл этилацетата. Органический слой концентрируют с получением ярко-желтого масла. Масло кристаллизуют в смеси метанол:вода (1:1), затем один раз перекристаллизовывают из смеси метанол:вода (1:1) и один раз из метиленхлорида:гексана (1:4) с получением 5,70 г (43,1%) бледно-желтого - не совсем белого твердого вещества.
Температура плавления 71,5-73,5°С.
Анализ сжиганием: %С: 69,04 (рассчитано), 68,77 (найдено); %Н: 7,97 (рассчитано), 8,04 (найдено).
1Н ЯМР (d6-ДМСО): δ 12,0, с, 1Н; 7,57, дд, 1Н; 7,52, дт, 1Н; 7,15, д, 1Н; 7,00, дт, 1Н; 4,09, т, 2Н; 2,52, с, 3Н; 2,20, т, 2Н; 1,78, п, 2Н; 1,46, м, 4Н; 1,32, м, 4Н.
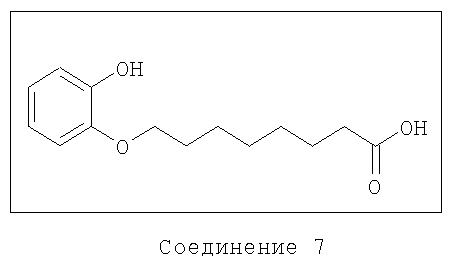
Получение соединения 7
8-(2-Гидроксифенокси)октановая кислота
Соединение 7 может быть получено следующим способом.
В 200 мл круглодонную колбу загружают 22,9 (3 экв.) свежеизмельченного гидроксида калия и 100 мл диметилсульфоксида. Эту смесь перемешивают при температуре 25°С в течение 5 минут. Добавляют катехол (15 г, 1 экв.) с последующим немедленным добавлением этил 8-бромоктаноата (34,2 г, 1 экв.). Полученный темно-коричневый раствор перемешивают при температуре 25°С в течение 2 часов.
Добавляют дистиллированную воду (100 мл) и полученный раствор нагревают до 85°С в течение 2 часов. Смесь охлаждают, подкисляют до рН ˜2 концентрированной водной хлористоводородной кислотой и экстрагируют этилацетатом (300 мл×2). Объединенные органические слои сушат над сульфатом магния, фильтруют и растворитель выпаривают. Неочищенный продукт очищают хроматографией на колонке с силикагелем с применением 30-60% этилацетата/гексана в качестве элюента. Желаемый продукт собирают и сушат с получением 6,6 г (19%) 8-(2-гидроксифенокси)октановой кислоты в виде не совсем белого твердого вещества.
Температура плавления 60-64°С.
Анализ сжиганием: %С: 66,65 (рассчитано), 66,65 (найдено); %Н: 7,99 (рассчитано), 8,10 (найдено).
1Н ЯМР (d6-ДМСО): δ 12,0, с, 1Н; 8,8, с, 1Н; 6,90-6,86, м, 1Н; 6,80-6,76, м, 3Н; 3,92, т, 2Н; 2,21, т, 2Н; 1,75-1,66, м, 2Н; 1,56-1,29, м, 8Н.
Альтернативный способ получения соединения 7
В 500 мл колбу Эрленмейера загружают 28 г (4 экв.) порошкообразного гидроксида калия и 400 мл диметилсульфоксида. Эту смесь перемешивают при комнатной температуре в течение 5 минут. Добавляют 2-бензилоксифенол (25 г, 1 экв.) и сразу же добавляют этил 8-бромоктаноат (37,6 г, 1,2 экв.). Полученный раствор перемешивают при комнатной температуре в течение 2 часов.
Реакционную смесь выливают в 200 мл дистиллированной воды и нагревают до температуры 80°С в течение 3 часов. Затем смесь подкисляют концентрированной водной хлористоводородной кислотой до рН приблизительно 2. Оседает беловатое твердое вещество. Полученное твердое вещество выделяют вакуумной фильтрацией и сушат в течение ночи при комнатной температуре в вакууме. Затем продукт этерифицируют взаимодействием неочищенной кислоты с 1 л метанола и 5 мл серной кислоты и последующим нагреванием до температуры 80°С в течение ночи. Смесь охлаждают и экстрагируют этилацетатом 3×400 мл, сушат над сульфатом магния, фильтруют и выпаривают с получением метилового эфира с количественным выходом.
Неочищенный эфир растворяют с 150 мл этанола и смешивают с 1 г 10% палладия на активированном угле. Полученную смесь помещают в автоклав Парра. Затем реакционный сосуд подвергают давлению водорода 200 фунт/кв.дюйм. Гетерогенную смесь перемешивают при температуре 50°С в течение 18 часов. Палладий отфильтровывают и фильтрат концентрируют с получением дебензилированного продукта.
Метиловый эфир омыляют 10 г гидроксида натрия, 400 мл метанола и 50 мл воды. Раствор нагревают до температуры 80°С в течение 1 часа, затем перемешивают при температуре окружающей среды в течение ночи. Метанол выпаривают. Добавляют 100 мл воды и водный слой подкисляют концентрированной водой хлористоводородной кислотой до рН 2. Водную фазу экстрагируют этилацетатом, 3×100 мл, сушат и выпаривают с получением целевого продукта. Неочищенный продукт затем очищают хроматографией на колонке с силикагелем с применением 30-60% этилацетата/гексана в качестве элюента с получением 22,24 г (71%) 8-(2-гидроксифенокси)октановой кислоты в виде не совсем белого твердого вещества.
Температура плавления 65-68°С.
Анализ сжиганием: %С: 66,65 (рассчитано), 66,98 (найдено); %Н: 7,99 (рассчитано), 8,22 (найдено).
1Н ЯМР (d6-ДМСО): δ 12,0, с, 1Н; 8,8, с, 1Н; 6,90-6,86, м, 1Н; 6,80-6,67, м, 3Н; 3,94, т, 2Н; 2,23, т, 2Н; 1,73, п, 2Н; 1,53-1,29, м, 8Н.
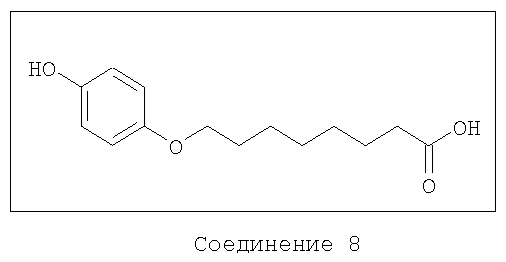
Получение соединения 8
4-Гидроксифенил-8-оксиоктановая кислота
Соединение 8 получают следующим способом.
Гидроксид калия (11,20 г, 200,0 ммоль) измельчают в ступке до порошка, затем добавляют в 0,5 л круглодонную колбу, содержащую 90 мл ДМСО. Полученную смесь перемешивают в течение 5 минут, затем добавляют 10,00 г (50,0 ммоль) 4-бензилоксифенола, и сразу же добавляют 12,55 г (50,0 ммоль) этил 8-бромоктаноата. Реакционную смесь перемешивают при комнатной температуре в течение двух с половиной часов. Реакционную смесь выливают в 200 мл дистиллированной воды и кипятят с обратным холодильником. Кипячение продолжают в течение трех с половиной часов. Затем кипячение реакционной смеси прерывают и реакционную смесь охлаждают до комнатной температуры в течение ночи. На следующий день снова начинают нагревание, если обнаружится, что гидролиз не закончен. После дополнительного нагревания в течение трех часов определяют завершение реакции и нагревание прекращают. Когда реакционная смесь охладится до комнатной температуры, ее подкисляют 2н раствором HCl, и полученное твердое вещество выделяют фильтрацией. Твердое вещество сушат в вакууме в течение ночи. Выделяют 17,96 г 4-бензилоксифенил-8-оксиоктановой кислоты.
Этот продукт используют на следующей стадии. 4-Бензилоксифенил-8-октановую кислоту помещают в 0,5 л круглодонную колбу с 120 мл этилового спирта. Смесь обрабатывают азотом в течение 15 минут, затем к реакционной смеси добавляют 10% палладий на активированном угле. Затем в колбе создают вакуум и содержащий водород баллон помещают сверху колбы таким образом, чтобы содержимое колбы было под водородом. Полученную смесь перемешивают в течение ночи при комнатной температуре и затем фильтруют через целит. Этиловый спирт удаляют в вакууме с получением белого твердого вещества, которое сначала перекристаллизовывают из смеси 90:10 этиловый спирт:вода и затем растворяют в 2н NaOH. Полученную смесь фильтруют и подкисляют 2н HCl. Полученное белое твердое вещество выделяют фильтрацией и сушат в вакууме. Выделяют 2,12 г 4-гидроксифенил-8-оксиоктановой кислоты.
Температура плавления 97-100°С.
Анализ сжиганием: %С: 66,67 (рассчитано), 66,43 (найдено); %Н: 7,94 (рассчитано), 7,80 (найдено).
1Н ЯМР (d6-ДМСО): δ 12,0, с, 1Н; 9,00, с, 1Н; 6,63, м, 4Н; 3,75, т, 2Н; 2,15, т, 2Н; 1,60, п, 2Н; 1,45, п, 2Н; 1,20, м, 6Н.
Получение соединения 10
N-(5-хлорсалицилоил)-8-аминокаприлат
Динатриевую соль соединения 10 получают способами, описанными в WO 00/59863.
Пример 2
Пероральная доставка бисфосфоната
Получают пероральные дозированные (ПО) композиции соединения-агента доставки и алендроната (безводный, мононатриевая соль) в воде. Обычно 400 мг соединения-агента доставки добавляют к 2,0 мл воды. Если соединение-агент доставки имеет на конце группу карбоновой кислоты, применяют натриевую соль соединения или свободную кислоту превращают в натриевую соль перемешиванием полученного раствора и добавлением одного эквивалента гидроксида натрия (10,0н) и разбавлением водой. Раствор перемешивают, затем нагревают (около 37°С) и обрабатывают ультразвуком. рН доводят до около 7 (7,0-8,5) добавлением NaOH или HCl. Добавляют еще NaOH (для агентов доставки с группой карбоновой кислоты на конце) или HCl (для соединений с аминогруппой на конце), если необходимо достигнуть однородной растворимости, и повторно доводят рН. Затем добавляют воду до общего объема около 2,5 мл (количество зависит от растворимости соединения агента-доставки). Алендронат (25 мкл) из исходного раствора (полученного из 2,0 г алендроната натрия в 10 мл деионизированной воды, рН доведен до около 7,5 добавлением 10н NaOH, перемешанного и обработанного ультразвуком при температуре 37°С с получением прозрачного раствора, замороженного и размороженного перед применением) добавляют к раствору. Конечные дозы составляют 200 мг/кг соединения-агента доставки (т.е. 200 мг соединения агента-доставки на 1 кг веса тела) и 2,5 мг/кг алендроната, и объем дозы составляет 1,0 мл/кг.
Типовые протоколы дозирования и отбора образцов следующие. Самцов крыс Sprague-Dawley, весящих 200-250 г, заставляют голодать в течение 24 часов перед дозированием. Для экспериментов, в которых дозирование проводится на не голодающих крысах, животным дают свободный доступ к пище и воде. Группе из пяти животных, предназначенной для дозирования, вводят один из растворов дозы. Для перорального дозирования 11 см катетер Rusch 8 French прикрепляют к 1 мл шприцу с пипеткой на конце. Шприц наполняют раствором дозы, пропуская раствор через катетер, который затем протирают досуха. Катетер помещают в пищевод, оставляя 1 см трубки после резцов. Раствор вводят нажатием поршня шприца.
После дозирования животных поодиночке помещают в герметичные обменные камеры. Пищу дают через 45 минут после дозирования. Воду дают в неограниченном количестве. Сбор мочи начинают сразу же после помещения животных в камеры. Образцы мочи отбирают через 14 часов после дозирования. Образцы хранят на сухом льду до начала отбора образцов. Количественную оценку проводят методом ВЭЖХ для алендроната.
В качестве контроля, 0,1 мг/кг алендроната (из 2 мл стерильного раствора в воде, полученного из 120 мкл раствора, полученного из: 3,33 мг алендроната натрия, 4,91 мг хлорида натрия, кристаллы USP реагента; 10,3 мг цитрата натрия USP, 2,88 мг лимонной кислоты USP в 10 мл деионизированной воды, рН около 5,0) внутривенно вводят через хвостовую вену без анестезии. Образцы мочи отбирают, как описано выше. Результаты показаны в таблице 1. ALN - алендронат.
Эффективность пероральной доставки алендроната
*[ALN] в общем количестве мочи, выделенной в течение 14 часов после дозирования
Примечание: доза агента доставки составляет 200 мг/кг
Все животные голодали в течение 24 часов.
Реакция на пероральную дозу: алендронат и соединение 1
+[ALN] в нг/мл общем количестве мочи, выделенной в течение 14 часов после дозирования
Все животные голодали в течение 24 часов.
Реакция на пероральную дозу: алендронат и соединение 10
Все животные голодали в течение 24 часов.
Пероральное введение алендроната: эффект голодания
Реакция на дозу агента доставки: алендронат и соединение 10
Все животные голодали в течение 24 часов.
Указанные выше патенты, заявки, методы тестирования и публикации включены в данное описание в качестве ссылок в полном объеме.
На основе представленного выше подробного описания специалист в данной области техники может осуществить множество вариаций данного изобретения. Все такие очевидные вариации включены в объем данного изобретения и формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ ИНДОЛЫ, ПРОТИВОВИРУСНЫЙ АКТИВНЫЙ КОМПОНЕНТ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2436786C1 |
| АРИЛ- И ГЕТЕРОАРИЛЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ МОЧЕВИНЫ, СПОСОБ ИНГИБИРОВАНИЯ КИНАЗЫ RAF И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2265597C2 |
| СПОСОБ ПОДАВЛЕНИЯ РОСТА ОПУХОЛЕВЫХ КЛЕТОК, ОПОСРЕДОВАННОГО КИНАЗОЙ RAF, ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ МОЧЕВИНЫ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 1998 |
|
RU2232015C2 |
| СОСТАВЫ И СМЕСИ ДЛЯ ДОСТАВКИ АКТИВНЫХ АГЕНТОВ | 2005 |
|
RU2403237C2 |
| ПРОИЗВОДНОЕ 1,3,5-ТРИАЗИНА И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2724333C2 |
| ТАКСАНЫ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СПОСОБЫ ИНГИБИРОВАНИЯ | 2001 |
|
RU2265019C2 |
| СПОСОБ ИНГИБИРОВАНИЯ ОСТЕОПОРОЗА, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ ДЛЯ ИНГИБИРОВАНИЯ ОСТЕОПОРОЗА | 1995 |
|
RU2149631C1 |
| Необязательно конденсированные гетероциклилзамещенные производные пиримидина, пригодные для лечения воспалительных, метаболических, онкологических и аутоиммунных заболеваний | 2015 |
|
RU2734261C2 |
| СПОСОБ ВВЕДЕНИЯ БИСФОСФОНАТОВ | 2001 |
|
RU2288722C2 |
| Необязательно конденсированные гетероциклил-замещенные производные пиримидина, пригодные для лечения воспалительных, метаболических, онкологических и аутоиммунных заболеваний | 2015 |
|
RU2719422C2 |
Настоящее изобретение относится к композициям для доставки бисфосфонатов к цели. Техническая задача - разработка простых и недорогих композиций для доставки бисфосфонатов. Предложены варианты композиций, содержащих по меньшей мере один бисфосфонат и по меньшей мере одно соединение - агент доставки. Предложенные композиции способствуют доставке бисфосфонатов к выбранным биологическим системам и улучшают биодоступность бисфосфонатов по сравнению с введением без соединения - агента доставки. Предложен также способ получения заявленной композиции, стандартная лекарственная форма с использованием заявленной композиции и способ введения бисфосфонатов животному. 6 н. и 42 з.п. ф-лы, 5 табл.
(A) по меньшей мере один бисфосфонат и
(B) по меньшей мере одно соединение А
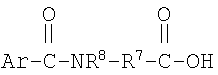
где Ar является фенилом или нафтилом, который замещен ОН-группой во 2-ом положении и дополнительно может иметь заместитель, выбранный из группы, включающей ОН, галоген, С1-C4алкил, С1-C4алкенил, С1-C4алкокси или С1-C4галоалкокси;
R7 выбирают из группы, включающей C4-C20алкил, фенил, (С1-С10алкил)фенил, (С1-С10алкенил)нафтил, фенил(С1-С10алкил), или
R8 выбирают из группы, включающей водород, С1-C4алкил, C2-C4алкенил, С1-C4алкокси, С1-C4галоалкокси;
R7 необязательно замещен С1-C4алкилом, C2-C4алкенилом, С1-C4алкокси, С1-C4 галоалкокси, -ОН, -SH и -CO2R9 или любым их сочетанием;
R9 является водородом, С1-C4алкилом или C2-C4алкенилом,
R7 возможно имеет гетероатом, выбранный из группы, включающей кислород, азот, серу или любое их сочетание,
при условии, что соединения не замещены аминогруппой в положении альфа по отношению к кислотной группе или их соли,
или его соль.
(A) по меньшей мере один бисфосфонат и
(B) по меньшей мере одно соединение В
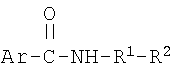
где Ar является фенилом или нафтилом, который замещен ОН-группой во 2-ом положении и дополнительно может иметь заместитель, выбранный из группы, включающей С1-C4алкил, С1-C4алкокси, C2-C4алкенил, C2-C4алкинил, арил, арилокси, гетероциклическое кольцо, C5-С7карбоциклическое кольцо, галоген, -ОН, -SH, CO2R6, -NR7R8 или -N+R7R8R9Y-;
(а) R1 является С1-C16алкиленом;
R2 является -NR3R4 или - N+R7R8R9Y-;
R3 и R4 независимо являются водородом; кислородом; гидрокси;
замещенным или незамещенным С1-C16алкилом; замещенным или незамещенным C2-C16алкенилом; замещенным или незамещенным C2-C16алкинилом; замещенным или незамещенным арилом; замещенным или незамещенным алкилкарбонилом; замещенным или незамещенным арилкарбонилом; замещенным или незамещенным алкансульфинилом; замещенным или незамещенным арилсульфинилом; замещенным или незамещенным алкансульфонилом; замещенным или незамещенным арилсульфонилом; замещенным или незамещенным алкоксикарбонилом; замещенным или незамещенным арилоксикарбонилом;
R5 независимо является водородом; замещенным или незамещенным С1-C16алкилом; замещенным или незамещенным C2-C16алкенилом; замещенным или незамещенным C2-C16алкинилом; замещенным или незамещенным арилом; замещенным или незамещенным алкилкарбонилом; замещенным или незамещенным арилкарбонилом; замещенным или незамещенным алкансульфинилом; замещенным или незамещенным арилсульфинилом; замещенным или незамещенным алкансульфонилом; замещенным или незамещенным арилсульфонилом; замещенным или незамещенным алкоксикарбонилом; замещенным или незамещенным арилоксикарбонилом;
(b) R1, R2 и R5 такие, как определены выше; и
R3 и R4 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца; или 5-, 6- или 7-членного гетероциклического кольца, замещенного С1-C6алкилом, С1-C6алкокси, арилом, арилокси, оксогруппой или карбоциклическим кольцом; или
(c) R2 и R5 такие как определены выше; и
R1 и R3 объединены с образованием 5-, 6- или 7-членного гетероциклического кольца; или 5-, 6- или 7-членного гетероциклического кольца, замещенного С1-C6алкилом, алкокси, арилом, арилокси или оксогруппой или карбоциклического кольца;
R4 является водородом; кислородом; гидрокси; замещенным или незамещенным С1-C16алкилом; замещенным или незамещенным C2-C16алкенилом; замещенным или незамещенным C2-C16алкинилом; замещенным или незамещенным арилом; замещенным или незамещенным алкилкарбонилом; замещенным или незамещенным арилкарбонилом; замещенным или незамещенным алкансульфинилом; замещенным или незамещенным арилсульфинилом; замещенным или незамещенным алкансульфонилом; замещенным или незамещенным арилсульфонилом; замещенным или незамещенным алкоксикарбонилом; замещенным или незамещенным арилоксикарбонилом;
R6 является водородом; С1-C4алкилом; С1-C4алкилом, замещенным галогеном или -ОН; C2-C4алкенилом; или C2-C4алкенилом, замещенным галогеном или -ОН;
R7, R8 и R9 независимо являются водородом; кислородом; С1-C4алкилом; С1-C4алкилом, замещенным галогеном или -ОН; C2-C4алкенилом; или C2-C4алкенилом, замещенным галогеном или -ОН; и
Y является галогеном, гидрокси, сульфатом, нитратом, фосфатом, алкокси, перхлоратом, тетрафторборатом или карбоксилатом,
или его соль.
(A) по меньшей мере один бисфосфонат и
(B) по меньшей мере одно соединение С
Ar-O-R11-COOH
где Ar представляет собой фенил или нафтил, имеющий по меньшей мере один заместитель, выбранный из ОН или кетогруппы;
R11 является С1-С10алкилом.
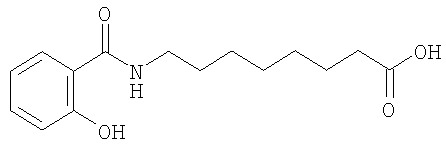
или его соль.
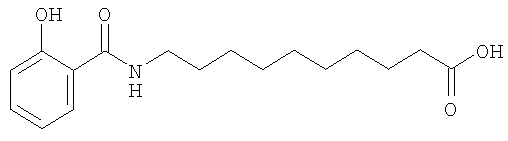
или его соль.
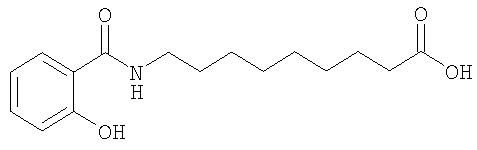
или его соль.
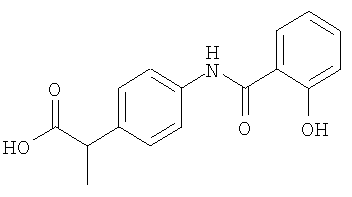
или его соль.
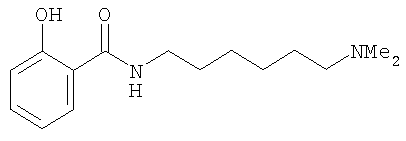
или его соль.
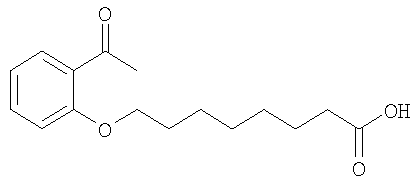
или его соль.
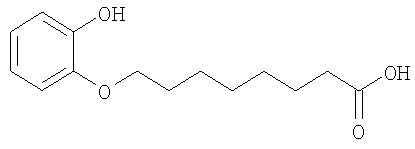
или его соль.
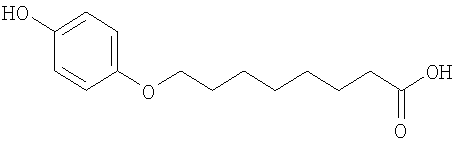
или его соль.
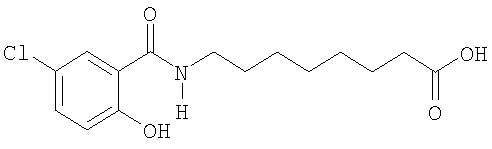
или его соль.
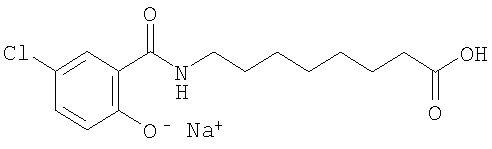
или его соль.
(A) композицию по любому из пп.1, 2 и 9-36; и
(B) (а) наполнитель,
(b) разбавитель,
(c) разрыхлитель,
(d) смазывающий агент,
(e) пластификатор,
(f) краситель,
(g) дозирующий носитель или (h) любое их сочетание.
(A) по меньшей мере, одного бисфосфоната;
(B) соединения, выбранного из соединений 1-9 и их солей; и
(C) необязательно, дозирующего носителя.
| US 5866536 А, 02.02.1999 | |||
| US 5650386 А, 22.07.1997 | |||
| СПОСОБ ИНГИБИРОВАНИЯ ОСТЕОПОРОЗА, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ ДЛЯ ИНГИБИРОВАНИЯ ОСТЕОПОРОЗА | 1995 |
|
RU2149631C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНОЛСУЛЬФОНАТНЫХ СЛОЖНЫХ ЭФИРОВ ГИДРОКАРБОИЛАМИНОКИСЛОТ | 1996 |
|
RU2158256C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛАЛКАНАМИДА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И СЕЛЬСКОХОЗЯЙСТВЕННЫЙ ИЛИ САДОВЫЙ ФУНГИЦИД | 1996 |
|
RU2156235C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 1993 |
|
RU2116074C1 |
Авторы
Даты
2007-11-10—Публикация
2002-03-01—Подача