Настоящее изобретение относится к применению гидроксиолеиновой (2-гидроксиолеиновой) кислоты и молекул аналогичной структуры в качестве противоопухолевых агентов, в качестве агентов с гипотензивной активностью и в качестве агентов для стимулирования снижения веса тела.
Настоящее изобретение также относится к применению 2-гидроксиолеиновой кислоты и аналогичных соединений для регулирования мембранной структуры, регулирования активности и/или локализации G-белков и регулирования активности рецепторов, связанных с G-белками, за счет регулирования мембранной структуры.
Настоящее изобретение также относится к применению 2-гидроксиолеиновой кислоты и аналогичных соединений для производства лекарственных средств, предназначенных для лечения рака, лекарственных средств для лечения сердечно-сосудистых заболеваний и лекарственных средств для лечения проблем, связанных с весом тела и ожирением.
Жирные кислоты представляют собой молекулы широкого применения как в продуктах питания, так и в промышленности. 2-Гидроксиолеиновая кислота, синтез которой описан ранее (Adam et al., 1998, Eur. J. Org. Chem., 9, 2013-2018), используется в промышленности в качестве эмульгатора при приготовлении косметических средств.
Например, с одной стороны, патент JP 10182338 относится к эмульгирующей композиции масло-в-воде, которая проявляет низкую раздражающую способность и высокую совместимость с солями, которая содержит: [A] неионногенные поверхностно-активные вещества, такие как монолаурат полиоксиэтиленсорбита, моноолеат полиоксиэтиленсорбита и моностеарат полиоксиэтиленсорбита, [В] 2-гидрокси-С10-С22-жирные кислоты, такие как 2-гидроксистеариновая кислота, [C] масла и [D] воду, где отношение А/В находится в интервале от 1:0,01 до 1:2.
Патент JP 09110635 также относится к композициям, которые могут быть использованы в качестве фармацевтических продуктов, косметических средств и пищевых продуктов и содержат: [A] сложные эфиры полиглицерина и жирных кислот, [В] 2-гидрокси-С10-С22-жирные кислоты, [C] масла и [D] воду, где массовое отношение А/С и В/С составляет 2,0 и 0,5 соответственно, а средний размер частиц находится в интервале от 10 до 300 нм. Эти композиции проявляют хорошую стабильность даже в кислых условиях или при низкой вязкости или в присутствии повышенных количеств солей, а следовательно совместимы с кожей.
С другой стороны, такая жирная кислота также используется в качестве ингибитора олеамидгидролазы, и оказывает снотворное действие (патент США 6096784 и WO 9749667).
Например, патент США 6096784 относится к разработке и синтезу ингибиторов олеамидгидролазы, отвечающей за гидролиз вызывающих сон липидов (цис-9-октадеценамид). Большинство эффективных ингибиторов имеет электрофильную карбонильную группу, способную обратимо образовывать (тио)полуацеталь или (тио)полуацеталь для имитации переходного состояния реакции, катализируемой протеазой цистеинового или серинового типа. Помимо ингибирующей активности некоторые ингибиторы проявляют агонистическую активность, которая вызывает сон у лабораторных животных.
Гексагональные мембранные структуры
Мембранные липиды способны сами распределяться в большее число вторичных структур, чем протеины и нуклеиновые кислоты. Обычный липидный бислой биологических мембран представляет собой как раз одну из таких вторичных конфигураций. Известно немного относительно распространенности и роли других вторичных структур в живых клетках. Одна из функций этих структур описана в предыдущей работе заявителей: повышение сродства к связыванию G-белков с мембранами (Escriba PV., Ozaita A., Ribas С., Miralles A., Fodor E., Farkas and Garcia-Sevilla JA; 1997 Proceedinds of National Academy of Sciences of USA 94, 11375-11380).
Концепция мембранной структуры выходит далеко за рамки концепции, описанной в некоторых патентах данной области техники (WO 87/04926 и WO 89/11286), в которых упоминается только текучесть мембран, и концепция распространяется на много более широкую область: мембранная структура. Молекулы, охватываемые патентом заявителя, действуют на перемещение или переход от ламеллярной к гексагональной структуре (Фиг.1).
Рассмотрение известного уровня техники показывает, что в данной области техники нет других заявок, связанных с 2-гидроксиолеиновой кислотой или подобными соединениями, которые представляли бы конкретный интерес при лечении рака, сердечно-сосудистых заболеваний и/или регулировании веса тела.
Имеются только описания диетических продуктов (GB 2140668, EP 0611568 и WO 02/0042) или экстрактов из культур M.cryophilus (WO 89/11286), состоящих из сложных смесей различных соединений, которые включают некоторые из соединений, описанных в изобретении, такие как жирные кислоты, в особенности, например, олеиновая и пальмитоолеиновая кислоты, и применения этих смесей при лечении артериальной гипертонии, для борьбы с ожирением или в качестве противоопухолевых агентов, но без приписывания любому из компонентов смеси, рассматриваемых в настоящем изобретении, конкретной роли в указанном терапевтическом действии. Только публикации WO 02/051406 и WO 94/01100 описывают применение некоторых жирных кислот (С14-С20) при лечении рака простаты, который не является объектом настоящего изобретения, исключительно при использовании указанных жирных кислот, описанных при рассмотрении уровня техники.
Задачей настоящего изобретения является новое применение 2-гидроксиолеиновой кислоты и аналогичных соединений, которое не связано с применением, описанным в предшествующем уровне техники.
Первая задача настоящего изобретения состоит в том, чтобы показать, что 2-гидроксиолеиновая кислота и ее аналоги обладают активностью, позволяющей использовать ее в качестве противоопухолевых агентов.
Вторая задача настоящего изобретения состоит в том, чтобы показать, что 2-гидроксиолеиновая кислота и ее аналоги обладают активностью, позволяющей использовать ее в качестве гипотензивных агентов.
Третья задача настоящего изобретения состоит в том, чтобы показать, что 2-гидроксиолеиновая кислота и ее аналоги обладают активностью, позволяющей использовать ее в качестве агентов, которые стимулируют снижение веса тела.
Четвертая задача настоящего изобретения состоит в том, чтобы показать, что 2-гидроксиолеиновая кислота и ее аналоги находят применение в качестве агентов, регулирующих переход от ламеллярной к гексагональной структуре клеточных мембран. Такое регулирование структуры мембраны оказывает влияние на активность G-белков, а также на молекулярную природу пути их трансдукции, то есть их путь распространения сигналов. Большое количество лекарственных средств действует на рецепторы, связанные с G-белками, за счет прямого взаимодействия с молекулами этого типа или за счет механизмов, связанных с клеточными сигналами, которые определяются их активностью. 2-Гидроксиолеиновая кислота и ее аналоги, однако, действуют на структуру мембраны.
Описанные ниже варианты применения 2-гидроксиолеиновой кислоты и ее аналогов ранее не упоминались, и их применение может оказаться полезным для лечения некоторых патологий. В частности, установлено, что 2-гидроксиолеиновая кислота и ее аналоги проявляют противоопухолевую активность, гипотензивную (или снижающую артериальное давление) активность и стимулируют снижение веса тела.
В настоящем изобретении новые применения 2-гидроксиолеиновой кислоты и ее аналогов подтверждены путем использования экспериментальных моделей, в особенности систем анализа in vitro, систем клеточных культур или живых организмов. Все эти модели анализа несомненно показывают, что 2-гидроксиолеиновая кислота и ее аналоги представляют собой молекулы, которые могут быть использованы при изготовлении лекарственных средств для лечения рака, для лечения сердечно-сосудистых заболеваний и для лечения людей с проблемами веса тела и ожирением, а также других заболеваний или состояний недостаточности на основе регулирования сигналов, связанных с G-белками, опосредуемых переходом мембранной структуры от ламеллярной к гексагональной.
Описание изобретения
В настоящем изобретении определение «2-гидроксиолеиновая кислота» означает α-гидроксиолеиновую кислоту, октадеценовую кислоту С18:1 цис Δ9 или цис-2-гидрокси-9-октадеценовую кислоту. Определение «аналоги» означает такие жирные кислоты, которые имеют двойную связь, перемещенную на одну или две позиции от центральной зоны, и/или которые имеют двойную связь, перемещенную на одну-пять позиций от центральной зоны, и/или имеют на от одного до шести атомов углерода (СН2-группы) больше или меньше на каждой стороне двойной связи, и/или которые имеют остаток (R) в положении 2, отличный от ОН, с небольшой атомной массой (Мw меньше или равна 200 Da). Неважно, имеет ли стереоизомер, соответствующий проекции группы R, R- или S-конфигурацию. Что касается различных испытанных молекул, то установлено, что молекулы, которые имеют общие формулы, представленные ниже, проявляют некоторые эффекты, аналогичные эффектам гидроксиолеиновой кислоты, и поэтому могут быть определены как ее аналоги.
Общая формула I: COOH-CHR-(CH2)m-СН=СН-(СН2)n-CH3, в которой m и n независимо друг от друга имеют значения 0-15, а R может представлять собой Н, ОН, NH2, CH3 или некоторые другие остатки с молекулярной массой ниже 200 Da.
В настоящем изобретении определение «G-белки» означает белки, которые представляют собой белки, связывающие гуанин-нуклеотиды, образованные из трех субъединиц (одна альфа, одна бета и одна гамма), которые передают сигналы от рецепторов, связанных с G-белками, к эффекторам (аденилилциклазе, гуанилилциклазе, фосфолипазе С, ионным каналам и др.).
В настоящем изобретении определение «мембранная структура» означает вторичную структуру или расположение липидов в природных или синтетических мембранах (липосомах).
В настоящем изобретении определение «острый эффект» означает эффект, который продуцируется в интервале времени от минут до нескольких часов после однократного введения лекарственного средства.
В настоящем изобретении определение «хронический эффект» означает эффект, который продуцируется в интервале времени от нескольких дней до нескольких недель постоянного введения лекарственного средства.
В настоящем изобретении определение «фармацевтически приемлемые формы» означает любую из форм, обычно используемую в данной области, включая, но без ограничения: сложные эфиры, в особенности этиловые эфиры, благодаря их свойствам как солюбилизаторов жирных кислот, простые эфиры, амиды, соли и др.
Одним из объектов настоящего изобретения является применение 2-гидроксиолеиновой кислоты и ее аналогов для регулирования перехода от ламеллярной к гексагональной структуре клеточных мембран. Молекулярная основа этого явления лежит во взаимодействии 2-гидроксиолеиновой кислоты и ее аналогов с мембранами и в модуляции мембранной композиции и/или структуры (таблицы 1 и 2).
Влияние связывания 2-гидроксиолеиновой кислоты на температуру перехода от ламеллярной к гексагональной структуре (НII)
40:1
20:1
10:1
54
48
41
В таблице 1 представлены значения температуры перехода от ламеллярной к гексагональной структуре в мембранах диэлаидоил-фосфатидилэтаноламина (ДЭФЭ, DEPE). Контрольное значение (в отсутствие 2-гидроксиолеиновой кислоты) равно 63°С. Понижение (с концентрационной зависимостью), вызываемое 2-гидроксиолеиновой кислотой (2ОНОК), показывает, что эта молекула стабилизирована в присутствии неламеллярных структур. Эта важная модификация клеточной мембраны имеет значимые последствия для молекулярной и клеточной функции. Все аналоги 2-гидроксиолеиновой кислоты, которые имеют терапевтическую активность, также индуцируют эффекты на мембранной структуре (таблица 2).
Влияние различных аналогов гидроксиолеиновой кислоты (фосфолипид:аналог, 20:1, моль:моль) на ламеллярный-гексагональный переход фосфолипида диэлаидоилфосфатидилэтаноламина (ДЭФЭ)
Олеиновая кислота
Аминоолеиновая кислота
Метилолеиновая кислота
цис-Вакценовая кислота
Нервоновая кислота
45
49
50
53
55
Модуляция перехода от ламеллярной к неламеллярной структуре регулирует активность G-белков.
Гидроксиолеиновая кислота и родственные соединения способны модулировать активность G-белков, которую измеряют с помощью связывания [35S]GTPγS (Фиг.5).
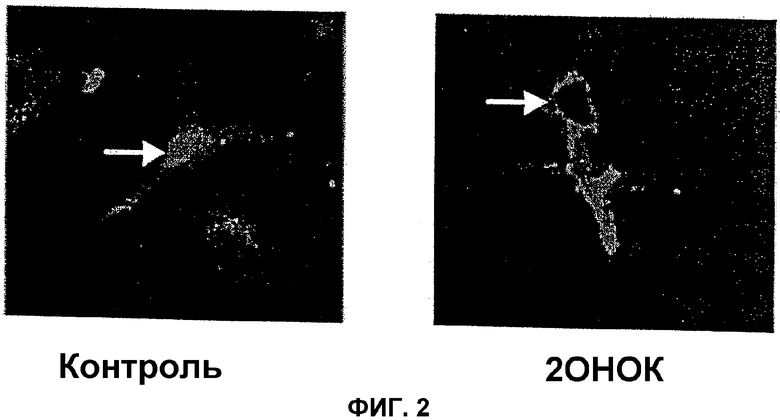
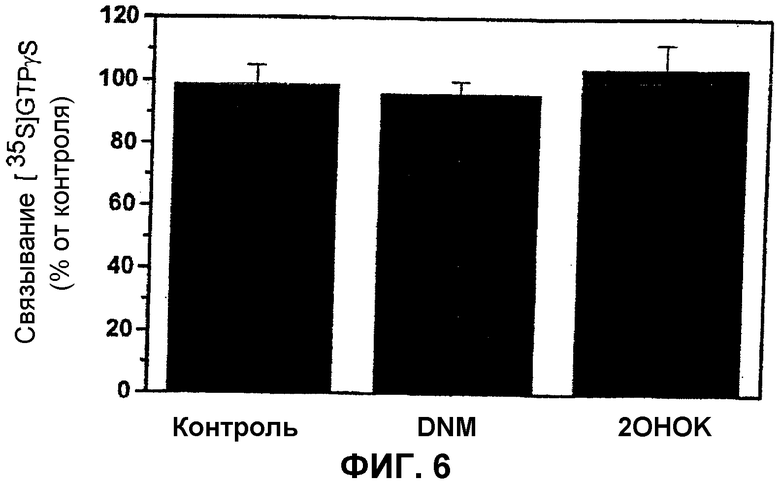
Это происходит, так как эти молекулы оказывают влияние на взаимодействие G-белков с мембранами и, следовательно, на их клеточную локализацию, как это показано на фотографиях конфокальной микроскопии (Фиг.2). Влияние гидроксиолеиновой кислоты и ее аналогов на локализацию и активность G-белков не обусловлено прямым воздействием на них. Фиг.6 иллюстрирует влияние, которое эти молекулы оказывают на активность очищенных G-белков в отсутствие мембраны. В отличие от того, что происходит, когда G-белки связаны с мембранами, дауномицин (DNM) и гидроксиолеиновая кислота (2ОНОК), а также аналоги последней, не оказывают влияния на активность этих белков (которые активированы только тогда, когда они находятся в мембранах в контакте с рецепторами, связанными с G-белками).
Рецепторы, связанные с G-белками, распространены повсеместно, составляя до 80% мембранных рецепторов, которые передают сигналы, инициируемые нейротрансмиттерами, гормонами, нейромодуляторами, цитокинами, факторами роста и др. Наряду с другими физиологическими процессами они регулируют кровяное давление, рост и пролиферацию клеток, а также вес тела. Таким образом, молекулы, описанные в этом изобретении, могут регулировать упомянутые выше процессы.
Испытания на мембранной структуре
Наиболее эффективной и сильной методикой для исследования мембранной структуры является дифракция/рассеивание рентгеновских лучей. С использованием этой методики установлено, что структура мембран меняется с помощью 2-гидроксиолеиновой кислоты и ее аналогов. Понижение температуры перехода от ламеллярной к гексагональной структуре указывает на важный эффект распределения липидных молекул в мембране. Такое регулирование распределения составляет основу для эффекта, оказываемого 2-гидроксиолеиновой кислотой и ее аналогами. Все изученные аналоги, которые согласуются с общей формулой, обладают активностью в отношении модуляции мембраны и регулирования клеточной пролиферации (эффективность при раке), кровяного давления (эффективность при сердечно-сосудистых процессах) и веса тела (эффективность при ожирении).
- Задачей настоящего изобретения является демонстрация того, что 2-гидроксиолеиновая кислота и ее аналоги обладают активностью в качестве противоопухолевых агентов.
Во-первых, клеточный цикл регулируется факторами роста, которые связываются со специфическими рецепторами на поверхности клеток. Связывание указанных факторов роста с рецепторами вызывает каскад реакций, которые предназначены для активации митогенных киназ (cdk), которые образуют димерный комплекс с белками, связанными с клеточным циклом, называемыми циклинами. Комплексы cdk/циклин регулируют фазы клеточного цикла и его развитие для продуцирования митоза и деления клеток.
Много специфических рецепторов на поверхности клеток связывается с G-белками так, что, когда фактор роста взаимодействует с рецептором, G-белок активируется, запуская каскад реакций, упомянутых ранее.
Таким образом, модуляция локализации и активности G-белков делает возможным контроль роста клеток и деления клеток.
Механизм, связанный с противоопухолевыми эффектами 2-гидроксиолеиновой кислоты и ее аналогов, основан на том факте, что они индуцируют модуляцию локализации и активности G-белков и других периферических белков, таких как протеинкиназа С или небольшие G-белки (типа Ras, Raf и др.). Такая модуляция ассоциируется с регулированием структуры мембранных липидов.
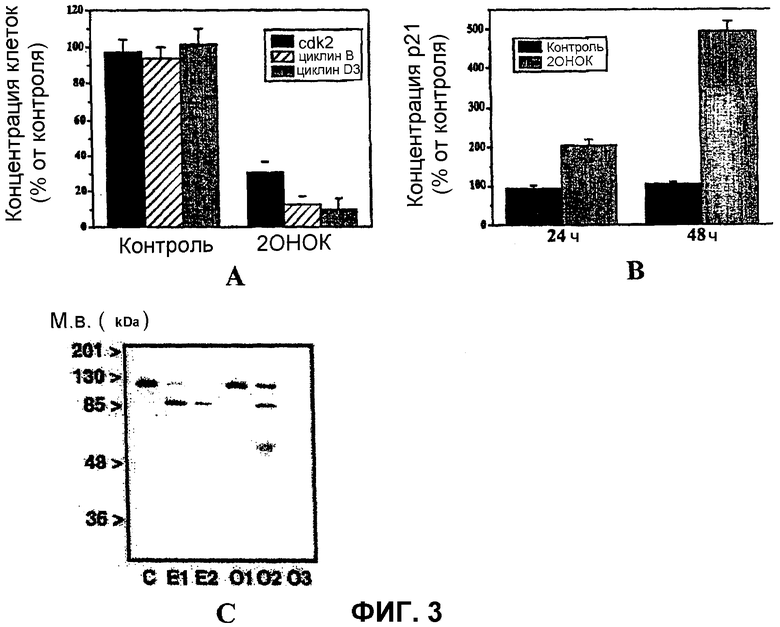
Установлено, что 2-гидроксиолеиновая кислота действует как ингибитор транслокации G-белков к ядру (Фиг.2). В этом случае достигается ингибирование пролиферации клеток, что подтверждается заметным и значительным повышением уровней белков р21 и снижением белков клеточного цикла cdk2 и циклинов В и D3 (Фиг.3А и В). Более того, установлено, что в клетках культуры 2-гидроксиолеиновая кислота и ее аналоги индуцируют значительное повышение протеинкиназы С (повышение в интервале от 40 до 120%).
Отмеченное изменение в клеточной локализации G-белков продуцирует модуляции их функции в большей степени, чем модуляции, продуцируемые лекарством дауномицином, широко используемым при лечении рака. Такие изменения оказывают значительные ингибирующие эффекты на пролиферацию и выживание опухолевых клеток (Фиг.4).
Важным регулятором клеточного цикла является белок р53, который оказывает регулирующее действие отрицательного типа путем замедления деления клеток на уровне G1 (стадия до митоза). Этот белок синтезируется самими клетками в ответ на появление изменений ДНК. Если воспроизведенная ДНК может оказывать отрицательное влияние на дочерние клетки, белок р53 активируется, вызывая апоптоз (запрограммированная гибель клетки). Активация указанного белка р53 означает, что другие гены экспрессируют такой код для регуляторных белков, таких как р21, р27, р16 и др., который ингибирует активность/экспрессию циклинов и cdk (вовлеченных в процесс клеточного цикла).
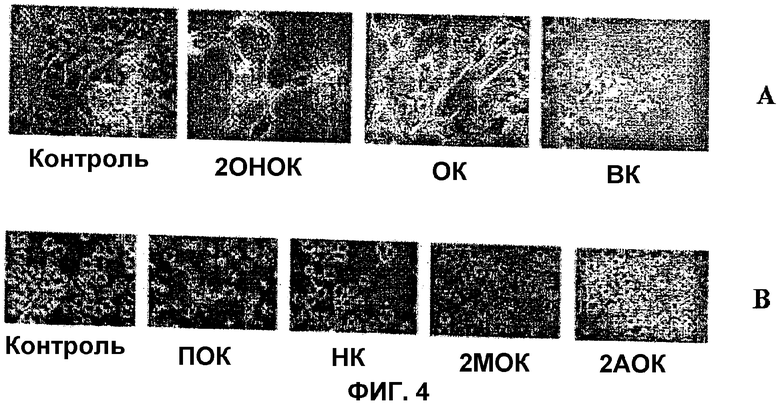
Во многих типах опухолевых клеток белок р53, как оказывается, мутирует и/или инактивируется, и имеет место пролиферация преобразованных (раковых) клеток. Присутствие 2-гидроксиолеиновой кислоты и/или ее аналогов в клетках индуцирует активацию сигнального пути, связанного с р53, что индуцирует начало апоптоза или остановку клеточного цикла в различных типах опухолевых клеток. С целью осуществления первого объекта настоящего изобретения используют модели in vitro и in vivo. В этой связи 2-гидроксиолеиновая кислота и все структурные аналоги, которые согласуются с общей формулой I, описанной ранее, как показано, обладают значительной противоопухолевой способностью. Были испытаны молекулы, которые являются аналогами 2-гидроксиолеиновой (2-гидрокси-цис-9-октадеценовой) кислоты: 2-метилолеиновая (2-метил-цис-9-октадеценовая) кислота, 2-аминоолеиновая (2-амино-цис-9-октадеценовая) кислота, олеиновая (цис-9-октадеценовая) кислота, пальмитоолеиновая (цис-9-гексадеценовая) кислота, цис-вакценовая (цис-11-октадеценовая) кислота и нервоновая (цис-15-тетракозеновая) кислота. Эти молекулы, как показано, останавливают пролиферацию клеток или вызывают гибель различных типов опухолевых клеток (например, клеток рака легких человека А549, лимфоцитов Jurkat T и др.) (Фиг.4). Полученные результаты демонстрируют противоопухолевую активность описанных жирных кислот и показывают, что основная структура 2-гидроксиолеиновой кислоты может иметь небольшие изменения без изменения их противоопухолевой активности.
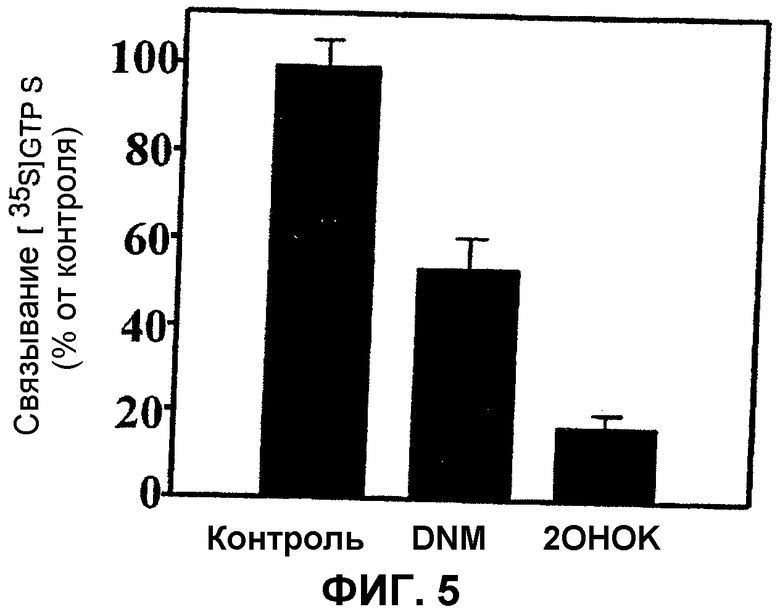
Другие молекулярные модели позволяют подтвердить, что 2-гидроксиолеиновая кислота и ее аналоги обладают противоопухолевой активностью, которая больше, чем активность, проявляемая другими противоопухолевыми лекарственными средствами, например, антрациклинами, и поэтому они представляют собой соединения, имеющие большой терапевтический интерес. В мембранах 3Т3 фибропластов успешно получено доказательство, что присутствие 200 мкМ 2-гидроксиолеиновой кислоты и/или олеиновой кислоты (одного из аналогов 2-гидроксиолеиновой кислоты), вызывает ингибирование 75-84% активности G-белков в клетках NIH 3Т3, тогда как 200 мкМ дауномицина вызывает ингибирование 46% указанной активности (Фиг.5).
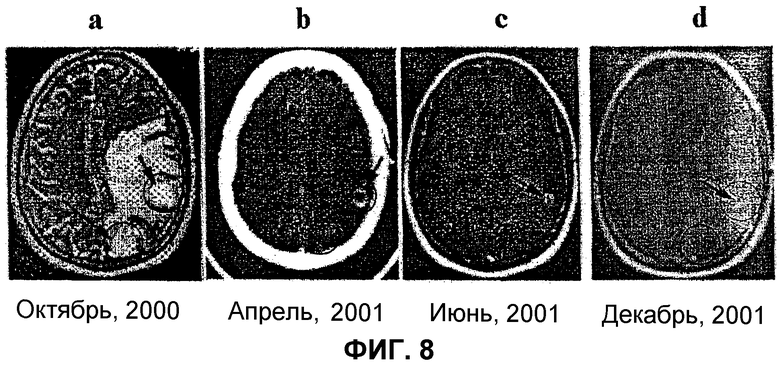
Противоопухолевая эффективность 2-гидроксиолеиновой кислоты и ее аналога олеиновой кислоты представлена на Фиг.8, где можно увидеть исчезновение некоторых церебральных опухолевых метастаз, образовавшихся от легочной аденокарциномы, после лечения с помощью 2-гидроксиолеиновой кислоты. Лечение такой 2-гидроксиолеиновой кислотой и олеиновой кислотой вызывает полное исчезновение рака. Эти результаты показывают, что (а) 2-гидроксиолеиновая кислота и ее аналоги представляют собой молекулы, которые могут быть использованы при приготовлении лекарственных средств, предназначенных для лечения рака; что (b) они могут иметь широкий спектр действия (они эффективны на различных типах опухолевых клеток в культуре и в живых организмах) и что (с) они превосходят другие молекулы, используемые для лечения рака, по их противоопухолевой эффективности отсутствием побочных эффектов и тем, что они могут быть введены перорально, хотя также возможно внутривенное или подкожное введение.
Противоопухолевые испытания
Антипролиферативная эффективность гидроксиолеиновой кислоты показана на примере клеток рака легких человека А549 и на клетках лейкемии человека (Jurkat). На Фиг.3 показана индукция антипролиферативного белка р21, которую осуществляют уменьшением белков cdk2, циклина В и циклина D3, необходимых, чтобы клетки опухоли были способны к делению. Аналогичные эффекты продуцируются всеми испытанными аналогами, которые согласуются с общей структурной формулой, приведенной ранее. Такой антипролиферативный эффект 2-гидроксиолеиновой кислоты и ее аналогов показан с помощью снижения плотности клеток в опухолевых клетках в культуре (Фиг.4). Этот антипролиферативный эффект также наблюдается при использовании других методик и других типов клеток: в первичных астроцитах крыс эти жирные кислоты проявляют антипролиферативный эффект, который изучен путем введения меченного тритием тимидина. Более того, гидроксиолеиновая кислота и ее аналоги способны индуцировать апоптоз или запрограммированную гибель клеток в клетках рака человека. С одной стороны, разложение PARP (Фиг.3С) и, с другой стороны, изменение в клеточной морфологии и присутствие клеточных остатков (Фиг.4) показывают эффект 2-гидроксиолеиновой кислоты и ее аналогов как индукторов гибели клеток. С использованием проточной цитометрии показано, что в присутствии 2-гидроксиолеиновой кислоты число живых клеток лейкемии человека (Jurkat) составляет только 10% от числа тех, которые остаются выжившими в случае этопозида, известного противоопухолевого агента.
И, наконец, изучение эффекта на людях показало, что 2-гидроксиолеиновая кислота и ее аналоги могут составить семейство противоопухолевых лекарственных средств большого значения. На Фиг.8 представлен эффект лечения с помощью 2-гидроксиолеиновой кислоты и олеиновой кислоты опухолей у человека. Показанный случай относится к больным женщинам, у которых предварительная химиотерапия и радиотерапия не привели к уменьшению опухолей мозга.
Задачей настоящего изобретения является демонстрация того, что 2-гидроксиолеиновая кислота и ее аналоги являются агентами с гипотензивной активностью.
Регулирование активности G-белков контролирует кровяное давление
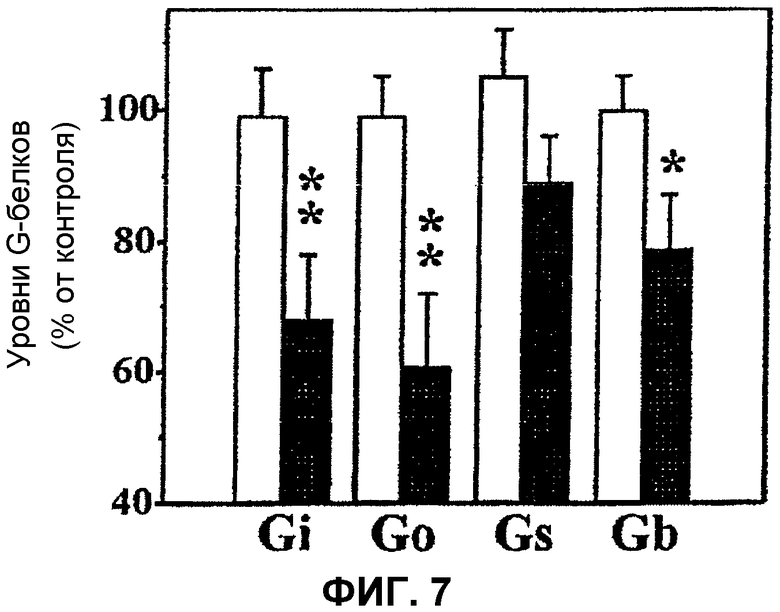
Существует зависимость между лекарственными средствами настоящего изобретения и активностью G-белков и кровяным давлением. Результат, который подтверждает ранее описанное, представляет собой исследование, проведенное на людях, где показано, что у пациентов с гипертонией наблюдаются изменения в уровнях мембранных липидов (таблица 3). Мембранные липиды оказывают влияние на ламеллярный/гексагональный переход, что, в свою очередь, иллюстрирует локализацию и функциональность G-белков. Действительно, у пациентов с гипертонией наблюдается изменение уровней G-белков, связанных с мембраной, которое обусловлено упомянутым выше изменением в мембранных липидах и легкостью образования гексагональных фаз. Если модификация неламеллярной мембранной структуры и последующая релокализация G-белков вызывает гипертонию, за счет регулирования ламеллярного/гексагонального перехода мембранных липидов можно обеспечить регулирование локализации мембранных белков и, в итоге, кровяного давления (Фиг.7).
Композиция жирных кислот фосфолипидов и сложных эфиров холестерина в мембранах эритроцитов у людей с нормальным кровяным давлением (контроль) и людей с повышенным кровяным давлением (мг/100 мг)
SFA (НЖК) - насыщенные жирные кислоты; MUFA (МНЖК) - мононенасыщенные жирные кислоты; PUFA (ПНЖК) - полиненасыщенные жирные кислоты. *Р<0,05, **Р<0,01, ***Р<0,001. n.d. - не определено.
Показано, что 2-гидроксиолеиновая кислота и ее аналоги также обладают заметным гипотензивным эффектом, так как они индуцируют уменьшение систолического и диастолического кровяного давления, не меняя частоту сердечных сокращений (Фиг.9а, 9b и 10). Гипотензивный эффект, продуцируемый 2-гидроксиолеиновой кислотой и ее аналогами, представляет собой эффект, который вызывает понижение кровяного давления в острой форме (который заметен после 2-часового лечения) и хронической форме (который сохраняется в течение дней и недель, пока продолжается лечение). Аминоолеиновая кислота, например, понижает кровяное давление на 15 мм рт.ст при постоянном лечении, длящемся неделю.
Кровяное давление контролируется различными системами рецепторов, связанных с G-белками, такими как рецепторы вазопрессина, адренергические рецепторы и др.
Взаимодействие между гормонами, вовлеченными в регулирование кровяного давления, с рецепторами, связанными со стимулирующими G-белками, модулируется за счет действия 2-гидроксиолеиновой кислоты и аналогичных молекул.
Такие жирные кислоты регулируют сообщение между рецептором, G-белком и эффектором. Результатом является модуляция сигналов циклического АМФ, фосфолипазы С и оксида азота, что вызывает снижение кровяного давления. Этот эффект также связан с регулированием мембранной структуры. Основное фармакологическое преимущество 2-гидроксиолеиновой кислоты и ее аналогов, в отличие от других гипотензивных лекарственных средств, состоит в том, что они не оказывают влияния на частоту сердечных сокращений (то есть, они не повышают или не понижают в значительной степени скорость сердечных сокращений). Дополнительное преимущество этих соединений состоит в том, что они контролируют другие факторы сердечно-сосудистого риска: профиль сывороточные липиды/липопротеин и вес тела (см. ниже). Так как регулирование кровяного давления недостаточно само по себе для продления жизни пациенту и так как необходимо регулировать другие факторы сердечно-сосудистого риска, такие жирные кислоты превосходят другие молекулы, используемые больными с сердечно-сосудистыми заболеваниями.
Гипотензивные испытания
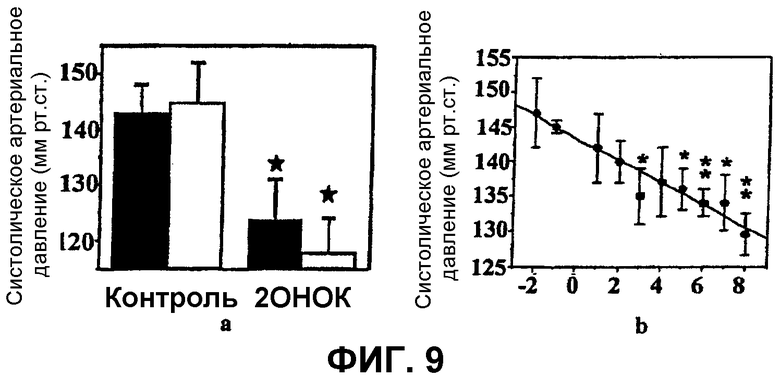
2-Гидроксиолеиновая кислота индуцирует значительные снижения кровяного давления у крыс (Фиг.9). Такие снижения имеют острую форму (через 2 часа лечения, 19±6 мм рт.ст., Р<0,01, n=6) и хроническую форму (1 неделя, 26±7 мм рт.ст., Р<0,001, n=6). Более того, лечение в острой и хронической форме в количестве от 1 до 10 мг/кг также дает значительное снижение кровяного давления, которое зависит от концентрации.
У людей 2-гидроксиолеиновая кислота также вызывает значительное снижение кровяного давления (см. Фиг.9).
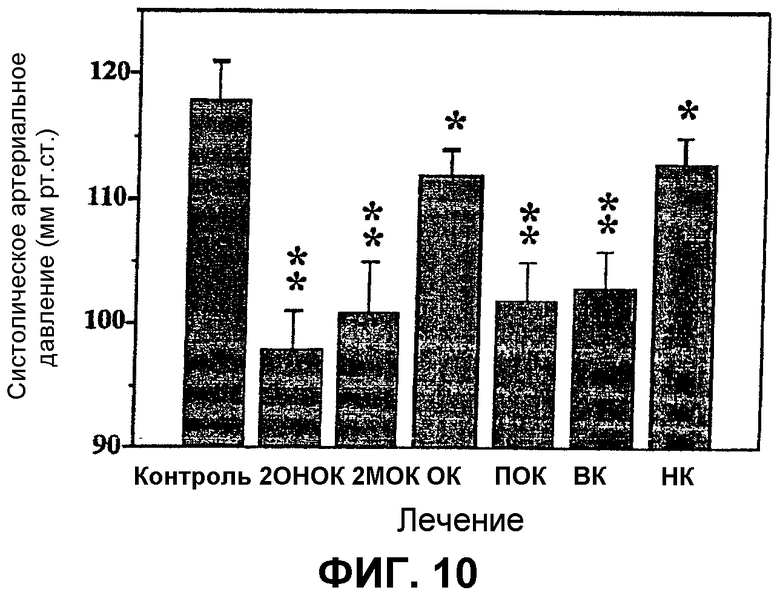
Более того, аналоги 2-гидроксиолеиновой кислоты, которые соответствуют общей формуле, приведенной выше, обладают гипотензивным эффектом (Фиг.10). Во всех случаях понижение кровяного давления значительно в сравнении с контролем (*Р<0,05, **Р<0,01).
Полученные результаты однозначно показывают, что 2-гидроксиолеиновая кислота и ее аналоги являются эффективными агентами для клинического/фармакологического лечения высокого кровяного давления.
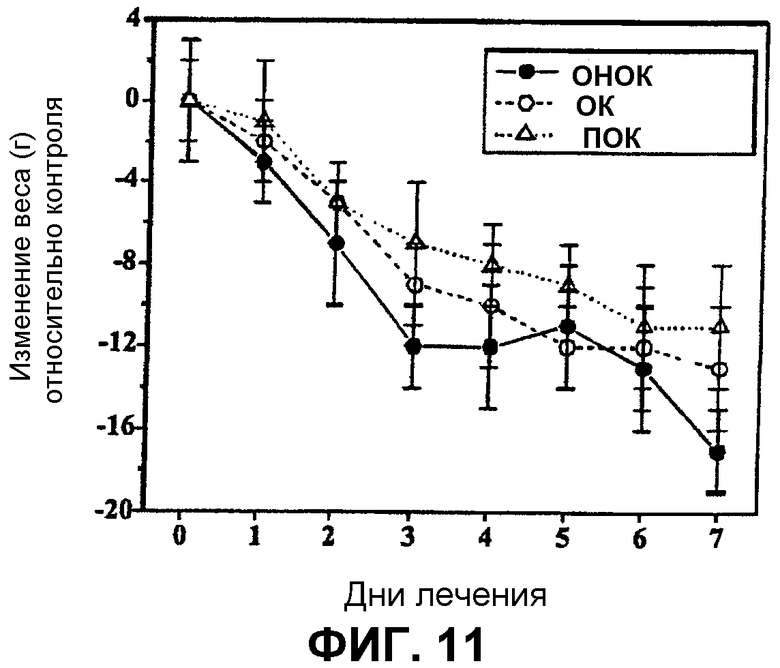
Задача настоящего изобретения заключается в том, чтобы показать, что 2-гидроксиолеиновая кислота и ее аналоги обладают активностью в качестве агентов, которые стимулируют снижение веса тела (Фиг.11).
Помимо противоопухолевой и гипотензивной активности 2-гидроксиолеиновая кислота и ее аналоги стимулируют снижение веса тела.
Снижение веса тела регулируется, наряду с другими обстоятельствами, такими факторами, как метаболическая активность и регулирование потребления пищи индивидуумом.
Регулирование потребления пищи определяют с помощью ощущения сытости, которое, в свою очередь, регулируется на гормональном уровне. Например, дефицит питательных веществ стимулирует секрецию гормонов, которые вызывают чувство аппетита. После еды, как только уровень питательных веществ восстановится, имеет место стимуляция секреции гормонов, которые вызывают ощущение сытости.
Установлено, что 2-гидроксиолеиновая кислота и ее аналоги дают эффект сытости, вызывая уменьшение поглощения пищи. Такое регулирование также опосредуется рецепторами цитокинов, лептинов, адреноцепторов и других рецепторов, связанных с G-белками, чья активность модулируется такими жирными кислотами.
Для изученных животных такое влияние на сытость означает потребление пищи на 15-30% меньше, чем контрольными животными.
Испытания по регулированию веса тела
Крысы, обработанные этими молекулами, теряют вес тела во время хронического лечения (от 5 до 17 дней). В этих опытах крысы, обработанные 2-гидроксиолеиновой кислотой или ее аналогами, в особенности аминоолеиновой кислотой, имеют свободный доступ к пище и воде, как и контрольная группа крыс, подвергающихся лечению (Фиг.11). В этих условиях наблюдается прогрессивное снижение веса тела крыс, начиная от первого дня лечения до 17 г на седьмой день лечения (5% от нормального веса тела крыс Sprague-Dowley возрастом 2-3 месяца). Пищу, даваемую этим животным, взвешивают, и потребление, как установлено, снижается за время лечения, подтверждая тот факт, что лечение молекулами, относящимися к данному изобретению, вызывает эффект сытости у животных. Аналогичные опыты, проведенные на взрослых мышах, в течение промежутков времени до 28 дней с 2-гидроксиолеиновой кислотой показывают уменьшение веса тела на 15-25% относительно контрольных мышей (обработанных носителем).
Описание чертежей
Фиг.1: показаны некоторые из большого числа структур, помимо ламеллярных, которые могут принимать мембраны.
Фиг.2 показывает клеточную локализацию Gαi2-белков, меченных флуоресцеином, в первичных астроцитах мозга крыс. В контрольных клетках метка указывает на присутствие этих белков по всей клетке, особенно в ядре (стрелка). В клетках, обработанных 2-гидроксиолеиновой кислотой (2ОНОК), метка проявляется в мембране и цитозоле, но не в ядре (стрелка).
Фиг.3 показывает влияние 2-гидроксиолеиновой кислоты в молекулярных маркерах клеточной пролиферации и гибели клеток. Часть А показывает влияние 2-гидроксиолеиновой кислоты (2ОНОК) на белки клеточного цикла cdk2, циклин В и циклин D3 в клетках рака легкого человека А549. Уменьшение этого белка показывает, что жирная кислота индуцирует остановку клеточного цикла, то есть остановку деления клеток. Часть В показывает влияние 2-гидроксиолеиновой кислоты (2ОНОК) на белок р21 в клетках А549 после выдерживания в течение 24 и 48 час. Белок р21 ингибирует клеточный цикл, так как он является антипролиферативным белком. Большие повышения, которые индуцирует 2-гидроксиолеиновая кислота на этом белке, объясняют остановку клеточного цикла и пролиферации опухолевых клеток. Часть С показывает разложение поли-АДФ рибоз-полимеразы (ПАРП) в клетках лейкемии человека (Jurkat) (этопозид: 25 [E1] и 250 мкМ [E2]; 2-гидроксиолеиновая кислота: 10[О1], 100[О2] и 1000 мкМ [О3]). Уменьшение уровней этого фермента или доказательство его разложения указывают на начало апоптоза или запрограммированной гибели клеток. В этих опытах используют этопозид в качестве положительного контроля, и эта молекула, как известно, является индуктором апоптоза и противоопухолевым агентом.
Фиг.4 показывает влияние 2-гидроксиолеиновой кислоты и ее аналогов на пролиферацию клеток рака легких человека А549 (А) и клеток Jurkat лейкемии человека (В). Как 2-гидроксиолеиновая кислота (2ОНОК), так и ее аналоги, которые соответствуют ранее приведенной формуле, индуцируют остановку деления и гибель опухолевых клеток (ОК: олеиновая кислота; ВК: цис-вакценовая кислота; ПОК: пальмитоолеиновая кислота; НК: нервоновая кислота; 2МОК: 2-метилолеиновая кислота; 2АОК: 2-аминоолеиновая кислота).
Фиг.5 показывает связывание [35S]GTPγS с мембранами клеток NIH 3T3, трансфецированных адреноцептором крыс α2A/D. Этот параметр измеряет активность G-белков. Присутствие 2-гидроксиолеиновой кислоты индуцирует понижение функции G-белков даже в большей степени, чем антрациклин дауномицин (DNM). Антрациклины являются эффективными противоопухолевыми лекарственными средствами, следовательно, 2-гидроксиолеиновая кислота потенциально более эффективна в отношении опухолей. Аналоги 2-гидроксиолеиновой кислоты продуцируют эффект, аналогичный эффекту 2-гидроксиолеиновой кислоты.
Фиг.6: гидроксиолеиновая кислота и ее аналоги не оказывают влияния на чистые G-белки (в отсутствие мембраны). Этот результат показывает, что их влияние на активность G-белков опосредуется путем регулирования неламеллярными мембранными структурами. Дауномицин (DNM) проявляет поведение, аналогичное контролю.
Фиг.7: Уровни G-белков в мембранах эритроцитов людей с нормальным кровяным давлением (не закрашенные столбцы) и у людей с повышенным давлением (закрашенные столбцы). Уровни белков Gαi1/2(Gi), Gαо (Go), Gαs (Gs) и G Gβ (Gb) значительно ниже у людей с повышенным давлением. Величины столбцов представляют собой средние значения ± стандартная ошибка среднего значения *Р<0,05, **Р<0,01.
Фиг.8 показывает метастазы мозга (опухоли), образовавшиеся от легочной аденокарциномы. Изображение слева (8а) соответствует опухолям до лечения, а изображения справа (8b, 8c и 8d) соответствуют опухолям после лечения с помощью 2-гидроксиолеиновой кислоты на различных датах. Можно увидеть, что одна из опухолей исчезает быстрее, а другая медленнее.
Фиг.9а показывает острый эффект (2 часа, черные столбцы) и хронический эффект (3 ежедневные инъекции в течение 7 дней, белые столбцы) гидроксиолеиновой кислоты (30 мг/кг) на систолическое артериальное давление крыс Sprague-Dowley. Более низкие дозы этой молекулы (1-10 мг/кг) дают аналогичные эффекты, но менее заметные. *Р<0,01.
Фиг.9b показывает влияние 2-гидроксиолеиновой кислоты (30 мг/кг) на кровяное давление у людей. Эта диаграмма показывает систолическое артериальное давление в зависимости от дня лечения. Дни до лечения показаны с помощью отрицательных значений. *Р<0,05, **Р<0,01.
Фиг.10 показывает влияние экстренного лечения с помощью 2-гидроксиолеиновой кислоты (2ОНОК) и ее аналогов 2-метилолеиновой кислоты (2МОК), олеиновой кислоты (ОК), пальмитоолеиновой кислоты (ПОК), цис-вакценовой кислоты (ВК) и нервоновой кислоты (НК). Все обработки, проведенные с помощью 2-гидроксиолеиновой кислоты и ее аналогов, которые соответствуют приведенной ранее общей формуле, индуцируют значительное понижение (*Р<0,05, **Р<0,001) систолического артериального давления у крыс Sprague-Dowley.
Фиг.11 показывает влияние 2-гидроксиолеиновой кислоты (2ОНОК) и ее аналогов, олеиновой кислоты (ОК) и пальмитоолеиновой кислоты (ПОК), на вес тела (3 ежедневные инъекции по 30 мг/кг). Животные (крысы Sprague-Dowley) имеют свободный доступ к пище и воде в любое время.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ 2-ГИДРОКСИПРОИЗВОДНЫХ ПОЛИНЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2513995C2 |
| АЛЬФА-ПРОИЗВОДНЫЕ ЦИС-МОНОНЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2009 |
|
RU2531353C2 |
| СПОСОБ СИНТЕЗА ГИДРОКСИТРИГЛИЦЕРИДОВ И ИХ ПРИМЕНЕНИЕ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2015 |
|
RU2679443C2 |
| ЭНАНТИОМЕРЫ 2-ГИДРОКСИПРОИЗВОДНЫХ ЖИРНЫХ КИСЛОТ | 2012 |
|
RU2687967C2 |
| ЭНАНТИОМЕРЫ 2-ГИДРОКСИПРОИЗВОДНЫХ ЖИРНЫХ КИСЛОТ | 2012 |
|
RU2637937C2 |
| УЛУЧШЕННЫЙ ВЕКТОР, ЭКСПРЕССИРУЮЩИЙ TOLL-ПОДОБНЫЙ РЕЦЕПТОР И АГОНИСТ, И ПРИМЕНЕНИЕ В ТЕРАПИИ РАКА | 2014 |
|
RU2682762C2 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ НОВЫХ ФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ, СОДЕРЖАЩИХ ПРОТИВООПУХОЛЕВЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА, СВЯЗАННЫЕ С ГИАЛУРОНОВОЙ КИСЛОТОЙ, В ЛЕЧЕНИИ НЕОПЛАЗИЙ | 2009 |
|
RU2581972C2 |
| Способ применения гидроксихлорохина и его производных для доставки химиотерапевтического лекарственного препарата в очаг ракового заболевания (варианты) | 2023 |
|
RU2834400C2 |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ПРОТИВООПУХОЛЕВЫХ АГЕНТОВ | 2000 |
|
RU2271829C2 |
| СПОСОБЫ EX VIVO ЭКСПАНСИИ ЕСТЕСТВЕННЫХ КЛЕТОК-КИЛЛЕРОВ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2814083C2 |
Настоящее изобретение относится к области лекарственных средств, в частности к применению 2-гидроксиолеиновой кислоты и ее аналогов при производстве лекарственных средств, которые могут быть использованы при заболеваниях, этиология которых основана на регулировании сигналов, связанных G-белками и опосредованных переходом мембранной структуры от ламеллярной к гексагональной. Описано применение соединений общей формулы I: СООН-CHR-(СН2)m-СН=СН-(СН2)n-СН3, где R представляет собой ОН или NH2, m и n имеют значения 6-11, при производстве лекарственных средств, которые могут быть использованы при лечении рака, и соединений общей формулы I: СООН-CHR-(СН2)m-СН=СН-(СН2)n-СН3, где R выбирают из Н, ОН, NH2 или СН3, m и n имеют значения 6-11, при производстве лекарственных средств, которые могут быть использованы для лечения гипертонии, ожирения. 4 н. и 4 з.п. ф-лы, 11 ил., 3 табл.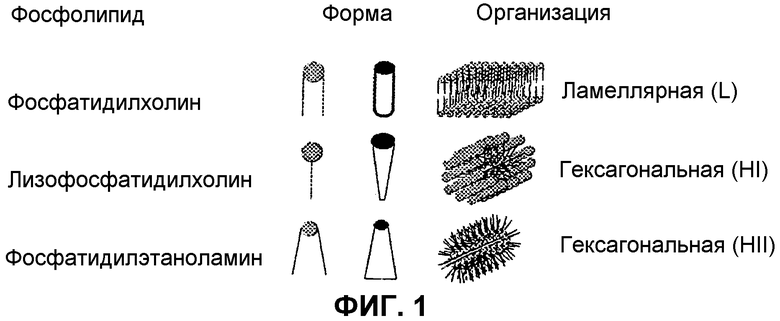
| WO 8704926 А2, 27.08.1987 | |||
| BANNI S | |||
| et al | |||
| Vaccenic acid feeding increases tissue levels of conjugated linoleic acid and suppresses development of premalignant lesions in rat mammary gland | |||
| Nutr Cancer | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| WO 9958121 A1, 18.11.1999 | |||
| ДЖЕНКИНС Г., Хартунг У., «Химия органических лекарственных препаратов», М.: Государственное издательство иностранной литературы, 1949, стр.232-233. | |||
Авторы
Даты
2007-11-20—Публикация
2002-10-09—Подача