Изобретение относится к химии хитозана и полиэдрических клозо-гидроборатов, которые могут применяться как активные компоненты в энергоемких составах, способу их получения и применения.
Известны соли хитозана, С6O4Н9NH2, с уксусной, фтористоводородной, соляной, серной и др. кислотами. Их образование обусловлено донорно-акцепторным взаимодействием пары электронов азота NH2-групп хитозана со свободной 1S орбиталью Н+-катионов этих кислот с полным переносом протона на аминогруппу и получением молекулярного катиона хитозания, C6O4H9NH3 +. Некоторые из солей хитозана достаточно хорошо растворимы в воде (ацетат, фторид, хитозания), некоторые плохо (хлорид, сульфат хитозания). Растворимые соли образуют вязкие прозрачные растворы, которые устойчивы при хранении. При испарении растворителя соли хитозана образуют твердый компактный продукт (в виде пленок, пластин, объемных материалов), легко измельчаемый в порошок. Он не содержит кристаллогидратной воды, слабо гигроскопичен, достаточно устойчив термически, нечувствителен к механическому воздействию (удар, трение, накол и т.п.), нетоксичен. (Плиско Е.А., Нудьга Л.А., Данилов С.Н. // Успехи химии. 1977. Т.XLVI. Вып.8. С.1470).
Известные соли хитозана получают его взаимодействием с кислотами или обменными реакциями между солями хитозана и кислотами или солями соответствующих кислот.
Например, хорошо растворимый ацетат хитозания получают растворением хитозана в уксусной кислоте, взятой в мольном соотношении 1 к 1, согласно следующему уравнению реакции:
С6O4Н9NH2+СН3СООН=С6O4Н9NH3СН3СОО
Полученный раствор упаривают досуха и получают твердый ацетат хитозания.
Плохо растворимый сульфат хитозания получают по обменной реакции между ацетатом хитозания и серной кислотой или растворимым сульфатом, согласно следующему уравнению реакции:
2C6O4H9NH3CH3COO+H2SO4(Na2SO4)=(С6O4Н9NH3)2SO4↓+2СН3СООН(2СН3COONa)
Выпавший в осадок сульфат хитозания отделяют фильтрованием, промывают водой и сушат.
Недостатком известных солей хитозана является низкое содержание кислорода и отсутствие даже слабо выраженных окислительных свойств. По-видимому, по этой причине ничего неизвестно об их применении в качестве активных окисляющих компонентов энергоемких составов.
Известен достаточно широкий ряд перхлоратов металлов и молекулярных катионов (аммония, гидразония, гидроксиламмония, нитрония и др.), которые применяются в качестве твердых источников кислорода в энергоемких составах различного назначения (Росоловский В.Я. Безводные перхлораты и перхлорметаллаты: синтез, структура, свойства. В сб. научн. тр. ИОНХ под ред. Кузнецова Н.Т. Химия неорганических гидридов. - М.: Наука, 1990. С.126).
Перхлораты получают взаимодействием хлорной кислоты, HClO4, с оксидами, гидрооксидами, карбонатами и хлоридами металлов и молекулярных катионов; электрохимическим окислением хлоратов; обменными реакциями NaClO4 с соответствующими солями (Химический энциклопедический словарь. Гл. редактор Кнунянц И.Л. - М.: Советская энциклопедия, 1983. 435 С.).
Недостатками известных перхлоратов является гигроскопичность и образование кристаллогидратов (LiClO4×3H2O, NaClO4×H2O, Mg(ClO4)2×6H2O), довольно низкая термическая устойчивость, взрывоопасность и чувствительность к механическому воздействию и нагреванию, токсичность (перхлораты гидразония, гидроксиламмония, нитрония). И хотя известные перхлораты обладают высоким содержанием кислорода, перечисленные недостатки приводят к усложнению их использования в составе энергонасыщенных материалов.
Наиболее близким к заявляемому соединению является перхлорат гидразония состава N2H5ClO4. Соединение представляет собой бесцветные кристаллы, хорошо растворимые в воде и полярных неводных растворителях. При быстром нагревании разлагается со вспышкой или взрывом, а при медленном в вакууме - диссоциирует на исходные соединения. Сильно ядовит. Используется в ракетном топливе в качестве окислителя. Перхлорат гидразония получают взаимодействием гидразина и хлорной кислоты, взятых в молярном соотношении 1 к 1 (Химическая энциклопедия. T.1. Гл. редактор Кнунянц И.Л. - М.: Советская энциклопедия, 1988. 547 С.). Выделение из растворов ведут или сушкой при умеренных температурах, т.к. соединение достаточно термически нестабильно, или высаливанием подходящим растворителем.
Задача изобретения состоит в получении нетоксичного, взрывобезопасного, устойчивого к влаге, нагреванию и механическому воздействию и при этом обладающего высокими окислительными свойствами соединения, которое может использоваться в энергоемких составах.
Поставленная задача решается перхлоратом хитозания состава С6O4Н9NH3ClO4 и способом его получения, включающим взаимодействие в водном растворе хитозана и хлорной кислоты, HClO4, взятых в эквимолярном соотношении, и последующее выделение соединения путем сушки образовавшегося раствора при температуре 105-110°С до постоянной массы или высаливанием подходящим растворителем.
Способ осуществляют согласно следующему уравнению реакции:
С6O4Н9NH2+HClO4=С6O4H9NH3ClO4
Получают вязкий раствор, который затем сушат на воздухе при обычной температуре или при температуре 105-110°С.
Осуществление способа в условиях избыточного количества хлорной кислоты приводит к загрязнению хлорной кислотой полученного соединения, так как поскольку она заметно нелетуча, удаление ее избытка затруднено, а сильный нагрев может привести к разложению и вспышке смеси. Недостаток кислоты приводит к загрязнению получаемого соединения хитозаном, который необходимо отделить, поскольку примесный хитозан играет роль балласта и понижает окислительные свойства перхлората хитозания.
Как показали проведенные исследования, перхлорат хитозания - С6O4Н9NH3ClO4 - имеет чрезвычайно высокую растворимость в воде. Например, при высушивании его разбавленного раствора образуется сиропообразная жидкость, которая при дальнейшем высыхании переходит в бесцветную однородную, прозрачную, напоминающую целлофан пленку, без образования в ней кристаллов или частичек перхлората хитозания. Перхлорат хитозания может быть выделен в виде твердых покрытий, пленок, пластин, объемных материалов, легко измельчаемых в порошок. Соль не содержит кристаллогидратной воды, слабо гигроскопична, не взрывается при ударе, трении и др. механическом воздействии, нетоксична. При нагревании чистого перхлората хитозания идет его спокойное разложение без вспышек и взрывных выбросов, начиная со 180°С. По данным дифрактометрии (ДРОН - 3,0, λCuKα) соединение рентгеноаморфно, что характерно для солей хитозана, а отражения, которые дает исходный хитозан, отсутствуют.
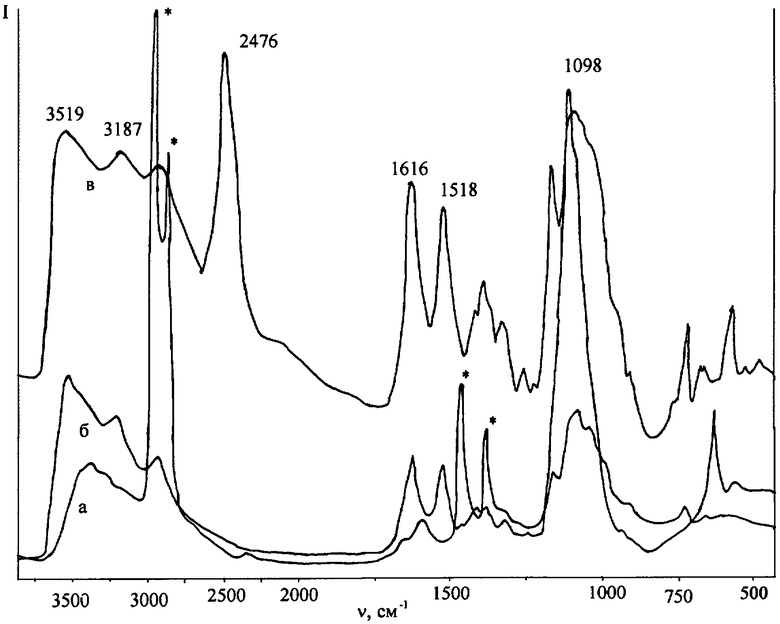
На чертеже приведены ИК-спектры (IFS EQUINOX-55S) «а» - чистого хитозана; «б» - перхлората хитозания; «в» - додекагидро-клозо-додекабората хитозания. Видно, что спектр перхлората хитозания, снятый с пленки перхлората хитозания (см. чертеж, б), содержит ряд полос в области 1518, 1616, 3187 и 3519 см-1, характеризующих анион хитозания (см. чертеж, в) (В.И.Салдин, Л. Н.Игнатьева, Ю.М.Николенко. Реакции додекагидро-клозо-додекаборной кислоты с хитозаном. // Журнал структурной химии. 2006. Т.47. №1. С.41-46) и которые отсутствуют в ИК-спектре чистого хитозана (см. чертеж, а). Полоса в области 1098 см-1, относится к валентным колебаниям ClO4 --аниона, подтверждая его вхождение в структуру заявляемого соединения.
Перхлорат хитозания проявляет свойства окислительного компонента. Так при растирании смеси перхлората хитозания в виде его концентрированного раствора с такими хорошо известными горючими компонентами пиротехнических и зажигательных составов как красный фосфор, и/или сера, и/или сульфид сурьмы, Sb2S3 и последующей сушке получают активно окисляющиеся компактные материалы. При этом в зависимости от соотношения перхлората хитозания и горючего компонента разложение может проходить как в виде быстрого горения, так и взрыва.
Преимуществом С6O4Н9NH3ClO4 по сравнению с другими известными окислителями, в том числе перхлоратами, применяемыми в окислительных смесях, является сочетание в этом соединении окислительных свойств со свойствами связующего. Влажные смеси перхлората хитозания с горючими компонентами безопасны в работе. Равномерное распределение компонентов достигается перетиранием компонентов и обеспечивается достаточно высокой вязкостью концентрированного раствора С6O4Н9NH3ClO4, благодаря чему исключается оседание твердых частиц компонентов. Из полученного пластичного материала легко формировать изделие нужной формы. При высыхании таких смесевых составов формируется плотный материал, что исключает такую небезопасную операцию как прессование.
В качестве энергоемких компонентов энергонасыщенных материалов известно применение соединений клозо-гидроборных анионов, в том числе додекагидро-клозо-додекабората хитозания (C6O4H9NH3)2B12H12 (п. РФ №2158221). Благодаря особенностям структуры этого соединения - тонкое на молекулярном уровне распределение горючего (В12Н12 2--анионы) и окислителя (кислородсодержащие группировки хитозана), свободный доступ кислорода и воздуха к центрам горения, вспучивание при нагревании с резким увеличением объема горящего материала - создаются благоприятные условия для быстрого и полного протекания твердо-газофазной реакции горения. При поджигании (С6O4Н9NH3)2В12Н12 воспламеняется и энергично сгорает с образованием черного остатка, представляющего собой смесь сажи и борного ангидрида и/или борной кислоты. Однако поскольку соединение имеет относительно высокую температуру вспышки (около 300°С), это ограничивает возможности его использования в качестве энергоемкого компонента энергонасыщенных материалов.
Для понижения температуры вспышки и увеличения активности и полноты сгорания энергонасыщенных составов предлагается композиция на основе додекагидро-клозо-додекабората хитозания (C6O4H9NH3)2B12H12 и перхлората хитозания С6O4Н9NH3ClO4 в эффективном соотношении, определяемом требуемым характером горения.
В отличие от индивидуальных С6O4Н9NH3ClO4 и (С6O4Н9NH3)2В12Н12 заявляемый состав проявляет гораздо более высокую энергоактивность. Как показали проведенные исследования, состав имеет более низкую температуру вспышки (около 240°С) и более высокую скорость и полноту сгорания по сравнению с индивидуальными компонентами. Это объясняется строением образующегося состава, который представляет собой равномерно распределенную смесь олигомеров хитозановых солей B12H12 2-- и ClO4 --анионов.
ClO4 --анионы являются более богатыми по кислороду и более активными окислителями, чем кислородсодержащие группировки хитозана. Поэтому при нагревании таких составов воспламенение (С6O4Н9NH3)2В12Н12 происходит при более низкой температуре, а его сгорание проходит намного интенсивнее, чем в индивидуальном виде. При этом активность составов определяется соотношением В12Н12 2--анионов, которые выступают в роли горючего, и ClO4 --анионов перхлората хитозания, проявляющих окислительные свойства. Поскольку додекагидро-клозо-додекаборат хитозания очень сильно дефицитен по кислороду, при увеличении количества перхлората хитозания активность заявляемых составов растет. Конкретный состав композиции определяется в зависимости от требуемого режима горения (медленное, быстрое или взрыв): при необходимости взрывного характера повышают концентрацию в смеси перхлората хитозания, а для обеспечения более спокойного характера горения - концентрацию додекагидро-клозо-додекабората хитозания.
Составы получают совместным концентрированием раствора перхлората хитозания с тонкодисперсным порошком додекагидро-клозо-додекабората хитозания. Равномерное распределение солей достигается не только за счет высокой вязкости образующегося раствора, но и благодаря тому, что B12H12 2--анионы являются электронно-дефицитными системами в отличие от ClO4 --анионов, содержащих в своей структуре большое число донорных атомов кислорода, имеющих неподеленные пары электронов. Поэтому при испарении воды идет сближение олигомеров солей за счет донорно-акцепторного взаимодействия B12H12 2- и ClO4 --анионов, что подтверждается смещением характеристических полос валентных колебаний исходных анионов по сравнению с индивидуальными соединениями. В результате образуется однородный, с равномерным распределением окислителя и горючего твердый полимерный состав.
Химический состав заявляемого перхлората хитозания C6O4H9NH3ClO4 определяют следующим образом.
Содержание хлора находят, прокаливая образцы с избытком пероксида натрия, Na2O2 в никелевой бомбе (Бабко А.К., Пятницкий И.В. Количественный анализ. - М.: Высшая школа, 1968. С.419). Реакционный продукт выщелачивают водой и определяют Cl--анион в виде AgCl по известной методике (Бабко А.К., Пятницкий И.В. Количественный анализ. - М.: Высшая школа, 1968. С.19).
Для анализа на остальные элементы и группы, входящие в состав перхлората хитозания, параллельную навеску образца обрабатывают избытком гидроксида натрия, в результате чего в осадок выпадает хитозан, а в раствор переходит перхлорат натрия согласно следующему уравнению реакции:
C6O4H9NH3ClO4+NaOH=С6O4Н9NH4↓+NaClO4+H2O (4)
Осадок хитозана отделяют фильтрованием, промывают водой и сушат при 105°С до постоянного веса. Анализ полученного хитозана на углерод, водород и азот проводят известными методами микроанализа органических веществ (Мазор Л. Методы органического анализа. М.: Мир, 1986. С.147).
Изобретение иллюстрируется следующими примерами.
Пример 1. В качестве исходного использовали хитозан, синтезированный по технологии ТОО "Комбио" (г. Владивосток, ТУ 15-01 482-88) в виде порошкообразного (пластинчатые частички не более 0,3 мм в поперечнике) продукта. Его элементный состав после сушки при 105°С до постоянного веса составляет (мас.%): С - 44,8; Н - 6,9; N - 8,6; O - 39,7. Это соответствует 98%-ной степени дезацетилирования хитина и условному молекулярному весу 162,02 у.а.е. К 300 мл раствора, содержащего 1.06 г (10.52 мг-моль) хлорной кислоты, добавляют 1.72 г (10,62 мг-моль) хитозана. После растворения основной массы хитозана, которое проходит в течение нескольких минут, заметно вязкий бесцветный раствор нагревают для ускорения диффузии кислоты к непрореагировавшим частицам хитозана. Затем нагретый раствор фильтруют, отделяя небольшой избыток хитозана и механические примеси. Для более высокого выхода целевого соединения образующийся осадок промывают 50 мл воды, поскольку раствор вязкий и остается в виде пленки как на стенках стакана, так и в пористой перегородке стеклянного фильтра. Часть раствора выливают тонким слоем (1.5-2 мм) в стеклянную чашку Петри и проводят выпаривание при 100°С. По мере концентрирования раствора его вязкость повышается. Целевой перхлорат хитозания получают в виде прозрачного бесцветного тонкого покрытия с высокой адгезией к стеклу. При выпаривании растворов, залитых толстым слоем (более 8 мм), покрытие довольно легко отделяется от поверхности в виде достаточно прочной и эластичной бесцветной прозрачной пленки. Всего в результате окончательной сушки при 105°С до постоянного веса получают 2.76 г (10.50 мг-моль) С6O4Н9NH3ClO4, что соответствует его 99.8%-ному выходу по хлорной кислоте. Полученное соединение разлагается спокойно, без вспышки и взрывных выбросов, при температуре выше 180°С.
Рассчитано для С6O4Н9NH3ClO4, мас.%: С - 27.54, Н - 4.63, N - 14.01, Cl - 13.55, O - 48.92.
Найдено для С6O4Н9NH3ClO4, мас.%: С - 27.51, Н - 4.66, N - 14.05, Cl - 13.58.
Пример 2. К 20 мл сметанообразного раствора, содержащего 1.44 г (3.04 мг-моль) свежеполученного тонкодисперсного (C6O4H9NH3)2B12H12, добавляют 0.40 г (1.52 мг-моль) С6O4Н9NH3ClO4 (мольное соотношение 2:1) и тщательно перемешивают. Образовавшийся в результате растворения твердого перхлората хитозания однородный вязкий раствор белого цвета выливают в чашку Петри и сушат до постоянного веса при температуре 110°С. Получают 1.82 г белесоватого полупрозрачного продукта. Температура вспышки 240°С. Разложение проходит в виде быстрого горения с разбросом горящего материала.
Пример 3. 1.17 г (2.50 мг-моль) сухого тонкодисперсного (С6O4Н9NH3)2В12Н12 засыпают в 20 мл вязкого раствора, содержащего 0.66 г (2.50 мг-моль) С6O4Н9NH3ClO4 (мольное соотношение 1:1), тщательно перемешивают и сушат, как подробно описано в примере 1. Получают 1.82 г продукта, что соответствует 100%-ному выходу целевого продукта. Температура вспышки 240°С. По сравнению с составом, полученным в примере 1, горение более энергичное.
Пример 4. 5 г влажного пастообразного продукта, содержащего 1.30 г (2.76 мг-моль) свежеполученного тонкодисперсного (C6O4H9NH3)2B12H12, добавляют в 40 мл вязкого раствора, содержащего 1.45 г (5.52 мг-моль) С6O4Н9NH3ClO4 (мольное соотношение 1:2), и тщательно перемешивают. Образовавшийся сметанообразный однородный вязкий раствор белого цвета выливают в чашку Петри и сушат до постоянного веса, как подробно описано в примере 1. Получают 2.75 г продукта, что соответствует практически 100%-ному выходу целевого продукта. Температура вспышки 240°С. Полученный состав демонстрирует самое быстрое и энергичное горение по сравнению с составами, полученными в двух предыдущих примерах.
| название | год | авторы | номер документа |
|---|---|---|---|
| АДДУКТЫ ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТА ХИТОЗАНИЯ С ХЛОРНОЙ КИСЛОТОЙ ИЛИ ПЕРХЛОРАТОМ АММОНИЯ | 2009 |
|
RU2394840C1 |
| ХРОМАТ ХИТОЗАНИЯ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЭНЕРГОЕМКИЙ СОСТАВ, ЕГО СОДЕРЖАЩИЙ | 2010 |
|
RU2439081C1 |
| АДДУКТЫ ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТА ХИТОЗАНА С НИТРАТАМИ ИЛИ ПЕРХЛОРАТАМИ МАГНИЯ ИЛИ АЛЮМИНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2596741C2 |
| АДДУКТЫ ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТА ХИТОЗАНА С СОЛЯМИ-ОКИСЛИТЕЛЯМИ ПЕРЕХОДНЫХ МЕТАЛЛОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2562480C2 |
| ПОЛУГИДРАТ ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТА МЕЛАМИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2617778C1 |
| БОРФТОРСОДЕРЖАЩАЯ ЭНЕРГОЕМКАЯ КОМПОЗИЦИЯ ДЛЯ ЭНЕРГЕТИЧЕСКИХ КОНДЕНСИРОВАННЫХ СИСТЕМ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2017 |
|
RU2640338C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРНОЙ КИСЛОТЫ | 2006 |
|
RU2323879C2 |
| АДДУКТЫ ХИТОЗАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1999 |
|
RU2172745C2 |
| ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТ ПОЛИЭТИЛЕНИМИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2556930C2 |
| ДОДЕКАГИДРО-КЛОЗО-ДОДЕКАБОРАТ УРОТРОПИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2282586C1 |
Описан перхлорат хитозания состава С6О4Н9NH3ClO4, который наряду с такими свойствами как взрывобезопасность, нетоксичность, устойчивость к влаге, нагреванию и механическому воздействию обладает высокими окислительными свойствами и свойствами связующего, что позволяет использовать его в энергоемких составах в смеси с додекагидро-клозо-додекаборатом хитозания, где он дополнительно несет функцию связующего. Количественное соотношение в композиции между додекагидро-клозо-додекаборатом хитозания и перхлоратом хитозания определяется требуемым режимом горения смеси: чем больше содержание перхлората хитозания, тем выше активность состава. 3 н.п. ф-лы, 1 ил.
| RU 2005134392 А, 10.06.2006 | |||
| ПОЛИЭДРИЧЕСКИЕ КЛОЗО-ГИДРОБОРАТЫ ХИТОЗАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2158221C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФАТИРОВАННОГО ХИТОЗАНА | 1992 |
|
RU2048474C1 |
| АДДУКТЫ ХИТОЗАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1999 |
|
RU2172745C2 |
Авторы
Даты
2008-01-27—Публикация
2006-08-08—Подача