Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса хиноксалин-3-спиро-2-пирролов и к способу их получения, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем, а также в медицине.
Известны структурные аналоги заявленных соединений, получаемые взаимодействием 1-арил-4-ароил-5-метоксикарбонил-2,3-дигидро-2,3-пирролдионов с замещенными 3-амино-5,5-диметил-2-циклогексен-1-онами в абсолютном бензоле (Журнал органической химии. 2004. Т.40. Вып.12. С 1840). Синтез структурных аналогов осуществляется по следующей схеме:
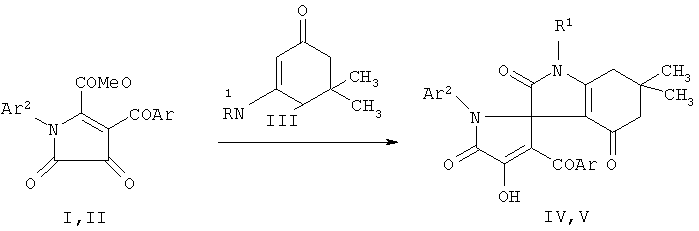
I,IV: Ar1=С6Н5, Ar2=С6Н4Cl-n; II,V: Ar1=С6Н4ОС2Н5-n, Ar2=С6Н4СН3-n
К недостаткам данного способа относится невозможность получения 1-ароилокси-4-гидрокси-3-оксо-1,2,3,4,4a,5,6,7,8,8а-декагидрохиноксалин-2-спиро(1-о-гидроксифенил-4,5-диоксо-2,3,4,5-тетрагидропирролов).
Задачей изобретения является разработка простого способа синтеза новых неописанных в литературе 1-ароилокси-4-гидрокси-3-оксо-1,2,3,4,4а,5,6,7,8,8a-декагидрохиноксалин-2-спиро(1-о-гидроксифенил-4,5-диоксо-2,3,4,5-тетрагидропирролов) с целью расширения ассортимента потенциальных антимикробных средств.
Поставленная задача осуществляется путем кипячения 3-ароил-2,4-дигидро-1Hпирроло[2,1-с][1,4]бензоксазин-1,2,4-трионов с 1,2-дигидроксиламиноциклогексаном, взятыми в соотношении 1:1, в инертном алротонном растворителе по схеме:
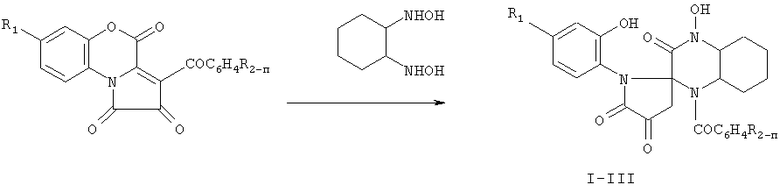
Процесс ведут при температуре 78-82°С, а в качестве растворителя используют абсолютный ацетонитрил. Данная реакция сопровождается неожиданной [1,4]миграцией ароильной группы от атома углерода к атому кислорода (С→O) в гетеросистеме декагидрохиноксалин-2-спиро-тетрагидропиррола.
Из патентной и технической литературы не были выявлены способы получения 1-ароилокси-4-гидрокси-3-оксо-1,2,3,4,4а,5,6,7,8,8а-декагидрохиноксалин-2-спиро(1-о-гидроксифенил-4,5-диоксо-2,3,4,5-тетрагидропирролов), имеющие сходные признаки с заявляемым способом, а именно не использовались исходные вещества, растворители, в которых проходит реакция, и температура, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 1-Бензоилокси-4-гидрокси-3-оксо-1,2,3,4,4а,5,6,7,8,8а-декагидро-хиноксалин-2-спиро-2-(1-о-гидроксифенил-4,5-диоксо-2,3,4,5-тетрагидропиррол) (I)
К раствору 3.33 г (10 ммоль) 3-бензоил-2,4-дигидро-7-метил-1H-пирроло[2,1-с][1,4]бензоксазин-1,2,4-триона в 50 мл ацетонитрила добавляли по каплям 1.49 г (10 ммоль) ди(гидроксиламино)циклогексана в 30 мл ацетонитрила, кипятили в течение 3-5 мин при температуре 78-82°С, охлаждали. Выпавшие через сутки бесцветные кристаллы соединения (I) отфильтровали, кристаллизовали из ацетонитрила. Выход 3.74 г (78%). Т.пл. 210-212°С.
Найдено, %: С 62.42; Н 5.30; N 8.82. C25H25N3O7
Вычислено, %: С 62.62; Н 5.26; N 8.76
Пример 2. 1-n-Толилокси-4-гидрокси-3-оксо-1,2,3,4,4а,5,6,7,8,8а-декагидрохиноксалин-2-спиро-2-(1-o-гидроксифенил-4,5-диоксо-2,3,4,5-тетрагидропиррол) (II)
К раствору 3.33 г (10 ммоль) 3-толуоил-2,4-дигидро-1H-пирроло[2,1-с][1,4]бензоксазин-1,2,4-триона в 50 мл ацетонитрила добавляли по каплям 1.49 г (10 ммоль) ди(гидроксиламино)циклогексана, кипятили в течение 3-5 мин при температуре 78-82°С, охлаждали. Выпавшие через сутки бесцветные кристаллы соединения (II) отфильтровали, кристаллизовали из ацетонитрила. Выход 3.84 г (80%). Т.пл. 161-162°С (разл).
Найдено, %: С 62.59; Н 5.19; N 8.80. C25H25N3О7
Вычислено, %: С 62.62; Н 5.26; N 8.76
Пример 3. 1-n-Толилокси-4-гидрокси-3-оксо-1,2,3,4,4а,5,6,7,8,8а-декагидрохиноксалин-2-спиро-2-(2-гидрокси-4-метилфенил-4,5-диоксо-2,3,4,5-тетрагидропиррол) (III)
К раствору 3.47 г (10 ммоль) 3-толуоил-2,4-дигидро-7-метил-1H-пирроло[2,1-с][1,4]бензоксазин-1,2,4-триона в 50 мл ацетонитрила добавляли по каплям 1.49 г (10 ммоль) ди(гидроксиламино)циклогексана в 30 мл ацетонитрила, кипятили в течение 3-5 мин при температуре 78-82°С, охлаждали. Выпавшие через сутки бесцветные кристаллы соединения (III) отфильтровали, кристаллизовали из ацетонитрила. Выход 3.90 г (79%), Т.пл. 199-200°С (разл.).
Найдено, %: С 63.19; Н 5.48; N 8.49. С26H27N3О7
Вычислено, %: С 63.28; Н 5.51; N 8.51
Пример 4. Соединение III обладает слабой антимикробной активностью. Противомикробное действие изучали методом двукратных серийных разведений в мясопептонном бульоне [1] по отношению к условно-патогенным культурам кишечной палочки Escherichia coli (штамм 1257) и золотистого стафилококка Staphylococcus aureus (штамм 209-Р). Минимальная ингибирующая концентрация (МИК) соединения III составляет 2000 мкг/мл, что находится на уровне используемого на практике антимикробного препарата этакридина лактата (2000/500 мкг/мл) и превышает активность все еще используемого в медицинской практике бесалола (фенилсалицилата) (4000/4000 мкг/мл) [2].
В ИК спектрах (вазелиновое масло) соединений I-III наблюдаются полосы валентных колебаний следующих групп: группы ОН в области 3250-3410 см-1, лактамной и лактонной групп - 1740-1780 см-1, кетонной группы - 1730-1740 см-1, ароильной группы - 1650-1690 см-1.
В спектрах ЯМР1Н соединений I-III, снятых в ДМСО-d6, кроме сигналов ароматических протонов и связанных с ними групп, присутствуют следующие сигналы: триплет 2 протонов метиленовой группы в области - 1.25-1.27 м.д., мультиплет 4 метиленовых протонов - 1.56-1.58 м.д., сигналы двух неэквивалетных протонов в виде дублета дублетов в области 1.51-2.03 (2Н, СН2), сигналы 2 метиленовых протонов (АВ-система) в области 3.06-3.65 м.д., два синглета фенольных ОН групп в области 8.65-10.54 м.д. Структура соед. 111 подтверждена данными РСА.
Предлагаемый способ достаточно прост в осуществлении, одностадиен и позволяет получить неописанные в литературе 1-алкил-6,6-диметил-2,4-диоксо-2,3,4,5,6,7-гексагндро-1H-индол-3-спиро-2-(1-арил-3-ароил-4-гидрокси-5-оксо-2,5-дигидропирролы) практически с количественным выходом. Указанные соединения являются перспективными в качестве исходных веществ для синтеза новых гетероциклических систем, а также найдут применение в медицине.
Список литературы
1. Першин Г.Н. Методы экспериментальной химиотерапии. М.: Медицина, 1971. С.100.
2. Машковский М.Д. Лекарственные средства. Т.2. М.: Медицина, 1985. С.398, 409.
Настоящее изобретение относится к новым соединениям класса хиноксалин-2-спиропирролов общей формулы I
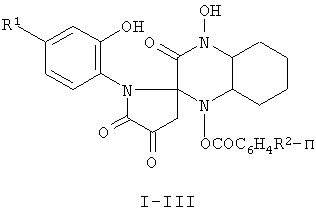
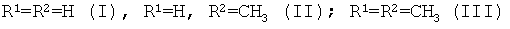
Соединения могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине в качестве антимикробных средств. Описан также способ получения соединений. 2 н.п. ф-лы.
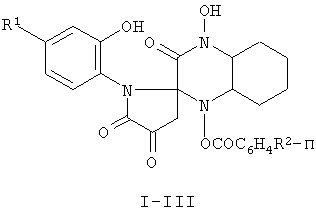
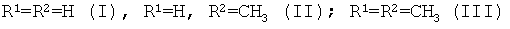
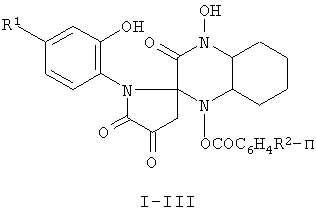
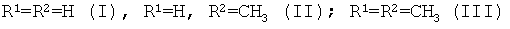
заключающийся, в том, что 3-ароил-2,4-дигидро-1Н-пирроло[2,1-с][1,4]бензоксазин-1,2,4-трионы подвергают взаимодействию с 1,2-ди(гидроксиламино)циклогексаном при температуре 78-82°С в среде инертного апротонного растворителя (абсолютный ацетонитрил) с последующим выделением целевых продуктов.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2008-03-27—Публикация
2007-01-31—Подача