Изобретение относится к области органической химии, а именно к способу получения новых индивидуальных соединений класса индол-3-спиро-2-пирролов, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем.
Известны структурные аналоги заявляемых соединений, получаемые взаимодействием пирроло[2,1-с][1,4]бензоксазин-1,2,4-трионов с 3-амино-5,5-диметил-2-циклогексен-1-оном (Химия Гетероциклических Соединений, 2002, Вып. 4. С. 563). Синтез структурных аналогов осуществляется по следующей схеме 1:
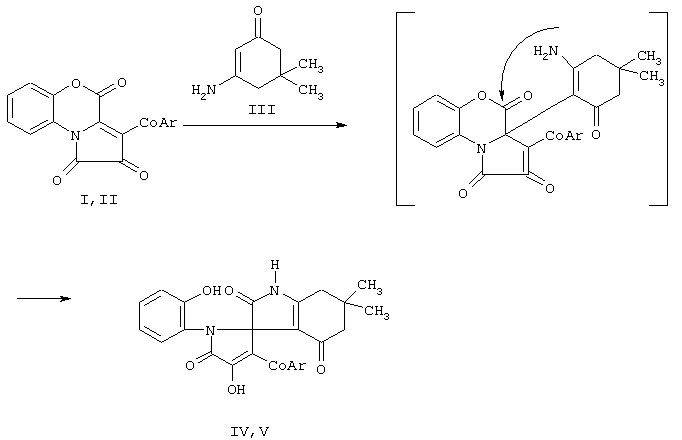
где I, IV: Ar - p-CH3С6H4; II,V: Ar - α-C10H7.
К недостаткам данного способа относится невозможность получения 1-алкил-6,6-диметил-2,4-диоксо-2,3,4,5,6,7-гексагидро-1H-индол-3-спиро-2-(1-арил-3-ароил-4-гидрокси-5-оксо-2,5-дигидропирролов).
Задачей изобретения является разработка простого способа синтеза не описанных в литературе 1-алкил-6,6-диметил-2,4-диоксо-2,3,4,5,6,7-гексагидро-1H-индол-3-спиро-2-(1-арил-3-ароил-4-гидрокси-5-оксо-2,5-дигидропирролов).
Поставленная задача осуществляется путем кипячения 1-арил-4-ароил-5-метоксикарбонил-2,3-дигидро-2,3-пирролдионов с 3-алкиламино-5,5-диметилциклогексен-2-онами-1, взятыми в соотношении 1:1, в инертном апротонном растворителе по схеме 2:
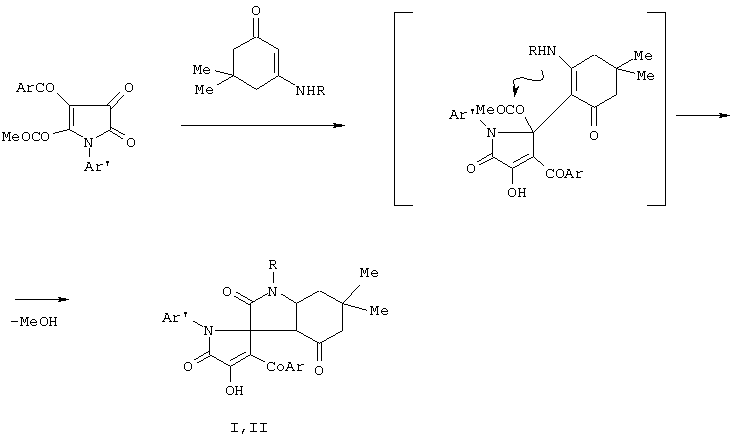
где R - СН2С6Н5 (I), С6Н11-c (II); Ar - p-NO2С6Н4 (I), С6Н5 (II); Ar’ - C6H5 (I), p-СlС6Н4 (II).
Процесс ведут при температуре 79-80°С, а в качестве растворителя используют абсолютный бензол.
Из патентной и технической литературы не были выявлены способы получения 1-алкил-6,6-диметил-2,4-диоксо-2,3,4,5,6,7-гексагидро-1H-индол-3-спиро-2-(1-арил-3-ароил-4-гидрокси-5-оксо-2,5-дигидропирролов), имеющие сходные признаки с заявляемым способом, а именно не использовались исходные продукты, растворители, в которых проходит реакция, и интервал температур, на основании чего можно сделать вывод о соответствии заявленного технического решения критериям “новизна” и “изобретательский уровень”.
Изобретение иллюстрируется следующими примерами.
Пример 1. 1-Бензил-6,6-диметил-2,4-диоксо-2,3,4,5,6,7-гексагидро-1Н-индол-3-спиро-2-(4-гидрокси-3-n-нитробензоил-5-оксо-1-фенил-2,5-дигидропиррол) (I).
К раствору 0,005 моль 5-метоксикарбонил-4-n-нитробензоил-1-фенил-2,3-дигидро-2,3-пирролдиона в 2 мл абсолютного бензола добавили раствор 0,005 моль 5,5-диметил-3-бензиламиноциклогексен-2-она-1, кипятили в течение 10 мин, охладили, выпавший осадок отфильтровали. Выход 95%. Т.пл. 254-256°С (разл., из этилацетата). Соединение (I) C33H27N3O7.
Найдено, %: С 68,66; Н 4,68; N 7,31.
Вычислено, %: С 68,62; Н 4,71; N 7,27.
Пример 2. 6,6-Диметил-2,4-диоксо-1-циклогексил-2,3,4,5,6,7-гексагидро-1H-индол-3-спиро-2-(3-бензоил-4-гидрокси-5-оксо-1-n-хлорфенил-2,5-дигидропиррол) (II).
К раствору 0,005 моль 4-бензоил-5-метоксикарбонил-1-n-хлорфенилфенил-2,3-дигидро-2,3-пирролдиона в 2 мл абсолютного бензола добавили раствор 0,005 моль 5,5-диметил-3-циклогексиламиноциклогексен-2-она-1, кипятили в течение 10 мин, охладили, выпавший осадок отфильтровали. Выход 95%. Т.пл. 251-252°С (разл., из этилацетата). Соединение (II) С32Н31СlN2O5.
Найдено,%: С 68,69; Н 5,52; С1 6,40; N 5,00.
Вычислено,%: С 68,75; Н 5,59; С1 6,34; N 5,01.
Соединения (I, II) - светло-желтые кристаллические вещества с высокими температурами плавления, легкорастворимые в ДМСО и ДМФА, труднорастворимые в обычных органических растворителях, нерастворимые в воде и алканах, дающие положительную пробу (вишневое окрашивание) на наличие енольного гидроксила со спиртовым раствором хлорида железа (III). Устойчивы при хранении в обычных условиях.
В ИК спектрах соединений (I, II), снятых в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний енольной группы ОН в виде широкой полосы в области 3180-3240 см-1, двух лактамных карбонильных групп в виде одной или двух полос в области 1730-1750 см-1, двух еноновых карбонильных групп в виде широкой полосы в области 1630-1640 см-1.
В спектрах ПМР соединений (I, II), снятых в растворе в ДМСО-d6, кроме сигналов протонов ароматических колец присутствуют два синглета метильных групп в области 0,60-0,90 м.д., сигналы неэквивалентных протонов двух групп СН2 димедонового фрагмента в виде группы сигналов в области 2,00-2,45 м.д., сигналы двух протонов группы СН2 бензильного фрагмента [у соединения (I)] в виде дублета дублетов (АВ-системы), расщепленные вследствие неэквивалентности из-за соседства с хиральным центром, в области 4,80-5,08 м.д., сигналы протонов циклогексильного остатка [у соединения (II)].
Предлагаемый способ достаточно прост в осуществлении, одностадиен и позволяет получить не описанные в литературе 1-алкил-6,6-диметил-2,4-диоксо-2,3,4,5,6,7-гексагидро-1H-индол-3-спиро-2-(1-арил-3-ароил-4-гидрокси-5-оксо-2,5-дигидропирролы) практически с количественным выходом.
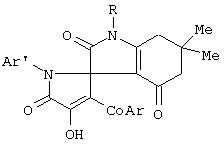
Изобретение относится к области органической химии, а именно к способу получения новых индивидуальных соединений класса индол-3-спиро-2-пирролов формулы
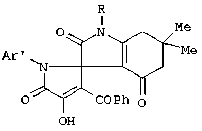
где R - СН2С6Н5 (I), С6Н11-c (II); Ar - p-NO2С6Н4 (I), С6Н5 (II); Ar’ - C6H5 (I), p-ClC6Н4 (II). Способ заключается во взаимодействии 1-арил-4-ароил-5-метоксикарбонил-2,3-дигидро-2,3-пирролдиона формулы
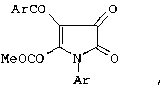
с 3-алкиламино-5,5-диметилциклогексен-2-оном-1 формулы
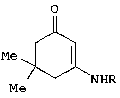
в среде инертного апротонного растворителя, например абсолютного бензола, при температуре 79-80°С с последующим выделением целевых продуктов. Получаемые соединения могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем. 2 з.п. ф-лы.
где R - СН2С6Н5 (I), С6Н11-c (II);
Ar - p-NO2С6Н4 (I), С6Н5 (II);
Ar’ - C6H5 (I), p-СlС6Н4 (II),
отличающийся тем, что 1-арил-4-ароил-5-метоксикарбонил-2,3-дигидро-2,3-пирролдионы
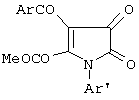
подвергают взаимодействию с 3-алкиламино-5,5-диметилциклогексен-2-онами-1
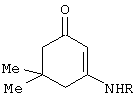
в среде инертного апротонного растворителя с последующим выделением целевых продуктов.
| Химия гетероциклических соединений | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| ПРИСПОСОБЛЕНИЕ К КОСЕ ДЛЯ КОСЬБЫ ДВУМЯ РУКАМИ (ОКОСЬЕ) | 1921 |
|
SU565A1 |
Авторы
Даты
2004-10-20—Публикация
2003-05-19—Подача