ОБЛАСТЬ ТЕХНИКИ
Это изобретение относится к лингвальным таблеткам, иными словами, к таблеткам для перорального введения, которые быстро дезинтегрируют (рассасываются) в полости рта, в частности, менее чем за 30 секунд, и к способу их изготовления.
ПРЕПШЕСТВУЮШИЙ УРОВЕНЬ ТЕХНИКИ
Создание твердых лекарственных форм, которые быстро дезинтегрируют (рассасываются) во рту, не требуя воды, вызвало большой интерес к преимуществам этих лекарственных форм, которые предполагают их применение для пациентов, имеющих проблемы с глотанием, таких как старики, дети младшего возраста, пациенты с психическими расстройствами и неконтактные пациенты, а также для населения в целом, поскольку это позволяет принимать лекарство не запивая его водой.
В Приложении 4.1 к 4 изданию Европейской фармакопеи, опубликованному в октябре 2001 года, лингвальные (orally disintegrating) таблетки определены как непокрытые оболочкой таблетки для размещения во рту, которые быстро дезинтегрируют (рассасываются) до того, как они будут проглочены. В этом документе также установлено время 3 минуты, как временной интервал, за который они должны дезинтегрировать в тесте на дезинтеграцию для таблеток и капсул в соответствии со способом 2.9.1. Европейской фармакопеи.
Были разработаны различные технологии, основанные на альтернативных способах, которые в отличие от стандартных способов, применяющихся для получения таблеток, позволяют получать лекарственные формы, быстро рассасывающиеся в полости рта и имеющие очень приятный вкус. Самые известные включают технологии, позволяющие получать лиофилизаты - матриксы для перорального приема, путем прессования частиц "волокон сдвинутой формы" ("shearform floss") на основе сахарида и пленок или облаток. Однако композиции, полученные с использованием указанных технологий, в большей или меньшей степени обладают такими недостатками, как их высокая ломкость, чрезвычайная чувствительность к атмосферной влажности, технологические трудности при получении и, в особенности, высокая стоимость при производстве в промышленном масштабе.
Чтобы упростить упомянутые технологии и, в частности, чтобы уменьшить затраты на производство и преодолеть указанные недостатки, были оптимизированы стандартные способы производства таблеток.
Наиболее часто применяемые способы изготовления таблеток включают:
a) Получение таблеток прямым прессованием смесей, которые содержат, по меньшей мере, один неорганический нерастворимый в воде наполнитель, например, фосфат кальция, один или более дезинтегрирующих агентов, например, кросповидон, и возможно, водорастворимые наполнители. Указанная технология зарегистрирована как Ziplets® фирмой Eurand и описана в международной публикации WO 9944580. Однако применяемые композиции содержат высокий процент нерастворимых наполнителей, значительное количество которых остается во рту и ставит под угрозу их вкусовую привлекательность.
b) Получение таблеток посредством прямого прессования смесей, которые содержат, по меньшей мере, наполнитель для непрямого прессования, например, декстрозу, маннит, сорбит, лактозу, и смазывающий агент. Указанная технология зарегистрирована как Durasolv® фирмой Cima и описана в патенте США №6024981.
c) Получение многокомпонентных таблеток, изготовленных из смесей микроинкапсулированных активных ингредиентов и наполнителей, которые содержат один или несколько дезинтегрирующих агентов, один или несколько гигроскопичных агентов и растворимый разбавитель для прямого прессования. Указанная технология зарегистрирована как Flashtab® фирмой Prographarm и описана в патенте ЕР 0548356.
d) Получение лингвальных таблеток, которые дезинтегрируют (рассасываются) в полости рта менее чем через 60 секунд и которые содержат высушенный распылением маннит, кросповидон и другие наполнители, посредством прямого прессования. Указанная технология описана в международной публикации WO 00/57857 фирмой Yuhan Corporation.
Однако все упомянутые способы изготовления таблеток имеют, в большей или меньшей степени, следующие недостатки:
- высокое содержание нерастворимых наполнителей или микроинкапсулированных активных ингредиентов, которые дают композицию, которая после того как она распадается в полости рта вызывает ощущение зернистости и, следовательно, проблемы, касающиеся вкусовой привлекательности.
- чрезмерно длительное время дезинтеграции таблетки по сравнению с лиофилизатами или облатками для перорального приема, которые обычно растворяются менее чем через 10 секунд.
- недостаточная механическая прочность таблетки, для того чтобы выдерживать стандартные процедуры упаковки и транспортировки.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В первом аспекте настоящего изобретения предложены таблетки для перорального введения, которые быстро дезинтегрируют (рассасываются) в полости рта, в частности, менее чем за 30 секунд, и которые едва могут быть замечены на языке после их дезинтеграции (рассасывания).
Во втором аспекте настоящего изобретения предложен способ изготовления указанных лингвальных таблеток (таблеток для рассасывания) посредством прямого прессования, где прямое прессование понимают как способ производства, который включает только операции просеивания, смешивания и прессования.
В настоящем изобретении неожиданно было обнаружено, что при использовании разбавителя с высокой скоростью растворения и высокой прессуемостью и при ограничении количественного соотношения и размера частиц нерастворимых ингредиентов можно получать смеси с оптимальной прессуемостью. Эти смеси позволяют получать лингвальные таблетки, которые рассасываются во рту менее чем за 30 секунд, предпочтительно менее чем за 20 секунд, после того как они приходят в контакт со слюной в полости рта, и которые едва заметны на языке.
Дополнительное преимущество состоит в том, что таблетки, описанные в изобретении, обладают достаточной механической прочностью, чтобы выдерживать процессы производства и обращения лекарственных средств, в отличие от других быстро дезинтегрирующих композиций, таких как пероральные лиофилизаты, таблетки из "волокон сдвинутой формы" ("shearform floss") на основе сахарида и облаток. Таблетки согласно настоящему изобретению имеют хрупкость менее 0,5%, предпочтительно менее 0,2%, как установлено в соответствии с п.2.9.7. Европейской фармакопеи. Эти значения хрупкости позволяют упаковывать их в любой вид упаковки, используя стандартное производственное оборудование, и не требуют специального внимания при хранении на промежуточном складе для бестарного хранения таблеток или в дозирующих системах, использующихся в процессе упаковки.
Таким образом, первый аспект настоящего изобретения относится к таблетке для перорального введения, как определено в пп.1-11 формулы изобретения.
Теоретически в этом изобретении не существует никаких ограничений, касающихся активных ингредиентов, хотя активные ингредиенты, показанные для пациентов, имеющих проблемы с глотанием, таких как дети младшего возраста (до 2-7 лет), или старики, и/или неконтактные пациенты, например пациенты с психическими расстройствами, являются предпочтительными кандидатами.
Особый интерес представляют активные ингредиенты с дозировкой предпочтительно менее 50 мг на таблетку. Предпочтительные соединения выбирают из следующих ингредиентов (но не ограничиваются ими): противоязвенные средства: фамотидин; противорвотные средства: ондансетрон, гранисетрон, доласетрон, домперидон, метоклопрамид; гипотензивные средства: эналаприл, лозартан, кандезартан, валзартан, лизиноприл, рамиприл, доксазозин, теразозин; антигистаминные средства: лоратадин, цетиризин; нейролептические средства: рисперидон, оланзапин, кветиапин; антидепрессанты: пароксетин, флуоксетин, миртазапин; анальгетики и противовоспалительные средства: пироксикам; антигиперхолестеринемические средства: симвастатин, ловастатин, правастатин; средства против мигрени: золмитриптан, наратриптан, ризатриптан; противоэпилептические средства: ламотригин; противопаркинсонические средства: селегилин, апоморфин; анксиолитики: диазепам, лоразепам, золпидем; противоастматические средства: зафирлукаст, монтелукаст; агенты против эректильной дисфункции: силденафил; как в форме их свободного основания, так и в форме их фармацевтически приемлемых солей, гидратов, сольватов или изомеров.
Лингвальные таблетки, описанные в настоящем изобретении, распадаются менее чем через 30 секунд, предпочтительно, менее чем через 20 секунд, после того как они приходят в контакт со слюной в полости рта. Для определения времени дезинтеграции (рассасывания) вместе с тестом на дезинтеграцию in vivo был стандартизирован альтернативный способ in vitro, который является более дифференцированным, чем способ, описанный в 2.9.1. Европейской фармакопеи. Как видно, значения, полученные в обоих тестах, являются воспроизводимыми и взаимосвязанными, так как результаты, полученные in vivo, всегда меньше, чем результаты, полученные in vitro (см. Экспериментальная часть, Пример 1). Используемые тесты описаны ниже в части "характеристика таблеток", представленной в Экспериментальной части этого изобретения.
Высушенный распылением маннит - наполнитель, который имеется в продаже, такой как высушенный распылением маннит Mannogen™ EZ фирмы SPI Pharma и Pearlitol® SD фирмы Roquette, имеет физико-химические свойства, которые делают его идеальным для создания подходящего разбавителя для этого изобретения. Следующее представляет особый интерес:
- Он легко растворяется в воде (1 часть маннита в 5,5 частях воды при 20°С);
- Он быстро растворяется в воде (5 г растворяются примерно через 5 сек в 150 мл воды при 20°С). Эта скорость дезинтеграции является гораздо более высокой, чем скорость дезинтеграции маннита, полученного прямым прессованием, порошкообразного маннита и других родственных сахаридных наполнителей. Высушенный распылением маннит образуется в основном кристаллической формой α, в отличие от других типов маннита, которые образуются β-формой. Обе формы можно легко различить с помощью ИК-спектра.
- Он имеет оптимальную текучесть для способов прямого прессования (сыпучесть: 6 секунд, и осаждаемость: 16-18 мл).
- Он обладает высокой прессуемостью (коэффициент сцепления (Cohesion Index): 1500-2000).
- Он обладает хорошей разбавляющей способностью благодаря размеру и форме частиц, что позволяет адсорбировать большое количество активных ингредиентов, которые с трудом прессуются.
- Он представляет собой продукт, который при воздействии на него давления деформируется путем раздавливания, образуя новые поверхности частиц и становясь нечувствительным к потере прессуемости благодаря большему смазыванию гидрофобными смазывающими агентами.
- Он является химически очень стабильным, негигроскопичным и не вступает в реакции Майяра (Maillard) с аминогруппами подобно другим родственным сахаридным наполнителям.
- Он имеет оптимальные органолептические свойства благодаря отрицательной теплоте растворения (ощущение свежести), его подслащивающей способности, составляющей примерно 50% от таковой для сахарозы, и его превосходному вкусу из-за небольшого размера частиц.
Было установлено, что соединения по настоящему изобретению должны содержать, по меньшей мере, 59,5% высушенного распылением маннита.
Что касается растворяющей способности высушенного распылением маннита, то в общем было установлено, что для того чтобы гарантировать прессуемость и текучесть смеси, которая подлежит прессованию, содержание активного ингредиента не должно превышать 10 мас.% от общей массы таблетки. А для гарантии приятного вкуса конечного продукта и однородности смеси активный ингредиент должен представлять собой тонкий порошок, где, по меньшей мере, 90 мас.% активного ингредиента имеют размер частиц менее 100 мкм.
Для минимизации времени дезинтеграции и максимизации механической прочности таблеток по настоящему изобретению была разработана система активации дезинтеграции, включающая следующее:
- Микрокристаллическую целлюлозу (например, Avicel® PH 101 или Emcocel® 50 М) со средним размером частиц примерно 50 мкм, где, по меньшей мере, 99 мас.% микрокристаллической целлюлозы имеют размер частиц менее 250 мкм. Относительное количество микрокристаллической целлюлозы составляет от 10 до 18 мас.% от общей массы таблетки, предпочтительно, от 12 до 15%. Указанное количество позволяет существенно улучшить прессуемость, уменьшить хрупкость и достичь существенного уменьшения времени дезинтеграции. Более высокие количества имеют отрицательное влияние на вкусовую привлекательность композиции, а меньшие количества ухудшают возможности активатора дезинтеграции.
- Кроскармеллозу натрия (например, Ac-Di-Sol®), присутствующую в количестве от 1 до 4% от общей массы таблетки, предпочтительно, от 2 до 3%. Более высокие количества имеют отрицательное влияние на вкусовую привлекательность композиции и не дают значительных преимуществ в отношении скорости дезинтеграции.
- При необходимости, может быть добавлен поглотитель влажности, такой как осажденный силикагель (например, Syloid®) в количестве от 0,1 до 0,5 мас.% от общей массы таблетки, который может нейтрализовать гидрофобность некоторых активных ингредиентов и улучшить текучесть смеси.
Предпочтительно, чтобы указанная система активации дезинтеграции присутствовала в количестве от 14 до 18,5% от общей массы смеси.
Для улучшения приема пациентом, таблетки по настоящему изобретению могут содержать также систему подсластитель/корригент, включающую:
Искусственный подсластитель или его комбинацию, которые должны соответствовать органолептическим свойствам активного ингредиента. Можно использовать следующее, но этот перечень не исключает других вариантов: аспартам, цикламат натрия, сахарин натрия, глицирризинат аммония, неогесперидина дигидрохалкон. Содержание искусственного подсластителя составляет от 0,5 до 2 мас.% от общей массы таблетки.
- Корригент, предпочтительно микроинкапсулированный порошковый корригект на носителе, который растворяется и дезинтегрирует в воде. Содержание корригента составляет от 0,5 до 2 мас.% от общей массы таблетки.
При необходимости, могут быть добавлены ионообменные смолы или полимеры, которые образуют комплексы с активными ингредиентами, позволяющие маскировать неприятный вкус. Можно использовать следующее, но этот перечень не исключает других вариантов: поливидон, β-циклодекстрин, полакрилин калия.
Особенно хорошие результаты, что касается маскировки неприятного вкуса активных ингредиентов, были получены при использовании системы, включающей аспартам, глицирризинат аммония, ментоловый ароматизатор и L-ментол (0,1-0,2 мас.%), которая благодаря ее освежающему эффекту имеет синергический эффект с высушенным распылением маннитом и хорошую способность корригировать вкус и запах лекарства благодаря ее остаточному эффекту. Поэтому композиция по настоящему изобретению с использованием этой системы подсластитель/корригент является выгодной, так как ее приготовление не связано с применением дорогостоящих способов, таких как микроинкапсуляция или покрытие оболочкой активных ингредиентов для маскировки их горького вкуса.
В конце концов, для облегчения процедуры прессования должны быть добавлены смазывающий агент и, при необходимости, антиагдезионный (противоприлипающий) агент в подходящем соотношении. Хотя предпочтительным смазывающим агентом является стеарат магния, могут быть использованы и другие, менее гидрофобные смазывающие агенты, противостоящие гидрофобности в случае некоторых специфических активных ингредиентов, таких как фумарат натрия, полиэтиленгликоль 6000, лаурилсульфат натрия и комбинация стеарата магния с лаурилсульфатом натрия (9:1) и эфиры сахарозы. Относительное количество смазывающего агента должно составлять от 0,5 до 2 мас.% от общей массы таблетки. Относительное количество антиагдезионного агента, такого как тальк, коллоидный диоксид кремния, должно составлять от 0,5 до 2 мас.% от общей массы таблетки.
Другое преимущество состоит в том, что вкусовая привлекательность улучшается еще больше, если относительное количество нерастворимых ингредиентов составляет менее 20%. Нерастворимые ингредиенты композиции по изобретению включают микрокристаллическую целлюлозу, кроскармеллозу натрия, поглотитель влажности, смазывающие агенты, антиагдезионные агенты и нерастворимые активные ингредиенты.
Настоящее изобретение демонстрирует, что можно оказывать существенное влияние на скорость рассасывания таблетки, изменяя размеры и форму таблетки. Обычно чем тоньше таблетка и больше ее пористость, тем быстрее нарушается структура матрикса, когда он соприкасается со слюной, так как процесс рассасывания (дезинтеграции) начинается после смачивания всего матрикса с помощью капиллярного воздействия. Также любая форма, которая максимизирует поверхность контакта со слюной, будет вызывать значительное уменьшение времени рассасывания, давая значения рассасывания менее 20 секунд. Предпочтительной формой по настоящему изобретению является плоская, круглая, со скошенными краями таблетка толщиной от 2,2 до 1,8 мм, хотя этим вариантом не ограничиваются.
Таким образом, смеси из указанных компонентов должны быть преобразованы в лингвальные таблетки (таблетки для рассасывания) в соответствии со способом их изготовления, описанным ниже и определенным в пунктах 12-14 формулы изобретения. Согласно изобретению, таблетки имеют:
- Хрупкость менее 0,5%, предпочтительно, менее 0,2%.
- Время рассасывания в полости рта менее 30 секунд, предпочтительно, менее 20 секунд.
- Объемную плотность от 1,1 до 1,3 г/мл.
Объемную плотность таблеток вычисляют путем деления массы (м) на объем (например, если таблетка является плоской и круглой, аналогично предпочтительной форме, предложенной настоящим изобретением, V=π·r2·h, где r представляет собой радиус и h - толщину таблетки). Было показано, что объемные плотности таблеток, полученные из композиций по настоящему изобретению, коррелируют с прочностью таблеток на излом и со временем их рассасывания во рту. Было также показано, что таблетки с объемными плотностями от 1,1 до 1,3 г/мл позволяют гарантировать такие технические требования хрупкости и дезинтеграции (рассасывания), которые являются задачей настоящего изобретения.
Обратили внимание также на то, что для того чтобы гарантировать выполнение такого технического требования как время рассасывания в полости рта, таблетки должны дезинтегрировать менее чем за 40 секунд в тесте на дезинтеграцию in vitro, описанном в Экспериментальной части настоящего изобретения, в части, посвященной характеристике таблеток.
Как указано выше, настоящее изобретение также относится к способу изготовления указанных лингвальных таблеток, включающему прямое прессование. Таблетки, описанные в изобретении, получают путем прессования порошкообразной смеси в твердую форму, размеры и форма которой позволяют еще больше минимизировать время дезинтеграции (рассасывания).
В частности, способ изготовления таблетки для перорального введения, как определено выше, включает следующие стадии:
1) Просеивание и смешивание компонентов, за исключением смазывающего агента;
2) Просеивание смазывающего агента;
3) Смешивание всех компонентов;
4) Прямое прессование конечной смеси.
В некоторых случаях может потребоваться последовательное смешивание, для того чтобы гарантировать однородность содержимого смеси или функциональную активность некоторых наполнителей (например, смесей активного ингредиента с полимерами без корригирования вкуса).
Благодаря высокой прессуемости композиций по настоящему изобретению, можно получать таблетки с подходящей механической прочностью, используя низкие давления при осуществлении способа прессования, предпочтительно, от 3 до 10 кН.
Смеси, которые рассматриваются в качестве подходящих для прессования, представляют собой смеси, которые обладают сыпучестью менее или равной 10 секундам, определенной в соответствии со способом, описанным в 2.9.16. Европейской фармакопеи, и/или осаждаемостью (V10-V500) менее или равной 20 мл, определенной в соответствии с 2.9.15. Европейской фармакопеи.
Предпочтительно, смесь должна также обладать предпочтительным коэффициентом сцепления (Cl от англ. Cohesion Index) свыше 700, где Cl - наклон прямой линии, которая определяет значения твердости (Ньютоны) в соответствии с силой прессования (декаНьютоны), умноженной на 105.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Чертеж схематически демонстрирует тест на дезинтеграцию in vitro. На указанном чертеже, таблетку 1 помещают в чашку Петри 2 на фильтровальную бумагу с 9-10 мл среды 3 для дезинтеграции.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Конкретные осуществления настоящего изобретения представлены следующими примерами без ограничения объема изобретения.
Общий способ:
- Взвешивание всех компонентов композиции.
- Просеивание, за исключением смазывающего агента, через 0,5 мм сито.
- Смешивание в миксере Túrbula T2B в течение 5 минут.
- Просеивание смазывающего агента через 0,32 мм сито.
- Смешивание в миксере Túrbuia T2B в течение 2 минут.
- Прессование в машине, снабженной подходящим прессовочным оборудованием, в соответствии с техническими требованиями установленной массы, толщины и твердости.
Характеристика таблеток:
Твердость (Н):
Определяется в дюрометре Schleuniger 6D с использованием способа определения прочности на излом, описанного в 2.9.8. Европейской фармакопеи. Среднее значение и диапазон определений подробно описываются.
Масса (мг):
Определяется с помощью аналитических весов с использованием образца (пробы) из 10 таблеток. Среднее значение и диапазон определений подробно описываются.
Толщина (мм):
Определяется штангенциркулем с использованием образца из 10 таблеток. Среднее значение и диапазон определений подробно описываются.
Хрупкость (%):
Определяется в анализаторе хрупкости Pharmatest с использованием способа, описанного в 2.9.7. Европейской фармакопеи.
Прочность на разрыв (Предел прочности) (Н/мм2):
Вычисляется на основе средних значений твердости и толщины согласно формуле T=2·F/π·d·h; где "F" означает прочность на излом, "d" означает диаметр таблетки, и "h" означает толщину.
Тест(ы) на дезинтеграцию in vitro:
На стеклянную чашку Петри 100×10 мм помещают фильтровальную бумагу диаметром 90 мм (ссылка: WH 1442090) и наливают в указанную чашку при комнатной температуре 9-10 мл среды для дезинтеграции (10% (мас./мас.) водный раствор 6-водного хлорида кобальта (II) Со(Cl)2·6Н2O). Наклоняют чашку до тех пор, пока вся бумага не будет смочена и под ней не останется никаких воздушных пузырей. Сразу после приготовления таблетку помещают на чашку и включают хронометр. Наблюдают, как вода поднимается благодаря капиллярному воздействию, и конечной точкой дезинтеграции считают время, когда таблетка полностью увлажнится. На каждой чашке анализируют шесть таблеток (см. чертеж, тест на дезинтеграцию in vitro).
Тест(ы) на дезинтеграцию (рассасывание) in vivo:
Лингвальную таблетку кладут на язык, включают хронометр и активно сосут до тех пор, пока она полностью не дезинтегрирует. Считают, что полная дезинтеграция достигается, когда таблетка полностью разрушится во рту, даже если все же останется не проглоченный остаток. Отмечают время в секундах. Выполняют тест с максимальным количеством из трех таблеток.
Пример 1
Лингвальные таблетки плацебо получали, используя общий способ, описанный выше, и композицию, представленную в Таблице 1. Таблица 1 дает краткое изложение результатов, полученных при характеристике таблетки. Таблицы 2 и 3 суммируют результаты, полученные в тестах на дезинтеграцию in vitro и in vivo двумя разными специалистами.
Нет статистически значимых различий между индивидуумами при определении конечной точки в тесте на дезинтеграцию in vitro (p=0,9804).
Нет статистически значимых различий между индивидуумами при определении конечной точки в тесте на дезинтеграцию in vivo (p=0,4817). Однако есть различия между тестами на дезинтеграцию in vivo и in vitro (p<0,05). Обычно значения, полученные в тесте in vitro, выше значений, полученных in vivo.
Примеры 2-6
Были приготовлены пять лингвальных таблеток плацебо с соединениями для определения оптимального содержания системы активации дезинтеграции и предложенного разбавителя с использованием общего способа, описанного выше, и композиций, подробно описанных в Таблице 4. Результаты, полученные при характеристике таблеток, представлены в Таблице 5.
Результаты, полученные из этой серии экспериментов, подтверждают идеальную природу системы активации дезинтеграции, предложенную в настоящем изобретении.
Пример 7
Приготавливали смесь для лингвальных таблеток, содержащих ондансетрон, используя общий способ, описанный выше, с использованием композиции, представленной в Таблице 6. Чтобы определить влияние формы и размеров таблетки на время дезинтеграции, соединение прессовали тремя различными форматами. Полученные результаты представлены в Таблице 7.
Показано, что плоские таблетки распадаются значительно быстрее, чем выпуклые таблетки, и что толщина также оказывает влияние на время дезинтеграции.
Пример 8
Приготавливали смесь для лингвальных таблеток, содержащих гранисетрон, используя общий способ, описанный выше; используемая композиция и результаты представлены в Таблице 8.
Пример 9
Приготавливали смесь для лингвальных таблеток, содержащих рисперидон, используя общий способ, описанный выше; используемая композиция и результаты представлены в Таблице 9. Результаты, полученные при характеристике таблеток, также представлены в Таблице-9.
Пример 10
Приготавливали смесь для лингвальных таблеток, содержащих флуоксетин, используя общий способ, описанный выше; используемая композиция и результаты представлены в Таблице 10. Результаты, полученные при характеристике таблеток, также представлены в Таблице 10.
Пример 11
Приготавливали смесь для лингвальных таблеток, содержащих пароксетин, используя общий способ, описанный выше; используемая композиция и результаты представлены в Таблице 11. Результаты, полученные при характеристике таблеток, также представлены в Таблице 11.
Несмотря на то, что изобретение было описано со ссылкой на упомянутые конкретные примеры осуществления изобретения, все модификации и изменения, которые могут быть сделаны специалистом в данной области в качестве рутинной практики, должны рассматриваться в пределах объема правовой защиты настоящего изобретения.
Изобретение относится к лекарственным средствам и касается таблеток для перорального ведения, быстро рассасывающихся в полости рта, которые содержат, по меньшей мере, 59,5% высушенного распылением маннита; активный ингредиент в количестве менее или равном 10%; микрокристаллическую целлюлозу в количестве от 10 до 18% со средним размером частиц примерно 50 мкм, где, по меньшей мере, 99 мас.% микрокристаллической целлюлозы имеет размер частиц менее 250 мкм; 1-4% кроскармеллозы натрия и 0,5-2% смазывающего агента; где, если не указано иначе, проценты выражены по массе от общей массы таблетки. Также предложен способ, включающий: просеивание и смешивание компонентов, за исключением смазывающего агента; смешивание всех компонентов и прямое прессование конечной смеси. Таблетки согласно настоящему изобретению обладают меньшим временем рассасывания, улучшенной вкусовой привлекательностью и повышенной механической прочностью. 2 н. и 10 з.п. ф-лы, 1 ил., 11 табл.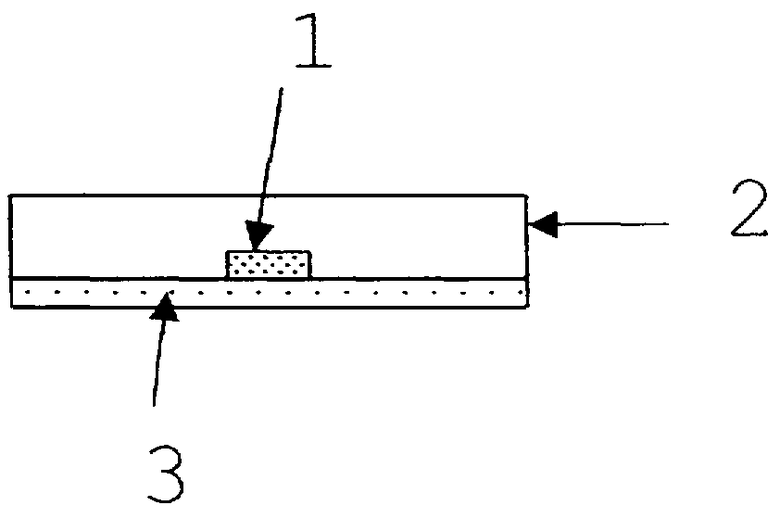
1) высушенный распылением маннит в количестве, по меньшей мере, 59,5%;
2) активный ингредиент в количестве меньшем или равном 10%,
3) микрокристаллическую целлюлозу в количестве от 10 до 18%, со средним размером частиц примерно 50 мкм, где, по меньшей мере, 99 мас.% микрокристаллической целлюлозы имеет размер частиц менее 250 мкм;
4) кроскармеллозу натрия в количестве от 1 до 4%; и
5) смазывающий агент в количестве от 0,5 до 2 мас.%,
где, если не указано иначе, проценты выражены по массе от общей массы таблетки.
1) просеивание и смешивание компонентов, за исключением смазывающего агента;
2) просеивание смазывающего агента;
3) смешивание всех компонентов; и
4) прямое прессование конечной смеси.
| Способ изготовления зеркальных лимбов, шкал и сеток | 1938 |
|
SU57857A1 |
| Питатель коробконамазывающей машины для автоматической линии набивки и окраски спичек | 1957 |
|
SU112161A1 |
Авторы
Даты
2008-04-10—Публикация
2003-06-04—Подача