Настоящая заявка испрашивает приоритет предварительной заявки Соединенных Штатов №60/474603, поданной 2 июня 2003 года, которая приведена здесь в качестве ссылки в полном объеме.
Область техники
Изобретение относится к области клинической патофизиологии и, более конкретно, к способам лечения нервно-мышечных нарушений, таких как мышечные дистрофии. Изобретение относится также к фармацевтическим композициям, содержащим кортикостероиды и ингибиторы роста и дифференцировки.
Уровень техники
Мышечные дистрофии (МД) являются прогрессирующими наследственными нервно-мышечными нарушениями, которые характеризуются мышечной атрофией и слабостью (Emery (2002) The Lancet, 358: 687-695). Большинство форм мышечных дистрофий являются летальными и в настоящее время неизлечимыми.
Наиболее распространенным заболеванием является мышечная дистрофия Дюшена (ДМД), Х-связанное нервно-мышечное заболевание. Эта болезнь обусловлена мутациями в гене ДМД, кодирующем дистрофин. Изменение или отсутствие этого белка приводит к патологическому разрыву плазматической мембраны мышечного волокна сарколеммы. Отличительными признаками данного заболевания являются патологическое изменение диаметра мышечных волокон (атрофические и гипертрофические волокна) в проксимальных мышцах и прогрессирующее повреждение мышц. Поврежденная мышца выделяет внутриклеточный фермент креатинкиназу (КК). В результате сывороточные уровни КК у пациентов с ДМД являются особенно высокими (до десятикратного уровня по сравнению с нормальным). Этот патофизиологический каскад осложняется воспалением ткани, некрозом мышечного волокна и заменой мышцы фиброзно-жировой тканью.
Другой аллельный вариант гена ДМД вызывает более мягкую форму МД, известную как мышечная дистрофия Беккера (БМД). БМД клинически сходна с ДМД, но возникновение симптомов происходит в более позднем возрасте.
Многие фармакологические агенты были испробованы в МД, но ни один из них не был эффективным в остановке хода этого заболевания. Существующий режим лечения все еще находится в области физической медицины и реабилитации.
Ряд испытаний с использованием кортикостероидов (например, преднизона и/или его производных) продемонстрировали улучшение у индивидуумов с МД, в частности, в пределах короткого срока. Хотя точный механизм, при помощи которого кортикостероиды ослабляют фенотип заболевания, является неясным, предполагалось, что кортикостероиды действуют посредством уменьшения воспаления, супрессии иммунной системы, улучшения гомеостаза кальция, повышающей регуляции экспрессии компенсаторных белков и увеличения пролиферации миобластов (Khurana et al. (2003) Nat. Rev. Drug Discovery 2: 279-386). Однако кортикостероиды, вводимые на протяжении времени, могут индуцировать мышечную атрофию, которая действует, прежде всего, на проксимальные мышцы - именно те мышцы, которые поражаются в ДМД и БМД. Индуцированная кортикостероидом мышца и другие побочные эффекты могут ограничивать долгосрочную эффективность кортикостероидной терапии.
GDF-8 является членом суперсемейства TGF-β и функционирует в качестве отрицательного регулятора мышечного роста. Подобно другим членам этого суперсемейства, GDF-8 синтезируется в виде молекулы-предшественника, но перед секрецией он расщепляется на N-концевой ингибиторный пропептид и С-концевой активный зрелый GDF-8. Пропептид может оставаться связанным с GDF-8, ингибируя тем самым биологическую активность зрелого GDF-8. Пропептид должен диссоциироваться из этого комплекса, чтобы GDF-8 связывался с рецептором активина типа II (ActRIIB). При связывании ActRIIB инициирует каскад передачи сигнала, приводя, в конечном счете, к ингибированию прогрессирования миобластов. Было показано, что опосредованное антителами ингибирование GDF-8 in vivo значительно увеличивает размер скелетных мышц у здоровой взрослой мыши (Whittemore et al. (2003) BBRC, 300: 965-971) и ослабляет дистрофический фенотип на mdx-мышиной модели ДМД (Bogdanovich et al. (2002) Nature, 420 (28): 418-421).
Сущность изобретения
Одной из целей настоящего изобретения являются способы и композиции для лечения нарушений, характеризующихся или ассоциированных с риском уменьшения функции мышц. Дополнительные объекты изобретения представлены в последующем описании и частично будут понятны из описания или могут быть обнаружены при применении на практике изобретения.
Настоящее изобретение основано, частично, на обнаружении и демонстрации того, что на мышиной модели ДМД лечение введением нейтрализующего анти-GDF-8-антитела и преднизона является более эффективным для увеличения массы и силы мышц относительно лечения только преднизоном. Далее, настоящее изобретение основано, частично, на обнаружении и демонстрации того, что введение анти-GDF-8-антитела с преднизоном уменьшает индуцированную преднизоном атрофию мышц.
Таким образом, настоящее изобретение относится к способам лечения нервно-мышечных нарушений у млекопитающих. Описанные способы предусматривают введение субъекту, имеющему риск развития нервно-мышечного заболевания или страдающему нервно-мышечным заболеванием, терапевтически эффективных количеств по меньшей мере одного ингибитора GDF-8 и по меньшей мере одного кортикостероида, так чтобы поддерживать желаемые уровни целостности мышц или функции, оцениваемые, например, по сывороточной концентрации креатинкиназы (КК), гистологии мышц, томографии мышц, активностей повседневной жизни, мышечной силе и/или массе. Популяции, подвергаемые лечению способами настоящего изобретения, включают, но не ограничиваются ими, пациентов, имеющих мышечную дистрофию или имеющих риск развития мышечной дистрофии, такой как, например, ДМД или БМД, и субъектов, подвергающихся кортикостероидной терапии в отношении этих или других нарушений.
Настоящее изобретение относится также к способам лечения мышечной слабости и способам лечения индуцированной кортикостероидами мышечной атрофии. Изобретение включает в себя способы лечения кардиомиопатии.
Представлены способы введения и композиции, используемые в способах настоящего изобретения. В описанных способах ингибитор GDF-8 и кортикостероид вводят одновременно или через чередующиеся перекрывающиеся или неперекрывающиеся интервалы.
Ингибиторы GDF-8, используемые в способах настоящего изобретения, включают в себя, но не ограничиваются ими, антитела к GDF-8; антитела к рецепторам GDF-8; растворимые рецепторы GDF-8 и их фрагменты (например, слитые полипептиды ActRIIB, описанные в заявке на патент США №10/689677, включающие в себя растворимые рецепторы ActRIIB, в которых ActRIIB соединен с Fc-частью иммуноглобулина); пропептид GDF-8 и его модифицированные формы (например, описанные в WO 02/068650 или заявке на патент США №10/071499, включая формы, в которых пропептид GDF-8 присоединен в Fc-части иммуноглобулина, и/или форму, в которой GDF-8 является мутированным при остатке аспартата (asp), например, asp-99 в мышином пропептиде GDF-8 и asp-100 в пропептиде GDF-8 человека); ингибитор GDF-8 с малой молекулой; фоллистатин (например, описанный в патенте США №6004937) или содержащие домен фоллистатина белки (например, GASP-1 или другие белки, описанные в заявках на патент США 10/369736 и 10/369738); и модуляторы металлопротеазной активности, которые влияют на активацию GDF-8, описанные в заявке на патент США №10/662438.
В некоторых вариантах осуществления ингибитором GDF-8 является моноклональное антитело или его фрагмент, который блокирует связывание GDF-8 с его рецептором. Не ограничивающие иллюстративные варианты включают в себя моноклональное анти-GDF-8-антитело не человека, например, мышиное моноклональное антитело JA-16 (описанное в заявке на патент США №10/253532; номер депозита в АТСС РТА-4236); его производные, например гуманизированное антитело; и полностью человеческие моноклональные анти-GDF-8-антитела (например, Myo29, Myo28 и Myo22, описанные в заявке на патент США №10/688925; номера депозитов в АТСС РТА-4741, РТА-4740 и РТА-4739 соответственно) или их производные.
Кортикостероиды, используемые в способе настоящего изобретения, включают в себя, но не ограничиваются ими, беклометазона дипропионат, будесонид, кортизол, дексаметазон, флутиказона пропионат, мометазона фуроат, преднизон, триамцинолона ацетонид и их производные.
Должно быть понятно, что как предыдущее общее описание, так и последующее подробное описание являются только иллюстративными и поясняющими и не являются ограничивающими настоящее изобретение, как оно заявлено в формуле изобретения.
Краткое описание графического материала
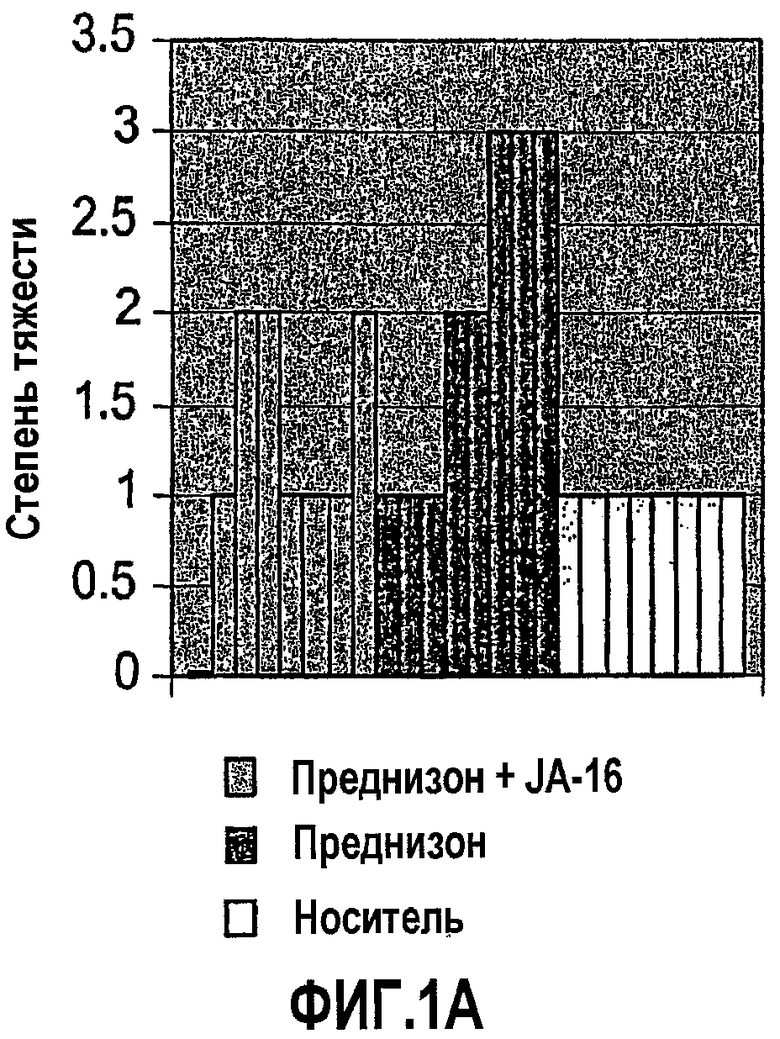
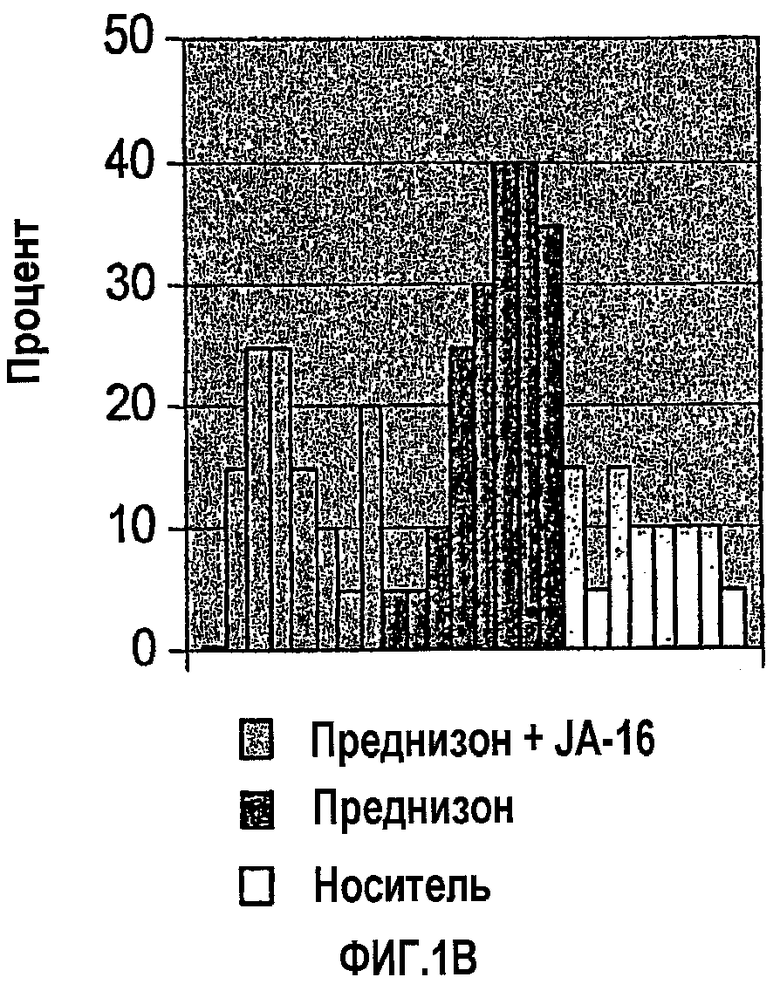
Фиг.1А и 1В изображают результаты гистологического анализа мышцы диафрагмы от мышей mdx, подвергнутых лечению в течение четырех недель нейтрализующим анти-GDF-8-антителом JA-16 (60 мг/кг, один раз в неделю) и преднизоном (2 мг/кг, 3 раза в неделю), одним преднизоном или одним контрольным носителем. Фиг.1А показывает тяжесть атрофии мышечных волокон по шкале 0-4 в конце этого испытания. Фиг.1В показывает процент пораженных (атрофированных) мышечных волокон в конце испытания. Каждый столбец представляет единственную мышь.
Подробное описание изобретения
I. Определения
Для более легкого понимания настоящего изобретения сначала даются определения некоторым терминам. Дополнительные определения приведены на протяжении этого подробного описания.
Термин «антитело», как использовано в данном описании, относится к иммуноглобулину или его части и включает в себя любой полипептид, содержащий антигенсвязывающий сайт, независимо от источника, способа получения и других характеристик. В качестве неограничивающего примера термин «антитело» включает антитела человека, орангутана, мыши, крысы, козы, овцы и курицы. Этот термин включает, но не ограничивается ими, поликлональные, моноклональные, моноспецифические, полиспецифические, неспецифические, гуманизированные, одноцепочечные, химерные, синтетические, рекомбинантые, гибридные, мутированные и CDR-трансплантированные антитела. Для целей настоящего изобретения он включает, если не указано иное, фрагменты антител, такие как Fab, F(ab′)2, Fv, scFv, Fd, dAb и другие фрагменты антител, которые сохраняют антигенсвязывающую функцию.
Антитела могут быть получены, например, посредством традиционных гибридомных способов (Kohler and Milstein (1975) Nature, 256: 495-499), способов рекомбинантных ДНК (патент США №4816567) или способов фагового дисплея, использующих библиотеки антител (Clackson et al. (1991) Nature, 352: 624-628; Marks et al. (1991) J. Mol. Biol., 222: 581-597). В отношении различных других способов получения антител см. Antibodies: A Laboratory Manual, eds. Harlow et al. Cold Spring Harbor Laboratory, 1988.
Термин «антигенсвязывающий домен» относится к части молекулы антитела, которая содержит зону, специфически связывающую часть антигена или весь антиген или комплементарную части антигена или всему антигену. Если антиген является большим, антитело может связываться только с конкретной частью этого антигена. Эпитоп или антигенная детерминанта является частью молекулы антигена, которая ответственна за специфические взаимодействия с антигенсвязывающим доменом антитела. Антигенсвязывающий домен может быть обеспечен одним или несколькими вариабельными доменами антитела (например, так называемым Fd-фрагментом антитела, состоящим из VH-домена). Антигенсвязывающий домен содержит вариабельный район (VL) легкой цепи антител и вариабельный район (VH) тяжелой цепи антитела.
Термин «анти-GDF-8-антитело» или «антитело к GDF-8» относится к любому антителу, которое специфически связывается по меньшей мере с одним эпитопом GDF-8. Термины «GDF-8-рецептор-антитело» и «антитело к рецептору GDF-8» относится к любому антителу, которое специфически связывается по меньшей мере с одним эпитопом GDF-8-рецептора, такого как ActRIIB. Термин «нейтрализующее антитело» относится к антителу, которое является ингибитором GDF-8.
Термин «специфическое взаимодействие", или "специфически связывается", или т.п. означает, что две молекулы образуют комплекс, который является относительно стабильным в физиологических условиях. Этот термин применим также, когда, например, антигенсвязывающий домен является специфическим в отношении конкретного эпитопа, который может присутствовать на ряде антигенов. Специфическое связывание характеризуется высокой аффинностью с умеренно высокой емкостью. Неспецифическое связывание обычно имеет низкую аффинность с умеренно высокой емкостью. Обычно связывание считается специфическим при константе аффинности Ка, большей, чем 106 М-1, чем 107 М-1, или предпочтительно большей, чем 108 М-1. Если необходимо, неспецифическое связывание может быть уменьшено по существу без влияния на специфическое связывание изменением условий связывания. Такие условия известны в данной области и специалист с квалификацией в данной области может с использованием рутинных способов выбрать соответствующие условия. Эти условия обычно определяются в терминах концентрации антител, ионной силы раствора, температуры, времени, предоставляемого для связывания, концентрации посторонних молекул (например, сывороточного альбумина, казеина молока) и т.д.
Термин "функция мышц" относится к способности мышцы выполнять физиологическую функцию, такую как сокращение, измеряемую количеством силы, генерируемой во время либо судорожного сокращения, либо титанического сокращения. Другие способы для оценки функции мышц хорошо известны в данной области и включают в себя, но не ограничиваются ими, измерения мышечной массы, силы сжимания (схватывания), уровня КК в сыворотке, активности повседневной жизни, тесты движения или силы, гистологию ткани (например, E&А-окрашивание или окрашивание коллагеном III) или томографию тканей. Не ограничивающие иллюстративные способы оценки функции мышц приведены в примерах.
Термин «GDF-8» относится к специфическому фактору-8 роста и дифференцировки и, при необходимости, факторам, которые структурно или функционально родственны GDF-8, например ВМР-11 и другим факторам, принадлежащим к суперсемейству TGF-β. Этот термин относится к полноразмерной непроцессированной форме предшественника GDF-8, а также к зрелой форме и форме пропептида, образующихся в результате посттрансляционного расщепления. Этот термин относится также к любым фрагментам и вариантам GDF-8, которые сохраняют по меньшей мере некоторые биологические активности, ассоциированные со зрелым GDF-8, как обсуждалось выше, в том числе последовательностям, которые были модифицированы. Настоящее изобретение относится к GDF-8 от всех видов позвоночных, включая, но не ограничиваясь ими, человека, коровы, курицы, мыши, крысы, свиньи, овцы, индейки, павиана и рыбы (в отношении информации о последовательностях см., например, McPherron et al. (1997) Proc. Natl. Acad. Sci. USA, 94: 12457-12461).
Термин «зрелый GDF-8» относится к белку, который отщепляется от карбоксиконцевого домена белка-предшественника GDF-8. Зрелый GDF-8 может присутствовать в виде мономера, гомодимера или в виде латентного комплекса GDF-8. В зависимости от условий зрелый GDF-8 может устанавливать равновесие между любыми или всеми этими различными формами. В его биологически активной форме зрелый GDF-8 называют также «активным GDF-8».
Термин «пропептид GDF-8» относится к полипептиду, который отщепляется от аминоконцевого домена белка-предшественника GDF-8. Пропептид GDF-8 способен связываться с пропептидсвязывающим доменом на зрелом GDF-8.
Термин «латентный комплекс GDF-8» относится к комплексу белков, образованному между гомодимером зрелого GDF-8 и пропептидом GDF-8. Считают, что два пропептида GDF-8 ассоциируются с двумя молекулами зрелого GDF-8 в гомодимере с образованием тетрамерного комплекса. Этот латентный комплекс может включать в себя другие ингибиторы GDF вместо одного или нескольких пропептидов GDF-8 или в дополнение к одному или нескольким пропептидам GDF-8.
Термин "активность GDF-8" относится к одной или нескольким физиологически регулирующим рост или морфогенетическим активностям, ассоциированным с белком GDF-8. Например, активный GDF-8 является отрицательным регулятором массы скелетных мышц. Активный GDF-8 может также модулировать образование специфических для мышц ферментов (например, креатинкиназы), стимулировать пролиферацию миобластов и модулировать дифференцировку преадипоцитов в адипоциты. Примерные методики для измерения активности GDF-8 in vivo и in vitro описаны, например, в заявке на патент США №10/688925.
Как использовано в данном описании, "ингибитор GDF-8" относится обычно к любому соединению, которое понижающим образом регулирует активность GDF-8 и включает любой агент, способный ингибировать активность, экспрессию, процессинг или секрецию GDF-8. Ингибитор GDF-8 может, например, влиять на стабильность или превращение молекулы предшественника в активную зрелую форму; мешать связыванию GDF-8 с одним или несколькими рецепторами; или мешать внутриклеточной передаче сигналов рецептора GDF-8 ActRIIB. Такие ингибиторы включают в себя белки, антитела, пептиды, пептидомиметики, рибозимы, антисмысловые олигонуклеотиды, двухцепочечную РНК и другие малые молекулы, которые специфически ингибируют GDF-8. Говорят, что такие ингибиторы "ингибируют", "нейтрализуют" или «уменьшают» биологическую активность GDF-8.
Термины «нейтрализуют», «нейтрализующие», «ингибирующие» и родственные им термины относятся к уменьшению активности GDF-8 ингибитором GDF-8, относительно активности GDF-8 в отсутствие того же ингибитора. Уменьшение активности равно предпочтительно по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или более. Способы оценки нейтрализующей или ингибирующей биологической активности ингибиторов GDF-8 известны в данной области и могут быть выполнены, например, с использованием анализа ActRIIB (например, как описано в Whittemore et al. (2003) BBRC, 300: 965-87; или заявке на патент США №10/253532) и RGA-анализов (описанных в Thies (2001) Growth Factors, 18: 251-259 или заявке на патент США №10/253532).
Термин «терапевтически эффективная доза» или «терапевтически эффективное количество» относится к такому количеству соединения, которое приводит к предупреждению, уменьшению риска возникновения или ослаблению симптомов у пациента, или к желаемому биологическому результату, например улучшенной функции мышц, задержанному возникновению клинических симптомов и т.д. Эффективное количество может быть определено, как описано в последующих разделах.
Термин "лечение", "терапевтический способ" и близкие к ним термины относятся к лечению или профилактическим/превентивным мероприятиям. К субъектам, нуждающимся в лечении, могут относиться индивидуумы, уже имеющие конкретное медицинское нарушение, а также индивидуумы, которые могут, в конечном счете, приобрести это нарушение. Лечение включает в себя любое уменьшение в любом симптоме описанного в данной заявке нарушения. Кроме уменьшения или ослабления симптомов, лечение включает также поддержание существующего состояния пациента при ожидании ухудшения или предотвращение возникновения симптома у субъекта, у которого ожидается возникновение симптома, нарушения или заболевания. Лечение может заключаться в уменьшении или снижении одной или нескольких физиологических функций относительно нормальной функции. Оно может также включать уменьшение в сравнении с ожидаемыми симптомами или ожидаемым прогрессированием состояния, нарушения или заболевания.
II. Компоненты для применения в способах изобретения
В способах настоящего изобретения используют один или несколько ингибиторов GDF-8 в комбинации с одним или несколькими кортикостероидами.
А. Ингибиторы GDF-8
Ингибиторы GDF-8, используемые в способах настоящего изобретения, включают, но не ограничиваются ими, антитела к GDF-8; антитела к GDF-8-рецепторам; растворимые рецепторы GDF-8 и их фрагменты (например, слитые полипептиды ActRIIB, описанные в заявке на патент США №10/689677, в том числе растворимые рецепторы ActRIIB, в которых ActRIIB присоединен к Fc-части иммуноглобулина); пропептид GDF-8 и его модифицированные формы (например, описанные в WO 02/068650 или заявке на патент США №10/071499, в том числе формы, в которых пропептид GDF-8 присоединен к Fc-части иммуноглобулина, и/или формы, в которых GDF-8 мутирован при остатке аспартата (asp), например asp-99, в мышином пропептиде GDF-8, и asp-100 в пропептиде GDF-8 человека); фоллистатин (например, описанный в патенте США №6004937) или содержащие домен фоллистатина белки (например, GASP-1 или другие белки, описанные в заявках на патент США 10/369736 и 10/369738); и модуляторы металлопротеазной активности, которые влияют на активацию GDF-8, описанные в заявке на патент США №10/662438.
В некоторых вариантах осуществления ингибитором GDF-8 является моноклональное антитело или его фрагмент, который блокирует связывание GDF-8 с его рецептором. Не ограничивающие иллюстративные варианты включают моноклональное анти-GDF-8-антитело не человека, например мышиное моноклональное антитело JA-16 (описанное в заявке на патент США №10/253532; номер депозита в АТСС РТА-4236); его производные, например, гуманизированные антитела; и полностью человеческие моноклональные анти-GDF-8-антитела (например, Myo29, Myo28 и Myo22, описанные в заявке на патент США №10/688925; номера депозитов в АТСС РТА-4741, РТА-4740 и РТА-4739 соответственно), или их производные.
В некоторых вариантах осуществления ингибитор GDF-8 блокирует GDF-8 от связывания с его рецептором, посредством связывания с GDF-8 или с рецептором GDF-8. В различных вариантах осуществления ингибитором GDF-8 является анти-GDF-8-антитело, которое имеет аффинность в отношении GDF-8, выраженную в виде константы аффинности (Ка), где Ка равна по меньшей мере 105 М-1, 106 М-1, 107 М-1, 108 М-1, 109 М-1, 1010 М-1, 1011 М-1 или 1012 М-1. Рассматривается также применение на людях ингибиторов, которые являются гуманизированными формами и производными антител не человека, полученных из любого вида позвоночных животных, описанными в цитируемых в данном описании заявках на патент, или в Antibody Engineering, ed. Borrebaeck, 2nd ed., Oxford University Press, 1995; и Antibodies: A Laboratory Manual, eds. Harlow et al. Cold Spring Harbor Laboratory, 1988.
В. Кортикостероиды
Кортикостероиды, используемые в способах настоящего изобретения, включают, но не ограничиваются ими, беклометазона дипропионат, будесонид, кортизол, дексаметазон, флутиказона пропионат, преднизон, мометазона фуроат, триамцинолона ацетонид и их производные.
Могут быть также использованы фармацевтически приемлемые соли описываемых соединений.
Кортикостероиды коммерчески доступны в различных фармацевтических готовых формах (Physician′s Desk Reference (PDR) 2003, 57th ed., Medical Economics Company, 2002). Например, в пероральных формах коммерчески доступны кортизон, гидрокортизон (Cortef®), преднизон (Deltasone®, Meticorten®, Orasone®), преднизолон (Delta-Cortef®, Pediapred®, Prelone®), триамцинолон (Aristocort®, Kenacort®), метилпреднизолон (Medrol®), дексаметазон (Decadron®, Dexone®, Hexadrol®), бетаметазон (Celestone®) и дефлазакорт (Calcort®). Другие формы этих и других кортикостероидов могут быть использованы в способах настоящего изобретения.
С. Терапевтические и профилактические способы
Настоящее изобретение относится к способам лечения субъектов млекопитающих, включая способы лечения потери функции мышц, мышечной слабости и/или индуцированной кортикостероидом мышечной атрофии.
Способы настоящего изобретения предусматривают введение млекопитающему терапевтически эффективного количества по меньшей мере одного ингибитора GDF-8 и терапевтически эффективного количества по меньшей мере одного кортикостероида в количествах и в течение периода времени, достаточных для лечения по меньшей мере одного симптома из потери функции мышц, мышечной массы, мышечной слабости, мышечной атрофии или кардиомиопатии. Эти способы могут быть использованы для лечения нервно-мышечных нарушений, таких как мышечные дистрофии. В некоторых вариантах осуществления, функция мышц улучшается относительно такого же лечения в отсутствие либо ингибитора GDF-8, либо кортикостероида. Мышцы, которые могут быть подвергнуты лечению, включают, но не ограничиваются ими, икроножную мышцу, переднюю большеберцовую мышцу, четырехглавую мышцу бедра, длинный разгибатель пальцев стопы, сердечную мышцу или мышцу диафрагмы.
Нервно-мышечные нарушения включают, но не ограничиваются ими, любое острое или хроническое заболевание или нарушение, которое ухудшает функцию мышц, вызывает повреждение мышцы или иным способом вызывает уменьшение мышечной массы и/или функции. Известно большое разнообразие заболеваний или нарушений, и они включают, например, мышечные дистрофии, такие как мышечная дистрофия Дюшена, мышечная дистрофия Беккера, мышечная дистрофия Эмери-Дрейфусса, тазово-плечевая мышечная дистрофия, синдром ригидной спины, синдром Ульриха, мышечная дистрофия Фукуяма, синдром Уокера-Варбурга, мышечная болезнь глаз, связанная с головным мозгом, плече-лопаточно-лицевая мышечная дистрофия, врожденная мышечная дистрофия, миотоническая дистрофия (болезнь Стейнерта), недистрофическая миотония, спинальная мышечная атрофия с периодическими параличами, семейный боковой амиотрофический склероз, наследственная двигательная и сенсорная невропатия, болезнь Шарко-Мари-Тутс, хроническая воспалительная невропатия, дистальная миопатия, миотубулярная/центронуклеарная миопатия, немалиновая миопатия, mini core disease, врожденная миопатия с поражением сердцевины мышечных волокон, десминопатия, миозит с тельцами включения, митохондриальная миопатия, врожденный миастенический синдром, дисфункция мышц после полиомиелита и нарушения, описанные в Emery (2002) The Lancet, 359: 687-695 и Khurana et al. (2003) Nat. Rev. Drug Disc., 2: 379-386. Пациенты могут проявлять слабую, умеренную или тяжелую мышечную слабость, атрофию мышц и влияния на независимое передвижение, связанные с таким нарушением. Пациенты, имеющие риск развития подобных нарушений, будут получать пользу от ингибитора GDF-8 и кортикостероида.
Обычно пациентом, который будет получать пользу от совместного введения ингибитора GDF-8 и кортикостероида, является пациент, который обнаруживает 2-10-кратное или более высокое увеличение активности КК в сыворотке, положительный семейный анамнез, атипичную вариацию диаметра мышечных волокон, недостаточность дистрофина или мутацию в гене дистрофина, потерю мышечной массы, слабость мышц, кардиомиопатию и/или потерю силы мышц. Диагностические процедуры, в том числе соответствующее генетическое тестирование, описаны в Diagnostic Criteria for Neuromuscular Disorders, ed. Emery, 2nd ed., Royal Society of Medicine Press, 1997. Это комбинированное лечение может быть также полезным для субъектов, подвергающихся кортикостероидной терапии в отношении нарушений, иных, чем нервно-мышечные нарушения, и/или субъектов с анамнезом долгосрочного применения кортикостероида, пока эти субъекты обнаруживают уменьшение функции мышц, характеризующееся мышечной слабостью, потерей мышечной массы и/или мышечной атрофией и т.д. или имеют риск такого уменьшения функции мышц. Примеры нарушений, для которых часто применяют кортикостероидную терапию, включают, но не ограничиваются ими, астму, аллергию, артрит, дерматологические нарушения (например, воспалительные дерматозы, экзему, псориаз и т.д.), системную красную волчанку и другие хронические воспалительные состояния.
Предоставлены способы введения и композиции, используемые в способах настоящего изобретения. Введение не ограничивается какой-либо конкретной системой доставки и может включать, без ограничения, парентеральное (в том числе подкожную, внутривенную, интрамедуллярную, внутрисуставную, внутримышечную или внутрибрюшинную инъекцию), ректальное, местное, трансдермальное или пероральное (например, в капсулах, суспензиях или таблетках) введение. Введение субъекту может выполняться в единственной дозе или в повторяемых введениях и в любой из различных физиологически приемлемых форм солей, и/или с приемлемыми фармацевтическим носителем и/или добавкой в виде части фармацевтической композиции. Физиологически приемлемые солевые формы и стандартные способы и эксципиенты для фармацевтических композиций хорошо известны специалистам в данной области (например, описанные в Physician′s Desk Reference (PDR) 2003, 57th ed., Medical Economics Company, 2002 и Remington: The Science and Practice of Pharmacy, eds. Gennado et al. 20th ed., Lippincott, Williams & Wilkins, 2000).
Ингибитор GDF-8 и кортикостероид вводят одновременно или последовательно через перекрывающиеся или неперекрывающиеся интервалы. При последовательном введении ингибитор GDF-8 и кортикостероид могут вводиться в любом порядке. В некоторых вариантах осуществления длина перекрывающегося или неперекрывающегося интервала составляет более чем 2, 4, 6, 12, 24 или 48 недель.
Для кортикостероидов практикующий врач рутинным образом выбирает дозу и схему введения. Например, преднизон используют при приблизительно 0,1-2 мг на килограмм массы тела в день и, обычнее, при 0,5-1 мг/кг/день, например 0,75 мг/кг/день. Кортикостероид может вводиться при средних недельных дозах приблизительно 1-14 мг/кг массы тела, включая приблизительно 1, 2, 5, 7, 10, 12 или 15 мг/кг массы тела в неделю, и практикующий врач может выбрать подходящую частоту введения. Могут быть выбраны единственная доза, непрерывное или периодическое введение кортикостероида, включая часовые, дневные интервалы, два раза в неделю, один раз в неделю или другие периодические интервалы. Предпочтительно кортикостероиды вводят перорально или инъекцией 1-4 раза в день. Доза кортикостероидов может быть оптимизирована в виде комбинированной терапии, и доза может быть понижена для уменьшения значимых побочных эффектов введения.
Ингибиторы GDF-8 могут вводиться отдельно или в смеси с кортикостероидом или другим соединением. Ингибиторы GDF-8 могут вводиться в дозе приблизительно от 1 мкг/кг до 25 мг/кг, в зависимости от физиологии, тяжести симптомов и прогрессирования заболевания. Могут быть выбраны единственная доза, непрерывное или периодическое введение, с интервалами между дозами ингибитора GDF-8, выбранными из часовых, дневных интервалов, два раза в неделю, один раз в неделю, два раза в месяц, один раз в месяц или других подходящих интервалов. Например, ингибиторы GDF-8, такие как антитела, могут вводиться в случае амбулаторного пациента один раз в неделю при дозе приблизительно 0,1-10 мг/кг внутривенной (IV) инфузией, внутрибрюшинной или подкожной инъекцией. Обычно подходящая терапевтически эффективная доза ингибитора GDF-8 выбирается лечащим врачом и может составлять диапазон приблизительно от 1 мкг/кг до 20 мкг/кг, от 1 мкг до 10 мг/кг, от 1 мкг/кг до 1 мг/кг, от 10 мкг/кг до 1 мг/кг, от 10 мкг/кг до 100 мкг/кг, от 100 мкг/кг до 1 мг/кг и от 500 мкг/кг до 5 мг/кг. Примерные эффективные дозы ингибитора GDF-8 составляют приблизительно 0,1, 0,3, 0,5, 1, 5, 10 или 20 мг/кг в неделю. Кроме того, могут быть использованы конкретные дозы, указанные в примерах или в Physician′s Desk Reference (PDR) 2003, 57th ed., Medical Economics Company, 2002.
D. Способы тестирования соединений на терапевтическую эффективность
Далее настоящее изобретение относится к способам для тестирования на животных, например грызунах или приматах, является ли терапевтическое соединение эффективным при введении в комбинации по меньшей мере с одним ингибитором GDF-8 и по меньшей мере одним кортикостероидом. В некоторых вариантах осуществления способ оценки эффективности соединения предусматривает: введение соединения первому животному в комбинации с ингибитором GDF-8 и кортикостероидом; введение ингибитора GDF-8 и кортикостероида второму животному; определение уровня функции мышц у первого и у второго животного после этих введений; и сравнение этих уровней функции мышц. Если уровень у первого животного является более низким, чем уровень у второго животного, это свидетельствует о том, что данное соединение или данная комбинация является эффективной.
В других вариантах осуществления соединение может оцениваться на эффективность в лечении мышечной дистрофии при введении в комбинации с ингибитором GDF-8 и/или кортикостероидом.
Для таких целей оценивания доступны несколько моделей животных. Например, была описана модель mdx, например, Torres et al. (1987) Brain, 110: 269-299 и Hoffman et al. (1987) Science, 238: 347-350. Чрезвычайно высокие уровни КК постоянно отмечаются с недостаточностью дистрофина у мышей mdx и у людей с ДМД вследствие повреждения сарколеммы (Bulfield et al. (1984) Proc. Natl. Acad. Sci. USA, 81: 1189-1192 и Matsuda et al. (1995) J. Biochem. (Tokyo), 118: 959-64). В качестве другого примера, могут быть использованы две другие модели животных: мыши mdx utr-/- (Gillis (2002) Neuromuscul. Disord., 12 (1): 90-84 и Deconick et al. (1997) Cell, 90: 729-738) и мыши mdx nu-/- (Morrison et al. (2000) Lab. Invest., 80: 881-891).
ПРИМЕРЫ
Пример 1
Действие нейтрализующего GDF-8 антитела на дистрофическую мышцу
Возможность ингибирования in vivo GDF-8 для ослабления мышечной дистрофии тестировали на модели ДМД мыши mdx. Пяти-семинедельных самцов мышей С57BL/10ScSn-mdx/j (Jackson Laboratory, Bar Harbor, ME) лечили еженедельными внутрибрюшинными инъекциями нейтрализующего GDF-8 мышиного антитела JA-16 (60 мг/кг, двойное введение дозы в первую неделю, n=11) и одного носителя (контрольная группа, n=10) в течение 12 недель. Этих мышей сравнивали также с мышами того же самого исходного штамма (С57BL/10, n=12) без недостаточности дистрофина.
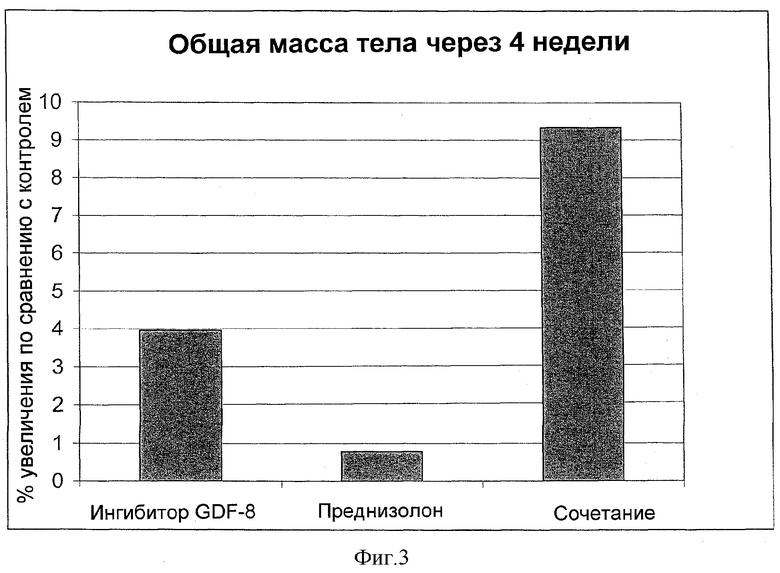
Массу тела подвергали мониторингу до, во время и после лечения. Мыши в группе лечения прибавляли массу относительно мышей в контрольной группе с носителем. Результаты показаны в таблице 1.
Общая масса тела (г). Средние величины с SEM
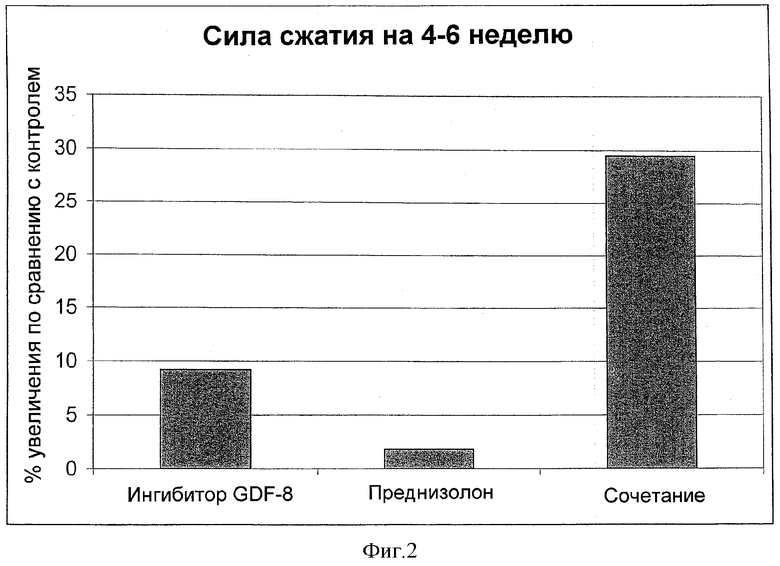
Мышей подвергали также тесту схватывания после 6 и 10 недель введения доз. Мыши в группе четырех- и десятинедельного лечения имели на 9% (р=0,09) и 19% (р<0,05) соответственно большую силу схватывания, чем мыши в контрольных группах с носителем. Результаты показаны в таблице 2.
Сила схватывания (Ib). Средние величины с SEM
Для количественного определения различия в мышечной массе между группой лечения и контролем-носителем животных умерщвляли, четырехглавые мышцы бедра иссекали и взвешивали. Четырехглавые мышцы из подвергнутых лечению животных весили на 13% больше, чем контроли (0,371±0,009 против 0,317±0,008 г; р<0,05). Икроножные мышцы из группы животных с лечением весили на 17% больше, чем контроли (0,223±0,008 против 0,197±0,005 г; р<0,0005).
Пример 2
Действие нейтрализующего GDF-8 антитела и преднизона на нормальную и дистрофическую мышцу
Самцы мышей С57BL/10ScSn-mdx/j и С57BL/10 ((Jackson Laboratory, Bar Harbor, ME). Мышиное моноклональное анти-GDF-8-антитело JA-16, преднизон (Р9901, Sigma) или носитель (арахисовое масло) инъецировали, начиная с возраста 5-7 недель в течение 4 недель. Мышей внутрибрюшинно (IP) инъецировали JA-16 при дозе 60 мг/кг в неделю (двойное введение доз в первую неделю) или подкожно (SC) инъецировали преднизоном при 2 мг/кг, 3 раза в неделю.
Массу тела и силу схватывания подвергали мониторингу до, во время и после обработки. Результаты показаны в таблице 3 и таблице 4 соответственно.
Общая масса тела (среднее ± SEM, г)
Сила схватывания (среднее ± SEM, 1b)
В конце этого исследования мышей умерщвляли и мышечную массу оценивали взвешиванием икроножной мышцы и четырехглавой мышцы бедра. Результаты показаны в таблице 5. Для подтверждения биологической активности преднизона сыворотки из отдельной группы мышей собирали и анализировали на IL-6 и IL-1β (Ani Lytics, Inc., Gaithersburg, MD). Было обнаружено, что оба цитокина снижены в сыворотках мышей, обработанных преднизоном.
Мышечная масса (среднее ± SEM, г)
Таким образом, эти результаты демонстрируют, что при мышечной дистрофии введение ингибитора GDF-8, т.е. анти-GDF-8-антитела, и преднизона является эффективным в увеличении мышечной массы и силы схватывания относительно обработки одним преднизоном или одним носителем.
Кроме того, в этих исследованиях действия обработки JA-16 плюс преднизон (пример 2) были большими, чем действия одного JA-16 (пример 1). Увеличение массы тела в сравнении с массой тела группы носителя после четырех недель обработки было более разительным для обработки JA-16 плюс преднизон, чем для обработки только JA-16. Увеличение силы схватывания в сравнении с носителем-контролем после четырех недель обработки JA-16 плюс преднизон было большим, чем увеличение после шести-десяти недель обработки только JA-16. Увеличение в сравнении с носителем-контролем мышечной массы после четырех недель обработки JA-16 плюс преднизон, было также большим, чем увеличение после двенадцати недель обработки только JA-16.
Пример 3
Действие нейтрализующего GDF-8 антитела на индуцированную преднизоном мышечную атрофию
У мышей, обработанных, как описано в примере 2, мышцу диафрагмы гистологически исследовали, как описано в примере 1. Морфологические изменения оценивали в независимой лаборатории патологии, которой не были известны отнесения к группам обработки. Степени тяжести оценивали по шкале от 0 до 4 (0 = отсутствует; 1 = минимальная; 2 = слабая; 3 = умеренная и 4 = заметная). Результаты показаны на фиг.1А (оценки тяжести в баллах) и фиг.1В (процент атрофированных мышечных волокон). Эти результаты показывают, что введение анти-GDF-8-антитела с преднизоном уменьшает индуцированную преднизоном мышечную атрофию.
Пример 4
Лечение мышечных дистрофий
В качестве примера лечения МД в людях, антитело MYO29 вводили в комбинации с преднизоном или преднизолоном. Не ограничивающие примерные схемы лечения и результаты суммированы в таблице 6. Другие схемы лечения могут быть определены лечащим врачом с диапазонами доз кортикостероидов и ингибиторов GDF-8 и введением, которые обсуждались выше.
Все цитируемые публикации и патенты и последовательности, идентифицированные номерами доступа или ссылочными номерами баз данных, включены в данное описание в качестве ссылки во всей их полноте.
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕЙТРАЛИЗУЮЩИЕ АНТИТЕЛА ПРОТИВ GDF-8 И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2360925C2 |
| УЛУЧШЕННЫЕ АНТИТЕЛА-АНТАГОНИСТЫ ПРОТИВ GDF-8 И ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2630634C2 |
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЯ ИЛИ НАРУШЕНИЯ СО СТОРОНЫ ПЕЧЕНИ, ПРЕДУСМАТРИВАЮЩЕЕ ПРИМЕНЕНИЕ АНТАГОНИСТОВ РЕЦЕПТОРОВ ACTRII | 2020 |
|
RU2838150C1 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ ЛОВУШЕК GDF И АКТИВАТОРОВ РЕЦЕПТОРОВ ЭРИТРОПОЭТИНА ДЛЯ ПОВЫШЕНИЯ СОДЕРЖАНИЯ ЭРИТРОЦИТОВ | 2010 |
|
RU2592670C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ ЛОВУШЕК GDF И АКТИВАТОРОВ РЕЦЕПТОРОВ ЭРИТРОПОЭТИНА ДЛЯ ПОВЫШЕНИЯ СОДЕРЖАНИЯ ЭРИТРОЦИТОВ | 2010 |
|
RU2642302C1 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ ЛОВУШЕК GDF И АКТИВАТОРОВ РЕЦЕПТОРОВ ЭРИТРОПОЭТИНА ДЛЯ ПОВЫШЕНИЯ СОДЕРЖАНИЯ ЭРИТРОЦИТОВ | 2017 |
|
RU2732229C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ МИОСТАТИНА, СОДЕРЖАЩИЕ ИХ КОМБИНАЦИИ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2781401C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ ЛОВУШЕК GDF И АКТИВАТОРОВ РЕЦЕПТОРОВ ЭРИТРОПОЭТИНА ДЛЯ ПОВЫШЕНИЯ СОДЕРЖАНИЯ ЭРИТРОЦИТОВ | 2020 |
|
RU2814047C2 |
| СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ, ВОВЛЕКАЮЩИХ МОДУЛЯЦИЮ РЕЦЕПТОРОВ РИАНОДИНА | 2013 |
|
RU2644350C2 |
| ВЫДЕЛЯЮЩИЕ ОКСИД АЗОТА СОЕДИНЕНИЯ | 2007 |
|
RU2560144C2 |
Группа изобретений относится к медицине, к способам лечения нервно-мышечных нарушений у млекопитающих. Способы включают введение терапевтически эффективных количеств ингибитора GDF-8 и кортикостероида субъекту, имеющему риск развития нервно-мышечного нарушения или страдающему нервно-мышечным нарушением - мышечной дистрофии, атрофии, в частности, индуцированной кортикостероидами, в течение времени, достаточного для поддержания желаемых уровней функции мышц. Это обеспечивает получение синергетического результата в отношении улучшения различных функций мышц. 4 н. и 24 з.п. ф-лы, 3 ил., 6 табл.
(а) по меньшей мере одного из следующих: беклометазона дипропионата, будесонида, кортизола, дексаметазона, флутиказона пропионата, мометазона фуроата, преднизона или триамцинолона ацетонида;
(b) производного по меньшей мере одного из следующих: беклометазона дипропионата, будесонида, кортизола, дексаметазона, флутиказона пропионата, мометазона фуроата, преднизона или триамцинолона ацетонида;
(c) фармацевтически приемлемой соли по меньшей мере одного из следующих: беклометазона дипропионата, будесонида, кортизола, дексаметазона, флутиказона пропионата, мометазона фуроата, преднизона или триамцинолона ацетонида.
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Машковский М.Д | |||
| Лекарственные средства, в 2 т | |||
| - М.: ООО «Новая Волна», Изд | |||
| С.Б.Дивов, 2001, т.2, с.25-39 | |||
| HUDECKI M.S | |||
| et al | |||
| Strength and endurance in the therapeutic evaluation of prednisone-treated MDX mice // Res | |||
| Commun | |||
| Chem | |||
| Pathol | |||
| Pharmacol | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
Авторы
Даты
2008-04-20—Публикация
2004-06-01—Подача