Изобретение относится к области биотехнологии, преимущественно связанной с получением липосомальных дисперсий для косметических и медицинских целей. Данные дисперсии могут найти применение в качестве систем доставки в живые организмы биологически активных веществ.
Классические или немодифицированные липосомы являются мульти- или одноламеллярными везикулами, преимущественно состоящими из фосфолипидов, кроме того часто в их состав входит холестерин (Хол). Последний повышает жесткость бислойной мембраны, снижает ее проницаемость для включенного вещества и увеличивает стабильность бислоя в присутствии биологических жидкостей [S.Vemuri, C.T.Rhodes, Preparation and characterization of liposomes as therapeutic delivery systems: a review.// Pharm. Acta Helv. 70 (1995) 95-111.].
Существуют разные способы получения липосом и выбор метода, как правило, зависит от задач, поставленных при разработке той или иной липосомальной формы.
Наиболее просто получаются мультиламеллярные липосомы, так как липиды, используемые для получения липосом, самопроизвольно образуют при гидратировании подобные бислойные структуры [V.Р.Torchilin and V.Weissig, Liposomes A Practical Approach, Second Edition, // Oxford University Press, 2003]. Однако их размер (до 100 мкм) ограничивает их применение, так, например, они не могут использоваться для внутривенного введения.
Одним из перспективных способов получения липосом является получение липосом из пролипосом. Пролипосомы - это субстанция, которая при разбавлении водой дает липосомы без дополнительной обработки ультразвуком, экструзией и т.д. Пролипосомы могут быть как жидкими (липосомы из них получают при разбавлении водой или соответствующим буферным раствором) [М.А.Schubert, C.C.Muller-Goymann. Solvent injection as a new approach for manufacturing lipid nanoparticles - evaluation of the method and process parameters.// Eur. J. Pharm. Biopharm., 2003, V.55, P.125-131] так и твердыми, обычно в этом случае как вспомогательное вещество применяют сорбит, (липидный слой на порошок сорбита наносится выпариванием из раствора липидов органического растворителя) [К.-Н. Song, S.-J. Chung, С.-К. Shim. Preparation and evaluation of proliposomes containing salmon calcitonin.// J.Cont. Rel., 2002, V.84, P.27-37].
Существует метод получения липосомальных дисперсий путем впрыска растворов липидов (в органических растворителях) в водные растворы [V.Р.Torchilin and V.Weissig, Liposomes A Practical Approach, Second Edition, // Oxford University Press, 2003].
Общим недостатком вышеперечисленных методов является недостаточная агрегационная устойчивость липосомальной дисперсии при необходимости длительного хранения.
Наиболее близким по достигаемому результату является следующий способ получения липосом. Раствор липидов в органическом растворителе упаривается до образования сухой липидной пленки, которая гидратируется водным раствором, в результате чего формируется липосомальная дисперсия, которая, при необходимости, измельчается путем экструзии [V.Р.Torchilin and V.Weissig, Liposomes A Practical Approach, Second Edition, // Oxford University Press, 2003]. Данному методу также присуща недостаточная агрегационная устойчивость получаемой липосомальной дисперсии при необходимости длительного хранения.
Техническим результатом предполагаемого изобретения является увеличение агрегационной устойчивости липосомальных дисперсий, которые могут быть использованы как системы доставки биологически активных веществ.
Данный технический результат достигается предлагаемым способом, заключающимся в использовании водных растворов, содержащих мочевину в концентрации от 0.1 до 5%, для гидратирования липидов при получении липосом.
Существенным отличием предложенного способа, позволяющим достичь данный технический результат, является использование для гидратирования липидов водного раствора, содержащего мочевину в концентрации от 0.1 до 5%, что позволяет стабилизировать липосомальные дисперсии, и универсальность метода, так как эффект стабилизации наблюдается вне зависимости от липидного состава и способа получения липосомальной дисперсии. Кроме того, при необходимости лиофилизации липосомалной дисперсии мочевина может выступать в качестве криопротектора [Jon P.Costanzo, Richard E. Lee, Jr, Cryoprotection by urea in a terrestrially hibernating frog.// The J. Experim. Biol. 208, 4079-4089].
Пример 1
Получали два образца липосомальных дисперсий (липидный состав: яичный фосфатидилхолин (яФХ)/Хол 7/3). Липидные пленки, полученные для каждого из образцов идентичным методом, гидратировали водными растворами, причем в раствор для гидратирования второго образца добавили 1.5% мочевины. Липосомы формировали экструзией через ядерные поликарбонатные мембраны с диаметром пор 200 нм.
Агрегационную устойчивость оценивали по относительному изменению оптической плотности образца липосомальной дисперсии на длине волны 650 нм до (D1) и после (D2) центрифугирования при 11000 g в течение 10 мин. Известно, что чем меньше относительное изменение оптической плотности образца, тем более агрегационно устойчива оцениваемая дисперсия.
Кроме того, размер и распределение частиц определяли с помощью спектрометра NICOMP-3 80 (Particle Sizing Systems, США).
I. Через 1 ч после получения
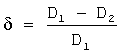
II. Через 1 сутки после приготовления дисперсии были получены следующие данные по размерам и распределению частиц:
1) первый образец (без мочевины)
252.5±1.3 нм (85%)
738.5±17.0 нм (15%)
2) второй образец (1.5% мочевины)
236.1±1.9 нм
III. Через 3 суток после получения
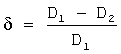
Были получены следующие данные по размерам и распределению частиц:
1) первый образец (без мочевины), измерения в надосадочной жидкости
255.1±0.4 нм (85%)
979.2±44.6 нм (15%)
2) второй образец (1.5% мочевины)
244.6±2.8 нм
Пример 2
Получали два образца липосомальных дисперсий (липидный состав: дипальмитаилфосфатидилхолин/дистеарилфосфатидилхолин/Хол 9/1/0.2). Липидные пленки, полученные для каждого из образцов идентичным методом, гидратировали водными растворами, причем в раствор для гидратирования второго образца добавили 1.62% мочевины. Липосомы формировали экструзией через ядерные поликарбонатные мембраны с диаметром пор 200 нм.
Агрегационную устойчивость оценивали по относительному изменению оптической плотности образца липосомальной дисперсии на длине волны 650 нм до и после центрифугирования при 11000 g в течение 10 мин.
Через 1 ч после получения
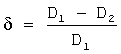
Пример 3
Получали два образца липосомальных дисперсий (липидный состав: яФХ/Хол 7/3) методом инжекции. Первый образец получали впрыскиванием при перемешивании 0,125 мл этанольного раствора, содержащего 4,5 мг смеси яФХ/холестерин 7/3, в 3 мл воды. Второй образец получали впрыскиванием этанольного раствора липидов в 3 мл 4,86% раствора мочевины.
Агрегационную устойчивость оценивали по относительному изменению оптической плотности образца липосомальной дисперсии на длине волны 650 нм до и после центрифугирования при 11000 g в течение 10 мин.
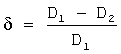
Использование предлагаемого способа получения липосомальных дисперсий обеспечивает по сравнению с существующими способами следующие преимущества:
а) увеличение агрегационной устойчивости липосомальных дисперсий вне зависимости от липидного состава и способа получения;
б) предлагаемое для повышения агрегационной устойчивости липосомальных дисперсий вещество - мочевина, является недорогим и доступным реагентом, разрешенным к использованию в сферах предполагаемого применения (медицинская и косметическая промышленность);
в) кроме указанной функции стабилизации мочевина может также одновременно использоваться в качестве криопротектора.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМ | 2009 |
|
RU2423967C1 |
| ВЫСУШЕННЫЕ ВОССТАНОВЛЕННЫЕ ВЕЗИКУЛЫ ДЛЯ ФАРМАЦЕВТИЧЕСКОГО ПРИМЕНЕНИЯ | 2007 |
|
RU2443412C2 |
| СПОСОБ СПЕКТРОФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ЛИПОСОМАЛЬНО ИНКАПСУЛИРОВАННЫХ ФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТОВ | 2007 |
|
RU2337358C1 |
| ЛИПОСОМАЛЬНАЯ КОМПОЗИЦИЯ ДЛЯ ИСПОЛЬЗОВАНИЯ В ПЕРИТОНЕАЛЬНОМ ДИАЛИЗЕ | 2013 |
|
RU2609860C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМАЛЬНОЙ ФОРМЫ ИЗОНИАЗИДА | 2009 |
|
RU2429841C1 |
| Способ получения липосомальных наноконтейнеров с иммобилизированным ферментом | 2022 |
|
RU2784321C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОЛИПИДНОГО НОСИТЕЛЯ ХОЛЕСТЕРИНА | 1994 |
|
RU2097038C1 |
| СРЕДСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ЕЕ ПРОВЕДЕНИЯ | 2004 |
|
RU2271801C2 |
| СРЕДСТВО ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ, СПОСОБ ПОЛУЧЕНИЯ ПРЕДЛАГАЕМОГО СРЕДСТВА И СПОСОБ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ С ИСПОЛЬЗОВАНИЕМ ПРЕДЛАГАЕМОГО СРЕДСТВА | 2010 |
|
RU2428981C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННЫХ ЛИПОСОМ | 1997 |
|
RU2144352C1 |
Изобретение относится к области биотехнологии и описывает способ получения липосом путем гидратирования липидов, сухих или в виде растворов, причем гидратирование проводят водным раствором, содержащим мочевину в концентрации от 0.1 до 5%. Данный способ позволяет повысить агрегационную устойчивость и сроки хранения липосомальных дисперсий. Данные дисперсии могут найти применение в качестве систем доставки в живые организмы биологически активных веществ.
Способ получения липосом путем гидратирования липидов, сухих или в виде растворов, отличающийся тем, что гидратирование проводят водным раствором, содержащим мочевину в концентрации от 0,1 до 5%.
| TORCHILIN V.P | |||
| and WEISSIG V., Liposomes A Practical Approach, Second Edition, // Oxford University Press, 2003 | |||
| K.-H | |||
| Song, S.-J | |||
| Chung, C.-K.Shim | |||
| Preparation and evaluation of proliposome containing salmon calcitonin // J.Cont | |||
| Rel, 2002, v.84, p.27-37 | |||
| ЛИПОСОМНАЯ КОМПОЗИЦИЯ ЧЕЛОВЕЧЕСКОГО КАЛЬЦИТОНИННОГО ГЕННОГО ПЕПТИДА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1997 |
|
RU2174843C2 |
Авторы
Даты
2008-05-27—Публикация
2007-04-17—Подача