Изобретение относится к области фармацевтики, а именно к способу получения липосомальной формы изониазида (ИН) для лечения туберкулеза.
Туберкулез - инфекционное заболевание с высоким уровнем смертности, от которого умирает ежегодно полтора миллиона человек. Разработана эффективная схема терапии, которая включает несколько противотуберкулезных препаратов, так как монотерапия (т.е. прием только одного лекарственного препарата) уже через 2 месяца приводит к появлению резистентных форм микобактерий. Препарат первого ряда - изониазид (ИН) обладает высокой бактериологической активностью в отношении возбудителя туберкулеза - Mycobacterium tuberculosis. Однако он быстро выводится из организма, что делает необходимым применение больших доз препарата, которые оказывают токсическое действие.
M.tuberculosis - это внутриклеточный паразит, который размножается в основном в макрофагах, куда проникает по механизму фагоцитоза. Хорошо растворимый в воде изониазид (ИН) не способен проникать через плазматическую мембрану макрофага. Для его доставки в макрофаги необходимо создать капсулированную форму, которая по механизму фагоцитоза попадала бы в макрофаг, и таким образом осуществлялась бы направленная доставка ИН к месту локализации микобактерий. Для получения капсул применяют два вида материалов: природные фосфолипиды, которые способны образовывать липосомы, и биодеградируемые синтетические полимеры, из которых получают наночастицы.
Следует учесть, что при введении в кровеносное русло препарата, который адсорбирован на поверхности различных носителей, происходит его сильное разбавление, которое приводит к десорбции препарата с поверхности липосом или наночастиц и выходу его из внутреннего водного пространства липосом наружу по градиенту концентраций. Поэтому для противотуберкулезного препарата важным является не столько общее содержание действующего вещества в составе капсулированной формы, сколько количество (процент) его включения в сами капсулы, будь это липосомы или наночастицы, которые затем захватываются макрофагами.
Известен способ получения наночастиц с изониазидом, включающий использование pH-чувствительных полимеров: ацетатфталатцеллюлозы, фталатоксипропилцеллюлозы, поливинилацетатфталатоксипропилметилцеллюлозы, альгиновые кислоты для орального введения частиц (Патент JP 2008056696, МПК А61К 9/06, А61К 31/4409, опубл. 13.03.2008).
Однако полученные частицы характеризуются большим размером и не могут применяться при внутривенном или аэрозольном введении.
Известен способ получения лекарственной формы ИН, иммобилизованного на полимерном носителе, представляющем собой частицы из полиалкилцианоакрилата (С2-С10), декстрана с молекулярной массой 20-70 кДа и наполнителей с размером частиц 200-700 нм (Патент РФ 2185818, МПК А61К 31/395, А61 К9/48, опубл. 27.07.2002).
Недостатком данной композиции является гетерогенность по размерам образующихся полимерных частиц и наличие фракции частиц с размером более 400 мкм, что затрудняет их прохождение по капиллярам.
Известен способ получения липосомальной композиции, содержащей ИН методом экструзии, при котором эмульсию липидов с противотуберкулезным препаратом продавливали через фильтры с малым размером пор, а для получения липосом использовали следующие компоненты: яичный фосфатидилхолин (ФХ), холестерин (ХЛ); дицетилфосфат (ДЦФ), О-стеариламинопектин, ганглиозиды, фосфатидилэтаноламин, ковалентно связанный с полиэтиленгликолем-2000 (Deol P., Khuller G.K., Joshi K. Therapeutic efficacies of isoniazid and rifampin encapsulated in lung-specific stealth liposomes against Mycobacterium tuberculosis infection induced in mice. // Antimicrob Agent Chemother. 1997. V.41. N.6. P.1211-1214).
Однако в данной работе не определяли количество включенного в липосомы ИН, а при оценке эффективности действия in vivo было установлено, что липосомальная форма ИН практически не отличается от водного раствора ИН.
Наиболее близким техническим решением к предлагаемому изобретению является способ получения липосом с ИН из индивидуального ФХ сои и его смеси с другими липидами (концентрация липидов 40 мг/мл) экструзией мультиламеллярных везикул (МЛВ) или обработкой МЛВ ультразвуком или методом пролипосом, с предварительным растворением липидов в органическом растворителе (хлороформ, этанол, диэтиловый эфир), удалением растворителя с использованием роторного испарителя и получением МЛВ диспергированием водным раствором ИН липидной пленки (Г.М.Сорокоумова, А.А.Селищева, Н.М.Маликова, А.С.Минина, В.И.Швец. Включение изониазида в липосомы разного липидного состава // Бюллетень экспериментальной биологии и медицины, 2004, т.137, №1, С.24-26). Определение включенного в липосомы ИН проводили во фракции липосом, отделенной от свободного ИН с помощью метода гель-фильтрации, а определение содержания ИН в полученной фракции липосом проводили спектрофотометрически на длине волны 264 нм.
Недостатками данного способа являются низкое включение ИН (не более 4%), что не позволяет такую систему использовать как основу для технологической схемы получения липосомальной формы ИН, дополнительные энергозатраты и применение токсичных растворителей, а использованный метод определения включенного в липосомы ИН характеризуется низкой чувствительностью.
Таким образом, существует потребность в препаратах изониазида, обладающих улучшенными фармакологическими свойствами, в частности продолжительным периодом нахождения в организме, и создании нового, более технологичного (исключая использование токсичных органических растворителей) и экономически оправданного способа получения липосомальных форм ИН.
Техническим результатом изобретения является разработка технологичного способа получения липосом малого размера (не более 400 нм), содержащих ИН, включенный в липосомы в максимально высокой концентрации.
Указанный технический результат достигается за счет того, что в предложенном нами способе готовят раствор изониазида с концентрацией 10-95 мг/мл в водной среде, на поверхность полученного раствора наслаивают порошок смеси липидов и диспергируют порошок при слабом перемешивании при температуре 15-25°С, предпочтительно - при комнатной температуре в течение 20-40 минут, предпочтительно - в течение 30 минут. Перемешивание может быть осуществлено с помощью любого подходящего устройства, например магнитной мешалкой. Далее дисперсию инкубируют при температуре 55-80°С в течение 10-20 минут.
В качестве водной среды применяют изотонический раствор NaCl. Предпочтительно изотонический раствор является стерильным, стерилизацию можно провести после приготовления раствора ИН или на любом этапе.
Липосомы с ИН получают при совместной инкубации водного раствора ИН (10-95 мг/мл) со смесью гликосфинголипиды/фосфолипиды (ГСЛ/ФЛ) с концентрацией 5-60 мг/мл при соотношении гликосфинголипиды : фосфолипиды от 1:1 до 5:1.
Смесь липидов для получения липосом включает гликосфинголипиды и фосфолипиды. В частности, смесь липидов содержала 60% гликосфинголипидов, 37% фосфолипидов и 3% холестерина и триацилглицеридов.
В качестве гликосфинголипидов применяли смесь цереброзидов с цереброзидсульфатами природного происхождения в соотношении от 1:1 до 3:1.
Фосфолипиды могут представлять смесь любых фосфолипидов животного и/или растительного происхождения, взятых в любом сочетании и соотношении. Предпочтительно, чтобы доля гликосфинголипидов превышала долю фосфолипидов.
В частности, могут быть использованы следующие фосфолипиды: фосфатидилхолин (ФХ), фосфатидилинозит (ФИ), фосфатидилэтаноламин (ФЭ), фосфатидилсерин (ФС), холестерин (ХЛ), кардиолипин (КЛ), лизо-фосфатидилхолин (лФХ). В частности, в качестве фосфолипидов можно применять смесь, содержащую 70-80 мас.% фосфатидилэтаноламина (ФЭ), остальное - холестерин (ХЛ).
Качественный и количественный состав смеси липидов может быть определен денситометрическим анализом ТСХ. В данной работе для получения препарата применяли смесь, содержащую 28% ФС, 8% ФЭ и следовые количества ФХ и СМ в качестве фосфолипидов. Фракция гликосфинголипидов состояла в основном из цереброзидов (Ц) в количестве 46% и цереброзидсульфатов (ЦС) в количестве 14%.
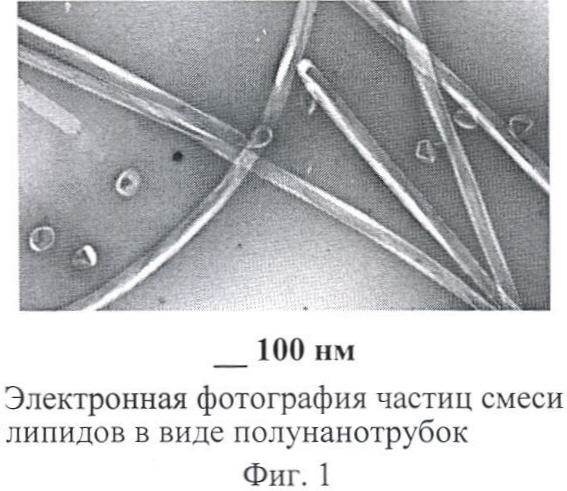
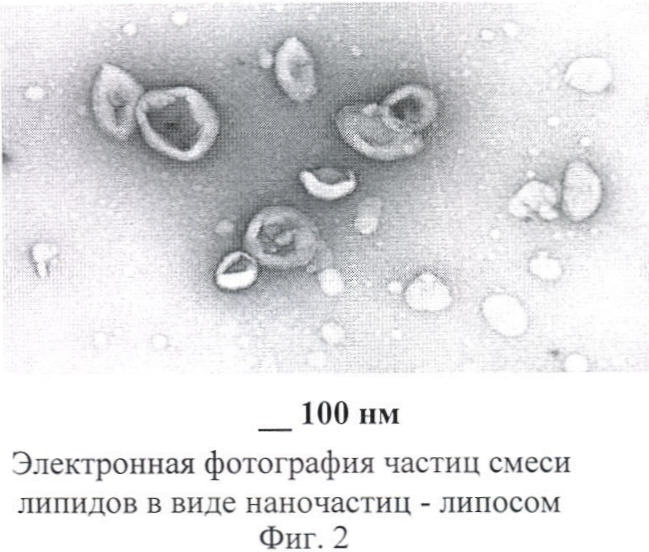
Используемая смесь фосфолипидов и гликосфинголипидов при вышеуказанном способе диспергирования образует в водных растворах протяженные структуры диаметром 200 нм и длиной более микрона. Они имеют вид желоба, и их называют полунанотрубками (фиг.1). Далее при инкубации дисперсии в течение 10-15 минут, предпочтительно - 10 минут, при температуре 55-80°С, предпочтительно 60°С из полунанотрубок самопроизвольно образуется гомогенная эмульсия сферических наночастиц - липосом (фиг.2) с высоким количеством (процентом) включения ИН размером не более 400 нм, стабильным после сильного разбавления препарата в ходе проведения процесса гель-фильтрации.
Образование липосом подтверждали измерением размера частиц методом турбидиметрии и/или анализом морфологии частиц методом электронной микроскопии.
Содержание (процент включения) ИН в липосомах определяли спектрофотометрически в виде продукта его взаимодействия с 2,4,6-тринитробензолсульфокислотой (ТНБС) при длине волны 434 нм. Такой способ позволяет определить до ·10-3 мг ИН/мл, что в 5 раз меньше концентрации ИН, определяемой по светопоглощению при 262 нм. При этом регистрация оптической плотности проводится в видимой области спектра и поглощение липидов не влияет на ее величину. Было установлено, что в выбранных условиях в липосомы включается более 10% исходного ИН, и величина включения зависит от условий, в которых получают липосомы.
Сущность предлагаемого способа иллюстрируется следующими примерами, включающими конкретные осуществления изобретения. Результаты представлены в табл.1.
Пример 1. Оптимизация температурного режима
Варьированием температуры получения липосом из длинных полунанотрубок от 40 до 80°С с контролем методами турбидиметрии и электронной микроскопии было установлено, что при температуре ниже 55°С наблюдаются исходные полунанотрубки. Выше 80°С наблюдается полный переход полунанотрубок в сферические частицы, однако повышается индекс окисленности липидов от 0,2 до 1,0, что говорит о том, что идет окисление и деградация липидов.
Оптимальной температурой, при которой достигается существенный переход полунанотрубок в сферические частицы при приемлемо низком индексе окисленности липидов, является температура 60°С.
Пример 2. Оптимизация липидного состава
Использовали липосомы из смеси фосфолипидов (ФХ:ХЛ) (15 мг) в молярном соотношении (7:3) и смесь ГСЛ/:ФЛ (15 мг) в молярном соотношении 5:1 при постоянной концентрации ИН, равной 10 мг/мл. Для отделения свободного ИН от включенного использовали микроколонку с сорбентом Sephadex G-25. Результаты приведены в нижеследующей табл.1.
При сравнении количества включения ИН в липосомы только из ФЛ и из смеси ГСЛ/ФЛ видно, что ИН очень плохо включается в липосомы из ФХ:ХЛ (7:3), и его включение составляет не больше 4% от исходного количества ИН. При использовании смеси ГСЛ/ФЛ в соотношении 1:1 для получения липосом с ИН эффективность его включения составляет 13%. Эта величина увеличивается до 17% при увеличении доли ГС Л в смеси. Процент включения ИН в липосомы зависит от липидного состава, который достигает максимального значения при включении в липосомы из смеси ГСЛ/ФЛ, в которой доля ГСЛ больше, чем ФЛ.
Пример 3. Влияние содержания ИН в изотоническом растворе
Содержание ИН в изотоническом растворе варьировали от 10 до 95 мг/мл. При концентрации ИН выше 95 мг/ мл выпадает осадок. Повышение исходной концентрации ИН до максимально возможной не влияет на процент включения, но в самих липосомах содержание ИН увеличивается (табл.1).
Пример 4. Влияние содержания смеси ГСЛ/ФЛ в исходной дисперсии
При получении липосом варьировали концентрацию смеси ГСЛ/ФЛ (3:2) в исходной дисперсии от 5 до 80 мг/мл. При определении включения ИН выявили, что включение ИН в липосомы прямо пропорционально концентрации липидов до концентрации 40 мг/мл. Повышение этой величины в дальнейшем не приводит к повышению включения, поскольку в этих условиях не происходит полного перехода полунанотрубок в сферические частицы, на что указывает большой размер частиц (табл.1).
Предложенное изобретение устраняет существенные недостатки известных способов получения липосом с ИН, а именно необходимость применения органических растворителей с их последующим выпариванием, а также использование дополнительного дорогостоящего оборудования (экструдера).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КАПСУЛИРОВАННОЙ ФОРМЫ ПРОТИВОТУБЕРКУЛЕЗНЫХ ПРЕПАРАТОВ РИФАМИЦИНОВОГО РЯДА | 2009 |
|
RU2420287C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМ | 2009 |
|
RU2423967C1 |
| СТАБИЛИЗИРУЮЩИЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ КАМПТОТЕЦИНА | 2016 |
|
RU2833053C2 |
| СТАБИЛИЗИРОВАННЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ КАМПТОТЕЦИНА | 2016 |
|
RU2732567C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИПОСОМ | 2007 |
|
RU2325150C1 |
| Стабилизатор липосомальных суспензий | 2015 |
|
RU2642786C2 |
| СРЕДСТВО ДЛЯ ДОСТАВКИ АКТИВНОГО АГЕНТА | 2017 |
|
RU2669354C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОЛИПИДНОГО НОСИТЕЛЯ ХОЛЕСТЕРИНА | 1994 |
|
RU2097038C1 |
| КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РИНИТА И РОДСТВЕННЫХ ЗАБОЛЕВАНИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2444351C2 |
| ФОСФОЛИПИДНАЯ ЭМУЛЬСИЯ, ВКЛЮЧАЮЩАЯ ДИГИДРОКВЕРЦЕТИН, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2007 |
|
RU2369383C2 |
Изобретение относится к области фармацевтики, а именно к способу получения липосомальной формы изониазида (ИН) для лечения туберкулеза. Способ получения липосом малого размера (не более 400 нм), содержащих ИН, включенный в липосомы в максимально высокой концентрации, отличается тем, что готовят раствор изониазида с концентрацией 10-95 мг/мл в водной среде, на поверхность полученного раствора наслаивают порошок смеси липидов, состоящей из гликосфинголипидов и фосфолипидов и диспергируют порошок при слабом перемешивании, после чего дисперсию инкубируют при температуре 55-80°С в течение 10-20 минут, отделяют полученные липосомы от свободного ИН с помощью метода гель-фильтрации. 6 з.п. ф-лы, 2 ил., 1 табл.
1. Способ получения липосомальной формы изониазида (ИН), отличающийся тем, что готовят раствор изониазида с концентрацией 10-50 мг/мл в водной среде, на поверхность полученного раствора наслаивают порошок смеси липидов и диспергируют порошок при слабом перемешивании при температуре 15-25°С в течение 20-40 мин, после чего дисперсию инкубируют при температуре 55-80°С в течение 10-20 мин, а в качестве липидов берут смесь гликосфинголипидов и фосфолипидов, в которой доля гликосфинголипидов должна превышать долю фосфолипидов.
2. Способ по п.1, отличающийся тем, что в качестве водной среды берут изотонический раствор NaCl, диспергирование проводят при комнатной температуре в течение 30 мин и дисперсию инкубируют при температуре 60°С в течение 10 мин.
3. Способ по любому из пп.1 и 2, отличающийся тем, что все операции проводят в стерильных условиях.
4. Способ по п.3, отличающийся тем, что в качестве фосфолипидов берут фосфатидилэтаноламин или смесь фосфатидилхолина с любыми фосфолипидами яичного желтка, и/или сои, и/или крупного рогатого скота.
5. Способ по п.4, отличающийся тем, что в качестве гликолипидов берут смесь цереброзидов и цереброзидсульфатов природного или синтетического происхождения.
6. Способ по п.5, отличающийся тем, что раствор ИН совместно со смесью липидов готовят при массовом соотношении ИН: липиды от 1:1 до 1:15.
7. Способ по п.6, отличающийся тем, что определение включенного в липосомы ИН проводят спектрофотометрически, анализируя содержание продукта взаимодействия ИН с тринитробензолсульфокислотой во фракции липосом, отделенной от свободного ИН с помощью метода гель-фильтрации.
| RU 2006142766 A, 20.06.2008 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2008 |
|
RU2372914C1 |
| Сорокоумова Г.М., Селищева А.А., Маликова Н.М., Минина А.С., Швец В.И | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| О ПЕРСПЕКТИВНОСТИ РАЦИОНАЛЬНОГО ИСПОЛЬЗОВАНИЯ ЖИРА БАЙКАЛЬСКОЙ НЕРПЫ В | |||
Авторы
Даты
2011-09-27—Публикация
2009-12-16—Подача