Настоящее изобретение относится к удерживаемой в желудке системе регулируемой доставки лекарственного средства, имеющей двухфазную модель высвобождения.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Системы регулируемой доставки лекарственного средства в организм доставляют лекарство таким образом, чтобы установить терапевтически эффективные уровни активного ингредиента в крови, причем как только такие уровни в крови достигаются, такие системы продолжают поддерживать постоянные уровни лекарственного средства в крови в течение продолжительного периода времени посредством доставки лекарственного средства в организм с такой же скоростью, с какой организм удаляет лекарственное средство из организма. Посредством предотвращения образования пиковых и минимальных уровней в крови, ассоциированных с общепринятыми формами дозировки, системы с регулируемой доставкой лекарственного средства позволяют снижать частоту появления отрицательных действий или побочных действий. Очень важно, что системы с регулируемой доставкой лекарственного средства снижают частоту приема, что удобно для пациента с точки зрения дозировки и соответствия строго определенным схемам приема лекарственного средства.
В общем известно, что скорость, с которой пероральная система с регулируемой доставкой лекарственного средства доставляет лекарственное средство в кровь, не является такой же, как скорость, с которой она высвобождает лекарственное средство в жидкость, используемую при исследовании, поскольку рН желудочно-кишечного сока, состав и интенсивность перемешивания изменяются в зависимости от определенного расположения системы регулируемой доставки лекарственного средства в желудочно-кишечном тракте, т.е. при поступлении из желудка в толстую кишку, в зависимости от голодного или сытого состояния, типа и количества проглоченной пищи, и изменяются также от индивидуума к индивидууму. Кроме того, лекарственное средство не может абсорбироваться таким же образом и с такой же склонностью, как это происходит в организме при движении из желудка в толстую кишку. Некоторые лекарственные средства имеют «окно абсорбции», т.е. они абсорбируются только из верхних частей желудочно-кишечного тракта, тогда как имеются другие лекарственные средства, абсорбция которых из прямой кишки не является равномерной или полной. Таким образом, расположение системы с регулируемой доставкой лекарственного средства в желудочно-кишечном тракте, а также скорость, с которой система регулируемой доставки лекарственного средства движется из желудка в толстую кишку, являются важными факторами, которые необходимо принимать во внимание при разработке пероральной системы регулируемой доставки лекарственного средства. Таким образом, специалистам в данной области известно, что следует разработать пероральную систему с регулируемой доставкой лекарственного средства не только с регулированием скорости, с которой система высвобождает лекарственное средство на протяжении периода доставки лекарственного средства (временное регулирование), но также с регулированием места расположения, из которого оно доставляется (пространственное регулирование). Пространственное регулирование может быть достигнуто пролонгированием периода удерживания системы в желудке. Системы желудочного удерживания также являются полезными, когда лекарственное средство является эффективным локально в желудке. Лекарственные средства, абсорбируемые в верхней части желудочно-кишечного тракта, могут обнаруживать вариабельность в адсорбции вследствие различий между индивидуумами или у одного и того же индивидуума в опустошении полости желудка и желудочно-кишечной двигательной функции. Такое изменение в адсорбции может быть вызвано введением лекарственной формы, включающей лекарственное средство, так чтобы небольшая часть лекарственного средства была доступна при немедленном высвобождении и большая часть было доступна при замедленном или регулируемом высвобождении.
Один из подходов, который использовали для достижения пространственного регулирования, включает повышение удерживания в желудке систем для замедленной или регулируемой доставки лекарственного средства посредством использования композиции, содержащего сильно набухаемые полимеры в смеси с генерирующим газ агентом, с образованием систем, которые являются большими по размеру, а также способны плавать на желудочном соке. Теперь стало совсем очевидно для специалиста в данной области, что системы, содержащие набухаемые полимеры, могут сразу плавать на желудочном соке, так как выделяемый и улавливаемый в этой системе газ снижает плотность. Набухание до большого размера является важным фактором в желудочном удерживании системы. Твердые вещества, имеющие размер меньше чем 5-7 мм проявляют задержанное желудочное выведение в условиях питания, но могут все же выходить из желудка вследствие того, что их размер меньше, чем сфинктер привратника. Даже плавающая система с размером меньше чем от 5 до 7 мм может выходить, если пациент находится в положении лежа на спине. Средний диаметр привратника в состоянии покоя составляет примерно 13+7 мм, и сообщалось, что дозированные лекарственные формы с диаметром приблизительно 12-18 мм в их расширенном состоянии обычно исключаются из прохождения через сфинктер привратника. Эта система должна быть также способна сохранять указанный размер в желудочной жидкости в течение продолжительных периодов времени в условиях перемешивания, создаваемого двигательной функцией желудка. Такие большие интактные системы не могут выводиться до появления интердигестивного мигрирующего моторного комплекса в начале интердигестивной фазы. Комбинация увеличения в размере и плавучести приводит к увеличенному удерживанию указанной системы в желудке. Работы известного уровня техники, приводящие к существующему состоянию в данной области, описываются ниже.
В патенте Соединенных Штатов №4101650 ('650), выданном Zaidan Hojin Biseibutsu Kagaku Kenkyu Kai, описана готовая препаративная форма, в которой гранулы, содержащие бикарбонат натрия, лактозу и поливинилпирролидон, покрыты слоем гидроксипропилметилцеллюлозы. Такие гранулы затем дополнительно покрывают суспензией, содержащей активный ингредиент пепстатин и гидроксипропилметилцеллюлозу, для образования плавающих микрокапсул с диаметром в диапазоне от 0,1 до 2 мм. Недостатком такой системы является то, что микрокапсулы значительно меньше по размеру, чем требуется для продолжительного удерживания в желудке.
В патенте Соединенных штатов №4777033 ('033), выданном Teijin Limited, описан пероральный фармацевтический препарат с замедленным высвобождением, включающий низший алкиловый эфир целлюлозы, полиакриловую кислоту или ее фармацевтически приемлемую соль, лекарственное средство и эффективное количество вскипающего пенообразующего агента. Таблетки, изготовленные из такой композиции, однако все же сохраняют вышеуказанные основные недостатки, общие с патентом '650, проявляющиеся в том, что таблетки системы '033 не остаются целыми, когда подвергаются испытанию на растворение.
В патенте Соединенных Штатов №4844905, выданном Eisai Co., описаны гранулы, включающие содержащую лекарственное средство сердцевину, генерирующий газ средний слой, включающий карбонат натрия и органическую кислоту, и наружный слой расширяемой полимерной пленки. Хотя гранулы предназначены для удерживания в желудке, они имеют недостаток, заключающийся в небольшом размере.
В патенте Японии №63014715, выданном для Zeria Shinyaku KK, описана композиция с медленным высвобождением, включающая (А) водорастворимый полимер с высокой вязкостью, предпочтительно простой эфир целлюлозы или поливиниловый спирт, (В) сшитый нерастворимый поливинилпирролидон и (С) компонент для вспенивания при контактировании с желудочным соком, предпочтительно карбонат, особенно карбонат кальция или осажденный карбонат кальция. Система, однако, не содержит часть лекарственного средства в немедленно высвобождаемой форме и часть в регулируемым образом высвобождаемой форме. Таким образом, даже в начале схемы приема лекарственного средства, когда лекарственное средство не является доступным для организма, система может начать выводить активный ингредиент с относительно низкой скоростью по сравнению с высвобождением композицией с немедленным высвобождением. Другим недостатком является то, что в то время как сильно набухающие и быстро набухающие полимеры могут быть желательны для удерживания в желудке, авторами обнаружено, что некоторые простые эфиры целлюлозы не отвечают этим требованиям.
В патенте Соединенных Штатов №5651985, выданном Bayer AG, описана фармакологически активная композиция, включающая фармакологически активное соединение, диспергированное в гомогенной смеси на молекулярном уровне поливинилпирролидона и полимера метакриловой кислоты, имеющего кислотное число между 100 и 1200 мг КОН/г полимерного твердого вещества, и, необязательно, образующую газ добавку. Однако система не содержит часть лекарственного средства в немедленно высвобождаемой форме и часть в регулируемом образом высвобождаемой форме и не обеспечивает двухфазную модель высвобождения. Скорость набухания таких систем также является медленной, так что они не достигают требуемого большого размера за короткий период от 15 до 30 минут. Кроме того, для достижения гомогенности двух полимеров на молекулярном уровне требуется трудоемкий и дорогой способ, например сушка при замораживании.
Публикация РСТ №WO 00/15198, выданная Ranbaxy Laboratories, относится к фармацевтической композиции, включающей лекарственное средство, генерирующий газ компонент, агент, вызывающий набухание, агент, придающий вязкость и, необязательно, гелеобразующий полимер. В качестве генерирующих газ агентов используют карбонаты или бикарбонаты. Агентом, вызывающим набухание, является супердезинтегрирующее средство, такое как сшитый поливинилпирролидон, сшитая карбоксиметилцеллюлоза и натриевая соль гликолята крахмала. Придающим вязкость агентом является углеводная камедь, которая придает вязкость немедленно. Система, однако, не содержит часть лекарственного средства в немедленно высвобождаемой форме и часть в регулируемым образом высвобождаемой форме и не является двухфазной моделью высвобождения.
Публикация РСТ №WO 01/10419, выданная Ranbaxy Laboratories, относится к фармацевтической композиции, включающей лекарственное средство, сахар, разбавитель и генерирующий газ агент, и публикация РСТ №WO 01/10405, выданная Ranbaxy Laboratories, относится к фармацевтической композиции, включающей лекарственное средство, инертное масло, сахар, разбавитель и генерирующий газ агент. Однако указанные системы не способны к набуханию до требуемого большого размера, подходящего для удерживания в желудке, поскольку они не содержат какое-либо набухаемое вещество.
В публикации РСТ №WO 00/23045, выданной Sanofi-Synthelabo, описана фармацевтическая композиция, содержащая два или три слоя и содержащая активный ингредиент в сочетании с эксципиентом, модифицирующим его высвобождение, и систему, способную генерировать диоксид углерода в набухаемой полимерной гидрофильной матрице. Приводятся примеры, в которых активный ингредиент находится в одном слое, содержащем набухаемые полимеры в качестве эксципиента, модифицирующего его высвобождение, и второй слой содержит набухаемый полимер в сочетании с карбонатом. Композиция находится в форме двухслойных или трехслойных таблеток. Однако система не содержит часть лекарственного средства в немедленно высвобождаемой форме и часть в регулируемым образом высвобождаемой форме и не является двухфазной моделью высвобождения.
В публикации РСТ №WO 01/10417, выданной Galenix Development, описана и заявлена фармацевтическая композиция, содержащая по меньшей мере одну фазу, включающую активный ингредиент в сочетании с одним или несколькими эксципиентами, и вторую фазу, называемую неактивной и состоящую по меньшей мере из одной генерирующей газ системы и по меньшей мере одного гидрофильного полимера или пористого минерального соединения, где активная фаза включает по меньшей мере 80% активного ингредиента. Ограничение использования не более чем 20% эксципиента, регулирующего скорость высвобождения, ограничивает гибкость, которую технолог имеет для достижения требуемой скорости высвобождения при обеспечении высокого уровня точности в воспроизводимости профиля высвобождения от партии к партии. С другой стороны, когда регулирующие скорость эксципиенты выбирают разумно, так чтобы они обеспечили хорошо воспроизводимый профиль высвобождения, даже когда их используют в небольших количествах, они сами не могут быть быстро и хорошо набухаемыми. В системе WO 01/10417 используют неактивную фазу для достижения состояния плавучести на поверхности, которая достигается посредством низкой плотности, являющейся результатом улавливания диоксида кремния в матрице неактивной фазы.
ЗАДАЧА ИЗОБРЕТЕНИЯ
Задачей настоящего изобретения является предоставление удерживаемой в желудке системы регулируемой доставки лекарственного средства, включающей:
а) регулирующую высвобождение лекарственного средства сердцевину, включающую лекарственное средство, хорошо набухаемый полимер и генерирующий газ агент, причем указанная сердцевина способна быстро набухать и быстро достигать состояния плавучести на поверхности при поддержании ее физической целостности в желудочно-кишечной жидкости в течение продолжительного периода времени,
b) быстро высвобождающую лекарственное средство, образующую покрытие композицию, включающую такое же лекарственное средство, как и сердцевина, и фармацевтически приемлемые эксципиенты, где образующая покрытие композиция окружает сердцевину так, что система обеспечивает двухфазное высвобождение лекарственного средства в желудочно-кишечной жидкости.
Другой конкретной задачей настоящего изобретения является предоставление удерживаемой в желудке системы доставки с регулируемым высвобождением лекарственного средства баклофена.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение предоставляет удерживаемую в желудке систему регулируемой доставки лекарственного средства, включающей:
(a) регулирующую высвобождение лекарственного средства сердцевину, включающую лекарственное средство, хорошо набухаемый полимер и генерирующий газ агент, причем указанная сердцевина способна быстро набухать и быстро достигать состояния плавучести при поддержании ее физической целостности в желудочно-кишечной жидкости в течение продолжительного периода времени, и
(b) быстро высвобождающую лекарственное средство, образующую покрытие композицию, включающую такое же лекарственное средство, как и сердцевина, и фармацевтически приемлемые эксципиенты, где образующая покрытие композиция окружает сердцевину таким образом, что система обеспечивает двухфазное высвобождение лекарственного средства в желудочно-кишечной жидкости.
Настоящее изобретение предлагает далее удерживаемую в желудке систему регулируемой доставки лекарственного средства, в которой сердцевина с регулируемым высвобождением активного ингредиента способна быстро набухать, по меньшей мере приблизительно в два раза относительно его первоначального объема, и поддерживать свою физическую целостность в желудочно-кишечной жидкости в течение продолжительного периода времени.
Настоящее изобретение предлагает также удерживаемую в желудке систему регулируемой доставки лекарственного средства, включающую баклофен или его фармацевтически приемлемую соль.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКОГО МАТЕРИАЛА
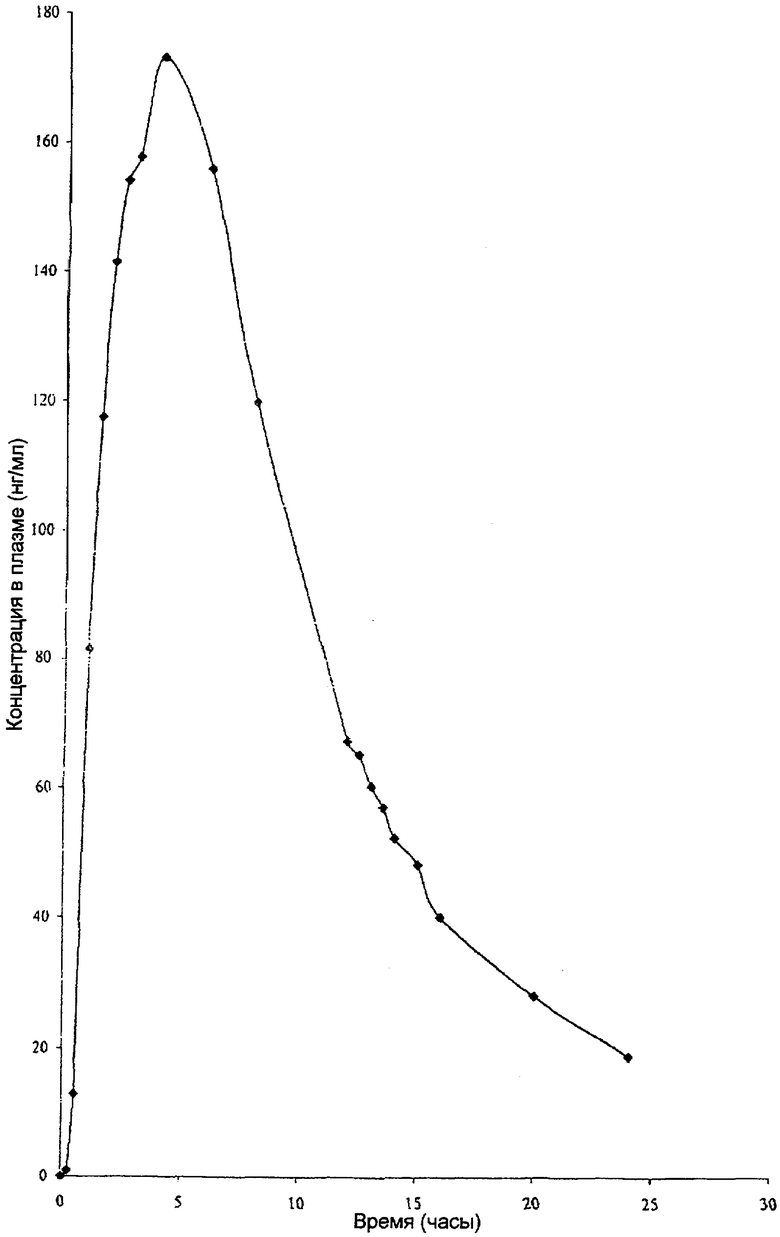
На чертеже показан профиль концентрации в плазме лекарственного средства в зависимости от времени при введении одного варианта осуществления удерживаемой в желудке системы регулируемой доставки лекарственного средства по настоящему изобретению, имеющей 30 мг баклофена.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к удерживаемой в желудке системе регулируемой доставки лекарственного средства, включающей:
а) регулирующую высвобождение лекарственного средства сердцевину, включающую лекарственное средство, хорошо набухаемый полимер и генерирующий газ агент, причем указанная сердцевина способна быстро набухать и быстро достигать состояния плавучести на поверхности при поддержании ее физической целостности в желудочно-кишечной жидкости в течение продолжительного периода времени, и
b) быстро высвобождающую лекарственное средство, образующую покрытие композицию, включающую такое же лекарственное средство, как и сердцевина, и фармацевтически приемлемые эксципиенты, где образующая покрытие композиция окружает сердцевину так, что система обеспечивает двухфазное высвобождение лекарственного средства в желудочно-кишечной жидкости.
Удерживаемая в желудке система регулируемой доставки лекарственного средства настоящего изобретения является полезной в обеспечении улучшенной доставки лекарственного средства. Лекарственные средства, которые можно использовать в удерживаемой в желудке системе регулируемой доставки лекарственного средства настоящего изобретения можно выбрать из: препараты, применяемые при злоупотреблении алкоголем, лекарственные средства, используемые для лечения болезни Альцгеймера, анестезирующие средства, агенты против агромегалии, аналгезирующие средства, антиастматические средства, антираковые средства, антикоагулянты и антитромботические агенты, противосудорожные средства, антидиабатических средств, противорвотных средств, средств против глаукомы, антигистаминов, противоинфекционных агентов, средств против болезни Паркинсона, противотромботических агентов, антиревматических агентов, спазмолитических средств и антихолинергических агентов, противокашлевых средств, ингибиторов угольной ангидразы, сердечно-сосудистых агентов, ингибиторов холинэстеразы, средств лечения нарушений ЦНС, стимуляторов ЦНС, контрацептивов, средств для лечения муковисцидоза, агонистов рецептора допамина, средств для лечения эндометриоза, средств для терапии эректильной дисфункции, агентов фертильности, желудочно-кишечных агентов, иммуномодуляторов и иммунодепрессивных средств, средств улучшения памяти, препаратов для лечения мигрени, миорелаксантов, аналогов нуклеозидов, средств для лечения остеопороза, парасимпатомиметиков, простагландинов, психотерапевтических агентов, седативных средств, снотворных средств и транквилизаторов, лекарственных средств, используемых для лечения кожи, стероидов и гормонов.
Примерами агентов для лечения акромагалии являются октреотид, лауреотид и пегвисомант.
Примерами препаратов, применяемых при злоупотреблении алкоголем, являются хлоразепат, хлордиазепоксид, диазепам, дисульфирам, гидроксизин, налтрексон и их соли.
Примерами анестезирующих средств являются адреналин, бупивакаин, хлоропрокаин, дезфлуран, этидокаин, левобупивакаин, лидокаин, мидазолам, пропофол, ропивакаин и их соли.
Примерами аналгетиков являются ацетаминофен, аспирин, бупивакаин, бупренофин, буторфанол, целекоксиб, хлофенадол, холин, клонидин, кодеин, дифлунизал, дигидрокодеин, дигидроэрготамин, дигидроморфин, этилморфин, этодолак, елетриптан, эптазоцин, эрготамин, фентанил, фентопрофен, гиалуроновая кислота, гидрокодон, гидроморфон, гилан, ибупрофен, линдометацин, кеторолак, кетотифен, левометадон, леваллорфан, леворфанол, лидокаин, мефенамовая кислота, мелоксикам, меперидин, метадон, морфин, набуметон, налбуфин, нефопам, налорфин, налоксон, налтрексон, напроксен, наратриптан, нефазодон, морметадон, оксапозин, оксикодон, оксиморфон, пентазоцин, петидин, пенпирамид, пиритрамид, пироксикам, пропоксифен, рефекоксиб, ризатриптан, салсалакетопрофен, сулиндак, суматриптан, тебакон, тилидин, толметин, трамадол, золмитриптан и их соли.
Примерами антиастматических средств являются аблукаст, азеластин, бунапроласт, циналукаст, кромитрил, кромолин, энофеласт, изамоксол, кетотифен, леверомекалин, лодоксамид, монтелукаст, онтазоласт, оксарбазол, оксатомид, пирипрост калий, пиролат, побилукаст эдамин, квиазоласт, репиринаст, ритолукаст, зулукаст, тетразоластмеглумин, тиарамид, мибенеласт, томелукаст, траниласт, верлукаст, верофиллин, зарирлукаст.
Примерами антираковых агентов являются адриамицин, алдеслейкин, аллопуринол, алтретамин, амифостин, анастрозол, аспарагиназа, бетаметазон, бексаротен, бикалутамид, блеомоцин, бусульфан, капецитабин, карбоплатин, кармустин, хлорамбуцил, цисплатин, кладрибин, конъюгированный эстроген, кортизон, циклофосфамид, цитарабин, дакарбазин, даунорубицин, дактиномицин, денилейкин, дексаметазон, дискодермолид, доцетаксел, доксорубицин, элопозидем, эпирубицин, эпоетин, эпотилоны, эстрамустин, этерифицированный эстроген, этинилэстрадиол, этопозид, эксеместан, флавопирдол, флуконазол, флударабин, фторурацил, флутамид, флоксуридин, гемцитабин, гемтузумаб, гозерелин, гексаметилмеламин, гидрокортизон, гидроксимочевина, идарубицин, ифосфамид, интерферон, иринотекан, лемипозид, летрозол, лейпролид, левамезол, левотироксин, ломустин, мехлоретамин, мелфалан, меркаптопурин, мехлоретамин, мегестерол, метотрексат, метилпреднизолон, метилтестостерон, митрамицин, митомицин, митотан, митоксантрон, митозоломид, мутамицин, нилутамид, паклитаксел, памидронат, пегаспаргаза, пентостатин, пликамицин, порфимер, преднизолон, прокарбазин, ритуксимаб, сарграмостим, семустин, стрептозоцин, тамоксифен, темозоламид, тенипозид, тестолактон, тиогуанин, тиотепа, томудекс, топотекан, торемифен, транстумузаб, третиноин, семустин, стрептозолоцин, валрубицин, вертепрофин, винбластин, винкристин, виндезин, винорелбин и их соли.
Примерами антикоагулянтов и антитромботических агентов являются варфарин, далтепарин, гепарин, тинзапарин, эноксапарин, данапароид, абциксимаб, алпростадил, алтиплаз, анагралид, анистреплаза, аргатробан, амапрост, берапрост, камонагрил, цилостазол, клинпрост, клопидогрел, клорикромен, дерматан, дезирудин, домитробан, дротаверин, эпопростенол, эптифибатид, фрадафибан, габексат, илопрост, избогрель, ламифибан, ламотеплаза, лефрадафибан, лепирудин, левозимендан, лексипафант, мелагатран, нафагрел, нафамостсат, низофенон, орбифибан, озагрел, памикогрел, парнапарин, хинобендан, ретеплаз, сарпогралат, сатигрел, силтеплаз, симендан, тиклопидин, вапипрост, тирофибан, хемилофибан, Y20811 и их соли.
Примерами противосудорожных средств являются карбамазепин, клоназепам, клоразепин, диазепам, дивалпроекс, этосуксимид, этотион, фелбамат, фосфенитоин, габапентин, ламотригин, леветирацетам, лоразепам, мефенитоин, мефобарбитал, метарбитал, метзуксимид, окскарбазепин, фенобарбитал, фенитоин, примидон, тиагабин, топирамат, валпроевая кислота, вигабатрин, зонисамид и их соли.
Примерами антидиабетических агентов являются акарбоза, ацетохексамид, карбутамид, хлорпропамид, эпалрестат, глиборнурид, гликлазид, глимепирид, глипизид, глихидон, глизоксепид, глибурид, глихексамид, метформин, миглитол, натеглинид, орлистат, фенбутамид, пиоглитазон, репаглинид, розиглитазон, толазамид, толбутамид, толцикламид, толрестат, троглитазон, воглибоза и их соли.
Примерами противорвотных средств являются алпразолам бензхинамид, бензтропик, бетагистин, хлорпромазин, дексаметазон, дифенидол, дименгидринат, дифенгидрамин, долазетрон, домперидон, дронабинол, дроперидол, гранизетрон, галоперидол, лоразепам, меклизин, метилпреднизолон, метоклопрамид, онданзетрон, перфеназин, прохлорперазин, прометазин, скополамин, трибутин, триэтилперазин, трифлупромазин, триметобензамид, тропизетрон и их соли.
Примерами средств против глаукомы являются алпреноксим, дапипразол, дипивефрин, латанопрост, набостат, пирнабин и их соли.
Примерами антигистаминов являются акривастин, активастин, албутерол, азеластин, битолтерол, алимемазин, амлексанокс, азеластин, бензидамин, бромфенирамин, цетиризин, хлорфенирамин, циметидин, клемастин, циклогептазин, ципрогептадин, диклофенак, дифенгидрамин, дотаризин, эфедрин, эпинастин, эпинефрин, этилнорэпинефрин, фенпотерол, фексофенадин, флурбипрофен, гидроксизин, ибупрофен, изоэтарин, изопротеренол, ипратропия бромид, кеторолак, левоцетиризин, лоратидин, мехитазин, метапротеренол, фенилэфрин, фенилпропаноламин, пирбутерол, прометазин, псевдоэфедрин, пириламин, салметерол, тербуталин, траниласт, производные ксантина, ксилометазолин и их соли.
Примерами противоинфекционных агентов являются абакавир, албендазол, амантадин, амфотерицин, амикацин, аминосалициловая кислота, амоксициллин, ампициллин, ампренавир, атовахин, азитромицин, азтреонам, карбенициллин, цефаклор, цефадроксил, цефамандол, цефазолин, цефдинир, цефепим, цефексим, цефоперазон, цефотаксим, цефотитам, цефоперазон, цефокситин, цефподоксин, цефпрозил, цефтазидим, цефтрибутен, цефтизоксим, цефтриаксон, цефуроксим, цефалексин, хлорохин, цидофовир, циластатин, ципрофлоксацин, кларитромицин, клавулиновая кислота, клиндамицин, колистиметат, далфопристин, дапсон, даунорубицин, денлавирдин, демеклоциклин, диданозин, доксициклин, доксорубицин, эфавиренц, эноксацин, эритромицин, этамбутол, этионамид, фамсифловир, флуконазол, флуцитоцин, фоскарнет, фосфомицин, ганциклавир, гатифлоксацин, гризеофульвин, гидроксихлорохин, имипенем, индинавир, интерферон, изониазид, итраконазол, ивермектил, кетоконазол, ламивудин, левофлоксацин, линизолид, ломефлоксацин, ловакарбеф, мебендазол, мефлохин, меропенем, метанамин, метронидазол, миноциклин, моксефлоксацин, налдиксовая кислота, нелфинавир, неомицин, невирапин, ниторофурантоин, норфлоксацин, офлоксацин, оселтамивир, окситетрациклин, паливизумаб, пенициллины, перфлоксацин, пиперациллин, празиквантел, пиразинамид, пириметамин, хинидин, хинупристин, ретонафир, рибавирин, рифабутин, рифампицин, римантадин, сахинавир, спарфлоксацин, ставудин, стрептомицин, сульфаметоксазол, терамицин, тербинафин, тетрациклин, тикарциллин, тиабендазол, тобрамицин, триметоприм, триметраксат, тролеандомицин, тровафлоксацин, валацикловир, ванкомицин, залцитабин, занамивир, зидовудин и их соли.
Примерами средств против болезни Паркинсона являются амантадин, адроголид, алтиниклин, бензтропин, бипериден, бразофензин, бромокриптин, будипин, каберголина, CHF-1301, дигидрекдисин, энтакапон, этилеводора, идазоксан, иометопан, лазабемид, мелеводопа, карбидопа/леводопа, мофегилин, моксираприн, перголид, прамипексол, хинелоран, разагилин, ропинирол, селигилин, талипексол, толкапон, тригексифенидил и их соли.
Примерами антиревматических агентов являются азатиприн, бетаметазон, целекоксиб, циклоспорин, диклофенак, гидроксихлорохин, индометацин, инфликсимаб, меркатобутандиовая кислота, метилпреднизолон, напроксен, пенцилламин, пироксикам, преднизолон, сульфазалазин и их соли.
Примерами противотромботических агентов являются абциксимаб, анагрелид, аспирин, цилостазол, клоридогрел, дипиридамол, эпопростенол, эптифибатид, тиклопидин, тинофибан и их соли.
Примерами спазмолитических средств и антихолинергических средств являются аспирин, атропин, диклофенак, гиосциамин, мезопростол, метокарбамол, фенобарбитал, скополамин и их соли.
Примерами противокашлевых агентов являются ацетаминофен, акривастин, албутерол, бензонатат, берактант, бромфенирамин, каффеин, калфактант, карбетапентан, хлорфенирамин, кодеин, колфусцерин, декстрометорфам, дорназа альфа, доксиламин, эпинефрин, фексофенадин, гуафенезин, ипратропий, левалбутерол, метапротеренол, монтелукаст, пентоксифилин, фенилэфрин, фенилпропаноламин, пирбутерол, порактант альфа, псевдоэфедрин, пириламин, салбутерол, салметерол, тербуталин, теофиллин, зафирлукаст, зилеутон и их соли.
Примерами ингибиторов угольной ангидразы являются ацетазоламид, дихлорфенамид, дорзоламид, метазоламид, сезоламид и их соли.
Примерами сердечно-сосудистых агентов являются абциксимаб, ацебутолол, активаза, аденозин, адреналин, амидарон, амилорид, амелодипин, амилнитрат, атенолол, аторвастатин, бензеприл, бепиридил, бетаксалол, бисопролол, кандесартан, каптоприл, картенолол, карведилол, церивастатин, хлорталидон, хлортиазол, клофибрат, клонидин, колестипол, колосевелам, дигоксиним, дилтиазем, дизопирамид, добутамин, дофетилид, доксазосин, эналаприл, эпопростенол, эпросартан, эсмолол, этакринат, эритритил, фелодипин, феноидапам, фозиноприл, флекаинид, флуросемид, флувастатин, гемфиброзил, гидрохлортиазид, гидрофлуметазин, ибутилид, индапамид, изосорбид, ирбесартан, лабетолол, лацидипин, лизиноприл, лозартан, ловастатин, мекамиламин, метапролол, метарминол, метазолон, метилхлотаизид, метилдопа, метирозин, мексилетин, мидродин, милринонр, моексиприл, надолол, ниацин, никардипин, никорандил, нифидепин, нимодипин, низолдипин, нитроглицерин, феноксибензамин, периндоприл, политиазид, правастатин, празосин, прокаинамид, пропафенон, пропранолол, хинфацин, хинаприл, хинидин, раниприл, ретеплаза, симвастатин, сомалол, спиронолактон, стрептокиназа, телмисартан, теразосин, тимолол, токаинамид, торсемид, трандолаприл, триамтерен, трапидил, валсартан и их соли.
Примерами ингибиторов холинэстеразы являются донерезил, эдрофоний, неостигмин, пиридостигмин, ривастигмин, такрин и их соли.
Примерами стимуляторов ЦНС являются кофеин, доксапрам, дексоамфетамин, донепезил, эдорфониум, метамфетамин, метилфенидат, модафинил, неостигмин, пемолин, фентермин, пириодстигмин, ривастигмин, такрин и их соли.
Примерами контрацептивов являются дезогестрал, этинилэстрадиол, этинодиол, левоноргестрел, медроксипрогестерон, местранол, норгестимат, норэтиндрон, норгестрел и их соли.
Примерами средств для лечения муковисцидоза являются дорназа альфа, панкрелипаза, тобрамицин и их соли.
Примерами агонистов рецептора допамина являются амантадин, каберголин, фенолдопам, перголид, прамипезал, ропинирол и их соли.
Примерами средств для лечения эндометриоза являются даназол, гозерелин, лейпролид, нафарелин, норетиндрон и их соли.
Примерами лекарственных средств, используемых для лечения эректильной дисфункции, являются альпростадил, силденафил, йохимбин и их соли.
Примерами агентов фертильности являются цитрореликс, кломифен, фоллитропин, ганиреликс, гонадотропин, менотропин, прогестерон, урофоллитропин и их соли.
Примерами желудочно-кишечных агентов являются алосетрон, бисакодил, висмута субсалицилат, целекоксиб, дифоксин, дифеоксилат, докузат, фамотидин, гликопирролат, инфликсимаб, лансопразол, лоперамид, метаклопрамид, низатидин, омепразол, пантопразол, рабепразол, ранитидин, симетикон, сукралфат и их соли.
Примерами иммуномодуляторов и иммуносупрессантов являются азатиоприн, цефтизоксин, циклоспорин, даклизумаб, глатирамер, иммуноглобулин, интерферон, лефлуномид, левамизол, микофенолят, маузоманаб, фталидомид, рибавирин, сиролимус и их соли.
Примерами лекарственных средств, используемых при лечении болезни Альцгеймера, являются СР 118954, донепезил, галантамин, метрифонат, ревастигмин, такрин, ТАК-147 и их соли.
Примерами лекарственных средств, используемых для препаратов от мигрени, являются ацетаминофен, дигидроэрготамин, дивалпроекс, эрготамин, пропранолол, ризатриптан, сумитриптан, триметрексат и их соли.
Примерами релаксантов мышц являются алкуроний-хлорид, азапропазон, атракурий, баклофен, каризопродол, производные хинина, хлоромезанон, хлорофенезинкарбамат, хлорозоксазон, циклобензаприн, дантролен, декаметонийбромид, диметилтубокураринийхлорид, доксакурий, фенирамидол, галламинтриэтиодид, гвайяфенсин, гексафлуоренийбромид, гексакарбахолинбромид, мемантин, мефенесин, мепробамат, метамизол, метаксалон, метокарбамол, мивакуриум, орфенадрин, панкуроний, феназон, фенпробамат, пипекуроний, рапакуроний, рокуроний, сукцинилхолин, суксаметонийхлорид, тетразепам, тизанидин, тубокураринхлорид, тубамат, векуроний и их соли.
В предпочтительных вариантах удерживаемой в желудке системы регулируемой доставки лекарственного средства используемым релаксантом мышц является баклофен или его фармацевтически приемлемая соль. Система регулируемой доставки лекарственного средства с удерживанием баклофена в желудке является неизвестной или неописанной, или не предложенной до настоящего изобретения.
Баклофен может быть использован в системе в количестве, составляющем приблизительно от 15 мг до приблизительно 80 мг. В системе регулируемой доставки лекарственного средства настоящего изобретения с удерживанием баклофена в желудке баклофен используют в количестве 30 мг. Систему изготовляют так, чтобы основная часть 30 мг дозы баклофена присутствовала в сердцевине и была доступной по мере регулируемого выделения, тогда как небольшая часть лекарственного средства присутствовала в покрытии и была доступна сразу. Таким образом, двухфазное высвобождение баклофена обеспечивается системой доставки настоящего изобретения.
Примерами аналогов нуклеозидов являются абакавир, ацикловир, диданозин, гамцикловир, гемцитабин, ламивудин, рибавирин, ставудин, залцитабин и их соли.
Примерами лекарственных средств, используемых для лечения остеопороза, являются алендронат, кальцитонин, эстрадиол, эстропипат, медроксипрогестерон, норэтиндрон, норгестимат, памидронат, ралоксифен, риздронат, золедронат и их соли.
Примерами парасимпатомиметиков являются бетанхол, биперидин, эдрофоний, гликопиролат, гиосциамин, пилокарпин, такрин, йохимбин и их соли.
Примерами простагландинов являются альпростадил, эпопростенол, мизопростол и их соли.
Примерами психотерапевтических агентов являются ацетофеназин, атентемол, алпертин, алпразолам, амитриптилин, априпразол, азаперон, бателапин, бефипирид, бенперидол, бензиндоперин, бимитил, бириперон, брофоксин, бромперидол, бромперидол, бупропион, буспирон, бутакламол, бутаперазин, бутаперазин, карфеназин, карвотролин, церикламин, хлоразепин, хлордиазепоксид, хлорпромазин, хлорпротиксен, цинперен, цинтриамид, циталопрам, кломакран, клоназепам, клопентиксол, клопимозид, клопипазан, клороперон, клотиапин, клотиксамид, клозапин, циклофеназин, дапипразол, дапоксетин, дезипрамин, дивалпроекс, дипуридамол, доксепин, дроперидол, дулоксетин, злтопразин, эптипирон, этазолят, фенимид, флибансерин, флуциндол, флумезапин, флуоксетин, флуфеназин, флуспиперон, флуспирилен, флутролин, флувоксамин, гепирон, гевотролин, галопемид, галоперидол, гидроксизин, гидроксинортриптилин, илоперидон, имидолин, ламотригин, локсапин, энперон, мазапертин, мефобарбитал, мепробамат, мезоридазин, мезоридазин, милнаципран, миртазепин, метиапин, миленперон, милипертин, молиндон, нафадотрид, наранол, нефазодон, нефлюмозид, окаперидон, одапипам, оланзапин, оксетиазин, оксиперомид, пагоклон, палиперидон, парокситен, пенфлуридол, пентиапин, перфеназин, фенелзин, пимозид, пиноксепин, пипамперон, пиперацетазин, пипотиазин, пихиндон, пирлиндол, пивагабин, прамипексол, прохлорперазин, прохлорперазин, промазин, кветиапин, ребоксетин, ремоксиприд, ремоксиприд, рисперидон, римказол, роболзотан, селегилин, сеперидол, сертралин, сертиндол, сетептилин, сетоперон, спиперон, сунипитрон, теририндол, тиоридазин, тиотиксен, тиаприд, тиоперидон, тиоспирон, топирамат, транилципромин, трипфлуоперазин, трифлуперидол, трифлупромазин, трифлупромазин, тримипрамин, венлафаксин, зипразидон и их соли.
Примерами седативных средств, снотворных средств и транквилизаторов являются бромазепам, биспирон, клазолам, клобазам, хлоразепат, диазепам, демоксепам, дексмедетомитин, дифинилгидрамин, доксиламин, энципразин, эстразолам, гидроксизин, кетазолам, лоразатон, лоразепам, локсапин, медазепам, меперидин, метобарбитал, мидазолам, набилон, низобамат, оксазепам, пентобарбитал, прометазин, пропофол, триазолам, залеплон, золпидем и их соли.
Примерами лекарственных средств, используемых для лечения кожных заболеваний, являются ацитретин, алклометазон, аллитретиноин, бетаметазон, кальципротрин, хлоргексидин, клобетазол, клокортолон, клотриамозол, коллагеназа, циклоспарин, дезонид, дифлуорозон, доксепин, эфлометин, финастерид, флуоцинолон, флурандренолид, флутиказон, галобетазол, гидрохлорохин, гидрохинон, гидроксизин, кетоконазол, мафенид, малатион, менобензон, неостигмин, нистатин, подофилокс, повидон, тазоротен, третиноин и их соли.
Примерами стероидов и гормонов являются алклометазон, бетаметазон, кальцитонин, цитрореликс, клобетазол, клокортолон, кортизоны, даназол, дезмопрессин, дезонид, дезогестрел, дезоксиметазон, дексаметазон, дифлоразон, эстрадиол, эстрогены, эстропипат, этинилэстрадиол, флуоцинолон, флурандренолид, флутиказон, глюкагон, гонадотропин, гозерелин, галобетазол, гидрокортизон, лейпролид, левоноргестрел, левотироксин, медроксипрогестерон, менотропины, метилпреднизолон, метилтестостерон, мометазон, наферелин, нордитропин, норэтиндрон, норгестрел, октриолид, оксандролон, оксиметолон, политропин, предникарбат, преднизолон, прогестерон, серморелин, соматропин, станозолол, тестостерон, урофоллитропин и их соли.
В соответствии с данным изобретением сердцевина достигает высокой степени набухания за короткий срок. Такая высокая степень набухания может быть достигнута посредством использования сильно и быстро набухаемых полимеров или посредством избегания высокого давления уплотнения набухаемых полимеров или посредством использования хорошо набухаемых полимеров, которые, по существу, прессуют до низкой плотности. Когда сердцевина, которую прессуют, имеет низкую плотность, она имеет достаточную прочность, так что если на нее нужно далее нанести покрытие прессованием, то она может быть перенесена механически из первого участка прессования, где ее прессуют, во второй участок прессования, где образуется покрытие прессованием; или, если на нее нужно далее нанести покрытие распылением, она может выдерживать жесткие условия перемешивания в оборудовании для нанесения покрытия.
Примеры сильно набухаемых полимеров, которые могут быть использованы в настоящем изобретении, включают:
- сильно набухаемые сорта простых эфиров целлюлозы, такие как гидрокси-С1-4-алкил-С1-4-алкилцеллюлозы, карбоксиалкилцеллюлозы, гидрокси-С-1-4-алкилцеллюлозы, предпочтительно гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, более предпочтительно сорт гидроксиэтилцеллюлозы с высокой вязкостью;
- камеди растительного, животного, минерального или синтетического происхождения, такие как (i) агар, альгинаты, каррагенин, фурцелларан, полученный из морских растений, (ii) камедь рожкового дерева, гуммиарабик, трагакантовая камедь, камедь карайи, камедь бобов рожкового дерева, пектин, полученный из наземных растений, (iii) микробные полисахариды, такие как декстран, геллановая камедь, рамзановая камедь, велановая камедь, ксантановая камедь, и (iv) синтетические или полусинтетические камеди, такие как альгинат пропиленгликоля, гидроксипропилированная камедь рожкового дерева;
- супердезинтегрирующий полимер, такой как сшитый поливинилпирролидон, сшитая натриевая соль карбоксиметилцеллюлозы, карбоксиметилкрахмал, гликолят крахмала натрия, сополимер метакрилата калия и дивинилбензола, поливиниловые спирты, амилоза, сшитая амилоза, производные крахмала, микрокристаллическая целлюлоза или производные целлюлозы, альфа-, бета- и гамма-циклодекстрин и производные декстрина;
- полимер акриловой кислоты, такой как сшитый полимер, доступный под фирменным наименованием Carbopol®;
- полимер винилпирролидона, такой как сшитый поливинилпирролидон или кросповидон; сополимеры винилпирролидона и винилацетата или их смеси.
В предпочтительных вариантах осуществления сильно набухаемый полимер представляет собой смесь супердезинтегрирующего средства и одного или нескольких связующих агентов, причем связующий агент выбран из гидрофильных полимеров, предпочтительно хорошо набухаемых полимеров. В предпочтительных вариантах осуществления используемый гидрофильный полимер представляет собой имеющее высокую вязкость производное целлюлозы, имеющее вязкость водного раствора, составляющую приблизительно от 500 мПа до приблизительно 120000 мПа. Смесь натриевой соли гликолята крахмала и сорта гидроксиэтилцеллюлозы с высокой вязкостью используют в качестве предпочтительного набухаемого полимера в одном варианте осуществления настоящего изобретения. Еще в одном предпочтительном варианте осуществления используемым полимером с высокой набухаемостью является смесь натриевой соли гликолята крахмала, сорта гидроксиэтилцеллюлозы с высокой вязкостью и гидроксипропилметилцеллюлозы.
Натриевой солью гликолята крахмала является натриевая соль карбоксиметилового эфира крахмала, имеющего молекулярную массу в диапазоне от 500000 до 1000000 дальтонов, она является коммерчески доступной как Explotab® и Primojel®. Натриевая соль гликолята крахмала вызывает дезинтеграцию быстрым поглощением воды с последующим быстрым и значительным набуханием. Преимущество использования натриевой соли гликолята крахмала в качестве дезинтегрирующего средства состоит в том, что на его эффективность не влияет присутствие гидрофобных эксципиентов, таких как смазывающие вещества, или повышенное давление прессования. Она способна набухать в воде до 300-кратного ее объема. Натриевую соль гликолята крахмала используют в качестве предпочтительного дезинтегрирующего средства в настоящем изобретении в количестве, составляющем приблизительно от 5 мас.% до приблизительно 50 мас.% сердцевины, предпочтительно приблизительно от 10 мас.% до приблизительно 40 мас.% сердцевины, более предпочтительно приблизительно от 15 мас.% до приблизительно 30 мас.% сердцевины.
Гидроксиэтилцеллюлоза является неионным водорастворимым полимером, который представляет собой частично замещенный поли(гидроксиэтиловый) эфиром целлюлозы и доступен в виде разных сортов, которые различаются вязкостью и степенью замещения. Она коммерчески доступна как Cellosize от Amerchol Corp. и Natrosol® от Aqualon. В качестве гидрофильного полимера в настоящем изобретении предпочтительно используют гидроксиэтилцеллюлозу, 2 мас./об.% водный раствор, которой имеет вязкость, составляющую от 9000 мПа до 30000 мПа. Ее используют в количестве, составляющем приблизительно от 5 мас.% до приблизительно 50 мас.% сердцевины, предпочтительно приблизительно от 10 мас.% до приблизительно 40 мас.% сердцевины, более предпочтительно, приблизительно от 15 мас.% до приблизительно 30 мас.% сердцевины.
Гидроксипропилметилцеллюлоза (НРМС) является частично О-метилированной и O-(2-гидроксипропилированной) целлюлозой, доступной в виде разных сортов, вязкость у которых разная. Молекулярная масса НРМС составляет от 10000 до 1500000. Она является коммерчески доступной как Benecel MHPC, Methocel и Metolose. В одном варианте осуществления настоящего изобретения в качестве набухаемого полимера используют НРМС сорта К4М в количестве, составляющем приблизительно от 5 мас.% до приблизительно 25 мас.% сердцевины, более предпочтительно приблизительно от 10 мас.% до приблизительно 15 мас.% сердцевины.
В предпочтительных вариантах осуществления в качестве хорошо набухаемого полимера используют смесь гидроксиэтилцеллюлозы с высокой вязкостью и натриевой соли гликолята крахмала, предпочтительно при массовом отношении гидроксиэтилцеллюлоза: натриевая соль гликолята в диапазоне от 1:9 до 9:1, более предпочтительно от 3:7 до 7:3 и еще более предпочтительно от 4:6 до 6:4. Сердцевины, образованные этой смесью, способны быстро набухать и достигать плавучести при поддержании их физической целостности на протяжении продолжительного периода времени.
Генерирующий газ агент, используемый в сердцевине системы доставки лекарственного средства настоящего изобретения с удерживанием в желудке, может включать один компонент, который генерирует газ при контактировании с желудочным соком, или может включать пару компонентов, генерирующих газ. Генерирующие газ компоненты, которые можно использовать в настоящем изобретении, включают карбонаты, такие как карбонат кальция, бикарбонаты, такие как бикарбонат натрия или калия, сульфиты, такие как сульфит натрия, бисульфит натрия или метабисульфит натрия и тому подобное. Указанные соли можно использовать как таковые или в комбинации с источником кислоты, таким как генерирующая газ пара компонентов. Источником кислоты может быть пищевая органическая кислота, соль пищевой органической кислоты или их смеси. Примеры органических кислот, которые можно использовать, включают лимонную кислоту, яблочную кислоту, янтарную кислоту, винную кислоту, фумаровую кислоту, малеиновую кислоту, аскорбиновую кислоту, глутаминовую кислоту и их соли и их смеси. Генерирующий газ агент используют в количестве, составляющем приблизительно от 1 мас.% до приблизительно 50 мас.% сердцевины, более предпочтительно приблизительно от 1 мас.% до приблизительно 15 мас.% сердцевины. В качестве генерирующего газ агента используют бикарбонат натрия.
Очень хорошо набухаемый полимер может дополнительно включать эксципиент, который повышает скорость набухания системы доставки. Этим эксципиентом может быть водорастворимое соединение, которое вызывает осмос, или впитывающий агент, такой как микрокристаллическая целлюлоза, который способствует притоку воды в систему. Водорастворимые соединения, подходящие для индуцирования осмоса, т.е. осмотические агенты или осмогенты, включают все фармацевтически приемлемые и фармакологически инертные водорастворимые соединения, относящиеся к фармакопеям, таким как United States Pharmacopoeia, а также в Remington: The Science and Practice of Pharmacy. Обычно предпочтительными являются фармацевтически приемлемые водорастворимые соли неорганических или органических кислот или неионные органические соединения с высокой водорастворимостью, например углеводы, такие как сахар, или аминокислоты. Примеры агентов, используемых для индуцирования осмоса, включают неорганические соли, такие как хлорид магния или сульфат магния, хлорид лития, натрия или калия, гидрофосфат лития, натрия или калия, дигидрофосфат лития, натрия или калия, соли органических кислот, такие как ацетат натрия или калия, сукцинат магния, бензоат натрия, цитрат натрия или аскорбат натрия; углеводы, такие как маннит, сорбит, арабиноза, рибоза, ксилоза, глюкоза, фруктоза, манноза, галактоза, сахароза, мальтоза, лактоза, рафиноза; водорастворимые аминокислоты, такие как глицин, лейцин, аланин или метионин; мочевина и тому подобное и их смеси. В предпочтительных вариантах осуществления сердцевина удерживаемой в желудке системы регулируемой доставки лекарственного средства включает один или несколько осмотических агентов, которые повышают скорость набухания системы. Осмотический агент, предпочтительно используют в количестве, составляющем приблизительно от 0,5 мас.% до приблизительно 50 мас.% сердцевины, более предпочтительно, от 2 мас.% до приблизительно 40 мас.% сердцевины.
Удерживаемая в желудке система регулируемой доставки лекарственного средства настоящего изобретения может включать также различные фармацевтически приемлемые эксципиенты, например дезинтегрирующие агенты, такие как крахмал, производные целлюлозы, камеди, сшитые полимеры и тому подобное; связующие, такие как крахмал, желатин, сахара, производные целлюлозы, поливинилпирролидон и тому подобное; смазывающие вещества, такие как тальк, стеарат магния, коллоидальный диоксид кремния, полиэтиленгликоль, производные целлюлозы и тому подобное, и их смеси.
В предпочтительных вариантах осуществления гидроксипропилметилцеллюлозу (НРМС) используют в качестве связующего. НРМС К4М предпочтительно используют в качестве связующего в количестве, составляющем приблизительно от 0,2 мас.% до приблизительно 5 мас.%, более предпочтительно приблизительно от 0,2 мас.% до приблизительно 2 мас.% сердцевины.
Примеры смазывающих веществ, которые могут быть использованы в настоящем изобретении, включают тальк, стеарат магния, стеарат кальция, стеарат алюминия, стеариновую кислоту, гидрогенизированные растительные масла, коллоидальный диоксид кремния, полиэтиленгликоль, производные целлюлозы, такие как карбоксиалкилцеллюлоза и ее соли щелочных металлов или их смеси. В предпочтительных вариантах используемое смазывающее вещество является смесью силикатизированной микрокристаллической целлюлозы, талька и полиэтиленгликоля. Силикатизированная микрокристаллическая целлюлоза представляет собой синергическую тесную физическую смесь микрокристаллической целлюлозы и коллоидального диоксида кремния, имеющую размер частиц в диапазоне от 20 до 200 мкм, и обычно содержит 2 мас.% коллоидального диоксида кремния. Она является коммерчески доступной как Prosolv® SMCC и имеет улучшенные свойства прессования по сравнению с микрокристаллической целлюлозой. Используемый полиэтиленгликоль (ПЭГ) представляет собой ПЭГ 8000. Смесь используют в качестве смазывающего вещества в количестве, составляющем приблизительно от 0,5 мас.% до приблизительно 40 мас.% сердцевины, предпочтительно приблизительно от 5 мас.% до приблизительно 30 мас.% сердцевины, более предпочтительно приблизительно от 10 мас.% до приблизительно 25 мас.% сердцевины.
Сердцевину удерживаемой в желудке системы регулируемой доставки лекарственного средства окружают композицией покрытия с быстрым высвобождением, содержащей такое же лекарственное средство, как в сердцевине, и фармацевтически приемлемые эксципиенты. В предпочтительном варианте осуществления настоящего изобретения композиция покрытия включает баклофен и фармацевтически приемлемые эксципиенты, такие как пленкообразующие агенты, пластификаторы и тому подобное. Пленкообразующие агенты выбраны из группы, состоящей из простых и сложных эфиров целлюлозы, таких как метилцеллюлоза, этилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза (НРМС); полимеры акриловой кислоты, такие как сополимеры метакрилата и метилметакрилата и тому подобное и их смеси. В предпочтительных вариантах осуществления гидроксипропилметилцеллюлозу используют в качестве пленкообразующего агента в количестве, составляющем приблизительно от 0,5 мас.% до приблизительно 5 мас.% сердцевины, предпочтительно приблизительно от 1 мас.% до приблизительно 3 мас.% сердцевины. Быстро высвобождающая композиция может дополнительно содержать один или несколько пластификаторов, выбранных из группы, включающей глицерин, пропиленгликоль, полиэтиленгликоль, ацетилированный моноглицерид, цитратные эфиры, такие как триэтилцитрат, и фталатные эфиры, такие как диэтилфталат. В предпочтительных вариантах осуществления в качестве пластификатора используют пропиленгликоль. В альтернативном варианте раствор для покрытия гидроксипропилметилцеллюлозы, коммерчески доступный как Opadry® II от Colorcon, может быть смешан с лекарственным средством и использован для покрытия сердцевин с регулируемым высвобождением.
Изготовление таблеток с покрытием может быть проведено в две стадии. В первой стадии изготовления композицию сердцевины добавляют в полость пресс-формы в первом участке прессования, прессуют и выталкивают при помощи нижнего штампа. Вторая стадия состоит в нанесении покрытия на сердцевину общепринятыми способами, такими как нанесение покрытия распылением или нанесение покрытия прессованием. Покрытие распылением включает экспонирование поверхности сердцевины посредством вращения ее в подходящем сосуде для нанесения покрытия или посредством псевдоожижения их в псевдоожижающем устройстве и нанесение композиций покрытия, содержащих лекарственное средство и полимеры. Лекарственное средство включают либо в ту же самую композицию, содержащую полимер для покрытия в жидком наполнителе, либо наносят слоем в виде порошка. Покрытие прессованием включает помещение композиции для покрытия для нижней половины таблетки в пресс-форму во втором участке прессования, перенос сердцевины из первого участка прессования во второй участок прессования и помещение ее в центр композиции для покрытия, уже помещенной в пресс-форму, фазу прессования с образованием покрытой таблетки и фазу выбрасывания, которая служит для удаления таблетки с нанесенным прессованием покрытием из пресс-формы с помощью нижнего штампа.
Удерживаемая в желудке система регулируемой доставки лекарственного средства настоящего изобретения быстро набухает, в то же время сохраняя свою физическую целостность в желудочно-кишечной жидкости в течение продолжительных периодов времени. Низкая плотность достигается улавливанием газа, генерированного генерирующим газ агентом, так что система держится на поверхности желудочного сока. Набухание и улавливание газа могут происходить быстро, так что система способна достигать плавучести в бане растворения, содержащей 0,1 н. HCl, через 15 минут, предпочтительно меньше чем через 10 минут.
Следующие примеры не ограничивают объем изобретения, а используются в качестве иллюстраций.
Пример 1
Удерживаемую в желудке систему регулируемой доставки лекарственного средства получали, как указано ниже на табл.1.
Сердцевину удерживаемой в желудке системы регулируемой доставки лекарственного средства получали пропусканием баклофена, лактозы, гидроксиэтилцеллюлозы, натриевой соли гликолята крахмала, бикарбоната натрия и части НРМС К4М через сито #40 ASTM (American Society for Testing and Materials) и смешиванием ингредиентов для получения сухой порошкообразной смеси. Водный раствор НРМС К4М затем использовали для грануляции сухой порошкообразной смеси. Таким образом полученные гранулы пропускали через подходящее сито и сушили. Сухие гранулы смазывали смесью Prosolv SMCC 90, тальком, ПЭГ 8000 и НРМС К4М и прессовали для получения сердцевин. Сердцевины затем покрывали водным раствором, содержащим баклофен и Opadry II для получения удерживаемой в желудке системы регулируемой доставки лекарственного средства настоящего изобретения.
Полученные таким образом таблетки подвергали испытанию на растворение при 37°С с использованием аппаратуры растворения United States Pharmacopoeia Type II (лопасти) при вращении 50 об/мин. Используемой средой растворения было 1000 мл 0,1 н. HCl. Таблетки достигали плавучести приблизительно через 10 минут. Результаты испытания на растворение показаны в приведенной ниже табл.2.
Пример 2
Удерживаемую в желудке систему регулируемой доставки лекарственного средства получали, как показано ниже на табл.3.
Сердцевину удерживаемой в желудке системы регулируемой доставки лекарственного средства получали пропусканием баклофена, маннита, гидроксиэтилцеллюлозы, натриевой соли гликолята и бикарбоната натрия через сито # 40 ASTM (American Society for Testing and Materials) и смешиванием ингредиентов с получением сухой порошкообразной смеси. Для гранулирования сухой порошкообразной смеси использовали водный раствор НРМС К4М. Таким образом полученные гранулы пропускали через подходящее сито и сушили. Сухие гранулы смазывали смесью Prosolv SMCC 90, талька и ПЭГ 8000 и прессовали для получения сердцевин. Сердцевины затем покрывали водно-спиртовым раствором смеси баклофена, НРМС Е5, талька, пропиленгликоля и диоксида титана с получением удерживаемой в желудке системы регулируемой доставки лекарственного средства настоящего изобретения.
Полученные таким образом таблетки подвергали испытанию на растворение при 37°С с использованием аппаратуры растворения United States Pharmacopoeia Type II (лопасти) при вращении 50 об/мин. Используемой средой растворения было 1000 мл 0,1 н. HCl. Таблетки достигали плавучести приблизительно через 6 минут. Результаты испытания на растворение показаны в приведенной ниже табл.4.
Пример 3
Удерживаемую в желудке систему регулируемой доставки лекарственного средства получали, как показано ниже на табл.5.
Часть баклофена, гидроксиэтилцеллюлозу, часть натриевой соли гликолята крахмала, часть микрокристаллической целлюлозы и часть поливинилпирролидона смешивали вместе, и гранулировали с изопропанолом, и смазывали тальком и стеаратом магния с образованием гранулята сердцевины. Оставшиеся части баклофена, микрокристаллической целлюлозы, поливинилпирролидона и натриевой соли гликолята крахмала смешивали вместе и гранулировали с водой с образованием гранулята покрытия. Гранулят покрытия прессовали и покрытие наносили на сердцевину с использованием способа покрытия прессованием. Таким образом полученная удерживаемая в желудке система регулируемой доставки лекарственного средства в форме покрытых таблеток проявляет высокую степень набухаемости за короткое время, имеет высокую прочность при манипулировании с ней, а также остается целой в водных жидкостях и способна обеспечивать двухфазный профиль регулируемого высвобождения.
Пример 4
Исследовали фармакокинетики баклофена после введения удерживаемой в желудке системы регулируемой доставки лекарственного средства, включающей 30 мг баклофена (пример 2). Для этого проводили многодозовое, однодозовое, рандомизированное, сравнительное и двуфакторное исследование с открытой меткой.
Фармакокинетическая оценка была основана на уровнях баклофена в плазме измеренных отбором проб крови. Образцы крови получали до введения дозы и в следующие периоды времени после введения испытуемого лекарственного средства - 0,25, 0,5, 1, 1,5, 2, 2,5, 3, 4, 6, 8, 12, 12,5, 13, 13,5, 14, 15, 16, 20 и 24 часа.
Двенадцать мужчин-волонтеров с хорошим здоровьем были зарегистрированы для исследования, и все они завершили исследование. Субъекты голодали на протяжении ночи, и перед дозированием им давали завтрак с высоким содержанием жира. Им было запрещено потреблять питьевую воду за два часа до дозирования и через два часа после этого, но давали ad lib в другое время. Стандартную пищу давали через 4 часа и 8 часов после дозирования и в определенное время после этого. Схемы питания были идентичными для обоих периодов.
Субъекты в течение пяти дней получали после голодания одну удерживаемую в желудке таблетку регулируемой доставки баклофена (30 мг) с 240 мл воды при температуре окружающей среды.
Концентрацию баклофена в плазме определяли для собранных образцов в различные точки времени и усредняли для всех двенадцати волонтеров. Данные показаны на приведенной ниже табл.6. Профиль зависимости концентрации баклофена в плазме от времени показан на чертеже.
Удерживаемая в желудке система регулируемой доставки лекарственного средства была подходящей для введения один раз в сутки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ МЕТФОРМИНА С ДЛИТЕЛЬНЫМ ВЫСВОБОЖДЕНИЕМ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2433821C2 |
| СПОСОБ ПРОГРАММИРУЕМОЙ ПЛАВУЧЕЙ ДОСТАВКИ | 2007 |
|
RU2420268C2 |
| ЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ГИПРОМЕЛЛОЗНЫЕ МАТРИЦЫ КОНТРОЛИРУЕМОГО ВЫСВОБОЖДЕНИЯ | 2006 |
|
RU2414241C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С НАБУХАЮЩИМ ПОКРЫТИЕМ | 2004 |
|
RU2375048C2 |
| ТАБЛЕТКА С КОНТРОЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ И СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ | 2011 |
|
RU2603469C2 |
| ПЕРОРАЛЬНАЯ КОМПОЗИЦИЯ ТЕДИСАМИЛА С ЗАМЕДЛЕННЫМ ВЫСВОБОЖДЕНИЕМ, ОБЛАДАЮЩАЯ СВОЙСТВОМ ЗАДЕРЖКИ В ЖЕЛУДКЕ | 2005 |
|
RU2385724C2 |
| ТВЕРДАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2002 |
|
RU2234915C2 |
| ТВЕРДЫЕ ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТИВНЫЕ ФОРМЫ С РЕГУЛИРУЕМЫМ ВЫСВОБОЖДЕНИЕМ НА ОСНОВЕ СУЛЬФОАЛКИЛОВЫХ ЭФИРОВ ЦИКЛОДЕКСТРИНА | 2000 |
|
RU2233176C9 |
| НОВЫЙ ПРЕПАРАТ | 2000 |
|
RU2240110C2 |
| МАТРИЧНАЯ ТАБЛЕТКА С МОДИФИЦИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ НЕРАМЕКСАНА | 2006 |
|
RU2422135C2 |
Настоящее изобретение относится к области лекарственных средств, в частности к удерживаемой в желудке таблетке регулируемой доставки лекарственного средства, содержащей: а) регулирующую высвобождение лекарственного средства сердцевину, содержащую лекарственное средство, хорошо набухаемый полимер, генерирующий газ агент, и b) композицию быстро высвобождающего покрытия, содержащую то же лекарственное средство, что и сердцевина, и фармацевтически приемлемые эксципиенты, где композиция покрытия окружает сердцевину, обеспечивая двухфазное высвобождение лекарственного средства в желудочно-кишечные жидкости. Кроме того, изобретение относится к таблетке для терапии 1 раз в день, включающей сердцевину, содержащую баклофен в форме регулируемого высвобождения, и покрытие, образующее композицию быстрого высвобождения, которая состоит из баклофена или его фармацевтически приемлемой соли и фармацевтически приемлемых наполнителей, и средство для удержания таблетки в желудке в течение длительных периодов. Технический результат заключается в удерживании в течение длительного периода указанных таблеток и обеспечении двухфазной доставки лекарственного средства регулируемым образом. 3 н. и 11 з.п. ф-лы, 1 ил., 6 табл.
а) регулирующую высвобождение лекарственного средства сердцевину, содержащую
i. лекарственное средство,
ii. хорошо набухаемый полимер, состоящий из смеси, по меньшей мере, двух из следующих полимеров:
хорошо набухаемые эфиры целлюлозы, выбранные из гидрокси С1-4 алкил С1-4 алкилцеллюлоз, карбоксиалкил целлюлоз, гидрокси С1-4 алкил целлюлоз;
смола растительного, животного, минерального или синтетического происхождения;
супердезинтегрантный полимер;
полимер акриловой кислоты;
полимер винил пирролидона, сополимеры винил пирролидона и винил ацетата или их смеси;
где, по меньшей мере, один из полимеров - это супердезинтегрантный полимер,
iii. генерирующий газ агент, выбранный из группы, содержащий карбонаты, бикарбонаты, сульфиты или метабисульфит натрия, где генерирующий газ агент дополнительно включает кислотный источник, выбранный из группы, состоящей из лимонной кислоты, яблочной кислоты, янтарной кислоты, винной кислоты, фумаровой кислоты, малеиновой кислоты, аскорбиновой кислоты, глутаминовой кислоты или их солей или их смесей,
где хорошо набухаемый полимер и генерирующие газ агенты присутствуют в количествах, достаточных для обеспечения характеристик набухаемости и плавучести для сердцевины, одновременно поддерживая ее физическую целостность и желудочно-кишечных жидкостях в течение длительных периодов времени, и
b) композицию быстро высвобождающего покрытия, содержащую то же лекарственное средство, что и сердцевина, и фармацевтически приемлемые эксципиенты, где композиция покрытия окружает сердцевину, обеспечивая двухфазное высвобождение лекарственного средства в желудочно-кишечной жидкости.
| WO 9947128 A1, 23.09.1999 | |||
| US 5096714 A, 17.05.1992 | |||
| US 4892739 A, 09.01.1990 | |||
| Метод сульфидирования никеля и кобальта в окисленных рудах | 1956 |
|
SU108670A1 |
| ДИФФУЗИОННО-ОСМОТИЧЕСКАЯ ФАРМАЦЕВТИЧЕСКАЯ СИСТЕМА С РЕГУЛИРУЕМЫМ ВЫДЕЛЕНИЕМ ЛЕКАРСТВА (ВАРИАНТЫ) И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ (ВАРИАНТЫ) | 1994 |
|
RU2133605C1 |
| Способ получения твердой лекарственной формы с регулируемым выделением лекарственного средства | 1988 |
|
SU1816213A3 |
Авторы
Даты
2008-05-27—Публикация
2002-07-04—Подача