Все приведенные в настоящем описании документы полностью включены в него в качестве ссылки.
Область техники
Данное изобретение относится к области получения везикул в целях иммунизации.
Предшествующий уровень техники
Одним из различных подходов к иммунизации против инфекции N.meningitidis является применение везикул наружной мембраны (OMV). Эффективная вакцина OMV против серологической группы В была изготовлена Норвежским национальным институтом общественного здравоохранения [см. ссылку 1], но, хотя указанная вакцина безопасна и предотвращает заболевание менингитом В, ее эффективность ограничена штаммом, используемым для изготовления вакцины.
Вакцина "RIVM" основана на содержащих везикулы шести различных подтипах PorA, и было показано, что она иммуногенна у детей на II фазе клинических испытаний [2].
В ссылке 3 раскрыта вакцина против различных патогенных серологических типов менингококка серологической группы В на основе OMV, которые сохраняют белковый комплекс 65 кДа. В ссылке 4 раскрыта вакцина, содержащая OMV из штаммов менингококков, полученных методами генной инженерии, причем OMV содержали по меньшей мере один белок наружной мембраны класса 1 (ОМР), но не содержали ОМР класса 2/3. В ссылке 5 раскрыты OMV, содержащие ОМР, которые имеют мутации в их поверхностных петлях, и OMV, включающие в себя производные менингококкового липополисахарида (LPS).
В ссылке 6 раскрыты композиции, включающие в себя OMV с добавками белков, связывающих трансферрин (например, TbpA и TbpB), и/или Cu,Zn-супероксиддисмутазы. В ссылке 7 раскрыты композиции, включающие в себя OMV с добавками различных белков. В ссылке 8 раскрыты препараты везикул мембраны, полученные из N.meningitidis модифицированным геном fur.
Так же как серологическая группа В N.meningitidis, везикулы были получены для других бактерий. В ссылке 9 раскрыт способ получения вакцин на основе OMV для менингококка серологической группы А. В ссылках 10 и 11 раскрыты везикулы из N.gonorrhoeae. В ссылке 12 раскрыты препараты из N.Lactamica. Везикулы также получали из Moraxella catarrhalis [13, 14], Shigella flexneri [15, 16], Pseudomonas aeruginosa [15, 16], Porphyromonas gingivalis [17], Treponema pallidum [18], Haemophilus influenzae [19 и 20] и Helicobacter pylori [21].
Один недостаток препаратов везикул бактерий состоит в том, что отсутствуют важные защитные антигены. Для сохранения антигенов, таких как NspA, в препаратах OMV, в ссылке 20 речь идет о том, что экспрессия nspA должна подвергаться стимулирующей регуляции сопутствующим «выбиванием» porA и cps. Целью изобретения является предоставление дополнительных и улучшенных препаратов везикул вместе со способами их изготовления. В частности, целью изобретения является предоставление везикул, которые сохраняют важные бактериальные иммуногенные компоненты из N.meningitidis.
Описание изобретения
Способы с применением препарата менингококковых OMV включают в себя использование детергента во время разрушения бактериальной мембраны [например, см. ссылку 22, где используется дезоксихолатный детергент]. Изобретение основано на удивительном открытии, что разрушение мембраны по существу в отсутствие детергента приводит к получению OMV, которые сохраняют важные бактериальные иммуногенные компоненты, в частности (i) защитный поверхностный белок NspA, (ii) белок '287' и (iii) белок '741'.
Поэтому изобретение предоставляет способ изготовления препарата везикул наружной мембраны из бактерии, где бактериальную мембрану разрушают по существу в отсутствие детергента. Предоставляются также препараты OMV, которые можно получить способами согласно изобретению.
Для получения везикул NspA+ve способ согласно изобретению гораздо проще, чем выполнение множественных генетических манипуляций, как описано в ссылке 20.
Способ согласно изобретению обычно должен включать в себя следующие основные этапы: (а) обработку бактериальных клеток по существу в отсутствие детергента; (b) центрифугирование композиции, полученной на этапе (а), для отделения везикул наружной мембраны от обработанных клеток и клеточного дебриса и сбор надосадочной жидкости; (с) выполнение высокоскоростного центрифугирования надосадочной жидкости, полученной на этапе (b), и сбор везикул наружной мембраны в осадке в пробирке после центрифугирования; (d) повторное диспергирование в пробирке полученного после центрифугирования осадка с этапа (с) в буфере; (е) выполнение второго высокоскоростного центрифугирования в соответствии с этапом (с), сбор везикул наружной мембраны в осадке, полученном в пробирке после центрифугирования, (f) повторное диспергирование осадка, полученного в пробирке после центрифугирования на этапе (е) в водной среде.
Способ может также включать в себя следующие этапы: (g) выполнение стерильной фильтрации по меньшей мере через 2 фильтра с уменьшающимся размером пор повторно диспергированной композиции, полученной на этапе (f); и (h) необязательно включение композиции, полученной на этапе (g), в фармацевтически приемлемый носитель и/или композицию адъюванта.
Этап (а) дает получение везикул наружной мембраны бактерий, и везикулы в целом включают в себя компоненты наружной мембраны по существу в их нативной форме. Преимущество заключается в сохранении компонентов NspA, '287' и '741'.
Этап (b) должен обычно включать в себя центрифугирование примерно при 5000-10000 g в течение до 1 ч.
Этапы (с) и (е) должны обычно включать центрифугирование примерно при 35000-100000 g в течение периода вплоть до 2 ч.
Этапы центрифугирования предпочтительно выполняются при температуре от 2 до 8°С.
Любой подходящий буфер можно использовать на этапе (d), например Трис-буфер, фосфатный буфер, гистидиновый буфер и т.д.
Этап (f) может также включать в себя использование буфера, который может представлять собой такой же буфер, который используется на этапе (d), или может просто включать в себя использование воды (например, воды для инъекций).
Этап (g) предпочтительно заканчивается фильтрованием через фильтр с размером пор примерно 0,2 мкм.
Изобретение также представляет собой композицию везикул N.meningitidis, отличающуюся тем, что везикулы содержат (i) белок NspA, (ii) белок '287' и (iii) белок '741'.
Бактерия
Бактерия, из которой получают OMV, может быть грамположительной, но она предпочтительно является грамотрицательной. Бактерия может быть из рода Moraxella, Shigella, Pseudomonas, Treponema, Porphyromonas или Helicobacter (предпочтительные виды см. выше), но предпочтительно она из рода Neisseria. Предпочтительными видами Neisseria являются N.meningitidis и N.gonorrhoeae. В пределах N.meningitidis можно использовать любую из серологических групп А, С, W135 и Y, но предпочтительно получать везикулы из серологической группы В. Предпочтительными штаммами в пределах серогруппы В являются МС58, 2996, Н4476 и 394/98.
Для снижения пирогенной активности предпочтительно, чтобы бактерия имела низкие уровни эндотоксина (LPS). Подходящие мутантные бактерии известны, например, мутантная Neisseria [23] и мутантная Helicobacter [24]. Способ получения наружных мембран с истощенными запасами LPS грамотрицательных бактерий раскрыты в ссылке 25.
Бактерия может представлять собой бактерию дикого типа или она может представлять собой рекомбинантную бактерию. Предпочтительные рекомбинантные бактерии избыточно экспрессируют (относительно соответствующего штамма дикого типа) иммуногены, такие как NspA, '287' и '741', TbpA, TbpB, супероксиддисмутаза [6] и т.д. Бактерия может экспрессировать более чем один белок наружной мембраны класса I PorA, например, 2, 3, 4, 5 или 6 подтипов PorA: Р1.7,16; Р1.5,2; Р1.19,15; Р1.5 с,10; Р1.12,13; и Р1.7h,4 [например, ссылки 26, 27].
Способ согласно изобретению обычно должен включать в себя начальный этап культивирования бактерий, необязательно с последующим этапом концентрирования культивированных клеток.
Разрушение мембраны
Разрушение мембраны для образования везикул выполняется по существу в отсутствие детергента.
В частности, разрушение мембраны может выполняться по существу в отсутствие дезоксихолатного детергента, причем присутствие других детергентов необязательно.
Разрушение мембраны может выполняться по существу в отсутствие ионного детергента, причем присутствие неионного детергента необязательно. Альтернативно, оно может выполняться по существу в отсутствие неионного детергента, причем присутствие ионного детергента необязательно. В некоторых вариантах реализации не присутствует ни ионный, ни неионный детергент.
Этапы после разрушения мембраны и образования везикул могут включать в себя использование детергента. Таким образом, способ, при котором разрушение мембраны происходит в отсутствие детергента, но детергент добавляется к полученным везикулам позднее, входит в объем данного изобретения.
Термин «по существу в отсутствие» означает, что рассматриваемый детергент присутствует в концентрации не более чем 0,05% (например, ≤0,025%, ≤0,015%, ≤0,010%, ≤0,005%, ≤0,002%, ≤0,001% или даже 0%) во время разрушения мембраны. Таким образом, способы, где микроколичества детергента присутствуют во время получения везикул, не исключаются.
Разрушение мембраны в отсутствие детергента может выполняться на интактных бактериях с использованием физических методик, например, обработки ультразвуком, гомогенизации, микрофлюидизации, кавитации, осмотического шока, помола, французского пресса, перемешивания и т.д.
Везикулы
Способы согласно изобретению продуцируют везикулы наружной мембраны. OMV получают из наружной мембраны культивированных бактерий. Их можно получить из бактерий, выращенных в бульоне или в твердой культуральной среде, предпочтительно путем отделения бактериальных клеток от культуральной среды (например, путем фильтрации или высокоскоростного центрифугирования для осаждения клеток), лизирования клеток (без детергента) и отделения фракции наружной мембраны от цитоплазматических молекул (например, путем фильтрации, дифференциального осаждения или агрегации наружных мембран и/или OMV, способами аффинного разделения с использованием лигандов, которые специфически распознают молекулы наружной мембраны, или высокоскоростного центрифугирования, которое осаждает наружные мембраны и/или OMV.
OMV можно отличить от микровезикул (MV [28]) и нативных OMV ('NOMV' [66]), которые представляют собой естественно встречающиеся везикулы мембраны, которые спонтанно образуются во время роста бактерий, и которые высвобождаются в культуральную среду. MV можно получить путем культивирования Neisseria в бульонной культуральной среде путем отделения цельных клеток от бульонной культуральной среды (например, путем фильтрации или низкоскоростного центрифугирования для осаждения только клеток, а не более мелких везикул), а затем сбора MV, которые присутствуют в среде, лишенной клеток (например, путем фильтрации, дифференциального осаждения или агрегации MV, высокоскоростного центрифугирования для осаждения MV). Штаммы для использования при продукции MV можно в целом отобрать на основании количества MV, продуцированного в культуре. В ссылках 29 и 30 описаны Neisseria с высокой продукцией MV.
Сохраненные бактериальные иммуногенные компоненты
По существу отсутствующий детергент в способах согласно изобретению приводит к получению препаратов везикул, которые сохраняют иммуногенные компоненты бактериальной поверхности, которые при использовании основанных на детергентах способов предшествующего уровня техники иначе были бы утрачены или содержание которых уменьшилось бы. В N.meningitidis 3 иммуногена, которые преимущественно сохраняются при применении изобретения, включают в себя, не ограничиваясь ими: (1) NspA; (2) белок '741' и (3) белок '287'.
NspA (белок А поверхности Neisseria) раскрыт в ссылках 31-37 и в виде последовательностей SEQ ID 4008-4033 из ссылки 38. Это перспективная вакцина для предотвращения заболевания, вызванного менингококками. Она очень сохранна у различных штаммов. Однако несмотря на существовавшую надежду, в настоящее время считается, что NspA сам по себе не будет адекватным защитным антигеном, и его нужно будет вводить с дополнительными антигенами [например, ссылка 36 и пример 11 из ссылки 38]. Было обнаружено, что NspA удалялся при использовании способов получения предшествующего уровня техники на основе детергента. Однако в соответствии с настоящим изобретением, NspA может сохраняться в везикулах. Такие везикулы NspA+ve имеют преимущество, потому что комбинацию двух известных активных иммуноглобулинов (т.е. везикул + NspA) получают в одном способе при усилении каждым иммуногеном эффективности другого.
Белок '741' раскрыт в виде 'NMB1870' в ссылке 39 (GenBank: AAF2204, GI:7227128). Он также раскрыт в ссылках 40 и 41. Он вызывает продукцию сильных бактерицидных антител. Было обнаружено, что белок '741' частично удаляется в носителях, полученных способами на основе детергентов предшествующего уровня техники. Однако в соответствии с настоящим изобретением, '741' может сохраняться в везикулах. Такие везикулы NspA+ve имеют преимущество, потому что комбинацию двух известных активных иммуноглобулинов (т.е. везикул+741) получают в едином процессе, при усилении каждым иммуногеном эффективности другого.
Белок '287' раскрыт под видом 'NMB2132' в ссылке 39 (GenBank: AAF2240, GI:7227388). Он также раскрыт в ссылках 40 и 42. Он вызывает продукцию сильных бактерицидных антител. Белок '287' обычно не присутствует в везикулах, полученных способами на основе детергентов предшествующего уровня техники, и ранее предлагалось, что для предотвращения его удаления к препаратам OMV можно добавлять 287 [43]. Однако в соответствии с настоящим изобретением, '287' может сохраняться в везикулах. Такие везикулы 287+ve имеют преимущество, потому что комбинацию двух известных активных иммуноглобулинов (т.е. везикул + 287) получают в едином процессе, при усилении каждым иммуногеном эффективности другого.
Предпочтительный NspA (а) имеет по меньшей мере идентичность последовательности α% с аминокислотной последовательностью GI:1518522 и/или (b) включает в себя фрагмент по меньшей мере χ аминокислот из аминокислотной последовательности GI:1518522. Предпочтительный '741' (а) имеет по меньшей мере идентичность последовательности b% с аминокислотной последовательностью GI:7227128 и/или (b) включает в себя фрагмент по меньшей мере из χ аминокислот из аминокислотной последовательности GI:7227128. Предпочтительный '287' (а) имеет по меньшей мере идентичность последовательности с% с аминокислотной последовательностью GI:7227388 и/или (b) включает в себя фрагмент по меньшей мере из χ аминокислот из аминокислотной последовательности GI:7227388. Величины а, b и с независимы друг от друга, но каждая величина составляет по меньшей мере 70 (например, 75, 80, 85, 90, 95, 96, 97, 98, 99, 99,5 или 100). Величины x, y и z независимы друг от друга, но каждая величина составляет, по меньшей мере, 8 (например, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250 и т.д.). Фрагменты предпочтительно включают в себя эпитопы.
Предпочтительные белки NspA, 287 и 741 по существу сохраняют способность белков дикого типа (как обнаружено в интактных бактериях) вызывать продукцию бактерицидных антител у пациентов.
Иммуногенные фармацевтические композиции
Способ согласно изобретению обеспечивает получение везикул. Для введения пациенту везикулы предпочтительно составлены в виде иммуногенных композиций, а предпочтительнее, в виде композиций, подходящих для использования в качестве вакцины для человека (например, детей или взрослых). Вакцины согласно изобретению могут быть или профилактическими (т.е. для предотвращения инфекции), или терапевтическими (т.е. для лечения заболевания после инфекции), но обычно профилактическими.
Композиция согласно изобретению является предпочтительно стерильной.
Композиция согласно изобретению является предпочтительно лишенной пирогенов.
Композиция согласно изобретению в целом имеет рН от 6,0 до 7,0, предпочтительнее, от 6,3 до 6,9, например, 6,6±0,2. Композиция предпочтительно забуферена при данном рН.
Другие компоненты, подходящие для введения человеку, раскрыты в ссылке 44.
Композиция должна в целом включать в себя адъювант. Предпочтительные адъюванты для усиления эффективности композиции включают в себя, не ограничиваясь ими, (А) MF59 (5% Squalene, 0,5% Tween 80 и 0,5% Span 85, составленные в субмикронные частицы с использованием микрофлюидизаторов) [см. главу 10 ссылки 45; см. также ссылку 46]; (В) микрочастицы (т.е. частицы диаметром от ˜100 нм до ˜150 мкм, предпочтительнее, диаметром от ˜200 нм до ˜30 мкм, а наиболее предпочтительно, диаметром от ˜500 нм до ˜10 мкм), образованные из материалов, которые являются биологически разлагаемыми и нетоксичными (например, поли(α-гидроксикислоту), полигидроксимасляную кислоту, сложный полиортоэфир, полиангидрид, поликапролактон и т.д.), причем предпочтительнее поли(лактид-когликолид), необязательно имеющий заряженную поверхность (например, путем добавления катионного, анионного или неионного детергента, такого как SDS (отрицательного) или СТАВ (положительного) [например, ссылки 47 и 48]); [см. главу 23 ссылки 45], (С) липосомы [см. главы 13 и 14 ссылки 45]; (D) ISCOM [см. главу 23 ссылки 45], которые могут быть лишены дополнительного детергента [49]; (E) SAF, содержащий 10% Squalane, 0,4% Tween 80, 5% плюроник-блок-полимер L121 и thr-MDP, или микрофлюидизированный в субмикронную эмульсию, или перемешанный в вихревой мешалке для создания эмульсии с частицами большего размера [см. главу 12 ссылки 45]; (F) систему адъюванта Ribi™ (RAS), (Ribi Immunochem), содержащую 2% Squalane, 0,2% Tween 80, и один или несколько компонентов стенок бактериальных клеток из группы, состоящей из монофосфориллипида А (MPL), димиколата трегалозы (TDM) и каркаса клеточной стенки (CWS), предпочтительно, MPL+CWS (Detox™); (G) адъюванты сапонина, такие как QuilA или QS21 [см. главу 22 ссылки 45], также известные как Stimulon™; (H) хитозан [например, 50]; (I) полный адъювант Фрейнда (CFA) и неполный адъювант Фрейнда (IFA); (J) цитокины, такие как интерлейкины (например, IL-1, IL-2, IL-4, IL-5, IL-6, IL-7, IL-12 и т.д.), интерфероны (например, интерферон-γ), колониестимулирующий фактор макрофагов, фактор некроза опухоли и т.д. [см. главы 27 и 28 ссылки 45]; (K) сапонин (например, QS21)+3dMPL+IL-12 (необязательно + стерин) [51]; (L) монофосфориллипид А (MPL) или 3-О-дезацилированный MPL (3dMPL) [например, глава 21 ссылки 45]; (М) комбинации 3dMPL, например, с QS21 и/или эмульсиями масло-в-воде [52]; (N) олигонуклеотиды, содержащие мотивы CpG [53], т.е. содержащие по меньшей мере один динуклеотид CG, с 5-метилцитозином, необязательно используемым вместо цитозина; (О) простой полиоксиэтиленовый эфир или сложный полиоксиэтиленовый эфир [54]; (P) поверхностно-активный сложный полиоксиэтиленовый эфир сорбитана в комбинации с октоксинолом [55] или поверхностно-активный простой или сложный полиоксиэтиленалкиловый эфир в комбинации по меньшей мере с одним дополнительным неионным поверхностно-активным веществом, таким как октоксинол [56]; (Q) иммуностимулирующий олигонуклеотид (например, олигонуклеотид CpG) и сапонин [57]; (R) иммуностимулятор и частицу соли металла [58]; (S) сапонин и эмульсию масло-в-воде [59]; (T) термолабильный энтеротоксин E.coli ("LT") или его детоксифицированные мутанты, такие как мутанты К63 или R72 [например, глава 5 ссылки 60]; (U) холерный токсин («СТ») или его детоксифицированные мутанты [например, глава 5 ссылки 60]; (V) двунитевую РНК; (W) соли алюминия, такие как гидроокиси алюминия (включая оксигидроокиси), фосфаты алюминия (включая гидроксифосфаты), сульфат алюминия и т.д. [главы 8 и 9 в ссылке 61]; (X) имитаторы монофосфорилового липида А, такие как производные фосфата аминоалкилглюкозаминида, например, RC-529 [62]; (Y) полифосфазен (РСРР); или (Z) биоадгезивное вещество [63], такое как микросферы эстерифицированной гиалуроновой кислоты [64], или мукоадгезивное вещество, выбранное из группы, состоящей из поперечно сшитых производных поли(акриловой кислоты), поливинилового спирта, поливинилпирролидона, полисахаридов и карбоксиметилцеллюлозы. Можно также использовать другие вещества, которые действуют в качестве иммуностимулирующих средств для усиления эффективности композиции [например, см. главу 7 ссылки 45]. Соли алюминия (особенно фосфаты и/или гидроокиси алюминия) представляют собой предпочтительные адъюванты для парентеральной иммунизации. Мутантные токсины представляют собой адъюванты слизистой мембраны.
Везикулы в композициях согласно изобретению должны присутствовать в «иммунологически эффективных количествах», т.е. введение такого количества индивиду либо в однократной дозе, либо в виде части серии введений эффективно для лечения или предотвращения заболевания. Данное количество варьируется, в зависимости от здоровья и физического состояния индивида, которого предстоит лечить, возраста, таксономической группы индивида, которого предстоит лечить (например, нечеловекообразного примата, примата и т.д.), способности иммунной системы индивида синтезировать антитела, степени необходимой защиты, состава вакцины, оценки медицинской ситуации лечащим врачом, а также других релевантных факторов. Ожидается, что это количество подпадет под относительно широкий диапазон, который можно определить посредством стандартных испытаний. Дозировка лечения может представлять собой схему с однократной дозой или схему с множеством доз (например, включая бустерные дозы). Вакцину можно вводить в сочетании с другими иммунорегуляторными средствами.
Обычно композиции согласно изобретению получают в виде препаратов для инъекций. Прямая доставка композиций обычно осуществляется парентеральной (например, путем инъекции, либо подкожно, внутрибрюшинно, внутривенно, либо внутримышечно, либо путем доставки в интерстициальное пространство ткани), либо через слизистую оболочку (например, перорально или интраназально [65, 66]). Композиции можно также вводить в очаг поражения.
После составления композиции согласно изобретению можно вводить непосредственно индивиду. Индивиды, подлежащие лечению, могут представлять собой животных; в частности, можно лечить человека. Вакцины особенно полезны для вакцинации детей и подростков.
Композиция может включать в себя везикулы из нескольких серологических подтипов N.meningitidis [28]. Аналогичным образом, композиция может включать в себя несколько типов везикул, например как MV, так и OMV.
Так же как везикулы, композиция согласно изобретению может включать в себя другие антигены. Например, композиция может включать в себя один или несколько из следующих дополнительных антигенов:
- антигены из Helicobacter pylori, такие как CagA [67-70], VacA [71, 72], NAP [73, 74, 75], HopX [например, 76], HopY [например, 76] и/или уреаза;
- сахаридный антиген из N.meningitidis серогруппы А, С, W135 и/или Y, такой как олигосахарид, раскрытый в ссылке 77, из серогруппы С [см. также ссылку 78], или олигосахариды ссылки 79;
- сахаридный антиген из Streptococcus pneumoniae [например, 80, 81, 82];
- антиген из вируса гепаптита А, такой как инактивированный вирус [например, 83, 84];
- антиген из вируса гепаптита В, такой как поверхностные и/или сердцевинные антигены [например, 84, 85];
- антиген из Bordetella pertussis, такой как коклюшный голотоксин (РТ) и нитевидный гемагглютинин (FHA) из B.pertussis, необязательно также в комбинации с пертактином и/или агглютиногенами 2 и 3 [например, ссылки 86 и 87];
- дифтерийный антиген, такой как дифтерийный токсоид [например, глава 3 ссылки 88], например, мутант CRM197 [например, 89];
- столбнячный антиген, такой как столбнячный токсоид [например, глава 4 ссылки 108];
- сахаридный антиген из Haemophilus influenzae B [например, 78];
- антиген из вируса гепатита С [например, 90];
- антиген из N.gonorrhoeae [например, 91, 92, 93, 94];
- антиген из Chlamydia pneumoniae [например, ссылки 95-101];
- антиген из Chlamydia trachomatis [например, 102];
- антиген из Porphyromonas gingivalis [например, 103];
- антиген(ы) полиомиелита [например, 104, 105], такой как OPV, или, предпочтительно, IPV;
- антиген(ы) бешенства [например, 106], такой как лиофилизированный инактивированный вирус [например, 107, RabAvert™];
- антигены вирусов кори, эпидемического паротита и/или краснухи [например, главы 9, 10 и 11 ссылки 108];
- антиген(ы) вируса гриппа [например, глава 19 ссылки 108], такие как гемагглютинин и/или поверхностные белки нейраминидазы;
- антиген из Moraxella catarrhalis [например, 109];
- белковый антиген из Streptococcus agalactiae (стрептококк группы В) [например, 110, 111];
- сахаридный антиген из Streptococcus agalactiae (стрептококк группы В);
- антиген из Streptococcus pyrogenes (стрептококк группы А) [например, 111, 112, 113];
- антиген из Streptococcus aureus [например, 114];
- антиген из Bacillus anthracis [например, 115, 116, 117];
- антиген из вируса из семейства Flaviviridae (род Flavivirus), такого как вирус желтой лихорадки, вирус японского энцефалита, 4 серотипа вируса денге, вируса клещевого энцефалита, вируса западного Нила;
- антиген пестивируса, такого как классический вирус свиной лихорадки, вирус коровьей вирусной диареи и/или вирус пограничного заболевания;
- антиген парвовируса, например, из парвовируса В19;
- белок приона (например, белок приона CJD);
- амилоидный белок, такой как пептид бета [118];
- раковый антиген, такой как антигены, перечисленные в табл.1 ссылки 119, или в табл.3 и 4, ссылки 120.
Композиция может включать в себя один или несколько из указанных дополнительных антигенов.
Токсические белковые антигены можно при необходимости детоксифицировать (например, дектоксификация коклюшного токсина химическими и/или генетическими средствами [87]).
Когда дифтерийный антиген включается в композицию, предпочтительно также включить столбнячный антиген и коклюшный антиген. Аналогичным образом, когда включен столбнячный антиген, предпочтительно также включить дифтерийный и коклюшный антигены. Аналогичным образом, когда включен коклюшный антиген, предпочтительно также включить дифтерийный и столбнячный антигены. Таким образом, предпочтительны комбинации DTP (дифтерийного, столбнячного и коклюшного антигенов).
Сахаридные антигены представлены предпочтительно в форме конъюгатов. Белки-носители для конъюгатов включают в себя белок наружной мембраны N.meningitidis [121], синтетические пептиды [122, 123], белки теплового шока [124, 125], белки коклюшного возбудителя [126, 127], белок D из H.influenzae [128], цитокины [129], лимфокины [129], гормоны [129], ростовые факторы [129], токсин А и В из C.difficile [130], захватывающие железо белки [131] и т.д. Предпочтительным белком-носителем является дифтерийный токсоид CRM197 [132].
Антигены серогруппы В N.meningitidis можно также добавлять к композициям OMV. В частности, можно добавить белковый антиген, такой как антиген, раскрытый в ссылках 133-139.
Антигены в композиции должны обычно присутствовать в концентрации по меньшей мере 1 мкг/мл каждый. В целом концентрация любого данного антигена должна быть достаточной для того, чтобы вызвать иммунную реакцию против указанного антигена.
В качестве альтернативы использованию белковых антигенов, в композиции согласно изобретению можно использовать нуклеиновую кислоту, кодирующую антиген. Таким образом, белковые компоненты композиций согласно изобретению можно заменить нуклеиновой кислотой (предпочтительно, ДНК, например, в форме плазмиды), которая кодирует белок.
Способы лечения пациентов
Изобретение обеспечивает везикулы согласно изобретению для применения в качестве лекарственных средств.
Изобретение также обеспечивает способ усиления иммунного ответа у пациента, включающий в себя введение пациенту композиции согласно изобретению. Иммунный ответ предпочтительно защищает против менингококкового заболевания и может включать в себя гуморальный иммунный ответ и/или клеточный иммунный ответ. Пациентом предпочтительно является ребенок.
Способ может повысить вторичный иммунный ответ у пациента, который уже был подвергнут первичной иммунизации против N.meningitidis. Схемы подкожной и интраназальной первичной/вторичной иммунизации для OMV раскрыты в ссылке 65.
Изобретение также предполагает применение везикул согласно изобретению при изготовлении лекарственного средства для усиления иммунного ответа у пациента. Лекарственное средство представляет собой предпочтительно иммуногенную композицию (например, вакцину). Лекарственное средство предпочтительно предназначено для предотвращения и/или лечения заболевания, вызванного Neisseria (например, вызывающими менингит, септицемию, гонорею и т.д.).
Способы и виды применения изобретения могут включать в себя введение везикул из нескольких серологических подтипов N.meningitidis [например, ссылка 28].
Композиция OMV
Изобретение обеспечивает композицию, содержащую везикулы наружной мембраны менингококков, адъювант гидроокиси алюминия, гистидиновый буфер и хлорид натрия, где (а) концентрация хлорида натрия больше чем 7,5 мг/мл; и/или (b) концентрация OMV составляет менее чем 100 мкг/мл.
Концентрация хлорида натрия составляет предпочтительно больше чем 8 мг/мл, а предпочтительнее, примерно 9 мг/мл.
Концентрация OMV составляет предпочтительно менее чем 75 мкг/мл, например, примерно 50 мкг/мл.
Гистидиновый буфер обеспечивает предпочтительно диапазон от рН 6,3 до рН 6,7, например, рН 6,5.
Адъювант можно использовать в концентрации примерно 3,3 мг/мл (выраженной в виде концентрации Al3+).
Определения
Ссылки на степень идентичности (в процентах) последовательностей между двумя аминокислотными последовательностями означают, что при выравнивании процентное содержание аминокислот одинаково при сравнении двух последовательностей. Указанное выравнивание и процентную гомологию или идентичность последовательностей можно определить с использованием пакетов программного обеспечения, известных в данной области, например тех, которые описаны в разделе 7.7.18 ссылки 140. Предпочтительный ряд определяется алгоритмом поиска гомологии Смита-Уотермана с использованием поиска аффинного гэпа со штрафом за «открытый гэп», составляющим 12, и штрафом за «протяженность гэпа», составляющим 2, матрицы BLOSUM из 62. Алгоритм поиска гомологии Смита-Уотермана хорошо известен и раскрыт в ссылке 141.
Термин «охватывающий» означает «включающий в себя», а также «состоящий», например композиция, «включающая в себя» Х, может либо состоять исключительно из Х, либо может включать в себя что-то дополнительное, например X+Y.
Термин «примерно» в отношении числовой величины χ означает, например, χ±10%.
Слово «по существу» не исключает «полностью», например, композиция, которая «по существу свободна» от Y, может быть полностью свободна от Y. При необходимости, слово «по существу» может быть опущено из определения изобретения.
Краткое описание чертежей
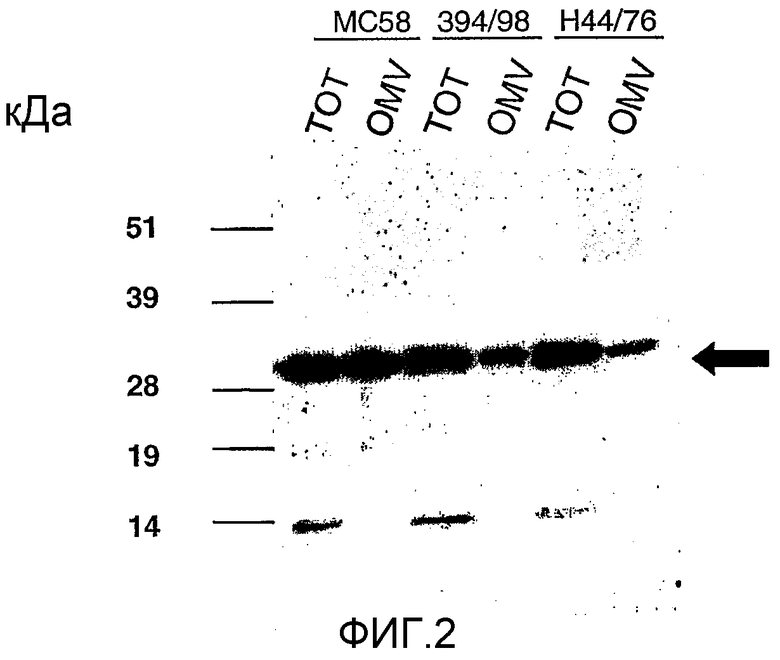
На Фиг.1 и 2 показано присутствие/отсутствие (1) белка '287' и (2) белка '741' в бактерии («ТОТ») и везикулах наружной мембраны ("OMV"), полученных из штаммов МС58, Н4476 и 394/98 N.meningitidis. Стрелка показывает положение '287' на фиг.1 и '741' на фиг.2.
На фиг.3 показаны аминокислотные последовательности, занесенные в банк генов GenBank GI:7227128, GI:7227388 и GI:1518522 от 29 августа 2002 г.
Способы осуществления изобретения
Получение OVM
OMV получали или «норвежскими» способами предшествующего уровня техники (штаммы Н4476 и 394/98), или следующим способом (штамм МС58):
- Бактерии из 2-5 чашек собирают в 10 мл буфера 10 мМ Трис-HCl (рН 8,0) и убивают нагреванием при 56°С в течение 45 мин. Образцы затем обрабатывают ультразвуком на льду (рабочий цикл 50 в течение 10 мин наконечником на 6/7) для разрушения мембран.
- Клеточный дебрис удаляют центрифугированием при 5000 g в течение 30 мин при 4°С или 10000 g в течение 10 мин.
- Надосадочную жидкость повторно центрифугируют при 50000 g в течение 75 мин при 4°С.
- Осадок в пробирке после центрифугирования повторно суспендируют в 7 мл 2% N-лауроилсаркозината (саркозил) в 10 мл 10 мМ Трис-HCl (рН 8,0) в течение 20 мин при комнатной температуре для солюбилизации цитоплазматических мембран.
- Образец центрифугируют при 10000 g в течение 10 мин для удаления материалов в виде частиц, а надосадочную жидкость центрифугируют при 75000 g в течение 75 мин при 4°С. Образец промывают в 10 мМ Трис-HCl (рН 8,0) и центрифугируют при 75000 g в течение 75 мин.
- Осадок в пробирке после центрифугирования повторно суспендируют в 10 мМ Трис-HCl (рН 8,0) или дистиллированной воде.
Бактерии и препараты OVM тестировали методом вестерн-блоттинга на присутствие NspA, 287 и 741 (фиг.1 и 2); полученные результаты сведены в следующую таблицу:
В отличие от способов предшествующего уровня техники на основе детергентов, отсутствие детергента приводит к сохранению NspA и позволяет избежать потери 287 и 741.
Составление композиции OVM, полученных из новозеландского штамма MenB
OVM получают из штамма 394/98 серогруппы В N.meningitidis. Их включали в композиции двумя различными путями, причем компоненты имеют следующие концентрации:
Было обнаружено, что композиция «В» в иммунологическом отношении лучше композиции «А». Композиция «В» отличается от композиции, раскрытой в ссылке 142, тем, что в ней содержится половина концентрации OMV, выше концентрации NaCl, и она несколько отличается значением рН.
Следует понимать, что изобретение было описано только в качестве примера, и модификации могут производиться в пределах объема и сущности изобретения.







| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ МЕНИНГОКОККОВЫХ ВАКЦИН С АДЪЮВАНТАМИ | 2002 |
|
RU2360699C2 |
| УСОВЕРШЕНСТВОВАНИЯ, КАСАЮЩИЕСЯ ВЕЗИКУЛ ВНЕШНЕЙ МЕМБРАНЫ МЕНИНГОКОККОВ | 2005 |
|
RU2420312C2 |
| НАБОР ДЛЯ ПОЛУЧЕНИЯ ИММУНОГЕННОЙ КОМПОЗИЦИИ ПРОТИВ Neisseria meningitidis СЕРОЛОГИЧЕСКОЙ ГРУППЫ В | 2008 |
|
RU2498815C2 |
| ЖИДКИЕ ВАКЦИНЫ ДЛЯ МНОЖЕСТВЕННЫХ СЕРОГРУПП МЕНИНГОКОККОВ | 2004 |
|
RU2378010C2 |
| МЕНИНГОКОККОВЫЕ ПОЛИПЕПТИДЫ fHBP | 2009 |
|
RU2475496C2 |
| ВАКЦИНЫ, СОДЕРЖАЩИЕ АЛЮМИНИЕВЫЕ АДЪЮВАНТЫ И ГИСТИДИН | 2007 |
|
RU2432173C2 |
| ЖИДКИЕ ВАКЦИНЫ ДЛЯ МНОЖЕСТВЕННЫХ СЕРОГРУПП МЕНИНГОКОККОВ | 2009 |
|
RU2595845C2 |
| ПОЛИПЕПТИДНЫЕ ВАКЦИНЫ ДЛЯ ШИРОКОЙ ЗАЩИТЫ ПРОТИВ РЯДОВ ПОКОЛЕНИЙ МЕНИНГОКОККОВ С ПОВЫШЕННОЙ ВИРУЛЕНТНОСТЬЮ | 2003 |
|
RU2333007C2 |
| ВЕЗИКУЛЫ НАРУЖНОЙ МЕМБРАНЫ | 2013 |
|
RU2662970C2 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТРАНСФЕРРИН-СВЯЗЫВАЮЩИЙ БЕЛОК И HSF ИЗ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ | 2003 |
|
RU2359696C2 |

Данное изобретение относится к медицине и фармакологии и может быть использовано для изготовления лекарственного средства для усиления иммунного ответа у пациентов. Настоящий способ получения препарата везикул наружной мембраны из бактерий рода Neisseria предусматривает разрушение оболочки бактерий и сбор везикул наружной мембраны в присутствии ≤0,05% дезоксихолатного детергента, причем бактерии в избыточном количестве экспрессируют TbpA. Изобретение позволяет сохранить важные бактериальные иммуногенные компоненты, в частности (i) защитный поверхностный белок NspA, (ii) белок '287' и (iii) белок '741'. 4 н. и 13 з.п. ф-лы, 2 табл., 3 ил.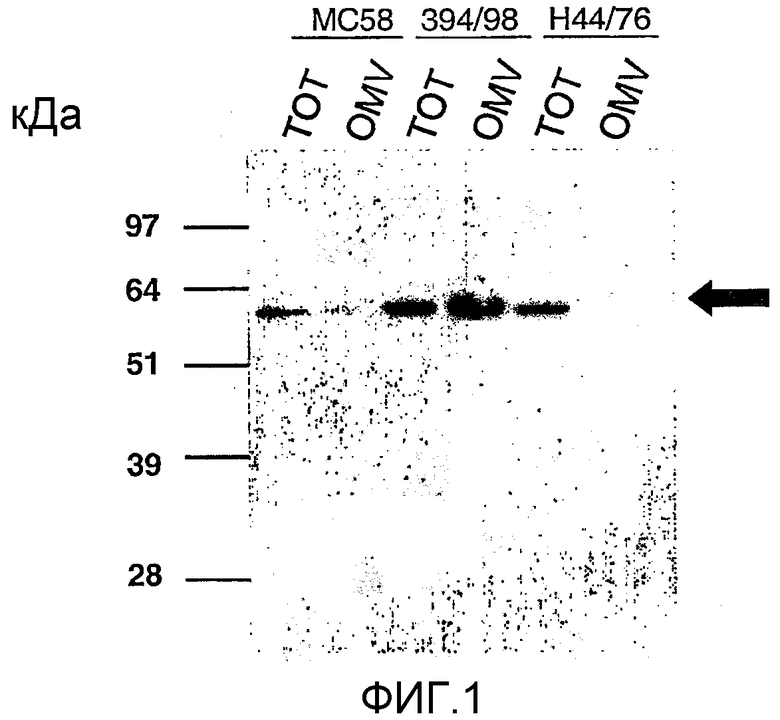
| WO 02062378 А2, 15.08.2002 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЭЛЕКТРОНООБМЕННОИ СМОЛЫ СУЛЬФОГИДРИЛЬНОГО ТИПА | 0 |
|
SU191788A1 |
| US 2002110569 A1, 15.08.2002 | |||
| WO 9957280 A1, 11.11.1999 | |||
| ФРАГМЕНТ ДНК, КОДИРУЮЩИЙ БЕЛОК ВНЕШНЕЙ МЕМБРАНЫ NEISSERIA MENINGITIDIS ШТАММА В:4:Р1:15, БЕЛОК ВНЕШНЕЙ МЕМБРАНЫ NEISSERIA MENINGITIDIS, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pМ-6, ШТАММ БАКТЕРИЙ ESCHERICHIA COLI НВМ 64, СПОСОБ ПОЛУЧЕНИЯ БЕЛКА ВНЕШНЕЙ МЕМБРАНЫ NEISSERIA MENINGITIDIS, ВАКЦИННАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2132383C1 |
Авторы
Даты
2008-05-27—Публикация
2003-09-01—Подача