Предпосылки изобретения
Настоящее изобретение относится к способам получения 5-[[2(R)-[1(R)-[3,5-бис(трифторметил)фенил]этокси]-3(S)-(4-фторфенил)-4-морфолинил]метил]-1,2-дигидро-3Н-1,2,4-триазол-3-она, апрепитанта,
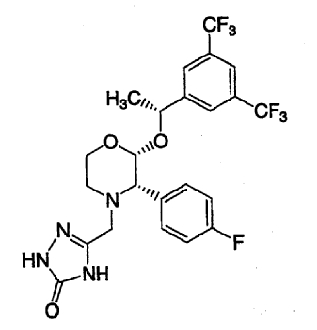
который является полезным терапевтическим агентом, особенно как антагонист рецептора вещества Р (нейрокинина-1). Это соединение раскрыто как обладающее применимостью в области терапии в патенте США № 5719147.
Патенты США №№ 5637699, 6096742, 6229010 и 6297376 относятся к способам получения и раскрытию полиморфных форм этого соединения. В отличие от ранее известных способов, настоящее изобретение относится к более практическому и экономичному способу получения соединения с относительно высоким выходом и чистотой. Как таковая, существует потребность в способе получения соединения, который был бы рентабельным и предусматривал использование легкодоступных реагентов.
Краткое изложение сущности изобретения
Настоящее изобретение относится к способу получения соединения формулы 1:
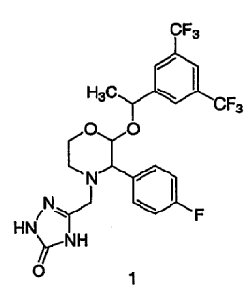
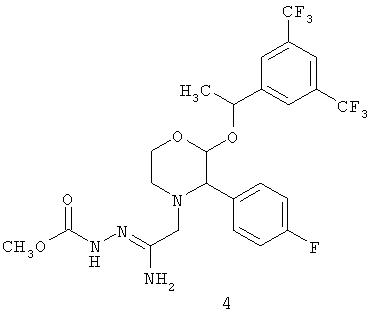
включающему циклизацию соединения формулы 4:
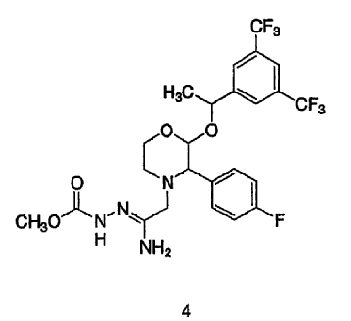
при температуре 140-150°С с образованием соединения формулы 1.
В частности, такие соединения представляют собой антагонисты рецептора вещества Р (нейрокинина-1), которые пригодны, например, при лечении психиатрических заболеваний, воспалительных заболеваний и рвоты.
Подробное описание изобретения
Настоящее изобретение относится к способу получения соединения формулы 1:
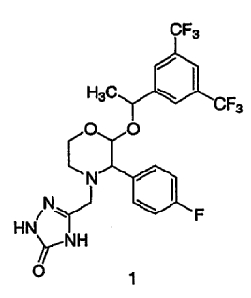
Способ включает
циклизацию соединения формулы 4:
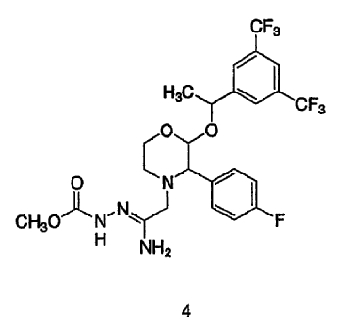
при температуре 140-150°С с образованием соединения формулы 1.
В частности, настоящее изобретение относится к способу получения соединения формулы 1:

Способ включает:
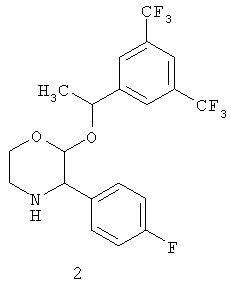
(а) взаимодействие гидрохлорида соединения формулы 2:
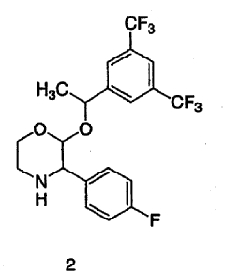
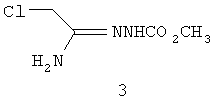
в присутствии неорганического основания и толуола с соединением формулы 3:
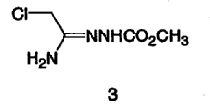
с образованием соединения формулы 4:

(b) промывание водной фазой, и
(c) циклизацию при температуре 140-150°С с образованием соединения формулы 1.
В частности, раскрывается способ получения соединения формулы 1а:
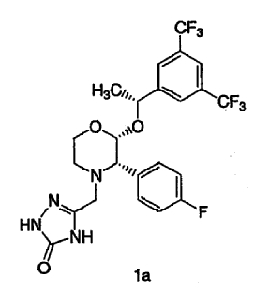
включающий взаимодействие гидрохлорида соединения формулы 2а:

в присутствии неорганического основания и толуола с соединением формулы 3:

с образованием соединения формулы 4а:
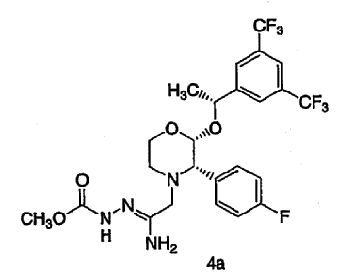
(b) промывание водной фазой, и
(с) циклизацию при температуре 140-150°С с образованием соединения формулы 1а.
Описанная в данном описании стадия промывания обычно предусматривает использование водной фазы, например воды, и может необязательно содержать соль. Представительные примеры солей, которые являются полезными, включают KCl, KHCO3, K2CO3, Na2CO3, NaHCO3, NaCl и аналогичные соли. KCl является предпочтительной солью.
В другом аспекте настоящего изобретения способ дополнительно включает стадию сушки перед циклизацией.
Использованный в настоящем описании термин «неорганическое основание» относится к соединениям, таким как карбонат натрия, карбонат цезия, гидроксид натрия, гидроксид калия, карбонат калия и т.п. В частности, предпочтительным неорганическим основанием является карбонат калия.
В частности, настоящее изобретение относится к способу, описанному выше, в котором соединение 2 или 2а взаимодействует с соединением 3 в присутствии неорганического основания, толуола и полярного апротонного растворителя. Использованный в настоящем описании термин «полярный апротонный растворитель» относится к растворителю, который ни отдает, ни принимает протоны и выбран, например, из группы, состоящей из: диметилформамид (ДМФ), диметилсульфоксид (ДМСО), N-метилпирролидон (NМП), ацетонитрил (МеСН), N,N-диметилацетамид (ДМАЦ) и гексаметилфосфорамид (ГМФА).
Способ, описанный в настоящем описании, неожиданно оказался эффективным, характеризуется минимальным образованием смеси изомеров и повышенной в результате этого производительностью и чистотой. Заявленный способ также предусматривает минимальное использование токсичных растворителей.
2-[1-[3,5-бис(трифторметил)фенил]этокси-3-(4-фторфенил)-1,4-оксазин], исходный материал 2, и (2R,2-альфа-R,3a)-2-[1-[3,5-бис(трифторметил)фенил]этокси-3-(4-фторфенил)-1,4-оксазин], исходный материал 2а, могут быть получены в соответствии с РСТ WO 01/94324 A1 (опубликованной 13 декабря 2001 г.) и US 2002/0052494 A1 (опубликованным 2 мая 2002) или при использовании их модификаций. Исходный материал может быть использован непосредственно или после очистки. Методы очистки включают кристаллизацию, перегонку, хроматографию с нормальной или обращенной фазой. Следующий пример приведен в иллюстративных целях и не предназначен для ограничения объема притязаний раскрытого изобретения.
Пример 1
[2R-[2α(R*),3α]]-5-[[2-[1-[3,5-бис(трифторметил)фенил]этокси]-3-(4-фторфенил)-4-морфолинил]метил]-1,2-дигидро-3Н-1,2,4-триазол-3-он
Смесь исходного материала в виде гидрохлорида (2R,2-альфа-R,3a)-2-[1-[3,5-бис(трифторметил)фенил]этокси-3-(4-фторфенил)-1,4-оксазина (2а) (1,00 кг; 2,11 моль) и карбоната калия (1,02 кг; 7,39 моль) в ДМСО (2,2 л) и толуоле (1,0 л) охлаждают до 15°С. Добавляют суспензию амидразона 3 (367 г; 2,22 моль) в толуоле (1,5 л). Смесь перемешивают, а затем распределяют между толуолом (4,0 л) и водой (5,0 л). Фазы разделяют при 40°С. Органический слой (содержащий 4а) промывают водой (5,0 л) при 40°С, а затем частично концентрируют при атмосферном давлении, в результате чего получают промежуточное соединение 4а, которое используют на следующей стадии без выделения. Образующийся раствор, содержащий промежуточное соединение 4а, нагревают до 140°С в течение 3 часов, а затем позволяют ему остыть до комнатной температуры. Твердые вещества фильтруют и сушат в вакууме при 40°С. Продукт (1,00 кг) растворяют в метаноле (10,0 л) и добавляют 50 г Darco. Смесь нагревают при 60°С в течение 1 ч, а затем фильтруют при указанной температуре. Фильтрату позволяют медленно остыть до комнатной температуры. Воду (5,0 л) добавляют медленно в течение 1 ч. Суспензию охлаждают до 5°С и твердые вещества отфильтровывают и сушат в вакууме при 40°С, в результате чего получают 0,96 кг (85% общий выход) продукта [2R-[2α(R*),3α]]-5-[[2-[1-[3,5-бис(трифторметил)фенил]этокси]-3-(4-фторфенил)-4-морфолинил]метил]-1,2-дигидро-3Н-1,2,4-триазол-3-она, (т.е. 5-[[2(R)-[1(R)-[3,5-бис(трифторметил)фенил]этокси]-3(S)-(4-фторфенил)-4-морфолинил]метил]-1,2-дигидро-3Н-1,2,4-триазол-3-он).
Промежуточное соединение 4а: [α]D 25=+84° (c=1,02, метанол); 1Н ЯМР(400 МГц, CDCl3) δ 7,64 (с, 2Н), 7,34 (шир.т, J˜7, 2Н), 7,16 (с, 1Н), 7,03 (т, J=8,4, 2Н), 5,8 (оч.шир.с, 2Н), 4,88 (кв, J=6,6, 1Н), 4,33 (д, J=2,8, 1Н), 4,24 (тд, J=11,6, 2,0, 1Н), 3,77 (с, 2Н), 3,66 (ддд, J=11,6, 3,2, 1,6, 1Н), 3,46 (д, J=2,8, 1Н), 3,31 (д, J=14,5, 1Н), 2,96 (шир.д, J=11,6, 1Н), 2,59 (д, J=14,5, 1Н), 2,50 (тд, J=12,1, 3,2, 1Н), 1,47 (д, J=6,6, 3Н). Элементный анализ: рассчитано для С24Н25F7N4O4: C 50,89; H 4,45; F 23,48; N 9,89. Найдено: С 50,48; H 4,40; F 23,43; N 9,84. Конечный продукт 1а: Т пл.: 255°С; [α]D 25=+69° (c=1,00; метанол); 1Н ЯМР (400 МГц, CD3OD) δ 7,70 (с, 1Н), 7,51 (м, 2Н), 7,32 (с, 2Н), 7,04 (т, J=8,7, 2Н), 4,94 (кв, J=6,3, 1Н), 4,35 (д, J=2,8, 1Н), 4,28 (тд, J=11,5. 2,8, 1Н), 3,66 (ддд, J=11,5, 3,3, 1,6, 1Н), 3,54 (д, J=14,3, 1Н), 3,48 (д, J=2,8, 1Н), 2,88 (шир.д, J=11,9, 1Н), 2,86 (д, J=14,3, 1Н), 2,49 (тд, J=11,9, 3,6, 1Н), 1,44 (д, J=6,3, 3Н); 13С ЯМР (100 МГц, CD3OD) δ 164,1 (д, J=245,9), 158,7, 147,6, 147,0, 134,1 (д, J=3,1), 132,7 (д, J=33,4), 132,4 (д, J=8,0), 127,8 (м), 124,6 (кв, J=272,0), 122,3 (м), 116,1 (д, J=21,6), 97,1, 73,7, 70,5, 60,4, 53,6, 52,2, 24,7. Элементный анализ, рассчитано для С23Н21F7N4O3: C 51,69; H 3,96; F 24,88: N 10,48. Найдено: C 51,50; H 3,82: F 24,73; N 10,44. МСВР: 534,1480 (измерено); 534,1502 (рассчитано для С23Н21F7N4O3).
Все патенты и патентные публикации, цитированные в описании, включены в качестве ссылок во всем объеме. Хотя изобретение описано и проиллюстрировано со ссылкой на некоторые конкретные варианты его осуществления, специалистам будет ясно, что различные изменения могут быть осуществлены без отклонения от существа и объема притязаний изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ МОРФОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ СНИЖЕНИЯ КОЛИЧЕСТВА ТАХИКИНИНОВ ПРИ ЛЕЧЕНИИ ИЛИ ПРОФИЛАКТИКЕ ФИЗИОЛОГИЧЕСКИХ СОСТОЯНИЙ, АССОЦИИРУЕМЫХ С ИЗБЫТКОМ ТАХИКИНИНОВ | 1994 |
|
RU2131426C1 |
| ЗАМЕЩЕННЫЕ МОРФОЛИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПРОТИВОДЕЙСТВИЯ ВЕЩЕСТВУ Р ИЛИ БЛОКИРОВАНИЯ РЕЦЕПТОРОВ НЕЙРОКИНИНА-1 | 1995 |
|
RU2170233C2 |
| Способ получения (6R,7S,7aS)-6-((R)-1-(3,5-бис(трифторметил)фенил)этокси)-7-(4-фторфенил)гексагидро-3Н-пирролизин-3-она | 2022 |
|
RU2789599C1 |
| МОРФОЛИНОВОЕ ПРОИЗВОДНОЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 1994 |
|
RU2201924C2 |
| ЗАМЕЩЕННЫЕ ГЕТЕРОЦИКЛЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ БЛОКАДЫ РЕЦЕПТОРОВ НЕЙРОКИНИНА-1 У МЛЕКОПИТАЮЩИХ, СПОСОБ ДЛЯ БЛОКАДЫ РЕЦЕПТОРОВ НЕЙРОКИНИНА-1 У МЛЕКОПИТАЮЩИХ | 1993 |
|
RU2140914C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРОВ ФОСФОДИЭСТЕРАЗЫ-4 | 2003 |
|
RU2323938C2 |
| ПРОИЗВОДНЫЕ АЗОЛОВ | 2012 |
|
RU2622639C2 |
| 2-[(4-ГЕТЕРОЦИКЛ-ФЕНОКСИМЕТИЛ)ФЕНОКСИ]-АЛКАНОАТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ ПОДАВЛЕНИЯ НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТИ | 1993 |
|
RU2113434C1 |
| КОНДЕНСИРОВАННЫЕ ТРИАЗОЛАМИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ Р2Х7 | 2010 |
|
RU2533122C2 |
| ПРОИЗВОДНЫЕ ДИГИДРОБЕНЗО[b][1,4]ДИАЗЕПИН-2-ОНА В КАЧЕСТВЕ АНТАГОНИСТОВ I mGluR2 | 2002 |
|
RU2270197C2 |
Изобретение относится к новому способу получения соединения 5-[[2(R)-[1(R)-[3,5-бис(трифторметил)фенил]этокси]-3(S)-(4-фторфенил)-4-морфолинил]метил]-1,2-дигидро-3Н-1,2,4-триазол-3-она формулы 1, включающему взаимодействие гидрохлорида соединения формулы 2, в присутствии неорганического основания, толуола и полярного апротонного растворителя с соединением формулы 3, с получением соединения формулы 4, циклизацию соединения формулы 4 при температуре 140-150°С с получением соединения формулы 1. Техническим результатом является более практичный и экономичный способ получения соединения, которое используется как антагонист рецептора вещества Р (нейрокинина-1), с относительно высоким выходом. 11 з.п. ф-лы.
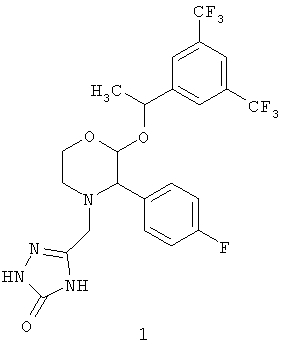
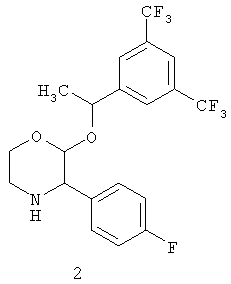
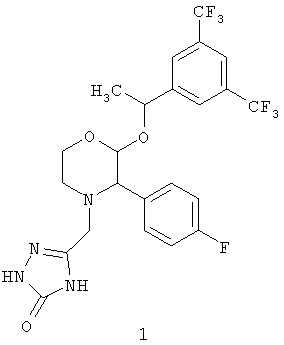
включающий:
взаимодействие гидрохлорида соединения формулы 2
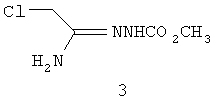
в присутствии неорганического основания, толуола и полярного апротонного растворителя с соединением формулы 3
с получением соединения формулы 4
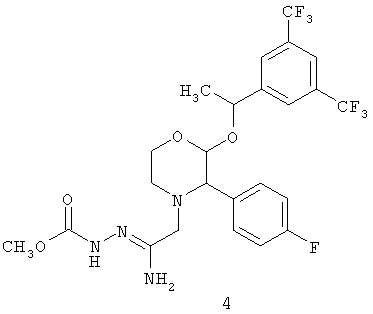
циклизация соединения формулы 4 при температуре 140-150°С с получением соединения формулы 1.
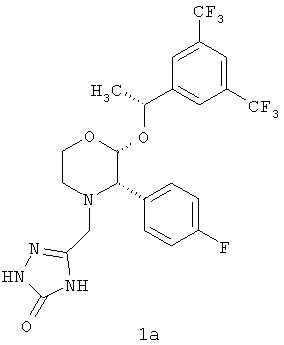
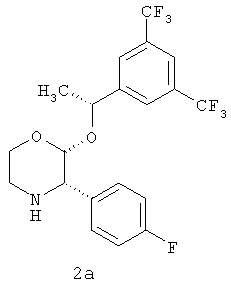
| WO 9516679 A1, 22.06.1995 | |||
| US 6096742, 01.08.2000 | |||
| US 6297376 B1, 02.10.2001 | |||
| US 6229010 B1, 08.05.2001 | |||
| US 5719147, 17.02.1998 | |||
| US 5637699, 10.06.1997 | |||
| ЗАМЕЩЕННЫЕ МОРФОЛИНЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПРОТИВОДЕЙСТВИЯ ВЕЩЕСТВУ Р ИЛИ БЛОКИРОВАНИЯ РЕЦЕПТОРОВ НЕЙРОКИНИНА-1 | 1995 |
|
RU2170233C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ МОРФОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ СНИЖЕНИЯ КОЛИЧЕСТВА ТАХИКИНИНОВ ПРИ ЛЕЧЕНИИ ИЛИ ПРОФИЛАКТИКЕ ФИЗИОЛОГИЧЕСКИХ СОСТОЯНИЙ, АССОЦИИРУЕМЫХ С ИЗБЫТКОМ ТАХИКИНИНОВ | 1994 |
|
RU2131426C1 |
Авторы
Даты
2008-06-20—Публикация
2003-04-17—Подача