Область техники, к которой относится изобретение
Изобретение относится к фармацевтической композиции, которая получена сублимационной сушкой и содержит оксалиплатин в качестве активного компонента, и фармацевтически приемлемый носитель, а также к применению этого препарата для снижения риска вирусного заражения, особенно возбудителем губчатой (спонгиозной) энцефалопатии животных.
Уровень техники
Оксалиплатин (международное (непатентованное) название "oxaliplatinum" согласно номенклатуре INN (International Nonproprietary Nomenclature)) был получен в оптически чистой форме в 1978 году выделением из смеси изомеров [J. Clin. Hematol. Oncol., 1977, 7(1), 197-210]. Химически оксалиплатин является комплексом {транс-(-)-1,2-циклогександиамин}-(оксалато)платины(II) формулы I
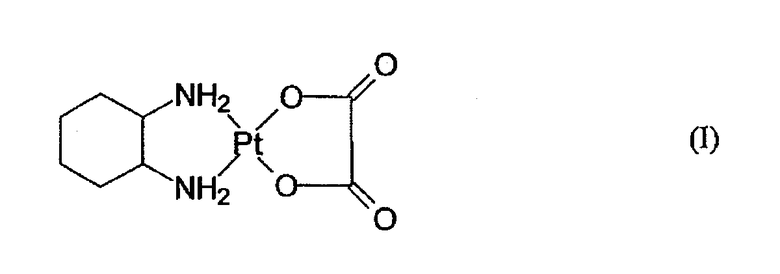
Оксалиплатин является цитостатическим средством, применимым в лечении тестикулярных и овариальных опухолей, злокачественной меланомы, бронхогенной карциномы и особенно метастазирующей карциномы толстой кишки, в комбинации с фторпиримидинами. В сравнении с цисплатиной, используемой до сих пор, оксалиплатин проявляет пониженную нефротоксичность и более широкий спектр противоопухолевой активности. Оксалиплатин обычно используется в дозах 100-135 мг/м2 в форме 2-6-часовых вливаний. Раствор для вливания получают разбавлением конечной лекарственной формы 5% водным раствором глюкозы.
В рамках предшествующего уровня техники был описан ряд жидких лекарственных форм оксалиплатина на основе его водных растворов, которые, однако, из-за их недостаточной стабильности пока не нашли применения. Причиной этой нестабильности является известный факт, что оксалиплатин гидролитически разрушается с образованием токсичных аквакомплексов платины. Единственной стабильной лекарственной формой оксалиплатина, известной до сих пор, является порошковый препарат, полученный сублимационной сушкой в вакууме (лиофилизацией). Наряду с оксалиплатином этот сухой порошковый препарат содержит носитель, состоящий из лактозы, которая обеспечивает сцепление сухой матрицы оксалиплатина, образованной лиофилизацией в вакууме, и предотвращает ее растрескивание, которое иначе привело бы к выделению части оксалиплатина из сосуда, в котором происходит лиофилизация. Существенным недостатком используемого лактозного носителя, который является животным продуктом, является риск вирусного заражения фармацевтического препарата вирусами, которые могут присутствовать в лактозе. С недавних пор снижение риска такого вирусного заражения, особенно переноса губчатой энцефалопатии животных, представляет собой широко распространенную проблему, касающуюся большинства лекарственных форм, которые содержат вспомогательные компоненты животного, в частности коровьего, происхождения. Лактоза, до сих пор применяемая в фармацевтических препаратах оксалиплатина, проявляет очень хороший криозащитный эффект, и ее замена другим подходящим носителем с сохранением свойств лиофилизата оксалиплатина и экономика процесса сублимационной сушки до сих пор не нашли удовлетворительного решения.
Раскрытие изобретения
Задача вышеупомянутой желательной замены лактозного носителя другим носителем, который в принципе устраняет упомянутый риск вирусного заражения, решается фармацевтической композицией по настоящему изобретению, полученной посредством сублимационной сушки в вакууме, которая содержит оксалиплатин в качестве активного компонента и фармацевтически приемлемый носитель, причем указанная композиция характеризуется тем, что содержит в качестве носителя по меньшей мере один спиртовой сахар неживотного происхождения, причем отношение оксалиплатина к этому спиртовому сахару или спиртовым сахарам неживотного происхождения составляет от 1:3 до 1:7 по массе.
Предпочтительно фармацевтический препарат по настоящему изобретению содержит оксалиплатин и спиртовой сахар или спиртовые сахара неживотного происхождения в соотношении 1:5 по массе.
В фармацевтической композиции по изобретению предпочтительным спиртовым сахаром неживотного происхождения является маннит.
Настоящее изобретение также относится к способу получения вышеупомянутой фармацевтической композиции, характеризующемуся тем, что стерильный водный раствор оксалиплатина и по меньшей мере одного спиртового сахара неживотного происхождения, содержащий оксалиплатин и спиртовой сахар неживотного происхождения или спиртовые сахара неживотного происхождения в массовом соотношении от 1:3 до 1:7 при общей концентрации упомянутых соединений от 2,8 до 3,2 мас.%, вводят в сосуд в объеме, равном не больше, чем 60% доступного объема сосуда, после чего содержимое сосуда охлаждают до 2-8°С, затем замораживают при линейном снижении температуры 0,1-0,5°С/мин до конечной температуры от -35 до -45°С, оставляют при этой температуре в течение 1-6 часов и затем подвергают сублимационной сушке в вакууме.
Наконец, изобретение также относится к использованию вышеупомянутой фармацевтической композиции в лечении опухолей, чувствительных к оксалиплатину.
После растворения в подходящем фармацевтически приемлемом растворителе фармацевтическая композиция по данному изобретению дает прозрачный раствор, который не содержит ни нерастворенного материала, ни мутности, и который, следовательно, особенно пригоден для парентерального применения. Препарат по изобретению может быть легко получен, высоко стабилен и его применение не представляет какого-либо риска вирусного заражения.
Способ по настоящему изобретению решает проблемы, которые имели бы место в случае простой замены лактозы маннитом без изменения существующего режима обработки лактозой. Во время обработки растворов, в которых лактозу просто заменяют маннитом, лиофилизат часто улетучивается из сосудов, а стеклянные сосуды трескаются в результате возрастающего механического напряжения вследствие изменения объема замороженного раствора, что проявляется как разрушение дна сосуда во время сублимационной сушки. Найдено, что температурный режим методики замораживания по изобретению значительно устраняет упомянутое растрескивание сосуда во время сублимационной сушки. Таким образом, найдено, что для того, чтобы достичь оптимальной скорости сублимационной сушки, общая концентрация оксалиплатина и по меньшей мере одного спиртового сахара в водном растворе перед сублимационной сушкой должна быть 2,8-3,2 мас.%. Далее, найдено, что сосуды могут быть наполнены стерильным раствором оксалиплатина и маннита в указанном массовом отношении в объеме до 60% доступного объема сосуда без изменения качества лиофилизата, без улетучивания лиофилизата из сосудов и без растрескивания сосудов, и этот раствор представляется очень выгодным раствором с точки зрения производительности оборудования лиофилизации.
По своим свойствам фармацевтическая композиция по изобретению особенно пригодна для применения в лечении опухолей, чувствительных к оксалиплатину.
В следующей части описания изобретение будет объяснено подробно с использованием примеров выполнения, которые являются иллюстративными и не ограничивают как-либо объем изобретения.
Примеры
Пример 1
В хороших производственных условиях (GMP (Good Manufacturing Practice) conditions), 0,50 кг оксалиплатина (фармакопейного качества) и 2,50 кг маннита (фармакопейного качества) постепенно растворяют при 20-25°С в 70 кг воды. Полученный раствор стерилизуют фильтрованием через фильтр 0,22 мкм и разливают в бесцветные прозрачные ампулы для антибиотиков первого гидролитического класса, тип 20Н (Saint Gobain Desjonqueres), причем количество раствора соответствует 50 мг растворенного активного компонента на ампулу. Заполненные ампулы снабжают крышками для сублимационной сушки и помещают в камеру сублимационной сушки, предварительно охлажденную до 5°С. После достижения температурного равновесия раствора в ампуле с окружающей средой раствор в ампуле медленно замораживают (линейное понижение температуры 0,2°С/мин) до конечной температуры -40°С. Замороженный раствор оставляют при этой температуре на 4 часа и затем подвергают сублимационной сушке в вакууме.
Полученный лиофилизат имеет форму белого компактного вещества и содержит 0,8% воды. Растворение полученного материала дает прозрачный раствор в соответствие с Европейской Фармакопеей, статья 2.2.1.
Пример 2
В хороших производственных условиях (GMP (Good Manufacturing Practice) conditions), 0,50 кг оксалиплатина (фармакопейного качества) и 2,50 кг маннита (фармакопейного качества) постепенно растворяют при 20-25°С в 70 кг воды. Полученный раствор стерилизуют фильтрованием через фильтр 0,22 мкм и разливают в бесцветные прозрачные ампулы для антибиотиков первого гидролитического класса, тип 20Н (Saint Gobain Desjonqueres), причем количество раствора соответствует 100 мг растворенного активного компонента на ампулу. Заполненные ампулы снабжают крышками для сублимационной сушки и помещают в камеру сублимационной сушки, предварительно охлажденную до 5°С. После достижения температурного равновесия раствора в ампуле с окружающей средой раствор в ампуле медленно замораживают (линейное понижение температуры 0,2°С/мин) до конечной температуры -40°С. Замороженный раствор оставляют при этой температуре на 4 часа и затем подвергают сублимационной сушке в вакууме.
Полученный лиофилизат имеет форму белого компактного вещества и содержит 1,0% воды. Растворение полученного материала дает прозрачный раствор в соответствии с Европейской Фармакопеей, статья 2.2.1.
Пример 3
Согласно данному примеру изучается стабильность фармацевтической композиции, полученной в Примере 1 во время ее хранения при 40°С и 75% относительной влажности. Полученные результаты приведены в Таблице 1.
Пример 4
Согласно данному примеру изучается стабильность фармацевтической композиции, полученной в примере 2, во время ее хранения при 40°С и 75% относительной влажности. Полученные результаты приведены в Таблице 2.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРОТИВОВИРУСНОГО СРЕДСТВА | 2010 |
|
RU2454221C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ БАКТЕРИАЛЬНОЙ ИНФЕКЦИИ | 2012 |
|
RU2520346C2 |
| Способ получения лиофилизата | 1987 |
|
SU1836079A3 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭПОПРОСТЕНОЛ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2007 |
|
RU2423130C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПАРЕНТЕРАЛЬНОЙ ДОСТАВКИ В ФОРМЕ ЛИОФИЛИЗАТА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2007 |
|
RU2370258C2 |
| ШТАММ БАКТЕРИЙ HISTOPHILUS SOMNI, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ПОЛУЧЕНИЯ МОНО- И ПОЛИВАЛЕНТНЫХ ИММУНОГЕННЫХ КОМПОЗИЦИЙ, НАПРАВЛЕННЫХ НА СПЕЦИФИЧЕСКУЮ ПРОФИЛАКТИКУ ГИСТОФИЛЕЗА (СТАДНОГО БЕСПЛОДИЯ) РОГАТОГО СКОТА | 2020 |
|
RU2754005C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОГО СОСТАВА РОКУРОНИЯ БРОМИДА В ФОРМЕ СТАБИЛЬНОГО ЛИОФИЛИЗАТА И ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2013 |
|
RU2594062C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНЪЕКЦИОННОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ФОСФОЛИПИДНОГО ПРЕПАРАТА "ФОСФОГЛИВ" ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОСТРЫХ И ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2005 |
|
RU2304430C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТИИШЕМИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2545833C1 |
| Фармацевтическая композиция нейропротекторного действия для парентерального применения на основе гексаметилендиамида бис-(N-моносукцинил-L-глутамил-L-лизина) в лиофилизированной лекарственной форме | 2017 |
|
RU2678203C2 |
Изобретение относится к фармацевтической композиции, полученной сублимационной сушкой в вакууме, содержащей оксалиплатин в качестве активного компонента и фармацевтически приемлемый носитель, в которой носителем является по меньшей мере один спиртовой сахар неживотного происхождения, причем массовое отношение оксалиплатина к спиртовому сахару неживотного происхождения или спиртовым сахарам неживотного происхождения составляет от 1:3 до 1:7. Изобретение обеспечивает снижение риска вирусного заражения, особенно возбудителем губчатой энцефалопатии животных. 3 н. и 2 з.п. ф-лы, 2 табл.
характеризующийся тем, что стерильный водный раствор оксалиплатина и по меньшей мере одного спиртового сахара неживотного происхождения, содержащий оксалиплатин и спиртовой сахар неживотного происхождения или спиртовые сахара неживотного происхождения в массовом отношении от 1:3 до 1:7 при общей концентрации упомянутых соединений от 2,8 до 3,2 мас.%, вводят в сосуд в объеме, равном не более чем 60% доступного объема сосуда, после чего содержимое сосуда охлаждают до 2-8°С, затем замораживают при линейном снижении температуры 0,1-0,5°С/мин до конечной температуры от -35 до -45°С, оставляют при этой температуре в течение 1-6 ч и затем подвергают сублимационной сушке в вакууме.
| WO 9412193 А1, 09.06.1994 | |||
| Устройство для быстродействующей телеграфии | 1935 |
|
SU48635A1 |
| «Элоксатан», Инструкция по медицинскому применению препарата, рег | |||
| Способ приготовления загустки для основных красителей | 1928 |
|
SU14616A1 |
| US 6306902 В1, 23.10.2001 | |||
| US 5049396, 17.09.1991 | |||
| СТАБИЛЬНАЯ ЛИОФИЛИЗИРОВАННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1996 |
|
RU2163801C2 |
Авторы
Даты
2008-07-20—Публикация
2004-08-31—Подача