Настоящее изобретение относится к применению субстанции для диагностического выявления sgk1 (зависящая от сыворотки и глюкокортикоида киназа 1) и к применению действующего вещества для воздействия на sgk1 с целью терапевтического лечения заболеваний, связанных с нарушенной активностью ТФ (тканевый фактор), а также к соответствующему диагностическому набору.
Многочисленные внешние сигналы, которым подвергается клетка со стороны окружающей ее среды, вызывают внутриклеточные каскады фосфорилирования/дефосфорилирования, предназначенные для быстрой и обратимой передачи этих сигналов от плазматической мембраны и ее рецепторов в цитоплазму и ядро клетки. Регуляция индивидуальных белков, участвующих в этих каскадах, позволяет, прежде всего, обеспечивать высокую степень специфичности и гибкости клеток, что позволяет клеткам очень быстро реагировать на внеклеточные сигналы. В этих регуляторных процессах участвуют, прежде всего, киназы, т.е. белки, которые переносят фосфатную группу на конкретные субстраты. Первоначально зависящую от сыворотки и глюкокортикоида киназу (sgk) клонировали из клеток карциномы молочной железы крысы (Webster M.K., Goya L., Firestone G.L., J.Biol. Chem. 268 (16), 1993, cc.11482-11485; Webster M.K., Goya L., Ge Y., Maiyar A.C., Firestone G.L., Mol. Cell. Biol. 13 (4), 1993, cc.2031-2040). Человеческую киназу hsgk клонировали из клеток печени в виде зависящего от объема клетки гена (Waldegger S., Barth Р., Raber G., Lang F., Proc. Natl. Acad. Sci. USA, 94, 1997, cc.4440-4445). Было установлено, что крысиная киназа (Chen S.Y., Bhargava A., Mastroberardino L., Meijer O.C., Wang J., Buse P., Firesone G.L., Verrey F., Pearce D., Proc. Natl. Acad. Sci. USA, 96, 1999, cc.2514-2519; Naray-Fejes-Toth A., Canessa С., Cleveland E.S., Aldrich G., Naraj-Fejes-Toth A., J. Biol. Chem., 274, 1999, cc.16973-16978) стимулирует эпителиальный Na+-канал (ENaC). Кроме того, было установлено, что повышение активности EnaC сопровождается гипертензией (Warnock D.G., Kidney Ind., 53(1), 1998, с.1824).
В DE 19708173 описано, что hsgk1 обладает значительным потенциалом с точки зрения диагностики при многих заболеваниях, связанных с патофизиологическим изменением объема клеток, таких, например, как гипернатриемия, гипонатриемия, сахарный диабет, почечная недостаточность, гиперкатаболизм, печеночная энцефалопатия и бактериальные или вирусные инфекции.
В DE 19917990 описаны ингибиторы киназы, такие, например, как стауроспорин, хелеритрин или трансдоминантно ингибирующие киназы, которые можно применять при лечении заболеваний, зависящих от объема клеток.
hsgk экспрессируется также в головном мозге (Waldegger S., Barth P., Raber G., Lang F., Proc. Natl. Acad. Sci. USA, 94, 1997, cc.4440-4445), где она регулирует зависящие от напряжения К+-каналы Kv1.3. Было установлено, что эти К+-каналы Kv1.3-типа участвуют в регуляции нейронной возбудимости (Pong О., Physiol. Rev., 72, 1992, cc.69-88), регуляции клеточной пролиферации (Cahalan M.D. и Chandy K.G., Cur. Opin. Biotech., 8(6), 1997, cc.749-756), а также апоптозной гибели клеток (Szabo I., Gulbins Е., Apfel Н., Zhan X., Barth P., Busch А.е., Schlottmann К., Pongs О., Lang F., J.Biol. Chem., 271, 1999, cc.20465-20469; Lang F., Szabo I., Lepple-Wienhues A., Siemen D., Gulbins E., News Physiol. Sci., 14, 1999, cc.194-200). Кроме того, Kv1.3 играют важную роль в регуляции пролиферации и функции лимфоцитов (Cahalan M.D. и Chandy K.G., Cur. Opin. Biotech., 8(6), 1997, cc.749-756). Были клонированы еще два представителя семейства sgk, а именно sgk2 и sgk3 (Kobayashi Т., Deak M., Morrice N., Cohen P., Biochem J. 344:, 1999, cc.189-197). Кроме того, было установлено, что sgk образуют семейство серин-треонин-протеинкиназ, которые поддаются транскрипционной и посттранскрипционной регуляции. Подобно sgk1, sgk2 и sgk3 активируются также, например, инсулином и IGF1 посредством Р13-киназного пути. Однако в настоящее время семейство белков sgk еще не полностью охарактеризовано.
Таким образом, в основу настоящего изобретения была положена задача разработать новые диагностические и терапевтические подходы, основанные на применении sgk1.
При создании изобретения неожиданно было установлено, что сверхэкспрессия интактной sgk1 по сравнению с экспрессией неактивной sgk1 приводит к повышению коагулирующей активности. В этой экспериментальной системе коагуляцию инициировали с помощью так называемого тканевого фактора (ТФ). ТФ представляет собой трансмембранный гликопротеин с молекулярной массой 47 кДа, который служит основным связывающим звеном между васкулярными клетками или мононуклеарными клетками и гемостатической системой. При этом ТФ инициирует каскад коагуляции крови (Davie E.W., Fujikawa К., Kisiel W., Biochemistry, 30, 1991, cc.10363-10370). ТФ инициирует коагуляцию крови путем связывания с высокой аффинностью с факторами VII/VIIa. Образовавшийся в результате этого комплекс инициирует активацию факторов IX и Х с последующим образованием тромбина. Тромбин, в свою очередь, катализирует превращение фибриногена в фибрин, что приводит к отложению фибрина и коагуляции крови (Nemerson Y., Blood, 71, 1998, cc.1-8).
Повышение экспрессии ТФ не обязательно связано с повышением биологической активности ТФ. Функционально активный ТФ зависит от экспрессии биологически активной формы на клеточной поверхности. В гладкомышечных клетках сосудов (ГМК) и моноцитах только 10-20% общего клеточного ТФ, который также представляет собой биологически активную форму, доступно на клеточной поверхности, в то время как остальная часть ТФ находится во внутриклеточных пулах (примерно 30%) и в виде латентного поверхностного ТФ (50-60%) (Preissner K.T., Nawroth P.P., Kanse S.M., J. Patol., 190, 2000, cc.360-372; Schlecter A.D., Giesen P.L., Taby О., Rosenfleld C.L., Rossikhina M., Fyfe B.S., Kohtz D.S., Fallon J.T., Nemerson Y., Taubmann M.B., J. Clin. Invest., 100, 1997, cc.2276-2285). Было установлено, что ТФ помимо своего коагулирующего действия (Ruef J., Hu Z.Y., Yin L.Y., Wu Y., Hanson S.R., Kelly A.B., Harker L.A., Rao G.N., Runge M.S., Patterson C., Circ. Res., 1997, cc.24-33) играет также важную роль в метастазировании опухолей и ангиогенезе (Lwaleed В.А. и Cooper A.J., Medical Hypotheses, 55, 2000, cc.470-473; Verheul H.M.W., Jorna A.S., Hoekman К., Broxterman H.J., Gebbink M.F.B.G., Pinedo H.M., Blood, 2000, cc.4216-4221). Таким образом, полученные результаты функциональных исследований свидетельствуют о том, что воздействия sgk1 могут оказывать влияние на экспрессию и/или функцию ТФ на клеточной мембране и тем самым оказывать косвенное влияние на коагулирующую способность крови, прилипание опухолевых клеток с последующим метастазированием и ангиогенез, а также на заболевания, в которых играет роль ангиогенез. Стимуляция sgk1 приводит к повышению экспрессии тканевого фактора, в то время как ингибирование sgk1 приводит к снижению экспрессии активного тканевого фактора и в результате этого оказывается возможным посредством стимуляции или ингибирования оказывать влияние на указанные выше показания.
В соответствии с этим задача настоящего изобретения решается с помощью объектов изобретения, сущность которых изложена в независимых пунктах 1, 6, 7, 22, 26 и 28. Предпочтительные варианты осуществления изобретения изложены в зависимых пунктах. Тем самым содержание всех этих пунктов включено в настоящее описание в качестве ссылки.
Объектом изобретения является применение по меньшей мере одной субстанции для обнаружения экспрессии и/или функции sgk1 в эукариотических клетках. Тем самым оказывается возможным прежде всего также устанавливать диагноз заболеваний, которые связаны с нарушением активности ТФ. Такая субстанция может представлять собой, например, антитело к sgk1, и его можно применять в методе обнаружения, известном специалисту в данной области, таком как ELISA (твердофазный иммуноферментный анализ). При таких иммунных анализах специфическое антитело (или в случае выявления антитела гомологичные тест-антигены) к подлежащему обнаружению антигену (sgk1) связывают с материалом подложки (например, целлюлозой или полистиролом), на котором после инкубации совместно с образцом образуется иммунный комплекс. На следующей стадии в эти иммунные комплексы вводят несущее метку антитело. Путем добавления к реакционной смеси хромогенного субстрата можно визуализировать комплексы: иммунный комплекс, связанный фермент/субстрат или оценивать концентрацию антигена в образце путем фотометрического определения связанных с иммунным комплексом маркерных ферментов на основе сравнения со стандартами, обладающими известной ферментативной активностью.
Другими субстанциями, которые можно использовать для диагностического обнаружения, являются так называемые олигонуклеотиды, которые пригодны для применения с использованием так называемой полимеразной цепной реакции (ПЦР) в методе молекулярной генетики, основанном на амплификации определенных выбранных фрагментов ДНК, для количественного выявления sgk1.
В другом предпочтительном варианте осуществления изобретения в качестве субстанций, применяемых согласно изобретению, используют полинуклеотиды, которые могут гибридизоваться с sgk1 в строгих условиях. Такие полинуклеотиды можно применять, например, в Саузерн- или Нозерн-блоттинге для определения содержания ДНК или РНК sgk1. Соответствующие методы известны специалисту в данной области. Таким путем можно, например, анализировать скорость транскрипции sgk1.
В особенно предпочтительном варианте применения согласно изобретению субстанцию, представляющую прежде всего антитела, олигонуклеотиды и/или полинуклеотиды, можно применять для выявления мутаций в sgk1. Представляет интерес тот факт, что определенные мутации в sgk1 связаны с повышенным уровнем экспрессии и/или активности киназы. Это проявляется, в частности, в случае двух нуклеотидных полиморфизмов нуклеотидов. Эти нуклеотидные полиморфизмы нуклеотидов в интроне 6 (Т→С) (первый) и в экзоне 8 (С→Т) (второй) в человеческом sgk1. В этой связи следует сослаться на WO 02/074987, в котором указано, что эти полиморфизмы нуклеотидов связаны с генетической предрасположенностью к гипертензии. Аналогичные данные получены также для других мутаций, прежде всего инсерционных мутаций. Таким образом, в изобретении предложено применение соответствующих антител, олигонуклеотидов и/или полинуклеотидов для выявления соответствующих мутаций, которые связаны с повышенным уровнем экспрессии и/или активности sgk1, и тем самым устанавления диагноза заболеваний, связанных с нарушенной активностью ТФ. Специалисту в данной области известны методические подходы, на которых основаны такие применения. Специалисту в данной области очевидны другие методы, с помощью которых можно количественно выявлять экспрессию и/или функцию sgk1, и они также подпадают под объем изобретения.
В изобретении предложено действующее вещество, которое позволяет оказывать влияние, прежде всего ингибировать или активировать экспрессию и/или функцию sgk1 в эукариотических клетках, с целью лечения заболеваний, связанных с нарушенной активностью ТФ. Поскольку sgk1, так же как и sgk2 и sgk3, представляет собой киназу, то можно рассматривать прежде всего ингибиторы киназы, известные специалисту в данной области, такие, например, как стауроспорин, хелеритрин и т.д., а также другие субстанции, такие, например, как трансдоминантно негативные мутанты киназы. Специалисту в данной области известны такие субстанции, и указанные субстанции можно получать из коммерческих (например, от фирм Sigma, Calbiochem и т.д.), а также некоммерческих источников. В качестве активаторов можно применять, например, генетически измененные мутанты sgk1, а также ингибиторы фосфатаз. Ингибиторы фосфатаз также известны специалисту в данной области, и некоторые из них также можно получать из коммерческих (например, от фирм Sigma, Calbiochem и т.д.), а также некоммерческих источников. С помощью ингибиторов фосфатаз можно ингибировать дефосфорилирование, в результате чего активированная sgk1 мишень (ТФ) сохраняется в активированном состоянии. Предпочтительным является применение таких действующих веществ для приготовления лекарственного средства или фармацевтической композиции.
В другом предпочтительном варианте осуществления изобретения действующее вещество направлено против самой sgk1. Действующие вещества могут представлять собой, например, антисмысловые последовательности, так называемые мутанты с дефицитом киназной активности, а также ингибиторы киназы, такие как уже упомянутые выше стауроспорин и/или хелеритрин или их аналоги. Кроме того, действующее вещество может представлять собой так называемое «низкомолекулярное соединение» или полинуклеотид, кодирующий пептид, который оказывает влияние, предпочтительно ингибирует или активирует экспрессию sgk1.
Еще в одном предпочтительном варианте осуществления изобретения действующее вещество направлено против активаторов, ингибиторов, регуляторов и/или биологических предшественников sgk1. Такие активаторы, ингибиторы, регуляторы и/или биологические предшественники могут представлять собой расположенные выше и ниже компоненты каскада трансдукции сигнала sgk1, факторы транскрипции, которые ответственны за уровень экспрессии sgk1, протеазы, которые осуществляют протеолитическое расщепление активаторов, ингибиторов, регуляторов и/или биологических предшественников sgk1, а также неизвестные до настоящего времени молекулы, на которые оказывает влияние действующее вещество и которые участвуют в экспрессии и/или функции sgk1.
Согласно изобретению можно применять как известные, так и неописанные до настоящего времени действующие вещества. В одном особенно предпочтительном варианте осуществления изобретения действующее вещество, направленное против активаторов, ингибиторов, регуляторов и/или биологических предшественников sgk1, представляет собой так называемое «низкомолекулярное соединение», прежде всего соединение с молекулярной массой (ММ)<1000. Низкомолекулярные соединения могут представлять собой, например, ингибиторы киназ, такие, например, как имидазольные производные SB 203580 (MM 377,4) или SB 202190 (MM 331,3), которые являются известными ингибиторами экспрессии киназ и поступают в продажу от фирмы Calbiochem.
Изобретение можно применять для лечения всех форм заболеваний, связанных с нарушенной активностью ТФ. В этой связи особо следует отметить коагулопатии и/или ангиопатии врожденного или приобретенного типа. Под коагулопатиями подразумеваются нарушения коагулирующей способности в целом. Примерами врожденных коагулопатии (так называемых дефектных коагулопатий) являются дисфибриногенемия, гипопроконвертинемия, гемофилия В, дефект Стюарта-Провера и т.д. Примерами приобретенных нарушений коагулирующей способности являются дефицит протромбинового комплекса, коагулопатия потребления, гиперфибринолиз, иммунокоагулопатия, а также комплексные коагулопатии. Обе формы коагулопатии вызываются дефицитом или функциональным нарушением различных факторов свертывающей системы плазмы. В соответствии с разной симптоматикой различают коагулопатии с геморрагической тенденцией (минус-коагулопатии) и коагулопатии с тенденцией к тромбозу (плюс-коагулопатии), а также гепатогенные, кардиогенные и иммунные коагулопатии в соответствии с местом их возникновения. Следовательно, путем активации или ингибирования sgk1 можно уменьшать или увеличивать предрасположенность крови к коагуляции и тем самым адаптировать к медицинским показаниям. Аналогичные соображения применимы также к ангиопатиям, т.е. заболеваниям, которые обозначают общим понятием «сосудистые заболевания», таким, например, как диабетическая ангиопатия, диабетическая микроангиопатия, легочная гипертензия, артериосклероз и т.д. В этом случае также можно применять действующее вещество, в частности, для лечения врожденных и/или приобретенных ангиопатий.
В особенно предпочтительных вариантах осуществления изобретения применяют субстанцию для выявления или действующее вещество для лечения легочной гипертензии и/или артериосклероза.
В другом предпочтительном варианте осуществления изобретения действующее вещество применяют для стимуляции или ингибирования ангиогенеза. Под ангиогенезом подразумевается развитие стенок сосудов, например, во время эмбрионального развития, и специалисту в данной области известен целый ряд зависящих от ангиогенеза заболеваний, таких, например, как сахарный диабет, генез опухоли и аутоиммунные заболевания. В другом предпочтительном варианте осуществления изобретения действующее вещество применяют для стимуляции или ингибирования заживления ран.
Кроме того, изобретение относится к диагностическому набору. Такой набор включает по меньшей мере одну субстанцию для обнаружения экспрессии и/или функции sgk1, для диагностики заболеваний, связанных с нарушенной активностью ТФ. Диагностический набор, предлагаемый в изобретении, отличается прежде всего тем, что субстанции, применяемые для обнаружения экспрессии и/или функции sgk1, представляют собой антитела к sgk1, олигонуклеотиды для полимеразной цепной реакции для амплификации фрагментов ДНК sgk1 и/или полинуклеотиды, которые могут гибридизоваться с sgk1 в строгих условиях. В этой связи наиболее предпочтительным является применение таких субстанций для выявления мутаций, прежде всего нуклеотидного полиморфизма и/или инсерций (мутации), связанных с повышением экспрессии и/или активности sgk1 (см. приведенное выше описание).
Кроме того, с помощью такого набора можно осуществлять диагностику заболеваний, которые связаны со сверхэкспрессией или с пониженной экспрессией или с гиперфункцией или гипофункцией sgk1. Такие диагностические агенты можно применять в диагностическом наборе целенаправленно для того, чтобы среди прочего выявлять заболевания, такие как описанные выше коагулопатии, ангиопатии, зависящие от ангиогенеза заболевания, заболевания, связанные с заживлением ран и т.д. В этом случае также заболевания можно выявлять путем обнаружения нарушенной экспрессии и/или функции sgk1. В частности, такая субстанция может представлять собой субстанцию, которая позволяет осуществлять такое обнаружение на нуклеотидном и/или пептидном уровне или на полинуклеотидном и/или полипептидном уровне. Другие отличительные признаки такой субстанции содержатся в соответствующем разделе приведенного выше описания.
Кроме того, под объем изобретения подпадает способ диагностики заболеваний, связанных с нарушенной активностью ТФ. В этом случае осуществляют количественное обнаружение экспрессии и/или функции или активности sgk1 в образце, взятом из тела пациента. Такой образец из тела может представлять собой, например, жидкость, такую как кровь или моча, или, например, клеточный образец. Количественное обнаружение осуществляют, например, с использованием антител к sgk1, олигонуклеотидов, которые можно применять в полимеразной цепной реакции для амплификации фрагментов ДНК sgk1 и/или с использованием полинуклеотидов, которые могут гибридизоваться с ДНК и/или мРНК sgk1 в строгих условиях. В этом способе наиболее предпочтительно указанные субстанции используют для обнаружения определенных мутаций, прежде всего нуклеотидного полиморфизма и/или инсерций в sgk1, где эти определенные мутации связаны с повышенной экспрессией и/или функцией или активностью sgk1. Подлежащими диагностике заболеваниями являются, например, заболевания, связанные с нарушенной коагулирующей способностью крови, или сосудистые заболевания, такие как легочная гипертензия или артериосклероз.
Кроме того, под объем изобретения подпадает фармацевтическая композиция, содержащая по меньшей мере одно действующее вещество, которое оказывает влияние на экспрессию и/или функцию sgk1, прежде всего ингибирует и/или активирует ее, и предпочтительно при необходимости фармацевтический носитель. При этом действующее вещество может представлять собой ингибитор киназ, такой как уже упомянутые выше ингибиторы стауроспорин, хелеритрин, SB 203580 и SB202190 или их аналоги, или также другие субстанции. Кроме того, действующее вещество может представлять собой полинуклеотид, кодирующий пептид, предпочтительно полипептид, где этот пептид оказывает влияние на экспрессию sgk1, предпочтительно ингибирует или активирует ее. Примером полипептида, предлагаемого в изобретении, может служить так называемый мутант с дефицитом киназной активности. Специалисту в данной области хорошо известны другие примеры методов, позволяющих оказывать влияние на экспрессию и/или функцию с помощью генетически измененных вариантов белка-мишени, и они описаны в целом ряде учебников/справочников, а также в руководствах для лабораторных исследований (см., например, Maniatis Т., Fritsch E.F., Sambrook J., изд-во Cold Spring Harbor Laboratory, Cold Spring Harbor, NY, 1996; Leonard G., Davis Ph.D., Michael W., Kuehl Md., James F., Battey M.D., изд-во McGraw-Hill Professional Publishing, 1995). Кроме того, действующее вещество, предлагаемое в изобретении, может представлять собой так называемое «низкомолекулярное соединение», предпочтительно «низкомолекулярное соединение», имеющее молекулярную массу (ММ)<1000. Кроме того, действующее вещество может представлять собой так называемую антисмысловую последовательность, т.е. последовательность, которая обладает способностью образовывать двухцепочечный дуплекс с мРНК и тем самым ингибировать трансляцию полипептида-мишени. Для достижения сверхэкспрессии можно также использовать последовательность самой sgk1, например, путем встраивания последовательности в векторы или плазмиды, при этом можно также предварительно модифицировать последовательность-мишень молекулами-«носителями», например промоторами. Другие отличительные признаки такой композиции представлены выше в соответствующем разделе описания.
Наконец, под объем изобретения подпадает фармацевтическая композиция, содержащая эффективное количество по меньшей мере одного действующего вещества, которое оказывает влияние, прежде всего ингибирует или активирует экспрессию и/или функцию активаторов, ингибиторов, регуляторов и/или биологических предшественников sgk1. Эта фармацевтическая композиция при необходимости предпочтительно может содержать также фармацевтический носитель. Такие активаторы, ингибиторы, регуляторы и/или биологические предшественники sgk1 могут представлять собой, например, другие киназы, которые участвуют в регуляции активности sgk1, факторы транскрипции, которые играют роль в уровне экспрессии sgk1, а также другие известные или в настоящее время еще неописанные представители семейства sgk1, участвующие в каскаде трансдукции, и уже описанные выше молекулы. В такой композиции могут присутствовать также полинуклеотиды, кодирующие пептид, который оказывает влияние, предпочтительно ингибирует или активирует экспрессию активаторов, ингибиторов, регуляторов и/или биологических предшественников sgk1. Можно использовать также так называемые «низкомолекулярные соединения», которые предпочтительно имеют молекулярную массу (ММ)<1000 и направлены против активаторов, ингибиторов, регуляторов и/или биологических предшественников sgk1 и при этом ингибируют или активируют экспрессию или функцию этой киназы. Другие отличительные признаки таких действующих веществ представлены выше в соответствующем разделе описания.
Указанные и другие отличительные признаки изобретения представлены в приведенном ниже описании предпочтительных вариантов осуществления изобретения в сочетании с зависимыми пунктами формулы изобретения и чертежами. При этом индивидуальные отличительные признаки в каждом случае можно реализовывать по отдельности или в сочетании друг с другом.
На чертежах показано:
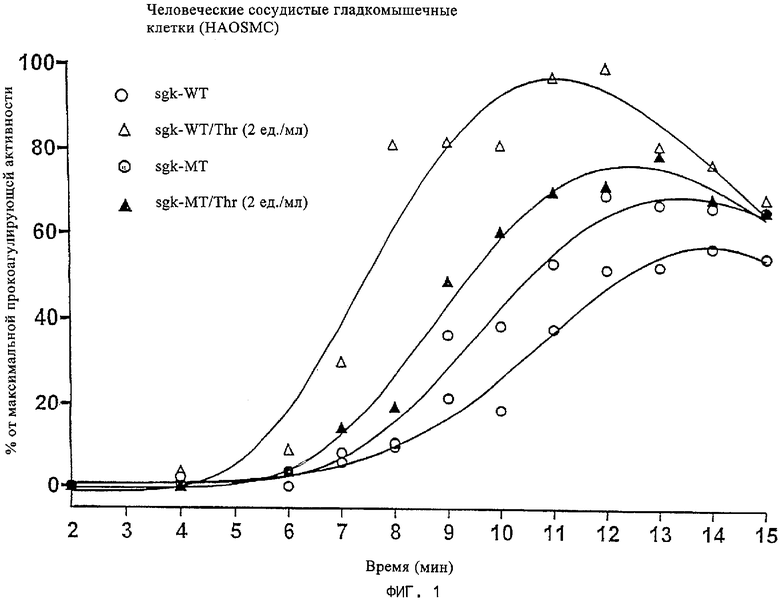
на фиг.1 - стимуляция прокоагулирующей активности сосудистых гладкомышечных клеток;
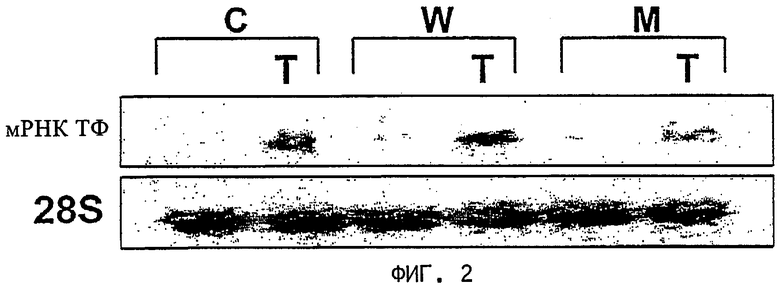
на фиг.2 - регуляция с помощью sgk тканевого фактора в человеческих сосудистых гладкомышечных клетках (Нозерн-блоттинг). Т: тромбин (3 ед./мл), 4 ч; С: контроль; W: sgk дикого типа; М: мутантная sgk.
Эксперимент
На фиг.1 представлена зависимость от времени прокоагулирующей активности в % от максимального значения после рекальцификации. В эксперименте, результаты которого представлены на фиг.1, прокоагулирующую активность человеческих сосудистых гладкомышечных клеток (HAOSMC) оценивали путем измерения образования тромбина в процессе коагуляции в рекальцифицированной тромбоцитопенической (РРР) крови (Beguin S., Lidhout Т., Hemker Н.С., Throm. Haemost., 61, 1998, cc.25-29). Для этого конфлюэнтные сосудистые гладкомышечные клетки выдерживали в течение 24 ч в бессывороточной среде, затем трижды промывали смесью HEPES-раствор Тироде, после чего инкубировали с человеческой РРР. Образование тромбина индуцировали путем добавления к среде для инкубации 16,7 мМ CaCl2. В каждом случае через каждые одну-две минуты отбирали 20 мкл супернатанта и определяли образование тромбина в выделенном объеме с помощью красителя S-2238 (фирма Haemachrom Diagnostica). Оптическую плотность определяли при 405 нм с помощью спектрофотометра (типа Uvicon, фирма Control Instruments). Зависимость поверхностной прокоагулирующей активности гладкомышечных клеток от доступности связанного с мембраной тканевого фактора демонстрировали с использованием нейтрализующих антител к человеческому тканевому фактору (МАт №4508, фирма American Diagnostica, 10 мкг/мл за 20 мин до рекальцификации РРР).
Как показано на фиг.1, прокоагулирующая активность человеческих сосудистых гладкомышечных клеток возрастала через несколько минут после добавления CaCl2. При экспрессии инактивированной киназы (sgk-MT) это увеличение происходило медленнее, чем при экспрессии нормальной киназы (sgk-WT). Как ожидалось, дополнительное введение тромбина (Thr) приводило к более быстрому возрастанию прокоагулирующей активности. При этом действие было более выраженным и быстрым в клетках, которые экспрессировали интактную киназу по сравнению с клетками, которые экспрессировали инактивированный мутант. В каждый момент времени клетки, которые экспрессировали интактную (дикого типа) киназу sgk-WT, характеризовались более высокой прокоагулирующей активностью, чем клетки, которые экспрессировали инактивированную мутантную sgk (sgk-MT), независимо от того, добавляли тромбин (sgk-WT/Thr и соответственно sgk-MT/Thr) или нет.
Эти результаты однозначно свидетельствуют о том, что сверхэкспрессия интактной sgk1 в сосудистых гладкомышечных клетках приводит к повышению коагулирующей активности. Наряду с известной важной ролью, которую ТФ играет в различных клеточных процессах, этот результат демонстрирует также, что гиперактивность sgk1 в сочетании с увеличением экспрессии тканевого фактора на клеточной мембране может стимулировать коагулирующую способность крови, что делает возможным прилипание опухолевых клеток с последующим метастазированием, а также усиливать ангиогенез. И, наоборот, этот механизм можно ингибировать путем ингибирования экспрессии sgk1 или путем подавления sgk1 фармакологическими средствами.
На фиг.2 представлены результаты Нозерн-блоттинга мРНК тканевого фактора (мРНК ТФ) контрольных клеток, несущих контрольную плазмиду (С: контроль), клеток, содержащих трансфектированную активную киназу (W: sgk дикого типа), и клеток, содержащих трансфектированную инактивированную киназу (М: мутантная sgk). Клетки представляли собой такие же человеческие сосудистые гладкомышечные клетки, что и в описанном выше эксперименте. В качестве внутреннего стандарта вносили 28S-рРНК. В качестве зонда использовали кДНК человеческого ТФ. В каждом случае клетки выдерживали в течение 4 ч без добавления и с добавлением тромбина (3 ед./мл). Результаты Нозерн-блоттинга свидетельствуют о том, что после обработки тромбином транскрипция мРНК тканевого фактора усиливалась в клетках, содержащих активную sgk (W), по сравнению с контрольными клетками, при этом транскрипция в клетках, содержащих инактивированную мутантную sgk, понижалась. Это однозначно свидетельствует о том, что sgk регулирует экспрессию тканевого фактора в человеческих сосудистых гладкомышечных клетках.
Изобретение относится к области биотехнологии. Предложено применение антитела к sgk1, такого, с помощью которого обнаруживается изменение экспрессии и/или функции sgk1 в эукариотических клетках, для диагностики заболеваний, связанных с нарушенной активностью тканевого фактора. Раскрыты способ диагностики указанных заболеваний и диагностический набор для выявления указанных заболеваний на основе антитела для диагностики заболеваний, связанных с нарушенной активностью тканевого фактора. Использование изобретения позволяет определять по изменению экспрессии sgk1 изменение экпрессии тканевого фактора, что может найти применение в медицине для диагностики заболеваний, связанных с нарушенной активностью тканевого фактора. 3 н. и 9 з.п. ф-лы, 2 ил.
| DE 19917990 А, 02.11.2000 | |||
| РОТОРНАЯ ГИДРОМАШИНА | 1994 |
|
RU2074987C1 |
| US 5242397 A, 07.09.1993 | |||
| WEBSTER et al | |||
| Characterization of SGK, a novel member of the serine/threonine protein kinase gene family which is trancriptionally induced by glucocorticoids and serum, molecular and cellular biology | |||
| - Washington, DC, US, vol.13, no.4, 1993, с.2031-2040 | |||
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА, ОБЛАДАЮЩЕГО ОПОСРЕДОВАННОЙ ФАКТОРОМ VII АКТИВНОСТЬЮ В СВЕРТЫВАНИИ КРОВИ | 1986 |
|
RU2122583C1 |
Авторы
Даты
2008-08-10—Публикация
2003-03-03—Подача