Изобретение относится к медицинской технике, а именно к многофункциональным биосовместимым наноструктурным пленкам, используемым в качестве модифицирующих пленок при изготовлении имплантатов, работающих под нагрузкой: ортопедические и стоматологические протезы, зубные коронки, имплантаты, используемые в челюстно-лицевой хирургии, искусственные сочленения, фиксаторы и др. Эти материалы должны обладать высокой твердостью, усталостной прочностью, износо- и коррозионной стойкостью, биосовместимостью и отсутствием токсичности.
Известен медицинский имплантат, покрытый аморфным слоем гидроксилапатита и титана, который имеет повышенную прочность соединения пленки с субстратом и низкую скорость растворения материала пленки. Имплантат состоит из субстрата и пленки, осажденного на поверхность субстрата из композиционной мишени, содержащей 10-75% титана и 90-25% гидроксилапатита (US 6344427, опублик. 5.02.02).
Способ производства такого имплантата включает следующие этапы: производство субстрата, производство композиционной мишени, состоящей на 10-70% по объему из титана и на 90-25% по объему из гидроксилапатита; нанесение на субстрат с помощью композиционной мишени поверхностной пленки методом ионного распыления, лазерного удаления или физического метода парового нанесения.
Однако данное покрытие не может быть использовано для имплантатов, работающих под нагрузкой (дентальных имплантатов, имплантатов для восстановительной и костно-пластической хирургии лицевого скелета, артрохирургии, имплантатов для фиксации шейного и поясничного отделов позвоночника, и др.), из-за низких значений механических и трибологических свойств.
Известен низкомодульный сплав, содержащий ниобий, тантал и не менее одного металла из группы, в состав которой входят цирконий, вольфрам и молибден. Изготовленные из данного сплава медицинские материалы обладают высокими функциональными характеристиками, являются биологически совместимыми, рентгеноконтрастными и пригодны для использования с магниторезонансной системой визуализации (ЕР 1444993, опублик. 11.08.04).
Однако данный биосовместимый сплав имеет низкую биоактивность, т.е. недостаточную скорость и степень остеоинтеграции имплантата в тканевую среду, а ниобий может вызывать токсические реакции.
Известен композиционный материал (RU 2227011, опублик. 20.04.04), включающий апатит в количестве ниже 90 об.%, предпочтительно 5-80 об.%, еще более предпочтительно 10-50 об.% и наиболее предпочтительно 25-45 об.%. Фаза апатита может быть чистым гидроксилапатитом или смесями фаз апатита, то есть гидроксилапатита и фторапатита. Основная биологически инертная масса в композиционном материале предпочтительно является конструкционной керамикой, предпочтительно одним или более оксидом, например, оксидом алюминия, оксидом циркония и/или оксидом титана. Основная биологически инертная масса может представлять собой конструкционный металл, предпочтительно на основе Fe или Со-Cr, или же конструкционный металл на основе Ti, Та или Zr. Содержание конструкционного металла может составлять 10-95 об.%, предпочтительно 40-95 об.% и более предпочтительно 55-85 об.%, и, соответственно, преобладать в материале. Кроме апатита и основной биологически инертной массы основы могут также присутствовать низкие содержания (предпочтительно ниже 10 об.%) других фаз.
Однако данный композиционный материал не является наноструктурным покрытием и не обладает всем комплексом служебных свойств, необходимых для имплантатов, работающих под нагрузкой, а именно высокими значениями биосовместимости, биоактивности, коррозионной стойкости в биологических средах, усталостной и разрывной прочностью, износостойкостью и низкими значениями модуля упругости и коэффициента трения.
Прототипом заявленного изобретения является биосовместимые многокомпонентные наноструктурные пленки для имплантатов (RU 2281122, 10.08.06), работающих под нагрузкой, на основе карбонитрида титана с введением дополнительных элементов, улучшающих механические и трибологические свойства пленки, а также обеспечивающих его биоактивность, биосовместимость и нетоксичность, при определенном соотношении суммарных концентраций основных и дополнительных элементов. При этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат.%: Ti 30-50, С 15-40, N 0.5-30, O 5-25, Са 0-7, Zr 0-20, Si 0-30, P 0-1.5, Mn 0-1.0, К 0-1.0
В изобретении достигается технический результат, заключающийся в создании многофункциональных биосовместимых наноструктурных пленок, обладающих по сравнению с прототипом более высокими пассивационными характеристиками и более низкой скоростью коррозии. Повышенная коррозионная стойкость пленок, в первую очередь, определяется танталом. Кроме того, пленки обладают повышенной твердостью, низким модулем упругости, высокой адгезионной прочностью, низким коэффициентом трения и скоростью износа как на воздухе, так и в различных физиологических средах, высокой стойкостью к упругой деформации разрушения и пластической деформации, низкой шероховатостью поверхности, отрицательным зарядом поверхности при кислотности среды (4,5<рН<9), повышенной биоактивностью; биосовместимостью и отсутствием токсичности. Указанный технический результат достигается следующим образом.
Биосовместимые многокомпонентные наноструктурные пленки для имплантатов, работающих под нагрузкой, выполнены на основе карбонитрида титана с введением дополнительных элементов, улучшающих механические и трибологические свойства пленки, а также обеспечивающих его биоактивность, биосовместимость и нетоксичность. Суммарные концентрации основных и дополнительных элементов в покрытии имеют следующее соотношение:
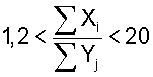
где Xi - суммарная концентрация основных элементов Ti, Та, С, N в покрытии,
Yj - суммарная концентрация дополнительных элементов Са, Zr, Si, К, Mn, О, Р в покрытии.
Концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат.%:
Ti - 30-50
Та - 6-50
С - 15-40
N - 0-35
O - 5-25
Са - 0-7
Zr - 0-20
Si - 0-30
Р - 0-1.5
Mn - 0-1.0
К - 0-1.0
Высокий комплекс физических, химических, механических, трибологических и биологических свойств пленок по изобретению достигается за счет включения в состав пленок компонентов в количественных соотношениях, указанных выше.
Карбонитрид титана обладает высокой твердостью, износо- и коррозионной стойкостью.
Осаждение пленок в среде аргона приводит к формированию грубой столбчатой структуры с повышенной пористостью. Содержание в составе пленки азота приводит к измельчению и уплотнению структуры, а в отдельных случаях и к полному подавлению колонной структуры. Размер кристаллитов, как правило, не превышает 20 нм. Шероховатость пленок снижается при введении азота в состав пленки.
Оптимальным является отношение металлических (Me) к неметаллическим элементам (NMe) Me/NMe=1.0-1.7, при котором пленки имели кубическую структуру типа NaCl.
При этом введение в состав пленок дополнительного элемента - тантала в количестве 6-50% положительно сказывается на всем комплексе механических, химических, трибологических и биологических свойств за счет образования комплексного карбонитрида титана и тантала (Ti,Ta)CxNy. Растворение тантала в карбиде (карбонитриде) титана приводит к росту микротвердости и коррозионной стойкости. Уникальное преимущество карбонитрида тантала TaCxNy состоит в том, что он более химически стабилен и биоактивен по сравнению с другими известными двойными карбидами и нитридами. Биосовместимые пленки с танталом имеют значения параметров Н/Е, описывающего сопротивление упругой деформации разрушения и Н3/Е2, описывающего сопротивление пластической деформации, соответственно, 0.1-0.15 и 0.5-0.9 ГПа, что значительно выше, чем у металлов, сплавов и керамики, используемых в качестве ортопедических и дентальных имплантатов. Пленки показали стабильно низкий коэффициент трения в интервале 0.17-0.22 (на воздухе) и 0.24-0.25 (в физиологическом растворе). Пленки, легированные танталом, имеют пассивационные характеристики выше, а скорости коррозии ниже, чем у пленок аналогичного состава, но без тантала, они обладают также повышенной биоактивностью, биосовместимостью и отсутствием токсичности.
При концентрации тантала в пленках менее 6% не наблюдается их количественных преимуществ по сравнению с прототипом из-за малого содержания комплексного карбонитрида (Ti,Ta)CxNy. При концентрации тантала более 50% возрастают остаточные напряжения в пленках, что приводит к отслоению пленки от подложки-имплантата.
Образование слоя апатита связывается с формированием гидроксилфункциональных групп на отрицательно заряженной поверхности биоактивной керамики во внутренней среде организма. Для этого в пленку вводятся такие элементы, как Са, Р и О в заявляемом количестве. Наличие ионов кальция стимулирует рост клеток на поверхности имплантата. Увеличение содержания Са, Р и О свыше заявляемого количества приводит к снижению механических и трибологических свойств пленок, а также к разрушению актинового цитоскелета клеток и ухудшению адгезионных свойств поверхности (таблица 1).
Во всем исследованном диапазоне значений рН (4,5<рН<9) поверхность пленок имеет отрицательный заряд. Пленки с азотом, как правило, имеют более отрицательный заряд поверхности. Это означает, что поверхность пленок может притягивать положительно заряженные ионы Са2+, которые находятся во внутренней среде организма, что способствует образованию сначала промежуточных, кальцийсодержащих фаз, а затем слоя гидроксиапатита, который является устойчивой фазой в физиологической среде.
Введение в пленку элементов Са, Zr и О приводит к существенному снижению коэффициента трения до 0.17-0.25 по сравнению с пленкими на основе карбида (0.85) или нитрида (0.55) титана.
Прикрепление клеток к поверхности имплантата определяется образованием интегрин-опосредованных фокальных контактов клеток с подлежащей поверхностью. Добавка Mn в количестве <1 ат.% приводит к активации интегринов и улучшению адгезии клеток. Дальнейшее увеличение содержания Mn приводит к снижению механических свойств пленок и уменьшению распластывания и размножения клеток. Кремний способствует увеличению активности остеобластов и образованию слоя апатита. При его содержании менее 30 ат.% пленки обладают однофазной гранецентрированной кубической структурой типа NaCl, что благоприятно сказывается на механических и трибологических свойствах.
Композиционные мишени и электроды могут быть получены методом самораспространяющегося высокотемпературного синтеза (СВС). В отличие от других известных методов получения композиционных катодов из тугоплавких соединений (прессование-спекание, газостатическое прессование, газотермическое напыление и др.) технология СВС имеет следующие преимущества: самоочистка продуктов горения от вредных растворимых и адсорбированных примесей в результате достижения высоких значений температуры (2500-3000°С) и скорости горения (2-10 см/с), развиваемых в волне горения СВС-систем; достижение высоких значений относительной плотности (97-99%) керамических материалов и тугоплавких соединений при сравнительно низких давлениях прессования; получение метастабильных состояний - пересыщенных твердых растворов; получение функциональных градиентных материалов (Левашов Е.А., Рогачев А.С., Юхвид В.И., Боровинская И.П. Физико-химические и технологические основы самораспространяющегося высокотемпературного синтеза, М., БИНОМ, 1999, 174 с.).
При этом неорганические добавки, например, гидроксилапатит (Са10(PO4)6(ОН)2), CaO, ZrO2, KMnO4 и TiO2 и др. могут вводиться на этапе получения композиционных катодов-мишеней для ионно-плазменного и/или ионно-лучевого распыления и электродов для электроискрового осаждения.
Основным технологическим преимуществом материала пленок по изобретению является наличие целого комплекса свойств, необходимых для модифицирования поверхности имплантатов, работающих под нагрузкой:
- высокая твердость Н=20-40 ГПа;
- низкий модуль упругости Е=150-300 ГПа;
- высокая адгезия пленки к подложке, измеряемая величиной критической нагрузки Lc - более 40 Н;
- низкий коэффициент трения в паре с Al2О3 в физиологических средах μ=0.1-0.25;
- низкая скорость износа Vw - менее 10-5 мм3/Нм;
- высокая стойкость к упругой деформации разрушения и пластической деформации 0.5<H3/E2<0.9 ГПа;
- отрицательный заряд поверхности в физиологических средах;
- наличие потенциала коррозии положительное - 0.2 В при проведении электрохимических испытаний согласно ГОСТ Р ИСО 10993-15-2001;
- скорость коррозии менее 0.05 мкм/год в различных биологических средах;
- контактный угол смачивания <90°;
- отсутствие разрушения актинового цитоскелета клеток при наличии биоактивности поверхности, биосовместимости и отсутствии токсичности.
Отклонение хотя бы по одному из приведенных выше свойств пленок влечет за собой ухудшение служебных характеристик всего изделия (имплантата) в целом.
Низкий модуль упругости пленок благоприятен с точки зрения уменьшения напряжений между покрытием и имплантатом, в качестве которого часто используется нержавеющая сталь Е=190-200 ГПа или титан Е=116 ГПа. Низкий модуль Юнга также приводит к лучшему переносу костью функциональных нагрузок и стимулирует нарастание костной ткани. Комбинация высокой твердости и упругого восстановления характеризует предложенные биосовместимые пленки как новый уникальный твердый, и в тоже время упругий материал, что является важнейшим фактором для материалов медицинского назначения, работающих под нагрузкой.
Изобретение осуществляют следующим образом.
Пример 1.
Технологический цикл получения предложенных биосовместимых пленок Ti-Ta-Ca-P-C-O-N состоит из двух основных стадий: получение композиционной мишени (Ti,Та)Сх+Са3(PO4)2, например методом самораспространяющегося высокотемпературного синтеза (СВС), и ее последующее магнетронное распыление на подложку.
Осаждение пленки Ti-Ta-Ca-P-C-O-N осуществляли в газовой смеси аргона с азотом Ar+N2 при парциальном давлении азота, равном 14%. В результате получено покрытие следующего состава, ат.%:
C - 26.0
O - 11.3
N - 6.0
Ca - 1.3
P - 0.6
Ti - 46.0
Ta - 8.8
Для измерения физико-механических и трибологических свойств пленки осаждались на подложки из титанового сплава марки ВТ 1-0, никелевого сплава Целит-Н, кобальтового сплава Целит-К, а также никелида титана.
Физико-механические и трибологические свойства пленок определялись при использовании следующих высокопрецизионных приборов: Нанотвердомер (Nano-Hardness Tester, CSM Instruments, Швейцария); Скратч-тестер (Revetest, CSM Instruments, Швейцария); Машина трения (Tribometer, CSM Instruments, Швейцария); Сканирующий силовой микроскоп, оборудованный модулем для измерения твердости материалов по методу склерометрии с помощью игл из ультратвердого фуллерита С60 (NanoScan, Россия); Оптический микроскоп AXIOVERT, оборудованный цифровой камерой и системой анализа изображения (Карл Цейс, Германия). Твердость и модуль упругости определялись по методу Оливера и Фара [G.M. Pharr, W.C. Oliver, F.R. Brotzen. J. Mater. Res. 3, 613 (1992)] с использованием индентора Берковича. Величину упругого восстановления (We) пленок рассчитывали по кривым нагружение-разгрузка по формуле: We=(hmax-hr)/hmax, где hmax - максимальная глубина проникновения индентора, a hr - остаточная глубина после снятия нагрузки. Коэффициент трения и скорость износа пленок измерялись с помощью машины трения по схеме "шарик-диск" при нагрузке 1 N и линейной скорости 10 см/с. Испытания проводились в физиологическом растворе (100 мл H2O + 0.9 г NaCl). В качестве контртела использовался неподвижный шарик из спеченного Al2О3 диаметром 3 мм.
Полученное покрытие имело твердость 39 ГПа, модуль упругости 330 ГПа, упругое восстановление 70%, коэффициент трения и скорость износа в физиологическом растворе соответственно 0.24 и 7×10-7 мм3/Н м.
Разрушения актинового цитоскелета клеток не обнаружено. Крысиные фибробласты Rat-1 и эпителиоциты IAR-2 рассеивали на поверхность пленок, осажденных на стекла. Клетки инкубировали 24, 48 и 72 часа при температуре 37°С. Стекла фиксировали в 3.7% параформальдегиде на фосфатном буфере в течение 10 мин, после чего окрашивали гема-токсилином и заключали в смесь глицерина с фосфатным буфером. С помощью световой микроскопии подсчитывали количество клеток в поле зрения. Клетки распластывались и размножались одинаково хорошо как на контрольных стеклах, так и на тестируемых пленких, что свидетельствует о том, что пленки адгезионны и нетоксичны для клеток.
Эксперименты in vivo проводились на мышах. Образцы из тефлона с осажденными на них пленкими вводились под кожу мышей. Через 16 недель имплантат с образовавшейся вокруг него капсулой извлекали и исследовали на биосовместимость. Результаты исследований показали отсутствие воспалительной реакции внутри капсулы, а клетки тканей плотно прилегали к поверхности пленок.
Пример 2.
Осаждение пленок осуществляли путем магнетронного распыления композиционной СВС мишени (Ti,Ta)Cx+CaO в атмосфере аргона. Получено покрытие следующего состава, ат.%:
С-34.2
0-15.0
N-0.1
Ti-40.6
Та-7.9
Са-2.1
Полученное покрытие имело твердость 40 ГПа, модуль упругости 340 ГПа, упругое восстановление 72% и коэффициент трения в физиологическом растворе 0.24.
Разрушения актинового цитоскелета клеток не обнаружено. Исследования in vitro и in vivo показали, что покрытие Ti-Ca-C-O-N является биосовместимым, биоактивным, не токсичным, не вызывает воспалительной реакции при его имплантации под кожу мышей. Клетки фибробластов и эпителиоцитов хорошо размножались и обладали высокой адгезией к поверхности пленки.
Примеры 3-16.
Для оптимизации состава пленок были проведены многочисленные эксперименты по получению катодов-мишеней различных составов и осаждению пленок по технологии магнетронного распыления. В таблице 1 в обобщенном виде представлены результаты исследований и свойства пленок, подтверждающие правомерность заявляемых составов.
Пленки предложенного состава обладают несколькими конкурентными преимуществами, необходимыми для материалов имплантатов, работающих под нагрузкой: высокой твердостью; низким модулем упругости; высокой адгезией; низким коэффициентом трения и скоростью износа; высокой стойкостью к упругой деформации разрушения и пластической деформации; низкой шероховатостью поверхности; отрицательным зарядом поверхности в физиологических средах (4,5<рН<9); биоактивной поверхностью; биосовместимостью и отсутствием токсичности.
Элементный состав и свойства пленок
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОСОВМЕСТИМЫЕ МНОГОКОМПОНЕНТНЫЕ НАНОСТРУКТУРНЫЕ ПОКРЫТИЯ ДЛЯ МЕДИЦИНЫ | 2005 |
|
RU2281122C1 |
| МНОГОКОМПОНЕНТНОЕ БИОАКТИВНОЕ НАНОКОМПОЗИЦИОННОЕ ПОКРЫТИЕ С АНТИБАКТЕРИАЛЬНЫМ ЭФФЕКТОМ | 2013 |
|
RU2524654C1 |
| Многокомпонентный двухслойный биоактивный материал с контролируемым антибактериальным эффектом | 2019 |
|
RU2697720C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОАКТИВНОГО ПОКРЫТИЯ С АНТИБАКТЕРИАЛЬНЫМ ЭФФЕКТОМ | 2014 |
|
RU2580627C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОАКТИВНОГО ПОКРЫТИЯ С АНТИБАКТЕРИАЛЬНЫМ ЭФФЕКТОМ | 2014 |
|
RU2580628C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИМПЛАНТАЦИОННОГО МАТЕРИАЛА НА ОСНОВЕ ПОРИСТОГО ПОЛИТЕТРАФТОРЭТИЛЕНА И МАТЕРИАЛ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2007 |
|
RU2325191C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО СТОМАТОЛОГИЧЕСКОГО ИМПЛАНТАТА С УГЛЕРОДНЫМ НАНОПОКРЫТИЕМ | 2014 |
|
RU2571559C1 |
| ПСЕВДОУПРУГИЙ БИОСОВМЕСТИМЫЙ ФУНКЦИОНАЛЬНО-ГРАДИЕНТНЫЙ МАТЕРИАЛ ДЛЯ КОСТНЫХ ИМПЛАНТОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2302261C1 |
| Способ получения многослойных металлокерамических покрытий на поверхности эндопротезов | 2021 |
|
RU2790959C1 |
| БИОИМПЛАНТАТ С МНОГОФУНКЦИОНАЛЬНЫМ БИОАКТИВНЫМ НАНОСТРУКТУРИРОВАННЫМ ПОКРЫТИЕМ | 2012 |
|
RU2482882C1 |
Изобретение относится к медицинской технике. Изобретение касается биосовместимых износостойких наноструктурных тонкопленочных материалов на основе карбонитрида титана, используемых в качестве пленок при изготовлении имплантатов, работающих под нагрузкой». Суммарные концентрации основных и дополнительных элементов в покрытии имеют следующее соотношение:
 где Xi - суммарная концентрация основных элементов Ti, Та, С, N в покрытии, Yj - суммарная концентрация дополнительных элементов Са, Zr, Si, К, Mn, О, Р в покрытии, при этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат.%: Ti - 30-50; Та - 6-50; С - 15-40; N - 0-35; О - 5-25; Са - 0-7; Zr - 0-20; Si - 0-30; Р - 0-1.5; Mn - 0-1.0; К - 0-1.0. Заявленное пленочное покрытие обладает высокой твердостью; низким модулем упругости; высокой прочностью сцепления с подложкой; низким коэффициентом трения и скоростью износа; высокой стойкостью к упругой деформации разрушения и пластической деформации; низкой шероховатостью поверхности; отрицательным зарядом поверхности в физиологических средах (4,5<рН<9); биоактивной поверхностью; биосовместимостью и отсутствием токсичности. 1 табл.
где Xi - суммарная концентрация основных элементов Ti, Та, С, N в покрытии, Yj - суммарная концентрация дополнительных элементов Са, Zr, Si, К, Mn, О, Р в покрытии, при этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат.%: Ti - 30-50; Та - 6-50; С - 15-40; N - 0-35; О - 5-25; Са - 0-7; Zr - 0-20; Si - 0-30; Р - 0-1.5; Mn - 0-1.0; К - 0-1.0. Заявленное пленочное покрытие обладает высокой твердостью; низким модулем упругости; высокой прочностью сцепления с подложкой; низким коэффициентом трения и скоростью износа; высокой стойкостью к упругой деформации разрушения и пластической деформации; низкой шероховатостью поверхности; отрицательным зарядом поверхности в физиологических средах (4,5<рН<9); биоактивной поверхностью; биосовместимостью и отсутствием токсичности. 1 табл.
Биосовместимые многокомпонентные наноструктурные пленки для имплантатов, работающих под нагрузкой, на основе карбонитрида титана с введением дополнительных элементов, улучшающих механические и трибологические свойства пленки, а также обеспечивающих его биоактивность, биосовместимость и нетоксичность, при следующем соотношении суммарных концентраций основных и дополнительных элементов:

где Xi - суммарная концентрация основных элементов Ti, Та, С, N в покрытии,
Yj - суммарная концентрация дополнительных элементов Са, Zr, Si, К, Mn, О, Р в покрытии, при этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат%:
| БИОСОВМЕСТИМЫЕ МНОГОКОМПОНЕНТНЫЕ НАНОСТРУКТУРНЫЕ ПОКРЫТИЯ ДЛЯ МЕДИЦИНЫ | 2005 |
|
RU2281122C1 |
| СПЕЧЕННЫЙ ТВЕРДЫЙ СПЛАВ НА ОСНОВЕ КАРБОНИТРИДА ТУГОПЛАВКОГО МЕТАЛЛА | 1991 |
|
RU2040572C1 |
| КЕРМЕТ, СОДЕРЖАЩИЙ СВЯЗУЮЩЕЕ С ПОВЫШЕННОЙ ПЛАСТИЧНОСТЬЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2212464C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТВЕРДОГО СПЛАВА НА ОСНОВЕ КАРБИДА ВОЛЬФРАМА И СЛОЖНОГО КАРБОНИТРИДА ТИТАНА-ТАНТАЛА-ВОЛЬФРАМА | 2004 |
|
RU2270737C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВОГО ПРОДУКТА ИЗ СОИ | 1995 |
|
RU2081618C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ КОМПОЗИЦИОННЫЙ МАТЕРИАЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2227011C2 |
| EP 1444993 B1, 11.08.2004 | |||
| US 6344427 A, 05.02.2002. | |||
Авторы
Даты
2008-09-10—Публикация
2007-04-16—Подача