Изобретение относится к химической промышленности, а именно к получению нового производного димеризованной жирной кислоты - ее тетрааминодиамида-4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида, который может быть использован в качестве отвердителя и пластификатора эпоксидных композиций, предназначенных для склеивания и герметизации различных материалов в промышленности и быту.
Димеризованная жирная кислота (4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-диоктановая кислота) представляет собой продукт термической полимеризации непредельных жирных кислот (C18), выделенных из природных растительных масел (таллового, льняного, соевого, тунгового) [Сорокин М.Ф., Кочнова З.А., Шодэ Л.Г. Химия и технология пленкообразующих веществ. М.: Химия, 1989, 480 с.].
Особые физико-химические характеристики димеризованной жирной кислоты обеспечивают эластичность, адгезионные свойства, водо- и химстойкость ее производных, что позволяет широко использовать их в качестве клеев-расплавов, отвердителей и модификаторов эпоксидных и фенолформальдегидных смол, а также в составе покрытий, лаков и красителей.
Известны производные димеризованной жирной кислоты, представляющие собой:
- полиамиды, используемые как клеи-расплавы [заявка ФРГ №4408276, С08L 77/08, опубл. 14.09.95 заявка ФРГ №4408277, С09J 177/00, опубл. 14.09.95];
- олигоаминоамиды и имидазолины, используемые как отвердители и модификаторы эпоксидных и фенолформальдегидных смол [Бобылев В.А. // Композитный мир. 2006. №4. С.20-24];
- олигоамиды, используемые в составе покрытий, лаков и красителей [Попова Т.А., Жилина Н.В., Родивилова Л.А. и др. Производство олигоамидов за рубежом. Обзорн. инф. Сер. «Пластические массы и синтетические смолы». М.: НИИТЭХИМ, 1979, 32 с].
Изобретательская задача состояла в поиске нового соединения, являющегося производным димеризованной жирной кислоты, которое при использовании его, например, в качестве отвердителя и пластификатора эпоксидных смол, позволило бы получить эпоксидные композиции, не содержащие модифицирующих добавок и обладающие при этом высокими технологическими и физико-химическими свойствами.
Поставленная задача решена 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]- дигептанамидом формулы
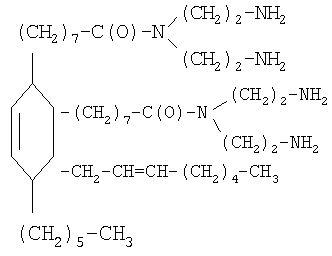
4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамид представляет собой вязкую жидкость золотистого цвета; полученный из 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-(метилизобутилимино)-этил]-дигептанамида он характеризуется аминным числом 238,0 мг КОН/г продукта; кислотным числом 3,0 мг КОН/г продукта; 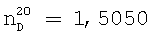 ;
; 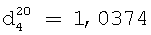 ; полученный из 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-циклогексанимино)этил]-дигептанамида характеризуется аминным числом 240,0 мг КОН/г продукта; кислотным числом 2,80 мг КОН/г продукта;
; полученный из 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-циклогексанимино)этил]-дигептанамида характеризуется аминным числом 240,0 мг КОН/г продукта; кислотным числом 2,80 мг КОН/г продукта; 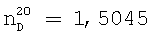 ;
; 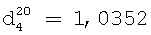 .
.
Структура 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди (2-аминоэтил)]-дигептанамида доказана данными элементного анализа, ИК и ЯМР спектроскопии.
Изобретение позволяет получить следующие преимущества: использование 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида в качестве отвердителя эпоксидной смолы способствует получению нелетучих двухкомпонентных клеевых композиций, характеризующихся хорошими смачивающими свойствами и высокой адгезионной прочностью. Кроме того, благодаря внутримолекулярной пластификации, обусловленной наличием объемных алкильных заместителей, отвержденные эпоксидные композиции обладают выраженной гибкостью и ударопрочностью.
Заявляемое новое производное димеризованной жирной кислоты получено следующим способом.
Для реализации способа используют следующие вещества: димеризованная жирная кислота «Pripol 1013» (получена полимеризацией линолевой кислоты; содержание димеров не менее 97%) - CAS №61788-89-4
Способ реализуется в четыре стадии:
1. Синтез дихлорангидрида димеризованной жирной кислоты по схеме:
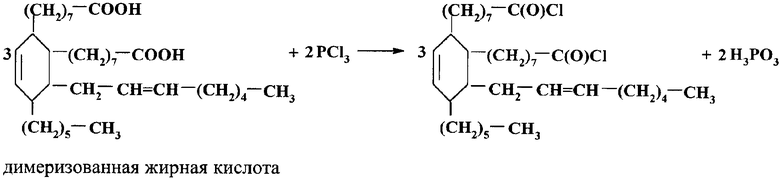
димеризованная жирная кислота
В колбу, снабженную холодильником и капельной воронкой с хлоркальциевыми трубками, помещают 290 г (0,52 моль) димеризованной жирной кислоты и по каплям в течение 40 минут добавляют 52,6 мл (0,6 моль) треххлористого фосфора. Нагревают реакционную смесь до 50°С и выдерживают при этой температуре 3 часа, после чего оставляют на ночь при комнатной температуре. В смесь добавляют 150 мл толуола, перемешивают и снова нагревают в течение 2 часов при температуре 50°С. Затем реакционную смесь декантируют, отгоняют из нее растворитель, после чего фильтруют и вакуумируют при 50-60°С и 3 мм рт.ст. до постоянного веса.
Выход дихлорангидрида составляет 95,6%.
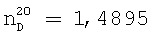 ;
; 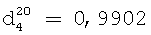 .
.
Молекулярная масса 597.
Найдено, %: С 77,20; Н 11,10; Cl 11,80.
Вычислено, %: С 77,14; Н 11,07; Cl 11,89. С36Н62O2Cl2.
ИК спектр: характерная полоса поглощения валентных колебаний С=O группы хлорангидрида (˜1805 см-1).
ЯМР спектр: ЯМР1Н (δ, м.д.): 0.85-0.88 (-СН3); 1.26 (-(CH2)n-), 4.5-5.36 и 6.79-7.0 (-СН=СН-).
ЯМР13 С (δ, м.д.): 14.2 (-СН3), 22.8-47.2 (-(СН2)n-), 173.6 (-C(O)Cl).
2. Синтез азометина по схеме:
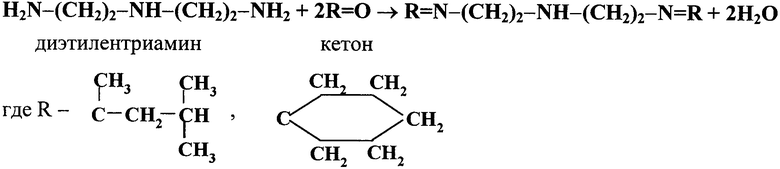
В колбу, снабженную мешалкой и насадкой Дина-Старка с холодильником, помещают 100 г (1,0 моль) диэтилентриамина и 300 г (3,0 моля) метилизобутилкетона или 300 г (3,06 моля) циклогексанона, из них 15 г - в насадку. Нагревают реакционную смесь при температуре 130-150°С в течение 5-8 часов до прекращения выделения воды. Избыток кетона и остатки воды отгоняют под вакуумом в течение 3-5 часов при температуре 80-140°С и постепенном повышении давления от 40 до 1 мм рт.ст.
Азометин выделяли в процессе вакуумной разгонки при 138-140°С и 1 мм рт.ст.
Выход азометина, полученного из диэтилентриамина и метилизобутилкетона, составляет 85,6%.
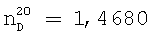 ;
; 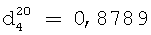 .
.
Аминное число 609,40 мг КОН/г продукта.
Молекулярная масса 267.
Найдено, %: С 71,88; Н 12,39; N 15,70.
Вычислено, %: С 71,91; Н 12,36; N 15,73. C16Р33N3.
ИК спектр: характерные полосы поглощения валентных колебаний C=N-групп (˜1662 см-1); NH-групп (3200-3500 см-1) и деформационных колебаний С-Н в гемдиметильной группе (расщепление в дуплет полосы 1380 см-1).
ЯМР спектр: ЯМР1Н (δ, м.д., J/Гц): 0.90 (д, 12Н, СН(СН3)2, J=6.3); 1.81 (c, 6H, N=CCH3); 1.98 (м, СНМе); 2.13 (м, 4H, N=CCH2); 2.93 (т, 4H, CH2NH, J=6,3); 3.36 (т, 4H, CH2N, J=6,3).
По данным ЯМР13С и DEPT-135 продукт является смесью двух Е,Е (I) и Z,E (II) - изомеров относительно двойной С=N связи.
Спектр ЯМР13С изомера I (δ, м.д.): 17.6 (N=ССН3); 22.3 (СН(СН3)2); 25.9 (СНМе2); 50.4, 51.6 и 51.1 (СН2С=NCH2CH2NH); 170.4 (C=N); изомера II (δ, м.д.): 17.6 ((E)-N=CCH3; 22.5 (СНСН3); 26.2 (СНМе2); 27.3 ((Z)-N=ССН3); 41.2 ((Z)-N=CCH2); 50,6 ((E)-N=CCH2); 50.8 и 51.0 (HNCH2CH2N=C); 170.5 ((Е)-С=N); 170.8 ((Z)-C=N).
Азометин выделяли в процессе вакуумной разгонки при 190-194°С и 1 мм рт.ст.
Выход азометина, полученного из диэтилентриамина и циклогексанона, составляет 86%.
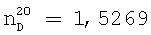 ;
; 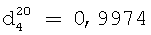 .
.
Аминное число 586,50 мг КОН/г продукта.
Молекулярная масса 263.
Найдено, %: С 72,96; Н 11,08; N 15,94.
Вычислено, %: С 73,0; Н 11,03; N 15,97. C16H29N3.
ИК спектр: характерные полосы поглощения C=N - групп (˜1664 см-1); NH-групп (3300 см-1).
ЯМР спектр: ЯМР1Н (δ, м.д.): 3.41 ((-C=N-CH2), 2.91 (CH2-NH), 2.29 (β-протоны циклогексильного фрагмента CH2-C=N).
ЯМР13С и DEPT(δ, м.д.): 50.1-51.3 (-C=N-CH2-CH2-NH-), 173.0 (-C=N).
3. Синтез 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-алкил/циклоалкилимино) этил]-дигептанамида по схеме:

В колбу, снабженную мешалкой, термометром, холодильником и капельной воронкой с хлоркальциевыми трубками, помещают 100 г (0,37 моль) азометина, растворенного в 200 мл толуола и 50,5 г (0,5 моль) триэтиламина, растворенного в 50 мл толуола, перемешивают. Дихлорангидрид димеризованной жирной кислоты в количестве 110,45 г (0,185 моль) растворяют в 150 мл толуола и по каплям в течение 2 часов при комнатной температуре добавляют в реакционную смесь, которую перемешивают еще 1 час и оставляют на ночь. К продукту реакции прибавляют 50 мл толуола и фильтруют под вакуумом на фильтре Шотта, постепенно повышая давление до 45 мм рт.ст. Избыток толуола и триэтиламин отгоняют в вакууме при 70-10 мм рт.ст. и температуре 45-75°С.
Выход 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-метилизобутилимино)этил]-дигептанамида составляет 97,4%.
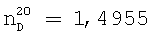 ;
; 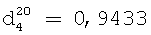 .
.
Кислотное число 2,30 мг КОН/г продукта.
Молекулярная масса 1058.
Найдено, %: 77,53; Н 11,96; N 7,85.
Вычислено, %: С 77,13; Н 11,91; N 7,94. С68Н126N6О2.
ИК спектр: сложный характер поглощения ˜1650 см-1 - суммарные валентные колебания С=O третичной амидной группы и C=N-групп.
ЯМР спектр: ЯМР1Н (δ, м.д.):0.85-0.88 (-СН3 группы), 1.26 ((СН2)n), 2.12 (СН3-C=N), 2.8-2.9 и 3.3 (-C=N-CH2-CH2-N-C(O)-), 4.5-5.36 и 6.79-7.0 (СН=СН)
ЯМР13С (δ, м.д.): 14.2 (-СН3 группы)); 22.8 ((CH2)n); 48.5-51.73 (-C=N-CH2-CH2-N-С(O)-) 122.0, 123.6 и 135.8 (СН=СН).
Выход 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-циклогексанимино)этил]-дигептанамида составляет 96,5%.
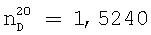 ;
; 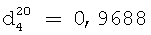 .
.
Кислотное число 1,80 мг КОН/г продукта.
Молекулярная масса 1050.
Найдено, %: С 77,65; Н 11,30; N 7,90.
Вычислено, %: С 77,71; Н 11,24; N 8,0. С68H118N6O2.
ИК спектр: сложная полоса поглощения с ˜1650 см-1 - суммарные валентные колебания С=O третичной амидной группы и C=N-групп.
ЯМР спектр: ЯМР1Н (δ, м.д.): 0.85-0.87 (-СН3 группы), 1.26 ((СН2)n), 2.9-3.1 (-C=N-CH2-CH2-N-C(O)-), 4.53-5.38 и 6.77-7.1 (СН=СН).
ЯМР13С (δ, м.д.): 14.4 (-СН3 группы)); 22.6 (CH2)n); 48.8-52.0 (-C=N-CH2-CH2-N-C(O)-) 122.0, 123.7 и 135.6 (СН=СН); 173.1 (-C(O)-N-).
4.Синтез 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида по схеме:
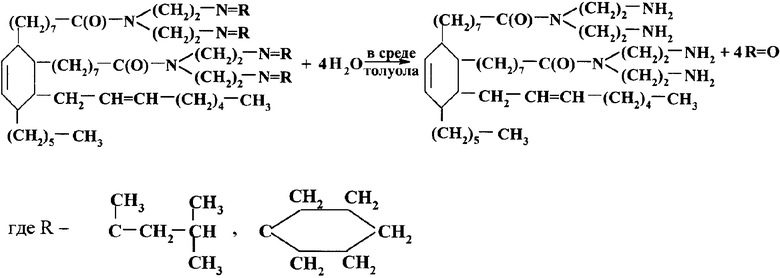
В колбу, снабженную мешалкой, термометром и холодильником помещают 100 г (0,09 моль) 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-алкил/циклоалкилимино)этил]-дигептанамида, 30 г (1,67 моль) дистилированной воды (избыток) и 200 мл толуола. При активном перемешивании нагревают реакционную смесь до температуры 65-70°С в течение 2 часов. Образующийся кетон, избыток воды и растворитель толуол отгоняют под вакуумом в течение 3-5 часов при 60-90°С, постепенно повышая давление от 160 до 3 мм рт.ст.
По своим физико-химическим свойствам 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамид, полученный гидролизом 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-метилизобутилимино)-этил]-дигептанамида, соответствует 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамиду, полученному гидролизом 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-циклогексанимино)этил]-дигептанамида.
Выход 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида, полученного гидролизом 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди [N,N-ди(2-алкил/циклоалкилимино)этил]-дигептанамида составляет 96,8%.
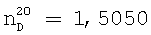 ;
; 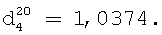
Аминное число 238,0 мг КОН/г продукта.
Кислотное число 3,0 мг КОН/г продукта.
Молекулярная масса 730.
Найдено, %: С 72,36; Н 11,79; N 11,47.
Вычислено, %: С 72,33; Н 11,78; N 11,51. С44Н86N6O2.
ИК спектр: 1650 см-1 - валентные колебания С=O-группы третичного амида; 3500-3200 см-1 и 1560 см-1 - соответственно валентные и деформационные колебания N-H первичной аминной группы.
ЯМР спектр: ЯМР1Н (δ, м.д.): 0.85-0.94 и 1.26 (-СН3- и -(СН2)n- группы), 2.8-2.9 и 3.3 (H2N-CH2-CH2-N-C(O)-).
ЯМР13С и DEPT (δ, м.д.): 14.1 (-СН3); 22.7-36.7 (-(CH2)n-); 48.5-51.7 (H2N-CH2-CH2-N-C(O) -); 173.0 (N-C(O)-).
Ниже приведены примеры конкретного применения предлагаемого нового химического соединения. Однако эти примеры не исчерпывают другие его возможные области применения.
Пример: Использование 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида в качестве отвердителя и пластификатора эпоксидных композиций, предназначенных для склеивания и герметизации различных материалов в промышленности и быту.
Эпоксидную композицию готовят путем тщательного смешения компонентов в соотношениях, указанных в таблице.
Испытания эпоксидных клеевых композиций проводили на образцах из стали марки Ст.3 и алюминиевого сплава Д16АТ.
Для обеспечения необходимой прочности и долговечности клеевого соединения стальные образцы обезжиривали ацетоном и обрабатывали шлифовальной шкуркой до равномерной шероховатости, алюминиевые образцы обезжиривали ацетоном и протравливали в специальном растворе. Обработку поверхностей склеиваемых образцов осуществляли по методикам [Кардашов Д.А. Конструкционные клеи. М.: Химия, 1980, 288 с.].
Эпоксидные композиции наносят на поверхности образцов, соединяют и фиксируют изделие для обеспечения правильного положения склеиваемых деталей относительно друг друга.
Жизнеспособность композиций ЭД-20: ЦГ в соотношениях 100:100 и 100:50 (вес.ч.) при 13-20°С составляет 3-5 часов, затем начинается процесс желатинизации.
Наряду с использованием 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида в качестве отвердителя эпоксидной смолы при склеивании металлов, данное соединение испытывали в композициях состава: ЭД-20:4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамид: диэтилентриамин (соотношение 100:48:11 вес.ч.) и ЭД-20:4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамид:полиэтиленполиамин (соотношение 100:24:7 вес.ч.) для соединения стеклопластика марки ГАРС. Прочность клеевого соединения при сдвиге составила соответственно 8,0 МПа и 12,0 МПа.
Исследование 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида в качестве дополнительного компонента системы ЭД-20: полиэтиленполиамин (соотношение 100:14 вес.ч.) показало, что данная композиция, полученная без 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида, представляет собой хрупкое вещество, растрескивающееся при определении твердости по Бриннелю (ГОСТ 4670-91). Введение в композицию 24 вес.ч. 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида позволяет получить продукт с твердостью по Бриннелю 18 Н/мм2, что указывает на значительные пластифицирующие свойства данного соединения, обусловленные наличием в его составе объемного циклоалкиленового фрагмента.
| название | год | авторы | номер документа |
|---|---|---|---|
| 4-ГЕКСИЛ-3-(ОКТЕН-2-ИЛ)-5-ЦИКЛОГЕКСЕН-1,2-ДИ[N,N-ДИ(2-АЛКИЛ/ЦИКЛОАЛКИЛИМИНО)-ЭТИЛ]-ДИГЕПТАНАМИД | 2007 |
|
RU2331633C1 |
| ДИМЕТАКРИЛОВЫЕ ЭФИРЫ ДИМЕРИЗОВАННОЙ ЖИРНОЙ КИСЛОТЫ | 2011 |
|
RU2453531C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-АЛКИЛ-N,N-ДИ(АЛКАДИИНИЛ)АМИНОВ | 2015 |
|
RU2626008C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АЛКИЛ-2-АЛКИЛ(ЦИКЛОАЛКЕНИЛ, БЕНЗИЛ)ЦИКЛОПРОПАНОЛОВ | 2009 |
|
RU2433990C2 |
| Способ получения этоксикарбонилометилен-ди-трет-бутил(N-алкил-N-фениламино)-фосфоранов | 1989 |
|
SU1754721A1 |
| БЕТА-АДРЕНОБЛОКАТОРЫ НА ОСНОВЕ ПРОИЗВОДНЫХ ПИРИДОКСИНА | 2014 |
|
RU2569900C1 |
| Лиганд для получения комплекса переходного металла, способ его получения и способ получения комплекса переходного металла с использованием лиганда | 2015 |
|
RU2616628C2 |
| N, N-ДИ(2-ХЛОРЭТИЛ)-N'-МОРФОЛИЛ-N'' - ЦИКЛОГЕКСИЛТРИАМИДЫ ФОСФОРНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 1986 |
|
SU1363822A1 |
| N,N'-ДИ(АЛКАДИИНИЛ)ДИАЗАЦИКЛОАЛКАНЫ И СПОСОБ ПОЛУЧЕНИЯ N,N'-ДИ(АЛКАДИИНИЛ)ДИАЗАЦИКЛОАЛКАНОВ, ПРОЯВЛЯЮЩИХ ФУНГИЦИДНУЮ АКТИВНОСТЬ ПО ОТНОШЕНИЮ К ГРИБАМ Bipolaris sorokiniana и Rhizoctonia solani | 2019 |
|
RU2727138C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 2-, 3- И 4-(1,3,5-ДИТИАЗИНАН-5-ИЛ) ТИОФЕНОЛОВ | 2009 |
|
RU2425039C2 |
Изобретение относится к получению 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамида. Технический результат - 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамид, используемый в качестве отвердителя и пластификатора эпоксидных композиций, предназначенных для склеивания и герметизации различных материалов в промышленности и быту. 1 табл.
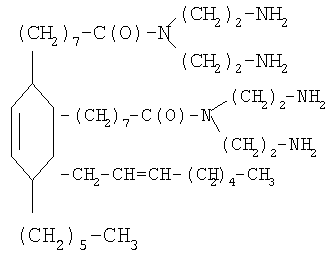
4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]-дигептанамид формулы

| СОРОКИН М.Ф | |||
| и др | |||
| Химия и технология пленкообразующих веществ | |||
| - М.: Химия, 1981, с.156-158 | |||
| СПОСОБ ПРОИЗВОДСТВА ЙОГУРТА | 1997 |
|
RU2112388C1 |
| US 4829142 А, 09.05.1989. | |||
Авторы
Даты
2008-09-10—Публикация
2007-04-16—Подача