Изобретение относится к химической промышленности, а именно к получению новых производных димеризованной жирной кислоты (ДЖК), которые могут быть использованы, например, в качестве связующих при изготовлении различных композиционных материалов, в составе заливочных компаундов и анаэробных герметиков.
Известны производные димеризованной жирной кислоты, представляющие собой
- полиамиды, используемые как клеи-расплавы (Заявка ФРГ №4408276, C08L 77/08, опубл. 14.09.1995 г., Заявка ФРГ №4408277, C09J 177/00, опубл. 14.09.1995 г.);
- олигоаминоамиды и имидазолины, используемые как отвердители и модификаторы эпоксидных и фенолформальдегидных смол (Бобылев В.А. // Композитный мир. 2006. №4. с.20-24);
- олигоамиды, используемые в составе покрытий, лаков и красителей (Попова Т.А., Жилина Н.В., Родивилова Л.А. и др. Производство олигоамидов за рубежом. Обзорная информация. Сер. «Пластические массы и синтетические смолы». М.: НИИТЭХИМ, 1979, с.32);
- 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди-[N,N-ди(2-алкил/циклоалкилимино)этил]дигептанамид, используемый в качестве отвердителя и пластификатора эпоксидных композиций (Патент РФ №2331633, С07С 251/14, опубл. 20.08.2008 г.);
- 4-гексил-3-(октен-2-ил)-5-циклогексен-1,2-ди[N,N-ди(2-аминоэтил)]дигептанамид, используемый в качестве отвердителя и пластификатора эпоксидных композиций (Патент РФ №2333197, С07С 237/16, опубл. 10.09.2008 г.);
- сложные эфиры димеризованной жирной кислоты и спирта, содержащего С3-С24 алкильные группы, используемые как пластификаторы термопластичных полимеров (Патент США №7285588, С08К 5/101, опубл. 23.10.2007 г.).
Известно также использование диметакриловых эфиров триэтиленгликоля, диэтиленгликоля и тетраэтиленгликоля в анаэробных композициях (Авторское свидетельство СССР №1206271, С07С 67/08, опубл. 23.01.1986 г.). Указанные диметакриловые эфиры при применении их в составе анаэробных герметизирующих композиций не обеспечивают высокую прочность соединения на замасленных поверхностях. Например, анаэробный герметик «Анатерм-8К» (ТУ 2257-338-00208947-2000), содержащий диметакрилат триэтиленгликоля, имеет момент отвинчивания через 24 часа при 20°С на обезжиренных поверхностях 5,3 Н·м, а на замасленных поверхностях 2,6 Н·м. При этом показатель сохранения прочности момента отвинчивания на замасленной поверхности составляет не более 49%.
Изобретательская задача состояла в получении новых соединений, являющихся производными димеризованной жирной кислоты, которые при использовании их, например, в составе анаэробных герметиков для машиностроения обеспечивали бы высокую прочность на замасленных поверхностях.
Поставленная задача решена диметакриловыми эфирами димеризованной жирной кислоты формулы
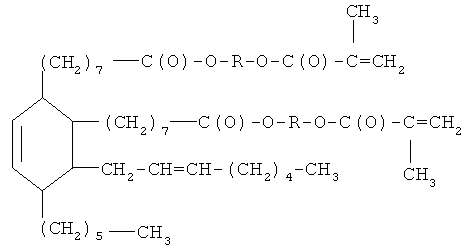
где R=CH2CH2OCH2CH2; CH2CH2OCH2CH2OCH2CH2; (CH2)4; CH2CH2;
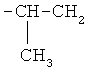 .
.
Исходные продукты для синтеза и свойства полученных диметакриловых эфиров димеризованной жирной кислоты представлены в таблице 1.
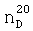
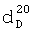
Метакриловая кислота
Метакриловая кислота
Метакриловая кислота
Монометакрилат этиленгликоля
Монометакрилат пропиленгликоля
Структуры синтезированных диметакриловых эфиров димеризованной жирной кислоты доказаны данными ИК- и ЯМР-спектроскопии.
Изобретение позволяет добиться следующих преимуществ: использование диметакриловых эфиров димеризованной жирной кислоты в составе анаэробных клеевых и герметизирующих композиций повышает прочность клеерезьбовых соединений на замасленных поверхностях, при этом обеспечивая высокий показатель сохранения прочности на замасленных поверхностях по сравнению с обезжиренными.
Для реализации способов получения метакриловых эфиров ДЖК используют следующие вещества:
димеризованная жирная кислота "Pripol 1013" (содержание димеров линолевой кислоты не менее 97%) - CAS №61788-89-4;
Дихлорангидрид димеризованной жирной кислоты [Фомина Е.В., Курский Ю.А., Червякова Г.Н. и др. Получение дихлорангидрида димеризованной жирной кислоты и олигоамидов на его основе методами низкотемпературной поликонденсации // Журнал прикл. химии. 2008. - T.81. - Вып.4. - С.621-626];
метакриловая кислота - ТУ 6-01-914-79;
диэтиленгликоль - ГОСТ 10136-77;
триэтиленгликоль - ТУ 6-01-5-88 с изм. 1, 2;
бутиленгликоль (1,4-бутандиол) - ТУ 64-5-105-86;
монометакриловый эфир этиленгликоля - ТУ 6-01-1240-80;
монометакриловый эфир пропиленгликоля - СТП 70-2005 (ФГУП "НИИ полимеров");
толуол - ГОСТ 5789-78;
гидрохинон - ГОСТ 2549-60;
n-метоксифенол - ТУ 6-09-1248-71;
n-толуолсульфокислота - ТУ 6-09-3668-77;
триэтиламин - ГОСТ 9966-88;
гидроксид натрия - ГОСТ 4328-77 с изм. 1, 2;
натрий хлористый - ГОСТ 4233-77;
вода дистиллированная - ГОСТ 6709-72.
Получение диметакриловых эфиров ДЖК проводили тремя способами:
1. Взаимодействием ДЖК с гликолем и метакриловой кислотой.
2. Взаимодействием ДЖК с моногликолем метакриловой кислоты.
3. Взаимодействием дихлорангидрида ДЖК с моногликолем метакриловой кислоты.
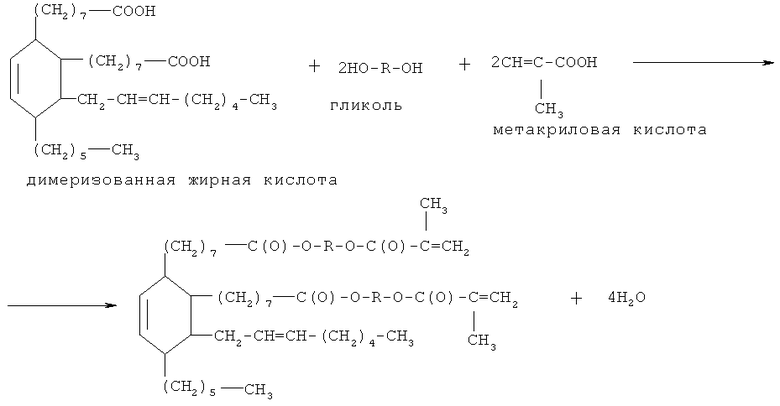
где R=CH2CH2OCH2CH2; CH2CH2OCH2CH2OCH2CH2; (CH2)4.
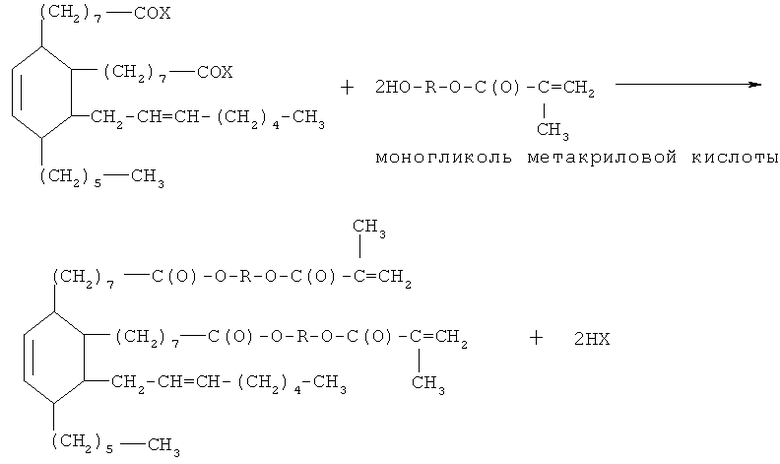
где X=OH или C1; R=CH2CH2; 
Пример 1. Синтез диметакрилата на основе ДЖК, диэтиленгликоля и метакриловой кислоты.
В колбу, снабженную мешалкой и насадкой Дина-Старка с холодильником, помещают 100 г (0,18 моля) димеризованной жирной кислоты, 42 г (0,4 моля) диэтиленгликоля, 34,1 г (0,4 моля) метакриловой кислоты, 0,36 г (0,0032 моля) гидрохинона, 4,4 г (0,0256 моля) n-толуолсульфокислоты и 250 мл (2,35 моля) толуола, из них 15 мл - в насадку.
Реакционную смесь нагревают при температуре 120-130°С в бане и 100-120°С в реакторе в течение 5-6 часов до прекращения выделения воды. Несколько раз в процессе синтеза, а также по его завершении определяют кислотное число реакционной массы по n-толуолсульфокислоте и димеризованной жирной кислоте. Содержимое колбы по окончании синтеза переливают в делительную воронку, разбавляют 300 мл толуола и 2-3 раза промывают 10%-ным водным раствором хлористого натрия. Затем синтезированный продукт нейтрализуют расчетным количеством гидроксида натрия, после чего промывают 10%-ным раствором хлористого натрия, а затем дистиллированной водой до нейтральной реакции. Полученный продукт фильтруют через ткань, добавляют в него 0,06 г (0,0005 моля) гидрохинона и отгоняют в вакууме толуол при 60-10 мм рт.ст. и температуре 50-60°С. После отгонки толуола продукт вакуумировали при 10-5 мм рт.ст. и 50-60°С в течение 1-2 часов.
Выход диметакрилата на основе димеризованной жирной кислоты, диэтиленгликоля и метакриловой кислоты составляет 78,4%.
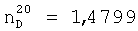 ;
; 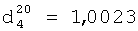 .
.
Число омыления 267,10 мг КОН/г продукта.
Эфирное число 266,38 мг КОН/г продукта.
Молекулярная масса 872.
Найдено, %: С 71,28; Н 9,84.
Вычислено, %: С 71,60; Н 10,10. C52H88O10.
ИК-спектр: характерные полосы валентных колебаний сложных эфиров С-O-С-групп при 1350-1100 см-1; С=С-связей при 1640 см-1; C=O-групп, сопряженных с С-С-связью (1720 см-1) и несопряженных (полоса в области ~1740 см-1); полосы поглощения деформационных колебаний (СН2)n групп алифатической цепи при ~725 см-1.
ЯМР спектр: ЯМР 1Н (δ, м.д.): 0.88 (м, СН3); 1.26 (с, - (CH2)n-); 1.62 (м, CH2); 1.95 (с, ОС(O)СН 3С=СH2); 2.33 (т, СН2С(O)O); 3.61÷3.79 (м, OCH2CH2O); 4.23 и 4.31 (оба т, CH2OC(O)); 5.58 и 6.14 (оба с,- С=СН2).
Пример 2. Синтез диметакрилата на основе ДЖК, триэтиленгликоля и метакриловой кислоты.
В колбу, снабженную мешалкой и насадкой Дина-Старка с холодильником, помещают 100 г (0,18 моля) димеризованной жирной кислоты, 60 г (0,4 моля) триэтиленгликоля, 34,1 г (0,4 моля) метакриловой кислоты, 0,36 г (0,0032 моля) гидрохинона, 4,85 г (0,0282 моля) n-толуолсульфокислоты и 250 мл (2,35 моля) толуола, из них 15 мл - в насадку.
Синтез и дальнейшее выделение продукта осуществляли, как описано в примере 1.
Выход диметакрилата на основе димеризованной жирной кислоты, триэтиленгликоля и метакриловой кислоты составляет 79,2%.
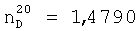 ;
; 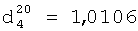 .
.
Число омыления 258,58 мг КОН/г продукта.
Эфирное число 256,42 мг КОН/г продукта.
Молекулярная масса 960.
Найдено, %: С 69,72; Н 9,76.
Вычислено, %: С 70,00; Н 10,0. C56H96O12.
ИК-спектр: характерные полосы поглощения С-O-С-групп (1350-1100 см-1); С=О-групп(~1730 см-1).
ЯМР спектр: ЯМР 1Н (δ, м.д.): 3.66 (с, OCH2CH2O) и 3.60÷3.77 (м); 4.22 и 4.30 (т, CH2OC(O)).
Пример 3. Синтез диметакрилата на основе ДЖК, бутиленгликоля и метакриловой кислоты
В колбу, снабженную мешалкой и насадкой Дина-Старка с холодильником, помещают 100 г (0,18 моля) димеризованной жирной кислоты, 36,0 г (0,4 моля) бутиленгликоля, 34,1 г (0,4 моля) метакриловой кислоты, 0,36 г (0,0032 моля) гидрохинона, 4,25 г (0,0379 моля) n-толуолсульфокислоты и 250 мл (2,35 моля) толуола, из них 15 мл - в насадку.
Синтез и дальнейшее выделение продукта осуществляли, как описано в Примере 1.
Выход диметакрилата на основе димеризованной жирной кислоты, бутиленгликоля и метакриловой кислоты составляет 84,3%.
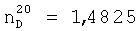 ;
; 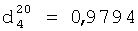 .
.
Число омыления 256,75 мг КОН/г продукта.
Эфирное число 255,39 мг КОН/г продукта.
Молекулярная масса 840.
Найдено, %: С 73,93; Н 10,19.
Вычислено, %: С 74,29; Н 10,48. C52H88O8.
ИК-спектр: характерные полосы поглощения С-O-С-групп (1340-1100 см-1); C=O-групп (1730-1715 см-1).
ЯМР спектр: ЯМР 1Н (δ, м.д.): 0.88 (м, СН3); 1.26 (с, -(СН2)n-);1.62 (м, CH2); 1.70÷1.81 (м, С(O)OCH2CH 2CH 2CH2O(O)С); 1,94 (с, ОС(O)СН3С=СН2); 2.29 (т, СН2С(O)O); 4.09-4.21 (м, CH2OC(O)); 5,55 и 6.10 (оба с, C=CH2); 4.95÷5.46 и 6.68÷7.10 (оба м, СН=СН).
Пример 4. Синтез диметакрилата на основе ДЖК и монометакрилата этиленгликоля.
В колбу, снабженную мешалкой и насадкой Дина-Старка с холодильником, помещают 100 г (0,18 моля) димеризованной жирной кислоты, 56,16 г (0,432 моля) монометакрилата этиленгликоля, 0,56 г (0,005 моля) гидрохинона, 3,90 г (0,0227 моля) n-толуолсульфокислоты и 250 мл (2,35 моля) толуола, из них 15 мл - в насадку.
Синтез и дальнейшее выделение продукта осуществляли, как описано в примере 1.
Выход диметакрилата на основе димеризованной жирной кислоты и монометакрилата этиленгликоля составляет 88,1%.
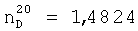 ;
; 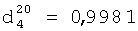 .
.
Число омыления 233,40 мг КОН/г продукта.
Эфирное число 227,62 мг КОН/г продукта.
Молекулярная масса 784.
Найдено, %: С 73,22; Н 9,93.
Вычислено, %: С 73,47; Н 10,20. C48H80O8.
ИК-спектр: характеристические частоты С-O-С-групп (1150-1080 см-1); С=О-групп (1730-1715 см-1).
ЯМР спектр: ЯМР 1Н (δ, м.д.): 0.88 (м, СН3); 1.26 (с, -(ОН2)n-); 1.62 (м, СН2); 1.95 (с, ОС(O)СН 3С=СН2); 2.33 (т, СН2С(О)О); 2.53 (м, CH 2CH); 4.34 (с, OCH2CH2O); 5.59 и 6.13 (оба с, -С=СН2); 6.73÷7.01 (м, СН=СН).
Пример 5. Синтез диметакрилата на основе ДЖК и монометакрилата пропиленгликоля.
В колбу, снабженную мешалкой и насадкой Дина-Старка с холодильником, помещают 100 г (0,18 моля) димеризованной жирной кислоты, 62,21 г (0,432 моля) монометакрилата пропиленгликоля, 0,62 г (0,0055 моля) гидрохинона, 4,06 г (0,0236 моля) n-толуолсульфокислоты и 250 мл (2,35 моля) толуола, из них 15 мл - в насадку.
Синтез и дальнейшее выделение продукта осуществляли, как описано в примере 1.
Выход диметакрилата на основе димеризованной жирной кислоты и монометакрилата пропиленгликоля составляет 94,5%.
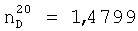 ;
; 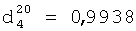 .
.
Число омыления 283,70 мг КОН/г продукта.
Эфирное число 281,72 мг КОН/г продукта.
Молекулярная масса 812.
Найдено, %: С 73,58; Н 10,06.
Вычислено, %: С 73,89; Н 10,34. C50H84O8.
ИК-спектр: характеристические частоты С-O-С-групп (1300-1150 см-1); С=О-групп (1750-1735 см-1).
ЯМР спектр: ЯМР 1Н (δ, м.д.): 0.88 (м, СН3); 1.26 (с, -(CH2)n-); 1.62 (м, СН3); 1.94 и 1.96 (оба с, ОС(O)СН 3С=СН2); 2.33 (т, СН2С(O)O); 2.53 (м, CH 2CH=С); 4.00÷4.25 (м, ОСН 2СНСН3О); 5.0÷5.40 (м, OCH2CHCH3O); 5.59÷5.60 (м, С=СН2); 6.10 и 6.15 (оба с, -С=СН2); 6.70÷7.25 (м, СН=СН).
Пример 6. Синтез диметакрилата на основе дихлорангидрида ДЖК и монометакрилата этиленгликоля.
В колбу, снабженную мешалкой и термометром, помещают 14,3 г (0,11 моля) монометакрилата этиленгликоля, растворенного в 260 мл (2,45 моля) толуола, 12,6 г (0,125 моля) триэтиламина и при перемешивании, по каплям, добавляют раствор 30 г (0,05 моля) дихлорангидрида димеризованной жирной кислоты в 200 мл (1,9 моля) толуола. Синтез проводят, перемешивая реакционную массу в течение 3 часов (первый час при 20°С, а затем 2 часа при температуре водяной бани 40°С). Образовавшуюся соль отделяют на фильтре Шотта, а фильтрат переносят в делительную воронку и несколько раз промывают водой и 20%-ным раствором хлористого натрия. Полученный продукт фильтруют, добавляют в него 0,197 г (0,0016 моля) n-метоксифенола и отгоняют толуол при вакууме 80-85 мм рт.ст. и температуре 50-55°С. После отгонки толуола продукт вакуумировали при 3 мм рт.ст. и 60-65°С в течение 2-3 часов.
Выход диметакрилата на основе дихлорангидрида димеризованной жирной кислоты и монометакрилата этиленгликоля составляет 87,06%.
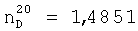 ;
; 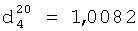 .
.
Число омыления 275,0 мг КОН/г продукта.
Эфирное число 272,60 мг КОН/г продукта.
Молекулярная масса 784.
Найдено, %: С 73,18; Н 9,94.
Вычислено, %: С 73,47; Н 10,20. C48H80O8.
ИК-спектр: характеристические частоты С-O-С-групп при 1150-1070 см-1; С=O-групп при 1745-1715 см-1.
ЯМР спектр: ЯМР 1Н (δ, м.д.): 2.34 (т, СН2С(O)O); 2.55 (м, СН 2СН=С); 4.33 (с, O(СН2)2O); 5.57 и 6.12 (оба с, -С=СН2); 6.69÷7.0 (м, СН=СН).
Пример 7. Синтез диметакрилата на основе дихлорангидрида ДЖК и монометакрилата пропиленгликоля.
В колбу, снабженную мешалкой и термометром, помещают 15,84 г (0,11 моля) монометакрилата пропиленгликоля, растворенного в 260 мл (2,45 моля) толуола, 12,6 г (0,125 моля) триэтиламина и при перемешивании, по каплям, добавляют раствор 30 г (0,05 моля) дихлорангидрида димеризованной жирной кислоты в 200 мл (1,9 моля) толуола.
Синтез и дальнейшее выделение продукта осуществляли, как описано в примере 6.
Выход диметакрилата на основе дихлорангидрида димеризованной жирной кислоты и монометакрилата пропиленгликоля составляет 85,4%.
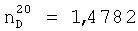 ;
; 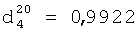 .
.
Число омыления 270,85 мг КОН/г продукта.
Эфирное число 268,22 мг КОН/г продукта.
Молекулярная масса 812.
Найдено, %: С 73,66; Н 10,10.
Вычислено, %: С 73,89; Н 10,34. C50H84O8.
ИК-спектр: характерные полосы поглощения С-O-С-групп (1350-1150 см-1); С=О-групп (1740-1715 см-1).
ЯМР спектр: ЯМР 1Н (δ, м.д.): 1.95 и 1.97 (оба с, OC(O)CH 3C=H2); 2.33 (т, СН2С(O)O); 2.54 (м, СН 2СН=С); 4.00÷4.28 (м, ОСН 2СНСН3О); 4.99÷5.50 (м, ОСН 2СНСН3О); 5.58÷5.59 (м, -С=OH2); 6.10 и 6.15 (оба с, -С=СН2); 6.71÷7.25 (м, СН=СН).
Ниже приведены примеры конкретного применения предлагаемых новых химических соединений. Однако эти примеры не исчерпывают другие возможные области их применения.
Полученные составы, содержащие синтезированные диметакриловые эфиры димеризованной жирной кислоты, исследовали в анаэробных клеевых композициях в резьбовом соединении болт-гайка. Композиции наносили на обезжиренные толуолом и замасленные (5%-ным раствором машинного масла М63Г в гексане) резьбовые пары и завинчивали гайки. После отверждения композиций измеряли момент отвинчивания резьбового соединения при сравнении с промышленно выпускаемым герметиком марки «Анатерм-8К» (ТУ 2257-338-00208947-2000), содержащим диметакрилат триэтиленгликоля.
Исследования показали, что анаэробные композиции, содержащие диметакриловые эфиры димеризованной жирной кислоты, обладают высокой прочностью на замасленной поверхности. Момент отвинчивания таких композиций составляет 3,7-5,2 Н·м, что в 1,4-2,0 раза выше, чем у «Анатерма-8К», полученного на основе известного диметакрилата алкиленгликоля. Сохранение прочности момента отвинчивания анаэробных композиций, содержащих диметакриловые эфиры димеризованной жирной кислоты, на замасленных поверхностях по сравнению с обезжиренной составляет 66-89%, что в 1,3-1,8 раза выше, чем у «Анатерма-8К».
| название | год | авторы | номер документа |
|---|---|---|---|
| 4-ГЕКСИЛ-3-(ОКТЕН-2-ИЛ)-5-ЦИКЛОГЕКСЕН-1,2-ДИ[N,N-ДИ(2-АЛКИЛ/ЦИКЛОАЛКИЛИМИНО)-ЭТИЛ]-ДИГЕПТАНАМИД | 2007 |
|
RU2331633C1 |
| 4-ГЕКСИЛ-3-(ОКТЕН-2-ИЛ)-5-ЦИКЛОГЕКСЕН-1,2-ДИ[N,N-ДИ(2-АМИНОЭТИЛ)]-ДИГЕПТАНАМИД | 2007 |
|
RU2333197C1 |
| ПОЛИАМИДОМОЧЕВИННЫЕ ПРОИЗВОДНЫЕ ДИМЕРИЗОВАННОЙ ЖИРНОЙ КИСЛОТЫ | 2016 |
|
RU2616298C1 |
| АМИДО(УРЕТАН)КАРБОНАТЫ ПОЛИМОЛОЧНОЙ КИСЛОТЫ | 2013 |
|
RU2537563C1 |
| ПОЛИЭФИРПОЛИКАРБОНАТЫ ОЛИГОМОЛОЧНОЙ КИСЛОТЫ | 2013 |
|
RU2527471C1 |
| КЛЕЕВАЯ КОМПОЗИЦИЯ ДЛЯ ИЗГОТОВЛЕНИЯ СИЛИКАТНЫХ ТРИПЛЕКСОВ | 1991 |
|
RU2015151C1 |
| КЛЕЙ-РАСПЛАВ (ВАРИАНТЫ) | 2003 |
|
RU2237697C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИ-(2-МЕТАКРИЛОИЛОКСИЭТИЛ)ИЗОФТАЛАТА | 1985 |
|
SU1354653A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОМОЛЕКУЛЯРНЫХ СЛОЖНЫХ ЭФИРОВ КАРБОНОВЫХ КИСЛОТ | 1994 |
|
RU2079481C1 |
| КЛЕЕВАЯ КОМПОЗИЦИЯ ДЛЯ ИЗГОТОВЛЕНИЯ СИЛИКАТНЫХ ТРИПЛЕКСОВ | 1991 |
|
RU2007431C1 |
Изобретение относится к новым диметакриловым эфирам димеризованной жирной кислоты, используемым в качестве связующих при изготовлении различных композиционных материалов, в составе заливочных компаундов и анаэробных герметиков. Диметакриловые эфиры димеризованной жирной кислоты имеют структурную формулу
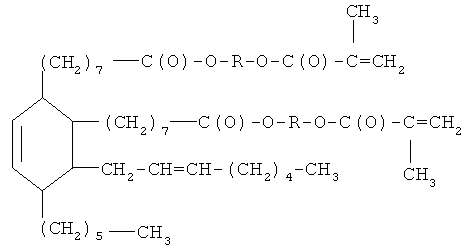
в которой R=CH2CH2OCH2CH2; СН2СН2ОСН2СН2ОСН2СН2; (СН2)4;
СН2СН2;  . 2 табл., 7 пр.
. 2 табл., 7 пр.
Диметакриловые эфиры димеризованной жирной кислоты формулы
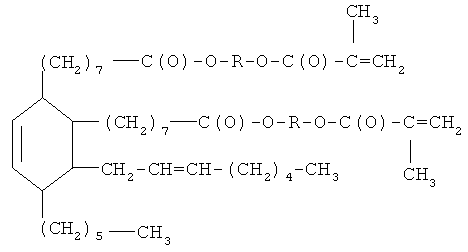
где R - CH2CH2OCH2CH2; СН2СН2ОСН2СН2ОСН2СН2; (СН2)4;
СН2СН2; 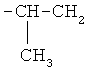
| US 6884832 А, 26.04.2005 | |||
| Состав для изготовления бумаги для сухого пастового сепаратора | 1989 |
|
SU1694760A1 |
| US 7232855 А, 19.06.2007 | |||
| US 7109264 В2, 19.09.2006 | |||
| US 6858664 А, 22.02.2005 | |||
| US 6174948 А, 16.01.2001 | |||
| US 20050038161 А, 17.02.2005 | |||
| US 7144937 В2, 05.12.2006 | |||
| Способ получения диметакриловых эфиров алкиленгликолей | 1981 |
|
SU1206271A1 |
Авторы
Даты
2012-06-20—Публикация
2011-01-11—Подача