Область техники
Изобретение имеет отношение к суспензионным топливным смесям для применения в электрохимических топливных элементах, способу производства электрической энергии с применением таких суспензионных топливных смесей, а также к топливным элементам, использующим такие суспензионные топливные смеси для производства электрической энергии.
Предшествующий уровень техники
Топливный элемент представляет собой устройство, в котором энергия химических реакций преобразовывается в электрическую энергию. Среди преимуществ топливных элементов перед другими источниками электрической энергии - высокий КПД и безвредность для окружающей среды. Хотя топливные элементы все больше и больше применяются в качестве источников электрической энергии, имеются технические трудности, мешающие широкому использованию топливных элементов во многих сферах применения, особенно для мобильных и портативных устройств.
Топливный элемент производит электрическую энергию, вводя топливо в контакт с каталитическим анодом, тогда как окислитель - в контакт с каталитическим катодом. Во время контакта с таким анодом топливо окисляется на каталитических центрах, образовывая электроны. Эти электроны перемещаются от анода к катоду по электрической цепи, соединяющей электроды. Одновременно окислитель каталитически восстанавливается на катоде, принимая электроны, образовывающиеся на аноде. Баланс массы и баланс заряда поддерживаются путем соответствующего образования ионов как на катоде, так и на аноде, и диффузии этих ионов к другому электроду через электролит, с которым контактируют электроды.
Распространенный вид топливных элементов использует водород в качестве топлива и кислород в качестве окислителя. В частности, водород окисляется на аноде с образованием протонов и электронов, как показано в уравнении (1)

Протоны проходят через электролит к катоду. Электроны же перемещаются от анода, через электрическую нагрузку, и к катоду. На катоде кислород восстанавливается, соединяясь с электронами и протонами, образованными из водорода, и образовывает воду, как показано в уравнении (2)
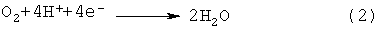
Хотя топливные элементы, использующие водород в качестве топлива, просты, чисты и производительны, чрезвычайная огнеопасность водорода и необходимость в массивных резервуарах высокого давления для хранения и транспортировки водорода означает, что топливные элементы, питающиеся водородом, неприемлемы для многих применений.
В целом хранение, использование и транспортировка жидкостей проще, чем газов. Благодаря этому жидкое топливо было предложено для применения в топливных элементах. Были разработаны способы для превращения в водород жидкого топлива, такого как метанол, на месте. Такие способы не просты, они нуждаются в стадии предварительной подготовки топлива и сложной регулировочной системы для топлива.
Топливные элементы с прямым окислением жидкого топлива являются решением такой проблемы. Поскольку такое топливо подается в топливный элемент непосредственно, топливные элементы с прямым питанием жидким топливом сравнительно просты. Наиболее распространенным топливом, используемым в топливных элементах такого типа, является метанол, потому что он дешев, доступен для получения из различных источников, а также имеет высокую удельную энергию (5020 (А·ч)/л).
В топливных элементах с прямым питанием метанолом метанол каталитически окисляется на аноде с образованием электронов, протонов и оксида углерода, как показано в уравнении (3)
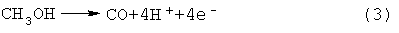
Оксид углерода плотно присоединяется к каталитическим центрам на аноде. Количество имеющихся в наличии центров для дальнейшего окисления уменьшается, что снижает выработку энергии. Одним из решений этой проблемы является применение анодных катализаторов, таких как платиновые/рутениевые сплавы, менее чувствительные к адсорбции СО. Другим решением является введение в такой элемент топлива в виде "анолита", т.е. смеси метанола с водным жидким электролитом. Метанол реагирует с водой на аноде с образованием диоксида углерода и ионов водорода, как показано в уравнении (4)
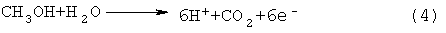
В топливных элементах, использующих анолиты, состав таких анолитов является важным предметом разработки. Этот анолит должен иметь как высокую электропроводимость, так и высокую подвижность ионов при оптимальной концентрации топлива. Наиболее распространены кислотные растворы. К сожалению, кислотные анолиты имеют наивысшую производительность при относительно высоких температурах, при которых кислотная среда может пассивировать или разрушить анод. Анолиты с рН, близким к 7, являются безвредными для анода, однако имеют электропроводимость, слишком низкую для эффективной выработки электрической энергии. Поэтому в большинстве известных метаноловых топливных элементов с прямым питанием используются мембраны из твердого полимерного электролита (ТПЭ).
В элементах с использованием ТПЭ-мембран катод подвергается действию кислорода воздуха и отделяется от анода протонообменной мембраной, которая действует, с одной стороны, как электролит, а с другой - как физический барьер, предотвращающий утечку из анодного пространства, где содержится жидкий анолит. Одной из мембран, широко используемой в качестве твердого электролита для топливных элементов, является перфторуглеродный материал, который изготовляется фирмой E.I.DuPont de Nemours (Уилмингтон, Делавер, США) под товарным знаком Nafion. Топливные элементы, в которых используются ТПЭ-мембраны, имеют более высокую удельную мощность и более длительные ресурсы эксплуатации, чем другие топливные анолитовые элементы.
Один из практических недостатков топливных элементов с ТПЭ-мембранами происходит из тенденции метанола в высоких концентрациях растворять мембрану и диффундировать сквозь нее. В результате значительная часть метанола, которая содержится в элементе, не используется для выработки электрической энергии, а наоборот - или теряется из-за испарения, или окисляется непосредственно на катоде, производя тепловую энергию вместо электрической.
Проблема проникновения топлива через мембрану преодолевается применением анолитов с низким (не выше 3%) содержанием метанола. Низкое содержание метанола ограничивает производительность топливных элементов, если ее измерять в единицах электрической емкости как функции от объема расходуемого топлива; также поднимаются вопросы транспортировки топлива, лишнего веса и утилизации отходов. Кроме того, применение анолитовых топливных элементов с питанием жидким топливом с низким содержанием метанола, особенно для мобильных и портативных применений, ограничивается стоимостью и сложностью необходимого дополнительного оборудования, необходимого для обеспечения циркуляции, пополнения, нагревания и дегазирования топлива.
Наконец, невзирая на высокую удельную энергию, метанол является скорее инертным при комнатной температуре, которая ограничивает удельную разрядную мощность метаноловых топливных элементов до приблизительно 15 мВт/см.
В качестве топлив для топливных элементов также предлагались и другие органические соединения, особенно высшие спирты, углеводород и ацетаты. Например, в работах O.Savadogo and X. Yang "The electrooxidation of some acetals for direct hydrocarbons fuel cell applications", IIIrd International Symposium on Electrocatalysis, Slovenia, 1999, с.57, а также С.Lamy at al. "Direct anodic oxidation of methanol, ethanol and higher alcohols and hydrocarbons in PEM fuel calls", IIIrd International Symposium on Electrocatalysis, Slovenia, 1999, с.95. Большинство из них продемонстрировали очень низкие свойства, обусловленные низкой электрохимической активностью, высокой стоимостью, а в некоторых случаях также и высокой токсичностью.
Неорганические водорастворимые восстановители, такие как гидриды металлов, гидразин и его производные, также предлагались в качестве топлива для топливных элементов. Например, в работах S.Lei "The characterization of an alkaline fuel cell that uses hydrogen storage alloys", Jornal of the Electrochemical Society, vol.149 no. 5, A603-A606 (2002), J. O'M. Bockris and S. Srinivasan Fuel cells: Their Electrochemistry, McGraw-Hill, New York, 1969, с.589-593, и Н.В.Корвин "Гидразин", Химия, Москва, 1980 (на русском), стр.205-224. Такие соединения имеют высокие удельные энергии и являются высокореактивными.
Одним из таких соединений является NaBH4. В воде NaBH4 диссоциирует на Na+ и BH4 -. В нейтральном растворе ВН4 - окисляется на аноде по уравнению (5)
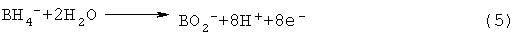
Самым большим недостатком водородсодержащих неорганических соединений как топлива является их разложение в кислых и нейтральных растворах. Например, ВН4 - разлагается на составные части по уравнению (6)
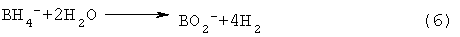
В основных растворах ВН4 - окисляется на аноде по уравнению (7)
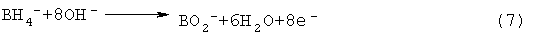
Соответствующее восстановление газообразного кислорода на катоде происходит по уравнению (8)
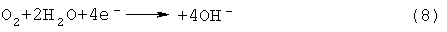
Баланс массы и баланс заряда сохраняются путем диффузии гидроксильных ионов с катода на анод через электролит.
Хотя ВН4 - стабилен в основных растворах, он разлагается на составные части при контакте с катализатором, если он имеется в наличии на аноде топливного элемента, по уравнению (6), даже когда этот топливный элемент не имеет электрической нагрузки.
Хотя газообразный водород, образовывающийся во время этой реакции, также может окисляться на аноде по уравнению (1), но электродная реакция, приведенная в уравнении (7), является значительно более производительной энергетически, чем электродная реакция, приведенная в уравнениях (1) и (6). Кроме того, каталитическое разложение ВН4 на аноде создает тенденцию к сокращению ресурса анода.
Эту проблему имеют в виду в РСТ заявке WO/02/054506, которая включена в это описание во всех аспектах путем ссылки, как если бы она была бы полностью приведена здесь непосредственно, когда добавляется спирт, такой как метанол, к основному раствору NaBH4. Кроме функции топлива как такового, такой спирт выступает ингибитором разложения таких гидридных ионов, как ВН4 -, на аноде. Предусматривается, что такой спирт будет ингибировать разложение гидридных ионов на аноде, по меньшей мере, посредством двух механизмов. Первый из этих механизмов заключается в том, что адсорбция молекул спирта к анодным каталитическим центрам стерически затрудняет доступ гидридных ионов к этим каталитическим центрам. Второй механизм заключается в том, что молекулы спирта будут сольватировать гидридные ионы.
Интуитивно можно предположить, что емкость (измеряемая в ампер-часах) топливного элемента, работающего на гидридном топливе, может представлять собой линейную зависимость от концентрации этих гидридов. Например, растворимость NaBH4 в 3М KOH составляет 1,25 моль/л, а растворимость NaBH4 в 3М NaOH составляет 4 моль/л; таким образом, можно предположить, что емкость топливного элемента, работающего на 3М NaOH, насыщенном NaBH4, будет в четыре раза больше емкости топливного элемента, работающего на 3М KOH, насыщенном NaBH4. Однако экспериментально это не подтверждается.
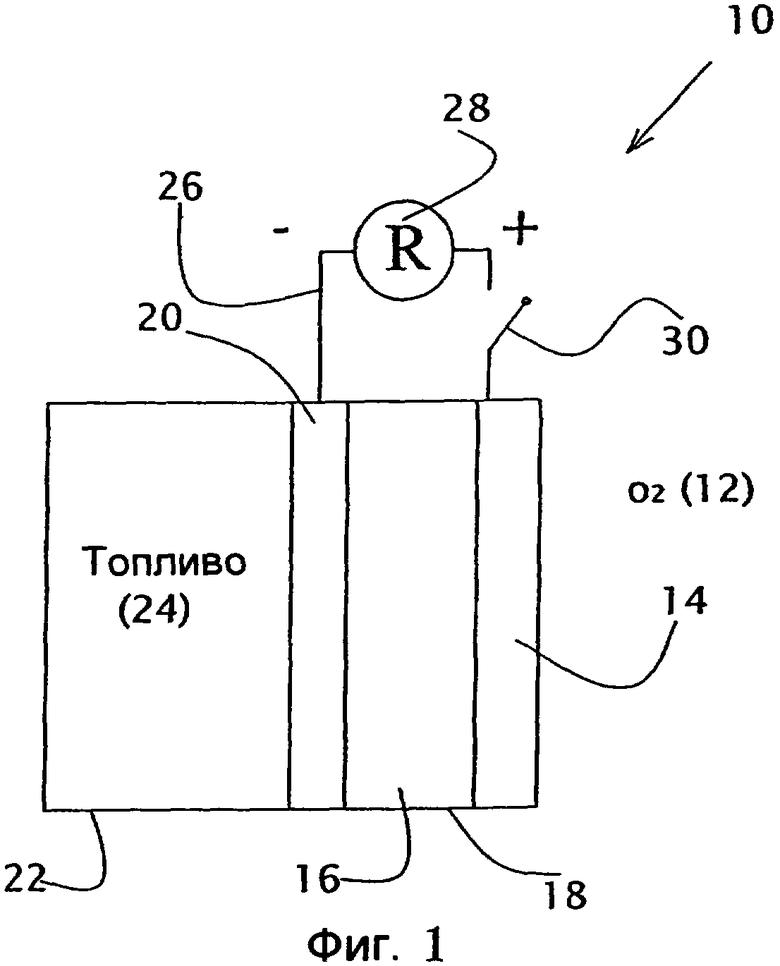
На фиг.1 схематически показано, что топливный элемент 10, состоящий из электролитной камеры 12, которая имеет с разных сторон катод 14 и анод 16 и содержит электролит. Катод 14 и анод 16 показаны соединенными электрической нагрузкой 20 и амперметром 22, предназначенным для измерения электрического тока, протекающего через электрическую нагрузку 20. С другой стороны анода 16 электролитной камеры 12 находится топливная камера 18, содержащая топливный раствор. Окислителем является атмосферный кислород, достигающий катода 14 с другой стороны катода 14 от электролитной камеры 12. В конкретном топливном элементе 10, который использовался в экспериментах, приведенных здесь, объем электролитной камеры 12 составлял 2 см3, объем топливной камеры 18 составлял 15 см3, а площадь каждого из электродов 14 и 16 составляла 4 см2. Катод 14 был изготовлен трафаретной печатью 20% платины на активированном угле на водонепроницаемую бумагу. Анод 16 был изготовлен трафаретной печатью 20% платины и 10% рутения на активированном угле на гидрофильную углеродистую бумагу.
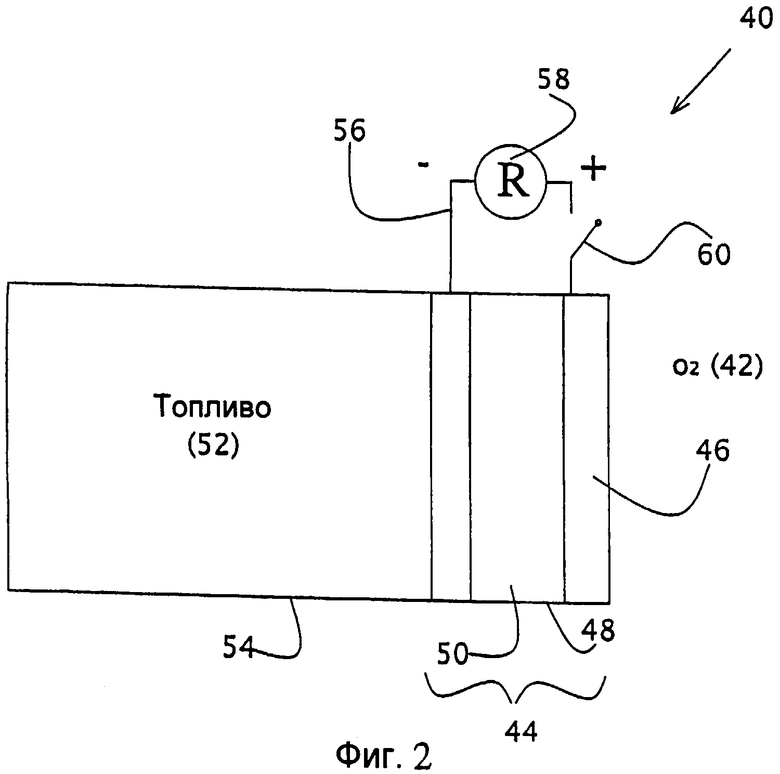
Емкость топливного элемента 10 измерялась с применением различных концентраций NaBH4 в 3,3 М водном топливном растворе NaOH в топливной камере 18, но с применением 6М водного электролита KOH в электролитной камере 12. Эффективная масса NaBH4 mF была определена как функция исходной концентрации NaBH4 с применением закона Фарадея
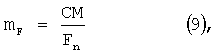
где С - измеряемая емкость, А·ч, F=26,8 А·ч/моль - постоянная Фарадея, М=38 г/моль - молекулярная масса NaBH4 и n=8 - количество электронов, которое образовывается анионом ВН4 - по уравнению (7). Результаты приведены в графическом виде на фиг.2. mF увеличивается вместе с увеличением исходной концентрации NaBH4, однако нелинейно. Чем выше исходная концентрация NaBH4, тем менее эффективно используется NaBH4. Кроме того, когда содержание NaBH4 в топливном растворе превышает приблизительно 50 г/л, происходит интенсивное разложение топлива на аноде 16. Это, в свою очередь, приводит к активному выделению газа и образованию пены, колебаниям анодного процесса и постепенному разрушению анода 16. Повышенная исходная концентрация NaBH4 также вызывает перетекание NaBH4 через анод 16 и электролит к катоду 14.
Таким образом, очевидны необходимость и полезность такой топливной смеси для топливных элементов, которая обеспечивала бы применение гидридных топлив с использованием всех их возможностей.
Краткое изложение сути изобретения
В соответствии с этим изобретением предложена топливная смесь, содержащая: (а) растворитель; (b) первую часть первого топлива, растворенную в упомянутом растворителе; и (с) вторую часть первого топлива, суспендированную в упомянутом растворителе.
В соответствии с этим изобретением предложен также способ выработки электрической энергии, который включает операции: (а) подготовки топливного элемента, содержащего катод и анод; (b) приведение в контакт окислителя с катодом; и (с) приведение в контакт топливной смеси с анодом, причем упомянутая топливная смесь содержит: (i) растворитель; (ii) первую часть топлива, растворенную в упомянутом растворителе; (iii) вторую часть упомянутого топлива, суспендированную в упомянутом растворителе.
Предметом изобретения является топливная смесь для топливных элементов, в которых первое топливо хранится в двух формах. Первая часть первого топлива хранится в виде раствора в растворителе. Вторая часть упомянутого первого топлива хранится в виде суспензии в растворителе. Эффективной концентрацией первого топлива является концентрация этого первого топлива в растворе, и эта концентрация поддерживается достаточно низкой для предотвращения нежелательных побочных эффектов, таких как разложение упомянутого первого топлива на аноде и разрушение упомянутого анода. В течение исчерпания растворенного первого топлива оно заменяется за счет растворения суспендированного первого топлива. Эффективная масса упомянутого первого топлива является близкой к общей массе двух этих частей первого топлива.
Предпочтительно растворитель представляет собой полярный растворитель, такой как вода. Предпочтительно концентрация растворенного первого топлива является концентрацией насыщения этого первого топлива в растворителе. В процессе эксплуатации топливного элемента при расходовании растворенного первого топлива оно заменяется в растворе упомянутым суспендированным первым топливом, поддерживая таким образом растворенную часть первого топлива на уровне его концентрации насыщения.
Предпочтительно упомянутым первым топливом является соль, анион которой является продуктом электродной реакции восстановления в растворителе, причем этот анион имеет стандартный потенциал восстановления, более отрицательный, чем стандартный потенциал восстановления водородного электрода в таком растворителе. Например, BH4 -, представляющий собой анион NaBH4, является анионом, который образовывается во время электродной реакции восстановления (в воде)
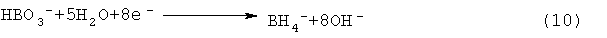
и имеет стандартный потенциал восстановления, равный -1,24 В.
Предпочтительно первым топливом является гидрид, такой как LiAlH4, NaBH4, LiBH4, (СН3)3NHBH3, NaAlH4, NaCNBH3, СаН2, LiH, NaH или KH. Более предпочтительно первым топливом является NaBH4. Другими предпочтительными топливами являются Na2S2O3, Na2HPO3, Na2HPO2, K2S2O3, K2HPO3, K2НРО2, NaCOOH и KCOOH, которые, подобно упомянутым гидридам, являются солями, анионы которых имеют в воде стандартный потенциал восстановления, более отрицательный, чем стандартный потенциал восстановления водородного электрода в воде. Для растворителей вообще, предпочтительные топлива для каждого конкретного растворителя содержат соли, анионы которых имеют стандартный потенциал восстановления в таком растворителе, более отрицательный, чем стандартный потенциал восстановления водородного электрода в таком растворителе. Предпочтительно массовая доля первого топлива составляет от приблизительно 0,1% до приблизительно 80% топливной смеси. Наиболее предпочтительно массовая доля первого топлива составляет от приблизительно 5% до приблизительно 25% топливной смеси.
Факультативно топливная смесь по этому изобретению также содержит спирт, например, метанол, этанол, пропанол, бутанол, пентанол, гексанол, этиленгликоль или глицерин. Предпочтительно массовая доля спирта составляет от приблизительно 0,1% до приблизительно 50% топливной смеси. Наиболее предпочтительно массовая доля спирта составляет от приблизительно 1% до приблизительно 25% топливной смеси. Спирт выполняет четыре функции:
1) спирт представляет собой второе топливо, которое окисляется вместе с первым топливом на аноде топливного элемента;
2) спирт регулирует растворимость первого топлива в растворителе, обеспечивая не слишком высокую концентрацию насыщения первого топлива;
3) как и в заявке WO/02/054506, относительно NaBH4, спирт представляет собой ингибитор разложения первого топлива на аноде топливного элемента;
4) спирт своим наличием стабилизирует суспензию в растворе первого топлива в растворителе согласно такой пропорции, которая делает плотность раствора практически равной плотности суспендированной части первого топлива таким образом, что эта суспендированная часть первого топлива не выпадает в осадок или всплывает на поверхность, а остается суспендированной.
В объем этого изобретения входит также применение любой пригодной примеси, которая добавляется с любой целью, указанной в этих четырех пунктах, однако спирты являются предпочтительными примесями.
Предпочтительно топливная смесь по данному изобретению содержит примесь для стабилизирования растворенной части первого топлива в растворителе. Предпочтительно такой примесью являются щелочи, такие как LiOH, NaOH или KOH, или основные соли. Предпочтительно такая примесь содержится в растворителе в концентрациях от приблизительно 0,1 моль/л до приблизительно 12 моль/л. Наиболее предпочтительно такая примесь содержится в растворителе в концентрациях от приблизительно 0,2 моль/л до приблизительно 5 моль/л.
Осборг (Osborg) в патенте США №4081252 описывает топливную смесь, предназначенную скорее для сжигания, чем для применения в топливном элементе. Она, подобно данному изобретению, содержит "носитель водорода", такой как гидразин, производные гидразина или неорганические борогидриды, которые, согласно реферату этого патента, могут быть растворены или суспендированы в основном топливе. Однако все примеры, приведенные Осборгом, касаются носителей водорода, растворенных в основном топливе. У Осборга не отмечено ни одно применение, которое касается как растворенных, так и суспендированных в основном топливе носителей водорода.
Объем данного изобретения включает в себя также топливный элемент, который питается топливной смесью по данному изобретению, а также и способ выработки электрической энергии с применением такого топливного элемента.
Краткое описание фигур
Суть изобретения объясняется только в виде примера со ссылкой на сопроводительные чертежи, на которых:
фиг.1 - схематическое изображение топливного элемента;
фиг.2 - график зависимости эффективной массы NaBH4 от исходной концентрации NaBH4 в составе нескольких известных топливных смесей;
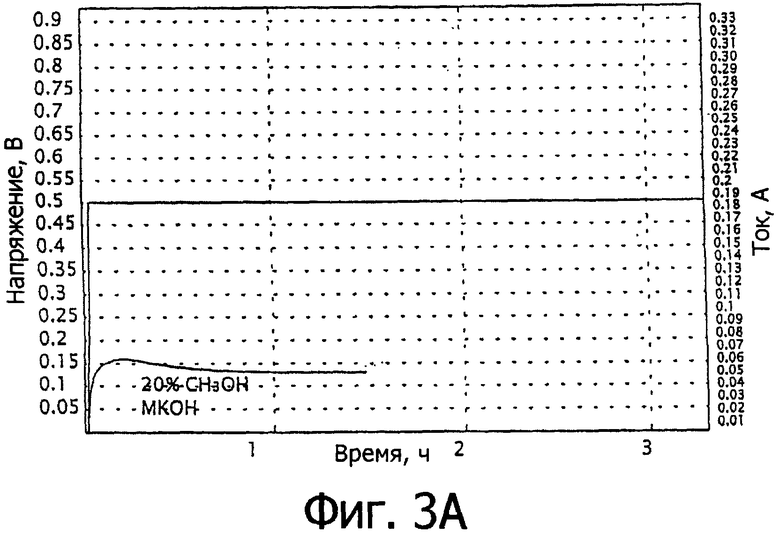
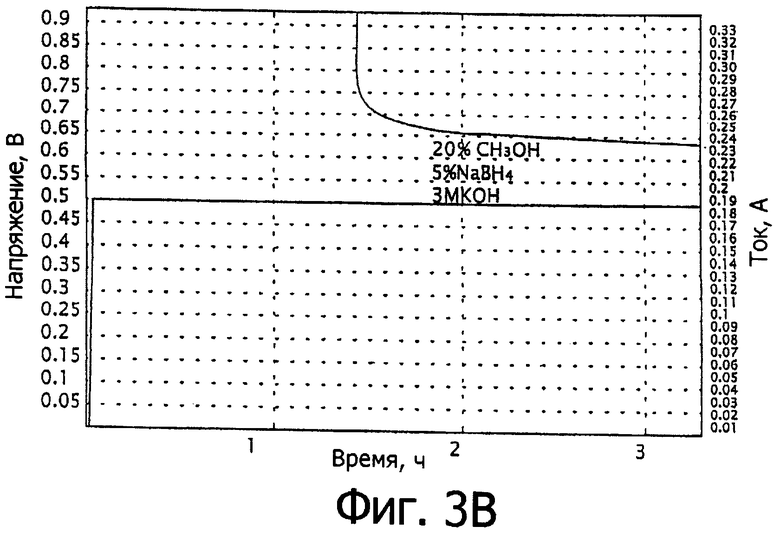
фиг.3 - графики электрического тока и емкости топливного элемента, изображенного на фиг.1, для топливной смеси по данному изобретению в сравнении с известными топливными смесями.
Описание предпочтительных вариантов осуществления
Предметом данного изобретения является топливная смесь, которая может быть применена для выработки электрической энергии в топливном элементе. В частности, данное изобретение позволяет эффективно применять гибридное топливо в топливном элементе.
Принципы действия и работа топливной смеси для топливных элементов по данному изобретению может быть лучше понята при помощи сопроводительных фигур чертежей и соответствующего описания.
На фиг.1, кроме изображения конструкции известного топливного элемента, также показан топливный элемент по данному изобретению, в котором топливная смесь по данному изобретению заменяет известную топливную смесь в топливной камере 18.
Топливная смесь по данному изобретению была подготовлена путем изготовления насыщенного раствора NaBH4 в количестве 45 мас.% в 3М водном растворе KOH в количестве 43 мас.% и добавления твердого порошкового NaBH4 с перемешиванием при помощи магнитной мешалки с целью образования суспензии NaBH4 в растворе KOH, насыщенном NaBH4. Средний размер частиц NaBH4 составлял приблизительно 10 мкм, а 90% частиц NaBH4 имели размер меньше, чем 100 мкм. Суспензия стабилизировалась при помощи добавления 12% глицерина по объему как диспергатора. 10% глицериновый диспергатор, придавая раствору KOH, насыщенному NaBH4, плотность 1,12 г/см2, также поддерживает равномерное распределение частиц NaBH4 в суспензии. Глицериновый диспергатор также удерживает в суспензии продукт реакции NaBO2, предотвращая снижение этим продуктом реакции каталитической активности на аноде 16, а также предотвращая снижение этим продуктом эффективности использования топлива. Исходное соотношение суспендированного NaBH4 к растворенному NaBH4 составляло 1:1. Электрический ток, который производился топливным элементом 10, а также соответствующая емкость (интегрированный ток) измерялись для топливного элемента 10, который питался этой топливной смесью, в сравнении с раствором NaBH4 в 3М водном растворе NaOH. Концентрация растворенного NaBH4 как в топливной смеси по данному изобретению, так и в известном топливном растворе, составляла 1,25М, что является концентрацией насыщения NaBH4 в водном растворе KOH. Нагрузка 20 была зафиксирована на уровне 0,5 В. На Фиг.3 показаны электрические токи в мА (левая ордината), а также емкости в мА·ч (правая ордината), как функции от времени в часах. Кривые, обозначенные «а», соответствуют известному топливному раствору, а кривые, обозначенные «b», соответствуют топливному раствору по данному изобретению. Топливная смесь по данному изобретению обеспечивает более стабильный электрический ток и большую емкость по сравнению с известным топливным раствором.
Несмотря на то, что изобретение было описано относительно ограниченного количества вариантов осуществления, понятно, что могут быть выполнены много вариантов, усовершенствований и применений данного изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ЖИДКОГО ТОПЛИВА ДЛЯ ЭЛЕКТРОХИМИЧЕСКИХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ И ТОПЛИВНЫЙ ЭЛЕМЕНТ НА ЕЕ ОСНОВЕ | 2002 |
|
RU2265643C2 |
| ЭЛЕКТРОЛИТ ДЛЯ ТОПЛИВНОГО ЭЛЕМЕНТА ПРЯМОГО ЭЛЕКТРООКИСЛЕНИЯ БОРГИДРИДОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ | 2009 |
|
RU2396640C1 |
| ТОПЛИВНЫЙ ЭЛЕМЕНТ И ЕГО ПРИМЕНЕНИЕ | 2006 |
|
RU2394311C2 |
| НЕ СОДЕРЖАЩИЕ ПЛАТИНУ ЭЛЕКТРОКАТАЛИТИЧЕСКИЕ МАТЕРИАЛЫ | 2003 |
|
RU2316850C2 |
| ТОПЛИВА ДЛЯ ГЕНЕРИРУЮЩИХ ВОДОРОД БАЛЛОНЧИКОВ | 2006 |
|
RU2444472C2 |
| ПОРТАТИВНЫЙ ИСТОЧНИК ТОКА | 2009 |
|
RU2396639C1 |
| ИСТОЧНИК ТОКА ПОРТАТИВНЫЙ | 2009 |
|
RU2402119C1 |
| ПРИМЕНЕНИЕ СЕРОСОДЕРЖАЩИХ ТОПЛИВ ДЛЯ ПРЯМООКИСЛИТЕЛЬНЫХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ | 2001 |
|
RU2280297C2 |
| Электрохимические вторичные элементы для применения в высокоэнергетических и высокомощных батареях | 2016 |
|
RU2721079C1 |
| ИСТОЧНИК ТОКА ПОРТАТИВНЫЙ | 2009 |
|
RU2402118C1 |
Изобретение относится к суспензионным топливным смесям для применения в электрохимических топливных элементах, способу производства электрической энергии с применением таких суспензионных топливных смесей, а также к топливным элементам, использующим такие суспензионные топливные смеси для производства электрической энергии. Технической задачей изобретения является необходимость получения топливной смеси для топливных элементов, которая обеспечивала бы применение гидридных топлив с использованием всех их возможностей. Поставленная задача решается тем, что топливная смесь содержит растворитель; первую часть первого топлива, растворенную в растворителе, причем концентрация первой части первого топлива представляет собой ее концентрацию насыщения и первое топливо выбрано из группы, которая включает Na2S2O3, Na2HPO3, Na2HPO2, K2S2О3, K2НРО3, K2HPO2, NaCOOH и KCOOH; вторую часть первого топлива, суспендированную в растворителе; первую добавку для стабилизации первой части первого топлива в растворителе; вторую добавку для стабилизации суспензии. 4 н. и 31 з.п. ф-лы, 3 ил.
растворитель;
первую часть первого топлива, растворенную в растворителе, причем концентрация первой части первого топлива представляет собой ее концентрацию насыщения и первое топливо выбрано из группы, которая включает Na2S2O3, Na2НРО3, Na2НРО2, K2S2О3, K2НРО3, K2НРО2, NaCOOH и KСООН;
вторую часть первого топлива, суспендированную в растворителе;
первую добавку для стабилизации первой части первого топлива в растворителе;
вторую добавку для стабилизации суспензии.
растворитель;
первую часть первого топлива, растворенную в растворителе, причем концентрация первой части первого топлива представляет собой ее концентрацию насыщения;
вторую часть первого топлива, суспендированную в растворителе;
первую добавку для контроля растворимости топлива в растворителе;
вторую добавку, для стабилизации первой части указанного топлива в растворителе;
третью добавку для стабилизации суспензии.
растворитель;
первую часть первого топлива, растворенную в растворителе, причем концентрация первой части первого топлива представляет собой ее концентрацию насыщения;
вторую часть первого топлива, суспендированную в растворителе; и
первую добавку, которая выполняет функцию ингибитора разложения первого топлива на аноде топливного элемента;
вторую добавку для стабилизации первой части первого топлива в растворителе;
третью добавку для стабилизации суспензии.
Приоритет по пунктам:
| US 3346506, 10.10.1967 | |||
| US 3460906, 12.08.1969 | |||
| СПОСОБ ПРОИЗВОДСТВА ЭЛЕКТРИЧЕСКОЙ ЭНЕРГИИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1990 |
|
RU2027046C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ТОПЛИВНЫХ ЭЛЕМЕНТОВ С ПРОДОЛЬНОЙ ВЫЕМКОЙ, ЗАПОЛНЕННОЙ ЗАЖИГАТЕЛЬНЫМ СОСТАВОМ, И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1992 |
|
RU2024594C1 |
Авторы
Даты
2008-09-27—Публикация
2003-07-29—Подача