Предлагаемое изобретение относится к областям биологии, биотехнологии, биохимии, физико-химической биологии, медицины, а именно, к дифференциальным титрационным калориметрам.
Для точных количественных расчетов по результатам измерений на дифференциальном титрационном калориметре необходимо, чтобы данный прибор позволял выполнять калибровку шкалы измеряемой мощности во всем диапазоне рабочих температур и при любых изменяющихся условиях эксперимента.
Известен изотермический дифференциальный титрационный калориметр [1], содержащий систему титрования с перемешиванием, тепловой экран и пару одинаковых калориметрических камер: эталонную и рабочую. Каждая камера объемом 1.4 мл - это полностью заполняемый сосуд, имеющий форму монеты. Камера имеет длинную узкую трубку, через которую исследуемые образцы вводятся или удаляются при помощи шприцов с длинными иглами. Каждая камера имеет два фототравленных нагревателя, расположенных одинаково на одной плоской внешней поверхности, в то время как вторая плоская поверхность камеры примыкает к специальному термоэлектрическому устройству, содержащему 264 кристалла теллурия висмута.
Шприцы для титрования объемом от 25 до 250 мкл - это точные стеклянные шприцы, длинные иглы которых из нержавеющей стали имеют на конце прикрепленную перемешивающую лопасть. Шприц для титрования помещается в узел подшипников, обладающих низким трением, который содержит встроенное времязадающее колесо. Этот перемешивающий узел со шприцом легко устанавливается внутрь тефлонового загружающего цилиндра, и времязадающее колесо сцепляется с точным перемешивающим двигателем. Весь этот узел непрерывно вращается в течение эксперимента со скоростью 400 об/мин (управляемый с помощью цифрового тахометра) и производит полное смешивание в камере в пределах нескольких секунд после титрования, что было установлено визуально. Эта базовая линия в присутствии перемешивания используется как исходная базовая линия. Таким образом, не требуется коррекция тепла из-за теплового эффекта перемешивания. Плунжер шприца механически соединен с точным цифровым шаговым двигателем (6400 шаг/дюйм). Эксперимент титрования (число титрований, объем добавки, время между титрованиями) устанавливается с помощью интерактивного ПО и выполняется без участия оператора. Все данные сохраняются на диске. Разностный сигнал мощности цепи обратной связи опрашивается с интервалом 33 мс и усредняется цифровым фильтром, выбранным оператором. Каждая усредненная точка регистрируется. При фильтрации среднеквадратичный шум на минутном интервале обычно составляет 5-10 нкал/с, когда используется нуль-детектор Keithly в качестве предусилителя в цепи обратной связи ячеек. Калибровка шкалы дифференциальной мощности может проводиться или электрически посредством ввода с клавиатуры, который активирует калибровочный нагреватель рабочей ячейки, или химически посредством титрования растворов, имеющих известную теплоту реакции. Однако, поскольку мешалка существует в контакте с реагентами и внутренней средой, то она становится теплопроводящим путем, который влияет на проведение эксперимента при температуре, отличной от температуры окружающей среды. Это приводит как к нестабильности измерений, так и к значительному снижению величины регистрируемой измерительной термобатареей мощности теплового эффекта из-за ее потерь за счет теплопередачи во внешнюю среду через вал мешалки. Кроме того, нагревательные элементы расположены на внешних поверхностях калориметрических камер. При такой конструкции нагревателя не обеспечивается равенство подводимой к нагревателям камер при компенсационном методе измерений электрической мощности, измеряемой мощности тепловых процессов, протекающих в калориметрических камерах, и усложняет калибровку калориметра.
Известен изотермический дифференциальный титрационный калориметр [2]. В нем также имеется вал с мешалкой, а нагреватель также выполнен на внешней поверхности калориметрических камер. Таким образом, этому титрационному калориметру присущи перечисленные в полной мере все недостатки аналога [1]: имеются потери мощности измеряемого теплового эффекта за счет теплопередачи во внешнюю среду через вал мешалки; при компенсационном методе измерений мощности теплового эффекта регистрируется только часть мощности измеряемого теплового эффекта, что усложняет калибровку калориметра. I.Wadso, говоря о калибровке калориметров, отмечает, что конструкция нагревателя, его размещение в калориметрической камере, теплопроводность материала камеры, эффективность перемешивания и др. могут привести к существенной систематической ошибке [3].
Наиболее близким по технической сущности является капиллярный дифференциальный титрационный калориметр [4], содержащий измерительные части капиллярных калориметрических камер, заключенные в термостатирующую оболочку, инъекционное устройство подачи реагента в камеры, содержащее дозирующую иглу для рабочей камеры и дозирующую иглу для эталонной камеры, устройство приведения игл инъекционного устройства в колебательное движение, пассивный тепловой шунт, охватывающий часть калориметрических камер и соединенный с термостатирующей оболочкой, активный тепловой шунт, расположенный вне термостатирующей оболочки и охватывающий пассивную часть капиллярных калориметрических камер, выполненных в виде прямых капилляров, средство измерения мощности тепловых процессов, происходящих в калориметрических камерах, устройство линейного перемещения инъекционного устройства вдоль оси калориметрических камер.
Впервые в мировой практике этот титрационный калориметр имеет калориметрические камеры в виде протяженных капилляров, расположенных горизонтально. Данный калориметр имеет преимущества перед современными аналогами благодаря новой системе перемешивания реагентов в калориметрических камерах, точной системе выделения измерительного объема, принципиально новой системе введения добавки в калориметрические камеры. Этот калориметр позволяет вести исследования на качественно новом уровне. Современные известные титрационные калориметры накладывают ограничения на выполнение таких работ, так как даже после завершения введения добавки происходит диффузия растворителя через сопло иглы в камеру, что приводит к недопустимой ошибке из-за паразитных тепловых эффектов, во много раз превышающих по мощности измеряемую мощность реакции. Капиллярной титрационный калориметр измеряет тепловую мощность каталитической реакции в данном процессе благодаря новой системе дозирования. В нем предусмотрен режим ввода добавки подвижной иглой, которая по окончании дозирования выводится из зоны чувствительного (рабочего) объема калориметрических камер, что исключает регистрацию паразитного тепла в процессе длительного измерения. Таким образом, обеспечена возможность измерения тепловой мощности каталитической реакции, которая на два порядка меньше паразитной тепловой мощности смешения в камере растворителя с образцом.
Кроме того, данное решение титрационного калориметра расширило круг объектов, изучаемых на титрационном калориметре, дисперсными системами. При этом равномерное распределение добавки по длине камеры и присутствие в камере вибрирующей иглы исключает образование осадка в камере, что является обязательным условием качественного проведения эксперимента. Новое построение калориметра обеспечивает введение иглы с титрантом в калориметрическую камеру без каких-либо ограничений на режим ввода добавки в камеру. Максимальная скорость введения иглы равна 13.7 мм/с. При прохождении иглой зоны активного теплового шунта обеспечивается выравнивание температур иглы и камеры. Принудительная турбулизация жидкости, характеризуемая коэффициентом Рейнольдса порядка 17 при температуре 30°С, образуется вибрирующей дозирующей иглой, что обеспечивает эффективность теплового шунта и исключает необходимость предварительного термостатирования добавки.
В капиллярном дифференциальном титрационном калориметре измеряемая тепловая мощность при взаимодействии вводимой добавки с исследуемым образцом возникает в области дозирующего отверстия иглы, перемещающейся равномерно по всей длине камеры в течение времени дозирования. При материалах калориметрической камеры с высокой температуропроводностью значительная часть измеряемой мощности теряется за счет теплопередачи по капилляру камеры на тепловой шунт. В худшем случае эта величина достигает 90%. Это не позволяет регистрировать всю энергию взаимодействия, что, соответственно, практически на порядок увеличивает допустимые концентрации реагентов при изучении взаимодействий, что, в свою очередь, на порядок снижает возможности прибора при оценке констант взаимодействия. При химической калибровке измеряется тепловая мощность взаимодействия образца с вводимой дозой титранта, которая при движении дозирующей иглы равномерно распределяется по длине рабочего объема камер. Измерение тепловой мощности исследуемых реагентов выполняется при точно таком же перемещении дозирующей иглы, т.е. условия калибровки идентичны условиям эксперимента, что определяет высокую точность измерений мощности регистрируемых процессов при химической калибровке шкалы измеряемой мощности. Недостатком данной калибровки является необходимость набора химических реагентов для всех условий работы прибора (температура, концентрация и др.). Из-за возникновения теплообмена между калориметрическими камерами и тепловым шунтом при взаимодействии образца с вводимым в камеру реагентом калибровка шкалы измеряемой мощности через нагреватель, установленный на поверхности камеры, в данном калориметре не применяется.
Задача изобретения - создание капиллярного дифференциального титрационного калориметра с электрической калибровкой, воспроизводящей измеряемые тепловые процессы в калориметрической камере, для обеспечения прецизионных измерений на данном калориметре во всем диапазоне температур и изменяющихся условий.
Решение задачи обеспечивает предлагаемый капиллярный дифференциальный титрационный калориметр, содержащий измерительные части капиллярных калориметрических, заключенные в термостатирующую оболочку, инъекционное устройство подачи реагента в камеры, содержащее дозирующую иглу для рабочей камеры и дозирующую иглу для эталонной камеры, устройство приведения игл инъекционного устройства в колебательное движение, пассивный тепловой шунт, охватывающий часть калориметрических камер и соединенный с термостатирующей оболочкой, активный тепловой шунт, расположенный вне термостатирующей оболочки и охватывающий пассивную часть капиллярных калориметрических камер, выполненных в виде прямых капилляров, средство измерения мощности тепловых процессов, происходящих в калориметрических камерах, устройство линейного перемещения инъекционного устройства вдоль оси калориметрических камер, отличающийся тем, что на конце дозирующей иглы рабочей камеры установлен малогабаритный резистор с первым и вторым электрическими выводами, а на дозирующей игле эталонной камеры установлены третий и четвертый электрические выводы, идентичные первому и второму выводам, при этом третий и четвертый выводы электрически соединены между собой на конце дозирующей иглы эталонной камеры, выходные концы второго и третьего выводов электрически соединены между собой, а выходные концы первого и четвертого выводов подсоединены к источнику электрической энергии.
На фиг.1 представлен капиллярный дифференциальный титрационный калориметр с электрической калибровкой шкалы измеряемой тепловой мощности, имеющий электрические выводы 1, 2, 3 и 4 нагревательного элемента 5, расположенного на конце дозирующей иглы для рабочей камеры 6. При этом выводы 1 и 2 расположены на игле для рабочей камеры 6, а выводы 3 и 4 расположены на игле для эталонной камеры 7. Предложенный калориметр имеет рабочую 6 и эталонную 7 калориметрические камеры в виде прямых капиллярных трубок с внутренним диаметром 2.0 мм. Полный объем калориметрической камеры равен 385 мкл, рабочий объем равен 224 мкл. Рабочим объемом калориметрических камер является объем части трубок, расположенный между дном камер и границей контакта с пассивным тепловым шунтом 8. Длина капилляров рабочего объема камер равна 50 мм. Калориметрические камеры заключены в термостатирующую оболочку 9. На выводных концах капилляров калориметрических камер установлен активный тепловой шунт 10, который снижает тепловой шум и исключает теплообмен калориметрических камер и пассивного теплового шунта с внешней средой через выводную часть капиллярных трубок. Данное построение не требует подводящих элементов в виде дополнительных трубок. Калориметрические камеры снабжены измерительной термобатареей 11. Калориметрические камеры, заключенные в термостатирующую оболочку 9, установлены в термохолодильник 12. На термостатирующей оболочке установлен датчик температуры 13, а на активном шунте установлен датчик температуры 14. Датчики температуры 13 и 14 подсоединены к многоканальному измерительному усилителю 15, связанному с компьютером 16, содержащим многоканальный АЦП и модуль PC-TIO-10, содержащий таймеры, связанные с блоком усилителей мощности 17, соединенным с нагревателем 18 термостатирующей оболочки и нагревателем 19 активного шунта. Калориметр снабжен измерителем мощности тепловых процессов, состоящим из термобатареи 11, связанной своим выходом со входом нановольтметра 20, который снабжен интерфейсом RS-232, связывающим нановольтметр с компьютером 16.
Калориметр снабжен инъекционным устройством, служащим для введения реагентов в калориметрические камеры и состоящим из шприца 21 для рабочей камеры и шприца 22 для эталонной камеры, размещенных в одном корпусе 23. Поршни дозирующих шприцов 24 и 25 объединены связывающей их пластиной 26. Для обеспечения введения реагентов в калориметрические камеры корпус шприцов связан с первым винтовым механизмом 27, а пластина связана со вторым винтовым механизмом 28. Винтовой механизм 27 приводится в движение шаговым двигателем 29, а винтовой механизм 28 - шаговым двигателем 30. Управление шаговыми двигателями осуществляется компьютером через блок усилителей мощности 17. Колебательный режим дозирующих игл обеспечивается вибрационным устройством 31, частота колебаний которого управляется компьютером через блок усилителей мощности 17.
Для калибровки шкалы измеряемой мощности используется нагреватель 5, снабженный выводами 1, 2, 3, 4, и источник электрической энергии блока усилителей мощности 17.
Предлагаемый дифференциальный титрационный калориметр работает следующим образом. Устанавливается заданная температура термостатирующей оболочки 9 в окне "Уставка температуры", затем камеры 6 и 7 и дозирующие шприцы 21 и 22 заполняются реагентами с помощью соответствующих заправочных шприцов.
В окне "Дозирование" устанавливается величина дозы вводимого реагента.
Устанавливается исходное положение дозирующих шприцов 21 и 22 из окна "Дозирование", при этом дозирующие иглы занимают положение максимального погружения в калориметрические камеры.
После окончания наблюдаемого в окне "Измерение" переходного процесса, связанного с введением игл в камеры, производится запуск архивирования данных.
Изотермические условия калориметрических камер дифференциального титрационного калориметра обеспечиваются термостатирующей оболочкой и активным тепловым шунтом, размещенными в термохолодильнике. Температура термостатирующей оболочки и активного теплового шунта автоматически регулируется по сигналам датчиков соответственно 13 и 14, связанных с компьютером через многоканальный измерительный усилитель. Сигналы с усилителя 15 поступают в компьютер на многоканальный АЦП. Сформированные сигналы ШИМ с выходов таймеров модуля PC-TIO-10 подаются в нагреватель термостатирующей оболочки и нагреватель шунта через усилитель мощности, обеспечивая автоматическое регулирование температуры в соответствии с уставкой, заданной на компьютере. Точное выделение рабочих объемов осуществляется шунтом 8, который охватывает часть калориметрических камер. В окне "Дозирование" производится подача дозы. Операция подачи дозы повторяется многократно в соответствии с заданной программой.
Дозирование реагентов осуществляется следующим образом. Заполненные реагентами шприцы посредством винтового механизма, приводимого во вращение шаговым двигателем 29, управляемого от компьютера через блок усилителей 17, устанавливаются в положение максимального погружения в заполненные реагентами калориметрические камеры.
После опускания шприцов осуществляется фиксация поршней планкой 26.
При введении дозы производится продольное перемещение шприцов механизмом 27 на всю длину калориметрических камер. Одновременно с этим производится перемещение поршней механизмом 28. За счет различной величины перемещений механизмов 27 и 28 шприцами осуществляется дозирование заданного количества реагентов. Возможен вариант дозирования из крайнего верхнего положения в сторону погружения игл в камеры.
Каждое новое дозирование производится из исходного положения.
Для приведения игл инъекционного устройства в колебательное движение с компьютера 16 подается сигнал заданной частоты, который через блок 17 подается на вибрационное устройство 31.
Тестирование калориметра проводилось с использованием принятых в мировой практике тестов [3].
На предлагаемом калориметре выполнено измерение теплоты связывания. Проводилось связывание жидких реагентов 18-Crown-6 [0,01 М] и Ва2+ [0,1 М] (Оба реагента получены от фирмы Sigma, США).
В рабочую и эталонную калориметрические камеры вводят по 224 мкл 18-Crown-6 при температуре 25°С. Затем в рабочую камеру по установленной временной программе вводят Ва2+, а в эталонную камеру - дистиллированную воду, дозами по 3.48 мкл 10 раз. Перемешивание вибрирующей иглой с амплитудой 1 мм и частотой 18.5 Гц.
В режиме измерения тепловой мощности без обратной связи сигнал с термобатареи 11, пропорциональный тепловой мощности, усиливается нановольтметром 20, снабженным интерфейсом RS-232, и поступает через него на компьютер, на котором регистрируется тепловая мощность как функция времени.
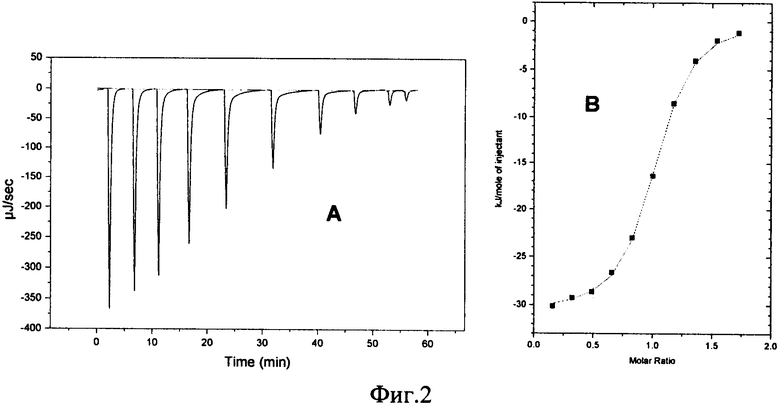
На фиг.2а представлены данные, полученные на предлагаемом калориметре при измерении взаимодействия Ва2+ [0,1 М] и 18-Crown-6 [0,01 М].
На фиг.2б представлена титрационная кривая по данным Фиг.2а.
Полученные при тестировании значения ΔН и константы связывания К: ΔН=31,77 кДж·моль-1, К=4389 моль-1 хорошо согласуются с эталонными значениями ΔН=31,42 кДж·моль-1, К=5900 моль-1 [3].
Включение в состав калориметра устройства приведения иглы инъекционного устройства в колебательное движение позволяет подтвердить полное смешивание реагентов в режиме диффузионного смешивания. Если данные ΔН и К, полученные в режиме диффузионного смешивания, равны ΔН и К, полученным в режиме использования колеблющейся иглы, то диффузионное смешивание обеспечивает полное смешение.
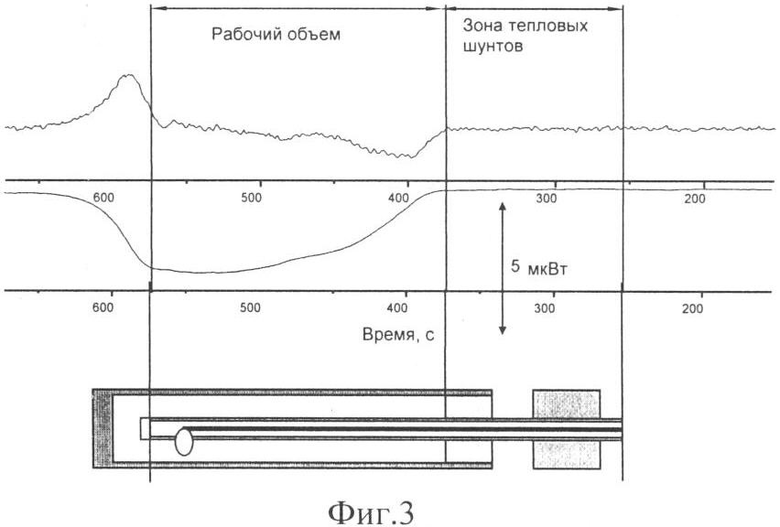
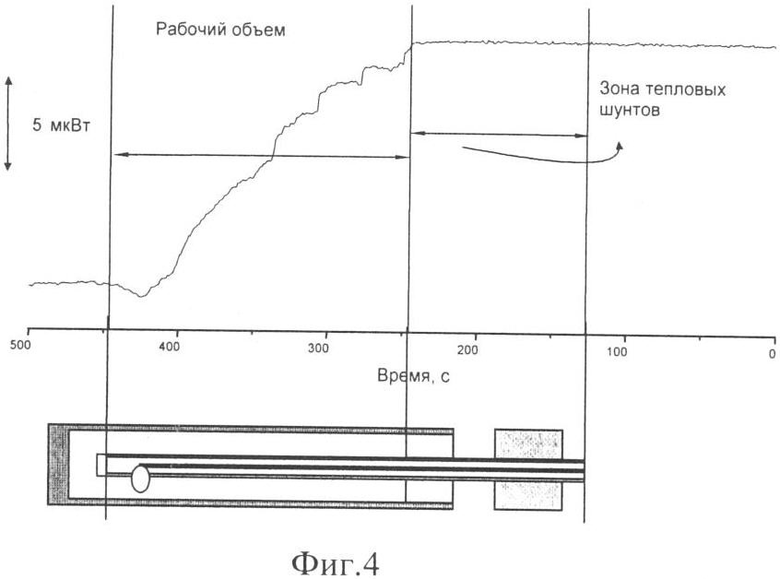
На фиг.3 представлены экспериментальные данные, иллюстрирующие работу тепловых шунтов при взаимодействии водного раствора спирта с водой (нижняя кривая), и кривая, полученная после дифференцирования нижней кривой. На фиг.4 представлена зарегистрированная калориметром мощность, вводимая в калориметрическую камеру одной колеблющейся иглой.
На Фиг.3 экспериментальные данные привязаны к калориметрической камере с шунтами, с обозначением зоны рабочего объема и зоны тепловых шунтов. Эти данные показывают, что тепловые процессы, происходящие в зоне тепловых шунтов, не распространяются в рабочем объеме калориметрических камер, а шунтируются тепловым шунтом. Соответственно, тепловые шумы от движения дозирующей иглы и от термостатирующей оболочки гасятся тепловым шунтом, в результате чего калориметр регистрирует только тепловые процессы, происходящие в рабочем объеме.
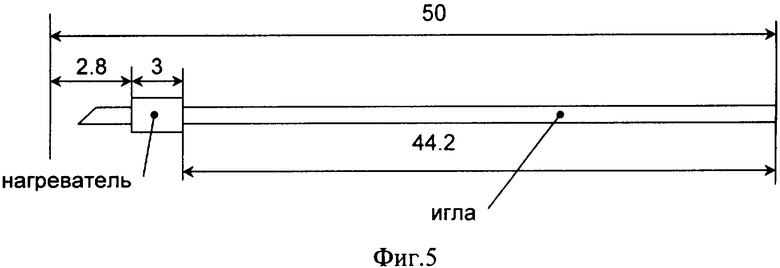
На фиг.5 представлен калибровочный нагреватель. Данный нагреватель выполнен малогабаритным, имеет номинал 0.926 Ом и установлен на конце дозирующей иглы одной из камер, например, рабочей камеры. На каждой из дозирующих игл установлено по два электрических вывода, через которые протекает один и тот же калибровочный ток. Данные выводы имеют одинаковое сопротивление и идентичны по геометрии, что при дифференциальной схеме калориметра дает нулевой сигнал от тепловых мощностей, выделяющихся в выводах при калибровке. Таким образом, калориметром регистрируется только тепловая мощность, выделяемая в калибровочном нагревателе. При этом данная тепловая мощность выделяется практически в тех же условиях, что и тепловая мощность от взаимодействия дозируемого реагента с образцом. Действительно, в обоих случаях тепловая мощность выделяется в зоне дозирующего сопла, которое перемещается по всей длине камеры. Таким образом, этот режим позволят воспроизвести при калибровке условия реального эксперимента, в том числе и при вибрирующей игле.
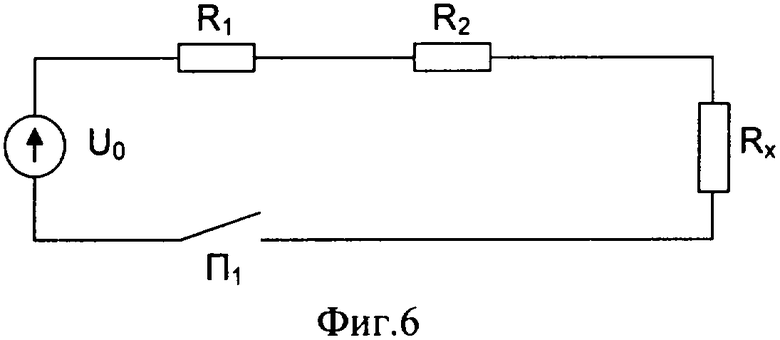
На фиг.6 представлена электрическая схема калибровки по электрической мощности для предложенного калориметра. Калибровочный ток: J=U0/R=10.1921·10-3 А и калибровочная мощность: РΔR=J2·ΔR=96.191861·10-6 Вт для конкретного примера калибровки, где R1=2.028 Ом, R2=2.954 Ом, Rx=150.04 Ом, U0=1.58 B, T=25°С; калибровочный нагреватель: ΔR=R2-R1=0.926 Ом; суммарное сопротивление калибровочной цепи: R=R1+R2+Rx=155.022 Ом.
Расчет тепловой энергии калибровки выполнен при следующих условиях: скорость перемещения иглы: V=50[мм]/200[с]=0.25 [мм/с]; время перемещения выводов: t1=L1/V=44.2/0.25=176.8 [с]; время перемещения нагревателя: t2=L2/V=3/0.25=12 [с].
Тепловая энергия калибровки: Q=РΔR·t1+(1/2)·РΔR·t2 и ее расчетное значение: Q=96.192·10-6 [Вт]·(176.8+12/2)[с]=17584·10-6 [Дж].
При калибровке шкалы измеряемой мощности дозирующая игла с нагревательным элементом вводится в рабочую камеру на всю ее длину. В режиме калибровки на время извлечения из камеры нагревателя в него подается известная электрическая мощность Q=96.192·10-6 [Вт]. При этом регистрируется на компьютере первый тепловой эффект (фиг.7). Аналогично может быть проведена калибровка при введении калибровочного нагревателя в камеру. Этот вариант калибровки дает второй тепловой эффект (фиг.7). Площади этих зарегистрированных тепловых эффектов одинаковы и равны 2050260 (интеграл оцифрованного сигнала). Соответственно, для калибра с энергией, равной 17584·10-6 [Дж], калибровочный коэффициент К равен 8.5764·10-9 Дж/ед. площади.
Сопоставление результатов электрической и химической калибровок выполнено с учетом следующих данных. Стандартные значения по барию: температура 25°С, энергия первого пика 42 мДж, объем добавки бария (0.1М) 14 мкл, объем камеры 900 мкл 18-crown-6 (0.01 M).
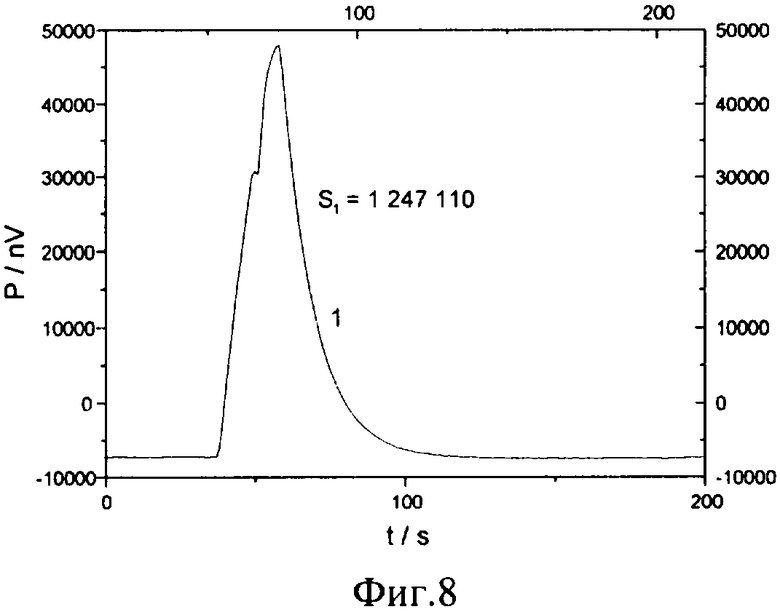
На объем камеры капиллярного калориметра 224 мкл соответственно уменьшена добавка до 3.484 мкл. Данной добавке должна соответствовать энергия, равная 10.7278 мДж (использовано 49 мм камеры) [3.41432 мкл · 0.1 М · 31.42 кДж/моль]. Площадь пика, зарегистрированного на капиллярном калориметре, равна 1247110 (фиг.8). Используя электрическую калибровку, получаем энергию теплового эффекта 10.6957 мДж. Таким образом, данные химической калибровки и электрической калибровки практически одинаковы, так как воспроизводятся с погрешностью 0.3%, что отвечает точностным требованиям экспериментальных исследований на титрационных калориметрах.
По данным термограммы (фиг.8) чувствительность калориметра 50 нВт при фильтрации (скользящее среднее) по 20 точкам. Масштабный коэффициент шкалы мощностей равен 1 мкВт/148.98 нВ.
Результаты эксперимента
На капиллярном калориметре выполнены следующие эксперименты.
Модельная реакция гидролиза модельного субстрата этилового эфира N-α-бензоил-L-аргинина (ВАЕЕ) трипсином в режиме единичной инъекции.
Термограмма реакции была преобразована в зависимость концентрации субстрата, [S], от времени, t, и обработана по уравнению Михаэлиса-Ментен:
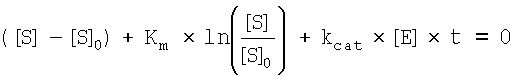
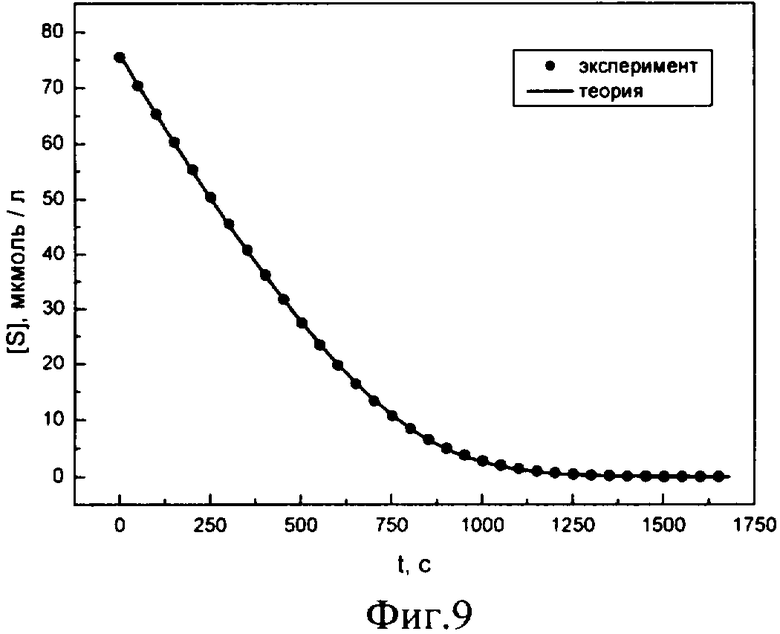
где [S]0, Km, kcat, [E] - начальная концентрация субстрата, константа Михаэлиса, каталитическая константа и концентрация фермента, соответственно. Кинетика гидролиза этилового эфира N-α-бензоил-L-аргинина (ВАЕЕ) трипсином получена по данным титровальной калориметрии: [S]0=76 мкмоль/л, [Е]=4.73 нмоль/л, 200 мМ Трис-HCl, рН 8.0, 50 мМ CaCl2, 0.2% ПЕГ-8000, 25°С. Эти данные приведены на фиг.9, где точки - экспериментальные данные, а кривая - рассчитана по уравнению Михаэлиса-Ментен, значения констант уравнения Михаэлиса-Ментен в табл.1.
Видно, что значения кинетических параметров гидролиза ВАЕЕ трипсином, полученные методом титровальной калориметрии, практически совпадают с литературными данными.
Сравнения каталитических свойств р- и s-фракций сополимеров N-винилкапролактама (НВКЛ) с N-винилимидазолом (НВИА) с соотношением НВКЛ: НВИА=85:15 моль/моль, синтезированных при 25 и 65°С.
Как известно, р- и s-фракции отличаются по растворимости в воде при температурах выше НКТР (нижняя критическая температура растворения) поли(N-винилкапролактама), ˜30°С. В этих условиях р-фракция осаждается из раствора, а s-фракция остается растворимой. Существует принципиальное различие между s-фракциями сополимеров, синтезированных при 25 и 65°С. s-Фракция сополимера, синтезированного при 65°С, (ts65) претерпевает кооперативный переход при нагревании из конформации статистического клубка в конформацию типа полимерной глобулы. Поскольку важнейшим свойством такой конформации является отсутствие глобальных флуктуаций пространственного распределения звеньев, можно было ожидать, что фракция ts65 будет превосходить остальные фракции по каталитическим свойствам.
В качестве тестовой реакции была выбрана реакция гидролиза п-нитрофенилпропионата при рН 7.3. Как правило, исходные концентрации сополимеров и субстрата были равны 2.6 мг/мл (3.0 мМ НВИА) и 2.4 мМ, соответственно. В качестве титранта использовали запасной раствор субстрата в ацетонитриле. Выбор этого растворителя был продиктован стремлением уменьшить паразитный тепловой эффект, связанный с разбавлением растворителя при инъекции титранта в водный раствор сополимера. После релаксации паразитного сигнала разбавления ацетонитрила выход калориметра на стационарный режим, соответствующий регистрации стационарной реакции гидролиза, достигался за 10-15 мин. Измерения были проведены при 25 и 50°С, т.е. ниже и выше температуры осаждения р-фракций и температуры конформационного перехода фракции ts65. Для нормировки тепловой мощности реакции гидролиза использовали значение стандартной энтальпии гидролиза одной сложноэфирной связи триацетина ΔH0=-95.2 кДж/моль [6]. Полученные значения начальной скорости гидролиза приведены в табл.2, где 1)ts25, tp25 - s- и р-фракции, синтезированные при 25°С; ts65, tр65 - s- и p-фракции, синтезированные при 65°С.
Полученные данные свидетельствуют, что кооперативный переход фракции ts65 в глобулярное состояние при нагревании приводит к значительному (более чем на порядок) увеличению ее каталитической эффективности. Этот результат наглядно подтверждает генеральную концепцию выполняемого проекта о том, что важнейшим условием проявления каталитической активности является подавление глобальных флуктуаций полимерной цепи в результате перехода клубок-глобула.
Определение каталитических параметров сополимеров.
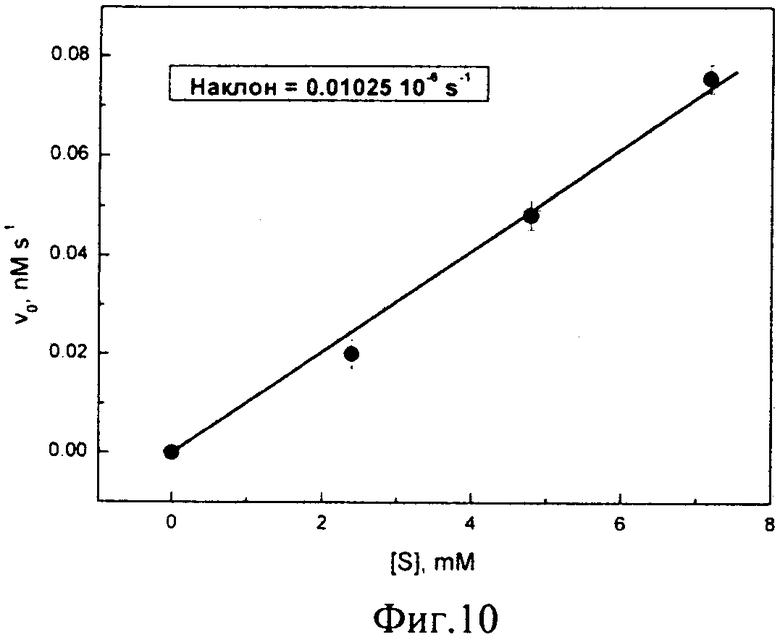
На фиг.10 дана зависимость начальной скорости гидролиза п-нитрофенилпропионата от его концентрации при 25°С для фракции ts65 в режиме многократной последовательной инъекции запасного раствора субстрата (титранта) в раствор сополимера.
Полученная зависимость похожа на начальный участок уравнения Михаэлиса-Ментен. Наклон зависимости связан с отношением каталитических параметров. Для их разделения необходимо провести эксперименты в более широком интервале концентраций субстрата.
Созданный капиллярный дифференциальный титрационный калориметр с электрической калибровкой, воспроизводящей измеряемые тепловые процессы в калориметрической камере, обеспечил возможность прецизионных измерений на данном калориметре во всем диапазоне температур и изменяющихся условий.
Литература
1. Rapid measurement of binding constants and heats of binding using a new titration calorimeter / Wiseman Т., Williston S., Brandts J.F. and Lin L. // Anal. Biochem. - 1989. - Vol.179. - P.131-137.
2. Development of an isothermal titration microcalorimetric system with digital control and dynamic power Peltier compensation. I. Description and basic performance / A.Velazquez-Campoy, O.Lopez-Mayorga, M.A.Cabrerizo-Vilchez// Rev. Sci. Instrum. - 2000. - Vol.71. - P.1824-1831.
3. Standards in isothermal microcalorimetry (IUPAC Technical Report) / I.Wadso, R.N.Goldberg // Pure Appl. Chem. - 2001. - Vol.73 (10). - P.1625-1639.
4. Моисеева С.П. Разработка калориметрического метода и капиллярного титрационного калориметра для изучения биохимических реакций: Автореф. дис. канд. техн. наук. - М., 2005. - 20 с.
5. Grant, D.A.; Hermon-Taylor, J. Biochim. Biophys. Acta 1979, 567, 207.
6. Willson, R.J. et al. Thermochim. Acta 1999, 325, 125.
Кинетические параметры гидролиза BAEE трипсином
Начальная скорость гидролиза п-нитрофенилпропионата фракциями сополимеров НВКЛ-НВИА (85:15) при рН 7.3.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАПИЛЛЯРНЫЙ КОМПЕНСАЦИОННЫЙ ДИФФЕРЕНЦИАЛЬНЫЙ ТИТРАЦИОННЫЙ КАЛОРИМЕТР | 2007 |
|
RU2335744C1 |
| ПРЕЦИЗИОННЫЙ КАПИЛЛЯРНЫЙ ДИФФЕРЕНЦИАЛЬНЫЙ ТИТРАЦИОННЫЙ КАЛОРИМЕТР | 2008 |
|
RU2381464C1 |
| СПОСОБ ИЗМЕРЕНИЯ ТЕПЛОВОЙ МОЩНОСТИ НА КАПИЛЛЯРНОМ ДИФФЕРЕНЦИАЛЬНОМ ТИТРАЦИОННОМ КАЛОРИМЕТРЕ | 2007 |
|
RU2347201C1 |
| Способ охлаждения и нагрева с постоянной скоростью протяженных калориметрических камер изотермического капиллярного дифференциального титрационного нанокалориметра, предназначенного для работы с короткоживущими объектами | 2018 |
|
RU2713808C1 |
| Капиллярный титрационный калориметр для исследования митохондрий | 2016 |
|
RU2610853C1 |
| Капиллярный титрационный нанокалориметр для исследования митохондрий | 2016 |
|
RU2618670C1 |
| ДИФФЕРЕНЦИАЛЬНЫЙ АДИАБАТНЫЙ СКАНИРУЮЩИЙ МИКРОКАЛОРИМЕТР ВЫСОКОГО ДАВЛЕНИЯ | 2008 |
|
RU2364845C1 |
| Реакционный сосуд микрокалориметра | 1981 |
|
SU1030672A1 |
| Дифференциальный сканирующий микрокалориметр | 1980 |
|
SU947655A1 |
| Дифференциальный микрокалориметр | 1979 |
|
SU857746A1 |

Титрационный калориметр является универсальным средством для измерения параметров кинетики ферментативных реакций и описания биомолекулярных взаимодействий. Решение задачи создания капиллярного дифференциального титрационного калориметра с электрической калибровкой, воспроизводящей измеряемые тепловые процессы в калориметрической камере, для обеспечения прецизионных измерений на данном калориметре во всем диапазоне температур и изменяющихся условий достигнуто благодаря тому, что на конце дозирующей иглы рабочей камеры установлен малогабаритный резистор с первым и вторым электрическими выводами, а на дозирующей игле эталонной камеры установлены третий и четвертый электрические выводы, идентичные первому и второму выводам, при этом третий и четвертый выводы электрически соединены между собой на конце дозирующей иглы эталонной камеры, выходные концы второго и третьего выводов электрически соединены между собой, а выходные концы первого и четвертого выводов подсоединены к источнику электрической энергии. Эти признаки позволяют воспроизвести при калибровке условия реального эксперимента и получить одинаковые результаты при электрической калибровке и при известных химических взаимодействиях. 10 ил., 2 табл.
Капиллярный дифференциальный титрационный калориметр, содержащий измерительные части капиллярных калориметрических камер, заключенные в термостатирующую оболочку, инъекционное устройство подачи реагента в камеры, содержащее дозирующую иглу для рабочей камеры и дозирующую иглу для эталонной камеры, устройство приведения игл инъекционного устройства в колебательное движение, пассивный тепловой шунт, охватывающий часть калориметрических камер и соединенный с термостатирующей оболочкой, активный тепловой шунт, расположенный вне термостатирующей оболочки и охватывающий пассивную часть капиллярных калориметрических камер, выполненных в виде прямых капилляров, средство измерения мощности тепловых процессов, происходящих в калориметрических камерах, устройство линейного перемещения инъекционного устройства вдоль оси калориметрических камер, отличающийся тем, что на конце дозирующей иглы для рабочей камеры установлен малогабаритный резистор с первым и вторым электрическими выводами, а на дозирующей игле для эталонной камеры установлены третий и четвертый электрические выводы, идентичные первому и второму выводам, при этом третий и четвертый выводы электрически соединены между собой на конце дозирующей иглы для эталонной камеры, выходные концы второго и третьего выводов электрически соединены между собой, а выходные концы первого и четвертого выводов подсоединены к источнику электрической энергии.
| DE 4409185 А, 21.09.1995 | |||
| Способ получения комплексного минерального дубителя | 1992 |
|
SU1831502A3 |
| CN 1322943 A, 21.11.2001 | |||
| Реакционный сосуд калориметра | 1977 |
|
SU696311A1 |
Авторы
Даты
2008-10-10—Публикация
2007-02-15—Подача