Изобретение относится к области медицины и химико-фармацевтической промышленности. Конкретно - к способам получения и выявления возможного спектра фармакологической активности и разработке соответствующих фармацевтических композиций, лечебно-косметических и гигиенических средств, содержащих новый полиактивный набор терпеноидов.
Выявление и разработка способов получения, а так же возможных путей использования новых полиактивных фармацевтических субстанций, способных проявлять не просто биологическую активность того или иного свойства, а оказывать высокий лечебный эффект, является целью и приоритетным направлением в области создания новых лекарственных препаратов, лечебно-косметических и гигиенических средств.
Одним из основополагающих условий для этого является наличие полиактивности у активных ингредиентов субстанций, более эффективных, чем известные аналоги.
Представлялось целесообразным сосредоточить круг поиска таких перспективных субстанций среди естественных растительных терпеноидных композиций. Этому способствует ряд факторов:
1. К терпеноидам относятся соединения с различным числом углеродных атомов, которые произошли из изопреновых единиц (C5H8). Их многочисленные кислородные производные представлены спиртами, альдегидами, кетонами, кислотами и т.д. Несмотря на то, что решение трудной задачи - идентификации новых терпенов еще не окончено, этих соединений насчитывается уже десятки тысяч и для них уже зафиксированы большинство из известных видов биологической активности.
2. Эти природные соединения - монотерпены (C10H16), сесквитерпены (C15H24), дитерпены (С20Н32), тритерпены (С30Н48), тетратерпены (С40Н64) и политерпены практически обнаружены во всех тканях лекарственных растений.
3. Функции растительных терпеноидов, многие из которых образуются в массе на конечных этапах специализированного (вторичного) обмена, до конца не изучены, но в настоящее время к основополагающей роли относят их экологическую составляющую. Считается, что именно терпеноиды обеспечивают выживание растений при неблагоприятных воздействиях окружающей среды (перепады температур, воздействие патогенных микробов, грибов, насекомых, наличие токсических веществ в воздушных массах, дисбаланс поступления питательных веществ и т.д.).
4. Терпеноиды являются активными участниками обменных процессов, а углеводородные цепи многих их представителей являются ключевыми промежуточными продуктами на пути биосинтеза таких биологически активных веществ, как стероидные гормоны, ферменты, антиокислители, витамины D, Е, К, желчные кислоты и т.д.
Однако существует огромный разрыв между количеством известных терпеновых соединений, объемом информации об их биологической активности, но ограниченным, хотя и длительным, использованием их в медицинской практике (камфора, валидол, капли Зеленина, корвалол, валокордин и т.д.). Объяснение этого может заключаться в том, что исследованию подвергаются, как правило, отдельные представители этого огромного класса, выделенные в чистом виде. Такой подход ведет к появлению токсичности и отсутствию полиактивности, что лишает такие соединения необходимых преимуществ.
Так работами ряда ученых (Inoule etal, 1986; Doll etal, 1962) было показано, что тритерпенглицирретиновая кислота способна ингибировать ферменты, принимающие участие в биосинтезе лейкотриенов, включая 5-липоксигеназную активность, что делает ее ответственной за противовоспалительную активность.
Поэтому в изучение были взяты отдельные производные глицирретиновой кислоты, обладающие противовоспалительной, противоязвенной, противоаллергической, противогепатитной и противовирусной активностями.
Была предложена серия таких соединений для использования в качестве средств профилактики и лечения язвы желудка: карбеноксол (патент США №3070623), аминокислотные соли глицерретиновой кислоты (патент Япония А-44-32798), амидные производные 11-дезоксиглицирретановой кислоты (патент Великобритании №1346871), амидные производные глицирретиновой кислоты (патент Бельгия №753773) и т.д.
Как известно, такие соединения не решили проблему лечения и профилактики язвы желудка, а просто обозначили возможный путь ее решения.
Известны также тритерпеновые композиции, способы их получения и применения для ингибирования эпителиальной клетки млекопитающего в предзлокачественном или злокачественном состоянии на фоне регуляции ангиогенеза. Такие тритерпеновые композиции выделены из растений вида Acacia victorial. Они представляют собой акациевую или олеановую кислоты, к которьм присоединены олигосахариды и монотерпеновые составляющие. Полученные тритерпеновые композиции характеризуются ограниченной или варьирующейся степенью эффективности в лечении патологических состояний млекопитающих или человека (патент США US 99/11041, WO 99/59578).
Известна также фармацевтическая композиция R-тетраола, полученная на основе фракции лабданоидодитерпеновых кислот из живиц хвойных пород видов Pinus sibirica, и/или Pinus cembra, и/или рода Abies, и/или рода Larix (патент RU 2196581 С2 по кл. А61К 31/337, 41/00, 35/78, C07D 305/14, А61Р 35/00). Полученная фармацевтическая композиция является аналогом противоопухолевого препарата таксола. Она может быть использована для производства противоопухолевого препарата с меньшей стоимостью. Однако обе эти фармацевтические композиции обладают ограниченным спектром биологической активности и широким диапазоном нежелательных сопутствующих воздействий.
Известна фармацевтическая композиция, содержащая терпеноидные альдегидофенолы (эуглобали), формулы С23Н30О5 или С28Н38O5, обладающая антимикробным, антивирусным и противовоспалительным действием со спектром применения в гинекологии и проктологии (патент RU 2102977, Кл. А61К 9/02, А61J 3/08). К причинам, препятствующим достижению описанного ниже лечебного эффекта, при использовании этой известной фармацевтической композиции, относится низкая биологическая активность взятых активных веществ, а так же ограничение по ассортименту лекарственных форм и способам введения препарата в организм.
Тем не менее, осуществлялись попытки создания и использования комплексных фармацевтических композиций на основе терпеноидов, которые с успехом могли удовлетворять критерию - «наличие активности». Это целый ряд известных препаратов, в качестве действующего вещества которых выступают терпены, содержащиеся в пихтовом масле (патент RU 2074730, кл. А61К 35/78; патент RU 2127584, кл. А61К 9/06, 35/64, 35/78; RU, патент №2127884 C1, A61К 9/06; SU, патент 178047, кл. А61К 9/06). В данном случае способ получения базируется на выделении не отдельных терпенов, а целой их группы, а именно монотерпеноидов, для которых свойственны те же ограничения.
К причинам, препятствующим достижению описанного ниже лечебного эффекта, относится их высокая токсичность, свойственная всем скипидарам (в том числе кедровым и сосновым), а так же ограничения по применяемым лекарственным формам, путям их применения и спектром биологической активности.
Более близкими комплексными терпеноидными композициями по способам получения и уровням биологической активности являются антимикробная (SU 1767737 А1 от 14.06.90.) и противоопухолевая (SU 1663819 А1 от 14.06.89).
Но указанные терпеноидные композиции обладают высокой, но ограниченной сферой биологической активности, кроме того, они не являются фармакологически значимыми.
Наиболее близким источником, который может быть указан в качестве прототипа, является «Средство «Абисил-1», обладающее противовоспалительной, антибактериальной и ранозаживляющей активностью» (Патент RU, №2054945 от 28.06.1995). Как известно, из описанного способа получения терпеноидной композиции Абисил-1 она состоит из природного капсульного экстракта пихты сибирской (Abies sibiricus Led.), обогащенного монотерпеноидными соединениями, взятых в определенных соотношениях.
Однако существует целый ряд ограничений и причин, препятствующих достижению высокого лечебного эффекта. К таким причинам относятся:
- отсутствие стандартизации известной терпеноидной композиции;
- ограничение по использованию сырьевых источников, а так же возможных сфер применения для терпеноидной фармацевтической композиции.
Недостатком известного решения является, прежде всего то, что отсутствие стандартизации не позволяет получить терпеноидную композицию с максимально возможной для нее биологической активностью, что соответственно препятствует получению эффективных средств, созданных на ее основе.
Целью настоящего изобретения является:
- повышение биологической активности терпеноидной композиции за счет выявленного и разработанного способа активации входящих ингредиентов;
- разработка нового способа получения терпеноидной композиции, на основе которой станет возможным осуществление совершенно необходимой стандартизации новых лекарственных, парфюмерно-косметических или гигиенических средств;
- получение новой стандартизированной лекарственной формы, отличной от "Абисил-1", обладающей повышенной биологической активностью, на основе активированных и стандартизированных ингредиентов терпеноидной субстанции;
- выявление разнообразия спектра клинических возможностей и способов использования новой лекарственной формы;
- снятие ограничений в отношении сфер использования комплекса действующих биологически активных веществ;
- расширение сырьевых источников.
Указанная цель достигается предлагаемой композицией, представляющей собой стандартизированную терпеноидную субстанцию Абисил-2, полученную на основе капсульного экстракта растений семейства Pinaceae, включающую следующие компоненты в массовой доле %, а именно:
- секвитерпеноиды (3-6%)
- нейтральные дитерпеноиды (11-15%)
- дитерпеновые кислоты (23-24%)
- тритерпеновые кислоты (8-16%)
- ненасыщенные и насыщенные жирные кислоты (0,1-0,3%)
- фенольные соединения (0,1-0,2%)
- монотерпеноиды остальное,
причем содержание монотерпеноида борнилацетата должно быть не менее 10,0% от общего состава терпеноидов.
Терпеноидная композиция представляет собой густую жидкость от желтого прозрачного до молочно-белого цвета со специфическим запахом и имеет определенные физические константы, а именно:
- кислотное число (70-90 мг)
- число омыления (100-130 мг)
- эфирное число (10-60 мг)
- показатель преломления (1,500 до 1,520 Не)
Полученная новая субстанция полиактивна, терапевтически высокоэффективна; не токсична и имеет длительный срок хранения.
Монотерпеноиды представляют собой смесь природных соединений указанного семейства и могут включать нижеупомянутые в таблице 1 монотерпеноиды.
Композиция включает секвитерпеноиды, такие как лонгифолен, кариофиллен, α-гумулен, α и j-мурулен, бизаболен, γ-кадинен, хамазулен и др.
В состав нейтральных дитерпенов входят углеводороды (тунберген, пимародиен), окиси (маноилоксид), спирты (абиенол, пимаринол, лариксол) и альдегиды (левопимараль).
Дитерпеновые или смоляные кислоты включают такие соединения, как левопимаровая, пимаровая, палюстровая, абиетиновая, дегидроабиетиновая и др.
Композиция включает природные тритерпеновые кислоты, такие как абиесоновая, абиесолидовая, фирамоновая, α-ацилакриловая предпочтительно.
Ненасыщенные и насыщенные жирные кислоты выбраны из таких природных кислот как яблочная, лимонная, винная, щавелевоуксусная, галловая и др. кислоты, жирные кислоты, подобные олеиновой, линолевой, линоленовой и др.
Композиция включает фенольные соединения указанного семейства растений, в том числе простые фенолы (фенилы, фенолоспирты, фенолокислоты, кумарины и др.), фенолы с двумя ароматическими кольцами (флавоноиды, флавоны, изофлавоноиды и др.), полимерные фенолы (полифенолы) - дубильные вещества или танины, кахетины и т.п.
В ходе исследований биологической активности терпеноидных субстанций в зависимости от исходного капсульного содержимого терпенов и полученных монотерпеноидов была обнаружена большая вариабельность активности.
В ответ на воздействие различных стрессовых факторов, например, грибковых или вирусных заболеваний ствола, кроны или корневой системы, в растительных сообществах семейства Pinaceae, принадлежащих к 4 родам: Pinus (сосна), Picea (ель), Abies, (пихта), Larix (лиственница) происходит переориентация в синтезе вторичных метаболитов, а именно - возрастает степень ненасыщенности жирных кислот липидов, усиливается синтез монотерпеноидов и низкомолекулярных жирных кислот.
Эти процессы являются защитными, направленными на купирование развития патологических изменений в растительных клетках.
Поиск аналогичных способов среди известных решений показал, что такой отличительный признак не был использован ранее при разработке различных способов получения растительных экстрактов, в том числе отсутствует его описание и при получении терпеноидной композиции Абисил-1 (RU, патент №2054945).
Классической установкой, как известно (Фармакогнозия, Москва: Медицина, 1991 г.) является указание на то, что сбор различного растительного сырья необходимо осуществлять в период максимально благоприятный для растительных сообществ, т.к. в этот период они имеют всю необходимую гамму биологически активных веществ. Вариации в сборе различного растительного сырья отмечаются только на указание периода цветения, зацветания или увядания.
Нами было установлено, что при использовании сырья, собранного в период максимального развития растений (июль), отмечается максимальный выход монотерпеноидов и это позволяет значительно экономить сырье. Кроме того, сбор сырья для получения монотерпеновых соединений, являющихся составными компонентами терпеноидной субстанции Абисил-2, предпочтительно осуществлять в период более высоких дневных температур, так как в это время идет увеличение содержания эфирных масел.
Однако, как установлено нами, можно получить значительные преимущества в активности, если осуществлять сбор сырья в период стресса растений (деревья вдоль туристических троп, резкие колебания дневных и ночных температур, поражения стволов и кроны деревьев грибками, паразитирующими лишайниками и т.д.). Так, например, низкие температуры или простукивание ствола деревьев провоцируют синтез липидов жидкой консистенции, для предотвращения образования в живых клетках льда или возникновения анатомических деструкции. Обогащенное именно этими соединениями сырье позволяет получить субстанцию Абисил-2 с более высокой биологической активностью (таблица 2, пример 1).
Таким образом, при получении терпеноидной композиции Абисил-2 предлагается использовать новый, более радикальный способ, чем просто выделение того или иного специфического агента из природного набора терпенов, заключенных в пихтовой капсуле. Он заключается в создании кратковременной стрессовой ситуации для деревьев путем механического простукивания стволов или возникновении независимого стресса в жизни растений (резкие колебания дневных и ночных температур в период вегетации, задымления, развитие различных заболеваний и т.д.).
Субстанция Абисил-2 в ходе ее получения из капсульного экстракта обогащается монотерпеновыми соединениями, которые вырабатываются также из исходного сырья, собранного по примеру 1 (Пример 2).
Таким образом, важным аспектом настоящего изобретения является разработка наиболее эффективного состава терпеноидной композиции Абисил-2, одним из условий которого является использование сырья со спровоцированным по выходу определенным набором терпенов, а для получения монотерпеноидов, наряду с этим, предпочтительным является соблюдение определенного атмосферного температурного режима.
Другим важным аспектом настоящего изобретения является расширение сырьевых источников для получения терпеноидной субстанции.
В настоящее время в роде пихты выделено 56 ботанических видов, 6 представителей которых имеют природные ареалы на территории Российской Федерации - это пихта сибирская (Abies sibiricus Led.), пихта белокорая (Abies nephrolepis Maxim}, пихта сахалинская (Abies sachalinensis), пихта камчатская (Abies gracilis), пихта цельнолистная (Abies holophylla Maxim) и пихта Майра (Abies mayriana Miyabe et Kudo).
Нами было установлено, что групповой химический состав природной субстанции Абисил-2 (таблица 3, пример 2) практически идентичен при получении из 6 различных видов пихт. Изменения в количественном составе также колеблются в идентичных интервалах для всех 6 видов пихт, но они характерны и для внутривидовых сообществ.
Таким образом, сырьем для получения полиактивной терпеноидной композиции Абисил-2, выступающей в роли субстанции для лекарственных, парфюмерно-косметических и гигиенических средств, могут служить компоненты капсул различных видов пихт.
Изучение противовоспалительной активности лекарственного препарата, полученного на основе субстанции "Абисил-2" из 6 различных видов пихт (пример 4, таблица 3) на модели инфицированной раны (стафилококк+клебсиела) у кроликов, показало его идентичность, как и предполагалось, исходя из их идентичности группового химического состава.
Кроме того, известно, что терпеноиды других представителей семейства Pinaceae, принадлежащие к 3 родам: Pinus (сосна), Picea (ель), Larix (лиственница), не отличаются по групповому химическому составу друг от друга. Терпеноиды их живиц, синтезирующихся в эпителиальных клетках, представлены смесью монотерпеновых углеводородов (C10H16), смесью дитерпеновых кислот (C19H29COOH), нейтральными сескви-, дитерпеноидами. Химический состав летучих компонентов, полученных из живиц различных хвойных деревьев, практически постоянен. В его состав входят: трициклен, лимонен, α-пинен, β-пинен, мирцен, Δ3-карен, камфен, β-мирцен, α-терпинен, терпинолен, α-фелландрен, β-фелландрен, 1,8-цинеол, γ-терпинен, n-цимол, цитраль, камфора, борнилацетат, кариофиллен, лонгифолен, α-гумулен, терпинеол, α-кадинен, β-кадинен, бизаболен, хамазулен и др.
Как известно, капсульный экстракт пихт отличается от других терпеноидов хвойных деревьев наличием структурно-модифицированным ланостановым углеродным скелетом три-терпеновых кислот. Все остальные компоненты идентичны представителям семейства Pinaceae.
Тем не менее, все терпеноиды хвойных пород деревьев отличаются по количественному содержанию отдельных соединений, а следовательно, и по физико-химическим свойствам. Однако, учитывая наличие разработанных способов разделения терпеноидов на отдельные групповые фракции и возможности их перегруппировки, существует реальная возможность получения сырья для производства субстанции Абисил-2 на основе терпенов, полученных из родов: ель, сосна и лиственница при условии их обогащения недостающими тритерпеновыми кислотами и осуществлением необходимых количественных сочетаний.
Использование такого подхода позволит использовать в качестве сырья не только капсульный экстракт различных видов пихт по примерам 1-3, но и живицы различных пород деревьев семейства Pinaceae.
В пользу этого подхода свидетельствует и тот факт, что к настоящему времени считается установленной свойственная всем терпеноидам антимикробная и антивирусная активность. Терпеноиды стимулируют различные физиологические процессы в древесине, в том числе могут нести сигнальную информацию, обеспечивая устойчивость в период стресса или развития болезни растений. Эта общность биологических функций, свойственная всем терпеноидам, естественна, так как она обусловлена наличием идентичных соединений.
Таким образом, достигается заявленная цель - расширение сырьевых источников для получения полиактивной терпеноидной композиции.
Согласно данному изобретению терпеноидная композиция Абисил-2 может быть использована в качестве активного вещества для изготовления лекарств, лечебно-косметических или гигиенических средств.
Как уже отмечалось, известно использование терпеноидов в качестве активного вещества при получении лекарственного средства "Абисил-1". Данная композиция обладает противовоспалительной, антибактериальной и ранозаживляющей активностью. Известна также лекарственная форма терпеноидов, представляющая собой полиактивные ректальные или вагинальные суппозитории для лечения и/или профилактики урологических, проктологических или гинекологических заболеваний (RU, №2198653).
Новая композиция проявляет полиактивность, а именно для нее зафиксированы множественные виды биологической активности: ранозаживляющая, противовоспалительная, антибактериальная, иммуномодулирующая, обезболивающая и противоопухолевая.
Кроме того, лекарственные средства, созданные на основе субстанции Абисил-2, пригодны как для локального применения, так и для воздействия на организм в целом, так как при различных патологических состояниях, сопровождающихся нарушением синтеза нейромедиаторов, инициируется синтез гуморальных медиаторов нервных окончаний головного мозга.
В прототипе способы же клинического применения вообще не разработаны.
Заявляемая нами полиактивная терпеноидная композиция Абисил-2 послужила субстанцией для получения фармакопейной субстанции Абисил и для изготовления лекарственной формы: "Абисил - раствор для местного и наружного применения масляный 20%". Для его приготовления предпочтительно использовать оливковое, подсолнечное или соевое масло.
Клинические испытания нового лекарственного средства, проведенные в Институте хирургии им. А.В.Вишневского РАМН, в Центральном научно-исследовательском институте стоматологии, в Областной клинической больнице г.Иркутска, в Морозовской детской городской клинической больнице г.Москвы, в Межобластном ожоговом центре г.Иркутска и др. центрах, рекомендованных Фармакологическим комитетом РФ, подтвердили его высокую эффективность для лечения:
1. В общехирургической практике: гнойно-воспалительных заболеваний кожи и мягких тканей (трофические язвы и длительно незаживающие гнойные послеоперационные и посттравматические раны, свищи, пролежни, ожоги и обморожения, абсцессы и флегмоны, в том числе челюстно-лицевой области).
2. В стоматологии: стоматитов, пародонтоза, гингивита, альвеолита, осложнений при протезировании зубов.
3. В оториноларингологии: отита, евстахеита, синусита, ринита, ринофарингита, фарингита, тонзиллита, состояния после тонзилэктомии, ларингита.
4. В дерматологии: рожистого воспаления, пиодермии.
Разработаны способы местного или наружного применения, а именно:
5. При гнойно-воспалительных заболеваниях кожи и мягких тканей предварительно проводят хирургическую обработку раневой поверхности и затем наносят препарат 1-2 раза в сутки равномерным тонким слоем. Длительность лечения зависит от формы и тяжести заболевания (обычно 5-10 дней) и заканчивается при появлении свежих грануляций, островков эпителия или полной эпителизации.
6. При воспалительных процессах в челюстно-лицевой области после вскрытия и хирургической обработки абсцессов и флегмон в карманы и послеоперационные раны вводят тампоны, пропитанные 20%-ным раствором Абисила-2. Процедуру повторяют ежедневно 5-7 дней.
7. При заболеваниях полости рта обрабатывать пораженную поверхность слизистой оболочки 2-3 раза в день или применять турунды, смоченные раствором препарата.
8. При отитах - ввести в наружный слуховой проход тампон, смоченный препаратом.
9. При лечении ринита, синусита закапывают в каждую ноздрю по 1-2 капли 3-4 раза в день. При гайморитах препарат вводят в гайморову пазуху после ее предварительной санации.
10. При лечении тонзиллита и других воспалительных заболеваний глотки и гортани - обрабатывать препаратом слизистые оболочки 2-3 раза в сутки.
11. При заболеваниях кожи - препарат наносят 1-3 раза в сутки тонким слоем на пораженные участки. Продолжительность курса индивидуальна и зависит от тяжести заболевания.
Полиактивная терпеноидная композиция Абисил-2 может представлять собой основное действующее вещество и предназначена для изготовления различных лекарственных препаратов. В зависимости от путей введения для приготовления композиций используются необходимые фармацевтически приемлемые вспомогательные вещества и носители.
Средняя эффективная доза композиции составляет предпочтительно от 50 до 200 мг/кг.
Заявляемая композиция совместима с любыми фармацевтическими носителями, имеющими липофильную основу: растворителями, мазями, желеобразующими веществами, наполнителями. Возможно использование растворов, мазей, эмульсий, капсул.
Возможность осуществления изобретения продемонстрирована на примерах, приведенных ниже.
Пример 1.
Капсульный экстракт, служащий сырьем для получения полиактивной терпеноидной композиции Абисил-2, получают из различных представителей рода пихт (Abies) путем прямого прокола и сбора в светозащитные флаконы.
Причем, естественная композиция терпенов должна содержать спровоцированный (по выходу и синтезу) состав для биозащиты от стрессовых факторов, обогащенный идентичными монотерпеновыми соединениями. В качестве стрессовых факторов могут быть естественные - это резкие колебания между дневными и ночными температурами, задымления, поражения деревьев различными заболеваниями или паразитирующими мхами, лишайниками и т.д., или специально спровоцированные (кратковременное простукивание стволов деревьев - механическое воздействие на кору давлением произвольной величины).
Химический и количественный состав полученного таким образом капсульного экстракта определяли методом ГЖХ (газожидкостный хроматографии)
Условия хроматографирования:
- газовый хроматограф с плазменно-ионизационным детектором типа «Кристалл 2000М»;
- колонка капиллярная Zebron ZB-1 (длина 30 м, диаметр 0.53 мм) или аналогичная, обеспечивающая требуемое разделение;
- температурный режим термостата колонок программируемый: начальная температура 135°С в течение 6 мин, далее нагрев до 210°С со скоростью 4 град/мин и поддержание этой температуры в течение 5 мин;
- температура детектора 250°С;
- температура испарителя 250°С;
- скорость газа-носителя (азот ОСЧ) - 4 мл/мин;
- деление потока 1:7;
- время анализа - 30 мин.
Регистрацию хроматограмм проводят с помощью компьютерной программы «Хроматэк Аналитик».
Содержание борнилацетата в процентах (х) рассчитывают по формуле:
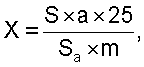
где а - навеска РСО борнилацетата в граммах;
m - навеска препарата в граммах;
S, Sa - площадь пика борнилацетата на хроматограмме испытуемого
раствора и раствора РСО соответственно;
Готовят отдельно раствор РСО борнилацетата. Около 0,08 г (точная навеска) борнилацетата (фирма «Fluka») помещают в мерную колбу, вместимостью 200 мл, растворяют в 40 мл эфира, доводят объем раствора до метки хлороформом и перемешивают. Срок годности раствора 1 сутки.
2. Проверка пригодности хроматографической системы. Хроматографическая система считается пригодной, если выполняются следующие условия:
- регистрируют не менее трех воспроизводимых хроматограмм раствора РСО борнилацетата;
- эффективность колонки, рассчитанная по пику борнилацетата, должна быть не менее 80000 теоретических тарелок;
- коэффициент асимметрии пика борнилацетата должен быть не более 1,2;
- относительное стандартное отклонение площади пика борнилацетата должно быть не более 4%.
На хроматограммах препарата и раствора РСО борнилацетата времена удерживания пиков борнилацетата не должны отличаться более чем на 2%.
Содержание борнилацетата должно быть не менее 10,0%. Поэтому в случае, если содержание меньше, к экстракту добавляют необходимое количество химически чистого борнилацетата.
Относительные времена удерживания компонентов эфирного масла составили:
Собранное сырье необходимо хранить в светозащитных флаконах с притертой пробкой, не допуская резкого колебания температуры и попадания конденсата или влаги во флаконы, т.к. нарушение этих условий исключит возможность стандартизации средств, изготовленных на основе этого сырья, по такому критерию как внешний вид.
Пример 2.
При получении монотерпеновых соединений, служащих для обогащения исходного сырья, следует учитывать тот факт, что содержание их в капсулах различных видов пихт рода пихта колеблется в течение года. Максимальное содержание отмечается в июле-августе, а минимальное - в холодное вегетационное время года. Так, например, в майском сырье их уровень не превышает 20-25%, а в июльском 30-40%. Так как выделение монотерпеновых соединений является промежуточным процессом в изготовлении субстанции Абисил-2 и требует идентичного сырья, то для их получения предпочтительно использовать июльский экстракт в целях экономии сырья.
Собранное сырье представляет собой полупрозрачную жидкость янтарно-желтого цвета со специфическим запахом.
Показатели данных анализа, полученного сырья:
1. ПD 20=1.5170,
2. dн20=1.0358 г/мл
3.LD=-12°
4. Данные элементарного анализа:
С-77,82; Н-10,19; S-нет; N-нет.
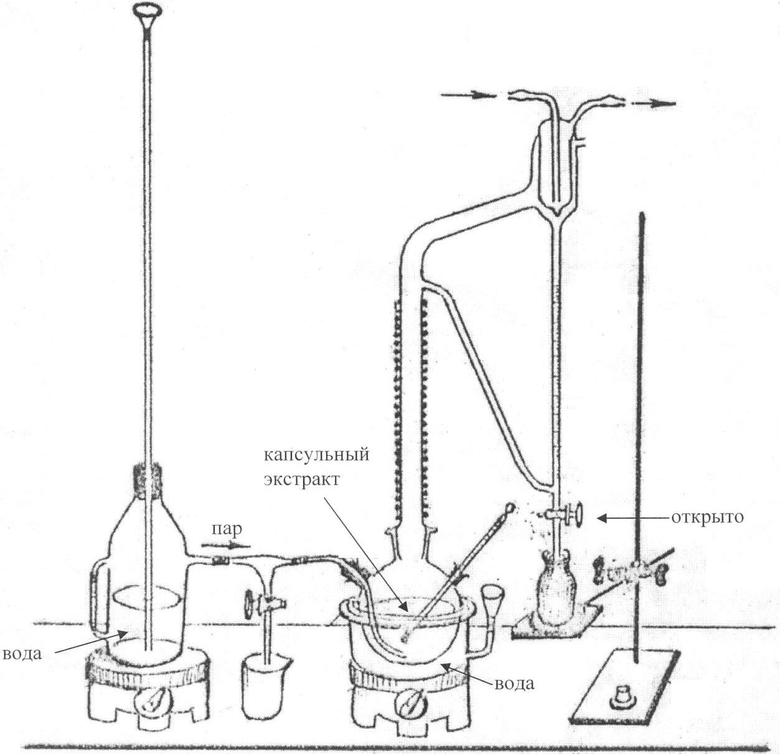
Выделение фракции монотерпеноидов осуществляют по схеме, изображенной на чертеже.
Берут 250 г исходного сырья (капсульный экстракт по примеру 1) и помещают в трех-горлую колбу с термометром и барботерной трубкой. Водяная баня имеет патрубок для заполнения и промежуточные кольца. Медный паровик имеет водомерное стекло, предохранительную трубку и тройник для сбора конденсата. Аппарат Клевенджера, подключенный к трехгорлой колбе, снабжен теплоизолированным участком отводного патрубка, пальчиковым холодильником и градуированной пипеткой со сливным краном. Сырье нагревают до прекращения выделения паров, которые конденсируют и сушат.
Собранная по этой схеме аппаратура уже через 7-10 часов позволяет получить необходимые монотерпеноиды.
Количество полученных монотерпеноидов составляет 33% от массы берущейся смеси и соответствует литературным данным (от 30 до 40%). Монотерпеноиды высушены над свежепрокаленным сульфатом магния. Их физико-химические показатели: dн20=0.884, ПD 20=1.4753, LD=-30.2°. Состав монотерпеноидов определен методом газо-жидкостной хроматографии (ГЖХ) на хроматографе ЛХМ-7А с детектором по теплопроводности (катарометром) и насыпной колонкой длиной 3.0 м, диаметром 5 мм, стационарная фаза "Apiezon-L" на полихроме, расход газа-носителя (гелий) 30 мл/мин, температура колонки 125°С, температура испарителя 180°С. Идентификация основных компонентов монотерпеноидов проведена по относительным временам удерживания (ОВУ) и методом подсадки соединений-свидетелей.
Количественный химический состав монотерпеноидов композиции
Пример 3.
Полиактивную терпеноидную композицию Абисил-2, служащую субстанцией для изготовления лекарственных, лечебно-косметических и гигиенических средств, готовят на основе капсульных терпенов различных представителей рода пихта (Abies), полученных по примеру 1, и монотерпеноидов, выделенных по примеру 2. Обогащение монотерпеноидами осуществляется при комнатной температуре, доводя содержание борнилацетата в смеси до отметки не менее 10,0%
На основе терпеноидной композиции Абисил-2, отвечающей необходимым стандартизированным параметрам, указанным выше, получают стандартизированный лекарственный препарат - "Абисил - раствор для местного и наружного применения масляный 20%", путем растворения этой субстанции в масле - оливковом, подсолнечном или соевом.
Изучение сравнительной противовоспалительной и ранозаживляющей активности идентичности лекарственных средств, полученных на основе различных субстанций Абисила-2, осуществляли на модели инфицированной раны (стафилококк+клебсиела) у кроликов (таблица 2).
Экспериментальные данные показывают значительный разрыв в сроках заживления ран у животных. Лекарственный препарат, полученный на основе сырья, собранного на фоне стрессовых изменений, проявляет более высокую противовоспалительную активность - заживление ран на 12-13 сутки, против 17-19 суток для сырья собранного из покоящихся капсул и 28 суток в контроле.
Пример 4.
Капсульный экстракт, служащий сырьем для получения полиактивной терпеноидной композиции Абисил-2, получают по Примеру 1, с той лишь разницей, что его осуществляют, используя не только пихту сибирскую (Abies sibiricus Led.), но и другие представители рода пихт (Abies), произрастающих на территории Российской Федерации, а именно:
- пихта белокорая (Abies nephrolepis Maxim)
- пихта сахалинская (Abies sachalinesis)
- пихта камчатская (Abies gracilis)
- пихта цельнолистная (Abies holophilla Maxim)
- пихта Майра (Abies mayriana Miyabe et Kudo)
В эксперименте была изучена биологическую активность всех 6 образцов, из которых было получено, по примерам 1-3, 6 образцов лекарственного препарата "Абисил - раствор для местного и наружного применения масляный 20%".
Эксперименты проводили на моделях инфицированной раны (стафилококк+клебсиела) у кроликов.
Результаты изучения на этой модели противовоспалительной активности (таблица 4) 6 серий лекарственного препарата "Абисил - раствор для местного и наружного применения масляный 20%", полученного на основе субстанции Абисил-2, изготовленной из сырья 6 видов рода пихт (Abies) свидетельствуют о наличии идентичной биологической активности.
Так, к 17 суткам эксперимента, процент заживления поверхностных ран у кроликов колеблется в интервалах 89,9-99,3%, а к 18 суткам составил 100% у всех 6 серий препарата, против 29 суток в контроле.
Пример 5
Испытания иммуномодулирующего действия
Эксперименты по изучению действия заявленной терпеноидной композиции проводили на мышах линии BALB/C (самцы массой 18-25 г). В каждую опытную группу включалось по 10 животных. В качестве Т-зависимого антигена использовали эритроциты барана в виде 5%-ной взвеси в объеме 0,5 мл. Одновременно с внутрибрюшинной иммунизацией антигеном контрольной группе животных осуществляют инъекции оливкового масла, которое используют в качестве растворителя для исследуемой субстанции. В опытных группах животных одновременно с иммунизацией Т-зависимым антигеном осуществляли инъекции заявленной композиции, растворенной в оливковом масле в объеме 0,2 мл в дозах 200,100, 10,1, и 0,1 мг/кг от массы животных.
Оценку эффективности осуществляли на основе анализа способности влиять на конечное звено иммуногенеза. Эти данные получали на 6-е сутки после однократной иммунизации. Количественную оценку определяли по характеру формирования антителообразующих клеток (АОК) в системе in vivo. Уровень стимуляции антителообразования определяли методом локального гемолиза по реакции Ерне в агаре на 6-е сутки после иммунизации животных. Определяли количество АОК на всю селезенку и рассчитывали коэффициент стимуляции по отношению к контролю. В реакции гемагглютинации (РГА) с эритроцитами барана определяли титр антител. Полученные опытным путем данные сравнивались с контрольными и обрабатывались методом математической статистики с использованием критерия Стьюдента.
Результаты представлены в таблице 5.
Пример 6
Исследование противоопухолевого действия
В опытах были использованы мыши BALB/c. В качестве моделей перевиваемых опухолей мышей были использованы штаммы - карциносаркома Уокера 256, меланома В-16.
В каждую опытную группу включалось по 10 животных. Инъекции препарата осуществляли per rectum. В качестве Т-зависимого антигена использовали эритроциты барана в виде 50% взвеси в объеме 0,5 мл.
Одновременно с внутрибрюшинной иммунизацией антигеном контрольным группам животных осуществляют инъекцию оливкового масла. Инокуляцию опухолевых штаммов вели внутрибрюшинно.
В опытных группах животных одновременно с иммунизацией Т-зависимым антигеном осуществляли per rectum инъекции заявленной композиции в объеме 0,2 мл в дозе 100 мг/кг массы животных. На протяжении последующих 6 дней опытным животным 2 раза в сутки (с интервалом 12 ч) вводилась per rectum лекарственная субстанция.
Оценка осуществлялась по способности индуцировать трансформацию лимфоцитов в антителообразующие клетки селезенки у животных опухоленосителей и по уровню продолжительности их жизни. Результаты приведены в таблице 6.
Отмечается ремиссия опухоли при использовании штамма карциносаркомы Уокера и значительный процент увеличения продолжительности жизни по отношению к контролю - 75%, в случае использования опухолевого штамма меланома В-16.
Пример 7
Изучение обезболивающего действия.
Исследование проводилось на группе из 30 человек (20 мужчин и 10 женщин) в возрасте от 20 до 75 лет. Критериями включения в исследование были: наличие боли в пояснично-крестцовой области, обусловленной остеохондрозом и спондилоартрозом позвоночника.
Оценка интенсивности болевых ощущений пациентов проводилась в ходе повседневной деятельности по десятибалльной визуальной аналоговой шкале и характеристике эффективности лечения по субъективному отчету больных.
Наносили местно в область поражения 20% раствор субстанции терпеноидов на оливковом масле. Через 1 час значительное уменьшение боли наблюдалось примерно у 12% пациентов. При нанесении дважды в день через двое суток - минимум у половины пациентов. Боль при движении значительно снизилась у 56% больных, у 12% пациентов эффект был сомнительным. Однако через две недели до 89% отмечали отсутствие болевых ощущений при движении.
Пример 8
Исследование острой токсичности использованных образцов субстанции "Абисил-2" в лекарственной форме 20% масляный раствор, проведенное на беспородных белых мышах, показало, что LD50 составило 8,5-9,3 мл/кг и LD100 - 15 мл/кг.
Таким образом состав согласно изобретению имеет следующие преимущества:
- на основе субстанции Абисил-2, созданной с учетом заявляемых способов получения, могут быть изготовлены лекарственные средства любой требуемой концентрации;
- препарат Абисил-2 пригоден для изготовления лекарственных средств, предназначенных для лечения заболеваний различной локализации;
- препарат Абисил-2 удобен в хранении и транспортировке;
- использование в клинической практике лекарственных средств, изготовленных на основе полиактивной терпеноидной композиции Абисил-2, позволяет оказывать локальный лечебный эффект, а также и на организм в целом.
- применение лекарственных средств, созданных на основе препарата Абисил-2, экономически выгодно, т.к., учитывая его полиактивность, исключает использование различных комплексных вспомогательных средств.
* на основе субстанции, полученной из сырья, собранного в благоприятное время года (июль - август), без стрессовых воздействий ** на основе субстанции, полученной из сырья, собранного на фоне стрессовых воздействий в июле - августе
Групповой химический состав природной терпеноидной композиции Абисил-2, полученной из 6 различных видов рода пихта (Abies)
1 - раствор для местного и наружного применения масляный 20%, приготовленный на основе субстанции Абисил-2, изготовленной из сырья Abies sibiricus Ledebur.
2 - раствор для местного и наружного применения масляный 20%, приготовленный на основе субстанции Абисил-2, изготовленной из сырья Abies nephrolepis Maxim
3 - раствор для местного и наружного применения масляный 20%, приготовленный на основе субстанции Абисил-2, изготовленной из сырья Abies sachalinesis
4 - раствор для местного и наружного применения масляный 20%, приготовленный на основе субстанции Абисил-2, изготовленной из сырья Abies gracilis
5 - раствор для местного и наружного применения масляный 20%, приготовленный на основе субстанции Абисил-2, изготовленной из сырья Abies holophilla Maxim
6 - раствор для местного и наружного применения масляный 20%, приготовленный на основе субстанции Абисил-2, изготовленной из сырья Abies mayriana Miyabe et Kudo
Испытания иммуномодулирующего действия
Исследования противоопухолевого действия
На чертеже изображена аппаратура, которая используется для выделения монотерпеноидов из исходного сырья (капсульного экстракта по примеру 1).
Необходимая аппаратура представлена двумя электроплитками с регулируемым нагревом, медным паровиком, снабженным водомерным стеклом, предохранительной трубкой и тройником для сбора конденсата, а также водяной баней, трехгорлой колбой (в которую помещают капсульный экстракт), аппаратом Клевенджера с теплоизолированным участком отводного патрубка, пальчиковым холодильником и градуированной разделительной пипеткой со сливным краном. Монотерпеноиды поступают в приемник.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО "АБИСИЛ-1", ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ, АНТИБАКТЕРИАЛЬНОЙ И РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ | 1995 |
|
RU2054945C1 |
| ПОЛИАКТИВНЫЕ РЕКТАЛЬНЫЕ ИЛИ ВАГИНАЛЬНЫЕ СУППОЗИТОРИИ НА ОСНОВЕ ПРИРОДНЫХ ТЕРПЕНОВ, ОБОГАЩЕННЫХ МОНОТЕРПЕНОИДАМИ, ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ УРОЛОГИЧЕСКИХ, ПРОКТОЛОГИЧЕСКИХ ИЛИ ГИНЕКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2198653C1 |
| СПОСОБ СТИМУЛЯЦИИ МИТОФАГИИ И АУТОФАГИИ В КЛЕТКАХ, СПОСОБ СТИМУЛЯЦИИ АУТОФАГИИ ИЛИ МИТОФАГИИ ДЛЯ ЛЕЧЕНИЯ СОСТОЯНИЯ, АССОЦИИРОВАННОГО С МИТОХОНДРИАЛЬНОЙ ДИСФУНКЦИЕЙ | 2020 |
|
RU2765414C1 |
| Липосомальная форма смолы Abies sibirica для неинвазивной доставки биологически активного вещества живицы Abies sibirica в мозг, обладающая антиоксидантной, цитотоксической активностью в отношении раковых клеток шейки матки, и способ ее получения | 2019 |
|
RU2757873C2 |
| ЭНДОГЕННАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПОЛУЧЕННАЯ НА ОСНОВЕ ЦЕЛЕНАПРАВЛЕННОЙ АКТИВАЦИИ ГУМОРАЛЬНЫХ МЕДИАТОРОВ НЕРВНЫХ ОКОНЧАНИЙ КОРЫ ГОЛОВНОГО МОЗГА | 2003 |
|
RU2244928C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОРАЛЬНОЙ ФОРМЫ СУБСТАНЦИИ, СОДЕРЖАЩЕЙ ИНСУЛИН | 2022 |
|
RU2818017C2 |
| ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО | 1998 |
|
RU2142782C1 |
| ОПОЛАСКИВАТЕЛЬ ДЛЯ ПОЛОСТИ РТА | 2006 |
|
RU2312657C2 |
| СРЕДСТВО "РЕКТОФИТ 1" | 2011 |
|
RU2470659C1 |
| СОСТАВ ЛЕКАРСТВЕННОЙ ФИТОСУБСТАНЦИИ С АНТИМИКРОБНЫМИ И ПРОТИВОВОСПАЛИТЕЛЬНЫМИ СВОЙСТВАМИ "ДЕНТОС" | 2009 |
|
RU2428171C1 |
Изобретение относится к фармацевтической промышленности, в частности к средству, обладающему ранозаживляющей, противовоспалительной, антибактериальной, иммуномодулирующей, обезболивающей и противоопухолевой активностью. Средство, обладающее ранозаживляющей, противовоспалительной, антибактериальной, иммуномодулирующей, обезболивающей и противоопухолевой активностью на основе терпеноидов, содержит капсульный экстракт растений семейства Pinaceae, подверженных кратковременному стрессовому воздействию, обогащенный монотерпеноидами, выделенными из капсульного экстракта. Фармацевтическая композиция, обладающая ранозаживляющей, противовоспалительной, антибактериальной, иммуномодулирующей, обезболивающей и противоопухолевой активностью, содержит вышеописанное средство в эффективном количестве и целевую добавку. Применение вышеописанного средства для приготовления лекарственного препарата для лечения гнойно-воспалительных заболеваний. Вышеописанное средство и фармацевтическая композиция на его основе обладают повышенной ранозаживляющей, противовоспалительной, антибактериальной, иммуномодулирующей, обезболивающей и противоопухолевой активностью. 3 н. и 5 з.п. ф-лы, 1 ил., 6 табл.
и имеет следующие физические константы: кислотное число 70-90, число омыления 100-130, эфирное число 10-60, показатель преломления 1,500 до 1,520, причем содержание монотерпеноида борнилацетата составляет не менее 10,0% от общего состава терпеноидов.
| СРЕДСТВО "АБИСИЛ-1", ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ, АНТИБАКТЕРИАЛЬНОЙ И РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ | 1995 |
|
RU2054945C1 |
| ПОЛИАКТИВНЫЕ РЕКТАЛЬНЫЕ ИЛИ ВАГИНАЛЬНЫЕ СУППОЗИТОРИИ НА ОСНОВЕ ПРИРОДНЫХ ТЕРПЕНОВ, ОБОГАЩЕННЫХ МОНОТЕРПЕНОИДАМИ, ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ УРОЛОГИЧЕСКИХ, ПРОКТОЛОГИЧЕСКИХ ИЛИ ГИНЕКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2198653C1 |
| Wada S | |||
| et al | |||
| Triterpenoid constituents isolated from the bark of Abies sachalinensis // J Nat Prod., 2002, 65(11): 1657-9, PMID: 12444693 | |||
| US 4668820, 26.05.1987. | |||
Авторы
Даты
2008-11-20—Публикация
2007-02-16—Подача