Настоящее изобретение относится к области медицины, а именно к способам стимуляции митофагии и аутофагии в клетке, предусматривающим обработку клеток индуктором на базе терпеноидов, извлеченным из растений семейства хвойных (Pinaceae), например пихты, сосны или кедра, к способам стимуляции аутофагии или митофагии для лечения состояния, ассоциированного с митохондриальной дисфункцией. Кроме того, настоящее изобретение относится к применению индуктора на основе терпеноидов для стимуляции митофагии и аутофагии в клетке и к применению индуктора на основе терпеноидов для стимуляции аутофагии или митофагии для лечения состояния, ассоциированного с митохондриальной дисфункцией.
Продолжительность жизни в экономически развитых странах постепенно увеличивается. Однако качество жизни людей с возрастом ухудшается, поскольку люди пожилого возраста часто страдают неизлечимыми заболеваниями.
Изменения в образе жизни за последние десятилетия (например, переедание, малоподвижный образ жизни) привели к увеличению числа людей с избыточным весом или ожирением, часто являющимся признаками и причинами таких состояний, как диабет и болезни сердца.
Исследованиями доказано, что если сосредоточиться не на конкретных болезнях старения, а на самих механизмах старения, можно добиться более значительного продления здорового периода жизни (Brian К. Kennedy и др., "Geroscience: Linking Aging to Chronic Disease", журнал Cell, № 159 от 6 ноября 2014, cc. 709-713, https://www.https://pubmed.ncbi.nlm.nih.gov/25417146).
Клеточное старение все чаще признается в качестве основной, связанной со старением причины потери здоровья и физической формы. Стареющие клетки, продолжая вырабатывать новые митохондрии, накапливают дисфункциональные и дефектные митохондрии. Митофагия, т.е. утилизация дефектных и дисфункциональных митохондрий посредством аутофагии, в стареющих клетках проходит вяло, угасает.
В настоящее время существует единодушное мнение, что нарушенная митофагия играет ключевую роль в развитии дегенеративных заболеваний, связанных со старением. Поэтому основное внимание в борьбе с рядом заболеваний, таких как болезнь Паркинсона, болезнь Альцгеймера, деменция, застойная сердечная недостаточность, саркопения, диабет 2-го типа, возрастная макулярная дегенерация (ВМД), атеросклероз, сердечно-сосудистые заболевания, рак, заболевания печени и поджелудочной железы, глазные заболевания, артрит, катаракта, остеопороз, гипертония и любые их комбинации, уделяется уже не симптоматическому лечению конкретного заболевания, а поиску путей активизации митофагии.
Соединения, которые могут замедлять старение, так называемые геропротекторы, обычно замедляют наступление старения и сопутствующих заболеваний и снижают риски смертности. В геропротекторах, активирующих процесс митофагии в клетках, в качестве активного действующего вещества (индуктора) обычно используют либо химические соединения определенного состава, полученные химическим путем, либо многокомпонентные смеси, обычно не точно определенного состава и извлеченные из растительного сырья или продуктов жизнедеятельности дрожжей и микроорганизмов.
Так, например, известен способ профилактики или лечения нейродегенеративного расстройства у субъекта, предусматривающий введение в его организм в терапевтически эффективном количестве агента-индуктора, увеличивающего Nix-опосредованную митофагию в клетке, а точнее увеличивающего биологическую активность или экспрессию полипептида Nix, его фрагмента, варианта или аналога и/или полипептида GABARAP-L1, его фрагмента, варианта или аналога в клетке и содержащего указанные компоненты (US 2019/091291 А1).
Недостатками известного способа являются технологическая сложность и высокая стоимость получения вещества, используемого в качестве индуктора, а также отсутствие полиактивности. Эти недостатки присущи всем другим известным способам, предусматривающим использование в качестве индуктора веществ химического происхождения, являющихся для клеток ксенобиотиками.
Известны также приемы для улучшения здоровья людей, особенно пожилых или слабых людей, заключающиеся в активации митофагии в клетках путем перорального введения в течение определенного времени определенных доз фармацевтической композиции на основе уролитинов, являющихся метаболитами, происходящими из продуктов микрофлоры толстой кишки млекопитающих (US 2018/256538 и US 2018/256539). Недостатками такого подхода являются высокая стоимость действующего вещества, обусловленная специфическими особенностями обработки исходного сырья и технологически сложным процессом выделения из него действующего начала, а также в первую очередь нестабильность фармакологического действия, варьирующегося от вполне эффективного до токсического.
Наиболее близким к предлагаемому в изобретении является способ активации митофагии в клетках кожи, заключающийся в воздействии на клетки кожи косметическим составом, содержащим активное вещество (индуктор), извлеченное из по крайней мере одного растения, выбранного из Helianthus annuus, Ceratonia siliqua, Nigella sativa, Withania somnifera, Secale Cornutum, Sesamum indicum, Ophiopogon japonicus, Alisma plantago-aquatica, Oryza sativa, Tropaeolum majus, Cichorium intybus, Prunus persica, Verbena officinalis, Panicum miliaceum, Rosa canina, Camelina sativa и Phaseolus vulgaris, либо из водорослей конкретных видов или дрожжей конкретных видов, а также адъюванты и вспомогательные вещества (WO 2013/178965).
Известный способ основан на использовании активного вещества, извлекаемого из растений, часть из которых произрастает в тропических странах либо которые культивируются в незначительных объемах как привозное растение. Поскольку состав и свойства активных веществ, содержащихся в растениях, зависят от условий их произрастания, терапевтическое действие выделенных из них веществ нестабильно. Многие из указанных растений содержат не одно, а целый набор биологически активных веществ разнонаправленного действия, причем некоторые из них, например вещества, содержащиеся в Secale Cornutum, Alisma plantago-aquatica, обладают сильным токсическим действием вызывает привыкание {Withania somnifera) или просто не применяются в официальной медицине в России {Ophiopogon japonicus). По указанным причинам известный способ промышленно неприменим без проведения дополнительных трудоемких исследований.
Стимулирование аутофагии, охватывающей митофагию как частный случай, также способствует оздоровлению клеток и оказывает на субъекта положительный терапевтический эффект, хотя в отличие от митофагии и не все механизмы оздоравливающего действия аутофагии выяснены до конца. Известен ряд способов стимулирования аутофагии и фармацевтических препаратов для этой цели.
В преобладающей части препаратов в качестве активного вещества-индуктора используются вещества химического происхождения несложного по сравнению с веществами растительного происхождения состава (WO 2019/204183, JP 2019218316, KR 20190114900, US 2019/160033, US 2019/336483). Соответственно, активность таких веществ является узконаправленной, а известные препараты применяются главным образом в косметических целях, когда трудно установить, является ли терапевтический эффект следствием воздействия активного вещества или целевых добавок.
В WO 2019/099531 предложено использовать в составе индуктора, стимулирующего аутофагию, синергетическую комбинацию соединений по меньшей мере из двух, а предпочтительно трех классов соединений. Благодаря этому достигается некоторое повышение эффективности способа, но не расширение сферы его эффективного применения.
Для устранения этого недостатка в WO 2019/204183 было предложено семь вариантов способа лечения или стимулирования роста волос путем введения субъекту одного или нескольких индуцирующих аутофагию агентов химического происхождения. В каждом из вариантов этого способа используется собственное определенное сочетание агентов. Само обилие предложенных вариантов говорит о том, что ни один из них не является однозначно и во всех случаях эффективным.
Кроме того, используемые согласно вышеуказанному уровню техники индуцирующие аутофагию вещества химического происхождения являются ксенобиотиками для клеток и организмов, дополнительно нагружают их метаболизирующие и элиминирующие системы и могут стать причиной развития побочных реакций.
В значительно меньшей степени указанные недостатки присущи фитопрепаратам, содержащим в качестве активного вещества растительные компоненты или продукты их переработки.
Из US 8512764 известен способ активации аутофагии клеток кожи с целью ее детоксикации или предотвращения старения, заключающийся в нанесении на кожу косметической композиции, содержащей в качестве активного ингредиента (индуктора) биологическую субстанцию, извлекаемую из водорослей, дрожжей или растений, выбираемых из группы Lithothamnium calcareum, Yarrowia lipolytica, Melilotus officinalis, Citrus limonum, Candida saitoana, Lens culinaris, Averrhoa carambola, Momordica charantia, а также адъюванты и вспомогательные вещества.
Активные вещества части вышеуказанных растений вызывают ряд нежелательных побочных эффектов. Так, в частности, кумарин, содержащийся в траве донника лекарственного (Melilotus officinalis), оказывает угнетающее действие на центральную нервную систему и обладает наркотическим действием. Биоактивный ингредиент, который получают из дрожжей вида кандида саитоана (Candida saitoana), настолько токсичен, что используется в качестве пестицида. Вещества, содержащиеся в карамболе (Averrhoa carambola), токсичны для уремических пациентов. Токсичны также вещества, содержащиеся в момордике (Momordica charantia). Ввиду токсичности активных веществ сфера применения этого известного способа ограничена косметическими процедурами, относящимися к лечению кожи или уходу за ней.
Наиболее близким к предлагаемому в изобретении является описанный в AU 2016101736 способ индуцирования аутофагии в клетках путем их контакта с тритерпиноидом, экстрагируемым из плюща обыкновенного (Hedera helix). Такой способ предложен для лечения нейродегенеративных заболеваний, а именно: болезни Паркинсона или болезни Хантингтона.
Недостатком этого способа является ограниченность сферы его применения лечением вышеуказанных болезней, обусловленная, вероятно, свойствами конкретного тритерпеноида, выделяемого из плюща. К настоящему времени установлено существование в растениях около 10000 терпенов и терпеноидов, функции большинства которых еще неизвестны. Кроме того, листья и плоды плюща ядовиты, и поэтому для снижения токсичности препарата приходится прибегать к технологически сложной многоступенчатой процедуре выделения нужного тритерпеноида из листьев и плодов плюща.
В основу настоящего изобретения была положена задача предложить способы стимуляции аутофагии и митофагии клеток путем воздействия на клетки индуктором, активное начало которого выбрано из широкого набора недорогих, доступных и нетоксичных терпеноидов, получаемых из распространенных в дикой природе России растений из семейства Pinaceae: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies). Другая задача настоящего изобретения состояла в разработке способов стимуляции аутофагии или митофагии для лечения состояния, ассоциированного с митохондриальной дисфункцией у субъекта, с использованием указанного индуктора. Еще одна задача настоящего изобретения состояла в том, чтобы предложить индуктор на основе терпеноидов, пригодный для применения для стимуляции митофагии и аутофагии в клетке и пригодный для применения для стимуляции аутофагии или митофагии для лечения состояния, ассоциированного с митохондриальной дисфункцией.
Технический результат от использования предлагаемого в изобретении решения состоит в повышении стабильности и эффективности воздействия на клетки и в снижении токсичности препаратов растительного происхождения, стимулирующих процесс устранения дисфункциональных компонентов клеток путем аутофагии и митофагии, приводящий к купированию и лечению состояний, ассоциированных с митохондриальной дисфункцией.
Указанный технический результат достигается благодаря тому, что при осуществлении способа стимуляции митофагии в клетках предлагаемым в изобретении способом, предусматривающего обработку клеток индуктором на основе терпеноидов, в качестве такого индуктора на основе терпеноидов используют в эффективной концентрации индуктор, извлеченный из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), и имеющий следующие физические константы: кислотное число от 70 до 90, число омыления от 100 до 130, эфирное число от 10 до 60, показатель преломления от 1,50 до 1,52.
В одном из предпочтительных вариантов индуктор на основе терпеноидов используют в концентрации от 0,05 до 200 мкг/мл, предпочтительно от 45 до 200 мкг/мл.
В еще одном предпочтительном варианте длительность обработки клеток индуктором на основе терпеноидов составляет от 6 до 72 ч, предпочтительно 16 ч.
В еще одном предпочтительном варианте клетки имеют происхождение из неопухолевых тканей, содержатся в субъекте или находятся ex vivo или in vitro. Обработку можно осуществлять путями и способами, известными специалистам в данной области. Так, например, при осуществлении предлагаемого в изобретении способа in vitro для приведения в контакт клеток и ингибитора можно культивировать клетки в присутствии индуктора в культуральной среде или путем добавления индуктора к клеткам. При осуществлении предлагаемого в изобретении способа ex vivo для приведения индуктора в контакт с клетками или тканями его можно, например, вводить в организм субъекта путями, которые известны специалисту в данной области, прежде всего любым из путей, которые обычно применяют в области генной терапии. Введение индуктора можно осуществлять различными путями, например путем внутривенного, внутриартериального, внутрибрюшинного, подкожного, чрескожного, внутритрахеального, внутримышечного введения, местного применения, внутрикожного, интраназального, легочного введения, введения путем ингаляции или путем внутрибронхиального, орального или ректального введения.
В еще одном предпочтительном варианте в качестве индуктора на основе терпеноидов можно использовать препарат "Абисил", "Абисил-1" или "Абисил-2", как таковой или с целевой добавкой, представляющей собой оливковое, подсолнечное, льняное, соевое, кокосовое или аргановое масло и витамин Е. Указанные препараты можно вводить перорально или наружно, например в виде 3-20%-ного по массе масляного раствора, например 3-15%-ного по массе масляного раствора, в частности 3%-ного, 4%-ного, 5%-ного или 15%-ного по массе масляного раствора (в оливковом, подсолнечном, льняном, соевом, кокосовом или аргановом масле), в виде капсул, липосом, спреев, крема и других лекарственных форм.
Указанный технический результат достигается также благодаря тому, что при осуществлении способа стимуляции аутофагии в клетках, предусматривающего обработку клеток индуктором на основе терпеноидов, в качестве такого индуктора на основе терпеноидов используют в эффективной концентрации индуктор, извлеченный из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), и имеющий следующие физические константы: кислотное число от 70 до 90, число омыления от 100 до 130, эфирное число от 10 до 60, показатель преломления от 1,50 до 1,52.
В одном из предпочтительных вариантов индуктор на основе терпеноидов используют в концентрации от 0,05 до 200 мкг/мл, предпочтительно от 45 до 200 мкг/мл.
В еще одном предпочтительном варианте длительность обработки клеток индуктором на основе терпеноидов составляет от 6 до 72 ч, предпочтительно 16 ч.
В еще одном предпочтительном варианте клетки имеют происхождение из неопухолевых тканей, содержатся в субъекте или находятся ex vivo или in vitro. Обработку можно осуществлять путями и способами, известными специалистам в данной области. Так, например, при осуществлении предлагаемого в изобретении способа in vitro для приведения в контакт клеток и ингибитора можно культивировать клетки в присутствии индуктора в культуральной среде или путем добавления индуктора к клеткам. При осуществлении предлагаемого в изобретении способа ex vivo для приведения индуктора в контакт с клетками или тканями его можно, например, вводить в организм субъекта путями, которые известны специалисту в данной области, прежде всего любым из путей, которые обычно применяют в области генной терапии. Введение индуктора можно осуществлять различными путями, например путем внутривенного, внутриартериального, внутрибрюшинного, подкожного, чрескожного, внутритрахеального, внутримышечного введения, местного применения, внутрикожного, интраназального, легочного введения, введения путем ингаляции или путем внутрибронхиального, орального или ректального введения.
В еще одном предпочтительном варианте в качестве индуктора на основе терпеноидов можно использовать препарат "Абисил", "Абисил-1" или "Абисил-2", как таковой или с целевой добавкой, представляющей собой оливковое, подсолнечное, льняное, соевое, кокосовое или аргановое масло и витамин Е. Указанные препараты можно вводить перорально или наружно, например в виде 3-20%-ного по массе масляного раствора, например 3-15%-ного по массе масляного раствора, в частности 3%-ного, 4%-ного, 5%-ного или 15%-ного по массе масляного раствора (в оливковом, подсолнечном, льняном, соевом, кокосовом или аргановом масле), в виде капсул, липосом, спреев, крема и других лекарственных форм.
Указанный технический результат достигается также благодаря тому, что при осуществлении способа стимуляции аутофагии или митофагии для лечения состояния, ассоциированного с митохондриальной дисфункцией у субъекта, со стадией введения индуктора в эффективной дозе в организм субъекта в качестве такого индуктора используют индуктор на основе терпеноидов, извлеченный из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), и имеющий следующие физические константы: кислотное число от 70 до 90, число омыления от 100 до 130, эфирное число от 10 до 60, показатель преломления от 1,50 до 1,52.
Субъектом является человек.
Состояние, ассоциированное с митохондриальной дисфункцией, выбрано из состояния, включающего мутации и/или эпигенетические нарушения митохондриального или ядерного генома, приводящие к нарушению митофагии, дефектам морфологии митохондрий и нарушениям мембранного потенциала митохондрий, и состояния, включающего лизосомные болезни накопления.
В одном из предпочтительных вариантов, индуктор на основе терпеноидов вводят в организм субъекта в дозе от 4 до 40 мг/кг веса тела, предпочтительно в дозе от 4 до 24 мг/кг веса тела.
Введение индуктора можно осуществлять различными путями, например путем внутривенного, внутриартериального, внутрибрюшинного, подкожного, чрескожного, внутритрахеального, внутримышечного введения, местного применения, внутрикожного, интраназального, легочного введения, введения путем ингаляции или путем внутрибронхиального, орального или ректального введения.
В еще одном предпочтительном варианте в качестве индуктора на основе терпеноидов можно использовать препарат "Абисил", "Абисил-1" или "Абисил-2" как таковой или с целевой добавкой, представляющей собой оливковое, подсолнечное, льняное, соевое, кокосовое или аргановое масло и витамин Е. Указанные препараты можно вводить перорально или наружно, например в виде 3-20%-ного по массе масляного раствора, например 3-15%-ного по массе масляного раствора, в частности 3%-ного, 4%-ного, 5%-ного или 15%-ного по массе масляного раствора (в оливковом, подсолнечном, льняном, соевом, кокосовом или аргановом масле), в виде капсул, липосом, спреев, крема и других лекарственных форм.
Указанный технический результат достигается далее благодаря применению индуктора на основе терпеноидов для стимуляции митофагии в клетках. Указанное применение предусматривает обработку клеток индуктором на основе терпеноидов, в качестве какового индуктора используют в эффективной концентрации индуктор, извлеченный из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), и имеющий следующие физические константы: кислотное число от 70 до 90, число омыления от 100 до 130, эфирное число от 10 до 60, показатель преломления от 1,50 до 1,52.
В одном из предпочтительных вариантов индуктор на основе терпеноидов используют в концентрации от 0,05 до 200 мкг/мл, предпочтительно от 45 до 200 мкг/мл.
В еще одном предпочтительном варианте длительность обработки клеток индуктором на основе терпеноидов составляет от 6 до 72 ч, предпочтительно 16 ч.
В еще одном предпочтительном варианте клетки имеют происхождение из неопухолевых тканей, содержатся в субъекте или находятся ex vivo или in vitro. Обработку можно осуществлять путями и способами, известными специалистам в данной области. Так, например, при осуществлении предлагаемого в изобретении способа in vitro для приведения в контакт клеток и ингибитора можно культивировать клетки в присутствии индуктора в культуральной среде или путем добавления индуктора к клеткам. При осуществлении предлагаемого в изобретении способа ex vivo для приведения индуктора в контакт с клетками или тканями его можно, например, вводить в организм субъекта путями, которые известны специалисту в данной области, прежде всего любым из путей, которые обычно применяют в области генной терапии. Введение индуктора можно осуществлять различными путями, например путем внутривенного, внутриартериального, внутрибрюшинного, подкожного, чрескожного, внутритрахеального, внутримышечного введения, местного применения, внутрикожного, интраназального, легочного введения, введения путем ингаляции или путем внутрибронхиального, орального или ректального введения.
В еще одном предпочтительном варианте в качестве индуктора на основе терпеноидов можно использовать препарат "Абисил", "Абисил-1" или "Абисил-2", как таковой или с целевой добавкой, представляющей собой оливковое, подсолнечное, льняное, соевое, кокосовое или аргановое масло и витамин Е. Указанные препараты можно вводить перорально или наружно, например в виде 3-20%-ного по массе масляного раствора, например 3-15%-ного по массе масляного раствора, в частности 3%-ного, 4%-ного, 5%-ного или 15%-ного по массе масляного раствора (в оливковом, подсолнечном, льняном, соевом, кокосовом или аргановом масле), в виде капсул, липосом, спреев, крема и других лекарственных форм.
Указанный технический результат достигается также благодаря применению индуктора на основе терпеноидов для стимуляции аутофагии в клетках. Указанное применение предусматривает обработку клеток индуктором на основе терпеноидов, в качестве какового индуктора используют в эффективной концентрации индуктор, извлеченный из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), и имеющий следующие физические константы: кислотное число от 70 до 90, число омыления от 100 до 130, эфирное число от 10 до 60, показатель преломления от 1,50 до 1,52.
В одном из предпочтительных вариантов индуктор на основе терпеноидов используют в концентрации от 0,05 до 200 мкг/мл, предпочтительно от 45 до 200 мкг/мл.
В еще одном предпочтительном варианте длительность обработки клеток индуктором на основе терпеноидов составляет от 6 до 72 ч, предпочтительно 16 ч.
В еще одном предпочтительном варианте клетки имеют происхождение из неопухолевых тканей, содержатся в субъекте или находятся ex vivo или in vitro. Обработку можно осуществлять путями и способами, известными специалистам в данной области. Так, например, при осуществлении предлагаемого в изобретении способа in vitro для приведения в контакт клеток и ингибитора можно культивировать клетки в присутствии индуктора в культуральной среде или путем добавления индуктора к клеткам. При осуществлении предлагаемого в изобретении способа ex vivo для приведения индуктора в контакт с клетками или тканями его можно, например, вводить в организм субъекта путями, которые известны специалисту в данной области, прежде всего любым из путей, которые обычно применяют в области генной терапии. Введение индуктора можно осуществлять различными путями, например путем внутривенного, внутриартериального, внутрибрюшинного, подкожного, чрескожного, внутритрахеального, внутримышечного введения, местного применения, внутрикожного, интраназального, легочного введения, введения путем ингаляции или путем внутрибронхиального, орального или ректального введения.
В еще одном предпочтительном варианте в качестве индуктора на основе терпеноидов можно использовать препарат "Абисил", "Абисил-1" или "Абисил-2", как таковой или с целевой добавкой, представляющей собой оливковое, подсолнечное, льняное, соевое, кокосовое или аргановое масло и витамин Е. Указанные препараты можно вводить перорально или наружно, например в виде 3-20%-ного по массе масляного раствора, например 3-15%-ного по массе масляного раствора, в частности 3%-ного, 4%-ного, 5%-ного или 15%-ного по массе масляного раствора (в оливковом, подсолнечном, льняном, соевом, кокосовом или аргановом масле), в виде капсул, липосом, спреев, крема и других лекарственных форм.
Указанный технический результат достигается далее благодаря применению индуктора на основе терпеноидов для стимуляции аутофагии или митофагии для лечения состояния, ассоциированного с митохондриальной дисфункцией у субъекта. Указанное применение предусматривает стадию введения индуктора в эффективной дозе в организм субъекта. В качестве такого индуктора используют индуктор на основе терпеноидов, извлеченный из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), и имеющий следующие физические константы: кислотное число от 70 до 90, число омыления от 100 до 130, эфирное число от 10 до 60, показатель преломления от 1,50 до 1,52.
Субъектом является человек.
Состояние, ассоциированное с митохондриальной дисфункцией, выбрано из состояния, включающего мутации и/или эпигенетические нарушения митохондриального или ядерного генома, приводящие к нарушению митофагии, дефектам морфологии митохондрий и нарушениям мембранного потенциала митохондрий, и состояния, включающего лизосомные болезни накопления.
В одном из предпочтительных вариантов, индуктор на основе терпеноидов вводят в организм субъекта в дозе от 4 до 40 мг/кг веса тела, предпочтительно в дозе от 4 до 24 мг/кг веса тела.
Введение индуктора можно осуществлять различными путями, например путем внутривенного, внутриартериального, внутрибрюшинного, подкожного, чрескожного, внутритрахеального, внутримышечного введения, местного применения, внутрикожного, интраназального, легочного введения, введения путем ингаляции или путем внутрибронхиального, орального или ректального введения.
В еще одном предпочтительном варианте в качестве индуктора на основе терпеноидов можно использовать препарат "Абисил", "Абисил-1" или "Абисил-2" как таковой или с целевой добавкой, представляющей собой оливковое, подсолнечное, льняное, соевое, кокосовое или аргановое масло и витамин Е. Указанные препараты можно вводить перорально или наружно, например в виде 3-20%-ного по массе масляного раствора, например 3-15%-ного по массе масляного раствора, в частности 3%-ного, 4%-ного, 5%-ного или 15%-ного по массе масляного раствора (в оливковом, подсолнечном, льняном, соевом, кокосовом или аргановом масле), в виде капсул, липосом, спреев, крема и других лекарственных форм.
Благодаря использованию действующего вещества на основе терпеноидов, извлеченных из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), достигается стабильная и существенная активизации аутофагии и митофагии в клетках при полном исключении возможности токсического воздействия на клетку.
Благодаря использованию действующего вещества на основе терпеноидов, извлеченных из растений семейства Pinaceae, например: рода ель (Picla), рода сосна (Pinus), рода кедр (Cedrus) и рода пихта (Abies), достигается стабильность процесса и результата активизации аутофагии и митофагии в клетках при полном исключении возможности токсического воздействия на клетку, что объясняется стабильностью состава и характеристик и отсутствием токсичности исходного растительного сырья, извлекаемого из указанных растений.
Использование указанного выше индуктора на основе терпеноидов и, в частности, препарата "Абисил", "Абисил-1" или "Абисил-2" как такового или с целевой добавкой позволяет добиться существенной активизации аутофагии и митофагии в клетках без необходимости использования индукторов на основе терпеноидов с другими параметрами, которые получены по иной технологии и эффективность действия которых еще только предстоит проверять и доказывать. Препараты "Абисил-1" и "Абисил" и способы их получения описаны в патентах RU 2054945, RU 2198653.
Препарат "Абисил-2" и способ его получения описаны в патенте RU 2338547. Препарат "Абисил-2" получен на основе капсульного экстракта растений семейства Pinaceae, подверженных кратковременному стрессовому воздействию, и содержит следующие компоненты:
при этом содержание монотерпеноида борнилацетата должно составлять не менее 10,0 масс. % от общего состава терпеноидов.
Терпеноидная композиция представляет собой густую жидкость с цветом от желтого прозрачного до молочно-белого со специфическим запахом и имеет следующие физические константы:
Ниже сущность изобретения поясняется со ссылкой на прилагаемые к описанию графические материалы, на которых показано:
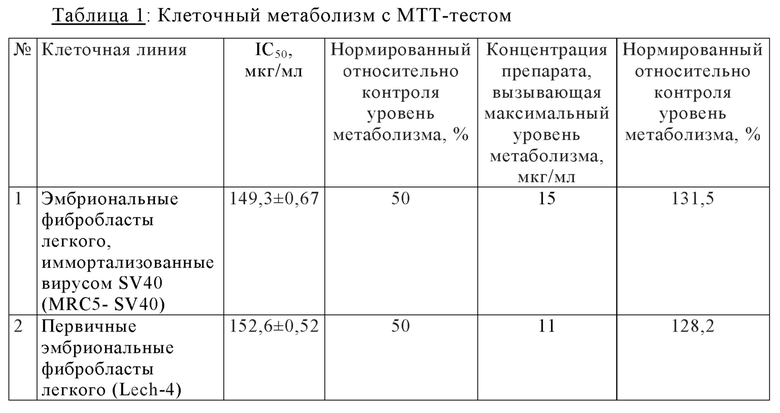
на фиг. 1- оценка метаболической активности клеток, обработанных "Абисилом" в различных концентрациях,
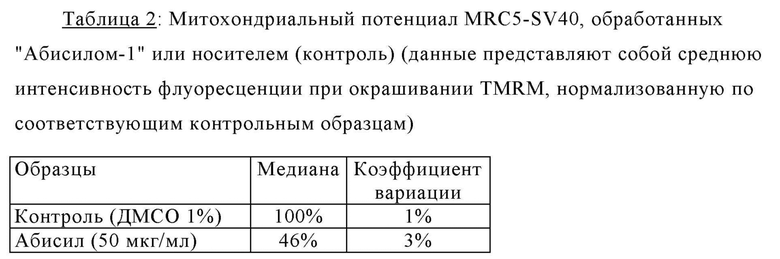
на фиг. 2 - оценка снижения митохондриального потенциала, вызванного "Абисилом" в иммортализованных клетках MRC5 и фибробластах легких Lech-4,
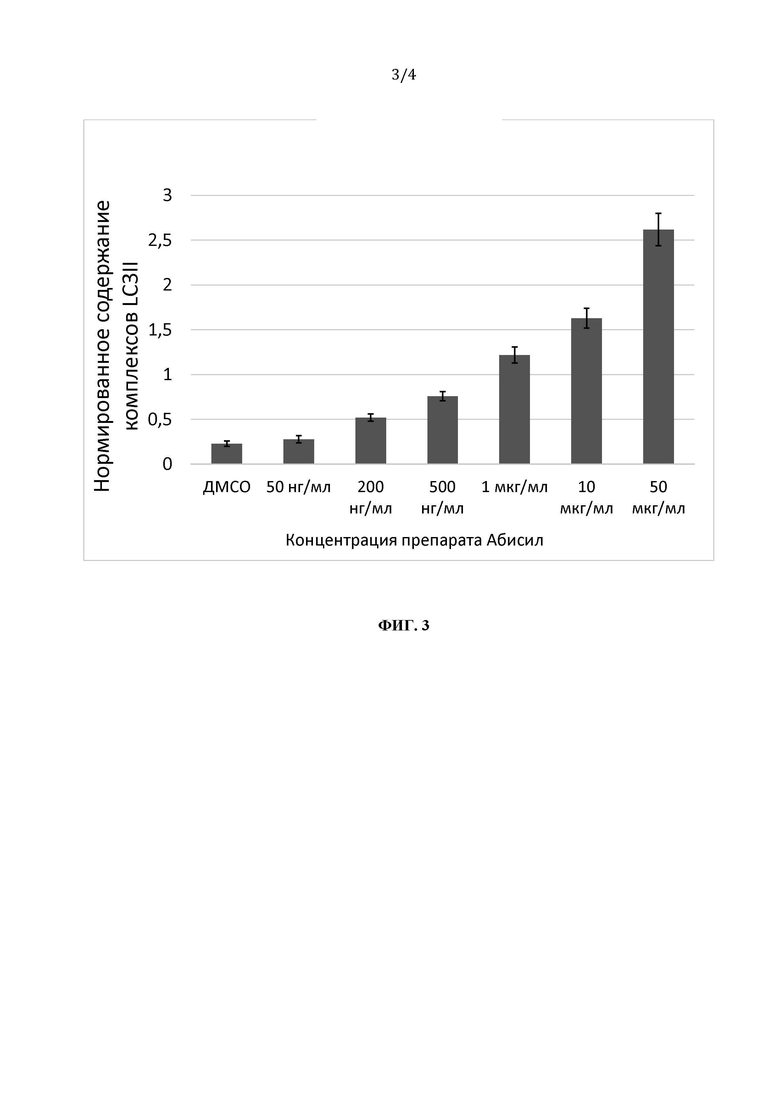
на фиг. 3 - оценка влияния предварительной обработки "Абисилом" на накопление конъюгата легкой цепи 3 и фосфатидилэтаноламина (LC3II) в трансформированных SV-40 эмбриональных фибробластах легкого (MRC5-SV40) по результатам денситометрического анализа относительно внутреннего контроля, и
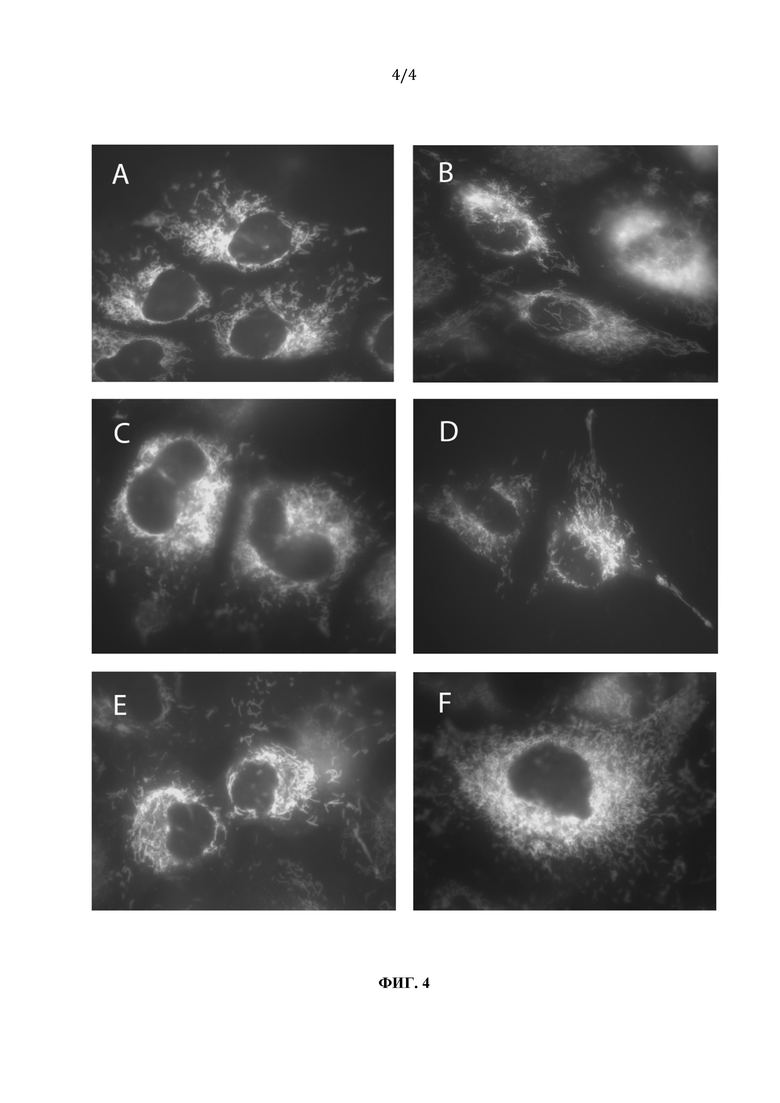
на фиг. 4 - оценка митофагии в клетках MRC5-SV40 при обработке препаратом в концентрациях 25 и 50 мкг/мл через 24 и 72 ч: А, В - контрольный образец (ДМСО, 0,5%), С - 24-часовая обработка в концентрации 25 мкг/мл, D -24-часовая обработка в концентрации 50 мкг/мл, Е - 72-часовая обработка в концентрации 25 мкг/мл, F - 72-часовая обработка в концентрации 50 мкг/мл.
Возможность осуществления изобретения может быть подтверждена следующими примерами.
Оценка митохондриального потенциала
Клетки MRC5-SV40 и Lech-4 высевали на 12-луночные планшеты по 40000 клеток на лунку. На следующий день проводили обработку препаратом "Абисил" в широком диапазоне концентраций (25-200 мкг/мл). Через 16 ч клетки окрашивали 100нМ и 200нМ метиловым эфиром тетраметилродамина (TMRM) (фирма Thermofisher Scientific) в течение 30 мин при 37°С. В качестве положительного контроля использовали 1 мкМ ротенон и 10 мкМ разобщитель окислительного фосфорилирования, представляющий собой карбонилцианид-4-(трифторметокси)фенилгидразон (FCCP) (фирма Sigma-Aldrich). Перед измерением клетки окрашивали на жизнеспособность с помощью 4',6-диамидино-2-фенилиндола (DAPI) (фирма Sigma-Aldrich) в концентрации 1 мкг/мл. Флуоресценцию детектировали с помощью цитофлуориметра BD LSRFortessa (фирма Beckman Dickinson). Анализ проводили с помощью программы Flowing Software 2.0 (фирма Perttu Terho, Turku Centre for Biotechnology). Результаты получены на основе трех независимых экспериментов с тремя биологическими повторностями.
Оценка аутофагии и митофагии
Оценку аутофагии проводили на панели клеточных линий, стабильно экспрессирующих репортерную конструкцию из 2 слитых белков EGFP (зеленый флуоресцентный белок) и LC3. Обработку препаратом "Абисил" проводили в широком диапазоне концентраций (25-200 мкг/мл) в течение 16 часов. В качестве положительного контроля использовали рапамицин (R0395, фирма Sigma-Aldrich).
Для оценки митофагии использовали линию клеток MRC5-SV40, стабильно экспрессирующих репортерную конструкцию EGFP-mCherry-FIS1, которая содержит два флуоресцентных белка и в которой тандемная метка mCherry-GFP прикреплена к сигналу локализации наружной митохондриальной мембраны, полученному из митохондриального белка FIS1 (аминокислоты 101-152). В качестве положительного контроля использовали FCCP (фирма Sigma-Aldrich).
Клетки обрабатывали препаратом "Абисил" в концентрациях 50 мкг/мл и 25 мкг/мл в течение 24 или 72 часов.
Для детекции митофагии в клетках Lech-4 их обрабатывали препаратом "Абисил" в концентрациях 25 мкг/мл и 50 мкг/мл в течение 24 или 72 часов. По окончании инкубации клетки в течение 20 минут окрашивали при 37°С 200 нМ потенциал-зависимым красителем митохондрий MitoTracker Red CMXRos (фирма Thermofisher Scientific), 100 нМ LysoTracker Green (фирма Thermofisher Scientific).
Для получения изображений использовали микроскопы Axiovert 200 (фирма Carl Zeiss) и конфокальный микроскоп Leica (фирма Leica Microsystems). МТТ-анализ
Клетки линии MRC5-SV40 высевали в 96-луночный планшет по 5000 клеток на лунку, культивировали в 100 мкл среды DMEM (питательная среда, модифицированная по способу Дульбекко) с 5% FBS (фетальная бычья сыворотка) при 37°С и инкубировали в течение 48 ч. Далее в течение суток обрабатывали препаратом "Абисил" (в концентрации 0, 9, 11, 15, 25, 50, 93, 125, 147 и 186 мкг/мл) при 37°С. Оценку уровня метаболизма клеток проводили с помощью MTS-теста (набор CellTiter 96® для нерадиоактивного анализа пролиферации клеток (МТТ), фирма Promega) в соответствии с протоколом производителя. Оптическую плотность окрашенного вещества, пропорциональную уровню метаболизма жизнеспособных клеток, измеряли при 590 нм с помощью планшетного ридера (фирма Tecan). Затем методом регрессионного анализа вычисляли значения IC50, а также концентрации, при которых наблюдался наиболее интенсивный клеточный метаболизм.
Вестерн-блоттинг
Клетки Lech-4 культивировали на чашках Петри диаметром 35 мм и при конфлюэнтности 50% проводили обработку препаратом "Абисил" в 5% DMEM с 5% FBS при 37°С в течение ночи. После инкубации клетки промывали холодным PBS (фосфатно-буферный солевой раствор) и лизировали в 200 мкл репортерного лизирующего буфера (фирма Promega), содержащего коктейль ингибиторов протеаз (№ Р8349, фирма Sigma-Aldrich), согласно инструкции производителя. Лизаты центрифугировали в течение 15 мин при 12000g и измеряли общее содержание белка в супернатанте белка по Брэдфорду. Белки разделяли электрофорезом в полиакриламидном геле в присутствии 12% додецилсульфата натрия (SDS) по Лэммли и осуществляли электроперенос на ПВДФ-мембрану Amersham Hybond Р, 0,45 мкм (фирма Amersham Biosciences, GE Healthcare) в буфере для переноса Товбин (25 мМ трис, 192 мМ глицин, 20% (об/об) этанола, рН 8,3). Мембраны блокировали в 4%-ном растворе обезжиренного молока в ФСБТ (ФСБ с 0,05% Твина 20) в течение 1 часа при комнатной температуре. Инкубацию с первичными антителами проводили в течение ночи при 4°С со вторичными антителами (козьи антитела к кроличьему IgG-HRP, sc-2004, фирма Santa Cruz Biotechnology) и в течение 1 часа при комнатной температуре. Для проявления использовали хемилюминесцентный субстрат типа Immobilon Western Chemiluminescent HRP Substrate (фирма Merck-Millipore, Sigma-Aldrich), определяя сигнал хемилюминесценции с помощью системы гель-документирования Bio-Rad ChemiDoc MP Imaging System (фирма Bio-Rad). Количественную оценку белковых полос выполняли с использованием программного обеспечения ImageJ (NIH, фирма Bethesda, шт. Мэриленд, США). Список использованных первичных антител:
- β-actin (D6A8, #8457, фирма Cell Signaling Technology);
- LC3 (D11, #3868, фирма Cell Signaling Technology).
Статистический анализ
Данные представлены в виде среднего значения ± стандартная ошибка. Статистический анализ выполняли с использованием t-критерия Стьюдента. Считается, что р<0,05 указывает на статистически значимое различие. Анализ был выполнен с использованием программы Microsoft Excel.
Реагенты для обработки клеток
Для обработки клеток использовали препарат "Абисил" в виде живицы от ООО "Инитиум-Фарм". Для получения стока для обработки клеточных культур "Абисил" растворяли в ДМСО.
Клетки выращивали в среде DMEM, содержащей 10% FBS, до 50-70%-ной конфлюэнтности. Непосредственно перед обработкой сток "Абисил" разводили в бессывороточной среде DMEM, обработку проводили в среде DMEM с 5% FBS.
Отрицательные контроли обрабатывали соответствующим количеством ДМСО в среде DMEM с 5% FBS.
Пример 1: Влияние "Абисила" на метаболическую активность клеток Влияние 48-часовой обработки "Абисилом" на метаболическую активность клеток изучали с использованием МТТ-теста на линиях эмбриональных легочных фибробластов (MRC5-SV40 и Lech-4). "Абисил" продемонстрировал значительную дозозависимость (см. фиг. 1). Рассчитанные значения IC50 составили 149,3±0,67 для MRC5-SV40 и 152,6±0,52 мкг/мл для Lech-4 соответственно (таблица 1). Кроме этого, обе клеточные линии продемонстрировали существенное повышение метаболической активности (р<0,001) при обработке препаратов в низких концентрациях (9-15 мкг/мл).
Пример 2: Влияние "Абисила-1" на снижение митохондриального потенциала
Иммортализованные клетки MRC5 и фибробласты легких Lech-4 (MRC5-SV40 (А)) инкубировали в соотношении 1:4000 "Абисилом-1" в течение ночи, окрашивали TMRM и флуоресценцию красителя измеряли в канале РЕ. Черная гистограмма на фигуре 2 представляет обработанные "Абисилом-1" клетки; серая гистограмма представляет на фигуре 2 контрольные клетки.
Обработка "Абисилом-1" вызывала приблизительно 2-кратное снижение митохондриального потенциала (р<0,05 (р<0,01)) (см. фиг. 2 и таблицу 2).
Таким образом, "Абисил-1" вызывает снижение митохондриального потенциала в иммортализованных клетках MRC5 и фибробластах легких Lech-4.
Пример 3: Влияние "Абисила" на интенсивность аутофагии и митофагии
В данном примере оценивали влияние "Абисила" на интенсивность аутофагии и митофагии черз 24 и 72 ч.
Оценку аутофагии проводили путем оценки количества комплексов LC3II в клетках MRC5-SV40, определяемого Вестерн-блоттингом. На фиг. 3 приведены результаты денситометрического анализа комплексов LC3II относительно внутреннего контроля, которые представлены в виде среднего значения ± стандартное отклонение, рассчитанного по трем независимым экспериментам. Отмечается существенное повышение содержания комплексов LC3II (более чем в 10 раз) при обработке "Абисилом" в концентрации 50 мкг/мл, что свидетельствует об эффективной стимуляции аэрофагии в клетках.
Пример 4: Влияние "Абисила" на снижение митофагии
Уменьшение митохондриального потенциала "Абисилом" может означать, что он индуцирует митофагию. Для изучения этого вводили конструкцию, кодирующую репортерную конструкцию GFP-mCherry-FIS1 в клетках MRC5-SV40, которая позволяет обнаруживать возможную фрагментацию митохондрий и активацию митофагии. FIS1 представляет собой белок, закрепленный на внешней митохондриальной мембране, и поэтому солокализованные GFP и mCherry будут давать желтый сигнал. Флуоресценция GFP гасится в лизосомах из-за низкого значения рН, и поэтому можно обнаружить расщепленные митохондрии в фаголизомах по красной флуоресценции (см. фиг. 4).
Действительно, после 24-часовой обработки "Абисил" вызвал образование множественных митофагосом. Однако "Абисил" не вызывал общей фрагментации митохондрий даже после 72-часовой обработки.
Далее определяли влияние обработки препаратом "Абисил" на клетках Lech-4 и исследовали солокализацию красителей в ходе окрашивания красным красителем Mitotracker Red с зеленым красителем Lysotracker Green, который окрашивает кислотные компартменты (лизосомы) в живых клетках. Наблюдается увеличение количества фаголизосом, однако они не солокализуются с красителем Mitotracker Red, что указывает на то, что "Абисил" способствует аутофагии, но специфически не вызывает фрагментацию митохондрий в эмбриональных фибробластах.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНОЕ 7-ГИДРОКСИКУМАРИНА ДЛЯ ИНДУКЦИИ МИТОФАГИИ В КЛЕТКАХ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2022 |
|
RU2819611C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ НИКОТИНАМИДРИБОЗИД И УРОЛИТИН | 2016 |
|
RU2751638C2 |
| ПОЛИАКТИВНАЯ ТЕРПЕНОИДНАЯ СУБСТАНЦИЯ АБИСИЛ-2, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ И СПОСОБЫ ЕЕ ПРИМЕНЕНИЯ | 2007 |
|
RU2338547C1 |
| Способ стимуляции регенерации печени у крыс | 2022 |
|
RU2792513C1 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА С ПРИМЕНЕНИЕМ ИНГИБИТОРА АУТОФАГИИ НА ОСНОВЕ ТИОКСАНТОНА | 2011 |
|
RU2627588C2 |
| СПОСОБЫ ЛЕЧЕНИЯ БОЛЕЗНИ ДАНОНА И ДРУГИХ НАРУШЕНИЙ АУТОФАГИИ | 2017 |
|
RU2777571C2 |
| Конструкция генетическая для экспрессии в лизосомах клеток млекопитающих родопсина NsXeR из организма наногалоархеон Nanosalina, позволяющего повышать pH лизосом | 2023 |
|
RU2820973C1 |
| СПОСОБ ВОЗДЕЙСТВИЯ НА ОРГАНИЗМ ПУТЕМ АДРЕСНОЙ ДОСТАВКИ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ В МИТОХОНДРИИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И СОЕДИНЕНИЕ, ПРИМЕНЯЕМОЕ ДЛЯ ЭТОЙ ЦЕЛИ | 2005 |
|
RU2318500C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГИБИРОВАНИЯ АУТОФАГИИ ДВИГАТЕЛЬНЫХ НЕЙРОНОВ И ЕЁ ПРИМЕНЕНИЕ | 2012 |
|
RU2585372C1 |
| Замещенные цианопирролидины, обладающие активностью ингибиторов USP30 | 2020 |
|
RU2822680C1 |
Изобретение относится к медицине, а именно к способам стимуляции митофагии. Способ стимуляции аутофагии в клетках, предусматривающий обработку клеток индуктором на основе терпеноидов, при этом в качестве такого индуктора на основе терпеноидов используют в эффективной концентрации препарат «Абисил», «Абисил-1» или «Абисил-2». Способ стимуляции аутофагии у субъекта, со стадией введения в организм эффективной дозы индуктора, при этом в качестве такого индуктора используют препарат «Абисил», «Абисил-1» или «Абисил-2» и стимуляция аутофагии обеспечивает лечение состояния, ассоциированного с митохондриальной дисфункцией. Вышеописанная группа изобретений позволяет повысить стабильность и эффективность воздействия на клетки и снизить токсичность препаратов растительного происхождения, стимулировать процесс устранения дисфункциональных компонентов клеток путем аутофагии, что приводит к купированию и лечению состояний, ассоциированных с митохондриальной дисфункцией. 4 ил., 2 табл., 4 пр.
1. Способ стимуляции аутофагии в клетках, предусматривающий обработку клеток индуктором на основе терпеноидов, отличающийся тем, что в качестве такого индуктора на основе терпеноидов используют в эффективной концентрации препарат «Абисил», «Абисил-1» или «Абисил-2».
2. Способ по п. 1, отличающийся тем, что индуктор на основе терпеноидов используют в концентрации от 0,05 до 200 мкг/мл, предпочтительно от 45 до 200 мкг/мл.
3. Способ по п. 1, отличающийся тем, что длительность обработки клеток индуктором на основе терпеноидов составляет от 6 до 72 ч, предпочтительно 16 ч.
4. Способ по п. 1, отличающийся тем, что препарат «Абисил», «Абисил-1» или «Абисил-2» используют с целевой добавкой.
5. Способ по одному из пп. 1-4, отличающийся тем, что клетки имеют происхождение из неопухолевых тканей.
6. Способ по п. 5, отличающийся тем, что клетки содержатся в субъекте.
7. Способ по любому из пп. 1-6, отличающийся тем, что клетки находятся ex vivo или in vitro.
8. Способ стимуляции аутофагии у субъекта, со стадией введения в организм эффективной дозы индуктора, отличающийся тем, что в качестве такого индуктора используют препарат «Абисил», «Абисил-1» или «Абисил-2» и стимуляция аутофагии обеспечивает лечение состояния, ассоциированного с митохондриальной дисфункцией.
9. Способ по п. 8, отличающийся тем, что состояние, ассоциированное с митохондриальной дисфункцией, выбрано из состояния, включающего мутации и/или эпигенетические нарушения митохондриального или ядерного генома, приводящие к нарушению митофагии, дефектам морфологии митохондрий и нарушениям мембранного потенциала митохондрий, и состояния, включающего лизосомные болезни накопления.
10. Способ по п. 8, отличающийся тем, что индуктор на основе терпеноидов вводят в организм субъекта в дозе от 4 до 40 мг/кг, предпочтительно от 4 до 24 мг/кг.
11. Способ по п. 8, отличающийся тем, что препарат «Абисил», «Абисил-1» или «Абисил-2» используют с целевой добавкой.
| AU 2016101736 A4, 03.11.2016 | |||
| WO 2013178965 A2, 05.12.2013 | |||
| СРЕДСТВО "АБИСИЛ-1", ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ, АНТИБАКТЕРИАЛЬНОЙ И РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ | 1995 |
|
RU2054945C1 |
| ПОЛИАКТИВНЫЕ РЕКТАЛЬНЫЕ ИЛИ ВАГИНАЛЬНЫЕ СУППОЗИТОРИИ НА ОСНОВЕ ПРИРОДНЫХ ТЕРПЕНОВ, ОБОГАЩЕННЫХ МОНОТЕРПЕНОИДАМИ, ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ УРОЛОГИЧЕСКИХ, ПРОКТОЛОГИЧЕСКИХ ИЛИ ГИНЕКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2198653C1 |
| ПОЛИАКТИВНАЯ ТЕРПЕНОИДНАЯ СУБСТАНЦИЯ АБИСИЛ-2, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ И СПОСОБЫ ЕЕ ПРИМЕНЕНИЯ | 2007 |
|
RU2338547C1 |
| CN 111603474 A, 01.09.2020. | |||
Авторы
Даты
2022-01-31—Публикация
2020-09-30—Подача