Настоящее изобретение относится к фармакологической композиции, содержащей кондиционированную культуральную среду, полученную при культивировании лейкоцитов периферической крови и стволовых и/или прогениторных клеток в культуральной среде, а также разрушенные культивируемые клетки. Клетки, используемые для кондиционирования среды, могут быть генетически модифицированы в целях изменения концентрации белков, присутствующих в данной среде. В среде культивации могут содержаться белки, полученные из тканей паренхиматозных органов. Фармакологическую композицию используют для стимуляции регенерации органов и тканей. Фармакологическую композицию можно применять в качестве косметических добавок, пищевых добавок и добавок в корм животных, а также для культивирования клеток, фармацевтического применения и для стимуляции роста волос.
Предпосылками создания изобретения послужил факт, что в процессе регенерации поврежденного органа, происходит активация лейкоцитов крови веществами, образующимися при разрушении тканей и органов. В результате проведенных исследований стало известно, что резекция паренхиматозных органов у экспериментальных животных вызывает изменение метаболической активности лейкоцитов, в особенности лимфоцитов. Перенос таких активированных клеток крови в организм интактного животного вызывает увеличение митозов в паренхиме того же органа, который был резецирован у оперированного животного. В процессе разрушения паренхиматозных клеток в кровь поступают вещества, как правило, внутриклеточный матрикс, которые вызывают метаболическую перестройку в лимфоидных органах. Лимфоциты начинают продуцировать вещества, способные изменять скорость пролиферации и дифференцировки других, не лимфоидных клеток, как правило, стволовых и прогениторных клеток костного мозга, а также стволовых клеток, находящихся в паренхиматозных органах.
Очевидно, что использовать вышеуказанные механизмы переноса возможно с помощью культивирования клеток, участвующих в механизмах переноса. Питательная среда, используемая для культивации клеток обычно включает незаменимые аминокислоты, витамины, минералы, углеводы, липиды и нуклеиновые кислоты. Внесение в питательную среду гормонов и ростовых факторов обеспечивает условия для нормального роста и дифференцировки культивируемых клеток. В процессе культивирования клеточная культура начинает продуцировать медиаторы и ростовые факторы, которые, как правило, призваны обеспечить оптимальные условия для пролиферации культивируемых клеток. Спектр продуцируемых веществ напрямую зависит от фенотипического состава культивируемых клеток, а также от факторов роста, которые были исходно привнесены в культуральную среду. Таким образом, в процессе культивирования клетки модифицируют культуральную среду, обогащая ее продуктами своей жизнедеятельности. В процессе культивирования клетки секретируют ряд важных клеточных метаболитов, регулирующих пролиферацию клеток, их адгезию, дифференцировку, миграцию, определяющих спектр синтезируемых и секретируемых метаболитов. Это могут быть различные клеточные метаболиты: секреторные, включая, например, биологически активные факторы роста, медиаторы воспаления и другие внеклеточные белки. В качестве примера можно привести: VEGF (сосудистый эндотелиальный фактор роста), FGF (фактор роста тромбоцитов) и IGF (инсулиноподобный фактор роста) (Gonzalez-Rubio, M. et al., 1996, Kidney Int. 50(1):164-73; Abramovitch, R. et al., 1997, Int. J. Exp. Pathol. 78(2):57-70; Stein I. et al., 1995, Mol. Cell. Biol. 15(10):5363-8; Yang W. et al., 1997, FEBS Lett. 403(2):139-42; West, N.R. et al. 1995, J. Neurosci. Res. 40(5):647-59). Трансформирующий фактор роста (TGF-β), индуцируется в процессе заживления ран. Было также показано, что TGF-β способствует повышению экспрессии белков внеклеточного матрикса, включая коллаген и фибронектин (Ignotz et al., 1986, J. Biol. Chem. 261:4337-4345), и ускорению заживления ран (Mustoe et al., 1987, Science 237:1333-1335). Рядом других факторов роста, обладающих способностью к индуцированию ангиогенеза и заживлению ран, являются VEGF и основный FGF. Также известно, что биологические эффекты клеточных факторов роста и цитокинов определяют не только концентрацией отдельного цитокина, но, во многом, биологический эффект определяется соотношением отдельных цитокинов, например соотношение γ-ИНФ и ИЛ-4 определяет тип развития иммунной реакции (клеточный или гуморальный).
Однако значительная часть ростовых факторов, гормонов, медиаторов и других внеклеточных белков, которые секретируются культивируемыми клетками, во внеклеточной среде быстро инактивируются, т.е. теряют свою биологическую активность. С другой стороны, в составе культивируемых клеток находятся секреторные гранулы, содержащие белки. Зачастую белки, входящие в состав секреторных гранул, находятся в неактивном состоянии в виде прогормонов. Поэтому получение композиции, состоящей из культуральной среды, обогащенной клеточными метаболитами, секретируемыми культивируемыми клетками, а также из клеточного лизата, содержащего внутриклеточные белки, в том числе белки секреторных гранул, является весьма перспективным для последующего производства препаратов, повышающих процессы регенерации.
При этом дополнительное добавление тканеспецифического антигена, состоящего из веществ, полученных при разрушении тканей и органов, в культуральную среду приводит к изменению метаболической активности культивированных клеток, что проявляется в изменении внутриклеточного синтеза и секреции клеточных метаболитов.
Прототипом предлагаемого изобретения является композиция, включающая средство для изменения скорости роста и репродукции клеток, содержащее кондиционированную клеточную культуральную среду, полученную при культивировании эукариотических клеток в трех измерениях, а также способ ее получения (Патент РФ 2280459 от 27.06.2006). Однако данная композиция не учитывает механизмов развития регенерации в ответ на действие повреждающих факторов.
Предложенное изобретение свободно от вышеуказанных недостатков, поскольку в ее основе учтен механизм переноса регенераторных свойств от поврежденного органа к регенерирующим клеткам.
Получение композиции, содержащей кондиционированную культуральную среду, полученную при культивировании лейкоцитов периферической крови и стволовых и/или прогениторных клеток в культуральной среде, а также лизат культивируемых клеток, а также композицию, полученную после того, как к культивируемым клеткам добавляется тканеспецифический антиген, получаемый из тканей того органа, регенерацию которого надо улучшить, открывает новые возможности в получении продуктов для использования в различных целях, включающих регенерацию тканей, например, при лечении ран и других дефектов ткани, а также при лечении хронических воспалительных и дегенерационных процессов внутренних органов и кожных покровов.
Заявителями настоящего изобретения описана композиция, содержащая кондиционированную культуральную среду, полученную при культивировании лейкоцитов периферической крови и стволовых и/или прогениторных клеток в культуральной среде и лизат культивируемых клеток, а также композицию, полученную после того, как к культивируемым клеткам добавляется тканеспецифический антиген, получаемый из тканей того органа, регенерацию клеток которого требуется простимулировать.
Композиции, могут состоять из любой известной определенной или неопределенной среды и могут быть кондиционированы с использованием любых стволовых и/или прогениторных клеток. Эта среда может быть кондиционирована стромальными клетками, паренхиматозными клетками, мезенхимными стволовыми клетками, резервными клетками печени, стволовыми нервными клетками, стволовыми клетками поджелудочной железы и/или эмбриональными стволовыми клетками.
Клеточный лизат получается из любых культивируемых клеток, которые после культивирования разрушаются с использованием физических (ультразвук, электрический разряд, замораживание оттаивание), химических (ферменты, химические реагенты), механических (растирание) и других факторов, а также их комбинации, в результате чего наступает нарушение целостности клеточных структур. В процессе разрушения культивируемых клеток возможно, но не обязательно, использовать физические (снижение температуры, использование инертных газов), химические (ингибиторы протеолитических ферментов) и другие факторы, а также их комбинацию для снижения скорости процесса разрушения клеточных метаболитов протеолитическими ферментами.
Тканеспецифический антиген, добавляемый в культуральную среду, получается из ткани органа, соответствующего тому, регенерацию которого требуется простимулировать. Тканеспецифический антиген получается при разрушении ткани органа с использованием физических (ультразвук, электрический разряд, замораживание-оттаивание), химических (ферменты, химические реагенты), механических (растирание) и других факторов, а также их комбинации, в результате чего наступает нарушение целостности клеточных структур. В процессе приготовления тканеспецифического антигена возможно, но не обязательно, использовать физические (снижение температуры, использование инертных газов), химические (ингибиторы протеолитических ферментов) и другие факторы, а также их комбинацию, для снижения скорости процесса разрушения клеточных структур протеолитическими ферментами.
Фармакологическая композиция, состоящая из кондиционированной культуральной среды, полученной при культивировании лейкоцитов периферической крови и стволовых и/или прогениторных клеток в культуральной среде, а также лизата культивируемых клеток может быть использована в любом состоянии. Физическими вариантами этой композиции являются, но не ограничиваются ими, жидкая или твердая среда, замороженная среда, лиофилизованная среда или среда, высушенная до порошкообразного состояния. Кроме того, эта композиция может быть приготовлена в сочетании с фармацевтически приемлемым наполнителем, используемым в качестве носителя для внутреннего введения, для введения непосредственно в пищу или пищевой продукт, для получения мази или растирания - для местного. Кроме того, указанная композиция может быть дополнительно обработана для увеличения или уменьшения концентрации одного или нескольких факторов или компонентов, содержащихся в данной композиции. Так, например, композиция может быть обогащена факторами роста с использованием иммуноаффинной хроматографии. Также композиция может быть приготовлена в сочетании с антибиотиком, противовоспалительным агентом, противовирусным агентом, противогрибковым агентом, гормоном, противоопухолевым агентом, анальгетиком, анестезирующим средством или любой их комбинации.
Подробное описание изобретения
Настоящее изобретение относится к новым фармакологическим композициям, содержащим любую кондиционированную определенную или неопределенную культуральную среду, полученную при культивировании лейкоцитов периферической крови и стволовых и/или прогениторных клеток в культуральной среде, а также лизат культивируемых клеток, полученный из культивированных клеток, подвергнутых разрушению с использованием химических, физических, механических факторов или их комбинации. Указанные клетки представляют собой клетки человека или животного и такими клетками являются стромальные клетки, клетки крови, клетки костного мозга, паренхиматозные клетки, мезенхимные стволовые клетки, резервные клетки печени, стволовые нервные клетки, панкреатические стволовые клетки и/или эмбриональные стволовые клетки. Фармакологическая композиция будет содержать различные естественным образом секретированные белки, а также внутриклеточные метаболиты, синтезируемые клеткой и содержащиеся преимущественно в секреторных гранулах.
Культуральная среда для культивирования клеток может быть любой средой для культивирования клеток, которая адекватно соответствует потребностям культивируемых клеток в питательных элементах. Примерами таких сред являются, но не ограничиваются ими, модифицированная по методу Дульбекко среда Игла (DMEM), среда Хэма F12, RPMI 1640, среда Исков, среда Маккой и другие композиции сред, известные специалистам, включая среды, описанные в работах Methods For Preparation of Media, Supplements and Substrate For Serum-Free Animal Cell Culture Alan R.Liss, New York (1984) и Cell & Tissue Culture: Laboratory Procedures, John Wiley & Sons Ltd., Chichester, England 1996. Указанная среда может быть дополнена любыми компонентами, необходимыми для поддержания нужной клеточной или тканевой культуры. Если это необходимо, то дополнительно может быть добавлена эмбриональная телячья сыворотка, которая представляет собой комплексный раствор альбуминов, глобулинов, стимуляторов роста и гормонов. Такая сыворотка не должна содержать патогенов и должна быть тщательно проверена на загрязнение микоплазмой, бактериями, грибками и вирусами.
В данной среде могут культивироваться стромальные клетки, паренхиматозные клетки, мезенхимные стволовые клетки (клетки, коммитированные или некоммитированные в отношении направления дифференцировки), резервные клетки печени, стволовые нервные клетки, стволовые клетки поджелудочной железы и/или эмбриональные стволовые клетки. Такими клетками, среди прочих, являются, но не ограничиваются ими, клетки костного мозга, кожи, печени, поджелудочной железы, почек, нервной ткани, надпочечника, эпителия слизистой и гладких мышц. Такие ткани и/или органы могут быть получены путем соответствующей биопсии или после аутопсии.
Стволовые клетки и/или прогениторные могут быть выделены известными методами. Так, например, популяции стволовых клеток и методы их выделения и использования были недавно описаны Keller et al., Nature Med, 5:151-152 (1999), Smith Curr. Biol. 8:R802-804 (1998), Методы выделения и культивирования мезенхимных стволовых клеток известны специалистам. См., Mackay et al. Tissue Eng. 4:415-428 (1988); William et al., Am. Surg. 65:22-26 (1999). Аналогичным образом стволовые клетки нервной ткани могут быть выделены способом, описанным Flax et al., Nature Biotechnol, 16:1033-1039 (1998); и Frisen et al., Cell. Mol. Life Sci., 54:935-945 (1998).
Эти клетки могут быть культивированы любым известным способом, например, в монослое, на гранулах или в трехмерном слое и любым другим способом (т.е. в чашках для культивирования, в роллер-флаконах, в системах с непрерывным потоком и т.п.). Методы культивирования клеток и тканей хорошо известны специалистам и описаны, например, в Freshney (1987), Culture of Animal Cells: A Manual of Basic Techniques.
Кроме того, данная среда может быть подвергнута 10-20-кратному концентрированию с использованием концентрирующего устройства, работающего при избыточном давлении и имеющего фильтр с отсечкой 10000 мол. масс. (Amicon, Beverly, MA).
Кроме того, кондиционированная среда может быть также обработана для выделения и очистки продукта, например, в целях удаления нежелательных протеаз. Используемые методы выделения и очистки продукта, которые позволяют сохранить оптимальную активность, хорошо известны специалистам. Так, например, может оказаться желательной очистка фактора роста, регуляторного фактора, пептидного гормона, антитела и т.п. Такими методами являются, но не ограничиваются ими, гель-хроматография (с использованием матриц, таких как сефадекс), ионообменная хроматография, аффинная хроматография на хелате металла с нерастворимой матрицей, такой как перекрестно-сшитая агароза, ВЭЖХ-очистка и гидрофобная хроматография кондиционированной среды. Эти методы более подробно описаны в Cell & Tissue Culture: Laboratory Procedure, см. выше. Само собой разумеется, что в зависимости от целей применения кондиционированной среды и/или полученных из нее продуктов должны быть приняты соответствующие меры для поддержания стерильности. Альтернативно может оказаться необходимой стерилизация, и она может быть осуществлена методами, известными специалистам, такими как, например, нагревание и/или стерилизация с помощью фильтра, при этом следует обеспечить сохранение нужной биологической активности.
Примеры осуществления изобретения
1 этап: Получение стволовых и прогениторных клеток для культивирования
На примере клеток костного мозга
Для забора костного мозга используют доступ из переднего гребня подвздошной кости. Забор костного мозга проводится в условиях операционной при соблюдении тех же правил асептики, как и при других оперативных вмешательствах.
После обработки кожи йодсодержащими растворами в области передних гребней делают прокол кожи и подкожно-жировой клетчатки, через который вставляют иглы для аспирации. После чего прокалывают кортикальную пластинку гребня подвздошной кости и аспирируют костный мозг из губчатого вещества кости. Для забора 50-150 мл костного мозга необходимо сделать несколько проколов кортикальной пластинки кости, для этого кожу и подкожно-жировую клетчатку перемещают аспирационной иглой. Классическая технология требует аспирировать костный мозг из каждого вкола малыми порциями (3-5) мл в 20-миллилитровый шприц.
Из аспирата костномозговой взвеси удаляют эритроциты. Для удаления эритроцитов можно использовать градиентное центрифугирование, лизис эритроцитов лизирующим раствором или комбинацию этих методов с другими, в результате чего наступает разделение эритроцитов и ядросодержащих клеток. Данные ядросодержащие клетки содержат как стволовые клетки, так и прогениторные.
На примере клеток, полученных из периферической крови
Вначале для повышения числа стволовых и прогениторных клеток в периферической крови животному перед забором клеток вводили в течение 2 дней внутривенно Г-КСФ (гранулоцитарный колониестимулирующий фактор). Введение препарата позволило повысить уровень гемопоэтических стволовых клеток с 0,5% (контроль) до 3,5% от общего количества мононуклеарных клеток в периферической крови
Далее проводят забор периферической крови любым известным способом и осуществляют удаление эритроцитов. Для удаления эритроцитов можно использовать градиентное центрифугирование, лизис эритроцитов лизирующим раствором или комбинацию этих методов с другими, в результате чего наступает разделение эритроцитов и ядросодержащих клеток. Данные ядросодержащие клетки содержат как стволовые клетки, так и прогениторные.
2 этап: Получение лейкоцитов периферической крови
Проводят забор периферической крови любым известным способом, после чего осуществляют получение лейкоцитарной суспензии: для этого 2 мл гепаринизированной крови смешивают с 1 мл подогретого до 37°С 3% раствора желатина и инкубируют в термостате при 37°С в течение 30 мин. После оседания эритроцитов слой плазмы, обогащенный лейкоцитами, отбирают в пластиковые пробирки и отмывают 10-кратным объемом фосфатно-солевого буфера (рН=7,4). Затем лейкоциты после центрифугирования в течение 10 мин при 1000 об/мин ресуспендируют в растворе Хенкса без Са2+ и Mg2+. После подсчета числа лейкоцитов концентрацию клеток доводят до 106 кл.
3 этап: Культивирование клеток
Полученные клетки, а именно лейкоциты периферической крови и стволовые и/или прогениторные клетки, ресуспендируют в культуральной ростовой среде. Клетки культивируют совместно при 37°С в атмосфере, содержащей 5% СО2 и при 95% влажности, в течение 1-60 суток.
4 этап: Получение композиции
После культивирования клетки вместе с культуральной средой переносят в пробирки, в которых клетки подвергаются разрушению с использованием физических (ультразвук, замораживание-оттаивание, электрический импульс и др.), и/или химических (ферменты, химические реагенты и др.), и/или механических (растирание и др.) методов или их комбинации, приводящих к нарушению клеточных структур. Полученную композицию, состоящую из культуральной среды и разрушенных культивированных клеток, можно использовать для приготовления инъекционных форм, таблетированных лекарственных форм, применять в виде пищевых добавок или высушивать, лиофилизировать, замораживать и т.д.
Мази готовятся с использованием в качестве основы медицинского вазелина. Фармакологическую композицию помещают в фарфоровую ступку и растирают фарфоровым пестиком до мелкодисперсного состояния. Затем к полученному порошку добавляют медицинский вазелин и тщательно перетирают до получения однородной (гомогенной) субстанции. Мазь наносилась на поверхность кожи.
Инъекционные формы готовились: Стерильную фармакологическую композицию растворяли в дистиллированной воде. Раствор вводили внутрибрюшинно, внутримышечно, внутривенно или подкожно.
Жидкие препараты для перорального введения могут быть изготовлены, например, в виде растворов, сиропов или суспензий. Такие жидкие препараты могут быть получены стандартными способами с использованием фармацевтически приемлемых добавок, таких как суспендирующие агенты (например, сорбитный сироп, производные целлюлозы или гидрогенизированные пищевые жиры); эмульгирующие агенты (например, лецитин или камедь акации); безводные носители (например, миндальное масло, жирные сложные эфиры, этиловый спирт или фракционированные растительные масла); и консерванты (например, метил- или пропил-п-гидроксибензоаты или сорбиновая кислота).
Дополнительно композиция может быть получена с добавлением антибиотика, противовоспалительного агента, противовирусного агента, противогрибкового агента, гормона, противоопухолевого агента, анальгетика, анестезирующего средства или любой их комбинации. При этом добавление того или иного агента производится с учетом необходимого терапевтического эффекта определяемого специалистом.
Дополнительно композиция может быть получена с добавлением к культивируемым клеткам тканеспецифичного антигена.
В данном примере композиции 1 и 2 проводятся согласно вышеизложенному примеру.
3 этап: Получение тканеспецифичного антигена
Для получения тканеспецифичекого антигена брали свежевыделенную ткань органа. В качестве источника может быть использована аллогенная или ксеногенная ткань, при возможности используется биопсийный материал.
Для получения тканеспецифического антигена клетки органа или тканей разрушают, используя физические (ультразвук, замораживание-оттаивание, электрический импульс и др.), и/или химические (ферменты, химические реагенты и др.) и/или механические (растирание и др.), методы или их комбинации, приводящие к нарушению клеточных структур. Как пример: Ткань механически гомогенизируется на фрагменты не более 0,5 мм3. Полученный гомогенат заливается раствором Хенкса 1:1 и помещается в морозильную камеру на 1 час, затем ткань размораживают, данный цикл повторяют 3 раза. Затем гомогенат центрифугируют при 2000 об/мин 10 мин. Супернатант отбирают и фильтруют через фильтр с диаметром пор 0,22 мкм для обеспечения стерильности раствора. Концентрация белка в растворе определяется методом Лоури и должна находиться в диапазоне от 0,5 до 1 мг/мл.
При этом отмечено, что в основе метода получения тканеспецифичного антигена (ТА) лежит разрушение клеточных структур и оно может осуществляться:
1. Механически - растирание ткани паренхиматозных органов (например, в фарфоровой ступке с использованием фарфорового пестика или в стеклянном гомогенизаторе).
2. С использованием физических методов (например, проведение циклов замораживания-оттаивания или обработка суспензии клеток ультразвуком).
3. С использованием химических методов (например, обработка клеточной суспензии детергентами, которые разрушают липидный бислой клеточных и внутриклеточных мембран).
4. Сочетанием вышеперечисленных методов (механическое перетирание ткани с последующем проведением циклов замораживания-оттаивания).
В нашей работе мы изучали разные способы приготовления ТА и остановились на сочетании механического истирания с последующим проведением циклов замораживания-оттаивания. Мы выбрали данный метод как наиболее простой и быстро выполнимый. Однако проведенные нами исследования показали, что другие (вышеперечисленные методы) позволяют добиться такого же результата (изменяется время манипуляции, ряд методов требует дополнительного оборудования). В своей работе мы определяли уровень активности внутрилизосомальных ферментов (в частности, кислой фосфатазы) в супернатанте после разрушения тканей различными методами. Нами не было зафиксировано достоверных отличий при использовании разных методов разрушения тканей. Таким образом, данный «тканеспецифичный антиген», по нашему мнению, может быть получен любым известным способом.
В нашей работе мы также изучали разные способы получения тканеспецифического антигена, тканеспецифический антиген, может быть получен не только при помощи центрифугирования и последующего фильтрования, но и он может быть в виде гомогената или супернанатата. Основным условием при этом является то, что он является тканеспецифическим антигеном ткани органа, «соответствующего поврежденному».
4 этап: Культивирование с использованием тканеспецифического антигена
Полученные клетки, а именно лейкоциты периферической крови и стволовые и/или прогениторные клетки, ресуспендируют в культуральной ростовой среде. В среду для культивирования клеток также добавляется тканеспецифический антиген, полученный из ткани того органа, регенерацию клеток которого требуется простимулировать. Клетки и тканеспецифический антиген культивируют совместно при 37°С в атмосфере, содержащей 5% СО2 и при 95% влажности, в течение 1-60 суток. Супернатант тканеспецифического антигена добавлялся в культуральную среду в соотношении в среднем 1:30 (проверялся диапазон от 1:10 до 1:80).
5 этап: Получение композиции проводят вышеуказанным способом
Примеры, подтверждающие эффективность предложенной композиции.
Пример 1. Эффективность применения субстрата, полученного из культивированных клеток костного мозга, была изучена в опытах с моделированием дислипидемического повреждения печени у морских свинок.
У морских свинок с хронической дислипидемией в течение 4 месяцев развивается жировая дистрофия печени и резко нарушается морфометрическая характеристика гепатоцитов (таблица 1). Для ускорения восстановительных процессов в печени животным была введена вышеописанная композиция - СККМ. В качестве 1 дозы принимали количество белка, полученное при разрушении 106 клеток культивированных в 5 мл культуральной среды, а также белок, содержащийся в культуральной среде, в которой клетки культивировались в среднем в течение 5 дней. В состав полученных из костного мозга клеток входили: стволовые мезенхимальные клетки (подтверждено культивированием), гемопоэтические прогениторные клетки (CD34+) и лимфоидные клетки. В качестве контроля был использован субстрат, полученный из мононуклеарных клеток периферической крови животных - СПК. Содержание белка в контрольном и опытном субстрате не отличалось друг от друга.
Как видно из представленных данных (табл.1), введение СПК повышало регенерационную способность гепатоцитов при жировой дистрофии печени. Однако данный эффект был недостаточно выражен. Введение СККМ приводит к достоверному повышению процессов регенерации гепатоцитов в печени экспериментальных животных.
Пример 2. Получения фармакологической композиции при использовании в процессе культивирования тканеспецифического антигена.
Использование композиции на модели повреждения миокарда крыс методом криодеструкции (КД). На 30 сутки в зоне повреждения ЛЖ происходило формирование рубцовой ткани округлой формы диаметром 6-7 мм со стороны эпикарда и 3 мм со стороны эндокарда; толщина стенки ЛЖ в центре рубца не превышала 1 мм. Как видно из таблицы 2, убыль относительной массы ЛЖ (на единицу массы тела) после криодеструкции составила примерно 13%, а для свободной стенки ЛЖ этот показатель составил 17%.
Площадь некроза после криодеструкции по отношению к общей площади свободной стенки ЛЖ составила со стороны эпикарда 25.1±3.6%, со стороны эндокарда - 23.0±4.2%. Площадь трансмурального некроза после криодеструкции по отношению к общей площади свободной стенки ЛЖ составила со стороны эпикарда 11.4±0.7%, со стороны эндокарда - 6.4±2.5%.
Таким образом, проведенная морфометрия макропрепаратов поврежденного сердца позволила установить достоверное снижение мышечной массы ЛЖ, что неизбежно должно было бы привести к снижению его сократительной активности.
Основные этапы:
а) Получение стволовых и прогениторных клеток.
Стволовые клетки и прогениторные клетки получали от интактного животного той же линии. Костный мозг забирали у животного, находящегося под общим эфирным наркозом, из бедренной кости, пунктируя кость и промывая ее раствором Хенкса. Эритроциты удаляли, добавляя к полученной суспензии лизирующий раствор в соотношении 1:10. После добавления лизирующего раствора клетки центрифугировали и полученный осадок ресуспендировали раствором Хенкса.
б) Лейкоциты периферической крови получали: 2 мл гепаринизированной крови смешивают с 1 мл подогретого до 37°С 3% раствора желатина и инкубируют в термостате при 37°С в течение 30 мин. После оседания эритроцитов слой плазмы, обогащенный лейкоцитами, отбирают в пластиковые пробирки и отмывали 10-кратным объемом фосфатно-солевого буфера (рН=7,4). Затем лейкоциты после центрифугирования в течение 10 мин при 1000 об/мин ресуспендируют в растворе Хенкса без Са2+ и Mg2+. После подсчета числа лейкоцитов концентрацию клеток доводят до 106 кл.
в) Получение тканеспецифического антигена (ТА):
ТА получали из сердца интактных крыс. Ткань сердца массой 500 мг тщательно механически измельчали ножницами (размер отдельных фрагментов не превышал 0,5 мм) при температуре 4°С. Затем ткань заливали раствором Хенкса в соотношении 1:1 и помещали в морозильную камеру на 1 час, затем ткань размораживали, данный цикл повторяли 3 раза. Гомогенат ткани сердца центрифугируют при 2000 об/мин в течение 10 минут. Супернатант отбирают и фильтруют через фильтр с диаметром пор 0,22 мкм для обеспечения стерильности раствора. Концентрация белка в растворе находилась в диапазоне от 0,5 до 1 мг/мл (по методу Лоури).
г) Полученные стволовые клетки и прогениторные клетки, а также лейкоциты периферической крови помещали в культуральную среду, состоящую из среды культивирования DMEM, 10% бычьей фетальной сыворотки. Одновременно с внесением клеток в культуральную среду вносили супернатант, содержащий тканеспецифический антиген. Супернатант тканеспецифического антигена добавлялся в культуральную среду в соотношении в среднем 1:30. Клетки культивировали в среднем в течение 7 суток (от 1 до 15 суток) при 37°С в атмосфере, содержащей 5% СО2 и при 95% влажности.
В состав культивированных клеток входили: стволовые мезенхимальные клетки (подтверждено культивированием), гемопоэтические прогениторные клетки (CD34+) и лимфоидные клетки.
д) Разрушение культивируемых клеток в культуральной среде после их культивирования.
После культивирования клетки в культуральной среде подвергали разрушению - 2 цикла замораживания-оттаивания и обработка ультразвуком.
е) Из полученной композиции готовили инъекционные препараты, которые вводили животному внутрибрюшинно в течение 7 дней (опытная группа). В качестве 1-го контроля использовали композицию, состоящую из культуральной среды и разрушенных культивированных клеток, которые культивировались без добавления тканеспецифичного антигена. В качестве 1-й дозы принимали количества белка получаемое из 106 клеток, которые культивировались в 10 мл культуральной среды. В качестве 2-го контроля использовали композицию, состоящую из культуральной среды и разрушенных клеток, которые не культивировались (106 клеток и 10 мл культуральной среды).
При введении животным с криодеструкцией (КД) контрольной (2-я контрольная группа) композиции, которая получалась из некультивированных клеток, нами было отмечено увеличение массы миокарда, улучшение сократительной способности сердца, однако ни в одном из проведенных опытов не было получено полного восстановления сердечной мышцы. В 1-й контрольной группе животных с КД, которым вводили композицию, которая получалась из культивированных клеток, но без добавления тканеспецифичного антигена, нами была отмечена достоверно более полная регенерация поврежденного органа. Следует отметить, что масса левого желудочка у крыс (опытная группа) с КД, которым в композицию, получаемую из культивированных клеток, к которым в процессе культивации был добавлен тканеспецифический антиген, достоверно не отличалась от массы миокарда интактных животных (таблица 2) и была достоверно выше по сравнению с 1-м и 2-м контролем. Уровень митозов в опытной группе был достоверно выше по сравнению с 1-й и 2-й группой.
Пример 3.
Эффективность применения композиции, полученной из лимфоидных, стволовых и прогениторных клеток, полученных из периферической крови животных, для лечения острого токсического гепатита.
В работе использовали крыс с моделью острого токсического гепатита (введение п/кожно 0,1 мл 40% масляного раствора CCL4 в течение 14 дней).
Фармакологическую композицию готовили из культивированных лимфоидных, стволовых и прогениторных клеток, полученных из периферической крови. Для повышения числа стволовых и прогениторных клеток в периферической крови животному перед забором клеток вводили в течение 2 дней в/в Г-КСФ (гранулоцитарный колониестимулирующий фактор). Ведение препарата позволило повысить уровень гемопоэтических стволовых клеток с 0,5% (контроль) до 3,5% от общего количества мононуклеарных клеток в периферической крови. В состав полученных из периферической крови клеток входили: гемопоэтические прогениторные клетки (CD34+) и лимфоидные клетки. Среди полученных для дальнейшего культивирования клеток отсутствовали мезенхимальные стволовые клетки, что было подтверждено в процессе культивирования.
а) Получение прогениторных клеток и лейкоцитов из периферической крови.
2 мл гепаринизированной крови смешивали с 1 мл подогретого до 37°С 3% раствора желатина и инкубировали в термостате при 37°С в течение 30 мин. После оседания эритроцитов слой плазмы, обогащенный лейкоцитами, отбирали в пластиковые пробирки и отмывали 10-кратным объемом фосфатно-солевого буфера (рН=7,4). Затем лейкоциты после центрифугирования в течение 10 мин при 1000 об/мин ресуспендировали в растворе Хенкса без Са2+ и Mg2+ После подсчета числа лейкоцитов концентрацию клеток доводили до 106 кл. Присутствие среди выделенных лейкоцитов гемопоэтических прогениторных клеток (CD34+) подтверждено с использованием проточного цитофлюориметра.
б) Тканеспецифичесий антиген (ТА) получали из печени интактных крыс. Ткань печени массой 500 мг тщательно механически измельчали ножницами (размер отдельных фрагментов не превышал 0,5 мм) при температуре 4°С. Затем ткань заливали раствором Хенкса в соотношении 1:1 и помещали в морозильную камеру на 1 час, затем ткань размораживали, данный цикл повторяли 3 раза. Полученный гомогенат подвергали обработке ультразвуком. Гомогенат ткани печени центрифугировали при 2000 об/мин в течение 10 минут. Супернатант отбирали и фильтровали через фильтр с диаметром пор 0,22 мкм для обеспечения стерильности раствора. Концентрация белка в растворе находилась в диапазоне от 0,5 до 1 мг/мл (по методу Лоури).
в) Полученные прогениторные клетки, а также лейкоциты помещали в культуральную среду, состоящую из среды культивирования DMEM, 10% бычьей фетальной сыворотки. Одновременно с внесением клеток в культуральную среду вносили супернатант, содержащий тканеспецифический антиген. Супернатант тканеспецифического антигена добавлялся в культуральную среду в соотношении в среднем 1:30. Клетки культивировали в среднем в течение 10 суток (от 5 до 30 суток) при 37°С в атмосфере, содержащей 5% СО2 и при 95% влажности.
В состав культивированных клеток входили: гемопоэтические прогениторные клетки (CD34+) и лимфоидные клетки.
г) Культивированные клетки вместе с культуральной средой разрушали (механически истирались, озвучивались ультразвуком, подвергались нескольким циклам замораживания-оттаивания).
За дозу вводимой композиции принимали количество белка, получаемого при разрушении 106 клеток, а также белок, содержащийся в 5 мл куьтуральной среды, в которой содержались эти клетки в течение 5 суток. В качестве контроля использовали разрушенные некультивированные клетки периферической крови и культуральную среду, в которой клетки не культивировали.
Полученную композицию вводили животным подкожно ежедневно в течение 7 дней.
Эффективность лечения оценивали по данным биохимии крови.
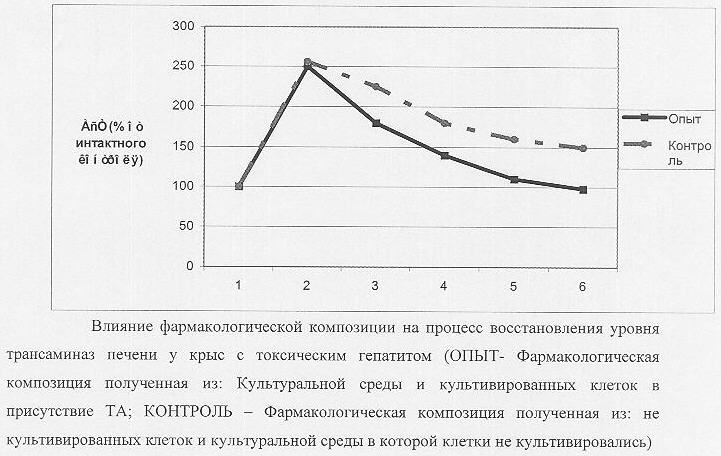
Как видно из данных, представленных чертеже, через 1 неделю после начала введения CCL4 в крови животных наблюдается резкий (в 2,5 раза) подъем уровня трансаминаз (АсТ), что свидетельствует о цитолитическом действии токсина. Ведение композиции, полученной из разрушенных, культивированных клеток периферической крови и культуральной среды, в которой эти клетки культивировались, приводит к выраженному и достоверному лечебному эффекту, который проявляется нормализацией уровня трансаминаз. (За 100% процентов принят уровень фермента в крови интактных крыс.)
Проведенные нами эксперименты на животных продемонстрировали, что композиция, полученная из кондиционированной культуральной среды и разрушенных культивированных клеток, увеличивает процесс регенерации клеток в поврежденном органе. Композиция, состоящая из кондиционированной культуральной среды и разрушенных культивированных клеток, которые были культивированы с добавлением в культуральную среду тканеспецифичного антигена, также достоверно повышает процесс регенерации в поврежденном органе и может быть использована для лечения острых и хронических воспалительных и дегенеративных заболеваний внутренних органов и кожных покровов.
Изобретение относится к области медицины и касается композиции, предназначенной для стимулирования роста и регенерации клеток, а также к способу ее получения. Композиция содержит разрушенные клетки лейкоцитов периферической крови и стволовые и/или прогениторные клетки в кондиционированной среде их культивирования. Способ получения данной композиции для стимуляции роста и регенерации клеток предусматривает получение композиции, состоящей из кондиционированной клеточной культуральной среды, полученной при культивировании лейкоцитов периферической крови и стволовых и/или прогениторных клеток, их разрушение в конденциорованной среде, объединение указанной композиции с фармацевтически приемлемым носителем. Преимущество изобретения заключается в том, что оно может быть использовано для роста и регенерации клеток. 4 н. и 16 з.п.ф-лы, 2 табл., 1 ил.
а) получение стволовых и/или прогениторных клеток;
в) получение лейкоцитов периферической крови;
б) совместное их культивирование;
в) разрушение культивируемых клеток в культуральной среде после их культивирования;
г) объединение указанной композиции с фармацевтически приемлемым носителем.
а) получение стволовых и/или прогениторных клеток;
б) получение лейкоцитов периферической крови;
в) получение супернатанта тканеспецифического антигена, соответствующего поврежденному органу, регенерацию которого требуется простимулировать;
г) совместное культивирование клеток с тканеспецифичным антигеном;
д) разрушение клеток в культуральной среде после их культивирования;
е) объединение указанной композиции с фармацевтически приемлемым носителем.
| СРЕДСТВО ДЛЯ ИЗМЕНЕНИЯ СКОРОСТИ РОСТА ИЛИ РЕПРОДУКЦИИ КЛЕТОК, СПОСОБ ЕГО ПОЛУЧЕНИЯ, СПОСОБ СТИМУЛЯЦИИ ЗАЖИВЛЕНИЯ РАН ИЛИ ЛЕЧЕНИЯ ОЖОГОВ, СПОСОБ КОРРЕКЦИИ КОСМЕТИЧЕСКОГО ДЕФЕКТА, СПОСОБ ИНГИБИРОВАНИЯ СТАРЕНИЯ КОЖИ И СПОСОБ СТИМУЛЯЦИИ РОСТА ВОЛОС | 2000 |
|
RU2280459C2 |
| US 6642048 B1, 04.11.2003 | |||
| US 6800480 B1, 05.10.2004 | |||
| US 7011828 B2, 14.03.2006. | |||
Авторы
Даты
2008-12-20—Публикация
2006-12-28—Подача