Настоящее изобретение относится к способам получения росиглитазона, росиглитазону, полученному такими способами, и фармацевтическим композициям и терапевтическому применению росиглитазона и способам лечения с его использованием.
Малеат росиглитазона, малеат 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона, имеет следующую общую структурную формулу (I):
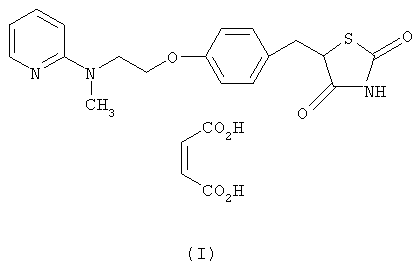
Росиглитазон является представителем класса тиазолидиндионовых соединений и является одним из самых сильнодействующих соединений данного класса. Было показано, что антидиабетики класса тиазолидиндионов, такие как пиоглитазон, энглитазон, росиглитазон, троглитазон и циглитазон, уменьшают резистентность к инсулину у людей. Поэтому росиглитазон является известным антидиабетическим соединением и более конкретно является предпочтительным лекарственным средством для инсулиннезависимого сахарного диабета (NIDDM). Сахарный диабет является комплексным хроническим прогрессирующим заболеванием, которое поражает функцию почек, глаз, сосудистой и нервной систем.
В патентной заявке РСТ WO 94/05659 раскрываются определенные производные тиазолидиндиона, обладающие гипогликемической и гиполипидемической активностью, включая малеат 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона.
В патентных заявках РСТ 99/31093, WO 99/31094 и WO 99/31095 раскрываются различные гидраты малеата росиглитазона с нестехиометрическим содержанием воды.
В патентных заявках РСТ WOOO/64893, WO 00/64896 и WO 02/026737 раскрываются полиморфы малеата росиглитазона. В патентной заявке WO 02/026737 раскрываются полиморфные формы I, II, III и IV малеата росиглитазона, способы их получения и их фармацевтические композиции.
Настоящее изобретение предлагает дополнительные способы получения росиглитазона, включая малеат росиглитазона, а также свободное основание росиглитазона. Что касается получения малеата росиглитазона согласно настоящему изобретению, то описано получение двух полиморфных форм, которые далее обозначены как формы А и В. Форма А малеата росиглитазона является термодинамически стабильной и может быть легко получена из формы В малеата росиглитазона или других безводных или гидратированных полиморфов малеата росиглитазона, описанных в предшествующем уровне техники.
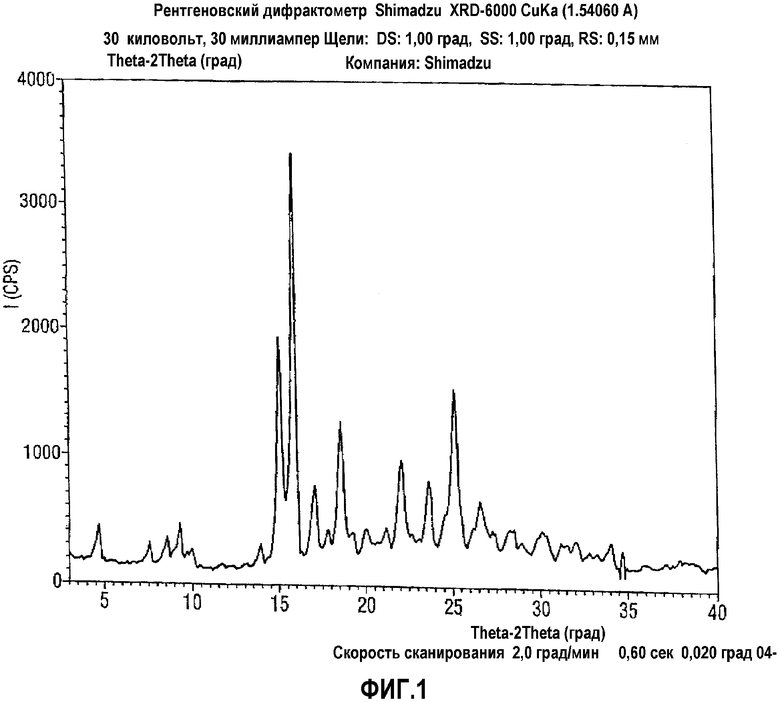
Кристаллическая форма А малеата росиглитазона, полученная согласно настоящему изобретению, имеет рентгенограмму или практически такую же рентгенограмму, как приведено на фиг.1. Более конкретно кристаллическая форма А малеата росиглитазона может быть охарактеризована рентгенограммой с характерными пиками (2θ): 9,25°, 15,86°, 15,02°, 17,00°, 18,52°, 21,99°, 23,58°, 25,06° и 26,55°.
Дополнительные данные рентгеноструктурного анализа, характеризующие кристаллическую форму А малеата росиглитазона, приведены в следующей таблице 1.
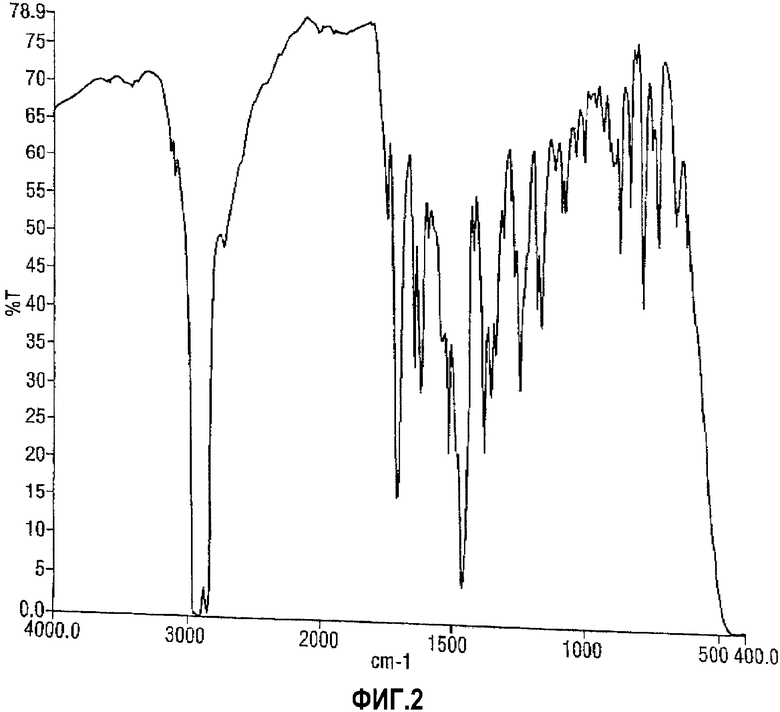
Кристаллическая форма А малеата росиглитазона может быть также охарактеризована, как обладающая инфракрасным спектром поглощения или практически таким же инфракрасным спектром поглощения, как приведено на фиг.2. Характерными пиками являются следующие: 1750, 1705, 1640, 1619, 1514, 1466, 1379, 1361, 1326, 1242, 1163, 866, 774, 715 и 669 см-1. Инфракрасный спектр дисперсии формы А малеата росиглитазона в минеральном масле снимали на спектрометре Perkin Elmer spectrum-1 FT IR.
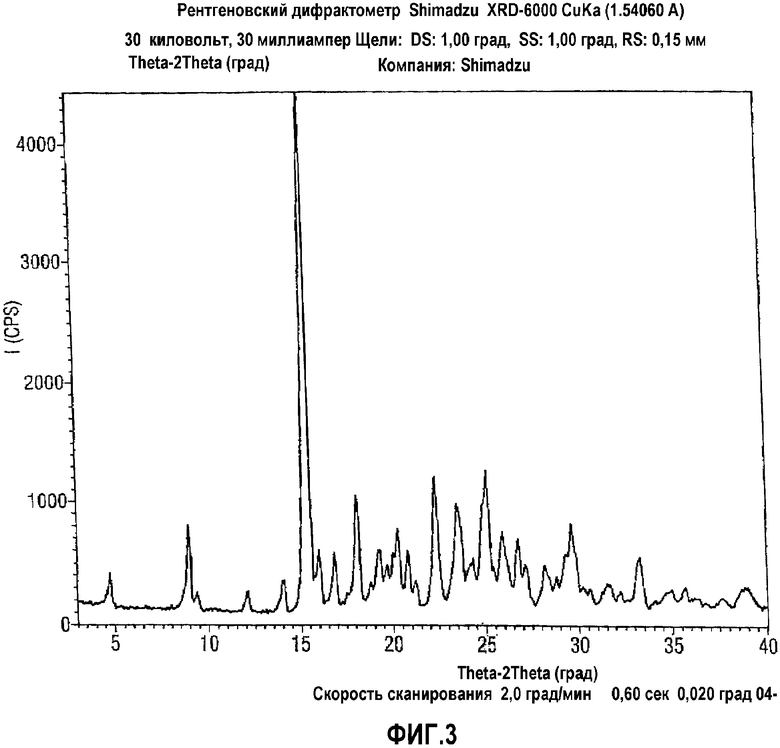
Кристаллическая форма В малеата росиглитазона, полученная согласно настоящему изобретению, имеет рентгенограмму или практически такую же рентгенограмму, как приведено на фиг.3. Более конкретно кристаллическая форма В малеата росиглитазона может быть охарактеризована рентгенограммой с характерными пиками (2θ): 8,93°, 15,37°, 15,86°, 18,05°°, 20,24°, 22,28°, 23,51°, 24,88°, 25,12°, 25,91°, 26,69° и 29,64°.
Дополнительные данные рентгеноструктурного анализа, характеризующие кристаллическую форму В малеата росиглитазона, приведены в следующей таблице 2.
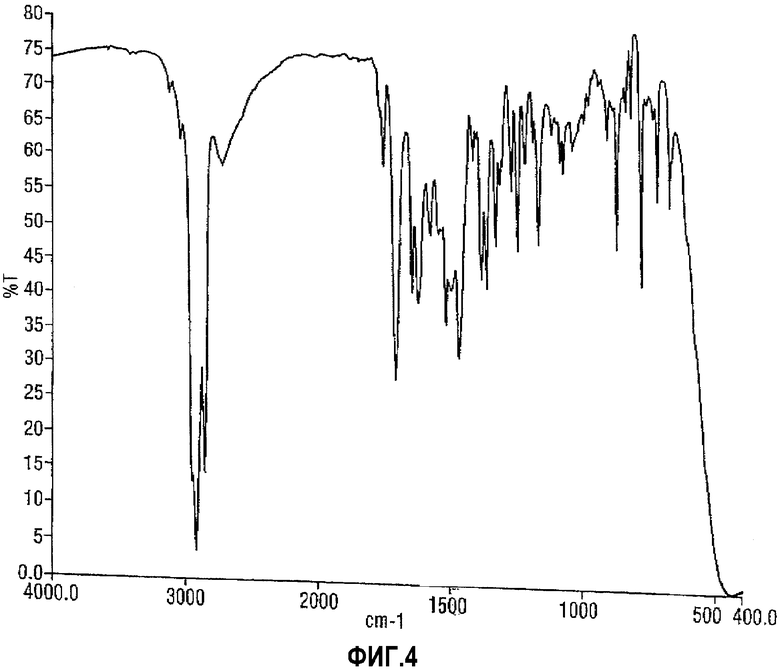
Кристаллическая форма В малеата росиглитазона может быть также охарактеризована, как обладающая инфракрасным спектром поглощения или практически таким же инфракрасным спектром поглощения, как приведено на фиг.4. Характерными пиками являются следующие: 1745, 1708, 1641, 1619, 1464, 1484, 1378, 1354, 1303, 1245, 1179, 1164, 1084, 1071, 862, 824, 778 и 719 см-1. Инфракрасный спектр дисперсии формы В малеата росиглитазона в минеральном масле снимали на спектрометре Perkin Elmer spectrum-1 FT IR.
Настоящим изобретением предлагается способ получения кристаллической формы А малеата росиглитазона, характеризующейся рентгенограммой с характерными пиками (2θ): 9,5, 15,86, 15,02, 17,00, 18,52, 21,99, 23,58, 25,06 и 26,55, который включает приготовление смеси, которая содержит свободное основание росиглитазона и малеиновую кислоту в смешивающимся с водой растворителе, перемешивание указанной смеси и нагревание, получая, таким образом, раствор, фильтрование, получая, таким образом, прозрачный фильтрат, и добавление к нему несмешивающегося с водой растворителя, с последующим перемешиванием и охлаждением, выделяя, таким образом, кристаллическую форму А малеата росиглитазона.
В указанном выше способе подходящим смешивающимся с водой растворителем являются С1-4спирты, причем предпочтительно использование метанола.
Исходную смесь, полученную указанным выше способом, предпочтительно нагревают по меньшей мере около при 45°С, с получением раствора, более пригодно до температуры в интервале около 45-50°С.
Предпочтительным не смешивающимся с водой растворителем является этилацетат, который соответственно добавляют к фильтрату при перемешивании при температуре в интервале около 25-30°С, с последующим дополнительным перемешиванием соответственно в течение около 1 часа при поддержании температуры около 30°С.
Более конкретно охлаждают до температуры около 5-10°С при дальнейшем перемешивании в течение около 1 часа при поддержании в основном вышеуказанной температуры. Образующееся твердое вещество отфильтровывают, промывают этилацетатом и сушат в вакууме, с получением формы А малеата росиглитазона.
Настоящим изобретением предлагается также способ получения кристаллической формы А малеата росиглитазона, характеризующейся рентгенограммой с характерными пиками (2θ): 9,5, 15,86, 15,02, 17,00, 18,52, 21,99, 23,58, 25,06 и 26,55, который включает приготовление смеси, которая содержит свободное основание росиглитазона и малеиновую кислоту в растворителе, кипячение с обратным холодильником указанной смеси, фильтрование указанной смеси и получение фильтрата, добавление затравочных кристаллов формы А малеата росиглитазона к указанному фильтрату с последующим перемешиванием и выделением кристаллической формы А малеата росиглитазона.
Соответственно, используемым растворителем является ацетон, и затравочные кристаллы формы А малеата росиглитазона добавляют при температуре около 35-40°С, как правило, около 40°С, с последующим перемешиванием при пониженной температуре (как правило, около при 30°С) в течение длительного периода времени, которое обычно составляет около 18 часов.
Способ соответственно дополнительно включает сушку в вакууме сначала при температуре около 25-35°С, как правило, около при 30°С и в течение около 5 часов, и затем при температуре в интервале около 45-55°С, как правило, около при 50°С, в течение около 6 часов, с получением формы А малеата росиглитазона.
Настоящим изобретением дополнительно предлагается способ получения кристаллической формы А малеата росиглитазона, характеризующейся рентгенограммой с характерными пиками (2θ): 9,5, 15,86, 15,02, 17,00, 18,52, 21,99, 23,58, 25,06 и 26,55, который включает приготовление смеси, которая содержит свободное основание росиглитазона и малеиновую кислоту в растворителе, кипячение с обратным холодильником указанной смеси, охлаждение указанной смеси и перемешивание, получая, таким образом, твердый осадок, отфильтровывание указанного твердого осадка и сушку с получением кристаллической формы А малеата росиглитазона.
Подходящим растворителем является ацетонитрил, и охлаждение обычно осуществляют до температуры около 25-35°С, более пригодно около 30°С, с последующим перемешиванием в течение около 5 часов при температуре 25-30°С с получением твердого осадка.
Соответственно способ дополнительно включает сушку в вакууме при температуре около 25-35°С, как правило, около при 30°С, в течение около 5 часов, и затем при температуре в интервале около 45-55°С, как правило, около при 50°С в течение около 6 часов с получением формы А малеата росиглитазона.
Настоящим изобретением предлагается также способ получения кристаллической формы А малеата росиглитазона, характеризующейся рентгенограммой с характерными пиками (2θ): 9,5, 15,86, 15,02, 17,00, 18,52, 21,99, 23,58, 25,06 и 26,55, который включает суспендирование полиморфа малеата росиглитазона или гидрата малеата росиглитазона в растворителе и нагревание, получая, таким образом, раствор, охлаждение и перемешивание указанного раствора, и выделение кристаллической формы А малеата росиглитазона.
Предпочтительным растворителем являются C1-4спирты, такие как изопропиловый спирт, и раствор получают нагреванием при температуре около 60-65°С. Раствор соответственно охлаждают до температуры около 25-30°С и перемешивают в течение продолжительного времени, например, в течение около 8 часов. Кристаллы, полученные в результате дополнительного охлаждения, отфильтровывают и сушат в вакууме при температуре около 45-55°С, около 50°С, с получением формы А малеата росиглитазона.
Альтернативно растворителем предпочтительно может являться этилацетат, и раствор получают нагреванием до температуры около 60-65°С. Затем охлаждение осуществляют до температуры около 20-25°С при перемешивании, с последующим дополнительным охлаждением до температуры ниже около 10°С, как правило, около при 5°С. Образующееся твердое вещество отфильтровывают, промывают этилацетатом и сушат в вакууме при температуре около 45-55°С, около при 50°С, с получением формы А малеата росиглитазона.
Настоящим изобретением предлагается также способ получения кристаллической формы В малеата росиглитазона, характеризующейся рентгенограммой с характерными пиками (2θ): 8,93, 15,37, 15,86, 18,05, 20,24, 22,28, 23,51, 24,88, 25,12, 25,91, 26,69 и 29,64, который включает суспендирование формы А малеата росиглитазона, характеризующейся рентгенограммой с характерными пиками (2θ): 9,5, 15,86, 15,02, 17,00, 18,52, 21,99, 23,58, 25,06 И 26,55, в растворителе и нагревание, получая, таким образом, раствор, охлаждение и выдерживание при стоянии, и выделение кристаллической формы В малеата росиглитазона.
Предпочтительно растворителем являются С1-4спирты, такие как изопропиловый спирт, и раствор соответственно получают нагреванием при температуре около 60-65°С. Растворителем также может быть тетрагидрофуран, и раствор получают кипячением с обратным холодильником.
Полученный раствор выдерживают при стоянии при температуре около от 0 до -5°С в течение продолжительного периода времени по меньшей мере около 48 часов, и образовавшиеся кристаллы отфильтровывают и сушат в вакууме при температуре около 45-55°С, более пригодно около при 50°С, с получением формы В малеата росиглитазона.
Настоящее изобретение также предлагает способ получения свободного основания росиглитазона восстановлением 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензилиден]тиазолидин-2,4-диона формулы (II)
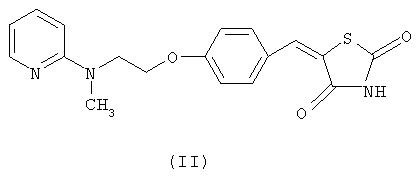
в присутствии иона кобальта, лиганда и восстановителя, где:
ион кобальта может находиться в любой форме, из таких как дихлорид кобальта, диацетат кобальта и трихлорид кобальта;
лиганд выбирают из группы, состоящей из диметилглиоксима, 2,2'-бипиридила и 1,10-фенатролина;
восстановитель выбирают из группы, состоящей из боргидрида натрия, боргидрида лития, боргидрида калия, боргидрида тетраалкиламония и боргидрида цинка;
и необязательно преобразование полученного таким образом свободного основания росиглитазона в фармацевтически приемлемую его соль.
Предпочтительно указанный выше способ осуществляют в присутствии дихлорида кобальта в качестве источника иона кобальта, и/или димитилглиоксима в качестве лиганда, и/или боргидрида натрия в качестве восстановителя. Соединение формулы (II) может быть легко получено по методикам синтеза, хорошо известным в данной области, например, как указано в патенте США 5585495.
Кроме того, предпочтительно, чтобы 5-[4-[2-(N-метилl-N-(2-пиридил)амино)этокси]бензилиден]тиазолидин-2,4-дион формулы (II) суспендировали в тетрагидрофуране в присутствии основания, где основанием является гидроксид щелочного металла, такой как гидроксид натрия. Соответственно реакционную смесь, содержащую 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензилиден]тиазолидин-2,4-дион, дихлорид кобальта, диметилглиоксим и боргидрид натрия, в присутствии тетрагидрофурана в качестве растворителя перемешивают в течение продолжительного периода времени, как правило, около в течение 16 часов, при температуре около 20-30°С.
В дополнение к указанному перемешиванию реакционную смесь соответственно подкисляют, например, добавлением ледяной уксусной кислоты в течение около 1-2 часов. Предпочтительно образовавшуюся суспензию дополнительно перемешивали в течение около 1-2 часов, отфильтровывали полученное твердое вещество, промывали водой и сушили в вакууме при температуре около 55-65°С, как правило, около при 60°С, с получением свободного основания росиглитазона.
Соответствующие фармацевтически приемлемые соли росиглитазона, предлагаемые способом согласно настоящему изобретению, включают соли, образованные с минеральными кислотами, такими как бромистоводородная, хлористоводородная и серная кислоты, или органическими кислотами, такими как метансульфоновая, винная и малеиновая кислоты. В частности, свободное основание росиглитазона, полученное методом согласно настоящему изобретению, предпочтительно превращают в малеат росиглитазона и, в частности, в форму А или форму В малеата росиглитазона, используя стадии способа получения указанных полиморфных форм, как в основном описано выше.
Настоящее изобретение дополнительно предлагает свободное основание росиглитазона, форму А малеата росиглитазона или форму В малеата росиглитазона в основном получаемые способом, описанным выше.
Росиглитазон, полученный согласно настоящему изобретению, полезен для лечения сахарного диабета типа II. Росиглитазон, полученный согласно настоящему изобретению, может быть также рекомендован для особого применения при лечении и/или профилактики других заболеваний, включая гиперлипидемию, гипертензию и сердечно-сосудистые заболевания, особенно атеросклероз. Кроме того, считается, что росиглитазон, полученный согласно настоящему изобретению, может быть полезен при лечении определенных расстройств питания, в частности, регулирования аппетита и приема пищи у субъектов, страдающих расстройствами, связанными с недоеданием, такими как нервная анорексия, и расстройствами, связанными с перееданием, такими как ожирение и анорексия при булимии.
Поэтому настоящее изобретение соответственно предлагает применение росиглитазона, полученного согласно настоящему изобретению, для лечения.
Соответственно настоящее изобретение предлагает применение росиглитазона, полученного согласно настоящему изобретению, для лечения и/или профилактики гипергликемии. В частности, предлагается росиглитазон, полученный согласно настоящему изобретению, для применения при лечении сахарного диабета.
Настоящее изобретение дополнительно предлагает применение росиглитазона, полученного согласно настоящему изобретению, для лечения и/или профилактики гиперлипидемии.
Настоящее изобретение также дополнительно предлагает применение росиглитазона, полученного согласно настоящему изобретению, для лечения гипертензии, сердечно-сосудистого заболевания и определенных расстройств питания. Сердечно-сосудистое заболевание включает в частности атеросклероз. Определенные расстройства питания включают регулирование аппетита и приема пищи у пациентов, страдающих расстройствами, связанными с недоеданием, такими как нервная анорексия, и расстройствами, связанными с перееданием, такими как ожирение и анорексия при булимии.
Соответственно, настоящее изобретение также предлагает фармацевтическую композицию, содержащую росиглитазон, полученный согласно настоящему изобретению, и фармацевтически приемлемый носитель для нее. В частности, форма А малеата росиглитазона, полученная согласно настоящему изобретению, удобна для применения в фармацевтических композициях, так как она является безводной, кристаллической и не гигроскопичной. Предпочтительно композиция, предлагаемая настоящим изобретением, может быть применена для перорального введения. Фармацевтические композиции данного изобретения, однако, могут вводиться любым удобным путем и в любой удобной форме, например, перорально в форме таблеток, капсул, жидких препаратов, гранул, лепешек, или парентерально в форме растворов или суспензий для инъекций или инфузий.
Фармацевтические композиции изобретения могут быть получены традиционными методами в данной области. Например, таблетки могут быть получены смешиванием активного ингредиента с обычными вспомогательными веществами и/или разбавителями и последующим прессованием смеси в обычной таблетировочной машине. Примеры вспомогательных веществ и разбавителей могут включать кукурузный крахмал, картофельный крахмал, тальк, стеарат магния, желатин, лактозу, камедь и подобные. Любые другие вспомогательные вещества или добавки красителей, ароматизаторов, консервантов или подобные также могут быть использованы, при условии их совместимости с росиглитазоном, полученным согласно настоящему изобретению.
Растворы для инъекций могут быть получены растворением росиглитазона, полученного согласно настоящему изобретению, и возможных добавок в части растворителя для инъекции, обычно стерильной воде, доведением раствора до требуемого объема, стерилизацией раствора и заполнением соответствующих ампул или флаконов. Может быть введена любая приемлемая добавка, обычно используемая в данной области, например тонизирующие вещества, консерванты, антиоксиданты и подобные.
Настоящее изобретение дополнительно предлагает способ лечения и/или профилактики гипергликемии у пациента, который предусматривает введение терапевтически эффективного количества росиглитазона, полученного согласно настоящему изобретению, пациенту с гипергликемией, нуждающемуся в этом. В частности, настоящее изобретение предлагает способ лечения и/или профилактики сахарного диабета у пациента, который включает введение терапевтически эффективного количества росиглитазона, полученного согласно настоящему изобретению, пациенту, страдающему или предрасположенному к сахарному диабету.
Настоящее изобретение дополнительно предлагает способ лечения гиперлипедемии у пациента, который включает введение терапевтически эффективного количества росиглитазона, полученного согласно настоящему изобретению, пациенту с гиперлипедемией, нуждающемуся в этом.
Настоящее изобретение дополнительно предлагает способ лечения гипертензии, сердечно-сосудистого заболевания или определенных расстройств питания, описанных выше, включающий введение терапевтически эффективного количества росиглитазона, полученного согласно настоящему изобретению, пациенту, нуждающемуся в этом.
В качестве дополнительного аспекта настоящее изобретение предлагает применение росиглитазона, полученного согласно настоящему изобретению, для изготовления лекарственного средства для лечения и/или профилактики гипергликемии. В частности, настоящее изобретение предлагает применение росиглитазона, полученного согласно настоящему изобретению, для изготовления лекарственного средства для лечения и/или профилактики сахарного диабета.
Настоящее изобретение также предлагает применение росиглитазона, полученного согласно настоящему изобретению, для приготовления лекарственного средства для лечения и/или профилактики гиперлипидемии.
Настоящее изобретение также предлагает применение росиглитазона, полученного согласно настоящему изобретению, для изготовления лекарственного средства для лечения и/или профилактики гипертензии, сердечно-сосудистого заболевания или определенных расстройств питания.
Выбор конкретной дозированной формы росиглитазона, полученного согласно настоящему изобретению, для терапевтического применения или лечения в соответствии с настоящим изобретением будет зависеть от подвергаемого лечению конкретного болезненного состояния, симптомов и тяжести заболевания. Предпочтительно путь введения и частота дозирования находятся в компетенции лечащего врача.
Настоящее изобретение далее будет проиллюстрировано следующими чертежами и примерами, которые никаким образом не ограничивают объем изобретения.
На фиг.1 приведена конкретная порошковая рентгенограмма формы А малеата росиглитазона.
На фиг.2 приведен ИК-спектр формы А малеата росиглитазона.
На фиг.3 приведена конкретная порошковая рентгенограмма формы В малеата росиглитазона.
На фиг.4 приведен ИК-спектр формы В малеата росиглитазона.
Примеры
Получение 1 по известному уровню техники
Малеат росиглитазона получали согласно описанию WO 94/05659, где 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-дион (470 г) и малеиновую кислоту (137 г) растворяли в этаноле (4 л) при кипении. Горячий раствор фильтровали через кизельгур и затем давали возможность медленно остыть при легком перемешивании. После выдерживания в холодильнике при 0-5°С в течение нескольких часов малеат отфильтровывали, промывали этанолом и сушили в вакууме при 50°С, получая в результате 446 г малеата росиглитазона, как предложено в WO 94/05659. Продукт идентифицировали как форму В по рентгенограмме и ИК-спектру, как можно видеть на фиг.3 и 4 соответственно.
Пример 1
5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензилиден]тиазолидин-2,4-дион (10 г) суспендировали в воде (30 мл) и тетрагидрофуране (30 мл) и к полученной суспензии добавляли 25 мл 4% гидроксида натрия. Полученную смесь охлаждали до 10°С и добавляли к ней раствор катализатора, полученный растворением 1,88 г диметилглиоксима и 0,200 г дихлорида кобальта в 30 мл тетрагидрофурана. Затем медленно добавляли раствор 3,2 г боргидрида натрия в 30 мл воды и 9,4 мл 4% гидроксида натрия при 10°С в течение 90 минут. Полученную реакционную смесь перемешивали при 25°С в течение 16 часов и затем подкисляли 60% ледяной уксусной кислотой, которую добавляли очень медленно в течение 1-2 часов. Образовавшуюся суспензию дополнительно перемешивали в течение 1,5 часов. Получаемое твердое вещество (в форме свободного основания росиглитазона) отфильтровывали, промывали водой и сушили в вакууме при 60°С, получая в результате 9,3 г 5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-диона.
Пример 2
5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-дион (свободное основание росиглитазона, 50 г, 0,140 моль) загружали в 100 мл метанола, добавляли раствор малеиновой кислоты (18,7 г, 0,16 моль) в метаноле (50 мл) при перемешивании и дополнительно нагревали до 45-50°С с получением прозрачного раствора. Полученный раствор (горячий) фильтровали через целит, медленно добавляли к прозрачному фильтрату этилацетат (500 мл) при перемешивании при 25-30°С и дополнительно перемешивали в течение 1 часа при 30°С, затем охлаждали до 5-10°С и перемешивали при этой температуре в течение 1 часа. Полученное твердое вещество отфильтровывали в атмосфере аргона и промывали 50 мл этилацетата. Твердое вещество сушили в вакууме при 50-55°С, получая в результате форму А малеата росиглитазона (60 г) с выходом 90%.
Пример 3
5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-дион (свободное основание росиглитазона, 100 г, 0,280 моль) суспендировали в 500 мл сухого ацетона и добавляли раствор малеиновой кислоты (38,99 г, 0,336 моль) в 200 мл сухого ацетона при 27°С с получением прозрачного раствора. Добавляли активированный уголь (5 г) и кипятили с обратным холодильником в течение 30 минут. Горячий раствор фильтровали через целит. К прозрачному фильтрату добавляли затравочные кристаллы формы А при 40°С и перемешивали в течение 18 часов при 30°С. Осажденное твердое вещество отфильтровывали в атмосфере аргона и промывали 100 мл сухого ацетона. Полученное твердое вещество сушили в вакууме при 30°С в течение 5 часов и при 50°С в течение 6 часов, получая в результате форму А малеата росиглитазона (95 г) с выходом 72%.
Пример 4
5-[4-[2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-дион (свободное основание росиглитазона, 50 г, 0,140 моль) перемешивали с 250 мл сухого ацетонитрила и добавляли суспензию малеиновой кислоты (19,50 г, 0,168 моль) в 100 мл сухого ацетонитрила при 27°С до получения прозрачного раствора, с последующим кипячением с обратным холодильником в течение 30 минут при 80-82°С. Реакционной массе давали постепенно остыть до 30°С и перемешивали в течение 5 часов при 25-30°С. Осажденное твердое вещество отфильтровывали в атмосфере аргона и промывали 50 мл сухого ацетонитрила. Полученное отфильтрованное твердое вещество сушили в вакууме при 30°С в течение 5 часов и при 50°С в течение 6 часов, получая в результате форму А малеата росиглитазона (45 г) с выходом 71%.
Пример 5
Форму В малеата росиглитазона (50 г, 0,105 моль) суспендировали в 1500 мл изопропилового спирта и нагревали до 60-65°С с получением прозрачного раствора. Раствор постепенно охлаждали до 27°С и перемешивали в течение 8 часов. Полученные кристаллы отфильтровывали и сушили в вакууме при 50°С, получая в результате форму А малеата росиглитазона (40 г) с выходом 80%.
Пример 6
5- [4- [2-(N-метил-N-(2-пиридил)амино)этокси]бензил]тиазолидин-2,4-дион (свободное основание росиглитазона, 25 г, 0,07 моль) суспендировали в 900 мл ацетона, добавляли по каплям раствор малеиновой кислоты (9,74 г, 0,083 моль) в 25 мл метанола в течение 20 минут при 25°С. К полученному выше прозрачному раствору добавляли активированный уголь (5,0 г), перемешивали при 25°С в течение 20 минут и затем фильтровали через целит. Полученный прозрачный фильтрат перемешивали в течение 12 часов при температуре окружающей среды. Осажденное твердое вещество выделяли фильтрованием и сушили в вакууме при 50°С, в результате получая желаемую форму В малеата росиглитазона (20 г).
Пример 7
Форму А малеата росиглитазона (20 г, 0,105 моль) суспендировали в 600 мл изопропилового спирта и нагревали до 60-65°С с получением прозрачного раствора. Раствор выдерживали при стоянии при температуре от 0 до -5°С в течение 48 часов. Полученные кристаллы отфильтровывали и сушили в вакууме при 50°С, получая в результате форму В малеата росиглитазона (15,0 г).
Пример 8
Форму А малеата росиглитазона (20 г, 0,105 моль) суспендировали в 400 мл тетрагидрофурана и кипятили с обратным холодильником, с получением прозрачного раствора. Раствор выдерживали при стоянии при температуре от 0 до -5°С в течение нескольких дней. Полученные кристаллы отфильтровывали и сушили в вакууме при 50°С, получая в результате форму В малеата росиглитазона (16,0 г).
Пример 9
Форму В малеата росиглитазона (50 г) суспендировали в 500 мл этилацетата и нагревали до 60°С в инертной атмосфере, образовавшийся раствор быстро охлаждали при перемешивании до 25°С, затем охлаждали до 5°С. Полученное твердое вещество отфильтровывали, промывали охлажденным этилацетатом и сушили в вакууме при 50°С, получая в результате форму А малеата росиглитазона.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТВЕРДЫЕ ФОРМЫ АЛЬФА, ОМЕГА ДИЗАМЕЩЕННОГО ДИГИДРОКСИЦИКЛОПЕНТИЛЬНОГО СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2014 |
|
RU2730520C2 |
| ПОЛИМОРФНЫЕ КРИСТАЛЛИЧЕСКИЕ ФОРМЫ 5-[4-2-[N-МЕТИЛ-N-(2-ПИРИДИЛ)АМИНО]ЭТОКСИ]БЕНЗИЛ]ТИАЗОЛИДИН-2,4-ДИОН МАЛЕАТА | 2001 |
|
RU2286345C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА ПРОИЗВОДНОГО ТИОФЕНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2022 |
|
RU2830948C1 |
| МАЛЕАТ 3-[2-(ДИМЕТИЛАМИНО)МЕТИЛ-(ЦИКЛОГЕКС-1-ИЛ)]ФЕНОЛА И ЕГО КРИСТАЛЛИЧЕСКИЕ ФОРМЫ | 2006 |
|
RU2434845C2 |
| СОЛЬ ПРИСОЕДИНЕНИЯ КИСЛОТЫ СОЕДИНЕНИЯ, ИНГИБИРУЮЩЕГО Trk | 2015 |
|
RU2708236C2 |
| КРИСТАЛЛИЧЕСКАЯ ФОРМА БИСУЛЬФАТНОГО ИНГИБИТОРА JAK-КИНАЗЫ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2015 |
|
RU2716260C2 |
| ЦЕОЛИТНАЯ КОМПОЗИЦИЯ UZM-35, СПОСОБ ПОЛУЧЕНИЯ И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2525417C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ ПОЗАКОНАЗОЛА И СПОСОБ ПОЛУЧЕНИЯ АМОРФНОГО ПОЗАКОНАЗОЛА | 2016 |
|
RU2750898C2 |
| КРИСТАЛЛЫ ЛОБАПЛАТИНА, СПОСОБЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ В ФАРМАЦЕВТИКЕ | 2014 |
|
RU2648990C1 |
| ПОЛИМОРФ МАЛЕАТА ИНГИБИТОРА ДИПЕПТИДИЛПЕПДИДАЗЫ IV(DPPIV) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2732577C1 |
Настоящее изобретение относится к способам получения росиглитазона, росиглитазону, полученному этими способами, и его фармацевтическим композициям и способам лечения с его использованием. Технический результат - получены новые кристаллические модификации росиглитазона, обладающие полезными биологическими свойствами. 10 н. и 38 з.п. ф-лы, 4 ил., 2 табл.
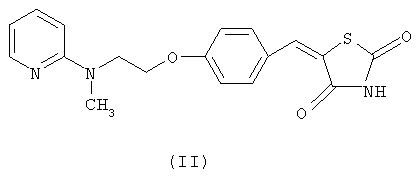
в присутствии иона кобальта, лиганда и восстановителя, в котором ион кобальта может находиться в любой форме дихлорида кобальта, диацетата кобальта и трихлорида кобальта;
лиганд выбирают из группы, состоящей из диметилглиоксима, 2,2'-бипиридила и 1,10-фенатролина;
восстановитель выбирают из группы, состоящей из боргидрида натрия, боргидрида лития, боргидрида калия, боргидрида тетраалкиламония и боргидрида цинка;
и необязательно превращение полученного таким образом свободного основания росиглитазона в фармацевтически приемлемую его соль.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| WO 00/64896 А, 02.11.2000 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| WO 00/64893 A, 02.11.2000 | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| EP 1284268 A, 19.02.2003 | |||
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ТИАЗОЛИДИНДИОНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2128179C1 |
| Полиуретановая композиция | 1984 |
|
SU1219620A1 |
| EP 1277753 A, 22.01.2003 | |||
| WO 00/64892 A, 02.11.2000. | |||
Авторы
Даты
2008-12-27—Публикация
2004-08-13—Подача