Изобретение относится к медицине и биологии в области генетики и может быть использовано для точного определения уровня генетической стабильности хромосом.
Известен способ оценки уровня поломок хромосом (А.А.Прокофьев-Бельговская, Н.П.Бочков, К.Н.Гринбер и др. Основы цитогенетики человека. М., Медицина. 1969. - 544 с.).
Однако в данном способе не предусматривается применение такого комплекса исследуемых параметров хромосом и статистическая обработка всех полученных результатов с выражением уровня генетической стабильности хромосом одним числом.
Целью изобретения является повышение точности определения уровня генетической стабильности хромосом человека.
Сущность заявляемого способа заключается в том, что для исследования генетической стабильности хромосом у людей из локтевой вены берется кровь для культивирования лимфоцитов и приготовления препаратов метафазных хромосом с последующим анализом хромосомных препаратов для изучения уровня хромосомных аберраций с последующей обработкой полученных данных системным многофакторным анализом.
Полученное значение является общим потенциалом генетической стабильности хромосом у каждого конкретного человека.
Способ отличается тем, что с применением нескольких технически простых и не требующих дорогостоящих реактивов, оборудования, затрат сил и времени методов, возможно определение уровня стабильности хромосом у каждого конкретного человека с последующим вычислением общего потенциала стабильности хромосом, по значению которого можно точно судить об уровне сохранности наследственного материала у того или иного индивида.
Способ осуществляется следующим образом. Постановка культуры лимфоцитов и приготовление препаратов метафазных хромосом проводится по описанной ниже схеме.
Используется гепарин фирмы "Ricter" (Венгрия), фитогемагглютинин фирмы "Difko-P" (США), среда 199, сыворотка крупного рогатого скота, колхицин, хлорид калия, метанол, ледяная уксусная кислота, серная кислота концентрированная, дихромат калия, нитрат серебра, раствор желатина, цитрат натрия, хлорид натрия, гидроортофосфат натрия, дигидроортофосфат калия, краситель Гимза фирмы "Merck" (США). Реактивы отечественного производства были марки "ХЧ" и "ОСЧ".
Культивирование крови и приготовление препаратов метафазных хромосом проводили по общепринятой методике [Методические рекомендации / ЦИУВ. - М.: Медицина, 1989. - 113 с.; Бочков, Н.П. Культура лимфоцитов как тест-объект для изучения генетических последствий у лиц, контактирующих с мутагенами. / Н.П.Бочков, B.C.Журков, Н.П.Кулешов // Докл. АН СССР. - 1974. - Т.218. - №2. - С.463-465]. Кровь забирали из локтевой вены (10 мл) и заполняли ею стерильные пенициллиновые флаконы, в которых находился раствор гепарина (0,1 мл на 1 мл крови). Гепарин использовали в разведении бидистилированной водой 1:20. Кровь культивировали в стерильных пенициллиновых флаконах с питательной средой при 37°С в течение 72 часов. Питательная среда состояла из среды 199 (6,0 мл) и сыворотки крупного рогатого скота (1,5 мл). В качестве стимулятора пролиферативной активности использовали фитогемагглютинин. За 2 часа до начала фиксации в культуру лимфоцитов добавляли колхицин в конечной концентрации 0,5 мкг/мл.
Фиксацию проводили на 72 часу культивирования. После центрифугирования и отсасывания надосадочной жидкости клетки инкубировали с предварительно подогретым до 37°С 0,75 М раствором хлорида калия в течение 20 минут при 37°С. После гипотонизации проводили центрифугирование и отбор надосадочной жидкости. Клетки фиксировали в фиксаторе Карнуа (метанол + уксусная кислота) в соотношении 3:1 в течение трех и более часов. За это время производили три смены фиксатора. После полного обесцвечивания суспензии клеток, ее раскапывали на обезжиренные предметные стекла, смоченные дистиллированной холодной водой. Препараты высушивали на воздухе и шифровали.
Посадку, культивирование лимфоцитов крови и приготовление препаратов проводили строго стандартно во всех случаях. После приготовления препараты выдерживали при комнатной температуре для окраски нитратом серебра 7-14 дней, а для рутинного окрашивания для изучения уровня хромосомных аберраций - 2-3 дня.
Для проведения исследований на мутагенез хромосомные препараты окрашивали с помощью красителя Романовского-Гимзы на воде в соотношении 1:50, без предварительной обработки. Время окрашивания в наших исследованиях 10 мин. Метафазные пластинки должны быть хорошо окрашены, без наложений друг на друга хромосом. На метафазных пластинках не должно быть «подложки» - остатков ядерной оболочки, что говорит о недостаточном времени культивирования.
Готовые препараты изучали под микроскопом, при этом у одного человека в нашем исследовании наблюдали 200 метафазных пластинок, их заносили в протокол, где указывался тип повреждения хромосомы, ее группа и координаты метафазной пластинки. По всем оцениваемым показателям уровня хромосомных аберраций (количество клеток с хромосомными аберрациями, количество хромосомных аберраций (на 100 кл.), общее количество фрагментов хромосом, количество обменов, количество одиночных фрагментов, количество парных фрагментов, количество хромосомных обменов, количество хроматидных обменов) вычисляли среднеарифметические значения.
Для определения весомости всех оцениваемых параметров и вычисления общего потенциала стабильности хромосом у обследованных применяется системный многофакторный анализ, позволяющий перевести исследуемые многомерные количественные характеристики с несопоставимыми абсолютными значениями в сопоставимые относительные величины (Углова М.В., Углов Б.А., Архипов В.В., Горшкова Т.В., Петунина Н.А., Оль Т.Л., Прохуровская М.А., Шубин С.И. Применение методов морфометрии и статистического анализа в морфологических исследованиях. Куйбышев, 1982. - 47 с.). Метод дает возможность выразить все показатели генетической стабильности хромосом единым интегральным показателем. Расчет производился по формулам:
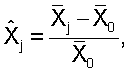
где 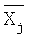 - исследуемый параметр,
- исследуемый параметр, 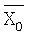 - нормативный параметр,
- нормативный параметр, 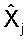 - относительная разность.
- относительная разность.
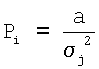
где Pi - весовой коэффициент (коэффициент влияния), а - постоянный множитель (в наших исследованиях а=0,1), σj - среднеквадратическое отклонение значения 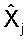 в относительных единицах.
в относительных единицах.
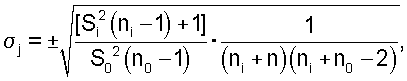
где Si 2 - дисперсия исследуемого параметра Xi, ni - количество наблюдений при определении Xi, S0 2 - дисперсия нормативного параметра Х0, n0 - количество наблюдений при определении Х0.
Нормативные значения получают при обследовании тщательно отобранных здоровых людей (n не менее 20) с вычислением среднеарифметических значений по каждому из оцениваемых показателей. Обработка полученных результатов системным многофакторным анализом с определением общего потенциала стабильности хромосом (ХBi ОПСХ) по приведенной ниже формуле позволяет адекватно оценивать стабильность генетической информации у обследуемых.
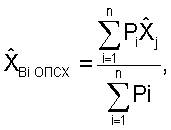
где 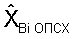 - величина, интегрально характеризующая уровень генетической стабильности хромосом в относительных единицах.
- величина, интегрально характеризующая уровень генетической стабильности хромосом в относительных единицах.
Общий потенциал стабильности хромосом 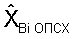 в норме составляет от 0,012 до 0,030. В случае, если его значения составляют от 0 до 0,011, то человек входит в группу риска по развитию нестабильности хромосом и возникновению различных заболеваний. Необходимо ежемесячное обследование этих пациентов на предмет уровня хромосомных аббераций с нормализацией образа жизни. При значении
в норме составляет от 0,012 до 0,030. В случае, если его значения составляют от 0 до 0,011, то человек входит в группу риска по развитию нестабильности хромосом и возникновению различных заболеваний. Необходимо ежемесячное обследование этих пациентов на предмет уровня хромосомных аббераций с нормализацией образа жизни. При значении 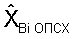 ниже «0» - у больных имеет место нестабильность генетического аппарата, требующая проведения антиоксидантной терапии и присоединения веществ, усиливающих репарацию ДНК (витамин В5).
ниже «0» - у больных имеет место нестабильность генетического аппарата, требующая проведения антиоксидантной терапии и присоединения веществ, усиливающих репарацию ДНК (витамин В5).
Внедрение данного способа оценки потенциала стабильности хромосом у больных в практику лечебных учреждений, центров планирования семьи и медикогенетических консультаций, позволит решить ряд насущных социально-экономических проблем современности. Своевременное и адекватное назначение корректирующего подхода для оптимизации 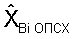 в каждом конкретном случае способно улучшить состояние генетического аппарата и обеспечить получение более здорового потомства от женщин, собирающихся забеременеть.
в каждом конкретном случае способно улучшить состояние генетического аппарата и обеспечить получение более здорового потомства от женщин, собирающихся забеременеть.
Пример 1. Жительница С. г.Курска, 36 лет, практически здорова, ведущая здоровый образ жизни, обследована во время профилактического осмотра по месту жительства. У женщины была взята кровь и исследована по изложенной выше схеме с оценкой уровня хромосомных аберраций и расчетом общего потенциала стабильности хромосом.
У обследуемой были найдены следующие значения оцениваемых показателей: количество клеток с хромосомными аберрациями 1,09±0,05, количество хромосомных аберраций (на 100 кл.) 1,13±0,02, общее количество фрагментов хромосом 1,23±0,07, количество обменов 0,112±0,04, количество одиночных фрагментов 0,58±0,01, количество парных фрагментов 0,42±0,09, количество хромосомных обменов 0,074±0,03, количество хроматидных обменов 0,056±0,08.
Полученные результаты были обработаны с помощью системного многофакторного анализа. В качестве нормативных значений взяты результаты обследования тщательно отобранных здоровых людей (n=28) (количество клеток с хромосомными аберрациями 1,07±0,08, количество хромосомных аберраций (на 100 кл.) 1,11±0,09, общее количество фрагментов хромосом 1,22±0,08, количество обменов 0,12±0,03, количество одиночных фрагментов 0,56±0,06, количество парных фрагментов 0,43±0,05, количество хромосомных обменов 0,07±0,02, количество хроматидных обменов 0,05±0,03). Установлено, что у обследованной Xj составлял для количества клеток с хромосомными аберрациями 0,0187, для количества хромосомных аберраций (на 100 кл.) 0,0180, для общего количества фрагментов хромосом 0,0082, для количества обменов -0,0667, для количества одиночных фрагментов 0,0357, для количества парных фрагментов -0,0233, для количества хромосомных обменов 0,0571, для количества хроматидных обменов 0,12, Pi составлял для количества клеток с хромосомными аберрациями 156,25, для количества хромосомных аберраций (на 100 кл.) 158,73, для общего количества фрагментов хромосом 159,74, для количества обменов 173,61, для количества одиночных фрагментов 156,25, для количества парных фрагментов 163,93, для количества хромосомных обменов 151,52, для количества хроматидных обменов 140,85, S2 составлял для количества клеток с хромосомными аберрациями 0,001681, для количества хромосомных аберраций (на 100 кл.) 0,001936, для общего количества фрагментов хромосом 0,00272484, для количества обменов 0,00013456, для количества одиночных фрагментов 0,00013456, для количества парных фрагментов 0,00003721, для количества хромосомных обменов 0,0000000361, для количества хроматидных обменов 0,0000000121.
Определение общего потенциала стабильности хромосом 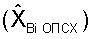 по формуле
по формуле
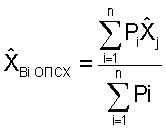
позволило оценивать в целом уровень стабильности генетической информации у обследуемой 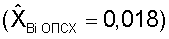 как высокий.
как высокий.
Обследуемой было рекомендовано и далее вести здоровый образ жизни.
Пример 2. Больная К. г.Курска, 42 года, страдающая язвенной болезнью желудка, обследована во время лечения в стационаре по поводу обострения язвенной болезни. У женщины была взята кровь и исследована по изложенной выше схеме с оценкой уровня хромосомных аберраций и расчетом общего потенциала стабильности хромосом.
У обследуемой были найдены следующие значения оцениваемых показателей: количество клеток с хромосомными аберрациями 1,10±0,09, количество хромосомных аберраций (на 100 кл.) 1,10±0,02, общее количество фрагментов хромосом 1,25±0,05, количество обменов 0,116±0,07, количество одиночных фрагментов 0,55±0,01, количество парных фрагментов 0,44±0,02, количество хромосомных обменов 0,078±0,04, количество хроматидных обменов 0,048±0,06.
Полученные результаты были обработаны с помощью системного многофакторного анализа. В качестве нормативных значений взяты результаты обследования тщательно отобранных здоровых людей (n=28) (количество клеток с хромосомными аберрациями 1,07±0,08, количество хромосомных аберраций (на 100 кл.) 1,11±0,09, общее количество фрагментов хромосом 1,22±0,08, количество обменов 0,12±0,03, количество одиночных фрагментов 0,56±0,06, количество парных фрагментов 0,43±0,05, количество хромосомных обменов 0,07±0,02, количество хроматидных обменов 0,05±0,03). Установлено, что у обследованной Xi составлял для количества клеток с хромосомными аберрациями 0,028, количества хромосомных аберраций (на 100 кл.) -0,009, общего количества фрагментов хромосом 0,0246, количества обменов - 0,033, количества одиночных фрагментов -0,0179, количества парных фрагментов 0,0233, количества хромосомных обменов 0,1143, количества хроматидных обменов -0,04), Pi составлял для количества клеток с хромосомными аберрациями 156,08, для количества хромосомных аберраций (на 100 кл.) 162,71, для общего количества фрагментов хромосом 157,16, для количества обменов 162,26, для количества одиночных фрагментов 164,18, для количества парных фрагментов 156,72, для количества хромосомных обменов 143,16, для количества хроматидных обменов 168,33, S2 составлял для количества клеток с хромосомными аберрациями 0,0017406, для количества хромосомных аберраций (на 100 кл.) 0,0017506, для общего количества фрагментов хромосом 0,002905, для количества обменов 0,00000021, для количества одиночных фрагментов 0,0001088, для количества парных фрагментов 0,0000000441, для количества хромосомных обменов 0,0000000441, для количества хроматидных обменов 0,00000000624.
Определение общего потенциала стабильности хромосом 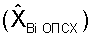 по формуле
по формуле
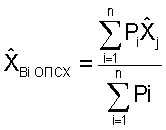
позволило оценивать в целом стабильность генетической информации у больной. Общий потенциал стабильности хромосом составил 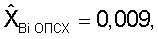 что указывало на снижение стабильности хромосом обследуемой.
что указывало на снижение стабильности хромосом обследуемой.
Обследуемой была рекомендована диета, богатая витаминами и молочными продуктами.
Пример 3. Житель Н. Курской области, 58 лет, страдающий раком прямой кишки, обследован во время лечения в Областном онкологическом диспансере. У больного была взята кровь и исследована по изложенной выше схеме с оценкой уровня хромосомных аберраций и расчетом общего потенциала стабильности хромосом.
У больного были найдены следующие значения оцениваемых показателей: количество клеток с хромосомными аберрациями 1,08±0,01, количество хромосомных аберраций (на 100 кл.) 1,13±0,07, общее количество фрагментов хромосом 1,24±0,03, количество обменов 0,11±0,09, количество одиночных фрагментов 0,58±0,05, количество парных фрагментов 0,41±0,02, количество хромосомных обменов 0,06±0,08, количество хроматидных обменов 0,047±0,02.
Полученные результаты были обработаны с помощью системного многофакторного анализа. В качестве нормативных значений взяты результаты обследования тщательно отобранных здоровых людей (n=28) (количество клеток с хромосомными аберрациями 1,07±0,08, количество хромосомных аберраций (на 100 кл.) 1,11±0,09, общее количество фрагментов хромосом 1,22±0,08, количество обменов 0,12±0,03, количество одиночных фрагментов 0,56±0,06, количество парных фрагментов 0,43±0,05, количество хромосомных обменов 0,07±0,02, количество хроматидных обменов 0,05±0,03). Установлено, что у обследованного Xj составлял для количества клеток с хромосомными аберрациями 0,0093, количества хромосомных аберраций (на 100 кл.) 0,018, общего количества фрагментов хромосом 0,0164, количества обменов - 0,0833, количества одиночных фрагментов 0,0357, количества парных фрагментов 0,0465, количества хромосомных обменов -0,1429, количества хроматидных обменов -0,06, Pi составлял для количества клеток с хромосомными аберрациями 158,98, для количества хромосомных аберраций (на 100 кл.) 158,35, для общего количества фрагментов хромосом 158,52, для количества обменов 169,58, для количества одиночных фрагментов 155,59, для количества парных фрагментов 322,58, для количества хромосомных обменов 158,53, для количества хроматидных обменов 171,23, S2 составлял для количества клеток с хромосомными аберрациями 0,0019386, для количества хромосомных аберраций (на 100 кл.) 0,0019386, для общего количества фрагментов хромосом 0,002809, для количества обменов 0,000000176, для количества одиночных фрагментов 0,00013456, для количества парных фрагментов 0,00003364, для количества хромосомных обменов 0,0000000154, для количества хроматидных обменов 0,00000000577.
Определение общего потенциала стабильности хромосом (ХBi ОПСХ) по формуле
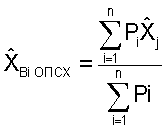
позволило оценивать в целом стабильность генетической информации у обследуемого. Общий потенциал стабильности хромосом составил 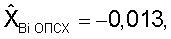 что указывало на нестабильность хромосом больного.
что указывало на нестабильность хромосом больного.
Обследуемому была рекомендована диета, богатая витаминами, морепродуктами и поливитаминными препаратами в течение полугода.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ АДАПТИВНЫХ ВОЗМОЖНОСТЕЙ ГЕНОМА ЧЕЛОВЕКА | 2009 |
|
RU2391662C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ УРОВНЯ ЛОМКОСТИ ХРОМОСОМ ЧЕЛОВЕКА | 2009 |
|
RU2395809C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ УСТОЙЧИВОСТИ ГЕНОМА | 2009 |
|
RU2405152C1 |
| СПОСОБ СТАБИЛИЗАЦИИ ЭНДОТЕЛИАЛЬНОЙ ВЫСТИЛКИ СОСУДОВ У БОЛЬНЫХ МЕТАБОЛИЧЕСКИМ СИНДРОМОМ | 2006 |
|
RU2329805C2 |
| СПОСОБ НОРМАЛИЗАЦИИ БИОЛОГИЧЕСКОГО ВОЗРАСТА У ЛИЦ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ | 2006 |
|
RU2332207C2 |
| СПОСОБ ОЦЕНКИ АКТИВНОСТИ ЯДРЫШКООБРАЗУЮЩИХ РАЙОНОВ ХРОМОСОМ В КЛЕТКАХ | 2007 |
|
RU2343483C1 |
| СПОСОБ УПРОЩЕННОЙ ОЦЕНКИ АКТИВНОСТИ ЯДРЫШКООБРАЗУЮЩИХ РАЙОНОВ ХРОМОСОМ | 2009 |
|
RU2390021C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ЭНДОТЕЛИАЛЬНОЙ ВЫСТИЛКИ СОСУДОВ У ЛИЦ С АРТЕРИАЛЬНОЙ ГЕПЕРТОНИЕЙ ПРИ МЕТАБОЛИЧЕСКОМ СИНДРОМЕ | 2007 |
|
RU2337679C1 |
| СПОСОБ КОРРЕКЦИИ ВЫСОКОЙ ЭНДОТЕЛИОЦИТЕМИИ У ЛИЦ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ | 2007 |
|
RU2338527C1 |
| СПОСОБ ПРОФЕССИОНАЛЬНОГО ОТБОРА ЛИЦ ДЛЯ РАБОТ ПО УНИЧТОЖЕНИЮ БОЕВЫХ ОТРАВЛЯЮЩИХ ВЕЩЕСТВ | 2016 |
|
RU2642603C2 |
Изобретение относится к медицине и биологии в области генетики и касается способа определения генетической стабильности хромосом человека. Сущность заявляемого способа заключается в том, что для исследования генетической стабильности хромосом у людей из локтевой вены берут кровь для культивирования лимфоцитов и приготовления препаратов метафазных хромосом с последующим анализом хромосомных препаратов для изучения уровня хромосомных аберраций с последующей обработкой полученных данных системным многофакторным анализом. Технический результат изобретения заключается в повышении точности определения уровня генетической стабильности хромосом человека.
Способ определения генетической стабильности хромосом человека, отличающийся тем, что после взятия крови, культивирования лимфоцитов, приготовления препаратов метафазных хромосом, окраски хромосомных препаратов с помощью красителя Романовского-Гимзы и проведения анализа хромосомных препаратов при наблюдении 200 метафазных пластинок у каждого обследуемого на предмет уровня хромосомных аберраций по показателям - количество клеток с хромосомными аберрациями, количество хромосомных аберраций (на 100 кл.), общее количество фрагментов хромосом, количество обменов, количество одиночных фрагментов, количество парных фрагментов, количество хромосомных обменов, количество хроматидных обменов с вычислением средних арифметических значений всех оцениваемых показателей и обработкой результатов исследования с помощью системного многофакторного анализа, переводя каждый из определяемых показателей в сопоставимые относительные величины, на основании которых с учетом весового коэффициента, определяемого для каждого показателя на основании среднеквадратического отклонения для данного показателя и постоянного множителя, равного 0,1, рассчитывают значение общего потенциала стабильности хромосом - ХBi ОПСХ по формуле
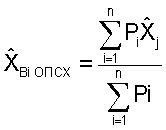
где Pi - весовой коэффициент отдельного оцениваемого показателя, 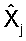 - относительная разность между исследуемым и нормативным параметрами отдельного оцениваемого признака, по значению которого определяют уровень сохранности хромосом у обследуемого: при значении
- относительная разность между исследуемым и нормативным параметрами отдельного оцениваемого признака, по значению которого определяют уровень сохранности хромосом у обследуемого: при значении 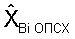 от 0,012 до 0,030 уровень стабильности хромосом можно оценить как высокий; при значении
от 0,012 до 0,030 уровень стабильности хромосом можно оценить как высокий; при значении 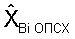 от 0 до 0,011 стабильность хромосом снижена; при уровне
от 0 до 0,011 стабильность хромосом снижена; при уровне 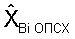 ниже 0 регистрируется нестабильность генетического аппарата.
ниже 0 регистрируется нестабильность генетического аппарата.
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ПОВРЕЖДЕНИЯ КЛЕТОК ОРГАНИЗМА | 1997 |
|
RU2156460C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕСТАБИЛЬНОСТИ ГЕНОМА У ДЕТЕЙ С ДЕТСКИМ ЦЕРЕБРАЛЬНЫМ ПАРАЛИЧОМ | 2005 |
|
RU2295130C1 |
| СПОСОБ ЭКСПРЕСС-ВЫЯВЛЕНИЯ ОБЛУЧЕННЫХ ПАЦИЕНТОВ С ПОВЫШЕННЫМИ ЧАСТОТАМИ ХРОМОСОМНЫХ АБЕРРАЦИЙ | 1997 |
|
RU2141658C1 |
| Способ определения функционального состояния кроветворения у экспериментальных животных | 1986 |
|
SU1697747A1 |
| БАК З., АЛЕКСАНДЕР П., Основы радиобиологии, М., Из-во иностранной литературы, 1963, стр.231-252. | |||
Авторы
Даты
2009-01-10—Публикация
2007-04-27—Подача