ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Область техники, к которой относится изобретение
Настоящее изобретение относится к действующим в качестве спермицидных средств и/или противогрибковых средств гексагидроинденопиридиновым соединениям, содержащим их спермицидным или противогрибковым композициям и способам нейтрализации подвижных сперматозоидов или грибков с применением соединений и композиций по настоящему изобретению.
Предпосылки изобретения
В США и большинстве стран Запада высокий и растущий спрос на противозачаточные средства является следствием определенного образа жизни, тогда как во многих развивающихся странах регулирование рождаемости является чрезвычайно важной задачей здравоохранения. Поскольку контрацепция является всеобщей потребностью охраны здоровья, хотя и по различным причинам в разных частях света, общий объем рынка противозачаточных средств для мужчин мог бы быть более значительным, чем представленный только в показателях по США.
На Западе рынок противозачаточных средств подвергся сравнительно небольшим изменениям за последние 50 лет с тех пор, как в 1951 была разработана «противозачаточная таблетка», которая остается единственным средством контрацепции, выбранным населением. Достижения в поисках средств для контрацепции обеспечили всего лишь несколько способов, все для женщин, которые, как исторически сложилось, несут основную ответственность, затраты и риск для здоровья (в особенности, риск развития сердечно-сосудистого заболевания и определенных типов рака, связанных с длительным применением гормональных противозачаточных средств) контрацепции. Презерватив, изобретенный в 16-ом веке, представляет собой единственно значимую форму контрацепции, доступную для мужчин (помимо прерванного полового акта и вазэктомии [иссечения семявыносящего протока]). Единственным действительно инновационным усовершенствованием, произошедшим с презервативом, явилось изобретение вулканизации резины в 19-ом веке. (Из New Scientist, 20 April 1994, Vol 142 No 1923.)
Вследствие разработки фармацевтическими компаниями соединений для лечения половой дисфункции (например, Виагра для лечения эректильной дисфункции) ожидается рост спроса на противозачаточные средства. Продажи презервативов в США за 1999 год выросли на 5,8%, принеся 260 миллионов долларов дохода, отражая тем самым то, что некоторые назвали бы новой американской сексуальной революцией. (Drug Store News, Nov 29, 1999, v.21, i.19, p.29.) Хотя большинство женщин детородного возраста уже применяют контрацептивы, (В мире 58% всех замужних женщин детородного возраста используют какой-либо способ контрацепции The Population Division of the United Nations Department of Economic and Social Affairs 2000), до сих пор половина всех беременностей является нежелательной. (NICHD, Contraception and Reproductive Health Branch: Report to the NACHHD Council September 1999.) Людей, ведущих здоровый образ жизни, и потребителей интересует создание дополнительных альтернативных способов, особенно способов, которые позволяют мужчинам взять на себя большую часть ответственности за контрацепцию. Всеобщий интерес побудил организации, такие как Всемирная организация здравоохранения и Family Health International, инициировать запуск проектов, направленных на поддержку разработки противозачаточных средств для мужчин. По крайней мере, две компании, Schering и Organon, за последние десять лет активно продвигают гормональные противозачаточные средства для мужчин на рынок.
В течение многих лет ведутся поиски безопасных и эффективных пероральных противозачаточных средств для мужчин. Однако было показано, что разработка лекарственного средства, которое может безопасно прерывать сперматогенез, не влияя на половое влечение, и, следовательно, использоваться в качестве противозачаточного средства для мужчин, является непростой задачей.
Идеальным противозачаточным средством для мужчин могло бы являться средство, способное эффективно подавлять продукцию сперматозоидов, блокировать их способность к оплодотворению без нарушения полового влечения или не влияя на вторичные половые признаки и их функции, и/или нейтрализовывать подвижные сперматозоиды. Кроме того, должна существовать большая разница между эффективной и токсичной дозами препарата, а способ контрацепции должен быть обратимым. В настоящее время нет такого совершенного противозачаточного средства для мужчин.
Некоторые неспецифические клеточные токсины, такие как противоопухолевые средства и алкилирующие агенты, влияют на сперматогенез, но, безусловно, неприемлемы в качестве противозачаточных средств. Соединения, препятствующие энергетическим процессам в клетке, такие как тиосахара, также влияют на сперматогенез, но в недостаточной степени селективны. Андрогены, такие как тестостерон и его аналоги, при введении в больших дозах влияют на сперматогенез, по-видимому, посредством механизма вовлечения гипоталамо-гипофизарной системы. Такие стероидные соединения успешно применялись в клинических испытаниях. Однако анаболические свойства этих стероидов могут давать риск возникновения нежелательных побочных эффектов.
В качестве соединений, эффективно блокирующих сперматогенез, активно изучали аналоги гонадотропин-релизинг фактора (GNRH). Однако аналоги GNRH влияют на эндогенную продукцию тестостерона и потому снижают половое влечение в отсутствие введения дополнительных андрогенов.
Один из подходов к созданию противозачаточных средств для мужчин основан на идентификации и использовании биохимических особенностей репродуктивного процесса мужчин. Яичко состоит из трех функциональных отделов. Первый, ответственный за производство сперматозоидов, состоит из семенных канальцев, которые содержат развивающиеся зародышевые клетки. Второй представляет собой расположенные внутри семенных канальцев клетки Сертоли, которые участвуют в организационной и функциональной координации процесса сперматогенеза и, возможно, выполняют паракринную и аутокринную роль. Благодаря комплексному организационному взаимодействию клеток Сертоли и развивающихся зародышевых клеток и наличию плотных контактов между соседними клетками Сертоли образуется гемато-тестикулярный барьер, разделяющий семенной каналец на участки, которые изолированы от прямого контакта с химическими и питательными веществами кровотока. В интерстициальной ткани семенные канальцы окружены клетками Лейдига, которые обладают несколькими эндокринными и паракринными функциями, среди которых наиболее описанной является продукция тестостерона.
Зародышевые клетки делятся и постепенно дифференцируются, продвигаясь по мере созревания от базальной мембраны к просвету семенного канальца. В базальном отделе находятся сперматогонии; избирательно выбранные сперматогонии митотически делятся и либо остаются клетками, продолжающими существовать в виде сперматогониев, либо дифференцируются в сперматоциты первого порядка. Сперматоциты первого порядка мигрируют через контакты между клетками Сертоли и митотически делятся с образованием сперматоцитов второго порядка. Сперматоциты второго порядка делятся с образованием сперматид. Сперматиды затем дифференцируются во взрослые сперматозоиды. Дифференцировку сперматид обычно называют сперматогенезом. Однако в контексте настоящей заявки под определением термина «сперматогенез» понимают весь процесс формирования и созревания (дифференцировки) сперматозоидов, а «антисперматогенным соединением» является соединение, которое нарушает любую часть этого процесса.
Краткий перечень функций клеток Сертоли представляет собой: (a) основа и питание сперматогенного эпителия, (b) высвобождение зрелых сперматид в просвет семенного канальца, (c) образование морфологического и физиологического гемато-тестикулярного барьера, (d) фагоцитоз разрушающихся зародышевых клеток, и (e) регуляция цикла сперматогенного эпителия.
Клетки Лейдига также содействуют сперматогенезу. Лютеинизирующий гормон (LH) гипофиза стимулирует продукцию тестостерона клетками Лейдига. Тестостерон и его метаболит, дигидротестостерон, необходимы для поддержания нормального сперматогенеза. Рецепторы тестостерона присутствуют на различных типах зародышевых клеток. Тестостерон доставляется через гематотестикулярный барьер, по-видимому, посредством транспорта в клетки Сертоли, где он превращается в процессе обмена веществ в эстардиол, дигидротестостерон или остается неизмененным.
Некоторые, если не все, типы зародышевых клеток, взаимодействуют с клетками Лейдига и/или Сертоли. Эти взаимодействия осуществляются посредством химических мессенджеров, которые продуцируются клетками Сертоли, клетками Лейдига и зародышевой клеткой (клетками). Например, пахитенный сперматоцит модулирует секрецию белкового фактора клеток Сертоли, который, в свою очередь, стимулирует биосинтез стероидных гормонов клетками Лейдига. Связывание сперматид происходит только с клетками Сертоли, которые становятся компетентными или функциональными после контакта с FSH. У крыс клетки Сертоли циклически секретируют несколько белков с максимальной продукцией на конкретной стадии развития сперматогенного эпителия, то есть при взаимодействии с конкретной группой зародышевых клеток. Кластерин максимально продуцируется клетками Сертоли, когда сперматогенный эпителий находится на VII или VIII стадии развития, то есть независимо от стимуляции FSH, что наводит на мысль о местной регуляции секреторной функции клеток Сертоли зародышевыми клетками.
Показано, что гексагидроинденопиридиновое соединение №20-438, разработанное Sandoz, Ltd. (соединение 1 на фиг.1), обратимо ингибирует сперматогенез при пероральном введении животным. См. Arch. Toxicol. Suppl., 1984, 7:171-173; Arch. Toxicol. Suppl., 1978, 1:323-326; и Mutation Research, 1979, 66:113-127.
Синтез различных инденопиридиновых соединений в виде рацемических смесей известен и описан, например, в патентах США №№2470108, 2470109, 2546652, 3627773, 3678057, 3462443, 3408353, 3497517, 3574686, 3678058 и 3991060. Указанные инденопиридиновые соединения имеют различные применения, включая применение в качестве обладающих противовоспалительными и обезболивающими свойствами антагонистов серотонина, ингибиторов агрегации тромбоцитов, седативных препаратов и нейролептиков, а также в качестве противоязвенных, гипотензивных и анорексигенных соединений.
В патентах США №№5319084 и 5952336 описаны обладающие антисперматогенным действием гексагидроинденопиридиновые соединения, в которых в 5-м положении в качестве заместителя содержится фенольное кольцо, содержащее заместитель в пара-положении.
Несмотря на обширные исследования в этой области по-прежнему существует необходимость в эффективных противозачаточных средствах для мужчин, обладающих обратимым действием и ограниченными побочными эффектами. Сохраняющейся проблемой является введение известных соединений в дозах, которые могут вызывать побочные эффекты. Дополнительной проблемой в этой области является отсутствие подходящих контрастных агентов, обладающих специфическими участками связывания в яичках. По-прежнему существует необходимость в соединениях, которые могут применяться в качестве контрастных агентов при изучении функции яичек и для диагностики дисфункции яичек.
В дополнение к пероральным противозачаточным средствам для мужчин необходимы более эффективные композиции для использования в качестве обычно применяемых методик местной/внешней контрацепции.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Соответственно настоящее изобретение относится к пероральному противозачаточному средству для мужчин, которое не влияет на половое влечение, обладает высокой эффективностью и активностью, и обладает минимальными побочными эффектами и токсичностью.
Настоящее изобретение также относится к пероральному противозачаточному средству для мужчин, которое ингибирует сперматогенез, и к способу ингибирования сперматогенеза с применением этого средства.
Кроме того, настоящее изобретение относится к композиции, которая действует в качестве спермицида, нейтрализуя подвижные сперматозоиды, и является, таким образом, эффективной в качестве противозачаточного средства для наружного применения.
Настоящее изобретение дополнительно относится к композиции, которая действует в качестве противогрибковой композиции.
Эти и другие цели настоящего изобретения были достигнуты благодаря созданию гексагидроинденопиридиновых соединений по настоящему изобретению и обнаружения, что эти соединения являются высокоэффективными, нарушают сперматогенез и действуют в качестве спермицида на подвижные сперматозоиды и обладают эффективным противогрибковым действием.
Соединения по настоящему изобретению решают указанные выше задачи. Соединения по настоящему изобретению являются высокоэффективными в дозах, меньших по сравнению с соединением 1, и снижают случаи возникновения побочных эффектов, таких как седативные эффекты, наблюдаемые для соединения 1. Кроме того, соединения по настоящему изобретению взаимодействуют с макромолекулярным участком яичек. Применение соединений по настоящему изобретению, которые содержат метку, такую как радиоактивная метка, решает проблему несовершенных контрастных агентов, предлагая контрастный агент, применимый для изучения функции яичек и при диагностике дисфункции яичек. Также было обнаружено, что соединения по настоящему изобретению действуют в качестве спермицидного средства, чрезвычайно эффективно и действенно нейтрализуя подвижные сперматозоиды, что предполагает применение этих соединений в составе различных спермицидных композиций. Также обнаружено, что соединения по настоящему изобретению обладают противогрибковым действием.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1 представлена структура трех гексагидроинденопиридиновых соединений и указана система нумерации атомов в этих соединений.
На фигуре 2 представлен процесс получения предшественников соединений по настоящему изобретению.
На фигуре 3 представлена схема энантиоселективного синтеза предшественников соединений по настоящему изобретению.
На фигуре 4 представлена схема йодирования предшественников, полученных, как представлено на фиг.2 и 3, и схема преобразования йодированных соединений в дополнительные соединения, подпадающие под объем настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Было обнаружено, что гексагидроинденопиридиновые соединения, имеющие представленную ниже структуру I(a), и предпочтительно имеющие представленную ниже структуру I(b):
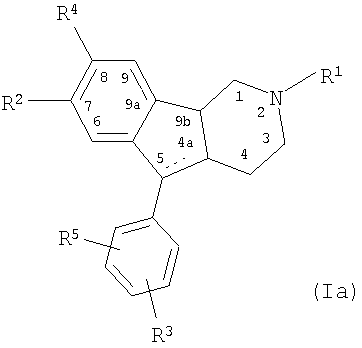
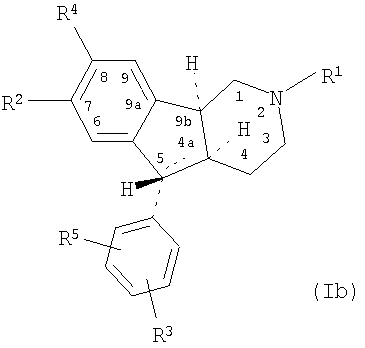
где атомы водорода в положениях 4a, 5 и 9b имеют представленную относительную стереохимию (атомы водорода в положениях 4a и 5 находятся в транс-положении относительно друг друга, и атомы водорода в положениях 4a и 9b находятся в цис-положении относительно друг друга; формула I(b)); или относительная стереохимия в положении 9b может быть обращена таким образом, что атомы водорода в положениях 4a и 5 находятся в транс-положении относительно друг друга, и атомы водорода в положениях 4a и 9b находятся в транс-положении относительно друг друга; или все три атома водорода могут находиться в цис-положении относительно друг друга; или
где пунктирная линия между 4a и 5 показывает, что соединение может также являться 4a,5-дегидросоединением, образуя, таким образом, двойную связь между атомами углерода в положениях 4a и 5, и где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью, предпочтительно C1-3-алкил или C3-C8-циклоалкил; R2 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью, предпочтительно C1-3-алкил, R3 и R5 независимо представляют собой атом водорода, атом галогена, SO3H, С1-6-алкил с неразветвленной или разветвленной цепью, CH2OH, CH2OMe, С1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (COOH) или группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, эфир карбоновой кислоты (COOR, где R представляет собой С1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена; и R4 представляет собой атом водорода, атом галогена, R3Si или COR,
являются не только антисперматогенными и при пероральном применении обладают приблизительно в 40 раз большей антисперматогенной активностью, чем описанные ранее в патенте США №5319084 соединения, но также действуют в качестве нейтрализующего подвижные сперматозоиды спермицида, а также действуют в качестве противогрибкового средства.
Представленный в контексте настоящего изобретения термин «антисперматогенный» относится к способности нарушать продукцию сперматозоидов в яичках, в то время как термин «спермицид» или «спермицидный» относится к способности нейтрализовывать подвижные сперматозоиды после их продукции и более предпочтительно после эякуляции.
Соединения по настоящему изобретению имеют относительную стереохимию, представленную на структуре (I). Настоящее изобретение включает обе энантиомерные формы (по существу оптически чистые), а также любые смеси этих форм, например, рацемическую смесь.
Фармацевтически приемлемые соли соединений, имеющих представленную выше структуру (I), также включены в настоящее изобретение. Фармацевтически приемлемые соли включают без ограничения соли взаимодействия основной функциональной группы (такой как без ограничения аминогруппа) с неорганическими кислотами, такие как гидрохлорид, гидройодид, сульфат, фосфат, дифосфат, гидробромид или нитрат, или соли взаимодействия основной функциональной группы с органическими кислотами, такие как ацетат, малат, малеат, фумарат, тартрат, сукцинат, цитрат, лактат, метансульфонат, пара-толуолсульфонат, пальмоат, салицилат и стеарат; или соли взаимодействия кислотной функциональной группы с ионами металлов, таких как без ограничения Na, K, Ca, или соли взаимодействия кислотной функциональной группы с ионом аммония, или соли взаимодействия кислотной функциональной группы с органическими ионами, такими как без ограничения амины и тетразамещенные ионы аммония.
Заместитель R1 предпочтительно представляет собой алкильную группу с неразветвленной цепью (н-алкильную группу), изоалкильную или циклоалкильную группы, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гексил, изогексил, циклопропил, циклопентил, циклогексил. Наиболее предпочтительно R1 представляет собой этил.
Заместитель R2 также предпочтительно представляет собой алкильную группу с неразветвленной цепью или изоалкильную группу, как описано выше для заместителя R1.
Заместитель R3 предпочтительно находится в пара-положении или в 4-м положении кольца и предпочтительно представляет собой группу, выбираемую из гидроксиметила (CH2OH), формила (CHO), карбоксила (COOH), эфира карбоновой кислоты (COOR, где R представляет собой С1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметилового эфира (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атома галогена.
Заместитель R4 предпочтительно представляет собой атом галогена, включая I, Br, Cl и F. Высокая активность этих соединений является неожиданной. Атом галогена может являться радиоактивным изотопом, например 123I, 125I или 131I. В представленных выше соединениях вместо обычных (нерадиоактивных) изотопов могут использоваться другие радиоактивные изотопы, такие как, например, 11C, тритий (3H) или 18F или радиоактивные изотопы брома и хлора.
Соединение 1 представляет собой рацемическую смесь. Структура соединения 1 представлена на фиг.1. Гексагидроинденопиридины имеют три центра асимметрии, которые могут быть определены по известной номенклатуре. Альтернативно относительная стереохимия может быть определена по цис-транс расположению атомов водорода, связанных с углеродной системой в положениях 4a, 5 и 9b трициклической кольцевой системы, что приводит к стереохимическим перераспределениям. По номенклатуре Кана-Ингольда-Прелога стереохимическими характеристиками и наименованием соединения 1 является (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-7-метил-5-(4-метилфенил)-1H-индено[1,2-c]пиридин.
В соединении 1 5-фенильная группа содержит гидрофобный метильный заместитель, соответствующий заместителю R3 в представленной выше структуре (I). Антисперматогенная активность соединения 1 присуща по существу исключительно (+)-изомеру (правовращающему, как измерено в условиях, описанных в Cook et al., 1995), который является эффективным антисперматогенным лекарством у мышей. Антисперматогенная активность других соединений этого ряда также присуща по существу исключительно одному оптическому изомеру. Как известно специалисту в области стереохимии, измеренное оптическое вращение может быть или (+) или (-) в зависимости от схемы замещения и условий измерения. С другой стороны, противогрибковые свойства соединений по настоящему изобретению не являются стереоспецифичными и являются и (+) и (-) активными изомерами, хотя их относительная активность может различаться.
Спермицидная активность соединений по настоящему изобретению была обнаружена у изомеров, обладающих антисперматогенной активностью, и предполагается ее наличие и в других изомерах.
Сильнополярная карбоксильная группа или группы, которые могут быть преобразованы в карбоксильную группу в процессе обмена веществ в физиологических условиях организма млекопитающих, могут находиться в любом положении, предпочтительно в пара-положении, 5-фенильного кольца соединений по настоящему изобретению без потери спермицидной и/или противогрибковой активности. Например, соединения, которые в пара-положении замещены гидроксиметильной (CH2OH), формильной (CHO), карбоксильной (COOH) и метоксикарбонильной (C(O)OCH3) группами, сохраняют высокую активность. Указанные соединения являются активными несмотря на присутствие полярного заместителя в пара-положении 5-фенильного кольца.
Под «преобразованием в процессе обмена веществ в физиологических условиях организма млекопитающих» подразумевают преобразование функциональной группы R3 в карбоксильную группу при введении соединения структуры (I) живому млекопитающему, которому требуется антисперматогенное воздействие. Введение может осуществляться при помощи любых традиционных средств и по любому пути, включая без ограничения пероральный, внутрибрюшинный, внутривенный, подкожный, внутримышечный, ингаляционный, трансбуккальный и чрескожный. Указанные пути введения пригодны для спермицидного и/или противогрибкового воздействия, равно как и для местного введения. Преобразование группы R3 в карбоксильную группу легко определяется путем осуществления контроля содержания метаболитов соединения структуры (I) в крови или в моче. Контроль содержания метаболитов может осуществляться с применением традиционных методов анализа, таких как масс-спектрометрия (MS), газовая хроматография (GC), и так далее.
При введении млекопитающему предпочтительно, по крайней мере, 50%, более предпочтительно, по крайней мере, 80% и, еще более предпочтительно 90%, 95% или 100% функциональных групп R3 преобразуются в процессе обмена веществ в карбоксильные группы, хотя это не является необходимым условием приобретения спермицидных и/или противогрибковых свойств. Процентная доля преобразования может быть определена при помощи одного из указанных выше традиционных методов анализа путем количественного определения в образце крови или мочи отношения содержания соединений, не подвергшихся преобразованию и содержащих функциональную группу R3, к содержанию соединений, в которых эта функциональная группа была преобразована в карбоксильную группу.
Антисперматогенная активность соединения 1 наблюдалась после его однократного перорального введения крысам в дозе 30 мг/кг, резко снижая массу яичек в течение 24 ч. Наблюдались дегенеративные изменения в семенных канальцах. Сперматиды становились пикнотичными, изредка образуя многоядерные слияния. Клетки Сертоли цитологически выглядели нормальными. Судя по всему, соединение 1 целенаправленно действует на сперматиды или на связанные с этими сперматидами клетки Сертоли, так как гистологические изменения наблюдались в первую очередь в этих сперматидах.
Соединение 1 вызывает некоторую заторможенность и седативный эффект у мышей при пероральной дозировке 30 мг/кг и очень сильную заторможенность в той же дозе, введенной подкожно. Заторможенность и седативный эффект, безусловно, являются нежелательными побочными эффектами противозачаточных средств. В отличие от наблюдаемой для соединения 1 заторможенности и седативного эффекта соединения по настоящему изобретению вызывают минимальную заторможенность.
Соединения по настоящему изобретению позволяют отделить противозачаточное действие от седативного действия, наблюдаемого для соединения 1. Поэтому соединения по настоящему изобретению являются эффективными противозачаточными лекарственными средствами, для которых нежелательные побочные эффекты в виде седативного эффекта и заторможенности заметно снижены.
Действие соединений по настоящему изобретению на сперматогенез было протестировано на мышах через трое суток после перорального однократного введения по приведенной ниже методике, описанной Cook et al (1995). Было показано, что соединения, проявившие активность в этом тесте, также являются противозачаточными средствами.
Антисперматогенная активность соединений проверялась путем принудительного введения самцам мышей на 1-е сутки выступающего в качестве контроля растворителя, соединения 1 (положительный контроль) или соединения по настоящему изобретению. Через 72 ч после введения животных убивали, оперативно удаляли яички, очищали их от жира и взвешивали. Одно яичко исследовали гистологически и определяли сперматогенный потенциал с применением «сперматогенного индекса» (J.M.Whitsett, P.F.Noden, J.Cherry and A.D.Lawton, J.Reprod. Fertil., 72, 277 (1984)), который представляет собой полуколичественную оценку способности яичек продуцировать сперматозоиды. Индекс основан на гистологическом выявлении сперматогенных клеток в семенных канальцах. Применяется шкала от 1 до 6, при этом нормальное значение составляет 5-6. Вторая оценка основывалась на массе яичек.
В таблицах 1 и 2 представлены соответствующие биологические результаты, отражающие изменение массы яичек (TW) и сперматогенного индекса (SI) относительно контроля, содержащего только вводимый растворитель без инденопиридина. В таблицах 1 и 2 значения заместителей R3 и R4 относятся к структуре Ib, где R3 находится в пара-положении; R1 представляет собой этил; R2 представляет собой метил; и R5 представляет собой атом водорода.
При наличии 8-йод-7-метил-4'-карбокси-заместителя или 4'-карбометокси-заместителя вводимая перорально доза 2 мкмоль/кг (1 мг/кг) рацемата приводила к снижению сперматогенного индекса на 57-67% и была, по крайней мере, также эффективна, как и доза 79 мкмоль/кг (30 мг/кг) соответствующего аналога без 8-йод-заместителя. В случае 8-бром-аналога или 8-хлор-аналога наименьшая протестированная доза (6 или 2 мкмоль/кг; 3 или 1 мг/кг) была, по крайней мере, также эффективна, как и доза 79 мкмоль/кг (30 мг/кг) негалогенированного аналога (см. таблицу 1). Сравнение активного левовращающего энантиомера 8-йод-7-метил-4'-карбометокси-аналога с активным энантиомером 8-H-7-метил-4'-карбометокси-аналога (таблица 2) показало, что первое соединение в дозе 0,6 и 2 мкмоль/кг (0,3 и 1 мг/кг) обладает тем же или большим эффектом, что и последнее соединение в дозе 25 и 75 мкмоль/кг (10 и 30 мг/кг). Таким образом, путем введения атома галогена в 8-е положение достигается приблизительно 40-кратное увеличение молярной эффективности.
Антисперматогенный эффект рацемической смеси инденопиридиновых соединений на взрослых самцах мышей линии SWISSa
Для неактивных соединений представлена только наибольшая доза.
Мышам принудительно вводили инденопиридин или растворитель в дозе 10 мл/кг.
Растворитель содержал 90% воды, 7% Tween 20 и 3% этанола.
Некропсию проводили на 3-и сутки, спустя приблизительно 72 ч после введения дозы.
bМасса яичек [% изменения относительно значения контроля с введением растворителя, равного 217,8±46,0 (S.E.) мг]
cСперматогенный индекс [% изменения относительно значения контроля с введением растворителя, равного 5,8±0,2 (S.E.)]
*Значимое различие относительно значения контроля с введением растворителя; односторонний критерий по Dunnett, p<0,05.
Статистический анализ проводили на необработанных данных перед пересчетом в % изменения.
Эффект введения атома йода в 8-е положение на сперматогенный эффект хиральных инденопиридиновых соединений на взрослых самцах мышей линии SWISSa (соединение 1 представляет собой рацемическую смесь; соединения 3 и 18 представляют собой левовращающие изомеры)
Мышам принудительно вводили инденопиридин или растворитель в дозе 10 мл/кг.
Некропсию проводили на 3-и сутки, спустя приблизительно 72 ч после введения дозы.
Растворитель представлял собой 1% Tween 20 в воде.
bМасса яичек [% изменения относительно значения контроля с введением растворителя, равного 227,5±8,6 мг]
cСперматогенный индекс [% изменения относительно значения контроля с введением растворителя, равного 5,7±0,2]
dn=6.
en=4.
*Значимое различие относительно значения контроля с введением растворителя; односторонний критерий по Dunnett, p<0,05.
Статистический анализ проводили на необработанных данных перед пересчетом в % изменения.
Спермицидная активность соединений по настоящему изобретению представлена в значительной степени только при однократном добавлении композиции к эякуляту, причем добавление композиции, содержащей лишь 3 мкМ соединения по настоящему изобретению, приводило к значительному подавлению подвижности сперматозоидов, а после добавления композиции, содержащей лишь 100 мкМ соединения по настоящему изобретению, подвижность сперматозоидов снижалась до нуля. Спермицидная композиция по настоящему изобретению может содержать соединение по настоящему изобретению в любой концентрации, достаточной для снижения подвижности сперматозоидов до уровня, не способного вызвать беременность, предпочтительно в концентрации 1-500 мкМ, более предпочтительно 3-300 мкМ, наиболее предпочтительно 10-200 мкМ. Спермицидную активность определяли по способу, описанному ниже.
Способ определения прямого эффекта агента на подвижность сперматозоидов
Прямой эффект агента на подвижность сперматозоидов определяли, используя следующие протоколы. В основном сперматозоиды получали либо из хвоста придатка яичка крыс, либо из эякулята кроликов, собранного при помощи искусственной вагины. Начальную подвижность сперматозоидов определяли вручную или при помощи анализатора спермы Hamilton Thorn IVOS. Затем сперматозоиды выдерживали при постоянной температуре 34°C, разбавляли до концентрации 10×106/мл и добавляли приблизительно к 3 мл буферного раствора или среды. На этом этапе снова определяли подвижность и регистрировали любое изменение. Затем к препарату сперматозоидов добавляли различные концентрации тестируемого агента. Затем образцы сперматозоидов выдерживали при той же температуре в течение часа и определяли подвижность. Результаты записывали как процент содержания подвижных сперматозоидов в образце.
Протокол определения прямого эффекта агента на подвижность сперматозоидов
Общая информация:
В ходе проведения эксперимента сперматозоиды выдерживали при 34°C. Концентрация сперматозоидов приблизительно составляла 10×106/мл (для достижения данной концентрации, возможно, потребует разбавления препарата буферным раствором или средой).
Для исследования на крысах (применяя сперматозоиды из хвоста придатка яичка):
Получали 1 мМ основной раствор инденопиридина в сбалансированном солевом растворе Хенкса (HBSS-буфер), содержащий бычий сывороточный альбумин (BSA; 5 мг в 10 мл=0,5 мкг/мкл; 0,5 мкг/мл=1 мкМ) и добавляли следующим образом:
1 мкМ=1 мкл основного раствора+949 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
3 мкМ=3 мкл основного раствора+947 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
10 мкМ=10 мкл основного раствора+940 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
30 мкМ=30 мкл основного раствора+920 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
100 мкМ=100 мкл основного раствора+850 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
300 мкМ=300 мкл основного раствора+650 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
1000 мкМ=1000 мкл основного раствора+50 мкл разбавленного раствора сперматозоидов
Подвижность сперматозоидов определяли через 1 час.
Для исследований на кроликах (применяя эякулят):
Получали 1 мМ основной раствор инденопиридина в среде М-199, содержащий бычий сывороточный альбумин (BSA; 2,5 мг в 5 мл=0,5 мкг/мкл; 0,5 мкг/мл=1 мкМ) и добавляли следующим образом:
1 мкМ=1 мкл основного раствора+949 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
3 мкМ=3 мкл основного раствора+947 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
10 мкМ=10 мкл основного раствора+940 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
30 мкМ=30 мкл основного раствора+920 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
100 мкМ=100 мкл основного раствора+850 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
300 мкМ=300 мкл основного раствора+650 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
1000 мкМ=1000 мкл основного раствора+50 мкл разбавленного раствора сперматозоидов
Подвижность сперматозоидов определяли через 1 час.
Для определения морфологических изменений получали микроскопические препараты и окрашивали эозином для определения клеточной гибели.
Результаты тестов на спермицидность представлены ниже в таблице 3 (сперматозоиды из эякулята кролика) и таблице 4 (сперматозоиды из хвоста придатка яичка крысы).
Подвижность сперматозоидов из эякулята кролика
**Сперматозоиды кажутся «разделенными на части» (головки сперматозоидов содержат много вакуолей, а мембраны не всегда интактны)
Подвижность сперматозоидов из хвоста придатка яичка крысы
Противогрибковое действие соединений по настоящему изобретению может быть достигнуто при любой концентрации, достаточной для снижения содержания грибков до уровня, недостаточного для индукции грибковой инфекции, и предпочтительно достигается при концентрациях 1-500 мкМ, более предпочтительно при концентрациях 20-300 мкМ, наиболее предпочтительно при концентрациях 20-200 мкМ.
Тестирование на чувствительность к противогрибковому воздействию проводили, следуя методическим рекомендациям NCCLS с незначительными изменениями. Кратко, суспензию клеток Candida albicans получали из чистых культур, выращенных в течение ночи при 35°C на солодовом агаре с дрожжевым экстрактом (YM-агар). Несколько небольших колоний отбирали с чашки Петри с YM-агаром и переносили в 5 мл 0,85% соляного раствора. Клетки суспендировали путем интенсивного перемешивания в течение 15 секунд и определяли на спектрофотометре плотность клеток в полученной суспензии. Плотность клеток корректировали путем добавления 0,85% соляного раствора до того момента, пока значение коэффициента пропускания, измеренного при длине волны 530 нм, не соответствовало 0,5 ед. стандарта Макфарланда. Алкивоту этой суспензии разбавляли средой RPMI-MOPS (1:1000) с получением рабочей суспензии. Сходным образом получали суспензию спор Aspergillus fumigatus с использованием спор, хранившихся при 40°C в 0,85% соляном растворе. Эти споры разбавляли 0,85% соляным раствором до соответствия коэффициента пропускания стандарту Макфарланда. Затем эту суспензию дополнительно разбавляли средой RPMI-MOPS (1:50) с получением рабочей посевной суспензии.
Проводили серии разведений тестируемых соединений в среде RPMI-MOPS, содержащей 2% ДМСО. Аликвоту каждого разведения добавляли в двух повторах в лунки стерильного 96-луночного плоскодонного микропланшета. Затем в каждую лунку добавляли либо суспензию клеток C.albicans, либо суспензию спор A.fumigatus до конечного объема, равного 200 мкл. Затем микропланшеты инкубировали при 35°C. Через 19 часов инкубации микропланшеты, засеянные C.albicans, оценивали невооруженным глазом, определяя минимальную подавляющую концентрацию (MIC), при которой не наблюдался рост грибков. Подобную оценку проводили через 48 часов на микропланшетах, засеянных A.fumigatus. Для всех разведений, при которых не наблюдался рост тестируемого грибка, определяли минимальную фунгицидную концентрацию (MFC) путем штриховой разводки 100 мкл среды из лунки-образца в чашке Петри с YM-агаром для выращивания C.albicans, или в чашке Петри с картофельным агаром с декстрозой для выращивания A.fumigatus. Подсчитывали число колониеобразующих единиц (КОЕ) и использовали эти значения для расчета процента выживших клеток или спор в посевном материале относительно числа КОЕ в рабочей посевной суспензии. Минимальные фунгицидные концентрации (MFC) представляли собой наименьшую концентрацию тестируемого соединения с процентом выживаемости, не превышающим 2%.
Результаты тестов на фунгицидность представлены ниже в таблицах 5-7.
Фунгицидная активность в отношении C.albicans
Фунгицидная активность в отношении A.Fumigatus
КОЕ = колониеобразующая единица;
Cidal = более 98% убитых клеток;
Static = лунка выглядит чистой, но убито менее 98% клеток;
*Колонии располагались слишком близко, чтобы произвести правильный подсчет. Скорее всего, в этом случае действие было близко к фунгицидному.
Следует отметить, что в лунках с соединениями 073d и 073l предположительно образуется некий вид осадка. Возможно, осадок «захватывал» споры. Для других соединений образование такого осадка не наблюдалось.
Сравнение наиболее эффективных фунгицидов
MFC = минимальная концентрация, при которой погибает более 98% клеток в лунке;
Fungistatic = соединение, для которого существует MIC, но при этом погибает менее 98% клеток;
выделенное курсивом соединение 4587-062 действовало только на A.fumigatus)
Концентрация для соединения 062: предположительно 0,1 мг в 50 мкл обеспечивает конечную концентрацию в анализируемой среде, составляющую 1/5 от той, о которой сообщалось. Тем не менее, эти концентрации являются общими оценками.
Различные соединения, протестированные в представленных выше таблицах, представлены ниже:
АНАЛОГИ ИНДЕНОПИРИДИНА
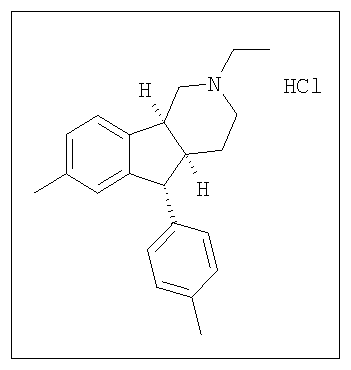
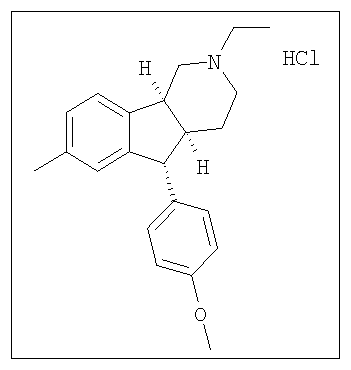


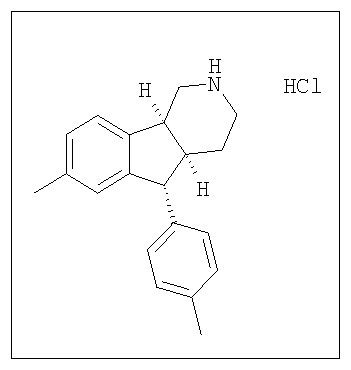

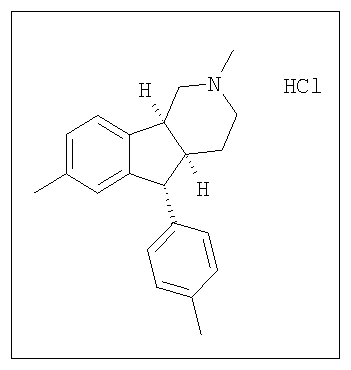


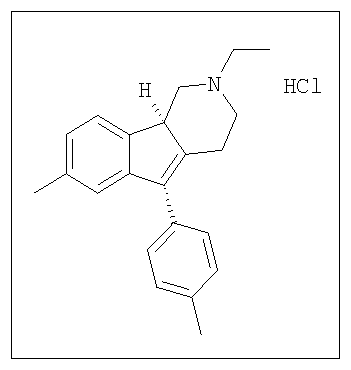

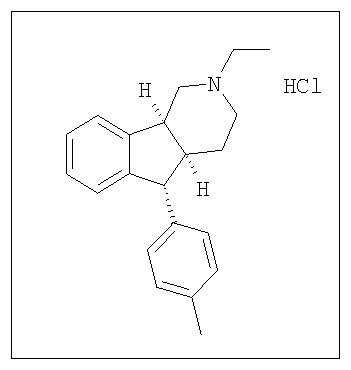

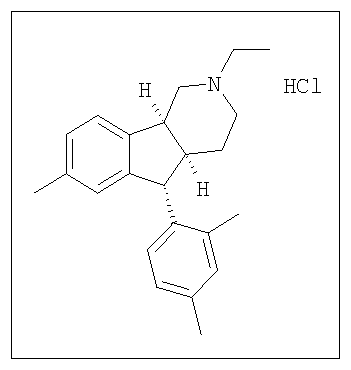
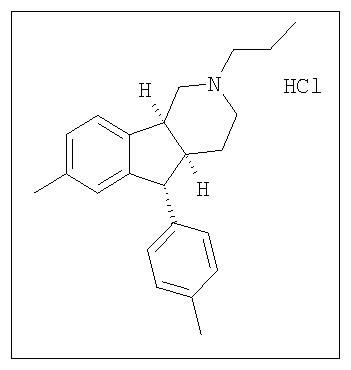
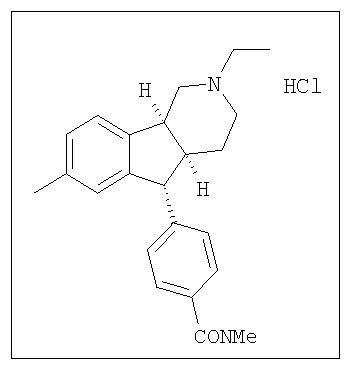
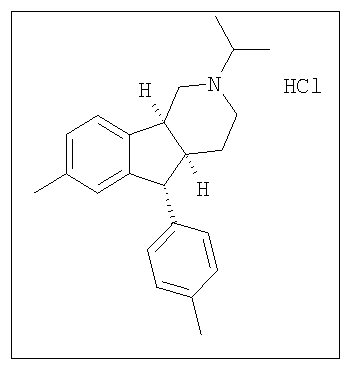

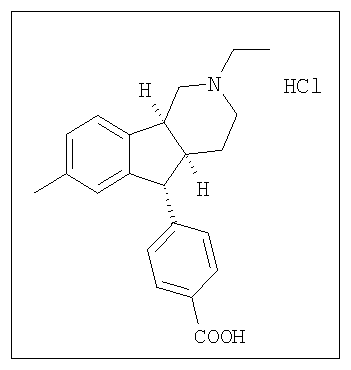
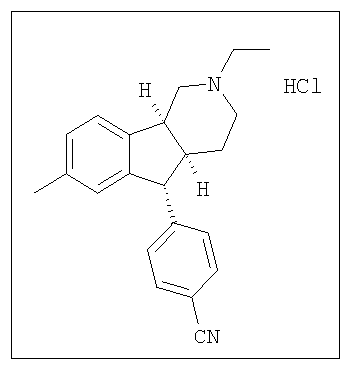
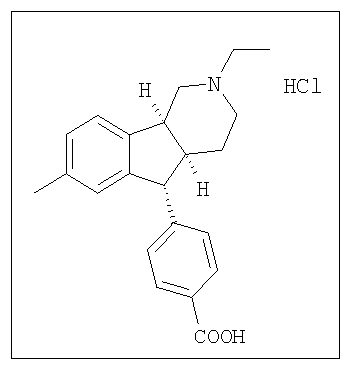
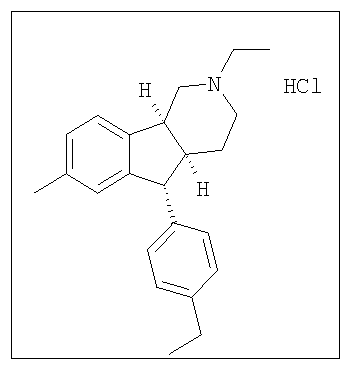
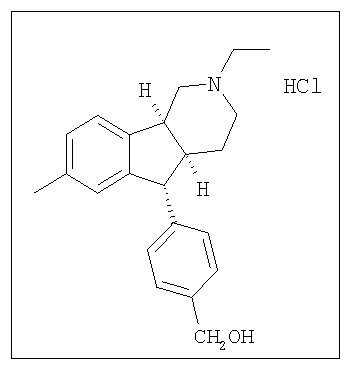
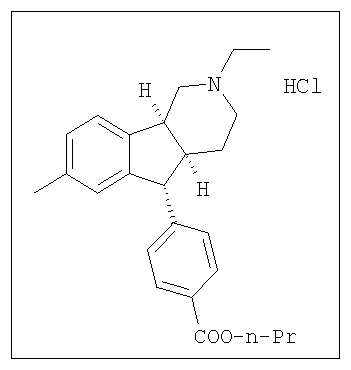
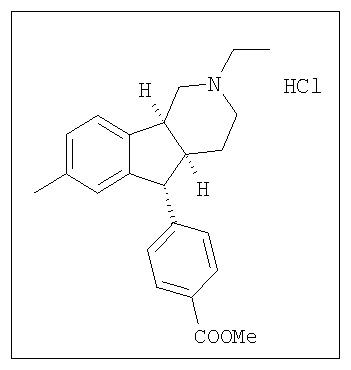
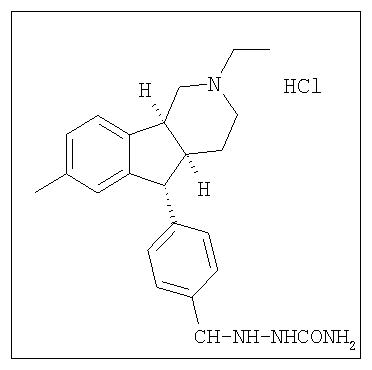
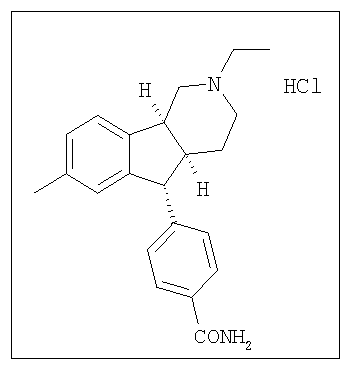


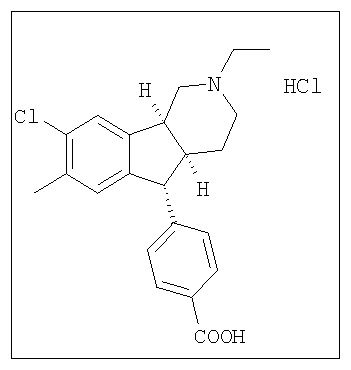
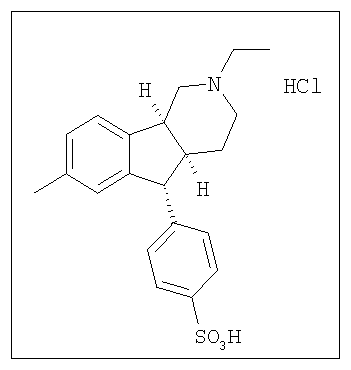
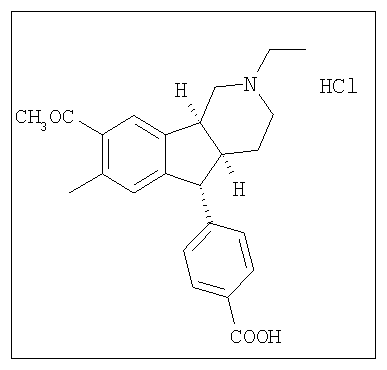
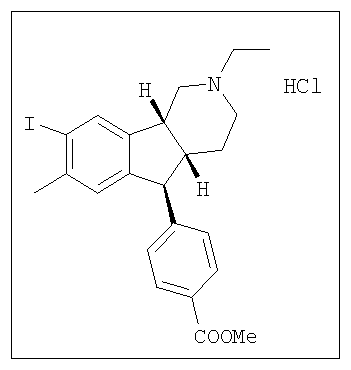
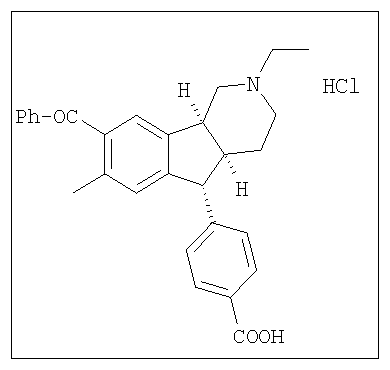
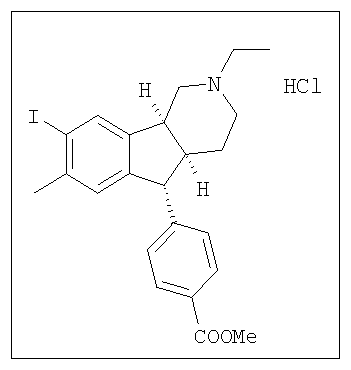
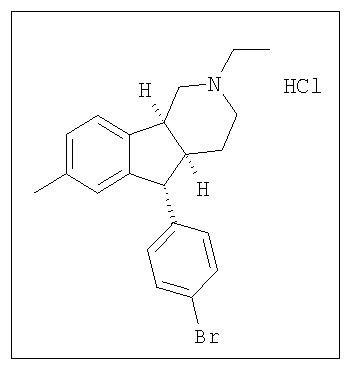
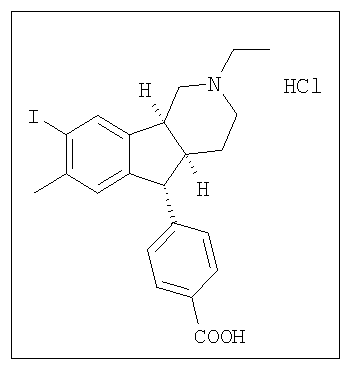
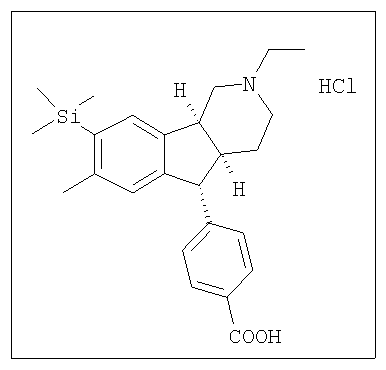
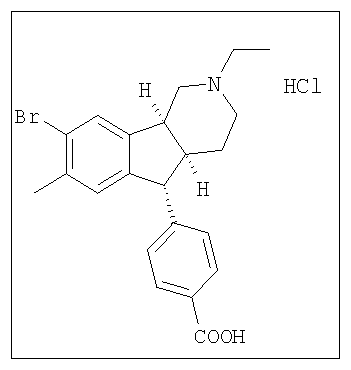
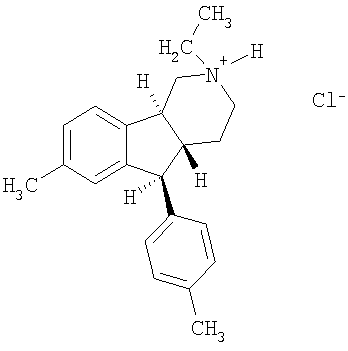

(Относительная стереохимия)
(Относительная стереохимия)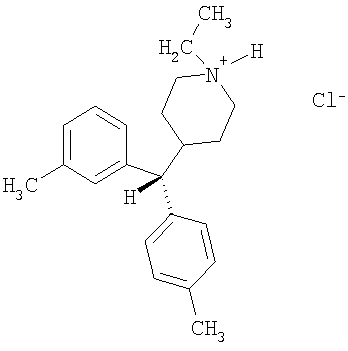

RTI-4587-006
(Относительная стереохимия)
(Относительная стереохимия)
Предшественники соединений по настоящему изобретению могут быть получены способом, описанным в патенте США №5319084, используя модификации способа, описанного в патенте США №3678057. Эти патенты включены здесь в качестве ссылки в полном объеме. Заместители R3 вводят в молекулу с использованием подходящего реактива Гриньяра или агента фениллития. Полученные по этому способу смеси энантиомеров разделяют на чистые энантиомеры путем солеобразования с последующим проведением избирательной кристаллизации или хроматографии. Например, разделение соединения 1 может быть выполнено путем солеобразования с S(+)- и R(-)-2,2'-(1,1'-бинафтил)фосфорной кислотой, а разделение соединения 3 может быть выполнено путем солеобразования с R- и S-миндальной кислотой, как описано в работе C.E.Cook et al, J. Med. Chem., 38:753 (1995). Оптическую чистоту устанавливали по методу высокоэффективной жидкостной хроматографии (ВЭЖХ) на колонке CHIRACEL-OD.
Соединения по настоящему изобретению могут быть получены, используя в качестве исходного продукта карбоновую кислоту 2 или один из ее сложных эфиров (например, соединения 3). Соединения, такие как соединения 2 и 3, получают, как описано в патенте США №5319084. Альтернативно они могут быть получены по способу, представленному на фиг.2, где сложный эфир N-замещенной 3-арилгексагидропиридин-4-карбоновой кислоты 4 гидролизуют до карбоновой кислоты 5, которую затем обрабатывают тионилхлоридом с получением хлорида 6. Обработка этого соединения AlCl3 приводит к циклизации соединения с получением трициклического кетона 7. Взаимодействие кетона 7 с пара-галоген-замещенным фенилмагнийгалогенидом или с пара-галогензамещенным фениллитием (4-бромфениллитием) приводит к образованию третичного спирта 8, который после обработки триалкилсиланом, например три-C1-6-алкилсиланом, таким как триэтилсилан и BF3, восстанавливается до соединения 9, которое затем кипятят с обратным холодильником с сильным основанием (например, с KOH) в спиртовом растворителе, предпочтительно при высокой температуре кипения, таком как н-бутанол, с получением бромфенильного соединения 10 с требуемой стереохимией. Преобразование бромфенильной группы до литиофенильной группы, например, с применением C1-6-алкиллитиевого соединения, и карбоксилирование (CO2) с применением известных реагентов приводит к образованию карбоновой кислоты 2, которая может быть этерифицирована при помощи обычных средств, хорошо известных в данной области техники, например, путем осуществления взаимодействия с C1-6-алканолом, с получением сложного эфира 3.
Приведенный выше способ синтеза может быть модифицирован для осуществления энантиоселективного синтеза активных энантиомеров соединений 2 и 3, которые затем могут применяться для синтеза активных энантиомеров по настоящему изобретению, как представлено на фиг.3. Так, N-замещенную 1,2,5,6-тетрагидропиридин-4-карбоновую кислоту (например, соединение 12) преобразуют в ее хлорангидрид, который применяют для ацилирования 1R(+)-(2,10)-камфорсультама или 1S(-)-(2,10)-камфорсультама. Для введения арильной группы в 3-е положение с большим преобладанием одного из энантиомеров полученный еноилсультам 13 обрабатывают арилмагнийгалогенидом, что приводит к 1,4-присоединению с высокой диастереомерной селективностью. После проведения кристаллизации получают чистый энантиомер 14. Амидную функциональную группу гидролизуют, а затем может быть восстановлено хиральное вспомогательное вещество. Затем карбоновую кислоту преобразуют до циклического кетона 7, как описано выше. Это соединение может быть преобразовано по существу в энантиомерно чистые соединения 2 и 3 путем обработки бромфениллитием и последующих стадий, как представлено на фиг.2. Альтернативно хиральный кетон 7 может быть преобразован в энантиомерно обогащенные соединения 2 и 3 по методике, описанной для синтеза рацематов в патенте США №5319084. Степень обогащения зависит от катализатора и температуры при восстановлении энантиомерного тетрагидроинденопиридина, аналогичного промежуточному продукту 5. См. фиг.3 патента США №5319084. Так, при 23°C с использованием PdCl2/NaBH4/H2(3 атм) преобладание одного из энантиомеров составляло 73% с полной рацемизацией при 55°C, в то время как при 60°C с использованием Pt/С/H2 преобладание одного из энантиомеров было сравнимо с таковым при 23°C (67% и 70%, соответственно).
Либо карбоновая кислота 2, либо ее сложные эфиры, такие как сложный метиловый эфир 3, могут быть йодированы с получением 8-йодзамещенных аналогов 17 или 18 путем осуществления взаимодействия с йодом в окислительных условиях или с окисленной формой йода (фиг.4). Например, осуществление взаимодействия соединения 3 приблизительно с 1 моль йода в присутствии оксида ртути приводит к высокому выходу 8-йодзамещенного соединения 18. Сложный эфир и кислота взаимно превращаются друг в друга по стандартным химическим методикам, известным в данной области техники. Могут применяться либо рацематы, либо энантиомеры. Для получения меченого аналога соединения 17 или 18 также может применяться радиоактивный изотоп йода, такой как 125I, 123I или 131I. Такие соединения применимы для определения местонахождения и места действия этих соединений и могут применяться в качестве радиоактивного препарата для диагностики у мужчин нарушений репродуктивной системы.
Йодзамещенные соединения, в особенности 8-йодзамещенная кислота 17, могут быть преобразованы в бромзамещенные или хлорзамещенные соединения путем образования кислотой соли металла, например натриевой соли, а затем путем образования 8-металлзамещенного промежуточного продукта, где металл представляет собой металл, такой как литий, или замещенный известными реагентами металл, такой как трет-бутиллитий. Осуществление взаимодействия 8-металлзамещенного промежуточного продукта с источником галогена, таким как гексахлорэтан или 1,2-дибромэтилен, приводит к образованию соответствующих 8-замещенных аналогов, таких как соединения 19 или 20, представленные на фиг.4. Соответствующие фторзамещенные соединения могут быть получены путем осуществления взаимодействия 8-металлзамещенного промежуточного продукта с хлортриметилсиланом с получением соответствующего 8-триметилсилильного соединения, которое затем вступает во взаимодействие с тетраэтилсвинцом в присутствии BF3-Et2O (см. De Mio et al., 1993, Tetrahedron, 49:8129-8138).
Радиоактивные аналоги различных соединений по настоящему изобретению могут быть получены, например, путем обработки 8-металлзамещенного промежуточного продукта реагентом, содержащим электрофильный атом галогена в виде его радиоактивного изотопа или, как указано ранее, радиоактивные аналоги соединений 17 или 18 могут быть получены путем замещения радиоактивного изотопа йода в описанном выше синтезе этих соединений. Меченное тритием соединение по настоящему изобретению может быть получено, например, путем восстановления 8-йодзамещенных соединений газообразным тритием, катализируемого благородным металлом, таким как палладий или платина. Меченные 14C аналоги могут быть получены, например, путем использования меченного 14C углекислого газа на стадии «g» синтеза соединения 2, как представлено на фиг.2. Также могут применяться другие способы изотопного мечения соединений, обычно используемые в области радиохимического синтеза.
Соединения по настоящему изобретению могут использоваться в качестве противозачаточных средств для особей мужского пола для контроля рождаемости у млекопитающих, включая человека. Кроме их возможного применения для контроля над рождаемостью соединения по настоящему изобретению также могут использоваться для контроля рождаемости у домашних, диких или одичавших животных в тех случаях, когда летальные меры нецелесообразны или нежелательны. Например, регуляция численности оленей в некоторых областях США является сложной задачей. Пероральное введение соединений по настоящему изобретению сезонно размножающимся животным, таким как олени, путем включения в подходящее время этих соединений в разбрасываемый корм, может значительно сократить репродуктивную способность. Другие интересующие животные включают грызунов, таких как мыши, крысы, луговые собачки и так далее, а также одичавшие козы, свиньи, лошади и так далее. Введение соединений по настоящему изобретению содержащимся в зоопарке животным является мерой контроля над рождаемостью у видов, численность которых стала чрезмерной.
Под применяемым в этом документе термином «контроль над рождаемостью» понимают снижение репродуктивной способности или плодовитости подвергаемых воздействию млекопитающих. Продолжительность бесплодия зависит от дозы, поэтому с применением значительных доз можно увеличить период бесплодия с тем, чтобы применение соединений по настоящему изобретению в значительных дозах вызывало стерилизацию; поэтому соединения по настоящему изобретению могут выступить заменой хирургическому иссечению семявыносящего протока как средству стерилизации особей мужского пола. При осуществлении подобной стерилизации соединения по настоящему изобретению вводят единой дозой или в виде множественных (двух или более) доз, и дозы являются достаточными для того, чтобы снизить у млекопитающего способность продуцировать сперматозоиды (сперматогенный индекс) до уровня бесплодия. То есть соединения по настоящему изобретению вводят в количестве и в течение промежутка времени, достаточного для того, чтобы уменьшить число сперматозоидов до уровня, недостаточного для воспроизводства.
Для упомянутых выше способов применения доза соединения по настоящему изобретению обычно изменяется в зависимости от конкретно применяемого соединения, способа введения и требуемой продолжительности бесплодия. Тем не менее, удовлетворительные результаты получают в случае перорального введения животным приблизительно от 0,02 приблизительно до 10 мг/кг, предпочтительно приблизительно 0,1-3 мг/кг массы тела в сутки. Для более крупных животных суточная доза, составляющая приблизительно 10-100 мг, может вводиться в виде однократной дозы для перорального применения или может быть разделена на дробные дозы, содержащие приблизительно 0,1-10 мг соединения по настоящему изобретению. В случае введения отдельного активного энантиомера, как правило, может вводиться более низкая доза по сравнению с введением рацемического соединения. При желании или необходимости соединения по настоящему изобретению могут вводиться вместе с твердыми или жидкими носителями или разбавителями или в виде формы с замедленным высвобождением. Получение композиций этих фармацевтических форм хорошо известно в данной области техники, и в случае соединений по настоящему изобретению может применяться любой традиционный способ твердых и жидких составов и составов с замедленным высвобождением. Соединения по настоящему изобретению могут также вводиться посредством обычных имплантатов или путем чрескожного введения, которые хорошо известны в этой области техники.
Соединения по настоящему изобретению могут применяться для контрацепции у мужчин либо путем обратимого блокирования сперматогенеза, либо для нехирургической стерилизации. В последнем случае введение соответственно высоких доз приводит к эффектам иссечения семявыносящего протока без применения хирургического вмешательства, устраняя тем самым возможные побочные эффекты иссечения семявыносящего протока.
Соединения по настоящему изобретению также применимы для контроля над рождаемостью у домашних, диких, одичавших и содержащихся в зоопарке животных. Например, соединения по настоящему изобретению могут применяться для контроля над рождаемостью у содержащихся в зоопарке животных. Популяции диких и одичавших животных, живущих по соседству с человеком, например оленей, или популяции животных, в большой мере зависящих от экологической обстановки, например диких мустангов или одичавших собак, могут регулироваться путем избирательного разбрасывания содержащего соединения корма без применения летальных мер, таких как отстрел или применение яда. В этом случае нарушается не поведение животных, а только плодовитость.
В том случае, если R4 представляет собой радиоактивную метку, соединения по настоящему изобретению применимы для изучения функции яичек и диагностики дисфункции яичек. Соединения, вводимые в указанных выше дозировках, связываются с тканями яичек.
Антисперматогенные свойства соединений по настоящему изобретению, их высокая степень хемо-, стерео- и энантиоселективности вместе с отсутствием у них эффектов общего характера, таких как снижение полового влечения, указывает на то, что они специфически связываются с макромолекулами в яичках. Обработка яичек или фракций, полученных из яичек, радиоактивным производным соединений по настоящему изобретению с последующим радиоактивным анализом в соответствии с методиками радиационной химии, известными в данной области техники, позволяет определить местоположение и идентифицировать часть яичка и макромолекулу, вовлеченную в антисперматогенный эффект. Это может быть применимо для определения и идентификации важного компонента яичек, нарушение функции которого приводит к эффекту бесплодия. Сравнение способности других соединений (таких как применяемых в настоящее время соединений или соединений из комбинаторных библиотек) ингибировать связывание радиоактивно меченного соединения может привести к получению более избирательных и эффективных антисперматогенных соединений. Кроме того, путем введения животному или человеку небольшой дозы (слишком малой для того, чтобы оказать клинически значимое воздействие на плодовитость) радиоактивно меченного соединения и измерения после этого величины радиоактивности в яичке или в конкретной части яичка можно показать, связана ли существующая проблема с плодовитостью с отсутствием этой макромолекулы. Радиоактивность может быть измерена у живого животного или у человека при помощи таких методик, как PET и SPECT, которые хорошо известны в области отображения биологических тканей.
Соединения по настоящему изобретению также применимы в качестве внутренних стандартов для аналитических целей. Так, например, соединение, такое как соединение 20, может быть добавлено в известном количестве к образцу крови, плазмы или ткани животного или человека, получившего дозу соединения 17. Затем образец крови, плазмы или ткани может быть экстрагирован органическим растворителем, экстракт подвергнут аналитической высокоэффективной жидкостной хроматографии или газовой хроматографии или с преобразованием до производного, такого как метиловый эфир, или без преобразования. Измерения участков хроматографических пиков, соответствующих соединениям 17 и 20, и сравнение с отношениями участков, полученных в тех же условиях, с известными количествами соединений 17 и 20, позволяют определить содержание соединения 17 в образце крови, плазмы или ткани. Вследствие близкого структурного сходства соединений 17 и 20 физико-химические свойства этих соединений будут сходны применительно к экстракции, что, таким образом, делает их практически идеальными стандартами друг по отношению к другу.
Для применения в качестве спермицида соединения по настоящему изобретению могут быть приготовлены в формах для различного введения. Традиционные формы спермицидных композиций легко приготавливают в соответствии с известными способами. Такие спермицидные композиции могут иметь форму гелей, пен, желе, кремов, мазей, смазок, и так далее. Для приготовления композиций применяют традиционные носители. Спермицидные композиции по настоящему изобретению могут вводиться по отдельности или в сочетании с одним или несколькими барьерными способами контрацепции, такими как диафрагма, губка или презерватив. Композиция может наноситься непосредственно на диафрагму, губку или презерватив непосредственно перед применением или может быть предварительно упакована с губкой или презервативом (или даже с диафрагмой, хотя большинство диафрагм предназначено для многократных применений и очищаются между применениями).
Для применения в качестве фунгицида соединения по настоящему изобретению могут быть приготовлены в любой форме, подходящей для введения в необходимую область. Формы введения включают без ограничения формы, перечисленные выше для спермицидных композиций, а также жидкие смеси. Также возможно применение одной из общих форм для введения для совместного использования фунгицидных и спермицидных свойств.
Другие особенности настоящего изобретения станут очевидными в процессе последующего описания примеров осуществления, которые представлены для пояснения настоящего изобретения и не предназначены для его ограничения.
ПРИМЕРЫ
Пример 1
Синтез (4aRS,5SR,9bRS)-2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-5-(пара-карбоксифенил-1H-индено[1,2-c]пиридингидрохлорида.
К этилизоникотинату (500 г, 3,31 моль) добавляли йодэтан (540 г, 3,41 моль) в метаноле (500 мл). Смесь осторожно кипятили с обратным холодильником в течение ночи. К полученному выше раствору порциями добавляли боргидрид натрия (140 г) при охлаждении на ледяной бане. После завершения добавления NaBH4 смесь перемешивали при комнатной температуре в течение ночи. Большую часть метанола упаривали, к раствору добавляли воду и эфир, и разделяли эфирный слой. Сухой (Na2SO4) эфирный слой упаривали с получением масла. Полученное красное масло перегоняли с получением желтоватого масла (470 г, 78%): т.кип.=160°C (при 0,5 мм рт.ст.).
Полученное выше соединение (146 г, 0,8 моль) в сухом эфире (200 мл) по каплям добавляли к 1M пара-толилмагнийбромиду в эфире (600 мл, 1,6 моль при -10°C.). После перемешивания в течение 3 ч реакционную смесь вливали в 10% водный раствор NH4Cl (200 мл). Водный слой экстрагировали эфиром. Сухой (Na2SO4) эфирный слой упаривали с получением желтовато-коричневого масла. Это масло растворяли в 18% водном растворе HCl (500 мл) и экстрагировали эфиром. Водный раствор HCl нагревали с обратным холодильником в течение 2 ч. Растворитель упаривали с получением соответствующей аминокислоты (181 г, выход 80%), 32 г которой смешивали с полифосфорной кислотой (500 г) и энергично перемешивали при 140°C в течение 3 ч. Реакционную смесь охлаждали и осторожно добавляли 50% водный раствор KOH. Превращенный в основание раствор экстрагировали эфиром. Сухой (Na2SO4) эфирный слой упаривали с получением 2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-1H-индено[1,2-c]пиридинона-5-она в виде масла (22,6 г, 87%). Аналитическую пробу получали путем пропускания через небольшую колонку с SiO2, элюируя градиентом MeOH в CHCl3 (0-5%): 1H ЯМР (90 МГц, CDCl3) δ 7,5 (1H, с, H-6), 7,3 (2H, м, H-8, H-9), 3,5 (1H, м), 3,0 (1H, м), 2,6 (2Н, м), 2,3 (3H, с, 7-Me), 2,2 (3H, м), 1,9-1,7 (3H, м), 1,1 (3H, т, Me); HRMS (М+): Рассчитано для C15H19NO: m/z 229,1467. Обнаружено: m/z 229,1466.
К механически перемешанному раствору пара-бромбензойной кислоты (1,6 г, 8,0 ммоль) в тетрагидрофуране (THF) (15 мл) при -78°C по каплям в течение 45 минут добавляли н-бутиллитий (16,2 ммоль, 6 мл 2,5M раствора в гексане). После дополнительного перемешивания смеси в течение 1,5 ч по каплям в течение 30 минут добавляли трициклический кетон (1,1 г, 5,1 ммоль) в виде раствора в THF (5 мл) и продолжали перемешивание в течение 2,5 ч при -78°C. Смесь вливали в холодную, как лед, 1M HCl (75 мл) и экстрагировали эфиром (2×30 мл). Кислотный водный слой перемешивали в течение 15 ч при комнатной температуре и концентрировали при пониженном давлении с получением твердого вещества. Это твердое вещество очищали по методу колоночной флэш-хроматографии на силикагеле, элюируя градиентом 10-20% MeOH в CHCl3, с получением 2-этил-7-метил-2,3,4,9b-тетрагидро-5-(пара-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида в виде желтого твердого вещества (1,1 г, 58%). 1Н ЯМР (250 МГц, CDCl3) δ 1,54 (3H, т, J=7,2 Гц), 2,35 (3H, шир.с), 2,25-2,42 (1H, м), 2,50-2,72 (1H, м), 2,94-3,0 (1H, м), 3,15-3,30 (2H, м), 3,50-3,80 (2H, м), 4,17-4,30 (1H, м), 4,40-4,52 (1H, м), 7,0-7,12 (2H, м), 7,32 (1H, д, J=7,5 Гц), 7,45 (2H, д, J=8,4 Гц), 8,20 (2H, д, J=8,4 Гц). HRMS (М+) Рассчитанный молекулярный вес для C22H23NO2: m/z 333,1729. Обнаружено: m/z 333,1725.
К раствору полученного выше соединения (379 мг, 1,03 ммоль) в этаноле/воде (40 мл смеси 1:1) добавляли NaCl (81 мг), PdCl2 (98 мг), NaBH4 (100 мг) и концентрированную HCl (10 капель). После перемешивания смеси на аппарате Парра в атмосфере водорода (при давлении 45 фунтов/дюйм2) при 50°C в течение 15 ч, смесь фильтровали через броунмиллерит и концентрировали при пониженном давлении. Полученное твердое вещество суспендировали в абсолютном этаноле, фильтровали через броунмиллерит и концентрировали фильтрат при пониженном давлении с получением (4aRS,5RS,9bRS)-2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-5-(пара-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида. 1Н ЯМР (250 МГц, CDCl3) δ 1,4 (3H, т, 7,2 Гц), 1,50-1,60 (1H, м), 1,85-2,00 (1H, м), 2,20 (3H, с), 2,20-2,40 (1H, м), 2,70-2,90 (3H, м) 2,90-3,15 (2H, м), 3,50-3,65 (1H, м), 3,90-4,10 (1H, м), 4,50 (1H, д, J=7,3 Гц), 6,95, (1H, шир.с), 7,10 (1H, д, J=7,5 Гц), 7,20 (1H, д, J=7,5 Гц), 7,30, (2H, д, J=8,0 Гц), 8,00 (2H, д, J=8,0 Гц). HRMS (М+) Рассчитанный молекулярный вес для C22H25NO2: m/z 335,18853. Обнаружено: m/z 335,1887.
К раствору гидроксида калия (15 г) в н-бутаноле (60 мл) одной порцией добавляли полученное выше соединение (2,99 г, 8,0 ммоль). После нагревания с обратным холодильником в течение 20 ч темно-коричневую смесь охлаждали до 0°C и подкисляли до pH 1 добавлением 18% HCl. Растворитель удаляли в вакууме с получением желтого твердого вещества. Это твердое вещество помещали в CHCl3, фильтровали через броунмиллерит и концентрировали фильтрат в вакууме с получением неочищенного (4aRS,5SR,9bRS)-2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-5-(пара-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида в виде не совсем белого твердого вещества. Это твердое вещество очищали по методу колоночной флэш-хроматографии, элюируя 10% MeOH-CHCl3, с получением 1,23 г (41%) указанного в заголовке соединения в виде белого твердого вещества: т.пл.=280°C (с разложением). 1Н ЯМР (250 МГц, CDCl3-CD3OD) δ 1,45 (3H, т, J=7,3 Гц), 1,8 (1H, шир.д, J=14,7 Гц), 2,2 (3H, с), 2,4-2,7 (2H, м), 3,0-3,4 (4H, м), 3,4-3,7 (2H, м), 3,7-4,0 (1H, м), 4,2 (1H, д, 11 Гц), 6,6 (1H, шир.с), 7,0-7,2 (4H, м), 8,0 (1H, д, J=7,7 Гц). HRMS (М+) Рассчитанный молекулярный вес для C22H25NO2: m/z 335,18853. Обнаружено: m/z 335,18830.
Аналитически рассчитано для C22H26ClNO2 1/2H2O: C, 69,37; H, 7,14; N, 3,68. Обнаружено: C, 69,72; H, 7,15; N, 3,55.
Пример 2
Синтез (4aRS,5SR,9bRS)-2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-5-(пара-карбометоксифенил)-1H-индено[1,2-c]пиридингидрохлорида
К раствору карбоновой кислоты примера 1 (3,6 г, 9,69 ммоль) в метаноле (50 мл) при -10°C в течение 10 минут добавляли тионилхлорид (1,1 мл, 14,5 ммоль). Полученный раствор выдерживали в холодильнике при 5°C в течение 68 ч, в течение которых продукт начинал выкристаллизовываться в виде тонких белых игл. Три полученных партии объединяли с получением 2,65 г указанного в заголовке соединения: т.пл.=204°C (с возгонкой). 1Н ЯМР (250 МГц, CDCl3) δ 1,1 (3H, т, J=7,2 Гц), 1,6 (1H, шир.д, J=14,2 Гц), 1,80-2,00 (2H, м), 2,1-2,2 (1H, м), 2,2 (3H, с), 2,4 (2H, кв., J=7,2 Гц), 2,5-2,6 (1H, м), 2,7-2,8 (1H, м), 2,9 (1H, дд, J=5,94, 11,64 Гц), 3,3-3,4 (1H, м), 3,9 (3H, с), 4,2 (1H, д, J=10,0 Гц), 6,7 (1H, шир.с), 7,0 (1H, д, J=7,5 Гц), 7,2 (1H, д, J=7,5 Гц), 7,3 (2H, д, J=8,0 Гц), 8,0 (2H, д, 8,0 Гц).
Аналитически рассчитано для C23H28ClNO2 1/4H2О: C, 70,75; H, 7,36; N, 3,59. Обнаружено: C, 70,67; H, 7,36; N, 3,59.
Пример 3
Синтез (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-8-йод-7-метил-5-(4-карбометоксифенил)-1H-индено[1,2-c]пиридингидрохлорида (18) и его (l)-энантиомера ((l)-18)
К перемешанному раствору (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-7-метил-5-(4-карбометоксифенил)-1H-индено[1,2-c]пиридина (341 мг, 0,88 ммоль) в ледяной уксусной кислоте (2 мл) добавляли 62% HClO4 (1 мл), а затем HgO (205 мг, 0,95 ммоль). Для придания раствору гомогенности смесь обрабатывали ультразвуком в течение короткого промежутка времени. По каплям в течение 15 минут добавляли раствор йода (235 мг, 0,925 ммоль) в ледяной уксусной кислоте (17 мл) и перемешивали полученную смесь при комнатной температуре в течение ночи. Оранжево-красную смесь вливали в воду (100 мл), охлаждали до 5°C, подщелачивали до pH 12 добавлением 30% NaOH и экстрагировали эфиром (3×75 мл). Прозрачные бесцветные эфирные экстракты объединяли, последовательно промывали водой (20 мл) и соляным раствором (30 мл), сушили (MgSO4), фильтровали и концентрировали в вакууме с получением неочищенного свободного основания соединения 18 (448 мг). Этот материал преобразовывали в гидрохлорид с применением 3% метанольного раствора хлороводорода и перекристаллизовывали из EtOAc-MeOH. Выход=400 мг (89%); т.пл.=>190°C (с разложением). 1Н ЯМР (250 МГц, CDCl3 как свободное основание): δ 1,15 (3H, т, J=7,2 Гц), 1,65 (1H, шир.д), 1,8-2,1 (3H, м), 2,32 (3H, с), 2,48 (3H, кв., J=7,2 Гц, +м), 2,80 (1H, шир.д), 2,97 (1H, дд, J=11,8, 5,8 Гц), 3,41 (1H, м), 3,91 (3H, с), 4,19 (1H, д, J=9,8 Гц), 6,78 (1H, с), 7,22 (2H, д, J=8,3 Гц), 7,73 (1H, с), 8,00 (2H, д, J=8,3 Гц). HRMS: Рассчитано для C23H26NO2I (соответствует свободному основанию): m/z 475,1008. Обнаружено: m/z 475,1004. Рассчитанный молекулярный вес для C23H27ClINO2 1/2H2O: C, 53,04; H, 5,42; N, 2,69. Обнаружено: C, 52,70: H, 5,60; N, 2,57. Активный энантиомер, (l)-18, синтезировали сходным путем, используя в качестве исходного вещества (l)-3. [α]=-5,6 (c=1,18, CHCl3).
Пример 4
Синтез (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-8-йод-7-метил-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида (17)
К раствору (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-7-метил-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида (250 мг, 0,673 ммоль) в 2 мл уксусной кислоты добавляли 6 мл смеси уксусной кислоты и перхлорной кислоты (1:1). Добавляли HgO (1,35 ммоль) и перемешивали реакционную смесь при комнатной температуре до тех пор, пока HgO не растворится. К реакционной смеси через капельную воронку по каплям добавляли раствор I2 (427 мг, 1,68 ммоль) в 4 мл уксусной кислоты и 6 мл CH2Cl2. Реакционную смесь перемешивали в течение ночи при комнатной температуре, а затем фильтровали через броунмиллерит. Красное твердое вещество промывали водой и CH2Cl2. Объединенный двухфазный фильтрат разделяли при помощи делительной воронки. Органическую фазу промывали насыщенным раствором гидросульфита натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали с получением 234 мг желто-коричневого твердого вещества, которое преобразовывали в гидрохлорид обычным путем. 1Н ЯМР (250 МГц, CDCl3/CD3OH) δ 1,28 (3H, т, J=7,2 Гц), 2,0-2,1 (1H, м), 2,3 (3H, с), 2,56 (2H, м), 3,04 (3H, м), 3,24 (1H, м), 3,46 (2H, м), 4,18 (1Н, д, J=11 Гц), 6,73 (1H, с), 7,13 (2H, д, J=8,2 Гц), 7,71 (1H, с), 7,89 (2H, д, J=8,2 Гц). HRMS Рассчитано для C22H24NO2I (соответствует свободному основанию): m/z 461,0852. Обнаружено: m/z 461,0857.
Пример 5
Синтез (4aRS,5SR,9bRS)-2-этил-8-бром-7-метил-2,3,4,4a,5,9b-гексагидро-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида (19)
(4aRS,5SR,9bRS)-2-Этил-8-йод-7-метил-2,3,4,4a,5,9b-гексагидро-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорид (200 мг, 0,402 ммоль) растворяли в 20 мл THF и 0,4 мл гексаметилфосфорамида. К раствору добавляли 50 мг гидрида натрия (60% в минеральном масле). Смесь нагревали с обратным холодильником в течение 1 ч, а затем охлаждали до -78°C. Медленно добавляли раствор трет-бутиллития (0,73 мл, 1,1M в пентане, 0,804 ммоль). После добавления смесь перемешивали при
-78°C в течение 20 минут. Добавляли 1,2-дибромэтилен (1 мл). Смесь дополнительно перемешивали при -78°C в течение 30 минут, а затем нагревали до комнатной температуры. К раствору добавляли 5% соляную кислоту до тех пор, пока раствор не становился кислотным. Смесь экстрагировали метиленхлоридом. Метиленхлоридный раствор промывали соляным раствором и сушили над MgSO4. Неочищенный продукт очищали по методу колоночной флэш-хроматографии, элюируя метиленхлоридом/этанолом (10:1), с получением указанного в заголовке соединения: 30 мг, выход 17%, т.пл=169,6-170,3°C. 1Н ЯМР (250 МГц, D2O-CDCl3) δ 1,25 (3H, т, J=7,0 Гц), 1,72 (1H, д, J=15 Гц), 1,90-2,15 (1H, м), 2,19 (3H, с), 2,36 (1H, т, J=12,5 Гц), 2,5-2,65 (1H, м), 2,7-3,0 (3H, м), 3,2-3,4 (4H, м), 3,4-3,6 (1H, м), 4,13 (1H, д, J=10,5 Гц), 6,71 (1H, с), 7,11 (2H, д, J=8,0 Гц), 7,43 (1H, с), 7,89 (2H, д, J=8,0 Гц). МС: 413 (М). Аналит. (C22H25O2BrClN 1,8H2O): Рассчитан С 54,68, H 5,22, N 2,90; Обнаружено С 54,77, H 5,52, N 2,57. HRMS Рассчитано для C22H24NO2Br (соответствует свободному основанию): m/z 413,0990. Обнаружено: m/z 413,0994.
Пример 6
Синтез (4aRS,5SR,9bRS)-2-этил-8-хлор-7-метил-2,3,4,4a,5,9b-гексагидро-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида (20)
(4aRS,5SR,9bRS)-2-Этил-8-йод-7-метил-2,3,4,4a,5,9b-гексагидро-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорид (250 мг, 0,5 ммоль) растворяли в 25 мл THF и 0,5 мл HMPA. К раствору добавляли 60 мг гидрида натрия (60% в минеральном масле). Смесь нагревали с обратным холодильником в течение 1 ч, затем охлаждали до -78°C. Медленно добавляли раствор трет-бутиллития (0,91 мл, 1,1M в пентане, 1,04 ммоль). После добавления смесь перемешивали при -78°C в течение 20 минут. Добавляли раствор гексахлорэтана (2,46 г, 10,4 ммоль) в 2 мл THF. Смесь дополнительно перемешивали при -78°C в течение 30 минут, а затем нагревали до комнатной температуры. К раствору добавляли 5% соляную кислоту до тех пор, пока раствор не становился кислотным. Смесь экстрагировали метиленхлоридом. Метиленхлоридный раствор промывали соляным раствором и сушили над MgSO4. Неочищенный продукт очищали по методу колоночной флэш-хроматографии, элюируя метиленхлоридом/этанолом (10:1), с получением указанного в заголовке соединения: 60 мг, выход 30%. 1Н ЯМР (250 МГц, D2O-CDCl3): δ 1,35 (3H, т, J=7,25 Гц), 1,75-1,95 (1H, м), 2,30 (3H, с), 2,45-2,75 (2H, м), 2,80-3,15 (2H, м), 3,20-3,50 (4H, м), 3,50-3,70 (1H, м), 4,25 (1H, д, J=10 Гц), 6,80 (1H, с), 7,25 (2H, д, J=7,5 Гц), 7,32 (1H, с), 8,0 (2H, д, J=7,5 Гц). МС: 370 (М). Аналит. (C22H25O2Cl2N): Рассчитано С 65,50, H 6,20, N 3,45; Обнаружено С 65,65, H 6,73, N 3,59. HRMS Рассчитано для C22H24NO2Cl (соответствует свободному основанию): m/z 369,1495. Обнаружено: m/z 369,1494.
Пример 7
Синтез (4aRS,9bRS)-2-этил-1,2,3,4,4a,9b-гексагидро-1H-индено[1,2-c]пиридин-5-она (7)
Неочищенный метил-1-этил-3-(4-метилфенил)-4-пиридинкарбоксилат (полученный из 165 г метил-1-этил-1,2,5,6-тетрагидропиридинкарбоксилата, как описано в патенте США №5319084 для аналогичного сложного этилового эфира) растворяли в 1 л водного раствора 18% HCl и экстрагировали эфиром (300 мл) для удаления битолила, оставшегося в качестве побочного продукта его синтеза. Затем водный раствор нагревали с обратным холодильником в течение 48 ч, а затем концентрировали при пониженном давлении с добавлением ацетонитрила (азеотроп) с получением неочищенного гидрохлорида 1-этил-1,2,5,6-тетрагидропиридинкарбоновой кислоты (283 г), который тщательно высушивали при 100°C в высоком вакууме. В связи с тем, что этот материал является сильно гигроскопичным, он хранился в атмосфере азота. К неразбавленному соединению 7 (45 г, 159 ммоль) при 5°C осторожно добавляли тионилхлорид (150 мл). После добавления ледяную баню удаляли и перемешивали полученный гомогенный раствор при комнатной температуре в течение 4 ч. Избыток SOCl2 удаляли в вакууме с получением темной, плотной пастообразной массы. К этому материалу добавляли 1,2-дихлорэтан (250 мл) и удаляли в вакууме 30 мл растворителя с целью удалить все остатки SOCl2. К мутной смеси в течение 45 минут порциями добавляли AlCl3 (53 г, 397 ммоль). При помощи водяной бани регулировали температуру на уровне приблизительно 25°C. После добавления темный красно-коричневый раствор перемешивали при 35-40°C в течение часа, а затем вливали в лабораторный стакан, в котором находилось приблизительно 400 г дробленого льда и 50 мл конц. HCl. Водный слой подщелачивали приблизительно до pH 12 добавлением 30% NaOH (приблизительно 350 мл) с охлаждением на бане с ледяной водой. Полученную смесь экстрагировали с охлаждением на бане с ледяной водой. Полученную смесь экстрагировали эфиром (3×400 мл), эфирные слои последовательно промывали объединенные водой и соляным раствором, сушили (MgSO4), фильтровали и концентрировали при пониженном давлении с получением оранжево-красного масла. Это масло перегоняли с применением аппарата Кугельрора (125-135°C при давлении 0,5 мм рт.ст.) с получением 21,6 г (59%) кетона 7 в виде ярко-желтого твердого вещества с ЯМР-характеристиками, идентичными подлинному материалу.
Пример 8
Синтез энантиомеров (4aRS,5SR,9bRS)-2-этил-7-метил-5-(4-карбометоксифенил)-2,3,4,4a,5,9b-гексагидроиндено[1,2-c]пиридина и (4aRS,5SR,9bRS)-2-этил-7-метил-5-(4-карбоксифенил)-2,3,4,4a,5,9b-гексагидроиндено[1,2-c]пиридина
Описание энантиомеров как (d)- или (l)-энантиомеров основано на оптическом вращении в D-линии натрия в данном растворителе. Соединения, обладающие тем же знаком вращения, необязательно имеют ту же абсолютную конфигурацию.
1-Этил-4-карбокси-1,2,5,6-тетрагидропиридингидрохлорид
Метил-1-этил-1,2,5,6-тетрагидропиридинкарбоксилат (11) нагревали с обратным холодильником в 250 мл 1,5M HCl в течение 4 ч. Для получения высококристаллического твердого вещества смесь упаривали досуха с применением подводимого тепла и струи азота. Твердое вещество перекристаллизовывали из MeOH с получением 19,6 г гидрохлорида соединения 12: т.пл.=265°C (с разложением). Аналитически рассчитано для C8H14ClNO2: C, 50,14; H, 7,36; N, 7,31. Обнаружено: C, 50,23; H, 7,36; N, 7,28.
(l)-Еноилсультам ((l)-13), полученный из 1S(-)-(2,10)камфорсультама
К гидрохлориду соединения 12 (1,3 г, 6,79 ммоль) добавляли тионилхлорид (15 мл) и нагревали полученную смесь с обратным холодильником в течение 2 ч. Избыток SOCl2 удаляли в вакууме, растирали остаток с 10 мл безводного толуола и концентрировали в вакууме. Процесс растирания повторяли еще дважды с получением желтого порошкообразного твердого вещества. В отдельном сосуде к раствору 1S-(-)-2,10-камфорсультама (3,16 г, 14,7 ммоль) в THF (30 мл) при 5°C по каплям добавляли н-бутиллитий (15 ммоль, 6,0 мл 2,5 M раствора в гексане). После добавления прозрачный бесцветный раствор доводили до комнатной температуры и дополнительно перемешивали в течение 45 минут. Затем раствор сультам-аниона добавляли через канюлю в колбу, содержащую при 5°C гидрохлорид хлорида аминокислоты. После добавления оранжевую смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 18 ч. Реакцию тушили добавлением насыщенного NH4Cl (приблизительно 1 мл) и концентрировали в вакууме с получением коричневого дегтеобразного остатка. Этот остаток распределяли между эфиром и водой и еще один раз промывали эфирный слой водой. Затем эфирный слой промывали разбавленным водным раствором HCl (приблизительно 5%) и разделяли. После перекристаллизации из абсолютного EtOH получали свободный сультам (эфирный слой) (1,2 г). Кислотный водный слой подщелачивали до pH 12 добавлением NH4OH, экстрагировали эфиром, упаривали эфирный слой и перекристаллизовывали остаток из н-гексана с получением продукта [(l)-13]. Соединение (l)-13 (1,9 г) получали в виде белых толстых игл: т.пл=120°C. [α]D 21=-74,8°C. (c=1,0, CHCl3). 1Н ЯМР спектр соединения был идентичен таковому для оптического антипода (см. ниже). Аналитически рассчитано для C8H28N2O3S: C, 61,33; H, 8,01; N, 7,95. Обнаружено: C, 61,35; H, 8,06; N, 7,89.
(d)-Еноилсультамный энантиомер соединения 13, полученный из 1R(+)-(2,10)камфорсультама. Это соединение получали из гидрохлорида аминокислоты 12 (6,5 г, 34,1 ммоль) и 1R-(+)-2,10-камфорсультама (15,4 г, 71,4 ммоль) по методике, сходной с описанной для получения оптического антипода (см. выше), с выходом 86%. Т.пл.=118,5°C-119,6°C (получали в виде плотных желтоватых листочков после перекристаллизации из гексана). [α]D 21=+74,1° (c=1,0, CHCl3); 1Н ЯМР (250 МГц, CDCl3) δ 1,00 (3H, с), 1,12 (3H, т, J=7,1 Гц), 1,22 (3H, с), 1,3-1,5 (2H, м), 1,8-2,1 (5H, м), 2,2-2,4 (1H, м), 2,55 (2H, кв., J=7,1 Гц), 2,6-2,7 (3H, м), 3,1-3,3 (2H, м), 3,38 (1H, д, J=13,6 Гц), 3,50 (1H, д, J=13,6 Гц), 4,0-4,1 (1Н, м), 6,5-6,6 (1H, м); Аналитически рассчитано для C18H28N2O3S: C, 61,33; H, 8,01; N, 7,95. Обнаружено: C, 61,48; H, 8,02; N, 7,98.
Кристаллическая форма этого материала варьировала в зависимости от скорости выпадения в осадок из гексана и от концентрации во время стадии очистки.
1,4-Аддукт (l)-14, полученный из (l)-13. К раствору еноилсультама (l)-13 (5,6 г, 16,0 ммоль) в толуоле (200 мл) при -78°C в течение 10 минут добавляли пара-толилмагнийбромид (33,6 ммоль, 33,6 мл 1,0M раствора в эфире). После дополнительного перемешивания в течение 30 минут при -78°C реакционную смесь помещали в морозильную камеру (-10°C) на ночь, а затем нагревали до +5°C в течение двух часов. Смесь тушили добавлением насыщенного раствора NH4Cl (200 мл). После экстракции водного слоя эфиром (400 мл) эфирный слой экстрагировали 3% HCl (3×200 мл). Кислотные слои объединяли, подщелачивали до pH 12 добавлением конц. NH4OH, экстрагировали эфиром (3×200 мл), промывали эфирные слои соляным раствором, сушили (MgSO4), фильтровали и концентрировали при пониженном давлении с получением твердого оранжевого вещества (7,12 г). Это твердое вещество перекристаллизовывали из эфира/гексана (приблизительно 40 мл смеси 1:2, соответственно) с выходом 3,64 г. Из следующей партии дополнительно получали 1,24 г. Общий выход составил 4,68 г (66%). Т.пл.=150,5-151,7°C (эфир/гексан; компактные, плотные желтоватые призмы). [α]D 21=26,2° (c=1,14, CHCl3); 1Н ЯМР (500 МГц, CDCl3) δ 0,44 (3H, с), 0,82 (3H, с), 1,13 (3H, т, J=7,16 Гц), 1,20-1,30 (2H, м), 1,40-1,55 (1H, м), 1,62-1,65 (1H, м), 1,70-1,85 (3H, м), 1,95-2,05 (1H, м), 2,05-2,10 (1H, м), 2,27 (3H, с), 2,55 (2H, кв., J=7,16 Гц), 2,55-2,62 (1H, м), 2,68-2,72 (1H, м), 2,82 (1H, дд, J=10,64, 3,47 Гц), 3,12 (1H, т, J=10,8 Гц), 3,24-3,28 (1H, м), 3,30 (1H, д, J=14,0 Гц), 3,32 (1H, д, J=14,0 Гц), 3,55-3,60 (1H, м), 3,67-3,71 (1H, м), 7,02 (2H, д, J=7,96 Гц), 7,15 (2H, д, J=7,96 Гц); Аналитически рассчитано для C25H36N2O3S: C, 67,53; H, 8,16; N, 6,30. Обнаружено: C, 67,58; H, 8,15; N, 6,30.
Энантиомерно чистый кетон (d)-7, полученный из (l)-14. Раствор 1,4-аддукта (l)-14 (6,86 г, 15,45 ммоль) в THF (40 мл) добавляли к свежеприготовленному раствору LiOH·H2O (6,43 г, 153 ммоль) в воде (40 мл). Полученную гетерогенную смесь энергично перемешивали при осторожном нагревании с обратным холодильником в течение 26 ч. Смесь охлаждали приблизительно до +5°C, подкисляли до pH 0 добавлением конц. HCl, и удаляли основную массу летучих компонентов путем направления струи газообразного азота средней силы над поверхностью смеси, которая была погружена в этот момент в теплую водяную баню (50°C). Оставшееся твердое вещество тщательно сушили в высоком вакууме. Проводили циклизацию полученного неочищенного материала до кетона (d)-7 по способу, сходному с описанным для рацемического материала (см. выше), с применением тионилхлорида и AlCl3 в 1,2-дихлорэтане. Получали 1,12 г свободного основания кетона (d)-7 в виде масла, которое затвердевало после выдерживания в течение ночи. Для получения физических данных часть этого материала очищали после восстановления на следующей стадии. [α]D 20=+95,9° (свободное основание, c=1,2, CHCl3); [α]D 20=+71,9° (соль HCl, c=1,1, CHCl3).
Энантиомерно чистый олефин (d)-15, полученный из кетона (d)-7. Этот материал получали из кетона (d)-7 (1,12 г, 4,89 ммоль) по способу, сходному с описанным для рацемического материала (см. патент США №5319084). Выход составил 850 мг (47%). [α]D 19=+21,2° (c=1,24, CHCl3).
Синтез (l)-2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-5-(4-бромфенил)-5-гидрокси-1H-индено[1,2-c]пиридина
К энергично перемешанному раствору 4-бромйодбензола (13,8 г, 48,9 ммоль) в 160 мл THF при -78°C очень медленно добавляли раствор н-бутиллития (19,6 мл, 2,5 M в пентане, 49 ммоль). После добавления раствор перемешивали при -78°C в течение 10 минут. Раствор становился желтым и мутным. Добавляли раствор (d)-2-этил-7-метил-1,2,3,4,4a,5,9b-гексагидроиндено[1,2-c]пиридин-5-она (8 г, 34,9 мМ) в 40 мл THF. Затем смесь перемешивали при -78°C в течение 2 ч. Охлаждающую баню удаляли и тушили смесь добавлением воды. Органическую фазу разделяли и экстрагировали водную фазу метиленхлоридом. Органические фазы объединяли, промывали соляным раствором и сушили над MgSO4. Растворитель упаривали и получали продукт, который перекристаллизовывали из метиленхлорида с получением указанного в заголовке соединения (10,8 г, 80%): т.пл.=169,6-170,3°C. 1Н ЯМР (250 МГц, CDCl3) δ 1,00 (3H, т, J=7,3 Гц), 1,70-2,00 (2H, м), 2,15-2,30 (1H, м), 2,29 (3H, с), 2,38 (2H, кв., J=7,3 Гц), 2,5-2,7 (2H, м), 2,70-2,85 (1H, м), 2,85-3,00 (1H, м), 3,30-3,50 (1H, м), 6,84 (1H, с), 7,17 (2H, кв., J=7,5 Гц), 7,31 (2H, д, J=11 Гц), 7,43 (2H, д, J=11 Гц). МС: 386 (М), 230 (100%). [α]D=-11,5° (c=1,03, CHCl3). Аналит. (C22H24OBrN): Рассчитано C, 65,28, H 6,26, N 3,62. Обнаружено С 65,11, H 6,21, N 3,64.
Синтез (l)-энантиомера (4aSR,SRS,9bSR)-2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-5-(4-бромфенил)-1H-индено[1,2-c]пиридина [(l)-10)]
Раствор (l)-2-этил-7-метил-2,3,4,4a,5,9b-гексагидро-5-(4-бромфенил)-5-гидрокси-1H-индено[1,2-c]пиридина (4,5 г, 13 ммоль) и 100 мл триэтилсилана в 300 мл безводного метиленхлорида охлаждали до -78°C. Раствор барботировали в течение 10 минут газообразным трифторбораном. Бесцветный раствор становился оранжевым. Смесь нагревали до комнатной температуры и добавляли 10 г карбоната калия, а затем воду. Органическую фазу разделяли и экстрагировали водный слой метиленхлоридом. Органические фазы объединяли, промывали соляным раствором и сушили над MgSO4. Растворитель упаривали с получением неочищенного продукта.
Неочищенный продукт растворяли в 40 мл н-бутанола. Добавляли гидроксид калия (9 г). Смесь нагревали с обратным холодильником при перемешивании. После нагревания с обратным холодильником в течение 20 ч смесь охлаждали до комнатной температуры и выливали на лед. Смесь экстрагировали метиленхлоридом. Метиленхлоридный раствор промывали соляным раствором и сушили над MgSO4. Растворитель упаривали и распределяли неочищенный продукт между диэтиловым эфиром и 18% раствором соляной кислоты. Слои разделяли и еще раз промывали водный слой диэтиловым эфиром. Водный раствор охлаждали до 0°C и подщелачивали до pH>14 добавлением 50% раствора гидроксида натрия. Смесь трижды экстрагировали метиленхлоридом. Органический раствор промывали соляным раствором и сушили над MgSO4. Растворитель упаривали и получали неочищенный продукт, который очищали по методу колоночной флэш-хроматографии на силикагеле, элюируя CH2Cl2 и MeOH (100:3), с получением указанного в заголовке соединения (l)-10 (3,2 г, выход 67% в два этапа). Гидрохлорид получали сходным путем. Т.пл.=240°C (с разложением). 1Н ЯМР (250 МГц, CDCl3) δ 1,12 (3H, т, J=7,25), 1,6-1,8 (1H, м), 1,80-2,05 (2H, м), 2,15-2,40 (2H, м), 2,26 (3H, с), 2,70-2,85 (1H, м), 2,90-3,10 (1H, м), 3,30-3,45 (1H, м), 4,12 (1H, д, J=10,25 Гц), 6,72 (1H, с), 7,00-7,30 (4H, м), 7,44 (2H, д, J=9,0 Гц). МС: 370 (М), [α]D=-7,8° (c=0,83, MeOH). Аналит. (C21H24BrNHCl): Рассчитано С 62,00, H 6,19, N 3,44. Обнаружено С 61,96, H 6,23, N 3,35.
Синтез (l)-энантиомера (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-7-метил-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида [(l)-2]
Раствор 100 мг (0,27 ммоль) соединения (l)-10 в 5 мл THF охлаждали до -78°C. К раствору добавляли 0,54 мл раствора н-бутиллития (2,5M в пентане, 1,35 ммоль). Раствор перемешивали при -78°C в течение 30 минут. Раствор барботировали в течение 10 минут углекислым газом, пропускаемым через иглу. Смесь дополнительно перемешивали при -78°C в течение 10 минут и нагревали до комнатной температуры. THF упаривали и подкисляли остаток добавлением 18% раствора соляной кислоты. Смесь экстрагировали метиленхлоридом. Метиленхлоридный раствор промывали соляным раствором и сушили над MgSO4. Осушитель фильтровали и концентрировали раствор с получением неочищенного продукта. Неочищенный продукт очищали по методу колоночной хроматографии на силикагеле, элюируя CH2Cl2 и MeOH (от 10:1 до 1:1), с получением 72 мг (выход 71%). [α]D=-15,5° (c=1,24, MeOH).
Синтез (d)-энантиомера (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-7-метил-5-(4-карбометокси)-1H-индено[1,2-c]пиридингидрохлорида [(d)-3]
Раствор соединения (l)-2 (20 мг) в 1 мл метанола охлаждали до -10°C (лед/ацетон). Добавляли избыток тионилхлорида. После добавления смесь нагревали до комнатной температуры и перемешивали в течение ночи. Избыток тионилхлорида и растворитель сдували азотом и сушили остаток в вакууме. Неочищенный продукт подвергали анализу по методу ВЭЖХ (Sumichiral, QA-4900, 4 мм × 25 см; растворители: 53,8% 1,2-дихлорэтана, 44% гексана, 2,2% этанола и 0,1% ТФУ; скорость течения: 0,8 мл/мин; детектор при λ=254 нм), который показал преобладание одного из энантиомеров >97% для (d)-3.
Синтез (d)-энантиомера (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b- гексагидро-7-метил-5-(4-карбоксифенил)-1H-индено[1,2-c]пиридингидрохлорида [(d)-2] и (l)-энантиомера (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-7-метил-5-(4-карбометокси)-1H-индено[1,2-c]пиридингидрохлорида [(l)-3].
Эти два соединения могут быть синтезированы с использованием в качестве исходного вещества описанного выше еноилсультама (d)-13 и путем выполнения описанной выше последовательности стадий, применяемой для получения (1)-энантиомеров. Свойства соединений были ранее описаны. См. Cook et al., J. Med. Chem., 38:753-763 (1995).
Очевидно, что в свете описанных выше методик возможно множество модификаций и разновидностей по настоящему изобретению. Поэтому следует понимать, что настоящее изобретения может быть осуществлено иначе, чем описано в этом документе, подпадая при этом под объем прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ КОНДЕНСИРОВАННОГО ИНДАНА | 2008 |
|
RU2451671C2 |
| ПРОИЗВОДНЫЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-B)ИНДОЛОВ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1995 |
|
RU2140417C1 |
| АЦЕТИЛЕНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ МЕТАБОТРОПНЫХ ГЛУТАМАТНЫХ РЕЦЕПТОРОВ (MGLUR5) | 2002 |
|
RU2341515C2 |
| ПРОИЗВОДНОЕ 1,2,3,4-ТЕТРАГИДРОХИНОКСАЛИНА, МЕТОД ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2804127C2 |
| МЕСТНОЕ ПРОТИВОГРИБКОВОЕ СРЕДСТВО | 2012 |
|
RU2593990C2 |
| НОВОЕ ПРОИЗВОДНОЕ БЕНЗОАЗЕПИНА И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2013 |
|
RU2642783C2 |
| КАРБОСТИРИЛЬНОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2430920C2 |
| ПРОТИВООПУХОЛЕВЫЕ СОЕДИНЕНИЯ | 2008 |
|
RU2493147C2 |
| ЦИКЛИЧЕСКИЕ СУЛЬФОНАМИДЫ ДЛЯ ИНГИБИРОВАНИЯ ГАММА-СЕКРЕТАЗЫ | 2004 |
|
RU2334743C2 |
| ТРИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2007 |
|
RU2456278C2 |
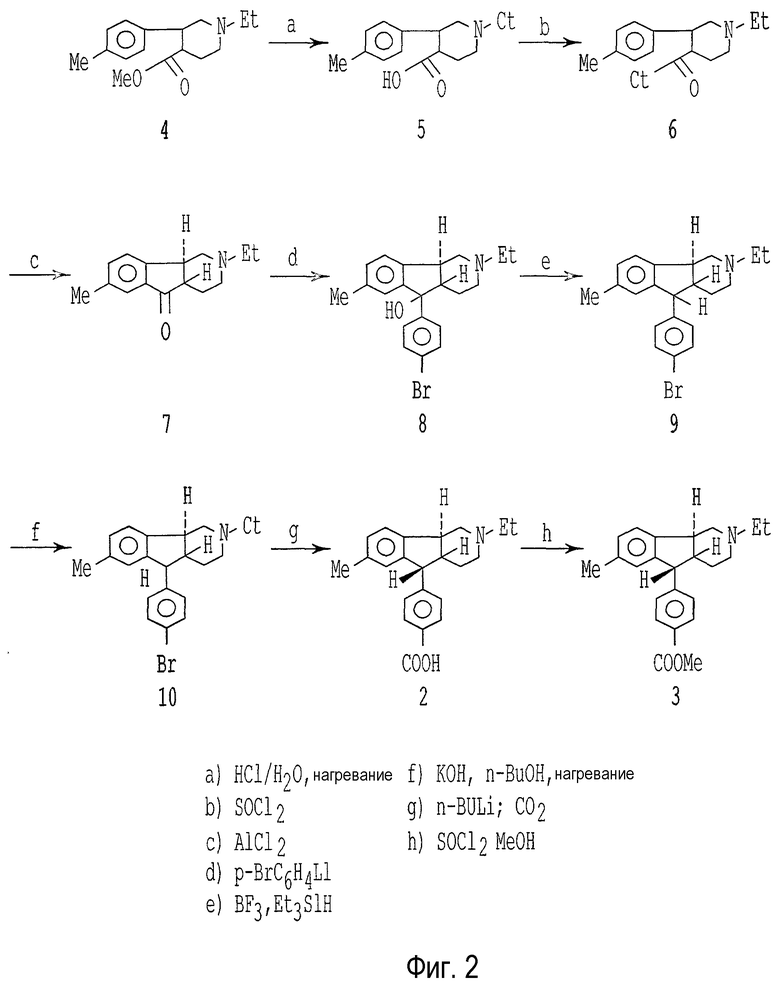


Группа изобретений относится к медицине, в частности к гинекологии и дерматологии, и касается вариантов спермицидной и/или противогрибковой композиций и способов контрацепции или лечения грибковых заболеваний с использованием таких композиций. Композиции по настоящему изобретению могут содержать эффективные количества гексагидроинденопиридиновых соединений, предотвращающие беременность, или оказывающие фунгицидное воздействие, и подходящий носитель. Изобретения обеспечивают эффективную контрацепцию и фунгицидное воздействие. 5 н. и 39 з.п. ф-лы, 4 ил., 7 табл.

где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью или С3-С8-циклоалкил;
R2 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью;
каждый R3 и R5 независимо представляет собой атом водорода, SO3Н, С1-6-алкил с неразветвленной или разветвленной цепью, СН2ОН, CH2OMe, C1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (СООН), неэфирную группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (CH2OC(O)R, где значения R определены выше, CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена; и
R4 представляет собой атом водорода, атом галогена, R3Si или COR.
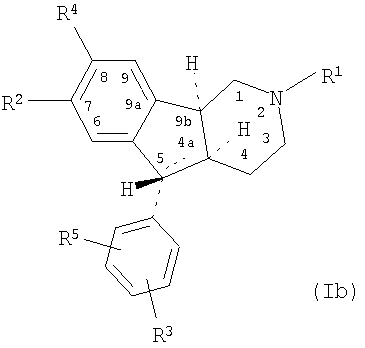
R2 выбран из группы, включающей атом водорода, метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гексил, изогексил;
R3 находится 4-м положении и выбран из группы, включающей атом водорода, SO3Н, С1-6-алкил с неразветвленной или разветвленной цепью, СН2ОН, СН2ОМе, С1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (СООН), неэфирную группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, гидроксиметил (СН2ОН), формил (СНО), карбоксил (СООН), эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (СН2ОС(О)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена;
R5 представляет собой атом водорода и
R4 выбран из группы, включающей атом водорода и атом галогена.
R2 представляет собой метил, этил, н-пропил или изопропил;
R3 представляет собой 4-СООН или 4-COOR, где значения R определены выше;
R5 представляет собой атом водорода и
R4 представляет собой атом галогена.
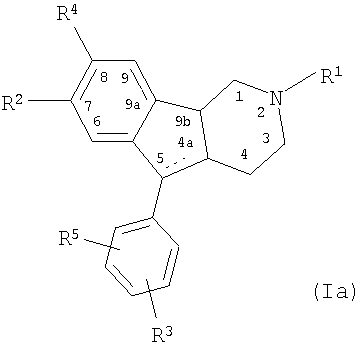
где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью или С3-С8-циклоалкил;
R2 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью;
каждый R3 и R5 независимо представляет собой атом водорода, SO3Н, C1-6-алкил с неразветвленной или разветвленной цепью, СН2ОН, СН2ОМе, C1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (СООН), неэфирную группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (СН2ОС(О)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH-NHNHCONH2 и атом галогена; и
R4 представляет собой атом водорода, атом галогена, R3Si или COR,
и подходящий носитель.

R2 выбирают из группы, включающей атом водорода, метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гексил, изогексил;
R3 находится 4-м положении и выбран из группы, включающей атом водорода, SO3Н, С1-6-алкил с неразветвленной или разветвленной цепью, СН2ОН, СН2ОМе, С1-6-алкоксигруппы с неразветвленной или разветвленной цепью, карбоксил (СООН), неэфирную группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, гидроксиметил (СН2ОН), формил (СНО), карбоксил (СООН), эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена;
R5 представляет собой атом водорода и
R4 выбран из группы, включающей атом водорода и атом галогена.
R2 представляет собой метил, этил, н-пропил или изопропил;
R3 представляет собой 4-СООН или 4-COOR, где значения R определены выше;
R5 представляет собой атом водорода и
R4 представляет собой атом галогена.
эффективное спермицидное количество соединения формулы I(а)

где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью или С3-С8-циклоалкил;
R2 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью;
каждый R3 и R5 независимо представляет собой атом водорода, SO3Н, С1-6-алкил с неразветвленной или разветвленной цепью, СН2ОН, СН2ОМе, C1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (СООН), неэфирную группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена; и
R4 представляет собой атом водорода, атом галогена, R3Si или COR,
носитель и барьерное противозачаточное средство.

R2 выбран из группы, включающей атом водорода, метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гексил, изогексил;
R3 находится 4-м положении и выбран из группы, включающей атом водорода, гидроксиметил (CH2OH), формил (СНО), карбоксил (СООН), эфир карбоновой кислоты (COOR, где R представляет собой С1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (СН2ОС(О)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атома галогена;
R5 представляет собой атом водорода и
R4 выбран из группы, включающей атом водорода и атом галогена.
R2 представляет собой метил, этил, н-пропил или изопропил;
R3 представляет собой 4-СООН или 4-COOR, где значения R определены выше;
R5 представляет собой атом водорода и
R4 представляет собой атом галогена.
введение при необходимости противогрибкового лечения субъекту, композиции, содержащей эффективное для нейтрализации грибков количество соединения формулы I(а)

где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной цепью;
R2 представляет собой атом водорода или С1-6-алкил с неразветвленной цепью;
каждый R3 и R5 независимо представляет собой атом водорода, С1-6-алкил с неразветвленной цепью, СН2ОН, С1-6-алкоксигруппу с неразветвленной цепью, эфир карбоновой кислоты (COOR, где R представляет собой С1-10-алкил) или CN и
R4 представляет собой атом водорода или атом галогена,
и приемлемый носитель.

R2 выбран из группы, включающей атом водорода, метил, этил, н-пропил, н-бутил, н-пентил и н-гексил;
R3 находится 4-м положении и выбран из группы, состоящей из атома водорода, гидроксиметила (СН2ОН), эфира карбоновой кислоты (COOR, где R представляет собой С1-6-алкил) и CN;
R5 представляет собой атом водорода и
R4 выбран из группы, включающей атом водорода и атом галогена.
R2 представляет собой метил, этил или н-пропил;
R3 представляет собой 4-COOR, где значения R определены выше;
R5 представляет собой атом водорода и
R4 представляет собой атом галогена.
пероральное введение субъекту композиции, содержащей эффективное количество первого соединения формулы I(а)

где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью или С3-С8-циклоалкил;
R2 представляет собой атом водорода или C1-6-алкил с неразветвленной или разветвленной цепью;
каждый R3 и R5 независимо представляет собой атом водорода, SO3Н, С1-6-алкил с неразветвленной или разветвленной цепью, СН2ОН, СН2ОМе, C1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (СООН), неэфирную группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, эфир карбоновой кислоты (COOR, где R представляет собой С1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена и
R4 представляет собой атом водорода, атом галогена, R3Si или COR,
и фармакологически приемлемый носитель и
сочетанное использование упомянутым субъектом обработанного
спермицидом механического противозачаточного средства, включающего:
эффективное количество второго соединения формулы I(а)

где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью или С3-С8-циклоалкил;
R2 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью;
каждый R3 и R5 независимо представляет собой атом водорода, SO3Н, C1-6-алкил с неразветвленной или разветвленной цепью, СН2ОН, СН2ОМе, C1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (СООН), неэфирную группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (СН2ОС(О)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена и
R4 представляет собой атом водорода, атом галогена, R3Si или COR,
и носитель и барьерное противозачаточное средство;
в котором указанное первое соединение формулы I(а) и указанное второе соединение формулы I(а) могут быть одинаковыми или разными.

R2 выбран из группы, включающей атом водорода, метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гексил, изогексил;
R3 находится 4-м положении и выбран из группы, включающей атом водорода, гидроксиметил (СН2OH), формил (СНО), карбоксил (СООН), эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена;
R5 представляет собой атом водорода и
R4 выбран из группы, включающей атом водорода и атом галогена.
R2 представляет собой метил, этил, н-пропил или изопропил;
R3 представляет собой 4-СООН или 4-COOR, где значения R определены выше;
R5 представляет собой атом водорода и
R4 представляет собой атом галогена.

R2 выбран из группы, включающей атом водорода, метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гексил, изогексил;
R3 находится 4-м положении и выбран из группы, включающей атом водорода, гидроксиметил (СН2OH), формил (СНО), карбоксил (СООН), эфир карбоновой кислоты (COOR, где R представляет собой C1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (СН2ОС(О)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена;
R5 представляет собой атом водорода и
R4 выбран из группы, включающей атом водорода и атом галогена.
R2 представляет собой метил, этил, н-пропил или изопропил;
R3 представляет собой 4-СООН или 4-COOR, где значения R определены выше;
R5 представляет собой атом водорода и
R4 представляет собой атом галогена.
| US 5952336, 14.09.1999 | |||
| RU 2001129136, 27.10.2002 | |||
| US 5319084, 07.06.1994 | |||
| US 4415548, 15.11.1983 | |||
| Кандидозная инфекция | |||
| Полиеновые антибиотики в лечении вагинального кандидоза | |||
| Гинекология | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| Старостина Т.А | |||
| и др | |||
| Современные методы контрацепции | |||
| В кн | |||
| Планирование семьи | |||
| - М.: Медицина, 1996, с.78 | |||
| COOK C.E | |||
| et al. | |||
Авторы
Даты
2009-02-20—Публикация
2004-01-23—Подача