Предметом настоящего изобретения является новый синтез производных с гидрофторметиленсульфонильным или гидрофторметиленсульфинильным радикалом.
Более конкретно, задачей изобретения является синтез производных дифторметансульфиновой или дифторметансульфоновой кислоты и, в частности, собственно кислоты, ее солей и ее хлорангидридов.
Сульфоновые кислоты, образуемые электроноакцепторными группами, в частности, образуемые электроноакцепторными группами, атом углерода которых, несущий сульфогруппу, несет также по меньшей мере один фтор, представляют собой к тому же интересные соединения, с одной стороны, потому что они позволяют придавать особые специфические свойства лекарствам или производным для сельского хозяйства и, с другой стороны, потому что они могут служить составными частями солей для батарей, в частности батарей, называемых литиевыми батареями.
Среди интересных продуктов следует отметить, в частности, сульфонилгалогениды и сульфинилгалогениды. Среди галогенидов можно назвать бромид, относительно неустойчивый, хлорид и фторид.
Способы получения указанных соединений являются обычно длительными и сложными или дают относительно низкие выходы или делают неизбежным использование особенно дорогостоящих растворителей или операционных условий.
Если более конкретно ссылаются на дифторметансульфокислоту, то ее синтез мало описан в литературе и требует применения относительно дорогостоящих растворителей и делает неизбежным образование солей в больших количествах.
Вот почему одной из задач настоящего изобретения является предложить способ синтеза кислот или производных кислот с гидрофторметиленсульфонильным или гидрофторметиленсульфинильным радикалом, который позволяет избежать использования нестабильных или сложных в применении дорогостоящих растворителей.
Другой задачей настоящего изобретения является предложить реакцию предыдущего типа, которая позволяет достичь хороших выходов и, в частности, высокие степени превращения (ВП, то есть выход желаемого продукта, полученный по отношению к израсходованному количеству исходного продукта), то есть больше 60%, предпочтительно больше 70%.
Другой задачей настоящего изобретения является предложить способ, имеющий многоцелевой характер, так чтобы он мог одинаково хорошо приводить к образованию солей кислот, кислот или галогенангидридов кислот.
Желательно также, чтобы можно было получить, по существу, кислоту, соответствующую сульфоновому радикалу.
Другой задачей настоящего изобретения является предложить способ, который дает возможность получения производных сульфинового типа.
Упомянутые задачи и другие задачи, которые проявятся впоследствии, достигнуты при помощи способа синтеза производных с гидрофторметансульфонильным или гидрофторметансульфинильным радикалом, включающего, по меньшей мере, следующие стадии:
а) стадию конденсации в растворителе меркаптида (то есть соли моноалкилсульфида), противокатион которого (то есть катион, обеспечивающий электронейтральность молекулы) является, предпочтительно, не основным (то есть катион, гидролиз которого при концентрациях 10-2 н. происходит только при рН, больших 10, предпочтительно 12) с соединением, содержащим атом углерода в гибридизации sp3, несущий водород, фтор, тяжелый галоген, выбранный из хлора, брома и иода, и электроноакцепторную группу, выбранную из фтора и электроноакцепторных групп, величина σр которых, по меньшей мере, равна 0,2, предпочтительно 0,4;
б) стадию окисления, преимущественно галогенирования, предпочтительно хлорирования или бромирования, в присутствии водной фазы;
при этом вышеупомянутый растворитель стадии а) выбран из растворителей, не смешивающихся с водой, из водных фаз и из двухфазных комбинаций растворителя, не смешивающегося с водой, и водной фазы, причем вышеупомянутые водные фазы содержат самое большее 1/3 по массе неводного растворителя, смешивающегося с водой; при этом соотношение между количеством эквивалентов меркаптида в эквивалентах и количеством воды в молях самое большее равно 50.
Когда используют водную фазу, содержащую растворитель, не смешивающийся с водой, предпочтительно, чтобы упомянутый растворитель не был бы чувствителен к основаниям, то есть чтобы он не разрушался в присутствии основания, в частности, по мере возможности, амидов и растворимых сложных эфиров следует избегать. Под выражением "смешивающийся с водой" следует понимать растворитель, смешивающийся с водой в любой пропорции. Растворители, не смешивающиеся с водой, выбраны, преимущественно, из растворителей, имеющих растворимость в воде по массе самое большее 10%, это означает, что вода может растворять самое большее 10% растворителя, не смешивающегося с водой, в нормальных условиях температуры и давления. В качестве растворителя, не смешивающегося с водой, можно использовать хлорированные ароматические производные и даже некоторые простые эфиры.
Предпочтительно также, чтобы растворимость вышеупомянутого не смешивающегося с водой растворителя в воде была бы самое большее 5 мас.%, предпочтительно 2 мас.%.
Среди растворителей, не смешивающихся с водой, можно, в частности, упомянуть ароматические производные, возможно, замещенные и, в частности, галогенароматические производные, такие как моно-, ди- или трихлорбензолы.
Анизол, как и другие простые эфиры фенола, способен представлять интерес. Однако активация кислородом или ароматическим циклом водорода алифатической природы может мешать на второй стадии и в таком случае надо будет удалить растворитель перед вышеупомянутой стадией галогенирования.
Однако согласно настоящему изобретению предпочтительно использовать в качестве растворителя водную фазу, содержащую немного или, предпочтительно, не содержащую смешивающегося с водой органического растворителя, но которая может содержать растворенные соли и, в частности, водорастворимые основания.
Важным пунктом настоящего изобретения является то, что для достижения максимального выхода очень предпочтительно использовать небольшое количество воды. Таким образом, предпочтительно, чтобы соотношение между количеством меркаптида, выраженным в эквивалентах, и количеством воды, выраженным в молях, было бы самое большее равно 30, преимущественно 20.
Количество меркаптида выражают в эквивалентах для того, чтобы принять во внимание случай, в котором будут использовать соединения, содержащие две сульфидные функциональные группы или две меркаптидные функциональные группы. Можно даже иметь ввиду, хотя это, вероятно, мало интересно с экономической точки зрения, использование соединений с несколькими тиольными группами. Согласно настоящему изобретению, предпочтительно, чтобы количество воды было бы достаточно большим для того, чтобы образовать значительную фазу. Таким образом, соотношение между количеством алкилсульфида в эквивалентах и количеством воды (в основной фазе или в основных фазах), выраженное в молях, должно бы быть по меньшей мере равно 0,5, преимущественно 1, предпочтительно 1,5.
Согласно настоящему изобретению, предпочтительно, чтобы вышеупомянутые водные фазы содержали самое большее одну четверть по массе неводного растворителя, предпочтительно самое большее десятую часть.
Равным образом, предпочтительно, чтобы молярное отношение [H2O]/([H2O]+[растворитель, смешивающийся с водой] было бы по меньшей мере равно 0,9, преимущественно 0,95. Наконец, предпочтительно ограничить концентрацию основания в водной фазе 0,5 эквивалента на кг водной фазы.
Следует отметить, что катионный меркаптид, который представляет собой один из субстратов стадии а), может быть получен in situ воздействием сульфида R-SH на основание, более сильное, чем R-S-.
Ограничение на концентрацию основания и, в частности, ОН- нацелено только на избыток основания и, следовательно, не принимает в расчет количество основания, израсходованное для получения меркаптида.
Меркаптид может быть записан в форме общей формулы R-S-M, где М соответствует металлу или катиону, который будучи ассоциирован с анионом ОН- образует сильное основание, то есть основание, ассоциированная кислота которого имеет рКа, по меньшей мере равное 10, преимущественно 12, предпочтительно 14.
Настоящее изобретение может в некоторых случаях, особенно, когда имеется органическая фаза, содержащая органический растворитель, не смешивающийся с водой, включать в себя агент межфазного переноса, упомянутые агенты хорошо известны специалисту и могут быть выбраны, в частности, среди ониевых соединений и среди иниевых соединений, среди простых краун-эфиров или простых криптандных эфиров, таких как TDA1(N[CH2-CH2-O-CH2-CH2]3N). Согласно настоящему изобретению предпочтительно работать с небольшим количеством (или избытком по отношению к количеству, необходимому для нейтрализации тиола в меркаптид) основания в водной фазе, причем упомянутое количество, преимущественно, по меньшей мере равно 5%, предпочтительно 10%, от количества вышеупомянутого меркаптида (R-S-M).
Тем не менее, предпочтительно, чтобы водная среда стадии а) содержала основание в количестве, самое большее равном однократному количеству вышеупомянутого меркаптида, предпочтительно, самое большее 50%, наиболее предпочтительно, самое большее 30%.
Согласно настоящему изобретению было показано, что желательно использовать сульфиды, образуемые алкилом, который был бы третичным или бензильного, или аллильного типа.
Данная активация углерода, несущего серу, позволяет облегчить разрыв связи углерод-сера, который осуществляется на стадии б). Однако, так как аллильный радикал способен давать реакции полимеризации и затрудняющие паразитные реакции, предпочтительно ограничиться алкильными производными третичного типа или бензильного типа.
Можно также выразить ограничение для смешивающегося с водой полярного органического растворителя, указав, что молярное соотношение между количеством возможного смешивающегося с водой полярного растворителя, выраженным в молях, и суммарным количеством, выраженным в эквивалентах, сокатионов сульфида и возможного основания самое большее равно 1, предпочтительно, самое большее равно 1,5, наиболее предпочтительно, 1/10.
Среди соединений, которые интересно синтезировать, можно назвать соединения с гидрофторметиленовыми радикалами формул I и IV'
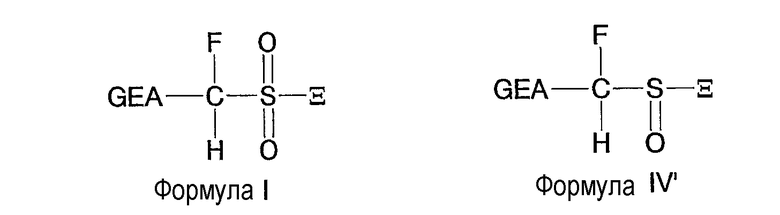
В данной формуле GEA представляет собой электроноакцепторную группу, выбранную из фтора и электроноакцепторных групп, величина σр (постоянная Гаммета) которых, по меньшей мере, равна 0,2, предпочтительно 0,4, где Ξ представляет собой либо галоген, преимущественно выбранный из хлора и брома, либо кислород, сам по себе или как носитель водорода, либо отрицательный заряд.
Реакция стадии может быть представлена следующим образом:

В формулах, приведенных выше, R обозначает алкил в этимологическом значении термина, то есть спирт, у которого удалена группа ОН.
Реакция галогенирования, которая представляет собой предпочтительный способ осуществления стадии б), может быть схематически представлена одной или несколькими из реакций, приведенных ниже:

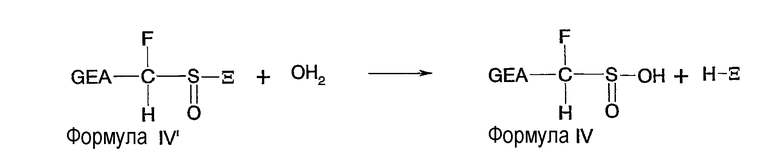
В упомянутой реакции констатируют, что галоген, обозначенный здесь Ξ2, окисляет серу, высвобождает алкил в форме алкилгалогенида R- Ξ и высвобождает три молекулы кислоты Н-Ξ. Данная реакция приводит к сульфиновому производному. Упомянутое сульфиновое производное, фигурирующее в данном уравнении, представляет собой саму сульфиновую кислоту. С одной стороны, можно выделить промежуточное производное IV', которое может представлять собой ценный реактив, и, с другой стороны, реакция не прекращается на данной стадии за исключением случая, когда ограничивают количество галогена, потому что сульфиновая кислота окисляется в сульфоновые производные; упомянутое производное может представлять собой либо сульфонилгалогенид согласно следующей реакции:
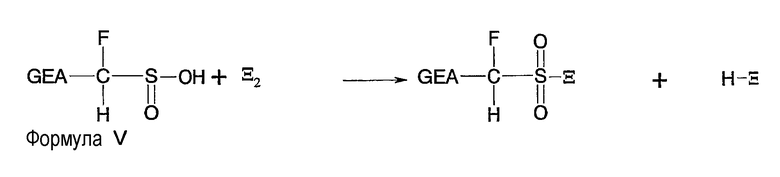
или, сообразно операционным условиям, она может приводить к сульфоновой кислоте или к ее солям и это согласно реакции, приведенной ниже:

Согласно настоящему изобретению может быть показано, что можно выбирать операционные условия для того, чтобы оптимизировать реакцию, либо в направлении образования сульфонилгалогенида, либо в направлении образования сульфоновой кислоты или ее солей.
Таким образом, когда хотят получить галогенангидрид кислоты, желательно, чтобы стадия б) проводилась в присутствии диссоциированной соли, растворенной в водной фазе, преимущественно, в количестве, достаточном для того, чтобы достичь и/или превзойти концентрацию 1 н., предпочтительно 2 н. (по аниону), преимущественно, анион представляет собой галогенид, предпочтительно галогенид, соответствующий галогенангидриду кислоты, который желают получить. Это, в частности, так, когда желаемый галогенангидрид кислоты представляет собой хлорангидрид кислоты и сульфонилхорид. Когда используют галогенид с атомным номером, большим атомного номера используемого галогена, разумеется, в качестве сульфонилгалогенида получают сульфонилгалогенид, соответствующий галогениду с самым большим номером, присутствующему в среде.
Другой характеристикой, способствующей образованию галогенангидрида кислоты, является поддерживание реакционной среды при рН, находящемся в интервале, изменяющемся от 4 до 9, предпочтительно от 5 до 8. Упомянутые два операционных условия не являются антагонистическими, можно их согласовать и таким образом получить хороший результат, используя солевой раствор с рН, изменяющимся в интервале от 4 до 9.
Предпочтительно, чтобы солевой раствор, точно определенный выше, представлял бы собой раствор галогенида щелочного металла (бромида и, предпочтительно, хлорида, но не иодида) с концентраций галогенида по меньшей мере 1 н., предпочтительно по меньшей мере 2 н.
Если хотят привилегизировать образование сульфоновой кислоты, тогда предпочтительно сместиться в кислые области рН, то есть рН, самое большее равные 2, предпочтительно, самое большее равные 1, предпочтительно, в окрестностях 0, и избежать осуществления хлорирования или гидролиза в солевой среде. Таким образом следует избегать содержания соли в среде больше 1 н. Желательно также для того, чтобы понизить содержание соли, отделить водную фазу от фазы сульфида, который образуется обычно во время стадии а). Когда на данной стадии сульфид не образуется, тогда желательно осуществить экстракцию в системе жидкость-жидкость или жидкость-твердое вещество для того, чтобы выделить сульфид, испарить растворитель и затем обработать фазу сульфида в водной фазе таким образом, чтобы осуществить разрыв связи между атомом серы и атомом углерода алкильного радикала, связанного с серой.
Одним из преимуществ настоящего изобретения является возможность осуществления синтеза галогенида (бромида и преимущественно хлорида) в одну стадию без замены среды, осуществляя реакцию в концентрированной водной среде на стадии а) и вновь возвращаясь к водной среде после возможного удаления растворителей, смешивающихся или не смешивающихся с водой, и осуществляя разрыв связи с образованием сульфинильной или сульфонильной группы, как описано на стадии б).
Температура реакции находится, преимущественно, в интервале от 50 до 110°С, предпочтительно от 60 до 90°С.
Давление является относительно высоким в связи с тем, что соединения, содержащие атом углерода в гибридизации sp3, несущий водород, фтор и тяжелый галоген, часто являются летучими, как наблюдается в случае, когда GEA представляет собой фтор, и что вышеупомянутое соединение и соединение, используемое в качестве хладоагента под названием R-22 (то есть хлордифторметан) являются очень летучими, что приводит к высокому давлению для того, чтобы поддерживать минимум вышеупомянутых соединений в жидкой фазе и, особенно, в водной фазе.
Согласно предпочтительной форме изобретения электроноакцепторная группа, такая как электроноакцепторная группа, которая обозначена GEA в предыдущих уравнениях, представляет собой высокофторированную группу, предпочтительно, общее число атомов углерода в GEA (электроноакцепторная группа), более специфически Rf, находится в интервале от 1 до 15, предпочтительно от 1 до 10.
Таким образом, электроноакцепторная группа выбрана, предпочтительно, из фтора и групп Rf; под Rf подразумевают радикал формулы:
GEA'-(CX2)p-
- где Х, одинаковые или разные, обозначают хлор, фтор или радикал формулы CnF2n+1 с целым n, самое большее равным 5, предпочтительно 2, при условии, что по меньшей мере один из Х должен представлять собой фтор, который, предпочтительно, несет атом углерода, связанный с серой ;
- где р представляет собой целое число, самое большее равное 2;
- где GEA' обозначает электроноакцепторную группу (то есть σр больше нуля, преимущественно 0,1, предпочтительно 0,2), возможные функциональные группы которой являются инертными в условиях реакции, предпочтительно, фтор или перфторированный остаток формулы CnF2n+1 с целым n, самое большее равным 8, преимущественно 5.
Так же, как уже было упомянуто, одним из предпочтительных способов осуществления изобретения является способ, который соответствует случаю, в котором электроноакцепторная группа представляет собой фтор, что означает, что соединение представляет собой R-22, то есть хлордифторметан.
На первой стадии, стадии а), желательно, чтобы было минимальное количество воды, и упомянутый минимум может быть определен следующим образом. Соотношение между количеством воды, выраженным в молях, и катионом, точнее, суммарным количеством присутствующих катионов, выраженным в эквивалентах, по меньшей мере равно 4, преимущественно 6, предпочтительно 8, во избежание того, чтобы среда не была бы слишком полярной и ограничивала растворимость субстрата, содержащего атом углерода в гибридизации sp3, несущий водород, фтор и тяжелый водород.
Преимущественно, катион или катионы, присутствующие в водной фазе, представляют собой одновалентные катионы. Предпочтительно, чтобы упомянутые катионы были выбраны из четвертичных фосфониевых катионов, четвертичных аммониевых катионов и катионов щелочных металлов, и, наиболее предпочтительно, среди последних из упомянутых, катионов, соответствующих натрию и соответствующих калию.
Для того чтобы получить удовлетворительную кинетику, предпочтительно, чтобы температура на стадии а) была бы по меньшей мере равна 80°С.
В ходе реакции образующийся галогенид RΞ выделяют, затем подвергают воздействию сульфида щелочного металла для того, чтобы вновь получить исходный продукт, а именно смешанный сульфид алкила и катиона.
Следующие примеры, не носящие ограничительного характера, иллюстрируют изобретение.
Пример 1 - Синтез дифторметилбензилсульфида
Один эквивалент гидроксида натрия в виде 40%-ного, по массе, раствора в воде смешивают с одним эквивалентом бензилмеркаптана с R-22 (1,1 молярного эквивалента) при 60°С в течение 1 ч. Опыты проводят в реакторе объемом 500 мл из хастеллоя при давлении, самостоятельно устанавливающемся при 60°С. Давление составляет 3,5 бар. В двух опытах, осуществленных в одинаковых условиях, при помощи количественного анализа методом ЯМР на изотопе 19F получают химический выход 75%.
Пример 2 - Изменение различных параметров синтеза дифторметилбензилсульфида исходя из бензилмеркаптана
Вновь был использован операционный способ, описанный перед этим, изменяя продолжительность и постепенно вводя большой избыток R-22 (хлордифторметан). Реакцию осуществляют при атмосферном давлении в течение промежутка времени 4 ч.
Детали операционных условий, а также различные выходы указаны в таблице, следующей ниже. Напомним, что СП обозначает степень превращения. Это есть соотношение между количеством рассматриваемого субстрата, которое исчезло в ходе реакции, и исходным количеством. Здесь выход вычислен по отношению к первоначально взятому бензилмеркаптану. ВР представляет собой выход реакции, то есть количество желаемого продукта, отнесенное к количеству рассматриваемого исходного субстрата, и ВП представляет собой выход превращения, то есть количество полученного желаемого продукта, разделенное на количество исчезнувшего рассматриваемого субстрата.
Следующая таблица резюмирует различные проведенные опыты.
экв, моль
5% мол.
экв, моль
(°С)
БМ
ДФБС
ДФБС
ченный
30%-ный р-р
30%-ный р-р
30%-ный р-р
30%-ный р-р
30%-ный р-р
30%-ный р-р
50 %
30%-ный р-р
30%
В таблице: БМ - обозначает бензилтиол, то есть бензилмеркаптан;
ДФБС обозначает дифторметилбензилсульфид (АМФ - обозначает агент межфазного переноса).
Пример 3 - Сравнительный пример - Роль воды
Условия опыта 2к были воспроизведены, значительно увеличив количество воды, так что имелось 5 молей бензилмеркаптана на кг воды, присутствующей в фазе. Полученный результат показывает сильное понижение выхода, а именно выход порядка 15%.
Пример 4 - Опыт по хлорированию
В реактор загружают 75 г воды, затем добавляют 26,1 г дифторметилбензилсульфида.
Реакционная среда бесцветная, двухфазная. Смесь охлаждают до 10°С и в массу медленно вводят хлор (32 г).
Чтобы поддерживать температуру 10°С, несмотря на очень сильную экзотермичность, камеру для поддержания температуры с двойными стенками настраивают на -5°С.
Когда выделение тепла прекращается и реакционная среда начинает желтеть, введение хлора прерывают.
Хлор вводят в течение 3 часов (точно 31, 6 г).
По окончании 3 часов дают реакционной среде возвратиться к температуре окружающей среды, осуществляют продувку азотом и прекращают перемешивание. Две фазы легко отстаиваются. Водная фаза - бесцветная и прозрачная. Органическая фаза - желтая, прозрачная.
Органическую фазу сушат над MgSO4 и фильтруют через стеклянный фильтр.
Выделяют m=37,6 г жидкой фазы, анализ которой методом газовой хроматографии показывает химический выход дифторметансульфонилхлорида 82%.
После перегонки получают 14,3 г дифторметансульфонилхлорида, имеющего степень чистоты больше 99% (температура кипения: 66°С при 300 мбар).
Настоящее изобретение относится к способу получения соединений, содержащих гидрофторметиленсульфонильный радикал, включающему;
а) стадию конденсации в растворителе меркаптида R-S-M, где R - третичный алкил или бензил, М - щелочной металл, с соединением, содержащим атом углерода в гибридизации sp3, несущим водород, фтор, тяжелый галоген, выбранный из хлора, брома и иода, и электроноакцепторную группу, выбранную из фтора или Rf;
б) стадию окисления соединения, полученного на стадии а) путем галогенирования, предпочтительно хлорирования или бромирования, в присутствии водной фазы. Более конкретно настоящее изобретение позволяет получить производные дифторметансульфиновой или дифторметансульфоновой кислоты. Настоящий способ позволяет избежать использования нестабильных или сложных в применении дорогостоящих растворителей. 10 з.п. ф-лы, 1 табл.
а) стадию конденсации в растворителе меркаптида R-S-M, где R-третичный алкил или бензил, М- щелочной металл, с соединением, содержащим атом углерода в гибридизации sp3, несущим водород, фтор, тяжелый галоген, выбранный из хлора, брома и иода, и электроноакцепторную группу, выбранную из фтора или Rf; где Rf означает радикал формулы
GEA'-(CX2)P,
где X, одинаковые или разные, обозначают хлор, фтор или радикал формулы CnF2n+1 с целым n, самое большее равным 5, предпочтительно, 2, при условии, что по меньшей мере один из Х должен представлять собой фтор, который, предпочтительно, несет атом углерода, связанный с серой;
где р представляет собой целое число, самое большее равное 2;
где GEA' обозначает электроноакцепторную группу, выбранную из фтора или перфторированного остатка формулы СnF2n+1 где n, самое большее, равно 8, преимущественно, 5;
б) стадию окисления путем галогенирования, предпочтительно, хлорирования или бромирования, в присутствии водной фазы;
при этом вышеупомянутый растворитель стадии а) выбран из растворителей, не смешивающихся с водой, из водных фаз и из двухфазных комбинаций растворителя, не смешивающегося с водой, и водной фазы, причем вышеупомянутые водные фазы содержат, самое большее, 1/3, по массе, неводного растворителя, смешивающегося с водой; при этом соотношение между количеством, выраженном в эквивалентах, алкилсульфида и количеством, выраженном в молях, воды, самое большее, равно 50, при этом вышеупомянутая водная среда стадии а) дополнительно имеет в своем составе сильное основание с рКа ассоциированной кислоты по меньшей мере равным 10, преимущественно, 12, предпочтительно, 14.
R представляет собой либо третичный алкил, либо аралкил бензильного типа, а
Ξ представляет собой галоген, предпочтительно хлор и бром, используют для того, чтобы вновь получить алкилсульфид.
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФОХЛОРИДОВ | 0 |
|
SU358313A1 |
| СПОСОБ ВВЕДЕНИЯ ЗАМЕЩЕННОЙ ДИФТОРМЕТИЛЬНОЙ ГРУППЫ | 1997 |
|
RU2192414C2 |
| РЕАКТИВ И СПОСОБ ДЛЯ ВВЕДЕНИЯ ЗАМЕЩЕННОЙ ДИФТОРМЕТИЛЬНОЙ ГРУППЫ В СОЕДИНЕНИЯ, ИМЕЮЩИЕ ПО МЕНЬШЕЙ МЕРЕ ОДНУ ЭЛЕКТРОФИЛЬНУЮ ФУНКЦИЮ | 1996 |
|
RU2204545C2 |
Авторы
Даты
2009-02-20—Публикация
2003-06-24—Подача