Область техники
Данное изобретение относится к лекарственному средству и пищевому продукту или напитку для улучшения функций поджелудочной железы, которые содержат 3-О-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол.
Уровень техники
Известно, что 4-метил-эргост-7-ен-3-ол представляет собой вещество, присутствующее в растениях (непатентный документ 1). Однако, что касается предшествующих знаний в данной области техники, то существуют только литературные данные о биосинтетической системе лофенола (одного из стереоизомеров 4-метил-холест-7-ен-3-ола), имеющего структуру, сходную с вышеупомянутым соединением (непатентный документ 2), а об использовании этих соединений, имеющих скелетную структуру лофенола, включая 4-метил-эргост-7-ен-3-ол, не известно вообще ничего.
Род Aloe семейства Liliaceae (лилейные) представляет собой группу растений, включающую в себя алоэ вера (Aloe barbadensis Miller), алоэ древовидное (Aloe arborescens Miller var. natalensis Berger) и так далее, о которых эмпирически известно, что они обладают разнообразными эффектами. Предшествующие знания в данной области техники, касающиеся растений рода Aloe, включают в себя данные о иммуномодулирующих полисахаридах (патентный документ 1); агентах, облегчающих состояние иммунодепрессии, содержащих бутанольную фракцию экстракта алоэ или алоин (патентный документ 2); агентах, подавляющих синтез белков семейства HSP60, содержащих производные алоина (патентные документы 3-5); белках, имеющих лектиновую активность и происходящих из кожицы листа алоэ (патентный документ 6), использовании для улучшения уровня глюкозы в крови (непатентные документы 3-7, патентные документы 7-10) и так далее.
Поджелудочная железа представляет собой орган, образованный островками ткани эндокринной железы (островки Лангерганса) и тканями экзокринной железы, секретирующими пищеварительные ферменты. В островках присутствуют β-клетки, α-клетки, δ-клетки, полипептидные клетки поджелудочной железы и так далее, которые существенно влияют на контроль уровня глюкозы в крови и метаболизм. Среди упомянутых β-клетки играют особенно важную роль как клетки, продуцирующие инсулин.
Сахарный диабет - это часто встречающееся метаболическое заболевание, выявленное у 10% взрослых японцев. По эпидемиологическим данным о дисфункции β-клеток поджелудочной железы, которая рассматривается как одна из причин сахарного диабета, при том, что дисфункция β-клеток, несомненно, наблюдается у индивидов с гипергликемией пограничного типа, среди индивидов, демонстрирующих нормальную переносимость глюкозы, имеются таковые с отчетливо пониженной до уровня 30% функцией β-клеток. Далее, считается, что у взрослых людей средний уровень социальной жизни в современной Японии очень часто в большей или меньшей степени вызывает резистентность к инсулину; полагают, что, как и у людей, страдающих инсулиновой резистентностью, среди тех, у кого нет дисфункции β-клеток, уровень глюкозы в крови не повышен, а среди тех, кто страдает дисфункцией β-клеток, уровень глюкозы повышен с соответствующего нормальной переносимости глюкозы до уровня, соответствующего гипергликемии пограничного типа (непатентный документ 8).
В настоящее время, несмотря на то, что при нарушениях функций поджелудочной железы используются терапевтические методы, стимулирующие спонтанное восстановление функции поджелудочной железы и основанные на устранении вызывающих их патологических состояний или факторов, какие-либо терапевтические способы или агенты для позитивного восстановления функций уже пораженной поджелудочной железы пока не использовались, поэтому в данной клинической области существует потребность в агентах, оказывающих защитное действие на клетки поджелудочной железы, или агентах, улучшающих состояние поврежденных клеток поджелудочной железы.
Нарушение функции поджелудочной железы означает патологическое состояние, при котором функции эндокринной или экзокринной желез поджелудочной железы понижены или ненормально повышены.
Что касается предшествующих данных об средствах, применяемых для лечения нарушений функции поджелудочной железы, то это средства, содержащие нейротропные факторы, такие как нейротропный фактор мозгового происхождения (BDNF), в качестве активного ингредиента (патентный документ 11); содержащие производные глицерина в качестве активного ингредиента (патентный документ 12); средства, улучшающие функцию поджелудочной железы и содержащие белки бетацеллюлины или их аналоги, появляющиеся в результате мутации (патентный документ 13), и так далее. В настоящее время полагают, что BDNF вместе с другими медиаторами выделяется из центральных окончаний небольших нейронов DRG при воспалении или повреждении нерва и вовлекается в запуск передачи болевого сигнала через фосфорилирование тирозина рецепторов N-метил-D-аспартата (NMDA) в клетках дорзального рога (непатентный документ 9), и, таким образом, в настоящее время считается имеющим ограниченное применение.
Далее, производные глицерина, описанные в патентном документе 12, представляют собой соединения, описанные в патентном документе 14, и являются агентами, обладающими активностью антитромбоцитарного активирующего фактора (PAF) при терапевтическом или профилактическом лечении генерализованного тромбогеморрагического синдрома (DIC), шока, аллергии, острого панкреатита, спазмов сосудов головного мозга при субарахноидальном кровоизлиянии и так далее; также обнаружено, что они обладают предупреждающим органопатию, лечебным и улучшающим эффектами в предупреждении, лечении и улучшении органопатии, вызванной сохранением органа в условиях ишемии; нарушениями кровотока, вызванными посттрансплантационной реперфузией крови или хирургическим вмешательством, и так далее. Однако трудно признать эти агенты пригодными для лечения хронических заболеваний поджелудочной железы без таких симптомов.
Далее, агенты, улучшающие функцию поджелудочной железы и содержащие белки бетацеллюлины или аналоги, описанные в патентном документе 13, также обладают действием на недифференцированные стволовые клетки и, таким образом, запускают их дифференцировку в β-клетки поджелудочной железы, продуцирующие инсулин, и действием, индуцирующим дифференцировку недифференцированных стволовых клеток в другие клетки поджелудочной железы, такие как F-клетки, продуцирующие панкреатические полипептиды, и такого эффекта невозможно ожидать в условиях, когда незрелые клетки исчерпаны. Кроме того, хотя мРНК этих белков обнаруживаются в различных органах помимо мозга, например в печени, почках, поджелудочной железе и т.д., детали их функционирования почти совсем не установлены и, следовательно, нельзя сказать, что они могут быть в настоящее время использованы для клинического использования.
Кроме того, в патентном документе 15 описано, что соединения, имеющие скелетную структуру ланостана или скелетную структуру 3,4-секоланостана, обладают активностью, усиливающей действие инсулина. Эффект этих соединений состоит в усилении действия инсулина в регуляции дифференцировки адипоцитов, а их эффект на заболевания поджелудочной железы остается неизвестным.
Что касается гликозидов, имеющих скелетную структуру происходящего из растений лофенола, сообщается, что 3-O-β-D-глюкопиранозил-4-метил-стигмаст-7-ен-3-ол содержится в брионии (переступень, Bryonia alba), растении семейства тыквенных (Cucurbitaceae) (непатентный документ 10). Однако, это - в целом несъедобное растение и полный синтез этого вещества не описан.
[Патентный документ 1] Международная патентная заявка, не прошедшая экспертизу, на японском языке (Kohyo) No. 2001-520019
[Патентный документ 2] Опубликованный патент Японии (Kokai) No. 08-208495
[Патентный документ 3] Опубликованный патент Японии No. 10-120576
[Патентный документ 4] Опубликованный патент Японии No. 10-045604
[Патентный документ 5] Опубликованный патент Японии No. 10-036271
[Патентный документ 6] Опубликованный патент Японии No. 09-059298
[Патентный документ 7] Опубликованный патент Японии No. 60-214741
[Патентный документ 8] Опубликованный патент Японии No. 2003-286185
[Патентный документ 9] Патент США No. 4598069
[Патентный документ 10] Публикация патентной заявки США No. 2003/0207818
[Патентный документ 11] Международная публикация No. WO 00/62796
[Патентный документ 12] Опубликованный патент Японии No. 07-285866
[Патентный документ 13] Опубликованный патент Японии No. 09-188630
[Патентный документ 14] Опубликованный патент Японии No. 02-131467
[Патентный документ 15] Опубликованный патент Японии No. 10-330266
[Непатентный документ 1] Chem. Pharm. Bull., pp.624-626, 1993
[Непатентный документ 2] Biochimica Biophysica Acta, pp.63-88, 2000
[Непатентный документ 3] Phytomedicine, Vol.3, pp.245-248, 1996
[Непатентный документ 4] Phytotherapy Research, Vol.15, pp.157-161, 2001
[Непатентный документ 5] Phytotherapy Research, Vol.7, pp.37-42, 1993
[Непатентный документ 6] Nippon Rinsho, No. 748, Vol.1, pp.615-617, 1999
[Непатентный документ 7] Nippon Rinsho, No. 808, Vol.2, pp.405-409, 2002
[Непатентный документ 8] "Insulin Resistance," Diabetes Mellitus current library, Bunkodo, April 17 2004
[Непатентный документ 9] Brain Res Rev, Vol.40, pp.240-249, 2002
[Непатентный документ 10] Химия природных соединений, т.3, СССР, 1977
Раскрытие изобретения
Задача данного изобретения состоит в том, чтобы предложить лекарственное средство и пищевой продукт или напиток, пригодные для улучшения функции поджелудочной железы, которые не содержат неблагоприятных ингредиентов для лекарственного средства, пищевого продукта или напитка, из сырья, которое с экспериментальной точки зрения безопасно для изготовления пищевых продуктов и легко доступно.
Авторы данного изобретения провели тщательные исследования с целью решения вышеупомянутых задач изобретения. В результате обнаружено, что 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол, новый гликозид, выделенный и очищенный из мезофилла (чистая гелевая фракция) алоэ вера (Aloe barbadensis Miller), может безопасно употребляться в пищевой продукт и имеет активность, защищающую эндокринные клетки поджелудочной железы или улучшающую функции эндокринных клеток поджелудочной железы. Данное изобретение создано на основе вышеупомянутых фактов.
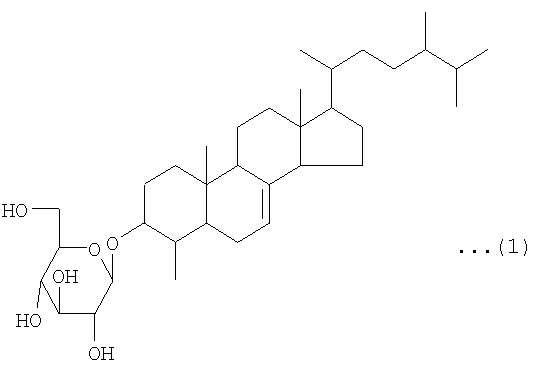
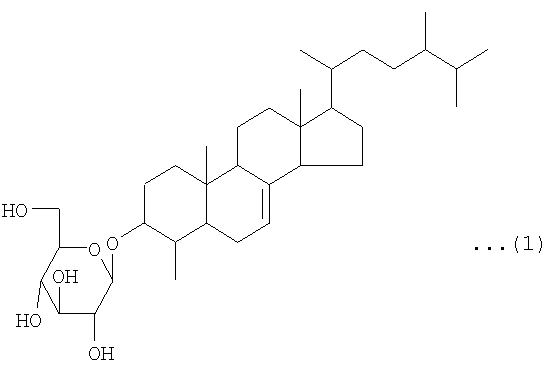
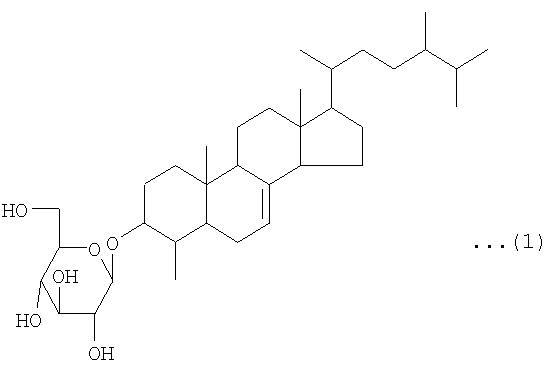
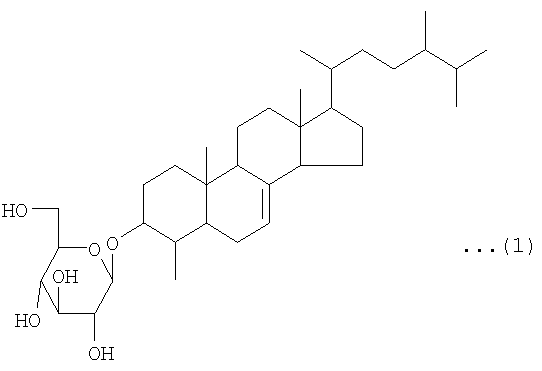
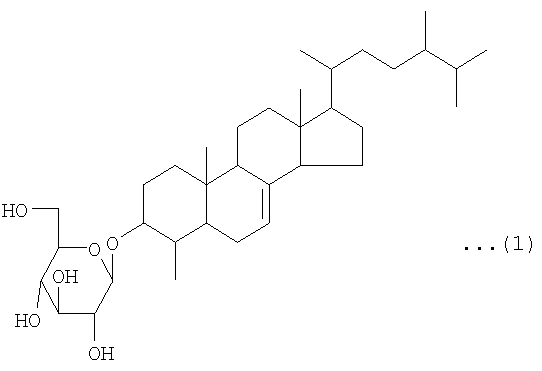
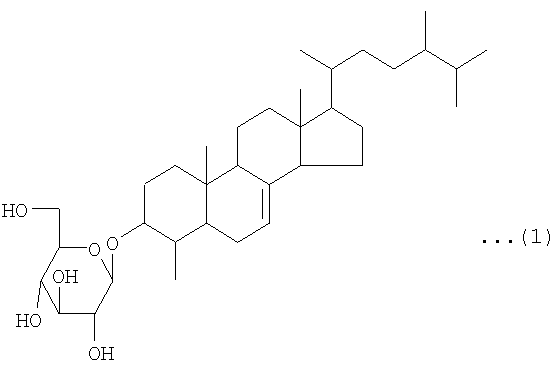
То есть, данное изобретение представляет лекарственное средство для улучшения функций поджелудочной железы, которое содержит соединение, представленное следующей химической формулой (1), в качестве активного ингредиента. В соответствии с предпочтительным вариантом реализации лекарственного средства по данному изобретению, улучшение функций поджелудочной железы состоит в защитном действии на эндокринные клетки поджелудочной железы или усилении функций эндокринных клеток поджелудочной железы:
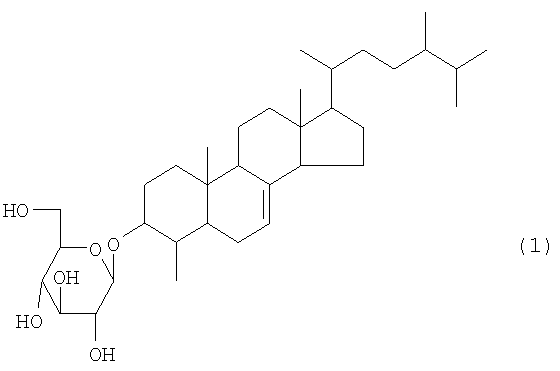
В соответствии с предпочтительным вариантом реализации лекарственное средство по данному изобретению содержит 0,001-10% вышеупомянутого соединения в расчете на сухую массу.
Данное изобретение также представляет лекарственное средство для улучшения функций поджелудочной железы, которое содержит экстракт растения семейства Liliaceae или его фракцию, содержащую в расчете на сухую массу 0,001-10% соединения, представленного вышеупомянутой химической формулой (1), в качестве активного ингредиента. В соответствии с предпочтительным вариантом реализации лекарственного средства по данному изобретению улучшение функций поджелудочной железы состоит в защитном действии на эндокринные клетки поджелудочной железы или улучшении функций эндокринных клеток поджелудочной железы.
Данное изобретение также представляет пищевой продукт или напиток для улучшения функций поджелудочной железы, которые содержат соединение, представленное вышеупомянутой химической формулой (1). В соответствии с предпочтительным вариантом реализации пищевого продукта или напитка по данному изобретению улучшение функций поджелудочной железы состоит в защитном действии на эндокринные клетки поджелудочной железы или улучшении функций эндокринных клеток поджелудочной железы.
Далее, в соответствии с предпочтительным вариантом реализации пищевой продукт или напиток содержит в расчете на сухую массу 0,0001-1% вышеупомянутого соединения.
Далее, данное изобретение представляет пищевой продукт или напиток для улучшения функций поджелудочной железы, который содержит экстракт растения семейства Liliaceae или его фракцию, содержащую в расчете на сухую массу 0,0001-1% соединения, представленного вышеупомянутой химической формулой (1). В соответствии с предпочтительным вариантом реализации пищевого продукта или напитка по данному изобретению улучшение функций поджелудочной железы состоит в защитном действии на эндокринные клетки поджелудочной железы или улучшении функций эндокринных клеток поджелудочной железы.
В соответствии с предпочтительным вариантом реализации пищевой продукт или напиток по данному изобретению снабжен указанием, что пищевой продукт или напиток используются для улучшения функций поджелудочной железы.
Данное изобретение также представляет применение соединения, представленного вышеупомянутой химической формулой (1), или композиции, содержащей его, в производстве лекарственного средства для улучшения функций поджелудочной железы. В соответствии с предпочтительным вариантом реализации использования данного изобретения улучшение функций поджелудочной железы состоит в защитном действии на эндокринные клетки поджелудочной железы или улучшении функций эндокринных клеток поджелудочной железы. Далее, в соответствии с предпочтительным вариантом применения данного изобретения вышеупомянутая композиция содержит экстракт растения семейства Liliaceae или его фракцию, которые в расчете на сухую массу содержат 0,001% вышеупомянутого соединения.
Данное изобретение также представляет способ защиты эндокринных клеток поджелудочной железы или улучшения функций клеток, который включает в себя введение соединения, представленного вышеупомянутой химической формулой (1), или композиции, содержащей его, субъекту, нуждающемуся в защите эндокринных клеток поджелудочной железы или улучшении клеточных функций. В соответствии с предпочтительным вариантом способа по данному изобретению улучшение функций поджелудочной железы состоит в защитном действии на эндокринные клетки поджелудочной железы или улучшении функций эндокринных клеток поджелудочной железы. Далее, в соответствии с предпочтительным вариантом реализации способа по данному изобретению вышеупомянутая композиция включает в себя экстракт растения семейства Liliaceae или его фракцию, которые в расчете на сухую массу содержат 0,001% вышеупомянутого соединения.
Краткое описание чертежей
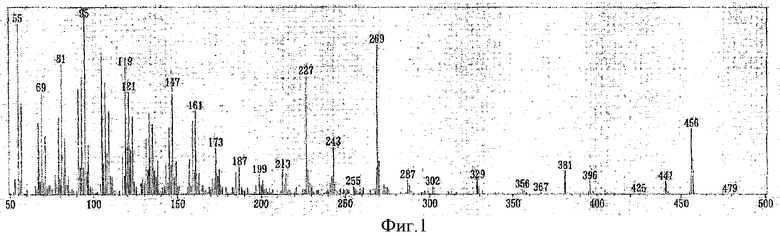
Фиг.1 показывает спектр газовой хроматографии - масс-спектрометрии (GC-MS) ацетилированного агликонового остатка гликозида по данному изобретению (фото для замены чертежа: полутоновое изображение показано на дисплее).
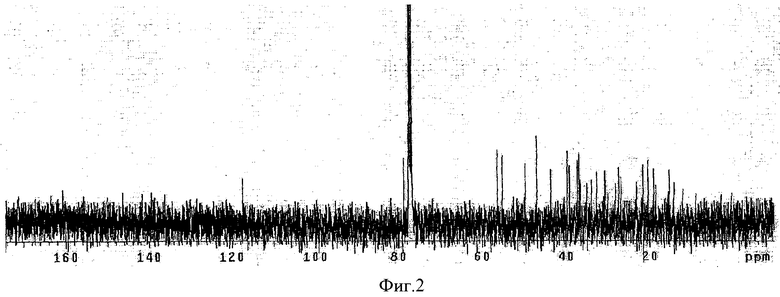
Фиг.2 показывает 13C-ЯМР диаграмму ацетилированного агликонового остатка гликозида по данному изобретению (фото для замены чертежа: полутоновое изображение показано на дисплее).
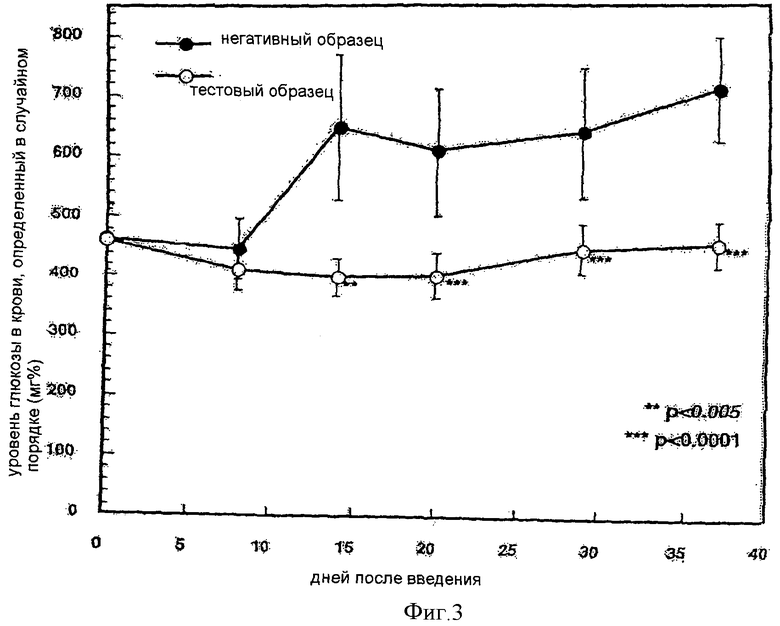
Фиг.3 показывает график изменений во времени выбранных в случайном порядке уровней глюкозы в крови у мышей, которым вводили соединение по данному изобретению.
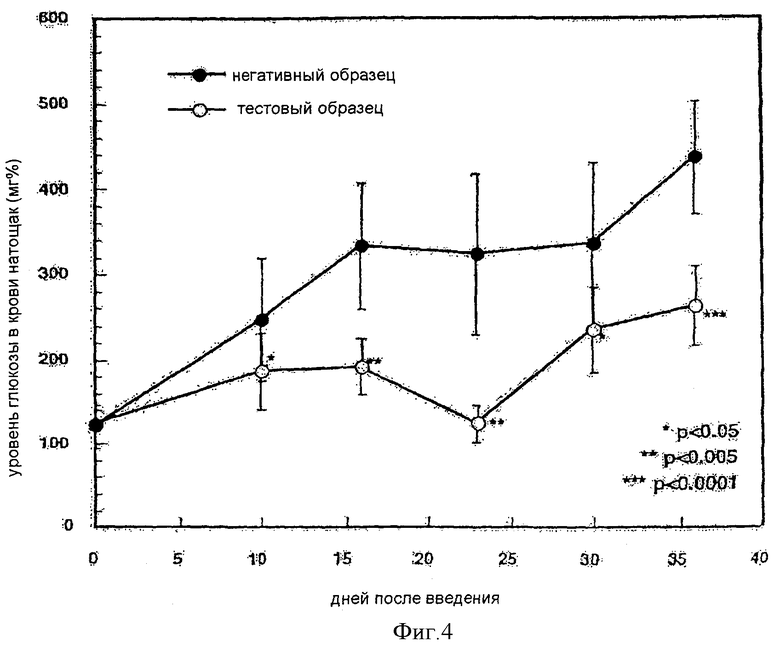
Фиг.4 показывает график изменений во времени уровней глюкозы в крови у мышей натощак, получивших соединение по данному изобретению.
Лучший способ реализации изобретения
Ниже предпочтительные варианты реализации данного изобретения будут описаны детально. Однако данное изобретение не ограничивается нижеследующими предпочтительными вариантами реализации и может быть легко модифицировано в рамках данного изобретения.
Соединение, используемое в качестве активного ингредиента лекарственного средства и пищевого продукта или напитка по данному изобретению (далее в данном документе упоминаемого как «соединение по данному изобретению»), представляет собой соединение, имеющее структуру, представленную вышеупомянутой химической формулой (1), то есть, 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол. То есть, соединение по данному изобретению имеет структуру, образованную дегидратированием и конденсацией с участием гидроксильной группы в 3-м положении 4-метил-эргост-7-ен-3-ола и гидроксильной группы в 1-м положении D-глюкозы.
Кроме того, композиция, использованная в качестве активного ингредиента лекарственного средства и пищевого продукта или напитка по данному изобретению (далее упоминаемая как «композиция по данному изобретению»), представляет собой экстракт растения семейства Liliaceae или его фракцию, содержащие в расчете на сухую массу 0,001% или более, предпочтительно - 0,01% или более в расчете на сухую массу, более предпочтительно - 0,1% или более в расчете на сухую массу вышеупомянутого соединения по данному изобретению при использовании в качестве активного ингредиента лекарственного средства, либо содержащие 0,0001% или более в расчете на сухую массу, предпочтительно - 0,001% или более в расчете на сухую массу, более предпочтительно - 0,1% или более в расчете на сухую массу вышеупомянутого соединения по данному изобретению при использовании в качестве активного ингредиента пищевого продукта или напитка.
Верхний предел содержания соединения по данному изобретению в композиции по данному изобретению точно не определен и может составлять, например, 50, 70 или 90% по массе.
Соединение по данному изобретению или композиция, содержащая таковое, могут быть получены, например, путем экстракции фракции, содержащей соединение по данному изобретению, из растения, принадлежащего к семейству Liliaceae и содержащего соединение по данному изобретению, его части или продукта его разрушения путем использования органического растворителя или горячей воды и концентрирования фракции.
Примеры вышеупомянутого растения, принадлежащего семейству Liliaceae, включают в себя растения рода Aloe или Allium. Примеры растений рода Aloe включают в себя Aloe barbadensis Miller, Aloe ferox Miller, Aloe africana Miller, Aloe arborescen* Miller var. natalensis Berger, Aloe spicata Baker и так далее. Хотя при производстве соединения по данному изобретению или композиции, содержащей таковое, может быть использовано вышеупомянутое растение целиком, предпочтительно использовать его мезофилл (чистую гелевую фракцию). Такое растение или его часть разрушают с использованием гомогенизатора или подобного ему устройства и таким образом переводят в жидкое состояние, а соединение по данному изобретению или композиция, содержащая таковое, экстрагируется из разрушенного продукта с использованием органического растворителя или горячей воды. Примеры органических растворителей включают в себя спирты, такие как метанол, этанол и бутанол и так далее; сложные эфиры, такие как метилацетат, этилацетат, пропилацетат и бутилацетат и так далее; кетоны, такие как ацетон и метилизобутилкетон и так далее; простые эфиры, такие как диэтиловый эфир и петролейный эфир и так далее; углеводороды, такие как гексан, циклогексан, толуол, бензол и так далее; галогенированные углеводороды, такие как четыреххлористый углерод, дихлорметан и хлороформ и так далее; гетероциклические соединения, такие как пиридин и так далее; гликоли, такие как этиленгликоль и так далее; многоатомные спирты, такие как полиэтиленгликоль и так далее; нитриловые растворители, такие как ацетонитрил и так далее, смеси этих растворителей и так далее. Кроме того, эти растворители могут быть безводными и водными. Среди таких растворителей смесь ацетат/бутанол (3:1) и смесь хлороформ/метанол (2:1) особенно предпочтительны.
Что касается способа экстракции, то может быть применен способ, используемый для обычной экстракции растительных компонентов. Обычно используется, например, способ кипячения с обратным холодильником 1-300 частей по массе органического растворителя с 1 частью свежего растения или высушенного растения с нагреванием до температуры кипения растворителя или ниже ее при перемешивании или встряхивании, или способ проведения экстракции с помощью ультразвука при комнатной температуре. Путем отделения нерастворимого материала от экстракционной жидкости с помощью пригодного для этого способа, такого как фильтрация или центрифугирование, может быть получен неочищенный экстракт.
Неочищенный экстракт может быть очищен с помощью хроматографии различных типов, таких как обычная или обращенно-фазная хроматография на колонке с силикагелем. Когда в качестве растворителя для элюции при хроматографии на колонке с силикагелем с обычной фазой используется градиент смеси хлороформ/метанол, соединение по данному изобретению элюируется при соотношении смеси хлороформ:метанол = около 5:1. Кроме того, когда в качестве растворителя для элюции при обращенно-фазной хроматографии на колонке с силикагелем используется градиент метанол/водная смесь, соединение по данному изобретению элюируется метанолом в концентрации около 95%.
Полученная фракция может быть затем очищена с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) или ей подобной.
Содержит ли соединение или композиция, содержащая таковое, полученная, как описано выше, соединение по данному изобретению, может быть подтверждено, например, способами, приведенными в Примерах, описанных ниже. Является ли соединение гликозидом, связанным с глюкозой в агликоновом остатке, и является ли агликоновый остаток 4-метил-эргост-7-ен-3-олом, может быть подтверждено с помощью, например, 13C-ЯМР или подобного.
Авторы данного изобретения ранее обнаружили, что 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол также обладает действием, улучшающим уровень глюкозы в крови, и 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол из алоэ вера очищали в Примере получения 1, упомянутом ниже, с использованием оценки эффекта улучшения уровня глюкозы в крови, показанного в Примере сравнения 1, в качестве показателя. Однако это соединение может быть также очищено с использованием в качестве показателя очистки эффекта улучшения функции поджелудочной железы, в частности защитного действия на эндокринные клетки поджелудочной железы или эффекта улучшения функции эндокринных клеток поджелудочной железы.
Соединение по данному изобретению может быть также получено путем конденсации D-глюкозы и 4-метил-эргост-7-ен-3-ола. 4-Метил-эргост-7-ен-3-ол может быть получен путем экстракции из растения и очистки. D-глюкоза и 4-метил-эргост-7-ен-3-ол могут быть конденсированы с помощью, например, комбинации способов, описанных в Jikken Kagaku Koza (Лекции по экспериментальной химии), 4th edition, vol. 26, 1992 (описано на с.272, с.297 и с.342). То есть, D-глюкоза полностью ацетилируется, а затем аномерное положение преобразуется в α-бромид. Затем 4-метил-эргост-7-ен-3-ол реагирует с α-бромидом в диэтиловый эфир, чтобы добиться β-гликозилирования, а затем ацетильная группа гидролизуется в смеси метилат натрия/метанол с получением заданного соединения.
Соединение по данному изобретению обладает действием, улучшающим функцию поджелудочной железы, в частности защитным действием на эндокринные клетки поджелудочной железы или действием, улучшающим функцию эндокринных клеток поджелудочной железы. Оно может быть использовано в качестве активного ингредиента лекарственного средства и пищевого продукта или напитка для улучшения функций поджелудочной железы, в частности, оказывая защитное действие на эндокринные клетки поджелудочной железы или улучшая функции эндокринных клеток поджелудочной. В данном изобретении защита эндокринных клеток поджелудочной железы означает защиту эндокринных клеток поджелудочной железы от денатурации вследствие различных причин или предупреждение снижения продукции инсулина, или предупреждение снижения способности продукции инсулина эндокринными клетками поджелудочной железы. Далее, улучшение функций эндокринных клеток поджелудочной железы означает усиление способности продукции инсулина эндокринными клетками поджелудочной железы, способность которых к продукции инсулина снижена. Денатурация эндокринных клеток поджелудочной железы, защитное действие на эндокринные клетки поджелудочной железы или улучшение функций эндокринных клеток поджелудочной железы можно оценить с помощью микроскопического наблюдения срезов ткани поджелудочной железы животного или измерением уровня инсулина в сыворотке.
Путем вышеупомянутых действий соединение по данному изобретению может предупреждать снижение способности эндокринных клеток поджелудочной железы продуцировать инсулин или усиливать способность продуцировать инсулин эндокринных клеток поджелудочной железы, в которых способность продуцировать инсулин снижена.
Что касается мышей линии db/db, использованных в примерах, упоминаемых ниже, известно, что развитие нарушений поджелудочной железы наблюдается у них с возрастом в пределах недели (Science, 153, 1127-1128, 1966). Хотя сообщалось, что введение этим мышам комбинации N-ацетил-L-цистеина, витамина C и витамина E как соединений, обладающих антиоксидантным действием, может частично предупреждать снижение числа β-клеток (Diabetes, 48, 2398-2406, 1999), доза одного только N-ацетил-L-цистеина составляет 100 г/60 кг, и следует ожидать, что требуется введение чрезвычайно больших доз. Напротив, в соответствии с данным изобретением можно ожидать, что защитное действие на эндокринные клетки поджелудочной железы или улучшение функции поджелудочной железы может быть достигнуто с использованием малых доз.
Лекарственное средство по данному изобретению может быть использовано как активный ингредиент агентов для профилактического лечения или терапевтического лечения заболеваний, вызываемых пониженной функцией эндокринных клеток поджелудочной железы, например нарушениями функции поджелудочной железы при остром панкреатите, хроническом панкреатите, сахарном диабете I типа и сахарном диабете II типа, пониженной функции поджелудочной железы, связанной со старческим снижением секреции инсулина и так далее. Кроме того, так как соединение по данному изобретению демонстрирует низкую токсичность, оно может быть использовано вместе с противоопухолевыми агентами при лечении рака поджелудочной железы. Предпочтительно, чтобы агент, используемый для улучшения состояния гипергликемии при заболеваниях, сопровождаемых сниженим способности к продукции инсулина, не входил в сферу лекарственного средства по данному изобретению.
Кроме того, поскольку кожица листа алоэ вера содержит барбалоин и алоэ-эмодин, обладающие слабительным действием, она обычно считается неприемлемой для пищи и напитков, у которых не предполагается слабительного действия. В то же время композиция по данному изобретению в соответствии с предпочтительным вариантом реализации может быть получена и фракционирована из мезофилла (чистая гелевая фракция) алоэ вера, который в пищевом отношении безопасен для потребления с эмпирической точки зрения и, следовательно, не содержит барбалоина и алоэ-эмодина, но содержит эффективное количество соединения по данному изобретению. Следовательно, композиция по данному изобретению также предпочтительна в качестве активного ингредиента лекарственного средства для оказания защитного действия на эндокринные клетки поджелудочной железы или улучшения функций эндокринных клеток поджелудочной железы.
Соединение или композиция по данному изобретению сами по себе могут быть использованы в качестве активного ингредиента лекарственного средства и пищевого продукта или напитка по данному изобретению. Кроме того, композиция по данному изобретению может представлять собой раствор, а также, после лиофилизации или высушивания распылением обычным образом, может храниться и использоваться в виде порошка.
В качестве лекарственного средства по данному изобретению соединение или композиция по данному изобретению или их комбинация с фармацевтически приемлемым носителем может вводиться млекопитающим, включая человека, перорально или парентерально. В составе лекарственного средства по данному изобретению соединение по данному изобретению может представлять собой фармацевтически приемлемую соль. Примеры фармацевтически приемлемых солей включают в себя как соли металлов (неорганические соли), так и органические соли, включающие в себя, например, таковые, перечисленные в "Remington's Pharmaceutical Sciences", 17th edition, p.1418, 1985. Конкретные примеры солей включают в себя, но не ограничиваются ими, неорганические соли, такие как гидрохлорид, сульфат, фосфат, дифосфат и гидробромат, и органические соли, такие как малат, малеат, фумарат, тартарат, сукцинат, цитрат, ацетат, лактат, метансульфонат, p-толуолсульфонат, памоат, салицилат и стеарат. Кроме того, соли могут представлять собой соли металлов, таких как натрий, калий, кальций, магний, алюминий и так далее, или соли аминокислот, таких как лизин и так далее. Кроме того, сольваты, такие как гидраты и так далее, вышеупомянутого соединения или его фармацевтически приемлемых солей также входят в сферу данного изобретения.
Фармацевтические формы лекарственного средства по данному изобретению конкретно не ограничены и могут быть подходящим образом подобраны в зависимости от терапевтической цели. Конкретные примеры этих форм включают в себя таблетку, пилюлю, порошок, раствор, суспензию, эмульсию, гранулы, капсулу, сироп, суппозиторий, инъекцию, мазь, пластырь, глазные капли, капли в нос и так далее. Для приготовления могут быть использованы обычно применяемые в обычных терапевтических и профилактических лекарственных средствах при заболеваниях внутренних органов, таких как поджелудочная железа, добавки фармацевтических носителей, такие как наполнители, связующие вещества, дезинтегрирующие агенты, смазывающие вещества, стабилизаторы, вкусовые агенты, разбавители, поверхностно-активные вещества, растворители для инъекций и так далее. Кроме того, постольку, поскольку эффект по данному изобретению не снижается, соединение или композиция по данному изобретению могут быть использованы в комбинации с другими лекарственными средствами, обладающими эффектом, улучшающим состояние при заболевании поджелудочной железы, или предупреждающим эффектом.
Хотя количество соединения или композиции по данному изобретению, содержащееся в лекарственном средстве по данному изобретению, точно не ограничено и может быть подходящим образом подобрано, это количество может составлять, например, 0,001-10% по массе, предпочтительно - 0,01-1% по массе, особенно предпочтительно - 0,05-1% по массе, имея в виду количество соединения по данному изобретению.
Кроме того, с помощью лекарственного средства по данному изобретению могут быть предупреждены различные заболевания, осложнения и так далее, возникающие вследствие гипофункции эндокринных клеток поджелудочной железы, а риски этих заболеваний, осложнений и так далее могут быть уменьшены.
Примеры таких разнообразных заболеваний и осложнений, вызываемых гипофункцией эндокринных клеток поджелудочной железы, включают в себя нервные заболевания, нефропатию, ретинопатию, катаракту, макроангиопатию, сахарный диабет и так далее.
Время введения агента или лекарственного средства по данному изобретению точно не ограничено и может быть подходящим образом подобрано в соответствии со способом лечения конкретного заболевания. Кроме того, путь введения предпочтительно определяется в зависимости от фармацевтической формы, возраста, пола и других характеристик пациента, тяжести симптомов у пациента и так далее.
Доза активного ингредиента в лекарственном средстве по данному изобретению подходящим образом подбирается в зависимости от режима введения, возраста и пола пациента, тяжести заболевания, других характеристик и так далее. Количество соединения по данному изобретению в качестве активного ингредиента обычно избирают в диапазоне предпочтительно 0,01-10 мг/кг/день, более предпочтительно - 0,1-1 мг/кг/день как пробная доза. Далее, когда используется композиция по данному изобретению, сухой вес композиции избирают в диапазоне, предпочтительно, 0,1-1000 мг/кг/день, более предпочтительно - 1-100 мг/кг/день, как пробное количество. В любом случае доза может быть введена один раз в день или несколько раз в виде отдельных порций.
Соединение или композиция по данному изобретению могут быть добавлены в пищевой продукт или напиток. Форма и свойства пищевого продукта или напитка конкретно не ограничиваются постольку, поскольку не разрушается активный ингредиент, и пищевой продукт пригоден к потреблению и может быть произведен обычным способом из сырья, обычно используемого для пищевого продукта и напитков, за исключением добавления вышеупомянутого активного ингредиента.
Количество соединения или композиции по данному изобретению, содержащихся в пищевом продукте или напитке по данному изобретению, конкретно не ограничено и может быть подобрано подходящим образом. Например, соединение или композиция по данному изобретению содержится в пищевом продукте или напитке в количестве 0,0001-1% по массе, предпочтительно - 0,001-1% по массе, особенно предпочтительно - 0,005-1% по массе, имея в виду количество соединения по данному изобретению.
Пищевой продукт или напиток по данному изобретению могут быть использованы для различных применений, использующих защитный эффект на эндокринные клетки поджелудочной железы или эффект улучшения функции эндокринных клеток поджелудочной железы. Например, они могут быть использованы в качестве пищевого продукта или напитка, пригодных для «тех, у кого понижена продукция инсулина», «тех, у кого понижена функция инсулина», «тех, кого беспокоит функционирование его поджелудочной железы», пищевой продукт или напиток пригодны для снижения или устранения факторов риска болезней, связанных со стилем жизни, таких как сахарный диабет, вызванных гипофункцией поджелудочной железы, и панкреатит, вызванный излишним потреблением алкоголя и стрессом.
Что касается пищевого продукта или напитка по данному изобретению, то выражение «защита эндокринных клеток поджелудочной железы или улучшение функций эндокринных клеток поджелудочной железы» означает улучшение или предупреждение различных нарушений здоровья вследствие гипофункции эндокринных клеток поджелудочной железы, а «защита функций островков Лангерганса», «улучшение функций островков Лангерганса», «защита функций β-клеток», «улучшение функций β-клеток», «усиление продукции инсулина», «предупреждение снижения продукции инсулина», «усиление активности инсулина», «предупреждение снижения активности инсулина» и так далее фигурируют в данном изобретении как термины, имеющие значение, сходное с вышеупомянутой «защитой эндокринных клеток поджелудочной железы или улучшением функций эндокринных клеток поджелудочной железы».
Кроме того, пищевой продукт или напиток по данному изобретению пригодны для профилактического лечения заболевания, возникающего вследствие гипофункции эндокринных клеток поджелудочной железы, например нарушений функции поджелудочной железы при остром панкреатите, хроническом панкреатите, сахарном диабете I типа и сахарном диабете II типа, гипофункции поджелудочной железы, связанной с сенильным снижением инсулина, и так далее. Кроме того, пищевой продукт или напиток по данному изобретению могут быть использованы для профилактического лечения различных заболеваний, осложнений и так далее, возникающих вследствие гипофункции эндокринных клеток поджелудочной железы, и могут снижать риски этих заболеваний, осложнений и так далее. Кроме того, поскольку соединение по данному изобретению демонстрирует низкую токсичность, пищевой продукт или напиток по данному изобретению также пригодны для пациентов, получающих противоопухолевые агенты при лечении рака поджелудочной железы.
Примеры таких разнообразных болезней и осложнений, возникающих вследствие гипофункции эндокринных клеток поджелудочной железы, включают в себя нервные заболевания, нефропатию, ретинопатию, катаракту, макроангиопатию, диабет и так далее.
Пищевой продукт или напиток по данному изобретению предпочтительно поставляются на рынок с прикрепленной к ним инструкцией о том, что пищевой продукт или напиток используются для защиты эндокринных клеток поджелудочной железы или улучшения функций эндокринных клеток поджелудочной железы, например, «пищевой продукт или напиток содержат соединение, обладающее защитным эффектом на эндокринные клетки поджелудочной железы или эффектом, улучшающим функцию эндокринных клеток поджелудочной железы», обозначенные как «для защиты эндокринных клеток поджелудочной железы или улучшения функций эндокринных клеток поджелудочной железы», «пищевой продукт или напиток, содержащие растительный экстракт, обозначенные как «для защиты эндокринных клеток поджелудочной железы или улучшения функций эндокринных клеток поджелудочной железы»», «пищевой продукт или напиток, содержащие экстракт алоэ вера, обозначенные «для защиты эндокринных клеток поджелудочной железы или улучшения функций эндокринных клеток поджелудочной железы»» и так далее.
Формулировка, использованная для таких инструкций, как упомянутые выше, не обязательно ограничена выражением «для защиты эндокринных клеток поджелудочной железы или улучшения функций эндокринных клеток поджелудочной железы», и какая-либо другая формулировка, обозначающая защитный эффект на эндокринные клетки поджелудочной железы или улучшение функций эндокринных клеток поджелудочной железы, несомненно входит в сферу данного изобретения. Что касается формулировки, например, возможны также указания, основанные на различных применениях, позволяющие потребителю распознать защитный эффект на эндокринные клетки поджелудочной железы или эффект улучшения функции эндокринных клеток поджелудочной железы. Примеры включают в себя инструкции «пригодно для лиц с пониженной продукцией инсулина», «пригодно для лиц с пониженной функцией инсулина», «полезно для снижения или устранения факторов риска (рисков) заболеваний, связанных с образом жизни, такими как сахарный диабет, вызванными снижением активности или продукции инсулина, панкреатит, вызванный избыточным потреблением алкоголя и стрессом» и так далее.
Вышеупомянутый термин «инструкция» включает в себя все действия, информирующие потребителя о вышеупомянутом применении, и любые указания, напоминающие или аналогичные вышеупомянутому применению, входят в сферу «инструкций» по данному изобретению, независимо от цели, содержания, конкретного предмета, информационного типа и т.д. Однако инструкция предпочтительно составляется в выражениях, которые позволяют потребителю непосредственно распознать вышеупомянутое применение. Конкретные примеры включают в себя действия, указывающие на вышеупомянутое применение на товарах или упаковках товаров, относящихся к пищевому продукту или напитку по данному изобретению, действия по представлению, доставке, демонстрации для целей представления или доставки или импорта таких товаров или упаковок товаров, предназначенных для вышеупомянутого применения, демонстрации и распространении рекламы, прейскурантов или деловых документов, относящихся к товарам, на которых указано вышеупомянутое применение, или предоставление информации, включая в себя тексты с указанием на вышеупомянутое применение в электронном виде (Интернет и т.д.) и так далее.
Инструкция предпочтительно представляет собой указание, подтвержденное администрацией и т.д. (например, указание в форме, основанной на подтверждении, квалифицированном на основе какой-либо законной системы, представленной администрацией), и особенно предпочтительно - указание на рекламных материалах при продаже за наличный расчет, на упаковках, контейнерах, в каталогах, буклетах и POPs, других документах и так далее.
Примеры инструкций также включают в себя такие указания, как «здоровый пищевой продукт», «функциональные продукты питания», «пищевой продукт, питательный для кишечника», «пищевой продукт для специального диетического применения», «пищевой продукт с объявленной питательной функцией», квазилекарственные препараты и так далее, также как инструкции, подтвержденные, например, министерством здравоохранения Японии, отдел труда и социального обеспечения, указания, подтвержденные на основе системы пищевых продуктов, предназначенных для лечебного питания и подобных систем. Примеры последних включают в себя такие указания, как пищевой продукт для специализированного лечебного питания, указания о пищевом продукте для специализированного лечебного питания с конкретными лечебными целями, указания на влияние на структуру организма и его функции, указания об уменьшении риска заболевания и так далее, и, более конкретно, типичные примеры включают в себя указания, как на пищевом продукте специализированного лечебного применения (особенно указания на использование в лечебных целях), представленные в правоприменительных правилах Закона о развитии здравоохранения (Министерство труда Японии, отдел труда и социального обеспечения, приказ министерства №86, Апрель 30, 2003) сходные указания.
Примеры
Данное изобретение будет объяснено более конкретно со ссылкой на нижеследующие примеры. Однако сфера данного изобретения не ограничена нижеследующими примерами.
Пример получения 1
Примеры получения 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ола из алоэ вера описаны ниже.
3-O-β-D-Глюкопиранозил-4-метил-эргост-7-ен-3-ол экстрагировали из алоэ вера и очищали, как описано ниже.
Мезофилл в количестве 100 кг (чистая гелевая фракция) алоэ вера переводили в жидкое состояние с помощью гомогенизатора с добавлением 100 л смеси этилацетат/бутанол (3:1) и перемешивали.
Смесь оставляли на ночь для разделения смеси этилацетат/бутанол и водного слоя, и смесь этилацетат/бутанол отделяли. Экстракт из этой смеси этилацетат/бутанол, полученный путем концентрации смеси этилацетат/бутанол при пониженном давлении, весил 13,5 г.
Эффект улучшения состояния гипергликемии определяли для вышеупомянутого водного слоя и экстракта из смеси этилацетат/бутанол на модели диабета мышей, описанной ниже в Сравнительном Примере 1, а эффект наблюдали при действии экстракта из смеси этилацетат/бутанол. Затем была предпринята попытка выделить и очистить компоненты экстракта. Во-первых, вышеупомянутый экстракт исследовали с помощью тонкослойной хроматографии (Merck Ltd., Silica gel 60F254 и RP-18F2543). В результате оказалось, что для этого пригоден способ выделения, основанный на хроматографии с обычной фазой на колонке с силикагелем с использованием смеси хлороформ/метанол. Соответственно, раствор 13 г вышеупомянутого экстракта в 1 мл смеси хлороформ/метанол (1:1) загружали в колонку, заполненную 400 г силикагеля 60 (Merck Ltd.), для того чтобы добиться адсорбции компонентов на колонке, а затем компоненты элюировали смесью хлороформ/метанол способом ступенчатого градиента, в котором концентрация метанола нарастала ступенчато (соотношения смешивания хлороформ:метанол = 100:1, 25:1, 10:1, 5:1 и 1:1), а элюат фракционировали для каждого соотношения смешивания вышеупомянутой смеси. Выход продуктов грубой очистки, полученный при фракционировании, после удаления растворителя составил 1,44; 3,0; 1,17; 1,28 и 2,27 г соответственно. Способом с использованием вышеупомянутых модельных животных подтверждено, что помимо этих фракций активный компонент присутствует во фракции, элюированной смесью хлороформ:метанол = 5:1 (продукт грубой очистки A). Наличие барбалоина или алоэ-эмодина анализом тонкослойной хроматографии не подтверждено.
Кроме того, чтобы выделить и очистить активный компонент из вышеупомянутого продукта грубой очистки A, продукт грубой очистки A исследовали с помощью тонкослойной хроматографии (фирма Merck Ltd., Silica gel 60F254 и RP-18F2543). В результате пригодным оказался способ выделения, основанный на обращенно-фазной хроматографии на колонке с силикагелем с использованием метанола. Соответственно, вышеупомянутый продукт грубой очистки A растворяли в 1 мл смеси хлороформ/метанол (1:1) и загружали на колонку, заполненную 180 г COSMOSIL 140 (фирма Nacalai Tesque, Inc.), чтобы добиться адсорбции компонентов на колонке. Затем проводили элюцию, последовательно используя 600 мл 85% раствора метанола, 600 мл 95% раствора метанола и 100 мл 100% метанола. 3-O-β-D-Глюкопиранозил-4-метил-эргост-7-ен-3-ол концентрировали и выделяли во фракции, элюируемой 95% метанолом, и получали в количестве 370 мг после удаления растворителя. Далее в данном документе этот продукт обозначается как соединение 1.
Поскольку соединение 1 демонстрирует значение Rf, очень близкое к таковому β-ситостеролгликозида при исследовании, основанном на тонкослойной хроматографии, было сделано предположение, что это - гликозид, в котором 1 молекула сахара связана с агликоновым остатком. Кроме того, чтобы исследовать состав сахара соединения 1, оно было подвергнуто метанолизу, что перевело его в TMS-производное, и измерению с помощью GC-MS. В результате измерения TMS-производного сахара в соединении 1 были показаны основные пики в временем задержки 14,28; 14,61 и 16,34 минуты, что в основном соответствует временам задержки основных пиков образца глюкозы (фирма Nacalai Tesque, Inc.), 14,27; 14,60 и 16,33 минуты. Кроме того, пики, соответствующие основным пикам образца галактозы (фирма Kishida Chemical Co., Ltd.) и образца ксилозы (фирма Kishida Chemical Co., Ltd.), не наблюдались. Таким образом, было подтверждено, что тип сахара, содержащегося в соединение 1, - это глюкоза.
На основе приведенных выше результатов было рассчитано, что соединение 1 представляет собой гликозид, в котором 1 молекула глюкозы связана с агликоновым остатком. Однако, когда соединение 1 исследовали с помощью 13C-ЯМР (125 МГц, CDCl3), было подтверждено присутствие загрязнений. Исходя из этого был сделан вывод о необходимости дальнейшей очистки для определения его структуры. Соответственно, соединение 1 было обработано метанолом, а затем ацетилировано, после чего структура агликонового остатка, так же как и сайт связывания агликонового остатка и сахара были подтверждены. Этот способ описан ниже.
Соединение 1 в количестве 50 мг растворяли в метаноле (50 мл), содержащем 5% соляной кислоты, и раствор нагревали при кипении с обратным холодильником в течение 6 часов для метанолиза и высушивали с получением осадка (около 30 мг). Этот осадок очищали на хроматографической колонке с силикагелем (гексан:хлороформ = 9:1) с получением соединения 2 (10 мг). К этому соединению 2 (5 мг) добавляли уксусный ангидрид и пиридин (по 2 капли каждого) и нагревали до 70°C в течение 30 минут для проведения ацетилирования, а затем растворитель реакционной смеси выпаривали с получением соединения 3. Результаты анализа этого соединения 3 с помощью GC-MS и 13C-ЯМР (125 МГц, CDCl3) показаны на Фиг.1 и 2 соответственно. Условия измерения и результаты представлены ниже. 3-Ацетокси-4-метил-эргост-7-ен, использовавшийся как эталонное вещество, получали экстракцией из алоэ, очисткой экстракта, подтверждая структуру очищенного продукта с помощью 13C-ЯМР и ацетилирования.
[Спектр 13C-ЯМР (значения d, в CDCl3)]; C-1:36,8, C-2:27,3, C-3:78,7, C-4:37,0, C-5:46,9, C-6:26,8, C-7:117,4, C-8:139,4, C-9:49,7, C-10:34,9, C-11:21,6, C-12:39,7, C-13:43,6, C-14:55,1, C-15:23,1, C-16:28,2, C-17:56,3, C-18:12,0, C-19:14,2, C-20:36,5, C-21:19,0, C-22:33,9, C-23:30,6, C-24:39,1, C-25:32,6, C-26:20,4, C-27:18,4, C-28:15,6, C-29:15,3
[GC-MS]
Прибор: GC-17A/GCMS5050A (фирма SHIMADZU)
Колонка GC: NEUTRA BOND-5 (фирма GL Scienses)
Температура колонки: 100°C (2 мин) → (10°C/мин) → 300°C (28 мин)
Температура инжектора: 250°C
Газ-носитель: He (1,3 мл/мин)
Температура детектора: 300°C
Режим MS: EI
Энергия ионизации: 70 эВ
Результаты
Эталонное вещество: 3-ацетокси-4-метил-эргост-7-ен: tR [min]=39,4; m/z 456 [M]+, 441 [M-CH3]+, 396 [M-AcOH]+, 381 [M-CH3-AcOH]+
Соединение 3: tR [min]=39,2; m/z 456 [M]+, 441 [M-CH3]+, 396 [M-AcOH]+, 381 [M-CH3-AcOH]+
Результаты измерения ЯМР соединения 3 соответствуют значениям для 3-ацетокси-4-метил-эргост-7-ена, указанным в литературе (Yukagaku (Oil Chemistry), Vol.36, No. 5, pp.301-319, 1987). Эти результаты показывают, что соединение 2 представляет собой 4-метил-эргост-7-ен-3-ол. Кроме того, в результате измерения с помощью масс-спектрометрии с бомбардировкой ускоренными атомами (FAB-MS) обнаружено, что молекулярный вес соединения 1 составляет 576. При конденсации соединения 2 (агликоновый остаток) и глюкозы молекулярный вес составляет 414 (соединение 2) + 180 (глюкоза) - 18 (вода) = 576, что соответствует молекулярному весу соединения 1.
Приведенные выше результаты показывают, что соединение 1 имеет структуру 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ола.
Брутто формулы, молекулярные веса и структурные формулы соединений приведены ниже.
Соединение 1
Брутто формула: C35H60O6
Молекулярный вес: 576
Структурная формула: нижеследующая структурная формула (1)

Соединение 2
Брутто формула: C29H50O
Молекулярный вес: 414
Структурная формула: нижеследующая структурная формула (2)
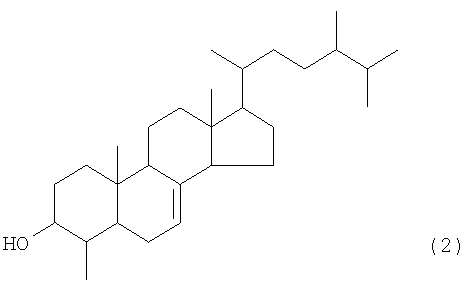
Соединение 3
Брутто формула: C31H52O2
Молекулярный вес: 456
Структурная формула: нижеследующая структурная формула (3)
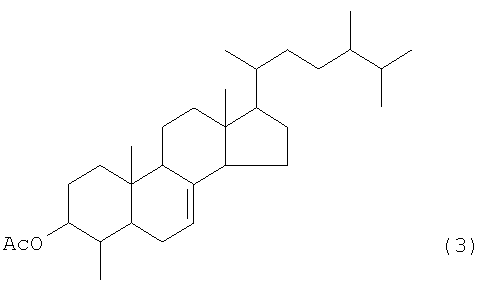
Пример получения 2
Мезофилл (чистая гелевая фракция) алоэ вера высушивали нагреванием, к 0,3 г высушенного порошка из разрушенного алоэ вера добавляли 60 мл 60, 80 или 100% этанола, и смесь нагревали с обратным холодильником при 60°C в течение 1 часа. Экстракт центрифугировали при 1500 об/мин в течение 20 минут, а супернатант концентрировали при пониженном давлении, чтобы полностью удалить этанол и, таким образом, получить неочищенный экстракт. Сухие веса неочищенных экстрактов, полученных экстракцией с помощью 60, 80 и 100% этанола, составили 65, 42 и 18 мг соответственно. С помощью тонкослойной хроматографии было подтверждено, что эти неочищенные экстракты содержат 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол.
Пример получения 3
Мезофилл (чистая гелевая фракция) алоэ вера высушивали нагреванием, к 0,3 г высушенного порошка из разрушенного алоэ вера добавляли 60 мл воды и смесь нагревали с обратным холодильником при 95°C в течение 5 часов. Экстракт центрифугировали при 1500 об/мин в течение 20 минут и супернатант лиофилизировали с получением 75 мг неочищенного экстракта. С помощью тонкослойной хроматографии было подтверждено, что неочищенный экстракт содержит 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол.
Пример получения 4
Мезофилл (чистая гелевая фракция) алоэ вера высушивали нагреванием, разрушали и высушивали, к 21 кг порошка алоэ вера, приготовленного таким образом, добавляли 90 л смеси хлороформ/метанол (2:1), оставляли на ночь в этой смеси при комнатной температуре и собирали осадок путем фильтрации, к полученному фильтрацией осадку добавляли еще 90 л смеси хлороформ/метанол (2:1). Эту процедуру повторяли полностью 4 раза. Полученный фильтрат (350 л) концентрировали при 28°C с получением в конце концов 784 г неочищенного экстракта. К 780 г неочищенного экстракта добавляли 2 л смеси хлороформ/метанол (2:1), перемешивали в течение 1 часа и фильтровали, чтобы получить слой смеси хлороформ/метанол (A). К осадку, полученному фильтрованием, последовательно добавляли 2,5 л воды и 2 л этилацетата, перемешивали в течение 1 часа и получали слой этилацетата (B). К оставшемуся водному слою снова добавляли 5 л хлороформа и перемешивали в течение 1 часа и получали слой хлороформа (C).
Полученные органические экстракты A, B и C смешивали, концентрировали при 23°C и загружали на колонку с силикагелем [стеклянная колонка: 52 мм × 350 мм, материал заполнения: IR-63/210-W (фирма Daiso Co., Ltd.)]. Затем, при контроле элюата тонкослойной хроматографией, через колонку пропускали 10 л смеси гексан/хлороформ (1:1), 10 л хлороформа, 20 л смеси хлороформ/метанол (10:1) и 20 л смеси хлороформ/метанол (5:1) именно в таком порядке и получали фракцию 1 (около 1 л), фракцию 2 (около 1,5 л), фракцию 3 (около 1,5 л) и фракцию 4 (около 1,5 л) в порядке использованных растворителей для элюции.
С помощью тонкослойной хроматографии было подтверждено, что среди прочих фракция 3 содержит искомый гликозид, затем растворитель из фракции 3 удаляли и получали 131,6 г неочищенного экстракта. Неочищенный экстракт в количестве 130 г опять загружали на колонку с силикагелем [стеклянная колонка: 70 мм x 500 мм, материал заполнения: SP-60-40/60 (фирма Daiso Co., Ltd.)] и элюировали последовательно с помощью 10 л смеси хлороформ/метанол (30:1), 50 л смеси хлороформ/метанол (20:1), 10 л смеси хлороформ/метанол (10:1) и 10 л смеси хлороформ/метанол (1:1) в качестве элюционных растворителей в условиях давления 10 кГ/см2 и скорости потока 40 мл/мин. Элюаты разделяли на 100-миллилитровые фракции с помощью коллектора фракций и собирали фракции 1-8.
Собранные фракции исследовали с помощью тонкослойной хроматографии, и в результате было показано, что искомый гликозид вместе с загрязнениями присутствует во фракции 7. Далее эту фракцию концентрировали, снова загружали на колонку с силикагелем [стеклянная колонка: 70 мм × 500 мм, материал заполнения: SP-60-40/60 (фирма Daiso Co., Ltd.)] и последовательно элюировали с помощью 10 л смеси хлороформ/метанол (20:1) и 10 л смеси хлороформ/метанол (10:1) в качестве элюционных растворителей в условиях давления 10 кГ/см2 и скорости потока 40 мл/мин. В результате получили 25,3 г 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ола, который является искомым гликозидом, содержащимся во фракции, элюированной смесью хлороформ/метанол (10:1).
Пример сравнения 1
Этот тест выполняли, чтобы оценить эффект 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ола на улучшение гипергликемического состояния.
(1) Получение образца
3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол, полученный в Примере получения 1, упомянутом выше, использовали в качестве тестового образца.
(2) Способ проведения теста
В качестве мышей, модельных для диабета II типа, использовали самцов мышей db/db в возрасте 6 недель (приобретали на фирме Clea Japan, Inc.). Эти мыши были разделены на группы, в каждой по 7 животных. Тестовый образец растворяли в диметилсульфоксиде (ДМСО), и устанавливали концентрацию 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ола на уровне 15 мкг/мл физиологическим раствором. Финальная концентрация ДМСО устанавливалась на уровне 0,2%. Мышам, модельным для диабета II типа, орально с помощью зонда вводили 1 мл раствора тестового образца один раз в день каждый день. Раствор, не содержащий тестового образца, использовали как негативный контрольный образец. Уровень глюкозы в крови натощак и случайный уровень глюкозы измеряли во времени с помощью Antsense II (фирма Bayer-Sankyo Co., Ltd.). Уровень глюкозы в крови натощак измеряли после 15 часов голодания.
(3) Эффект улучшения состояния гипергликемии
Изменения во времени случайных уровней глюкозы в крови и уровней глюкозы в крови натощак в ходе введения тестового образца показаны на Фиг.3 и 4. У мышей, которым вводили негативный образец, наблюдался быстрый подъем уровней глюкозы и случайного уровня глюкозы в крови, и уровня глюкозы крови натощак, тогда как с повторно вводимым тестовым образцом у мышей наблюдался ясный эффект подавления повышения уровня глюкозы в крови.
Тестовый пример 1
Этот тест выполняли, чтобы оценить защитное действие 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ола на функцию эндокринных клеток поджелудочной железы (способность продуцировать инсулин), с использованием мышей db/db, известных как модельные животные для гипофункции поджелудочной железы или дисфункции ткани поджелудочной железы.
(1) Получение образца
3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол, полученный в Примере получения 1, упомянутом выше, использовали в качестве тестового образца.
(2) Способ тестирования
В этом тесте использовали самцов мышей db/db в возрасте 6 недель (приобретенных на фирме Clea Japan, Inc.). Этих мышей разделяли на группы, по 7 животных в каждой. Каждый тестовый образец растворяли в ДМСО, устанавливая концентрации 0,1 или 1 мкг/мл с помощью физиологического раствора. Финальная концентрация ДМСО составила 0,2%. Этим модельным мышам орально с помощью зонда вводили 1 мл тестового образца в день в течение 42 дней. Уровень инсулина в сыворотке измеряли на 43-й день непрерывного введения с помощью набора для определения инсулина у мышей Lbis insulin mouse ELISA kit (фирма Shibayagi Co., Ltd).
(3) Результаты теста
Уровень инсулина в сыворотке на 43-й день непрерывного введения образца показан в Таблице 1. При введении тестового образца 1 в концентрации 1 мкг/животное уровень инсулина в сыворотке составлял 216% от наблюдавшегося при негативном тесте, и, таким образом, наблюдается четкий защитный эффект на функцию поджелудочной железы (способность продуцировать инсулин). С другой стороны, при введении [тестового образца] в концентрации 0,1 мкг/животное какого-либо существенного эффекта не наблюдалось. В период введения не наблюдалось никаких побочных эффектов с точки зрения веса тела и патологических признаков.
Тестовый пример 2
В этом тесте исследовали защитное действие 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол на ткань поджелудочной железы на мышах db/db, известных как модельное животное в отношении гипофункции поджелудочной железы или дисфункции ткани поджелудочной железы.
(1) Получение образца
3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол, полученный в Примере получения 1, упомянутом выше, использовали как тестовый образец.
(2) Способ проведения теста
В этом тесте использовали самцов мышей db/db в возрасте 6 недель (приобретенных на фирме Clea Japan, Inc.). Этих мышей разделяли на группы, по 7 животных в каждой. Каждый тестовый образец растворяли в ДМСО и устанавливали концентрацию 1 мкг/мл физиологическим раствором. Финальная концентрация ДМСО составляла 0,2%. Модельным мышам вводили 1 мл тестового образца один раз в день в течение 42 дней орально с помощью зонда. На 43-й день непрерывного введения выделяли поджелудочные железы, разделяли каждую из них на три порции - выше двенадцатиперстной кишки, на ее уровне и ниже, и фиксировали в растворе формалина, а затем обычным способом готовили парафиновые блоки. Из парафиновых блоков готовили срезы и окрашивали их гематоксилин-эозином. Число островков Лангерганса, присутствующих в 3 отделах поджелудочной железы, и площадь наибольшего островка Лангерганса в каждом срезе измеряли с помощью окуляр-микрометра микроскопа ("ECLIPSE E600", фирма NIKON CORP.).
(3) Результаты теста
Число островков Лангерганса в срезах поджелудочной железы на 43-й день непрерывного введения образца показано в Таблице 2, а максимальные площади островков Лангерганса на тот же день показаны в Таблице 3. Число островков Лангерганса у мышей, которым вводили тестовый образец, составило 188% к числу островков Лангерганса у мышей, которым вводили негативный образец, и было установлено, что это число действительно велико. Сходным образом, максимальная площадь островков Лангерганса у мышей, которым вводили тестовый образец, поддерживалась в 3,6 раза большей, чем наблюдавшаяся при негативном тесте, и, таким образом, обнаружено, что уменьшение островков Лангерганса вследствие дисфункции поджелудочной железы предупреждено. Исходя из этих результатов показано, что 3-O-β-D-глюкопиранозил-4-метил-эргост-7-ен-3-ол имеет защитное действие на ткани поджелудочной железы, особенно эндокринных клеток железы.
Промышленная применимость
Лекарственное средство и пищевой продукт или напиток по данному изобретению могут безопасно вводиться или потребляться и имеют защитное действие на эндокринные клетки поджелудочной железы, а также улучшают клеточные функции. Кроме того, в соответствии с предпочтительным вариантом реализации лекарственное средство и пищевой продукт или напиток по данному изобретению не содержат барбалоина или алоэ-эмодина, которые являются неблагоприятными компонентами лекарственного средства и пищевого продукта или напитка.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО И ПИЩЕВОЙ ПРОДУКТ ИЛИ НАПИТОК ДЛЯ УЛУЧШЕНИЯ ФУНКЦИЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2351340C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО И ПИЩЕВОЙ ПРОДУКТ ИЛИ НАПИТОК ДЛЯ УЛУЧШЕНИЯ ФУНКЦИЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2006 |
|
RU2353368C1 |
| ГЛИКОЗИДНОЕ ПРОИЗВОДНОЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ, КОМПОЗИЦИЯ, СРЕДСТВО ДЛЯ КОРРЕКЦИИ ГИПЕРГЛИКЕМИИ, ЛЕКАРСТВЕННОЕ СРЕДСТВО, ПИЩЕВЫЕ ПРОДУКТЫ, СПОСОБ КОРРЕКЦИИ ГИПЕРГЛИКЕМИИ | 2005 |
|
RU2315770C1 |
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ РЕЗИСТЕНТНОСТИ К ИНСУЛИНУ | 2006 |
|
RU2379037C2 |
| АГЕНТ ДЛЯ СНИЖЕНИЯ ИНСУЛИНОРЕЗИСТЕНТНОСТИ | 2006 |
|
RU2380103C2 |
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ НАКОПЛЕНИЯ ВИСЦЕРАЛЬНОГО ЖИРА | 2006 |
|
RU2372920C2 |
| ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ И ПИЩЕВОЙ ПРОДУКТ ИЛИ НАПИТОК ДЛЯ УЛУЧШЕНИЯ ГИПЕРГЛИКЕМИЧЕСКОГО СОСТОЯНИЯ | 2005 |
|
RU2327463C2 |
| СРЕДСТВО ДЛЯ УЛУЧШЕНИЯ СОСТОЯНИЯ ПРИ РЕЗИСТЕНТНОСТИ К ИНСУЛИНУ | 2006 |
|
RU2379313C2 |
| АНТИОКСИДАНТ | 2009 |
|
RU2465909C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО И ПИЩЕВОЙ ПРОДУКТ ИЛИ НАПИТОК ДЛЯ СНИЖЕНИЯ ГИПЕРГЛИКЕМИИ | 2005 |
|
RU2315601C1 |
Изобретение относится к фармацевтической промышленности, в частности к средству для улучшения функций поджелудочной железы. Лекарственное средство для улучшения функций поджелудочной железы, которое содержит определенное соединение. Лекарственное средство для улучшения функций поджелудочной железы, которое содержит экстракт растения семейства Liliaceae или его фракцию, содержащие определенное соединение в качестве активного ингредиента. Пищевой продукт или напиток для улучшения функций поджелудочной железы, который содержит определенное соединение. Пищевой продукт или напиток для улучшения функций поджелудочной железы, который содержит экстракт растения семейства Liliaceae или его фракцию, содержащую определенное соединение в качестве активного ингредиента. Применение определенного соединения или экстракта, содержащего указанное соединение для производства лекарственного средства для улучшения функций поджелудочной железы. Способ улучшения функций поджелудочной железы, который включает введение определенного соединения или экстракта, содержащего указанное соединение, субъекту, функции поджелудочной железы которого должны быть улучшены. Вышеописанные лекарственное средство, пищевой продукт или напиток эффективно улучшают функцию поджелудочной железы. 6 н. и 11 з.п. ф-лы, 4 ил., 3 табл.
| Устройство для обрезывания концов моркови | 1931 |
|
SU25803A1 |
| Beppu H., et al | |||
| Radical-scavenging effects of Aloe arborescens Miller on prevention of pancreatic islet B-cell destruction in rats //J | |||
| Ethnopharmacol | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| JP 2003113111,18.04.2003 | |||
| JP 09188630, 22.07.1997 | |||
| JP 2003286185, 07.10.2003 | |||
| Yen GY et al | |||
| Systematic review of herbs and dietary | |||
Авторы
Даты
2009-03-27—Публикация
2006-02-28—Подача