Настоящее изобретение относится к способу получения (меркаптоорганил)алкоксисиланов.
Известен способ получения меркаптоалкилсиланов по одностадийной реакции, заключающейся в том, что соответствующие (галогенорганил)алкоксисилановые соединения подвергают взаимодействию с тиомочевиной и аммиаком (DE AS 2035619). Один из недостатков этого способа состоит в том, что для достижения экономически приемлемых скорости и степени химического превращения требуется значительный по продолжительности технологический цикл (более 24 часов). Еще один недостаток такого подхода заключается в том, что он не обеспечивает стабильного высокого выхода продукта, достигающего лишь 75-80%, в пересчете на количество используемого (галогенорганил)алкоксисиланового соединения. Кроме того, при осуществлении данного способа образуется гидрохлорид гуанидина, отделение и утилизация которого требует дополнительных затрат.
Известны далее способы получения меркаптоалкилсиланов, заключающиеся в том, что гидрированием под давлением соединений, представляющих собой амид тиопропионовой кислоты - силаны (см. ЕР 0018094), или гидрированием цианоалкилсилановых соединений в присутствии элементарной серы либо сероводорода превращают указанные соединения в меркаптосиланы (см. патент US 4012403). Недостатком обоих способов является крайне низкий выход требуемых продуктов.
Из патента US 3849471 известен способ получения меркаптосиланов, осуществляемый взаимодействием соответствующих (галогенорганил)алкоксисилановых соединений с сероводородом в присутствии этилендиамина и больших количеств сульфидов тяжелых металлов. Недостаток этого способа состоит в том, что образуются различные побочные продукты, а их отделение связано со значительными трудностями.
Известна далее возможность улучшить предложенный в патенте US 3849471 способ превращения исходных силанов взаимодействием с сероводородом не в присутствии диаминов, а в присутствии аммиака, первичных, вторичных либо третичных аминов при определенных условиях дополнительно в присутствии полярных, протонных или апротонных сред (см. патент US 4082790). Недостаток такого подхода заключается в том, что для достижения требуемых для взаимодействия реагентов между собой температур реакции приходится проводить в автоклавах, работающих под давлением. Если же проводить реакции при отсутствии полярных сред, то для обеспечения приемлемой степени и скорости превращения приходится мириться с экономически нерентабельной значительной продолжительностью реакции. Кроме того, дозировка и обращение с высокотоксичным H2S в условиях промышленного производства являются крайне нежелательными, требуют существенных затрат и связаны со значительными мерами безопасности.
Из патента GB 1102251 известна обменная реакция, осуществляемая взаимодействием гидросульфидов щелочных металлов с (галогеналкил)алкоксисиланами в метанольной среде с получением таким путем соответствующих меркаптосиланов. Недостаток подобного подхода заключается в том, что, во-первых, для достижения высокой степени и скорости превращения требуется сверхдлительная продолжительность реакции (96 часов) и, во-вторых, не обеспечивается удовлетворительный выход целевого продукта.
Известен также способ получения (меркаптоалкил)алкоксисиланов, осуществляемый взаимодействием гидросульфида щелочного металла с соответствующими (галогеналкил)алкоксисиланами в присутствии 10-100%-ного молярного избытка H2S (патент US 5840952). Однако при реализации в промышленном масштабе этому способу присущи существенные недостатки, а именно: необходимость дозировать высокотоксичный H2S и постоянно так или иначе контактировать при обращении с ним, а сам способ приходится проводить в 2 стадии, что в конечном счете значительно снижает выход продукта с единицы объема в единицу времени.
Известен далее еще один способ получения (меркаптоалкил)алкоксисиланов, осуществляемый взаимодействием (галогеналкил)алкоксисиланов с гидросульфидом щелочного металла (NaSH) в полярных, апротонных растворителях (заявка ЕР 0471164). Недостаток данного способа состоит в том, что растворители приходится использовать в больших количествах, составляющих по меньшей мере 50 об.%, а в случае, например, диметилформамида к этой проблеме добавляется еще и токсичность. Кроме того, высокая температура кипения того же диметилформамида существенно затрудняет последующую дистиллятивную переработку и очистку реакционных продуктов.
С учетом вышеизложенного в основу изобретения была положена задача разработать способ получения (меркаптоорганил)алкоксисиланов, который позволил бы исключить применение газообразных исходных веществ и в первую очередь избежать необходимость дозировки и обращения с высокотоксичным сероводородом или токсичным диметилформамидом и который обеспечивал бы при превращении (галогенорганил)силанов высокий выход с единицы объема в единицу времени.
Объектом изобретения в соответствии с этим является способ получения (меркаптоорганил)алкоксисиланов, который отличается тем, что сульфид щелочного металла подвергают взаимодействию со смесью из (галогенорганил)алкоксисилана и (галогенорганил)галогенсилана в спирте в условиях, исключающих доступ воздуха, и при повышенном давлении.
(Меркаптоорганил)алкоксисиланы могут представлять собой соединения следующей общей формулы I
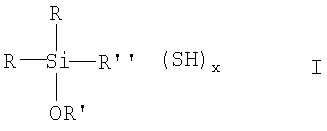
где R оба имеют идентичные или разные значения и представляют собой алкильную группу, предпочтительно СН3, алкенильную, арильную либо аралкильную группу с 1-8 С-атомами или группу OR',
R' имеет идентичные или разные значения и представляет собой разветвленную или неразветвленную, содержащую одинарную связь C1-C24-, предпочтительно C1-C4- или С12-С18-алкильную либо -алкенильную группу или арильную либо аралкильную группу,
R'' представляет собой разветвленную или неразветвленную, насыщенную или ненасыщенную, алифатическую, ароматическую либо смешанную алифатическую/ароматическую, содержащую двойную связь C1-С30углеводородную группу, необязательно замещенную фтором, хлором, бромом, иодом, группой NH2- или NHR',
x обозначает 1-3.
При х=1 R'' может представлять собой -СН2-, -СН2СН2-, -СН2СН2СН2-,
-СН2СН2СН2СН2-, -СН(СН3)-, -СН2СН(СН3)-, -СН(СН3)СН2-, -С(СН3)2-, -СН(С2Н5)-, -СН2СН2СН(СН3)-, -СН2СН(СН3)СН2- или
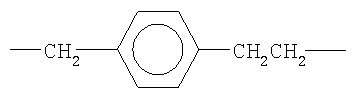
При х=2 R'' может представлять собой СН, -СН-СН2, -CH2-CH, -С-СН3,
-СН-СН2-СН2, -СН-СН-СН3 или -СН2-СН-СН2.
(Меркаптоорганил)алкоксисиланы общей формулы I могут представлять собой следующие соединения: 3-меркаптопропил(триметоксисилан), 3-меркаптопропил(триэтоксисилан), 3-меркаптопропил(диэтоксиметоксисилан), 3-меркаптопропил(трипропоксисилан), 3-меркаптопропил(дипропоксиметоксисилан), 3-меркаптопропил(тридодеканоксисилан), 3-меркаптопропил(тритетрадеканоксисилан), 3-меркаптопропил(тригексадеканоксисилан), 3-меркаптопропил(триоктадеканоксисилан), 3-меркаптопропил(дидодеканокси)тетрадеканоксисилан, 3-меркаптопропил(додеканокси)тетрадеканокси(гексадеканокси)силан, 3-меркаптопропил(диметоксиметилсилан), 3-меркаптопропил(метоксидиметилсилан), 3-меркаптопропил(диэтоксиметилсилан), 3-меркаптопропил(этоксидиметилсилан), 3-меркаптопропил(дипропоксиметилсилан), 3-меркаптопропил(пропоксидиметилсилан), 3-меркаптопропил(диизопропоксиметилсилан), 3-меркаптопропил(изопропоксидиметилсилан), 3-меркаптопропил(дибутоксиметилсилан), 3-меркаптопропил(бутоксидиметилсилан), 3-меркаптопропил(диизобутоксиметилсилан), 3-меркаптопропил(изобутоксидиметилсилан), 3-меркаптопропил(дидодеканоксиметилсилан), 3-меркаптопропил(додеканоксидиметилсилан), 3-меркаптопропил(дитетрадеканоксиметилсилан), 3-меркаптопропил(тетрадеканоксидиметилсилан), 2-меркаптоэтил(триметоксисилан), 2-меркаптоэтил(триэтоксисилан), 2-меркаптоэтил(диэтоксиметоксисилан), 2-меркаптоэтил(трипропоксисилан), 2-меркаптоэтил(дипропоксиметоксисилан), 2-меркаптоэтил(тридодеканоксисилан), 2-меркаптоэтил(тритетрадеканоксисилан), 2-меркаптоэтил(тригексадеканоксисилан), 2-меркаптоэтил(триоктадеканоксисилан), 2-меркаптоэтил(дидодеканокси)тетрадеканоксисилан, 2-меркаптоэтил(додеканокси)тетрадеканокси(гексадеканокси)силан, 2-меркаптоэтил(диметоксиметилсилан), 2-меркаптоэтил(метоксидиметилсилан), 2-меркаптоэтил(диэтоксиметилсилан), 2-меркаптоэтил(этоксидиметилсилан), 1-меркаптометил(триметоксисилан), 1-меркаптометил(триэтоксисилан), 1-меркаптометил(диэтоксиметоксисилан), 1-меркаптометил(дипропоксиметоксисилан), 1-меркаптометил(трипропоксисилан), 1-меркаптометил(триметоксисилан), 1-меркаптометил(диметоксиметилсилан), 1-меркаптометил(метоксидиметилсилан), 1-меркаптометил(диэтоксиметилсилан), 1-меркаптометил(этоксидиметилсилан), 1,3-димеркаптопропил(триметоксисилан), 1,3-димеркаптопропил(триэтоксисилан), 1,3-димеркаптопропил(трипропоксисилан), 1,3-димеркаптопропил(тридодеканоксисилан), 1,3-димеркаптопропил(тритетрадеканоксисилан), 1,3-димеркаптопропил(тригексадеканоксисилан), 2,3-димеркаптопропил(триметоксисилан), 2,3-димеркаптопропил(триэтоксисилан), 2,3-димеркаптопропил(трипропоксисилан), 2,3-димеркаптопропил(тридодеканоксисилан), 2,3-димеркаптопропил(тритетрадеканоксисилан), 2,3-димеркаптопропил(тригексадеканоксисилан), 3-меркаптобутил(триметоксисилан), 3-меркаптобутил(триэтоксисилан), 3-меркаптобутил(диэтоксиметоксисилан), 3-меркаптобутил(трипропоксисилан), 3-меркаптобутил(дипропоксиметоксисилан), 3-меркаптобутил(диметоксиметилсилан), 3-меркаптобутил(диэтоксиметилсилан), 3-меркаптобутил(диметилметоксисилан), 3-меркаптобутил(диметилэтоксисилан), 3-меркаптобутил(тридодеканоксисилан), 3-меркаптобутил(тритетрадеканоксисилан), 3-меркаптобутил(тригексадеканоксисилан), 3-меркаптобутил(дидодеканокси)тетрадеканоксисилан или 3-меркаптобутил(додеканокси)тетрадеканокси(гексадеканокси)силан.
При осуществлении способа получения (меркаптоорганил)алкоксисиланов могут образовываться соединения общей формулы I или же смеси из соединений общей формулы I.
В качестве (галогенорганил)алкоксисиланов могут применяться соединения общей формулы II
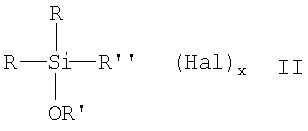
где x, R, R' и R'' имеют указанные выше значения, a Hal обозначает хлор, бром, фтор или иод.
Предпочтительно в качестве (галогенорганил)алкоксисиланов могут применяться следующие соединения: 3-хлорбутил(триэтоксисилан), 3-хлорбутил(триметоксисилан), 3-хлорбутил(диэтоксиметоксисилан), 3-хлорпропил(триэтоксисилан), 3-хлорпропил(триметоксисилан), 3-хлорпропил(диэтоксиметоксисилан), 2-хлорэтил(триэтоксисилан), 2-хлорэтил(триметоксисилан), 2-хлорэтил(диэтоксиметоксисилан), 1-хлорметил(триэтоксисилан), 1-хлорметил(триметоксисилан), 1-хлорметил(диэтоксиметоксисилан), 3-хлорпропил(диэтоксиметилсилан), 3-хлорпропил(диметоксиметилсилан), 2-хлорэтил(диэтоксиметилсилан), 2-хлорэтил(диметоксиметилсилан), 1-хлорметил(диэтоксиметилсилан), 1-хлорметил(диметоксиметилсилан), 3-хлорпропил(этоксидиметилсилан), 3-хлорпропил(метоксидиметилсилан), 2-хлорэтил(этоксидиметилсилан), 2-хлорэтил(метоксидиметилсилан), 1-хлорметил(этоксидиметилсилан) или 1-хлорметил(метоксидиметилсилан).
(Галогенорганил)алкоксисилан может представлять собой (галогенорганил)алкоксисилан формулы II или смесь (галогенорганил)алкоксисиланов формулы II.
В качестве (галогенорганил)галогенсиланов могут применяться соединения общей формулы III
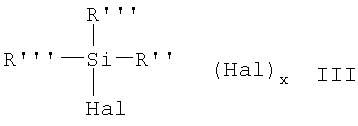
где x, Hal, R и R'' имеют указанные выше значения, а R''' оба независимо друг от друга представляют собой R или Hal.
Предпочтительно в качестве (галогенорганил)галогенсиланов могут применяться следующие соединения: 3-хлорбутил(трихлорсилан), 3-хлорпропил(трихлорсилан), 2-хлорэтил(трихлорсилан), 1-хлорметил(трихлорсилан), 3-хлорбутил(дихлорметоксисилан), 3-хлорпропил(дихлорметоксисилан), 2-хлорэтил(дихлорметоксисилан), 1-хлорметил(дихлорметоксисилан), 3-хлорбутил(дихлорэтоксисилан), 3-хлорпропил(дихлорэтоксисилан), 2-хлорэтил(дихлорэтоксисилан), 1-хлорметил(дихлорэтоксисилан), 3-хлорбутил(хлордиэтоксисилан), 3-хлорпропил(хлордиэтоксисилан), 2-хлорэтил(хлордиэтоксисилан), 1-хлорметил(хлордиэтоксисилан), 3-хлорбутил(хлордиметоксисилан), 3-хлорпропил(хлордиметоксисилан), 2-хлорэтил(хлордиметоксисилан), 1-хлорметил(хлордиметоксисилан), 3-хлорбутил(дихлорметилсилан), 3-хлорпропил(дихлорметилсилан), 2-хлорэтил(дихлорметилсилан), 1-хлорметил(дихлорметилсилан), 3-хлорбутил(хлор-)(метил-)метоксисилан, 3-хлорпропил(хлор-)(метил-)метоксисилан, 2-хлорэтил(хлор-)(метил-)метоксисилан, 1-хлорметил(хлор-)(метил-)метоксисилан, 3-хлорбутил(хлор-)(метил-)этоксисилан, 3-хлорпропил(хлор-)(метил-)этоксисилан, 2-хлорэтил(хлор-)(метил-)этоксисилан, 1-хлорметил(хлор-)(метил-)этоксисилан, 3-хлорбутил(хлордиметилсилан), 3-хлорпропил(хлордиметилсилан), 2-хлорэтил(хлордиметилсилан) или 1-хлорметил(хлордиметилсилан).
(Галогенорганил)галогенсилан может представлять собой (галогенорганил)галогенсилан общей формулы III или смесь (галоген органил)галогенсиланов общей формулы III.
(Меркаптоорганил)алкоксисиланы общей формулы I
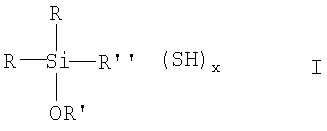
можно получать взаимодействием сульфида щелочного металла со смесью из (галогенорганил)алкоксисилана общей формулы II
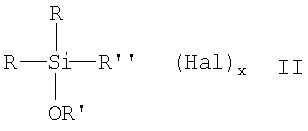
и (галогенорганил)галогенсилана общей формулы III
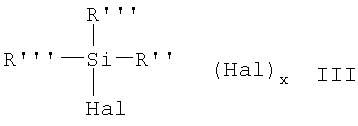
в спирте в условиях, исключающих доступ воздуха, и при повышенном давлении.
За счет выбора соответствующих (галогенорганил)алкоксисиланов и (галогенорганил)галогенсиланов можно активно и целенаправленно влиять на состав смесей из соединений общей формулы I.
Качество и тип состава смеси из (галогенорганил)алкоксисиланов и (галогенорганил)галогенсиланов можно определять по количеству и типу содержащихся в смеси гидролизуемых Si-Hal-связей.
Количество гидролизуемых Si-Hal-связей определяют следующим методом.
Максимум 20 г образца смешивают в химическом стакане вместимостью 150 мл с 80 мл этанола и 10 мл уксусной кислоты. Содержание галогенида определяют путем потенциометрического титрования с использованием раствора нитрата серебра (в концентрации AgNO3, равной 0,01 моль/л).
Предпочтительные молярные соотношения компонентов в смесях из (галогенорганил)алкоксисиланов и (галогенорганил)галогенсиланов могут зависеть, в частности, от числа Si-галогеновых функциональных групп в выбранных для использования (галогенорганил)галогенсиланах.
(Галогенорганил)алкоксисилан и (галогенорганил)галогенсилан могут применяться в молярном соотношении от 0,001:1 до 2:1. Так, например, в реакции с участием 3-хлорпропил(триметоксисилана) или 3-хлорпропил(триэтоксисилана) и 3-хлорпропил(трихлорсилана) предпочтительно использовать их в молярном соотношении от 2:1 до 2:1,5, особенно предпочтительно в соотношении от 2:1 до 2:1,25. При использовании же в реакции, например, 3-хлорпропил(метилдиметоксисилана) или 3 -хлорпропил(метилдиэтоксисилана) и 3-хлорпропил(метилдихлорсилана) предпочтительно их молярное соотношение составляет от 1:1 до 1:1,25, особенно предпочтительно от 1:1 до 1:1,15. Если же для реакции выбраны 3-хлорпропил(диметилметоксисилан) или 3-хлорпропил(диметилэтоксисилан) и 3-хлорпропил(диметилхлорсилан), то предпочтительно использовать их в молярном соотношении от 0,001:1 до 0,05:1.
Применяемую в способе согласно изобретению смесь из соответствующих (галогенорганил)алкоксисилана и (галогенорганил)галогенсилана в зависимости от используемой аппаратуры и требуемых эффектов, например от избирательности реакции, продолжительности реакции, пропускной способности реактора, материала, из которого выполнен реактор, или последовательности технологических операций, можно приготавливать уже до начала добавления сульфида щелочного металла.
В качестве сульфидов щелочных металлов Me2S могут применяться дилитийсульфид (Li2S), динатрийсульфид (Na2S), дикалийсульфид (K2S) и дицезийсульфид (Cs2S). Сульфид щелочного металла можно применять в молярном количестве, превышающем молярное количество используемого (галогенорганил)галогенсилана на 1-200%, предпочтительно на 1-150% и особенно предпочтительно на 1-110%.
Молярное соотношение между гидролизуемыми кремний-галогеновыми функциональными группами в смесях (галогенорганил)алкоксисилана и (галогенорганил)галогенсилана и сульфидом щелочного металла (Me2S) может составлять от 1:0,51 до 1:1,2, предпочтительно от 1:0,6 до 1:1,15, особенно предпочтительно от 1:0,75 до 1:1,05.
(Галогенорганил)алкоксисилан и (галогенорганил)галогенсилан можно смешивать друг с другом в любой последовательности, любым образом, при любой температуре и продолжительности и лишь после этого добавлять совместно либо последовательно спирт и сульфид щелочного металла.
(Галогенорганил)галогенсилан, сульфид щелочного металла и спирт можно смешивать друг с другом в любой последовательности, любым образом, при любой температуре и продолжительности и лишь после этого добавлять (галогенорганил)алкоксисилан.
(Галогенорганил)алкоксисилан, сульфид щелочного металла и спирт можно смешивать друг с другом в любой последовательности, любым образом, при любой температуре и продолжительности и лишь после этого добавлять (галогенорганил)галогенсилан.
В качестве спирта могут использоваться первичные, вторичные или третичные спирты с 1-24, предпочтительно 1-6, особенно предпочтительно 1-4 атомами углерода. В качестве первичных, вторичных или третичных спиртов приемлемы среди прочих метанол, этанол, н-пропанол, изопропанол, изобутанол или н-бутанол. Количество используемого спирта может составлять по меньшей мере 100 об.%, предпочтительно 250-1000 об.%, особенно предпочтительно 500-1000 об.%, соответственно в пересчете на применяемый силановый компонент.
В начале реакции и/или в ходе реакции, и/или в конце реакции к реакционной смеси можно добавлять полярные, протонные, апротонные, оснòвные или кислотные аддитивы.
Под повышенным давлением в контексте настоящего описания может иметься в виду давление, превышающее нормальное на 0,1-10 бар, предпочтительно на 1-7 бар.
Реакцию можно осуществлять при температурах в интервале от 0 до 180°С, предпочтительно от 50 до 150°С, особенно предпочтительно от 70 до 120°С. Оптимальная температура реакции в каждом случае с учетом предусматриваемого выхода целевого продукта и эффективности реакционного объема (аппарата) может варьироваться в зависимости от особенностей структуры применяемых (галогенорганил)алкоксисилана, (галогенорганил)галогенсилана и используемого в качестве растворителя спирта. Так, например, при проведении реакции в метаноле предпочтительной с учетом продолжительности реакции, количества образующихся побочных продуктов и создаваемого давления может оказаться температура в интервале от 60 до 95°С. При проведении же реакций, например, в этаноле предпочтительной с учетом продолжительности реакции, количества образующихся побочных продуктов и создаваемого давления может оказаться температура в интервале от 75 до 120°С.
Реакцию можно проводить в закрытом сосуде в атмосфере защитного газа.
Реакцию можно проводить в коррозионностойких автоклавах, которые могут быть выполнены из стекла, тефлона, эмалированной, соответственно из имеющей соответствующее покрытие стали, хастеллоя (коррозионностойкого никелевого сплава) или тантала.
Количество образующихся побочных продуктов благодаря соответствующему выбору условий реакции может составлять менее 20 мол.%.
Одно из преимуществ предлагаемого в изобретении способа состоит в том, что он позволяет отказаться от необходимости использовать в качестве доноров серы высокотоксичные газообразные вещества, такие как сероводород. Вместо подобных веществ создана возможность для использования в качестве доноров серы сульфидов щелочных металлов (например, высушенного динатрийсульфида), представляющих собой легко дозируемые твердые вещества.
Другое преимущество предлагаемого в изобретении способа состоит в том, что уже благодаря одной только возможности работать в закрытом сосуде (автоклаве и т.п.) удается повысить избирательность реакции.
Еще одно преимущество предлагаемого в изобретении способа по сравнению с известными способами заключается в том, что он обеспечивает высокую степень химического превращения при непродолжительном технологическом цикле получения каждой партии продукта и при легко реализуемых с технической точки зрения температурах.
Примеры
Анализ методом газовой хроматографии (ГХ-анализ)
ГХ-анализ реакционных смесей проводили с помощью газового хроматографа типа HP 6890 (фирма WLD) с колонкой DB5, толщиной 0,53 мм и толщиной пленки 1,5 мкм. В качестве детектора использовали детектор теплопроводности (прибор для определения содержания газа по величине теплопроводности). Программа изменения температуры включала следующие параметры:
- начальная температура 100°С,
- длительность начальной выдержки 1 мин,
- скорость нагрева до 280°С по 20°С в минуту,
- выдержка при 280°С в течение 10 мин.
Время удерживания для следующих компонентов составляло:
Пример 1
В выполненный из высококачественной стали автоклав со стеклянной вставкой и магнитной мешалкой при -10°С совместно помещают 29,6 г 3-хлорпропил(триэтоксисилана) и 200 мл этанола. Затем к раствору несколькими порциями добавляют 17,6 г высушенного Na2S. После добавления 16,4 г хлорпропил(трихлорсилана) автоклав быстро закрывают. Далее автоклав и находящиеся в нем вещества в течение 180 мин нагревают до 120°С. Давление при этом повышается до значений, превышающих нормальное давление на 3,2 бара. Затем автоклав охлаждают до нормальной температуры и отбирают образовавшуюся суспензию. Количество содержащегося в ней растворителя снижают с помощью роторного испарителя и выпавшее в осадок твердое вещество удаляют с помощью инертизированной фритты. Таким путем получают 38,4 г прозрачного раствора коричневатого цвета. По данным ГХ-анализа полученная смесь имеет следующий выраженный в процентах площади под кривой спектра состав:
Пример 2
В выполненный из высококачественной стали автоклав со стеклянной вставкой и магнитной мешалкой при -10°С совместно помещают 24 г 3-хлорпропил(триэтоксисилана) и 150 мл этанола. Затем к раствору несколькими порциями добавляют 12 г высушенного Na2S. После добавления 10,6 г 3-хлорпропил(трихлорсилана) автоклав быстро закрывают. Далее автоклав и находящиеся в нем вещества в течение 180 мин нагревают до 80°С. Давление при этом повышается до значений, превышающих нормальное давление на 3,2 бара. Затем автоклав охлаждают до нормальной температуры и отбирают образовавшуюся суспензию. Количество содержащегося в ней растворителя снижают с помощью роторного испарителя и выпавшее в осадок твердое вещество удаляют с помощью инертизированной фритты. Таким путем получают 29,2 г прозрачного раствора коричневатого цвета. По данным ГХ-анализа полученная смесь имеет следующий выраженный в процентах площади под кривой спектра состав:
Пример 3
40 г 3-хлорпропил(триэтоксисилана), 23 г высушенного Na2S и 22 г 3-хлорпропил(трихлорсилана) совместно помещают при комнатной температуре в автоклав с двойной стеклянной рубашкой и крышкой из высококачественной стали и автоклав закрывают. Затем к суспензии при комнатной температуре с помощью насоса высокого давления подают 400 мл этанола. Смесь нагревают до 80°С и в течение 5 ч выдерживают ее при этой температуре (80°С). После этого смесь охлаждают до комнатной температуры и анализируют посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов избирательность реакции составляет 89%, а степень превращения составляет 90%.
Пример 4
40 г 3-хлорпропил(триэтоксисилана), 26,5 г высушенного Na2S и 24,1 г 3-хлорпропил(трихлорсилана) совместно помещают при комнатной температуре в автоклав с двойной стеклянной рубашкой и крышкой из высококачественной стали и автоклав закрывают. Смесь нагревают до 60°С. Затем в автоклав при 60°С с помощью насоса высокого давления подают 400 мл этанола. Далее смесь продолжают нагревать до 80°С и в течение 5 ч выдерживают ее при этой температуре 80°С. После этого смесь охлаждают до комнатной температуры и анализируют посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов избирательность реакции составляет 82%, а степень превращения составляет 97%.
Пример 5
В автоклав с двойной стеклянной рубашкой и выполненной из сплава хастеллой С22 (коррозионностойкий никелевый сплав) крышкой и арматурой (фирма Buechi AG) совместно помещают при комнатной температуре 50 г высушенного Na2S и 650 мл сухого этанола. Образовавшуюся суспензию нагревают и в течение 20 мин перемешивают при 50°С. Затем к суспензии с помощью работающей на сжатом воздухе бюретки добавляют 128,2 г силановой смеси, состоящей из 3-хлорпропил(диэтокси(хлор)силана), хлорпропил(этокси(дихлор)силана), хлорпропил(трихлорсилана) и 3-хлорпропил(триэтоксисилана). Эту используемую в рассматриваемом случае смесь получают взаимодействием 80 г 3-хлорпропил(триэтоксисилана) и 48,2 г 3-хлорпропил(трихлорсилана). С помощью указанной бюретки к суспензии добавляют еще 150 мл этанола. Далее смесь нагревают при перемешивании до 97-102°С и температуру поддерживают на этом уровне в течение 180 мин. После этого смесь охлаждают до комнатной температуры. Затем отбирают ее образец и анализируют его посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в процентах площади под кривой спектра состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет более 99%, а избирательность реакции составляет 93%.
Пример 6
В автоклав с двойной стеклянной рубашкой и выполненной из сплава хастеллой С22 крышкой и арматурой (фирма Buechi AG) совместно помещают при комнатной температуре 50 г высушенного Na2S и 650 мл сухого этанола. Образовавшуюся суспензию нагревают и в течение 20 мин перемешивают при 50°С. Затем к суспензии с помощью работающей на сжатом воздухе бюретки добавляют смесь из 80 г 3-хлорпропил(триэтоксисилана) и 48,2 г 3-хлорпропил(трихлорсилана). С помощью указанной бюретки к суспензии добавляют еще 150 мл этанола. Далее смесь нагревают при перемешивании до 95-100°С и температуру поддерживают на этом уровне в течение 180 мин. После этого смесь охлаждают до комнатной температуры. Затем отбирают ее образец и анализируют его посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в процентах площади под кривой спектра состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет 97%, а избирательность реакции составляет 89,5%.
После этого содержимое реактора выгружают и реактор промывают небольшим количеством этанола с целью удаления из него возможных остатков. Полученную суспензию фильтруют. Отделенное твердое вещество промывают 400 мл н-пентана. Из образовавшегося раствора с помощью роторного испарителя при давлении 200-600 мбар и температуре 60-80°С удаляют летучие компоненты. Полученную суспензию тщательно смешивают с 200 мл пентана и в течение 10 ч выдерживают при 4-8°С. Выпавшее в осадок твердое вещество отделяют путем фильтрации и промывают 150 мл пентана. Из полученного прозрачного раствора пентан удаляют с помощью роторного испарителя при давлении 200-600 мбар и температуре 60-80°С. В результате получают 119,3 г бесцветной жидкости. По данным комбинированного анализа посредством ГХ, 1Н-ЯМР и 29Si-ЯМР полученный продукт имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет 96%, а избирательность реакции составляет 91%.
Пример 7
В автоклав с двойной стеклянной рубашкой и выполненной из сплава хастеллой С22 крышкой и арматурой (фирма Buechi AG) совместно помещают при комнатной температуре 50 г высушенного Na2S и 800 мл сухого этанола. Образовавшуюся суспензию нагревают и в течение 20 мин перемешивают при 50°С. Затем к суспензии с помощью работающей на сжатом воздухе бюретки добавляют смесь из 80 г 3-хлорпропил(триэтоксисилана) и 48,2 г 3-хлорпропил(трихлорсилана). С помощью указанной бюретки к суспензии добавляют еще 200 мл этанола. Далее смесь нагревают при перемешивании до 95-100°С и температуру поддерживают на этом уровне в течение 180 мин. После этого смесь охлаждают до комнатной температуры. Затем отбирают ее образец и анализируют его посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в процентах площади под кривой спектра состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет 98%, а избирательность реакции составляет 91%.
После этого содержимое реактора выгружают и реактор промывают небольшим количеством этанола с целью удаления из него возможных остатков. Полученную суспензию фильтруют. Отделенное твердое вещество промывают 400 мл н-пентана. Из образовавшегося раствора с помощью роторного испарителя при давлении 200-600 мбар и температуре 60-80°С удаляют летучие компоненты. Полученную суспензию тщательно смешивают с 200 мл пентана и в течение 10 ч выдерживают при 4-8°С. Выпавшее в осадок твердое вещество отделяют путем фильтрации и промывают 150 мл пентана. Из полученного прозрачного раствора пентан удаляют с помощью роторного испарителя при давлении 200-600 мбар и температуре 60-80°С. В результате получают 116,2 г бесцветной жидкости. По данным комбинированного анализа посредством ГХ, 1Н-ЯМР и 29Si-ЯМР полученный продукт имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет 99%, а избирательность реакции составляет 88%.
Пример 8
В автоклав с двойной стеклянной рубашкой и выполненной из сплава хастеллой С22 крышкой и арматурой (фирма Buechi AG) совместно помещают при комнатной температуре 57,8 г высушенного Na2S и 650 мл сухого этанола. Образовавшуюся суспензию нагревают и в течение 20 мин перемешивают при 50°С. Затем к суспензии с помощью работающей на сжатом воздухе бюретки добавляют смесь из 80,5 г 3-хлорпропил(триэтоксисилана) и 57,4 г 3-хлорпропил(трихлорсилана). С помощью указанной бюретки к суспензии добавляют еще 150 мл этанола. Далее смесь нагревают при перемешивании до 110-115°С и температуру поддерживают на этом уровне в течение 120 мин. После этого смесь охлаждают до комнатной температуры. Затем отбирают ее образец и анализируют его посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в процентах площади под кривой спектра состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет более 99%, а избирательность реакции составляет 91%.
После этого содержимое реактора выгружают и реактор промывают небольшим количеством этанола с целью удаления из него возможных остатков. Полученную суспензию фильтруют. Отделенное твердое вещество промывают 400 мл н-гексана. Из образовавшегося раствора с помощью роторного испарителя при давлении 200-600 мбар и температуре 60-80°С удаляют летучие компоненты. Полученную суспензию тщательно смешивают с 200 мл гексана и в течение 10 ч выдерживают при 4-8°С. Выпавшее в осадок твердое вещество отделяют путем фильтрации и промывают 150 мл гексана. Из полученного прозрачного раствора гексан удаляют с помощью роторного испарителя при давлении 20-600 мбар и температуре 60-80°С. В результате получают 121,3 г бесцветной жидкости. По данным комбинированного анализа посредством ГХ, 1Н-ЯМР и 29Si-ЯМР полученный продукт имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет более 99%, а избирательность реакции составляет 88%.
Пример 9
В автоклав с двойной стеклянной рубашкой и выполненной из сплава хастеллой С22 крышкой и арматурой (фирма Buechi AG) совместно помещают при комнатной температуре 57,7 г высушенного Na2S и 800 мл сухого этанола. Образовавшуюся суспензию нагревают и в течение 20 мин перемешивают при 50°С. Затем к суспензии с помощью работающей на сжатом воздухе бюретки добавляют смесь из 80,5 г 3-хлорпропил(триэтоксисилана) и 57,4 г 3-хлорпропил(трихлорсилана). С помощью указанной бюретки к суспензии добавляют еще 200 мл этанола. Далее смесь нагревают при перемешивании до 110-115°С и температуру поддерживают на этом уровне в течение 120 мин. После этого смесь охлаждают до комнатной температуры. Затем отбирают ее образец и анализируют его посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в процентах площади под кривой спектра состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет более 99%, а избирательность реакции составляет 88%.
После этого содержимое реактора выгружают и реактор промывают небольшим количеством этанола с целью удаления из него возможных остатков. Полученную суспензию фильтруют. Отделенное твердое вещество промывают 400 мл н-гексана. Из образовавшегося раствора с помощью роторного испарителя при давлении 200-600 мбар и температуре 60-80°С удаляют летучие компоненты. Полученную суспензию тщательно смешивают с 200 мл гексана и в течение 10 ч выдерживают при 4-8°С. Выпавшее в осадок твердое вещество отделяют путем фильтрации и промывают 150 мл гексана. Из полученного прозрачного раствора гексан удаляют с помощью роторного испарителя при давлении 20-600 мбар и температуре 60-90°С. В результате получают 116,3 г бесцветной жидкости. По данным комбинированного анализа посредством ГХ, 1Н-ЯМР и 29Si-ЯМР полученный продукт имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет более 99%, а избирательность реакции составляет 89%.
Пример 10
В автоклав с двойной стеклянной рубашкой и выполненной из сплава хастеллой С22 крышкой и арматурой (фирма Buechi AG) совместно помещают при комнатной температуре 50 г высушенного Na2S и 550 мл сухого этанола. Образовавшуюся суспензию нагревают и в течение 20 мин перемешивают при 50°С. Затем к суспензии с помощью работающей на сжатом воздухе бюретки добавляют смесь из 80 г 3-хлорпропил(триэтоксисилана) и 48,2 г 3-хлорпропил(трихлорсилана). С помощью указанной бюретки к суспензии добавляют еще 150 мл этанола. Далее смесь нагревают при перемешивании до 112-117°С и температуру поддерживают на этом уровне в течение 180 мин. После этого смесь охлаждают до комнатной температуры. При 50°С к реакционному раствору с помощью работающей под давлением бюретки добавляют 1,8 г муравьиной кислоты в 50 мл этанола. Образовавшуюся суспензию в течение 15 мин перемешивают при 50°С. Затем отбирают ее образец и анализируют его посредством газовой хроматографии. По данным ГХ-анализа полученная смесь имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет 98%, а избирательность реакции составляет 88%.
После этого содержимое реактора выгружают и реактор промывают небольшим количеством этанола с целью удаления из него возможных остатков. Полученную суспензию фильтруют. Отделенное твердое вещество промывают 400 мл н-пентана. Из образовавшегося раствора с помощью роторного испарителя при давлении 200-600 мбар и температуре 60-80°С удаляют летучие компоненты. Полученную суспензию тщательно смешивают с 200 мл пентана и в течение 10 ч выдерживают при 4-8°С. Выпавшее в осадок твердое вещество отделяют путем фильтрации и промывают 150 мл пентана. Из полученного прозрачного раствора пентан удаляют с помощью роторного испарителя при давлении 20-600 мбар и температуре 60-90°С. В результате получают 124,5 г бесцветной жидкости. По данным комбинированного анализа посредством ГХ, 1Н-ЯМР и 29Si-ЯМР полученный продукт имеет следующий выраженный в мас. процентах состав:
Полученные результаты подтверждают, что при использовании вышеуказанных компонентов степень превращения составляет 98%, а избирательность реакции составляет 85%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ (МЕРКАПТООРГАНИЛ)АЛКОКСИСИЛАНОВ | 2004 |
|
RU2360917C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНОСИЛАНОВ | 2006 |
|
RU2391291C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТООРГАНИЛ(АЛКОКСИСИЛАНОВ) | 2005 |
|
RU2387659C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТООРГАНИЛ(АЛКОКСИСИЛАНОВ) | 2005 |
|
RU2388763C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТООРГАНИЛ(АЛКОКСИСИЛАНОВ) | 2006 |
|
RU2412193C2 |
| РЕЗИНОВЫЕ СМЕСИ | 2012 |
|
RU2612148C2 |
| ФУНКЦИОНАЛИЗОВАННЫЕ АЗОКАРБОНИЛОМ СИЛАНЫ | 2015 |
|
RU2688516C2 |
| КАРБАМИДСОДЕРЖАЩИЕ СИЛАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2678320C2 |
| КАРБАМИДСОДЕРЖАЩИЕ СИЛАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2015 |
|
RU2677482C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБАМИДСОДЕРЖАЩИХ МЕРКАПТОСИЛАНОВ | 2015 |
|
RU2681218C2 |
Изобретение относится к способу получения (меркаптоорганил)алкоксисиланов. Техническая задача - разработка способа получения (меркаптоорганил)алкоксисиланов, позволяющего исключить применение газообразных и токсичных исходных соединений и обеспечивающего высокий выход целевого продукта. Предложен способ получения (меркаптоорганил)алкоксисиланов, в котором сульфид соответствующего щелочного металла подвергают взаимодействию со смесью из (галогенорганил)алкоксисилана и (галогенорганил)галогенсилана в спирте в условиях, исключающих доступ воздуха, и при повышенном давлении. 1 н. и 8 з.п. ф-лы.
1. Способ получения (меркаптоорганил)алкоксисиланов общей формулы I
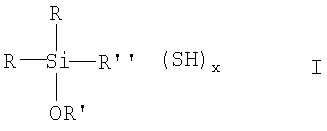
где x обозначает 1,
R оба имеют идентичные или разные значения и представляют собой алкильную группу с 1-8 С-атомами или группу OR',
R' имеет идентичные или разные значения и представляет собой разветвленную или неразветвленную, содержащую одинарную связь C1-C24алкильную группу,
R'' представляет собой разветвленную или неразветвленную, алифатическую, содержащую двойную связь C1-C30углеводородную группу, необязательно замещенную фтором, хлором, бромом или йодом,
отличающийся тем, что сульфид щелочного металла подвергают взаимодействию со смесью из (галогенорганил)алкоксисилана и (галогенорганил)галогенсилана в спирте в условиях, исключающих доступ воздуха, и при повышенном давлении.
2. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что в качестве (галогенорганил)алкоксисилана применяют соединения общей формулы II
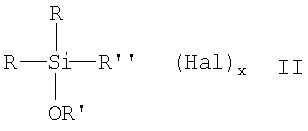
где R оба имеют идентичные или разные значения и представляют собой алкильную группу с 1-8 С-атомами или группу OR'',
R' имеет идентичные или разные значения и представляет собой разветвленную или неразветвленную, содержащую одинарную связь C1-C24алкильную группу,
R'' представляет собой разветвленную или неразветвленную, алифатическую, содержащую двойную связь C1-C30углеводородную группу, необязательно замещенную фтором, хлором, бромом, йодом,
x обозначает 1,
Hal обозначает хлор, бром, фтор или йод.
3. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что в качестве (галогенорганил)галогенсилана применяют соединения общей формулы III
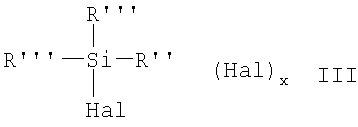
где x, Hal, R и R'' имеют значения, указанные для формулы II, а оба R''' имеют идентичные или разные значения и представляют собой R или Hal.
4. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что молярное соотношение между (галогенорганил)алкоксисиланом и (галогенорганил)галогенсиланом составляет от 0,001:1 до 2:1.
5. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что молярное соотношение между гидролизуемыми Si-галогеновыми функциональными группами в смесях из (галогенорганил)алкоксисилана и (галогенорганил)галогенсилана и сульфидом щелочного металла составляет от 1:0,51 до 1:1,2.
6. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что в качестве сульфида щелочного металла применяют дилитийсульфид (Li2S), динатрийсульфид (Na2S) или дикалийсульфид (K2S).
7. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что в качестве спирта применяют первичные, вторичные или третичные спирты с 1-24 атомами углерода.
8. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что в начале реакции, и/или в ходе реакции, и/или в конце реакции к реакционной смеси добавляют полярные, протонные, апротонные, основные или кислотные аддитивы.
9. Способ получения (меркаптоорганил)алкоксисиланов по п.1, отличающийся тем, что реакцию проводят при температурах в интервале от 0 до 180°С.
| US 5840952 А, 24.11.1998 | |||
| US 5107009 А, 21.04.1992 | |||
| Способ получения бис(триалкоксилилалкил) сульфидов | 1974 |
|
SU523101A1 |
Авторы
Даты
2009-07-10—Публикация
2004-11-05—Подача