Изобретение относится к области химии нитрометильных производных гетероцикла 1,3,5-триазина, конкретно - к способу получения 2,4-диарилокси-6-тринитрометил-1,3,5-триазинов общей формулы:
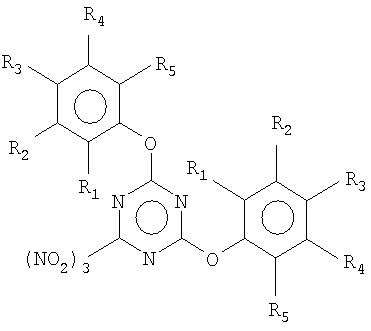
где R1-R5=H; Alk; F; Cl; Вr; I; NO2; COOAlk.
2,4-Диарилокси-6-тринитрометил-1,3,5-триазины могут использоваться в качестве биологически активных веществ и полупродуктов в синтезе биологически активных веществ [1, 2] [1. Бахарев В.В., Гидаспов А.А. Замещение тринитрометильной группы в 2-R-4,6-бис(тринитрометил)-1,3,5-триазинах под действием различных нуклеофилов // Известия Самарского научного центра РАН. Спецвыпуск «Химия и химическая технология». - Самара, СНЦ РАН. - 2004. - С.190-197. 2. Гидаспов А.А., Бахарев В.В., Качановская Е.В. и др. Синтез и цитотоксическая активность галогендинитрометильных производных 1,3,5-триазина // Хим.-фарм. журн. - 2004. - Т.38. - №8. - С.9-15].
Известный способ (способ-аналог; способ-прототип не обнаружен) введения арилоксигрупп в цикл 1,3,5-триазина заключается во взаимодействии производных 1,3,5-триазина с фенолом или замещенными фенолами, протекающем в присутствии оснований. Взаимодействие 2,4,6-трихлор-1,3,5-триазина (цианурхлорида) с фенолом и замещенными фенолами в среде органических растворителей в присутствии оснований сопровождается в зависимости от количества взятого в реакцию фенола образованием моно-, ди- и триарилоксизамещенных 1,3,5-триазинов [3, 4] [3. Quirke J.M.E. 1,3,5-Triazines. In Comprehensive Heterocyclic Chemistry. Vol.3. Pt. 2B. (Eds. KatrizkyA.R., Rees C.W.) - Oxford: Pergamon Press, 1984. - P. 457-530. 4. Погосян Г.М., Панкратов В.А., Заплишный В.Н., Мацоян С.Г. Политриазины. - Ер.: Издательство АН АрмССР, 1987. - 615 с.]. Взаимодействие 2-амино(алкокси)-4,6-бис(тринитрометил)-1,3,5-триазинов с фенолом и замещенными фенолами в среде органических растворителей в присутствии оснований сопровождается образованием 2-амино(алкокси)-4-арилокси-6-тринитрометил-1,3,5-триазинов [1]. Таким образом, известны способы получения арилоксипроизводных 1,3,5-триазина, содержащих две арилоксигруппы в сочетании с другим заместителем (но не тринитрометильной группой) и содержащих одну арилоксигруппу и одну тринитрометильную группу в сочетании с другими заместителями (но не арилоксигруппой). Однако получение 2,4-диарилокси-6-тринитрометил-1,3,5-триазинов по способу-аналогу в литературе не описано.
Техническим результатом изобретения является получение 2,4-диарилокси-6-тринитрометил-1,3,5-триазинов непосредственно из цианурхлорида в одну стадию. Технический результат достигается проведением реакции между цианурхлоридом, солями тринитрометана и фенолом или замещенными фенолами в органическом растворителе.
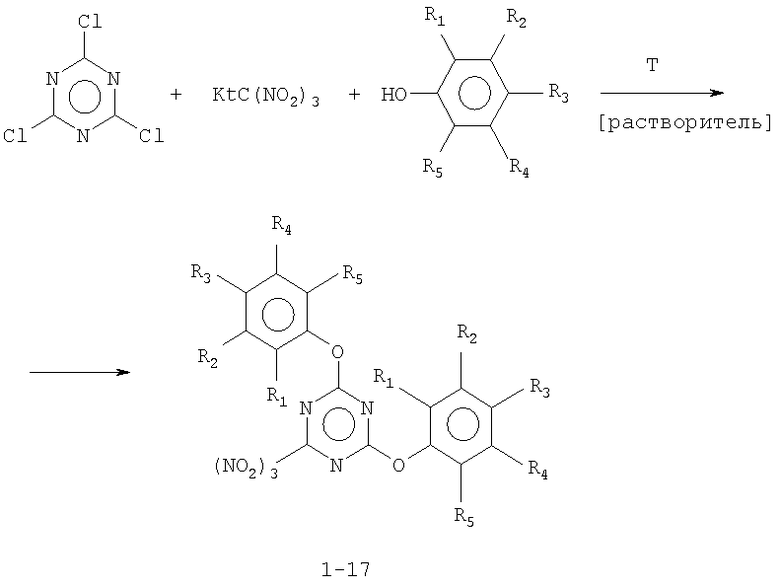
R1-R5=H (1,33%); R1=СН3, R2-R5=H (2,20%); R1=COOCH3, R2-R5=H (3,20%); R1=I, R2-R5=H (4,25%); R1=Cl, R2-R5=H (5,23%); R1=NO2, R2-R5=H (6,35%); R1=H, R2=СН3, R3-R5=H (7,40%); R1=H, R2=COOCH3, R3-R5=Н (8,54%); R1=H, R2=Cl, R3-R5=H (9,52%); R1=H, R2=NO2, R3-R5=Н (10,59%); R1-R2=H, R3=СН3, R4-R5=H (11,49%); R1-R2=H, R3=С(СН3)3, R4-R5=H (12,50%); R1-R2=H, R3=Сl, R4-R5=H (13,56%); R1-R2=H, R3=Вr, R4-R5=H (14,60%); R1-R2=H, R3=СООСН3, R4-R5=H (15,56%); R1-R2=H, R3=NO2, R4-R5=H (16,65%); R1=NO2, R2=H, R3=NO2, R4-R5=H (17,27%).
Kt+=K+, Na+, NH4 +, (C2H5)2NH2 +, (C2H5)3NH+, (CH3)4N+, (C2H5)3CH3N+, (C2H5)4N+ T: -20°C ÷ +40°C; τ=18-160 часов; растворитель: ацетонитрил, ацетон; ЦХ:KtС(NO2)3:фенол = 1:4:2-3,5 (в молях).
Выход 2,4-диарилокси-6-тринитрометил-1,3,5-триазинов составляет 20-65% от теории. В качестве органических растворителей для проведения реакции можно использовать ацетонитрил, ацетон. Реакцию можно проводить при температурах от -20°С до +40°С. Порядок смешения реактантов (цианурхлорид, соль тринитрометана, фенол или замещенные фенолы) не имеет существенного значения.
Для лучшего понимания предлагаемого способа рассмотрим пример синтеза 2,4-диарилокси-6-тринитрометил-1,3,5-триазинов.
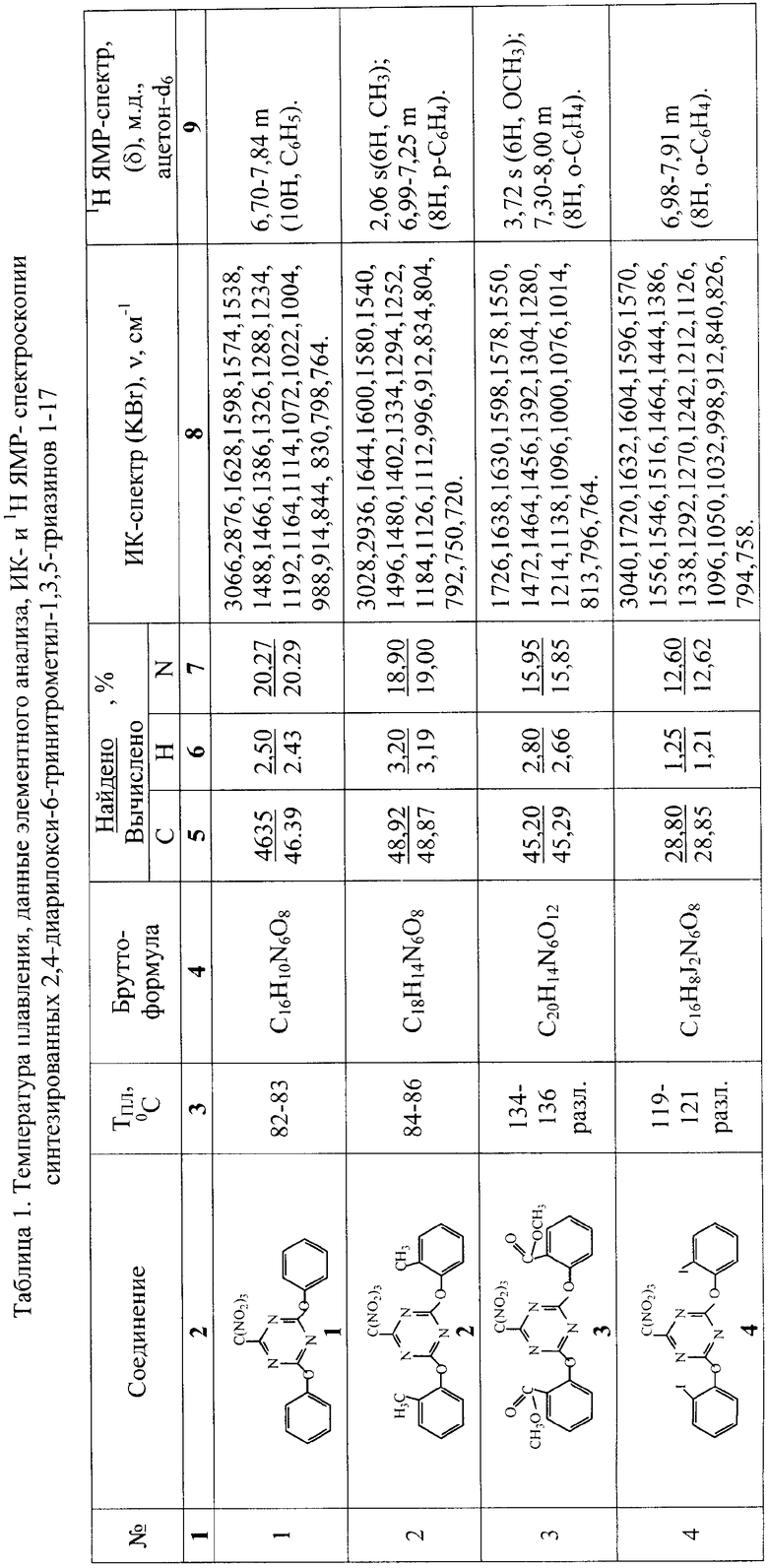
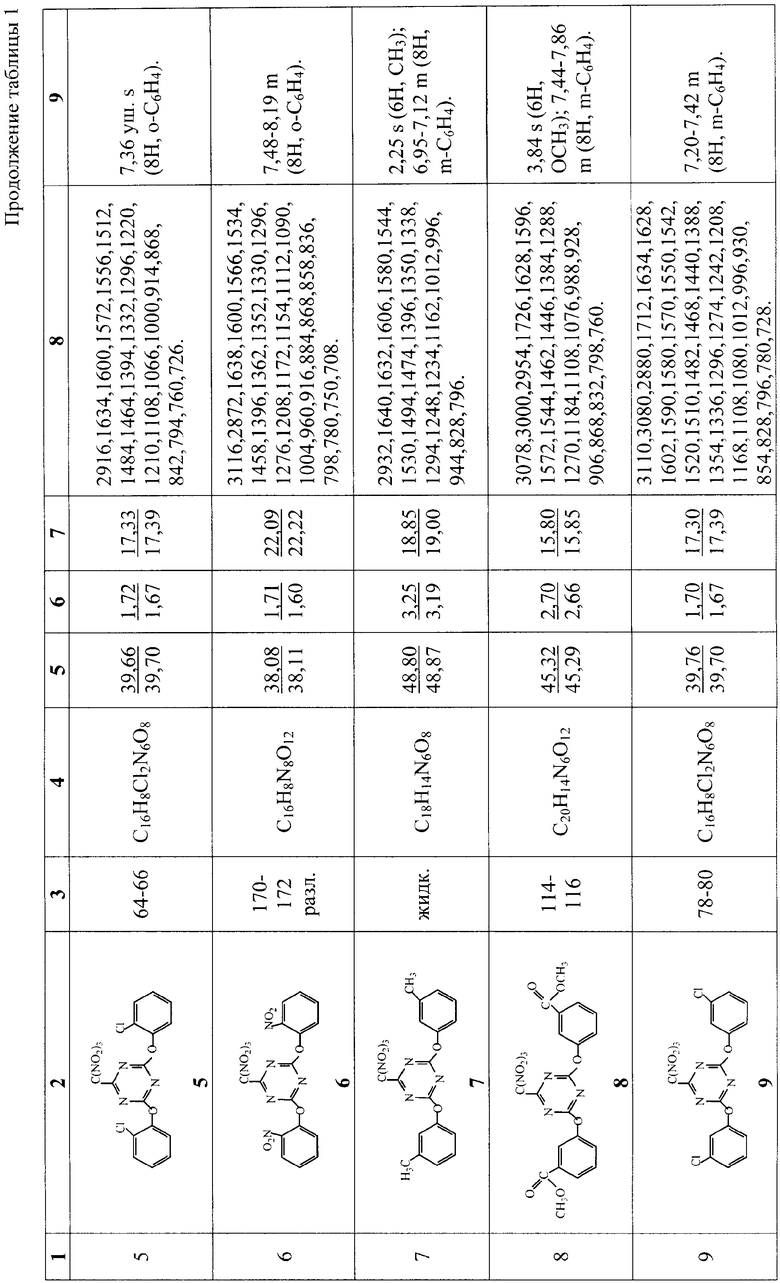
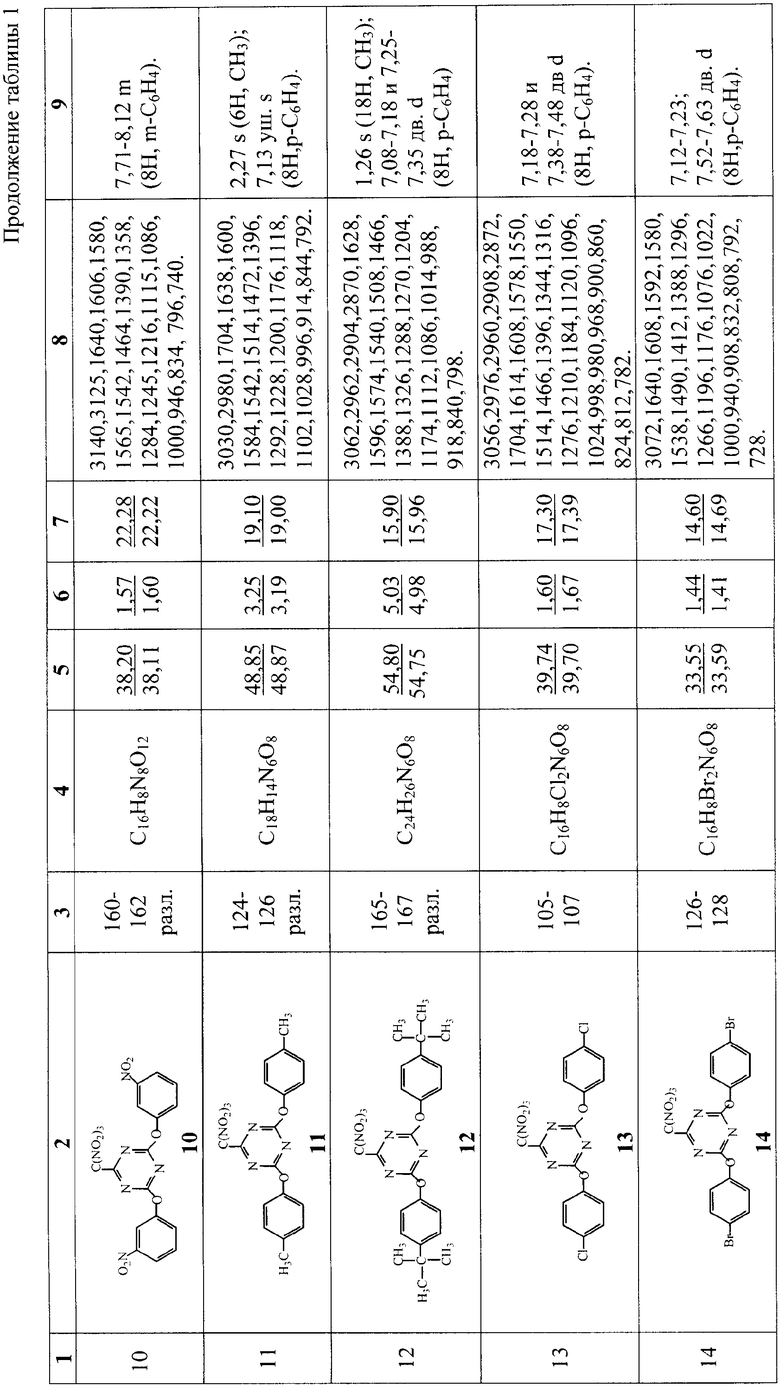
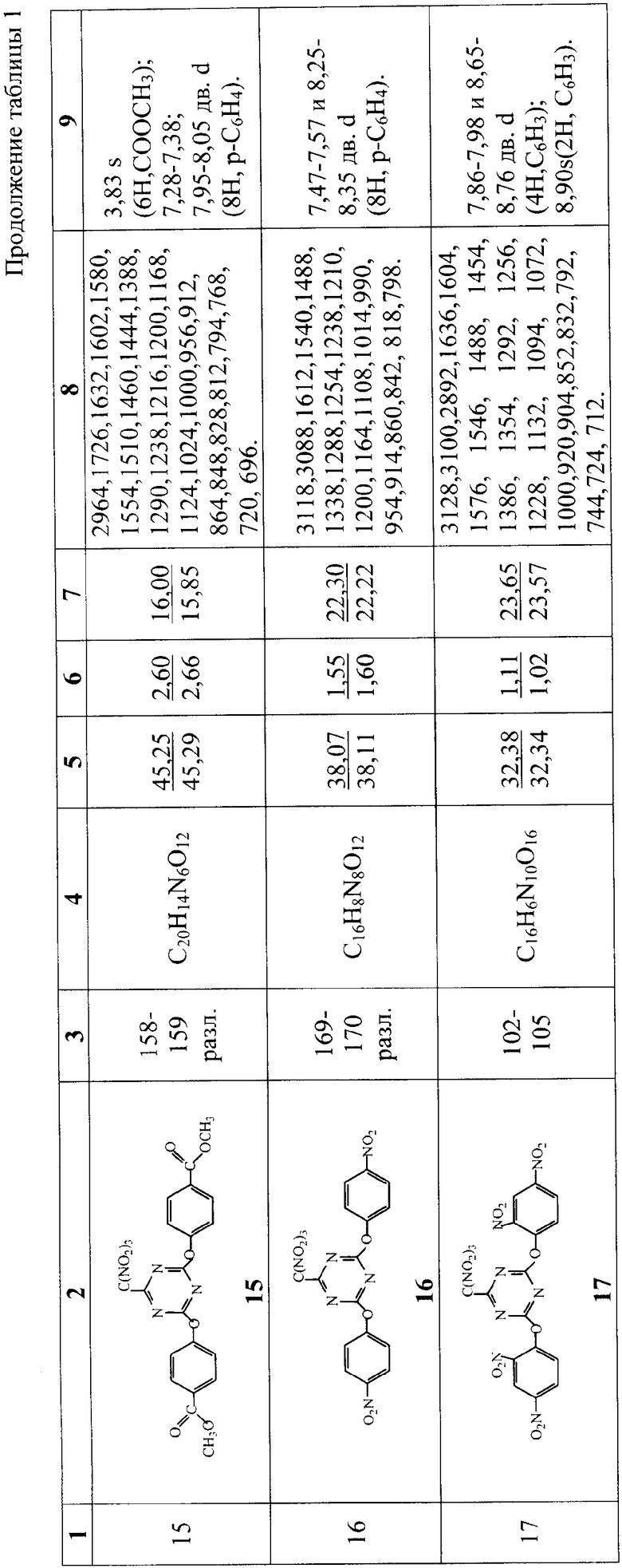
Пример 1. К раствору 1,84 г (0,01 моль) цианурхлорида в 16 мл ацетона при перемешивании и температуре 18-22°С присыпают 0,04 моля соли тринитрометана Kt+C(NO2)3 -, прибавляют 0,03 моля фенола или замещенного фенола, выдерживают при температуре 18-22°С до исчезновения по ТСХ цианурхлорида. Реакционную массу отфильтровывают и выливают фильтрат в 160 мл воды. Выпавший осадок отфильтровывают, несколько раз промывают на фильтре водой и перекристаллизовывают из изопропанола. В табл.1 приведены температуры плавления, данные элементного анализа, ИК- и 1Н ЯМР-спектроскопии синтезированных 2,4-диарилокси-6-тринитрометил-1,3,5-триазинов 1-17, подтверждающие строение полученных соединений. ИК-спектры сняты на приборе Specord M80 в таблетках КВr. 1Н ЯМР-спектры сняты на приборе Bruker WP 80DS (80 МГц, внутренний стандарт ГМДС, растворитель - ацетон-d6).
Таким образом, предлагаемый способ позволяет:
- получать 2,4-диарилокси-6-тринитрометил-1,3,5-триазины из цианурхлорида, солей тринитрометана и фенола или замещенных фенолов в одну стадию.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-АМИНО-4,6-БИС(ТРИНИТРОМЕТИЛ)-1,3,5-ТРИАЗИНОВ | 2006 |
|
RU2330026C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4-ДИАЛКОКСИ-6-ТРИНИТРОМЕТИЛ-1,3,5-ТРИАЗИНОВ | 2006 |
|
RU2371435C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАТРИЕВЫХ СОЛЕЙ 5-NRR-ТЕТРАЗОЛО[1,5-a]-1,3,5-ТРИАЗИН-7-ОНОВ | 2009 |
|
RU2433130C2 |
| ПРОИЗВОДНЫЕ 2-R1-4-R2-6-ПОЛИНИТРОМЕТИЛ-1,3,5-ТРИАЗИНОВ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2541525C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ГЕРБИЦИДНОГО СОСТАВА | 2007 |
|
RU2343708C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ГЕРБИЦИДНОГО СОСТАВА | 1993 |
|
RU2034467C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ГЕРБИЦИДНОГО СОСТАВА | 2007 |
|
RU2344600C1 |
| ПРОИЗВОДНЫЕ 1,3,5-ТРИАЗИНА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1999 |
|
RU2252937C2 |
| СОЕДИНЕНИЯ ЗАМЕЩЕННОГО ПИРАЗОЛА, СОДЕРЖАЩЕГО ПИРИМИДИНИЛ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2016 |
|
RU2687089C2 |
| ДИСПЕРСНЫЕ АЗОКРАСИТЕЛИ | 2004 |
|
RU2376334C2 |
Описывается новый способ получения 2,4-диарилокси-6-тринитрометил-1,3,5-
триазинов общей формулы

где R1-R5=H; C1-6алкил, F; Cl; Br; I; NO2; COOAlk, заключающийся в том, что цианурхлорид, соль тринитрометана
Kt+C(NO2)3 -, где Кt+ - катион и R1, R2, R3, R4, R5 - замещенный фенол, где R1-R5 имеют вышеуказанные значения, подвергают взаимодействию в среде инертного органического растворителя, такого как ацетон или ацетонитрил. Полученные соединения могут использоваться в качестве биологически активных веществ и/или полупродуктов в синтезе последних. Способ осуществляют в одну стадию с выходом 20-65% целевого продукта. 1 табл.
Способ получения 2,4-диарилокси-6-тринитрометил-1,3,5-триазинов общей формулы
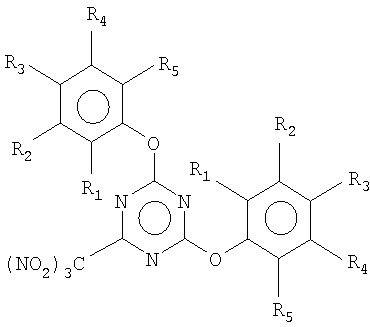
где R1-R5=H; C1-6алкил, в том числе разветвленный; F; Cl; Br; I; NO2; COOAlk, заключающийся в том, что цианурхлорид, соль тринитрометана Kt+C(NO2)3-, где Кt+ - катион, и фенол или R1, R2, R3, R4, R5 - замещенный фенол, где R1-R5 имеют вышеуказанные значения, подвергают взаимодействию в среде инертного органического растворителя, такого как ацетон или ацетонитрил.
| Гидаспов А.А | |||
| и др | |||
| Химико-фармацевтический журнал, 2004, т.38, № 8, с.9-15 | |||
| Погосян Г.М | |||
| и др | |||
| Политриазины, издательство АН Арм | |||
| ССР, 1987, с.615 | |||
| RU 95108543 А1, 27.12.1996 | |||
| ЕР 545149 А1, 09.06.1993. |
Авторы
Даты
2009-07-20—Публикация
2007-03-09—Подача