Изобретение относится к области биотехнологии и может быть использовано при промышленном производстве высокоиммуногенных, безвредных, удобных в применении жидких вакцин против бешенства животных.
Вакцина антирабическая для животных (УНИРЭВ), включающая вируссодержащую культуральную жидкость, содержащую инактивированный вирус бешенства штамм Щелково-51, репродуцированный в культуре перевиваемых клеток ВНК-21 и гидроокись алюминия (ГОА), отличающаяся тем, что она дополнительно содержит в своем составе этанол при следующем соотношении компонентов (мас.%):
Этанол в составе жидкой антирабической вакцины выполняет роль безвредного консерванта, который практически полностью исключает вероятность активации и размножения микрофлоры во флаконах с готовой продукцией (табл.1), куда она может случайно попасть (например, при расфасовке) и не всегда выявляться при производственном бактериологическом и биологическом контролях. При этом отпадает необходимость введения в состав жидких антирабических вакцин антибиотиков, производных ртути и других не безвредных в индивидуальном и экологическом плане консервантов.
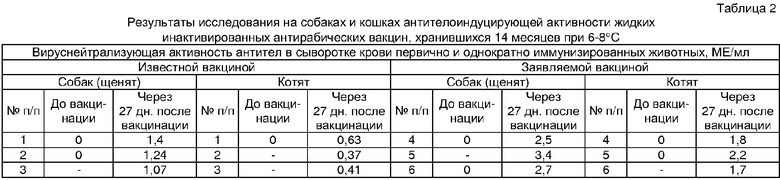
Кроме того, этанол повышает антителоиндуцирующую активность жидкой антирабической вакцины для целевых животных (в частности собак и кошек) и, следовательно, степень их защищенности от вируса бешенства (табл.2). Возможно, это связано с воздействием этанола на нервные рецепторы в местах введения препарата и притока к ним большего количества антигенпредставляющих клеток в ответ на соответствующий сигнал со стороны более возбужденной и информированной ЦНС.
Изобретение относится к области ветеринарной биотехнологии и может быть использовано при промышленном производстве высокоиммуногенных, безвредных, удобных в применении жидких вакцин против бешенства животных.
Известна сухая мозговая вакцина против бешенства животных, включающая вируссодержащую суспензию тканей головного мозга овец, зараженных вирусом бешенства штамм «Овечий», отличающаяся тем, что инактивацию вируса проводят 20-21% раствором этанола при 30-31°С в течение 12-14 суток. Затем добавляют защитную среду высушивания и полученную смесь подвергают сублимационному высушиванию (SU 770196 А, А61К 39/205, 1983). Естественно, что при высушивании вместе с влагой из препарата полностью удаляется этанол. Таким образом, этанол присутствует в составе вакцины только на стадии ее изготовления.
Недостатком известной вакцины является наличие в ее составе опасной энцефалитогенной ткани мозга овец, вызывающей поствакцинальные осложнения у прививаемых животных. Кроме этого из-за значительной инфицированности овец возбудителем скрейпи существует большая вероятность его попадания с мозговой тканью в состав изготовляемой вакцины и, как следствие этого, распространения прионовой инфекции среди прививаемого поголовья животных.
Известна также сухая культуральная вакцина для профилактики бешенства крупного рогатого скота, содержащая инактивированный β-пропиолактоном вирус бешенства штамм «Щелково-51», репродуцированный в культуре перевиваемых клеток ВНК-21, защитную среду высушивания и стимулятор иммунитета - сапонин (RU 955577 А, А61К 39/205, (46) 15.08.1994). Вакцина обладает высокой иммуногенной активностью, но содержит сапонин, который является токсичным для многих животных (собак, кошек, лошадей, свиней и др.). Поэтому ее применяют только для иммунизации мелкого и крупного рогатого скота.
Наиболее близким аналогом является широко применяемая в настоящее время вакцина антирабическая инактивированная жидкая культуральная «Рабиков», изготовляемая по способу RU 2191600 C1 А61К 39/205 (46) 27.10.2002), включающая вируссодержащую культуральную жидкость, содержащую инактивированный вирус бешенства штамм «Щелково-51», репродуцированный в культуре перевиваемых клеток ВНК-21 и гидроокись алюминия (ГОА) (Каталог лекарственных сред для животных, Торговый дом Биопром, М., 2004 г., стр.135). В отличие от сапонина ГОА не токсичен и вакцина может применяться для всех видов животных. Однако ее иммуностимулирующая активность не во всех случаях проявляется на уровне, обеспечивающим появление в крови первично однократно вакцинированных животных антител с активностью 0,5 МЕ/мл, признанной ВОЗ достаточной для защиты животных от бешенства (табл.2).
Недостатком аналога является также отсутствие в составе вакцины санкционированного консерванта, способного снять угрозу поствакцинальных осложнений при случайном применении препарата с активизированной в процессе хранения микрофлорой.
Задачей изобретения является совершенствование жидкой вакцины против бешенства животных.
Технический результат изобретения заключается в повышении безопасности и иммуногенности жидкой антирабической вакцины за счет введения в ее состав этанола.
Сущность изобретения. Вакцина антирабическая для животных УНИРЭВ, включающая вируссодержащую культуральную жидкость, содержащую инактивированный вирус бешенства штамм Щелково-51, репродуцированный в культуре перевиваемых клеток ВНК-21 и гидроокись алюминия (ГОА), отличающаяся тем, что она дополнительно содержит в своем составе этанол при следующем соотношении компонентов (мас.%):
Этанол в указанных концентрациях надежно предохраняет жидкую вакцину от бактериального пророста (табл.1). Кроме того, этанол повышает антителоиндуцирующую активность антирабической вакцины для целевых животных и, следовательно их защищенность от заболевания бешенством (табл.2).
Вакцина (УНИРЭВ), изготовленная по заявляемому способу универсальна, более безопасна в применении и обладает большей иммуногенностью. Ее применение позволит с большей эффективностью защищать животных от бешенства.
Изобретение иллюстрируется следующими примерами.
Пример 1. Культивирование зараженных вирусом бешенства клеток ВНК-21 осуществляют роллерным или псевдосуспензионным способами при температуре 37°С. В качестве ростовой и поддерживающей сред используют питательные среды Игла и 199 с добавлением нативной сыворотки крупного рогатого скота. Сбор вируссодержащей культуральной жидкости проводят через 3, 4, 5 и 6 суток культивирования. Замену питательной среды делают после каждого сбора вируса (вируссодержащей жидкости).
К 8 л вируссодержащей культуральной жидкости, содержащей вирус бешенства штамм Щелково-51, охлажденной до 4°С, добавляют при постоянном перемешивании 2,0 мл β-пропиолактона. Затем через 2 ч добавляют к ней 1,17 л 96%-ного этилового спирта ректификата и 2 л 6%-ного геля гидроокиси алюминия (ГОА). В результате получают заявляемую инактивированную этаноловую вакцину (УНИРЭВ), содержащую 71,63 мас.% вируссодержащей культуральной жидкости, 10,47 мас.% 96%-ного этилового спирта (10% чистого этанола) и остальное ГОА (17,9 мас.%).
Пример 2. Вирус бешенства, приготовленный как в примере 1, инактивируют УФ-светом при постоянном потоке вируссодержащей культуральной жидкости по поверхности лампы типа БУВ-30 из увиолетового стекла. Толщина слоя облучаемого материала составляет не более 0,5 мл, время облучения - 10 сек.
К 10 л культуральной жидкости, содержащей инактивированный УФ-светом вирус бешенства штамм Щелково-51, добавляют 1,3 л 96%-ного этилового спирта ректификата и 2,6 л 6%-ного ГОА. В результате получают заявляемую инактивированную этаноловую вакцину (УНИРЭВ), содержащую 71,94 мас.% вируссодержащей культуральной жидкости, 9,35 мас.% 96%-ного этилового спирта (9% чистого этанола) и остальное ГОА (18,7 мас.%).
Пример 3. Вирус бешенства, приготовленный как в примере 1, инактивируют этанолом. Для этого к 10 л культуральной жидкости добавляют при постоянном перемешивании 1,6 л 96%-ного этилового спирта ректификата. Получают смесь, содержащую 13,79% 96%-ного этанола. Смесь выдерживают 20 ч при 36-37°С для инактивации инфекционности вируса бешенства. Затем к инактивированному вирусу (вируссодержащей культуральной жидкости) добавляют 2,35 л 6%-ного ГОА. В результате получают заявляемую инактивированную этаноловую вакцину, содержащую 71,68 мас.% вируссодержащей культуральной жидкости, 11,47% 96%-ного этилового спирта (11% чистого этанола) и остальное ГОА (16,85 мас.%).
Для изготовления аналога используют тот же (предварительно отобранный из одной емкости) вирус, что и для изготовления заявляемой вакцины. К 10 л культуральной жидкости, содержащей вирус бешенства «Щелково-51», репродуцированный в культуре перевиваемых клеток ВНК-21, охлажденной до 4°С, добавляют при постоянном перемешивании 2,5 мл β-пропиолактона, затем через 2 часа добавляют 2,3 л ГОА. В результате получают известный препарат, содержащий 18,7 мас.% ГОА.
Приготовленные препараты не содержат в своем составе живого вируса бешенства и обладают практически одинаковой иммуногенной потенцией (2,53; 2,45; 2,50 и 2,47 МЕ/мл соответственно) при испытании их на мышах рекомендованным ВОЗ методом NIH (национальных институтов здоровья США). Однако для наиболее опасных для человека целевых животных (собак и кошек) предлагаемая вакцина обладает намного большей антителоиндуцирующей активностью, чем аналог (табл.2). Поэтому она с большей надежностью будет защищать их и, как следствие этого, человека от бешенства.
В процессе хранения предлагаемая вакцина более защищена от случайных контаминантов по сравнению с аналогом (табл.1).
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА АНТИРАБИЧЕСКАЯ СУХАЯ ДЛЯ КРУПНОГО И МЕЛКОГО РОГАТОГО СКОТА | 2009 |
|
RU2402348C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 2001 |
|
RU2191600C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 2005 |
|
RU2287343C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ ИНАКТИВИРОВАННОЙ КУЛЬТУРАЛЬНОЙ | 1994 |
|
RU2077338C1 |
| Вакцина антирабическая инактивированная эмульсионная культуральная для профилактической иммунизации домашних плотоядных и сельскохозяйственных животных | 2019 |
|
RU2722868C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНАКТИВИРОВАННОЙ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ ПРИ БЕЗОПОРНОМ ВЫРАЩИВАНИИ КЛЕТОК И РЕПРОДУКЦИИ В НИХ ВИРУСА В УКОРОЧЕННОМ ЦИКЛЕ КУЛЬТИВИРОВАНИЯ | 2012 |
|
RU2537183C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 2013 |
|
RU2538617C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ ПРОТИВ БЕШЕНСТВА ЖИВОТНЫХ | 1997 |
|
RU2134590C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ АНТИРАБИЧЕСКОЙ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ ДЛЯ СЕЛЬСКОХОЗЯЙСТВЕННЫХ ЖИВОТНЫХ | 2003 |
|
RU2244557C2 |
| СПОСОБ КОНТРОЛЯ ПОЛНОТЫ ИНАКТИВАЦИИ АНТИРАБИЧЕСКОЙ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ | 2012 |
|
RU2492452C1 |
Изобретение относится к области биотехнологии. Вакцина включает вируссодержащую культуральную жидкость, содержащую инактивированный вирус бешенства штамм Щелково-51, репродуцированный в культуре перевиваемых клеток ВНК-21 и гидроокись алюминия (ГОА). Дополнительно вакцина содержит в своем составе этанол при следующем соотношении компонентов (мас.%): вируссодержащая культуральная жидкость, содержащая инактивированный вирус бешенства штамм Щелково-51, репродуцированный в культуре перевиваемых клеток ВНК-21 - 70-80, этанол - 9-11, гидроокись алюминия - остальное. Этанол в указанных концентрациях надежно предохраняет жидкую вакцину от бактериального пророста. Кроме того, этанол повышает антителоиндуцирующую активность антирабической вакцины для целевых животных (собак, кошек) и, следовательно, их защищенность от заболевания бешенством. 2 табл.
Вакцина антирабическая для животных, включающая вируссодержащую культуральную жидкость, содержащую инактивированный вирус бешенства штамм Щелково-51, репродуцированный в культуре перевиваемых клеток ВНК-21, и гидроокись алюминия (ГОА), отличающаяся тем, что она дополнительно содержит в своем составе этанол при следующем соотношении компонентов, мас.%:
| СПОСОБ ПОЛУЧЕНИЯ АНТИРАБИЧЕСКОЙ ВАКЦИНЫ | 2001 |
|
RU2191600C1 |
| SU 955577 A1, 15.08.1994 | |||
| US 4664912 A, 12.05.1987 | |||
| US 4347239 A, 31.08.1982. | |||
Авторы
Даты
2009-09-10—Публикация
2008-02-27—Подача