Изобретение относится к области металлургии высокочистых сталей и металлических материалов, используемых в качестве имплантатов в различных областях хирургии, в частности в травматологии, ортопедии и стоматологии. Основными требованиями, предъявляемыми к таким материалам, являются биосовместимость, высокие антикоррозионные и прочностные свойства.
Многолетний опыт применения известных нержавеющих сталей (типа 316 по AISI) в травматологии показал, что они часто не удовлетворяют требованиям, предъявляемым травматологами, стоматологами и ортопедами к сталям, имплантируемым в человеческий организм на продолжительный период времени. В принципе, введение основных легирующих компонентов (хром, никель, молибден) уже обеспечивает достижение приемлемых механических свойств и удовлетворительных показателей химической инертности (потенциал питтингообразования ниже 1 В). Несмотря на большое значение химического состава сталей, выражающееся в оптимальном соотношении легирующих компонентов и низком содержании примесей внедрения, только за счет подбора химического состава и введения тех или иных добавок высокие значения как потенциала питтингообразования, так и других показателей нержавеющих сталей реализовать не удается в принципе. Иными словами, качество нержавеющих сталей для имплантатов складывается из двух основных факторов: оптимального химического состава и комплексной металлургической обработки. Последняя состоит из первичной выплавки стали и горячей деформационной обработки слитков. Как правило, первичную выплавку нержавеющих сталей производят в электродуговых или вакуумных индукционных печах, в некоторых случаях производят финишное вакуумирование расплава в ковше или в процессе разливки.
Из описанных в литературе нержавеющих сталей для имплантатов в медицине наиболее близким аналогом является сталь марки «316 по AISI» следующего состава, мас.%:
Сталь после закалки и отжига имеет следующие механические характеристики и антикоррозионные свойства (потенциал питтингообразования в 0,8% растворе NaCl, близком по составу к биологической среде):
После дополнительной деформации со степенью 25-35% при комнатной температуре
Хотя имплантаты из этой стали имеют вполне удовлетворительные характеристики и хорошо зарекомендовали себя при недлительном использовании их в биологической среде (до 1-2 месяцев), при более длительном пребывании в контакте с биологической средой, при знакопеременных нагрузках и существенных электрических потенциалах сталь «316 по AISI» не может противостоять питтинговой коррозии, вследствие чего возникает сильное отрицательное влияние инфицированной среды вокруг имплантата со следами коррозии на процесс регенерации окружающих тканей. Кроме того, имплантаты, изготовленные из аналогичных сталей, не выдерживают отдельные виды нагрузок и известно много случаев их разрушения особенно при лечении костных переломов.
Близким аналогом для изготовления имплантатов является нержавеющая сталь (Патент РФ №2233907, 08.10.2004), в которой выдержано следующее соотношение химических компонентов, мас.%:
Применение этой стали для изготовления имплантатов краткосрочного использования демонстрирует более высокие эксплуатационные характеристики, в частности коррозионную стойкость, по сравнению со сталью «316 по AISI», но при изготовлении ответственных конструкций или элементов длительного использования не удается избежать питтинговой коррозии.
Однако эксперименты, проведенные авторами, показали, что односторонний подход к решению проблемы питтинговой коррозии имплантатов только за счет подбора оптимального химического состава не может быть эффективным в принципе. Одним из существенных недостатков нержавеющих сталей является относительно высокая чувствительность к поверхностной питтинговой коррозии. Установлено, что количество микроочагов (питов) коррелирует с содержанием в объеме и на поверхности стали неметаллических микровключений, являющихся продуктами раскисления (финишной операции при производстве стали), и микродефектов структуры затвердевшего металла (газовые поры, микротрещины, границы зерен, примесные атмосферы на дефектах решетки). Снижение объема второй фазы приводит к уменьшению и даже к исключению случаев питтинговой коррозии на поверхности имплантатов, выполненных из нержавеющей стали. Оптимальным путем снижения объема неметаллических включений оказался дополнительный вакуумный переплав стали, полученной по любой известной плавильной технологии (индукционная вакуумная плавка, электродуговая вакуумная плавка и др.). Из уровня техники известны технологии производства чистой стали (SU 855007 А, С22В 9/22, 15.08.1981), которую дополнительно рафинируют в вакуумных электронно-лучевых печах. В принципе, эту технологию можно использовать для глубокой очистки любой стали, в т.ч. и нержавеющей.
Несколько иной путь снижения дефектности литой нержавеющей стали предложен в способе производства хирургических имплантатов из литой аустенитной нержавеющей стали (Патент США №847929, 04.10.1988). Он заключается в том, что получают отливку увеличенного размера, подвергаемую «теплой» ковке до получения изделия финишных размеров и формы. Использование литой стали в качестве исходного материала с последующим уменьшением размеров в результате «теплой» ковки существенно уменьшает пористость материала и соответственно повышает механические и антикоррозионные характеристики имплантата по сравнению с обычными технологиями. В той или иной мере недостатки при реализации известных способов состоят в том, что исключаются только определенные микродефекты (поры, трещины), сохраняются практически все неметаллические микровключения (вторая фаза), а содержание газовых примесей сильно повышается.
Задачей настоящего изобретения является повышение прочностных и антикоррозионных свойств стали за счет проведения дополнительного электронно-лучевого вакуумного переплава слитка нержавеющей стали, полученного одним из традиционных способов выплавки, проведения комплексной термомеханической обработки и введения дополнительных легирующих химических элементов, оптимизирующих механические свойства стали после соответствующей термомеханической обработки. Большое значение при этом имеет именно второй вакуумный переплав первичной литой нержавеющей стали в электронно-лучевой печи, когда осуществляется глубокая очистка расплава в тонкопленочном капельном режиме, эффективно происходит вакуумное раскисление, дегазация расплава и удаление неметаллических включений.
Поставленная задача, в результате решения которой достигаются высокие характеристики нержавеющей стали для изготовления имплантатов, реализуется таким образом, что в способе получения нержавеющей стали для изготовления хирургических имплантатов, включающем выплавку в вакуумной индукционной печи с финишным раскислением расплава и получением первичной литой нержавеющей стали, дополнительный вакуумный переплав первичной литой нержавеющей стали осуществляют в электронно-лучевой печи с получением слитка, который подвергают комплексной термомеханической обработке, включающей скоростное прессование, закалку при 1100-1150°С в воду, деформацию при 20°С или 600°С с обжатием 30%, старение при 600°С в течение 100 часов.
Достижение указанного результата осуществляется также благодаря тому, что предлагаемая нержавеющая сталь дополнительно содержит титан, иттрий и лантан при следующем соотношении компонентов, мас.%:
Как показали эксперименты, в результате этих процедур значительно улучшается структура стали и происходит измельчение зерен, что способствует более равномерному распределению упрочняющей фазы в аустените. Вследствие этого отсутствуют условия для концентрации напряжений, приводящих к возникновению трещин. Более низкое содержание таких элементов как марганец, сера и газовые примеси, по сравнению с их содержанием в известных сталях, а также меньший объем неметаллических микровключений и других микродефектов комплексно обеспечивают высокую коррозионную стойкость предложенной стали.
Пример
Для проверки эксплуатационных характеристик было выплавлено три плавки. Химический состав трех слитков этих плавок нержавеющей стали приведен в таблице 1. Видно, что охвачен практически весь диапазон предложенного химического состава.
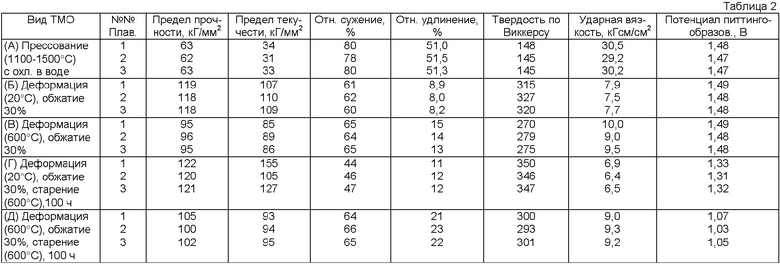
Экспериментальные технологии приготовления образцов предложенной стали включают выплавку в вакуумной индукционной печи с финишным раскислением расплава, дополнительное рафинирование в электронно-лучевой печи с повышенной скоростью плавки, скоростное прессование, термическую обработку, заключающуюся в закалке при температуре 1100-1150°С в воду, и последующую деформацию при 20°С или 600°С с обжатием 30%. После деформации образцы подвергнуты старению при 600°С в течение 100 часов. Механические характеристики и антикоррозионные свойства (потенциал питтингообразования в растворе 0,8% NaCl при 20°С) после указанных комплексных процедур двойного вакуумного переплава и термомеханической обработки (ТМО) представлены в таблице 2. Видно, что в зависимости от вида ТМО существенно изменяются все физико-механические и антикоррозионные характеристики образцов нержавеющей стали, имеющих практически одинаковый химический состав. Это лишний раз доказывает важность всех процедур обработки, описанных выше. Оптимальными с точки зрения изготовления имплантатов являются виды ТМО (Б), (В) и (Г) - высокие прочностные показатели и оптимальные показатели удлинения и сужения, а также потенциала питтингообразования. В зависимости от вида ТМО и физико-механических свойств финишной нержавеющей стали возможно изготовление изделий самого различного назначения, которые нуждаются в различных мех.свойствах: костные накладки, шурупы, спицы, массивные элементы и др.
Проведенные макроскопические и гистологические исследования костных регенератов не выявили никаких отрицательных эффектов предложенного способа получения и химического состава нержавеющей стали. После извлечения имплантатов, находившихся в организмах прооперированных пациентов от 2 до 3 лет, не были обнаружены следы механических или коррозионных повреждений.
Таким образом, предложенный способ получения нержавеющей стали, благодаря своему химическому составу, дополнительному вакуумному переплаву и комплексной термомеханической обработке, позволяет значительно повысить эксплуатационные свойства хирургических имплантатов и существенно ускорить заживление костных переломов различной сложности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА МОЛИБДЕНА ВЫСОКОЙ ЧИСТОТЫ ГЛЕБОВСКОГО | 2007 |
|
RU2351669C1 |
| СПОСОБ ПРОИЗВОДСТВА МОЛИБДЕНА ВЫСОКОЙ ЧИСТОТЫ | 2007 |
|
RU2349657C1 |
| СПОСОБ ПРОИЗВОДСТВА ВОЛЬФРАМА ВЫСОКОЙ ЧИСТОТЫ | 2007 |
|
RU2349658C1 |
| РАСПЫЛЯЕМАЯ МИШЕНЬ ИЗ МОЛИБДЕНА ВЫСОКОЙ ЧИСТОТЫ И СПОСОБ ЕЕ ПРОИЗВОДСТВА | 2007 |
|
RU2365673C2 |
| СОСТАВНАЯ МИШЕНЬ ДЛЯ РАСПЫЛЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2009 |
|
RU2392686C1 |
| РАСПЫЛЯЕМЫЕ МИШЕНИ ИЗ ВЫСОКОЧИСТЫХ СПЛАВОВ НА ОСНОВЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ И СПОСОБ ИХ ПРОИЗВОДСТВА | 2009 |
|
RU2392685C1 |
| АУСТЕНИТНАЯ ЖАРОПРОЧНАЯ И КОРРОЗИОННО-СТОЙКАЯ СТАЛЬ | 2015 |
|
RU2662512C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОЧИСТОГО ТИТАНА ДЛЯ РАСПЫЛЯЕМЫХ МИШЕНЕЙ | 2008 |
|
RU2370559C1 |
| АКСИАЛЬНАЯ ЭЛЕКТРОННАЯ ПУШКА | 2008 |
|
RU2364980C1 |
| Конструкционная криогенная аустенитная высокопрочная коррозионно-стойкая свариваемая сталь и способ ее обработки | 2017 |
|
RU2657741C1 |
Изобретение относится к области металлургии, а именно к нержавеющим корозионно-стойким хромоникелевым аустенитным сталям, предназначенным для изготовления хирургических имплантатов в травматологии, ортопедии и стоматологии. Способ включает выплавку в вакуумной индукционной печи с финишным раскислением расплава и получением первичной литой нержавеющей стали. При этом осуществляют дополнительный вакуумный переплав первичной литой нержавеющей стали в электронно-лучевой печи с получением слитка, который подвергают комплексной термомеханической обработке, включающей скоростное прессование, закалку при 1100-1150°С в воду, последующую деформацию при 20°C или 600°С с обжатием 30%, старение при 600°С в течение 100 часов. Сталь содержит компоненты при следующем соотношении, вес.%: углерод 0,06-0,08, фосфор 0,015-0,02, марганец 0,1-0,3, сера 0,015-0,003, кремний 0,8-1,5, кислород 0,002-0,003, водород 0,0005-0,001, азот 0,002-0,004, хром 16,0-18,0, титан 0,5-0,8, никель 9,0-11,0, молибден 2,0-3,0, лантан 0,023-0,026, иттрий 0,022-0,025, железо остальное. Изобретение позволяет повысить технологичность стали при изготовлении хирургических имплантатов путем повышения плотности, резкого снижения объема микровключений второй фазы и газовых примесей внедрения, вследствие чего происходит повышение физико-механических показателей нержавеющей стали при существенном увеличении потенциала питтингообразования. 2 н.п. ф-лы, 2 табл.
1. Способ получения нержавеющей стали для изготовления хирургических имплантатов, включающий выплавку в вакуумной индукционной печи с финишным раскислением расплава и получением первичной литой нержавеющей стали, отличающийся тем, что осуществляют дополнительный вакуумный переплав первичной литой нержавеющей стали в электронно-лучевой печи с получением слитка, который подвергают комплексной термомеханической обработке, включающей скоростное прессование, закалку при 1100-1150°С в воду, последующую деформацию при 20 или 600°С с обжатием 30%, старение при 600°С в течение 100 ч.
2. Нержавеющая сталь для изготовления хирургических имплантатов, содержащая углерод, марганец, кремний, хром, никель, молибден, фосфор, серу, кислород, водород, азот и железо, отличающаяся тем, что она дополнительно содержит титан, лантан и иттрий при следующем соотношении компонентов, мас.%:
| НЕРЖАВЕЮЩАЯ СТАЛЬ "ДЕНТАЛИТ" ДЛЯ ОРТОПЕДИЧЕСКОЙ СТОМАТОЛОГИИ | 2003 |
|
RU2233907C1 |
| Способ производства особо чистой стали | 1979 |
|
SU855007A1 |
| СПОСОБ ВЫПЛАВКИ СТАЛИ В ВАКУУМНОЙ ИНДУКЦИОННОЙ | 0 |
|
SU377331A1 |
| КОРРОЗИОННОСТОЙКАЯ СТАЛЬ | 1992 |
|
RU2016130C1 |
| Питатель стекловаренной печи | 1978 |
|
SU668889A1 |
| KR 940007374 В, 16.08.1994. | |||
Авторы
Даты
2009-09-20—Публикация
2007-12-11—Подача