Область техники
Настоящее изобретение относится к новому способу получения высокочистого диалкилпеметрекседа формулы (I) с применением реагента, замещенного трифенилфосфата формулы (IV), который является мягким, безопасным, недорогим, неокислительным и простым в обращении реагентом.

где R1 и R2 независимо представляют собой карбоксильные защитные группы.
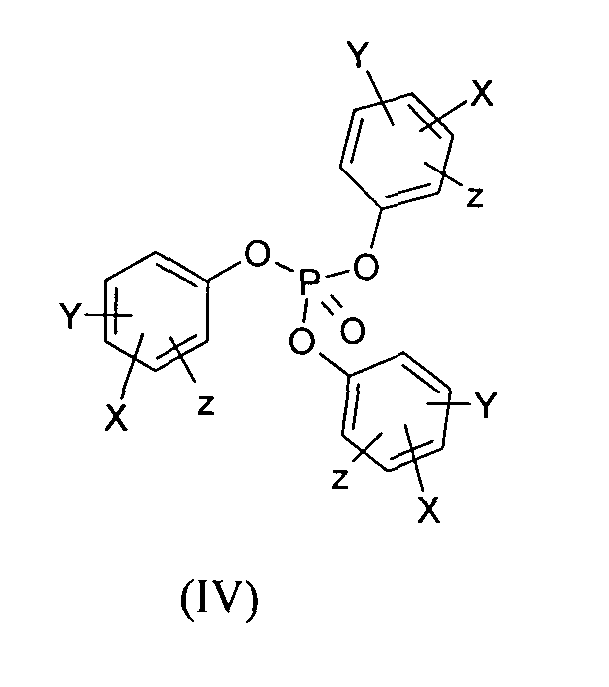
где X представляет собой электроноакцепторную группу; Y и Z независимо представляют собой водород, электроноакцепторную группу, алкил, содержащий 1-7 атомов углерода, алкоксигруппу, содержащую 1-7 атомов углерода, галоген, NR3R4, меркаптогруппу, тиоалкил, содержащий 1-7 атомов углерода, или Y и Z при ортоположении друг к другу образуют бензольное кольцо; R3 и R4 независимо представляют собой водород, алкил, содержащий 1-7 атомов углерода, или R3 и R4 вместе с азотом образуют 3-7-членное гетероциклическое кольцо.
Настоящее изобретение также относится к способу очистки диалкилпеметрекседа формулы (I), путем кристаллизации или порошкования, и его преобразования в высокочистый пеметрексед или его двунатриевую соль.
Область техники
Диалкилпеметрексед формулы (I) является промежуточным соединением в получении пеметрекседа, который представляет собой N{4-[2(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил)этил]бензоил}-L-глутаминовую кислоту. Известно, что пеметрексед обладает антифолатным действием. Двунатриевая соль пеметрекседа является мультицелевым антифолатным агентом, одобренным под торговой маркой Alimta® в качестве единого агента для лечения немелкоклеточного рака легких и в комбинации с цисплатином для лечения пациентов со злокачественной плевральной мезотелиомой.
Европейский патент EP 0334636 раскрывает получение пирролопиримидинглютамата путем конденсации пирролопиримидинилалкилбензойной кислоты с глутаминовой кислотой или ее сложным диэфиром с использованием карбодиимида, дифенилфосфорилазида или фосфороцианидата в качестве конденсирующих агентов, которые являются токсичными и опасными. Количество требуемого реагента составляет 1-20 эквивалентов. Предпочтительным реагентом, применяемым в этом патенте, является дициклогексилкарбодиимид (DCC), который является сильным аллергеном и сенсибилизатором, часто вызывает кожную сыпь.
EP 0334636 также раскрывает получение пирролопиримидинглютамата путем конденсации реактивных производных соединений пирролопиримидинилалкилбензойной кислоты с глутаминовой кислотой или ее сложным диэфиром. Реактивные производные соединения включают галиды кислоты, ангидриды кислоты, смесь ангидрида кислоты со сложными эфирами моноалкилкарбоновой кислоты, активные сложные эфиры, азид кислоты, смесь ангидрида кислоты со сложными диэфирами фосфорной кислоты, смесь ангидрида кислоты со сложными фосфорнокислыми диэфирами пирролопиримидинилалкилбензойной кислоты.
EP 0334636 не раскрывает, в частности, способ получения диэтилпеметрекседа и его превращение в пеметрексед или его фармацевтически приемлемые соли.
Пеметрексед и его получение были описаны впервые в патенте США US 5344932. Синтез диалкилпеметрекседа, раскрытый в этом патенте, не подходит для промышленного получения из-за большого количества стадий способа и низкого общего выхода. Патенты США US 6013828 и US 6066732 раскрывают получение двунатриевой соли пеметрекседа путем конденсации 2-(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил)этилбензойной кислоты с диэтил-L-глутаматом, с применением 4-хлор-2,6-диметокситриазина (CDMT) в качестве конденсирующего агента. Этот способ не подходит для промышленного применения, поскольку CDMT является опасным, так же как дорогим реагентом, который не является легкодоступным. Применение CDMT вызывает раздражение глаз, дыхательной системы и кожи. Обнаружено, что продукты, полученные с применением триазиновых реагентов, не являются бесцветными, а имеют синеватый до серого цвет, и необходима очистка колоночной хроматографией для получения бесцветных продуктов.
Получение диэтилпеметрекседа путем конденсации 2-(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил)этилбензойной кислоты с диэтил-L-глутаматом с применением CDMT и N-метилмофролина раскрыто в Organic Process Research and Development, 2005, 9, 738-742. Статья также раскрывает образование N-метилпеметрекседа в виде примеси, образующейся при побочной реакции CDMT с N-метилморфолином.
Следовательно, в области техники существует потребность в экономичном и подходящем для промышленного применения способе синтеза диалкилпеметрекседа.
Как любые соединения, полученные синтетическим путем, пирролопиримидинглютаматы могут включать посторонние соединения или примеси, которые могут появляться из любого источника. Примеси могут быть в виде непрореагировавших исходных веществ, сопутствующих продуктов реакции, продуктов побочных реакций или продуктов разложения. Пирролопиримидинглютаматы, содержащие примеси, могут приводить к получению загрязненного пеметрекседа или его солей. Примеси в пеметрекседе или его солях нежелательны и могут даже быть вредными для пациента, проходящего лечение содержащими их лекарственными формами.
Известными способами очистки диалкилпеметрекседа являются колоночная хроматография и очистка солеобразованием (например, тозилатная соль). Очистка колоночной хроматографией не применима в промышленности.
Патент WO 0114379 раскрывает очистку диэтилпеметрекседа через образование тозилатной соли, что может влиять на выход пеметрекседа. Очистка диэтилпеметрекседа через образование тозилатной соли не приводит к степени чистоты продукта более 99%.
Патент США 6066732 раскрывает очистку диэтилпеметрекседа посредством колоночной хроматографии и, следовательно, не подходит для промышленного применения.
Таким образом, несомненно, интересным остается поиск промышленного способа получения и очистки диалкилпеметрекседа, приводящего к удовлетворительному выходу и удовлетворительной чистоте конечного продукта.
Заявитель неожиданно обнаружил, что практически отсутствует какая-либо литература, раскрывающая применение замещенных триарилфосфатов в синтезе карбоксамидов из карбоновых кислот и аминов.
Цель изобретения
Поэтому целью настоящего изобретения является преодоление или улучшение, по крайней мере, одного недостатка в предшествующей области техники или разработка полезной альтернативы.
Другая цель настоящего изобретения состоит в том, чтобы создать способ получения высокочистого диалкилпеметрекседа с применением безопасного, мягкого, недорогого, неокислительного и простого в применении реагента.
Другая цель настоящего изобретения состоит в том, чтобы создать экономный и применимый в промышленности способ получения высокочистого диалкилпеметрекседа.
Еще одна цель настоящего изобретения состоит в том, чтобы создать короткий и применимый в промышленности способ очистки диалкилпеметрекседа для обеспечения продуктов со степенью чистоты более 99% при измерении посредством ВЭЖХ.
Еще одна цель настоящего изобретения состоит в превращении диалкилпеметрекседа, получаемого способом по настоящему изобретению, в высокочистый пеметрексед и его двунатриевую соль.
Сущность настоящего изобретения
В соответствии с вышеуказанными целями настоящее изобретение представляет короткий, экономичный и промышленно пригодный способ получения высокочистого диалкилпеметрекседа с применением безопасного, мягкого, недорогого, неокислительного и простого в обращении реагента.
Согласно одному аспекту настоящее изобретение представляет способ получения диалкилпеметрекседа, включающий реакцию 2-(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил) этилбензойной кислоты со сложным диэфиром глутаминовой кислоты или его солью в присутствии замещенного трифенилфосфата.
В другом аспекте настоящее изобретение представляет способ очистки производных соединений пирролопиримидинглютаминовой кислоты через кристаллизацию или порошкование в подходящем растворителе.
Другие особенности, цели и преимущества настоящего изобретения будут очевидны из прилагаемых примеров и формулы изобретения.
Подробное описание настоящего изобретения
Если не указано иное, все технические и научные термины, примененные в настоящем описании, имеют то же самое значение, которое обычно понимается специалистами в области техники, к которой принадлежит настоящее изобретение. Несмотря на то что на практике или тестировании настоящего изобретения могут быть применены любые способы и вещества или другое, эквивалентное описанному в настоящем описании, описаны предпочтительные способы и вещества. Для описания настоящего изобретения указанные конкретные термины определены в настоящем описании следующим образом.
Если не заявлено противоположное, любое из слов 'владеющий', 'содержащий', 'содержит', 'включающий' и 'включает' обозначает 'содержащий без ограничений' и не должно быть рассмотрено в качестве ограничения любого общего утверждения, за которым оно следует, специфичными или схожими позициями или наименованиями, следующими сразу за ними. Варианты осуществления настоящего изобретения не являются взаимоисключающими, но могут быть осуществлены в различных комбинациях. Описанные варианты осуществления настоящего изобретения и раскрытых примеров приведены для иллюстрации цели, а не ограничения настоящего изобретения, сформулированного в прилагаемой формуле изобретения.
Соответственно, настоящее изобретение обеспечивает способ для получения высокочистого диалкилпеметрекседа, включающий следующие стадии:
а) взаимодействие 2-(4-гидрокси-6-аминопирроло(2, 3-d)пиримидин-3-ил)этилбензойной кислоты формулы (II) с триарилфосфатом формулы (IV) с получением смешанного ангидрида формулы (V).
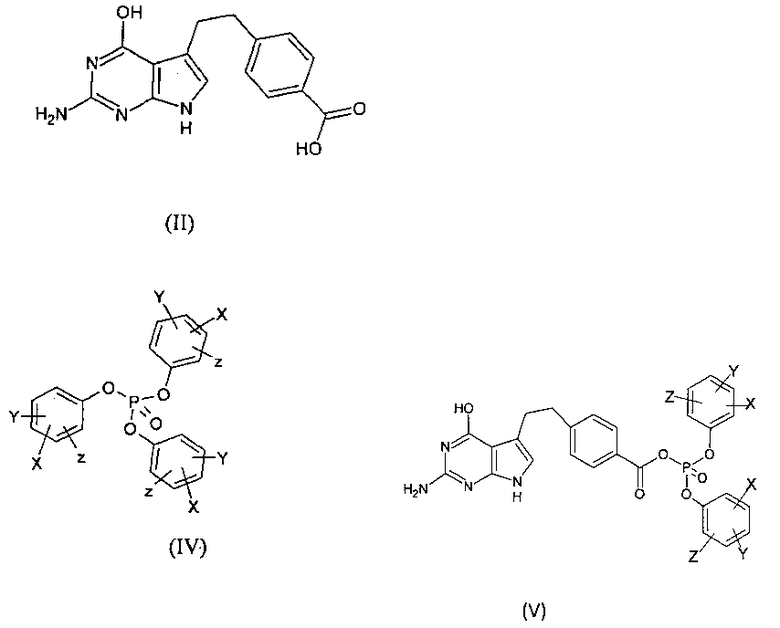
где X представляет собой электроноакцепторную группу; Υ и Ζ независимо представляют собой водород, электроноакцепторную группу, алкил, содержащий 1-7 атомов углерода, алкоксигруппу, содержащую 1-7 атомов углерода, галоген, NR3R4, меркаптогруппу, тиоалкил, содержащий 1-7 атомов углерода, или Υ и Ζ при ортоположении друг к другу образуют бензольное кольцо; R3 и R4 независимо представляют собой водород, алкил, содержащий 1-7 атомов углерода, или R3 и R4 вместе с азотом образуют 3-7-членное гетероциклическое кольцо.
b) взаимодействие смешанного ангидрида формулы (V), полученного на стадии a, in situ со сложным диэфиром глутаминовой кислоты или солью формулы (III) с получением диалкилпеметрекседа формулы (I),
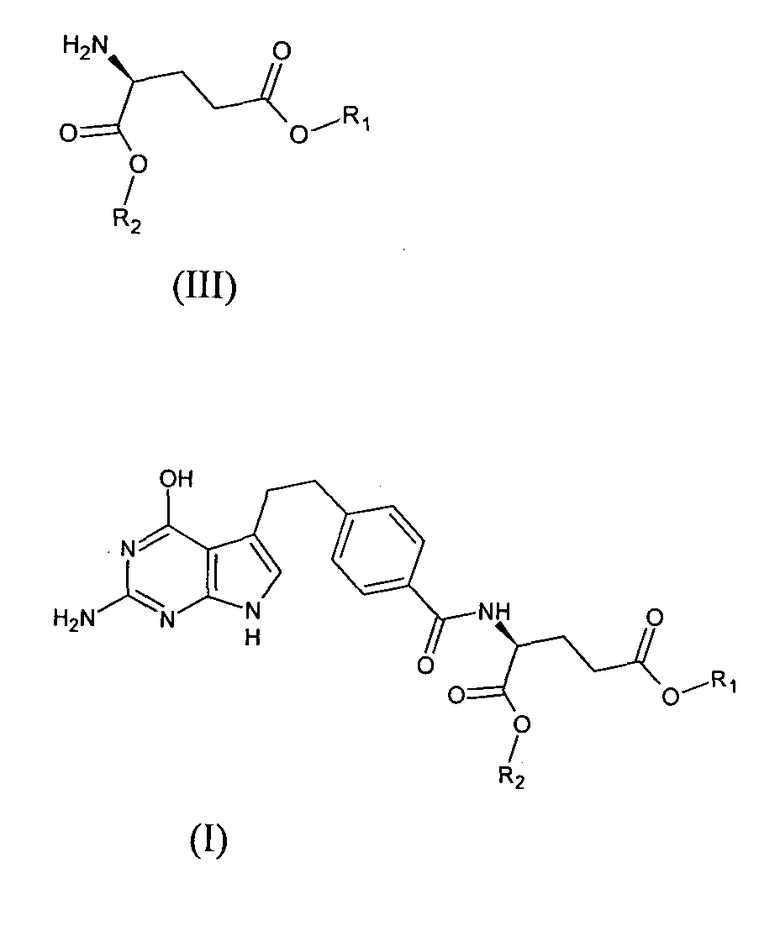
в которой R1 и R2 являются карбоксильными защитными группами. Предпочтительно R1 и R2 независимо представляют собой алкильные группы, содержащие 1-7 атомов углерода. Более предпочтительно, R1 и R2 независимо представляют собой метильные или этильные группы.
Способ по настоящему изобретению преимущественно осуществляют путем взаимодействия карбоновой кислоты формулы (II), с диэтил-L-глутаматом в присутствии трис(пара-нитрофенил)фосфата, трис(орто-нитрофенил)фосфата или трис(пара-цианофенил)фосфата. Такие фосфаты являются мягкими, безопасными, недорогими, неокислительными и простыми в обращении. Предпочтительным является использование трис(пара-нитрофенил)фосфата или трис(орто-нитрофенил)фосфата.
Трифенилфосфат формулы (IV), используемый в синтезе, берут в количестве 1-4 эквивалентов 2-(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил)этилбензойной кислоты, более предпочтительно, 1,2-3,5 эквивалентов. Самое предпочтительное количество реагента составляет 1,5-1,7 эквивалентов.
Предпочтительно, способ по настоящему изобретению осуществляют в присутствии основания и подходящего растворителя. Основание, которое может быть применено в настоящем изобретении, является органическим или неорганическим. Примеры органического основания включают третичные амины, такие как триалкиламин. Примеры неорганического основания включают карбонат щелочного металла, карбонат щелочноземельного металла, бикарбонат щелочного металла, бикарбонат щелочноземельного металла и их смеси.
Примеры карбоната щелочного металла включают карбонат калия и карбонат натрия. Примеры бикарбоната щелочного металла включают бикарбонат натрия и бикарбонат калия. Примеры карбоната щелочноземельного металла включают карбонат кальция и карбонат магния. Примеры бикарбоната щелочноземельного металла включают бикарбонат кальция и бикарбонат магния. Предпочтительным основанием является триэтиламин или карбонат натрия.
Основание предпочтительно используют в количестве по отношению к 2-(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил)этилбензойной кислоте, предпочтительно, в диапазоне от 1 до 6 эквивалентов, более предпочтительно от 2 до 5 эквивалентов. Самое предпочтительное количество основания составляет 4 эквивалента.
Растворитель может быть выбран из любого полярного растворителя. Предпочтительным растворителем является ацетонитрил или диметилформамид.
Способ по настоящему изобретению может быть осуществлен при подходящей температуре. Чтобы минимизировать разложение продуктов и образование примесей, реакцию проводят при 25-60°C, более предпочтительно при 35-55°C. Самая предпочтительная температура реакции составляет 45-50°C.
Реакция, как правило, завершается в промежутке 2-24 часа, более предпочтительно 10-18 часов, наиболее предпочтительно 12-13 часов.
По завершении реакции сложный диэфир пеметрекседа может быть регенерирован из реакционной массы удобным путем. Проведение реакции включает гашение реакционной смеси водой с последующей экстракцией смеси при помощи несмешивающегося с водой органического растворителя. Несмешивающийся с водой органический растворитель выбран из группы галоидированных или негалоидированных растворителей. Самым предпочтительным растворителем является этилацетат, хлороформ, дихлорметан, дихлорэтан или их смесь. Органический растворитель, содержащий диэтилпеметрексед, очищается от замещенных дифенилгидрофосфатов и замещенных фенолов путем промывания водным раствором карбоната щелочного металла. Карбонаты щелочных металлов выбраны из группы, содержащей карбонат лития, натрия или калия, наиболее предпочтительно карбонат натрия. Способ дополнительно включает выпаривание органического растворителя, содержащего сложный диэфир пеметрекседа, до сухого состояния. Выпаривание растворителя осуществляют дистилляцией растворителя при его точке кипения. Выпаривание растворителя осуществляют под пониженным давлением, и исходный сложный диэфир пеметрекседа отделяют при помощи ВЭЖХ с чистотой, по меньшей мере, 98%.
Отделенный сложный диэфир пеметрекседа очищают путем кристаллизации или порошкования в подходящем растворителе. Растворитель, применяемый для кристаллизации или порошкования, выбирают из класса галоидированных или негалоидированных растворителей или их смесей. Предпочтительно, растворитель, применяемый для очистки диалкилпеметрекседа, выбран из этилацетата, ацетона, дихлорметана, диметилформамида, диметилсульфоксида, диметилацетамида или их смесей. Самый предпочтительный растворитель, применяемый для очистки сложного диэфира пеметрекседа, является смесью диметилформамида и ацетона в отношении от 1:3 до 1:8 об./об., более предпочтительно от 1:4 до 1:7 об./об. или наиболее предпочтительно от 1:5 до 1:6 об./об. Очищенный диалкилпеметрексед имеет чистоту более 99%.
Очищенный сложный диэфир пеметрекседа подвергают гидролизу для получения двунатриевой соли пеметрекседа либо способами, известными в области техники, либо способом, раскрытым в настоящем описании. В типичном способе сложный диэфир пеметрекседа гидролизуют с применением гидроксида натрия для получения двунатриевой соли пеметрекседа. Гидролиз может быть выполнен при комнатной температуре.
Замещенный трифенилфосфат формулы (IV) может быть легко получен способами, известными в предшествующей области техники, или способом, раскрытым в настоящем описании. В типичном способе замещенный фенол взаимодействует с оксихлоридом фосфора в присутствии основания и растворителя с получением замещенного трифенилфосфата формулы (IV).
Растворитель, применяемый для получения замещенного трифенилфосфата формулы (IV), является апротонным растворителем, выбранным без ограничения из дихлорметана, тетрагидрофурана, этилацетата, ацетона, диметилформамида, толуола, ацетонитрила и диметилсульфоксида. Предпочтительным растворителем, применяемым для получения триарилфосфата, является толуол. Основание, используемое в получении триарилфосфата, предпочтительно, является пиридином.
Чистая двунатриевая соль пеметрекседа, получаемая способом по настоящему изобретению, может быть составлена в лекарственную форму вместе с одним или более фармацевтически приемлемых инертных наполнителей с применением известных технологий. Дополнительно, лекарственная форма может быть с быстрым высвобождением или с постепенным высвобождением.
Дальнейшие подробности способа по настоящему изобретению будут очевидны из примеров, представленных ниже. Представленные примеры являются только иллюстративными и не ограничены специфическими вариантами осуществления, проиллюстрированными в настоящем описании, а включают комбинации, которые очевидны из изложенного в настоящем описании.
Примеры
Пример 1
Получение трис(пара-нитрофенил)фосфата
В круглодонную колбу с четырьмя горлами объемом 2000 мл с конденсатором воды и хлоркальциевой трубкой помещали паранитрофенол (100,16 грамм, 0,72 моль), толуол (1000 мл) и пиридин (135 грамм, 1,708 моль) при комнатной температуре. Оксихлорид фосфора (36,8 грамм, 0,024 моль) добавляли по каплям в течение 15 минут. Реакционную массу осторожно нагревали с обратным холодильником при 110°C в течение 4 часов. Реакционную смесь охлаждали до 60°C. Толуол удаляли путем дистилляции под пониженным давлением для получения исходного твердого вещества. Твердое вещество растворяли в дихлорметане (1000 мл). Слой дихлорметана промывали 5%-ным раствором гидроксида натрия (3×500 мл) с последующим промыванием водой (1×500 мл). Органический слой высушивали над сульфатом натрия и концентрировали до сухого состояния с получением 89 грамм трис(пара-нитрофенил)фосфата в виде бесцветных кристаллов (выход 89 грамм, точка плавления 154-156°C, точка плавления по литературе 156°C (указано в Green Chemistry, 2005, 7, 217)). Для дальнейших реакций продукт применяли без очистки.
Пример 2
Получение трис(орто-нитрофенил)фосфат
Получение трис(орто-нитрофенил)фосфата осуществляли согласно примеру 1 с применением o-нитрофенола вместо п-нитрофенола. Выход составил 70%.
Пример 3
Получение диэтилпеметрекседа
В чистую и сухую круглодонную колбу объемом 250 мл (A) помещали 2-(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил)этилбензойную кислоту (20 грамм, 0,067 моль), диметилформамид (100 мл) и триэтиламин (23,04 грамм, 0,228 моль). Реакционную смесь перемешивали в течение 5 минут при 30-35°C. К реакционной смеси добавляли трис(пара-нитрофенил)фосфат (34 грамма, 0,0736 моль). Реакционную смесь перемешивали в течение 1 часа при 30-35°C. К реакционной смеси добавляли трис(пара-нитрофенил)фосфат (15,4 грамм, 0,0334 моль). В течение одного часа реакционную смесь поддерживали при 30-35°C. В другой колбе (B) растворяли диэтил-L-глютамат хлоргидрат (17,4 грамм, 0,0726 моль) в диметилформамиде (30 мл) и триэтиламине (7,92 грамм, 0,078 моль). Реакционную смесь перемешивали в течение 5 минут и фильтровали.
Фильтрат добавляли к реакционной смеси в колбу (A) и перемешивали в течение 11 часов при 40-45°C. Реакционную смесь охлаждали до 20°C, гасили дистиллированной водой (600 мл) при 20-25°C, и экстрагировали дихлорметаном (3×150 мл). Слои дихлорметана собирали и промывали 5%-ным раствором карбоната натрия (3×300 мл). Слой дихлорметана отделяли, промывали дистиллированной водой (300 мл), высушивали над сульфатом натрия и концентрировали. Ацетон (400 мл) помещали в концентрированную реакционную смесь и перемешивали при 30-35°C в течение 1 часа. Твердое вещество отфильтровывали, промывали ацетоном (2×50 мл) с получением неочищенного диэтилпеметрекседа (выход 20 грамм, чистота после ВЭЖХ 98,12%).
Пример 4
Получение диэтилпеметрекседа
В чистую и сухую круглодонную колбу объемом 100 мл помещали 2-(4-гидрокси-6-аминопирроло(2,3-d)пиримидин-3-ил)этилбензойную кислоту (5 грамм), гидрохлорид диэтил-L-глютамата (4,5 грамма), диметилформамид (40 мл) и триэтиламин (9,4 мл). Реакционную смесь нагревали до 40°C и перемешивали в течение 15-25 минут. Трис(пара-нитрофенил)фосфат (11,5 грамма) добавляли к реакционной смеси при 40°C и выдерживали в течение 3 часов. Обработку для получения диэтилпеметрекседа проводили как в примере 3 (выход 5,8 грамма, чистота после ВЭЖХ 98%).
Пример 5
Получение диэтилпеметрекседа
Получение диэтилпеметрекседа осуществляли согласно примеру 3 с применением трис(орто-нитрофенил)фосфата вместо трис(пара-нитрофенил)фосфата. (Выход 6,0 грамм, чистота после ВЭЖХ 99,2%).
Пример 6
Очистка диэтилпеметрекседа
Влажный и неочищенный диэтилпеметрексед, полученный в примере 3, добавляли к диметилформамиду (60 мл) и перемешивали при 30-35°C до осветления реакционной смеси. В реакционную смесь добавляли ацетон (400 мл), перемешивали при 30-35°C в течение 1 часа, фильтровали и промывали ацетоном (2×50 мл) с получением очищенного диэтилпеметрекседа (выход 17,5 грамма, чистота после ВЭЖХ 99,05%).
Пример 7
Очистка диэтилпеметрекседа
Диэтилпеметрексед, полученный в примере 4, очищали согласно примеру 6 с получением очищенного продукта с чистотой после ВЭЖХ 99,01%.
Пример 8
Очистка диэтилпеметрекседа
Диэтилпеметрексед, полученный в примере 5, очищали согласно примеру 6 с получением очищенного продукта с чистотой после ВЭЖХ 99,5%.
Пример 9
Получение двунатриевого гептагидрата пеметрекседа
Диэтилпеметрексед (17 г), полученный в примере 6, добавляли к 1 н. раствору гидроксида натрия (119 мл). Реакционную смесь перемешивали в течение 1 часа при комнатной температуре. pH реакционной смеси приводили к 7-9 при помощи уксусной кислоты. Реакционную смесь нагревали до 40°C. К реакционной смеси добавляли ацетон (425 мл) и перемешивали при 40-45°C в течение 10 минут. Реакционную массу дополнительно охлаждали до комнатной температуры и выдерживали в течение 1 часа. Полученное твердое вещество фильтровали и промывали ацетоном и высушивали с получением двунатриевого гептагидрата пеметрекседа (18,5 грамма, чистота после ВЭЖХ 99,09%). Двунатриевый гептагидрат пеметрекседа после ВЭЖХ сравнивали со стандартным образцом.
Пример 10
Получение двунатриевого гептагидрата пеметрекседа
Чистый диэтилпеметрексед (1 грамм), полученный в примере 7, гидролизовали согласно примеру 9 с получением двунатриевого гептагидрата пеметрекседа (выход 1 грамм, чистота после ВЭЖХ 99,13%). Двунатриевый гептагидрат пеметрекседа после ВЭЖХ сравнивали со стандартным образцом.
Пример 11
Получение двунатриевого гептагидрата пеметрекседа
Чистый диэтилпеметрексед (1 грамм), полученный в примере 8, гидролизовали согласно примеру 9 с получением двунатриевого гептагидрата пеметрекседа (выход 4,9 грамм, чистота после ВЭЖХ 99,2%). Двунатриевый гептагидрат пеметрекседа после ВЭЖХ сравнивали со стандартным образцом.
Пример 12
Получение пеметрекседа
Двунатриевый гептагидрат пеметрекседа (3 грамма), полученный в примере 9, растворяли в воде (60 мл). К реакционной смеси добавляли уксусную кислоту (4 мл) и нагревали при 70°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, перемешивали в течение одного часа, фильтровали и промывали дистиллированной водой с получением пеметрекседа (2,5 грамма, чистота после ВЭЖХ 99,42%). Пеметрексед после ВЭЖХ сравнивали со стандартным образцом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПЕМЕТРЕКСЕДА И ЕГО ЛИЗИНОВОЙ СОЛИ | 2013 |
|
RU2609006C2 |
| ПОЛИМОРФНАЯ ФОРМА ГИДРОХЛОРИДА ЛЕРКАНИДИПИНА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2425033C2 |
| СПОСОБ ПОЛУЧЕНИЯ (S)-3-[(1-ДИМЕТИЛАМИНО)ЭТИЛ]-ФЕНИЛ-N-ЭТИЛ-N-МЕТИЛ-КАРБАМАТА | 2005 |
|
RU2393148C2 |
| ДЕЙТЕРИРОВАННЫЙ ФЕНИЛАМИНОПИРИМИДИН И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТАКОЕ СОЕДИНЕНИЕ | 2014 |
|
RU2633694C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-[(3R)-3-МЕТИЛМОРФОЛИН-4-ИЛ]-4-(1-МЕТИЛ-1H-ПИРАЗОЛ-5-ИЛ)-8-(1H-ПИРАЗОЛ-5-ИЛ)-1,7-НАФТИРИДИНА | 2019 |
|
RU2802512C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ФОСФАТООРГАНИЧЕСКОГО СОЕДИНЕНИЯ, ФОСФАТООРГАНИЧЕСКОЕ СОЕДИНЕНИЕ И ЗУБНАЯ ПОЛИМЕРИЗУЕМАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2000 |
|
RU2241003C2 |
| ОПТИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ДИГИДРОПИРИДИНА, ИХ ПРИМЕНЕНИЕ И ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2003 |
|
RU2294328C2 |
| ОДНОСОСУДНЫЙ СПОСОБ ПОЛУЧЕНИЯ ПЕМЕТРЕКСЕДА ДИНАТРИЯ | 2012 |
|
RU2577251C2 |
| ОДНОРЕАКТОРНЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНОГО ПРОДУКТА КОНЪЮГАТА АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2020 |
|
RU2745738C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЯ БЕНЗО[b]ТИОФЕНА | 2012 |
|
RU2601420C2 |
Изобретение описывает способ получения и способ очистки диалкилпеметрекседа формулы (I), обладающего антифолатным действием. Соединение находит применение для лечения немелкоклеточного рака, а в сочетании с цисплатиной - для лечения злокачественной плевральной мезотелиомы легких. 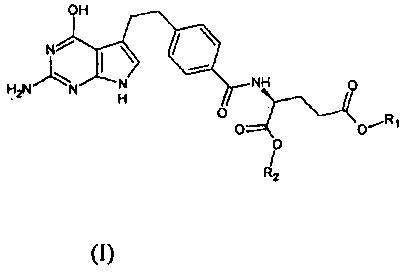
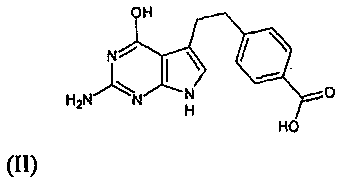
Способ заключается во взаимодействии карбоновой кислоты формулы (II) со сложным диэфиром глутаминовой кислоты формулы (III) или его кислотно-аддитивной солью. Процесс проводят в присутствии замещенного трифенилфосфата формулы (IV), основания и растворителя.

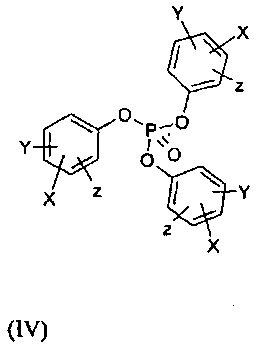
В формулах (I) и (III) каждый R1 и R2 независимо представляет алкильные группы. В формуле (IV) X, Y и Z имеют значения, указанные в формуле изобретения. Использование безопасного, мягкого, недорогого, неокисляющегося и простого в обращении трифенилфосфата позволяет упростить процесс и обеспечить получение, например, диэтилпеметрекседа со степенью чистоты более 99%. 2 н. и 12 з.п. ф-лы, 12 пр.
1. Способ получения диалкилпеметрекседа формулы (I),

включающий взаимодействие карбоновой кислоты формулы (II)

со сложным диэфиром глутаминовой кислоты формулы (III) или его кислотно-аддитивной солью
 ,
,
где R1 и R2 независимо представляют собой алкильные группы, в присутствии замещенного трифенилфосфата формулы (IV), основания и растворителя,
 ,
,
где X представляет собой электроноакцепторную группу, такую как водород, нитро, галоген, циано; Y и Z независимо представляют собой водород, нитро, галоген, циано, алкил, содержащий 1-7 атомов углерода, алкоксигруппу, содержащую 1-7 атомов углерода, NR3R4, меркаптогруппу, тиоалкил, содержащий 1-7 атомов углерода, или Y и Z при ортоположении друг к другу образуют бензольное кольцо; R3 и R4 независимо представляют собой водород, алкил, содержащий 1-7 атомов углерода, замещенный или незамещенный фенил, или R3 и R4 вместе с азотом образуют 3-7-членное гетероциклическое кольцо.
2. Способ получения диалкилпеметрекседа по п. 1, в котором X представляет собой нитрогруппу или цианогруппу; Y и Z представляют собой водород.
3. Способ получения диалкилпеметрекседа по п. 1 или 2, в котором замещенный трифенилфосфат представляет собой трис(пара-нитрофенил)фосфат или трис(орто-нитрофенил)фосфат.
4. Способ получения диалкилпеметрекседа по п. 1, в котором R1 и R2 независимо представляют собой алкильные группы, содержащие 1-7 атомов углерода.
5. Способ получения диалкилпеметрекседа по п. 4, в котором R1 и R2 независимо представляют собой метил или этил.
6. Способ получения диалкилпеметрекседа по п. 1, в котором основание выбрано из третичных аминов, карбоната щелочного металла, карбоната щелочноземельного металла, бикарбоната щелочного металла или бикарбоната щелочноземельного металла.
7. Способ получения диалкилпеметрекседа по п. 6, в котором основание является триэтиламином или карбонатом натрия.
8. Способ получения диалкилпеметрекседа по п. 1, в котором растворитель выбран из полярных растворителей.
9. Способ получения диалкилпеметрекседа по п. 8, в котором растворитель является ацетонитрилом или диметилформамидом.
10. Способ очистки диалкилпеметрекседа формулы (I)

в которой R1 и R2 независимо представляют собой алкильные группы, включающий кристаллизацию соединения формулы (I) в растворителе.
11. Способ очистки соединения формулы (I) по п. 10, в котором R1 и R2 независимо представляют собой метил или этил.
12. Способ очистки соединения формулы (I) по п. 10, в котором растворитель выбран из этилацетата, ацетона, дихлорметана, диметилформамида, диметилсульфоксида, диметилацетамида или их смесей.
13. Способ очистки соединения формулы (I) по п. 12, в котором растворитель является смесью диметилформамида и ацетона.
14. Способ очистки соединения формулы (I) по п. 12 или 13, в котором способ обеспечивает получение диэтилпеметрекседа со степенью чистоты более 99%.
| DOUGLAS P KJELL;et al., Determination of the source of N-methyl impurity in the synthesis of pemetrexed disodium heptahydrate, ORGANIC PROCESS RESEARCH AND DEVELOPMENT, 2005, Vol:9, Nr:6, Page(s):738-742 | |||
| US 6066732 A1, 23.05.2000 | |||
| US 6013828 A1, 11.01.2000 | |||
| ФОРМИРОВАТЕЛЬ ЗАДНЕГО ФРОНТА ВЫХОДНОГО ИМПУЛЬСА МОДУЛЯТОРА | 0 |
|
SU334636A1 |
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2015-06-10—Публикация
2010-10-27—Подача