Область, к которой относится изобретение
Настоящее изобретение относится к способу обнаружения высоких уровней аутоантител против эндотелиального рецептора белка С/активированного белка С (ЕРCR) в образце путем его детекции и количественной оценки in vitro.
Предшествующий уровень техники
Аутоиммунные заболевания
Аутоиммунные заболевания характеризуются иммунными реакциями, в результате которых иногда индуцируются иммунные реакции против тканей хозяина и продуцируются аномальные антитела, атакующие ткани хозяина (аутоантитела). В большинстве случаев аутоиммунные заболевания включают такие нарушения, как антифосфолипидный синдром (APLS), ревматоидный артрит, системная красная волчанка, аутоиммунный васкулит и т.п.
APLS характеризуется сосудистым (венозным, артериальным или микроваскулярным) тромбозом и осложнениями беременности (внутриутробной смертью плода, преждевременными родами или многократными самопроизвольными выкидышами), ассоциированными с присутствием антифосфолипидных антител. Эти антитела являются гетерогенными и распознают различные комбинации фосфолипидов, фосфолипид-связывающих белков, либо те и другие. Наиболее часто детектируемые подгруппы антител против фосфолипидов включают так называемые волчаночные антикоагулянты (антитела с антикоагулирующими свойствами от больных красной волчанкой) (АСL), антитела против кардиолипина и антитела против гликопротеина I β2. В настоящее время исследуются другие антитела против фосфолипидов, которые не включены в классические лабораторные критерии. Такие антитела направлены против фосфолипидов, отличных от кардиолипина, таких как фосфатидилэтаноламин, или против фосфолипид-связывающих белков, таких как аннексин V и белок S. Однако о механизмах, связанных с присутствием антифосфолипидных антител, вызывающих васкулярный тромбоз и выкидыш, известно очень немного.
Сосудистые заболевания
Сосудистые заболевания подразделяются на три главных типа, в зависимости от вида поражаемых сосудов (артериальных, венозных или капиллярных сосудов микроциркуляции). В случае артериальных сосудистых заболеваний пристеночный склероз приводит к снижению потока крови через просвет сосуда, а следовательно, и к постоянному снижению кровоснабжения участков, орошаемых поврежденным кровеносным сосудом. Такое атеросклеротическое поражение сосудов может приводить к серьезным осложнениям и к развитию тромбоза внутри артерии, что, в целом, приводит к ее окклюзии, а значит, и к прекращению кровоснабжения. В этом случае возникает инфаркт тканей. Наиболее характерными примерами такого поражения является инфаркт миокарда, возникающий в результате тромбоза коронарной артерии, или инсульт, если пораженным сосудом является артерия головного мозга. В случае венозного сосудистого заболевания тромбоз приводит к нарушению возврата кровотока в сердце. Если фрагмент тромба отделяется от стенок вен, пораженных тромбозом, то этот тромб будет перемещаться в кровотоке до тех пор, пока он не попадет в легочный венозный круг кровообращения, что приведет к острой легочной недостаточности (ситуация, известная как легочная эмболия). Заболевания, связанные с нарушением капиллярного кровообращения, являются вторичными заболеваниями, возникающими вследствие воспаления и/или тромбоза сосудов капиллярного кровообращения в различных органах и проявляющимися недостаточностью органов, в которых нарушено капиллярное кровообращение. Сосудистые заболевания являются главной причиной высокой заболеваемости и смертности в Западных странах. В частности, по данным Национального института статистических исследований (Instituto Nacional de Estadistica) (INE)(Испанский Национальный институт статистики) за 2000 год сердечно-сосудистые заболевания являются главной причиной смертности в Испании (которая составляет приблизительно 35,0% от всех случаев смертности). Среди наиболее часто встречающихся сердечно-сосудистых заболеваний первое место по смертности занимают сосудистые или тромботические артериальные заболевания сердца (главным образом, острый инфаркт миокарда). В настоящее время было установлено, что у некоторых пациентов причиной развития тромбоза являются различные молекулярные факторы риска. Одним из таких факторов риска является присутствие так называемых антифосфолипидных антител. Сначала считалось, что эти аутоантитела направлены против анионных фосфолипидов, однако позднее было обнаружено, что многие из этих аутоантител направлены против комплексов, образованных белками, такими как гликопротеин I β2 или протромбин, и фосфолипидами. Совсем недавно было установлено, что таким антикоагулирующим действием обладают и другие белки, такие как белок С (PC), белок S, тромбомодулин или аннексин V, и этот факт может служить объяснением, почему присутствие этих аутоантител провоцирует развитие тромбоза.
Осложнения беременности
Осложнения беременности, главным образом, включают внутриутробную смерть плода на десятой неделе беременности, преждевременные роды, самопроизвольный выкидыш в период беременности до 10 недель, замедленное внутриутробное развитие, эклампсию и преэклапсию.
EPCR
Активированный белок С (АРС) является одним из главных регуляторных белков каскада реакций свертывания крови. PC, то есть зимоген АРС, активируется тромбином, связанным с тромбомодулином на поверхности эндотелиальных клеток. АРС в комбинации с белком S (его не-ферментным кофактором) осуществляет свою антикоагулирующую функцию посредством протеолиза активированных факторов V и VIII. Генетические и приобретенные дефекты в тромбомодулине, PC и в белке S были детектированы у пациентов с венозным и/или артериальным тромбозом. Рецептор эндотелиальноного PC/активированного PC (EPCR) представляет собой гликопротеин, экспрессируемый на мембране эндотелиальных клеток, которые специфически и с высокой аффинностью связываются с PC и АРС. Для функционирования EPCR он должен быть связан с фосфолипидной молекулой, которая стабилизирует его трехмерную структуру. Связывание PC с EPCR приводит к заметному усилению его активации под действием комплекса “тромбин-тромбомодулин” на поверхности эндотелиальных клеток. Функция EPCR заключается в концентрировании PC на поверхности эндотелиальных клеток и его презентации комплексу “тромбин-тромбомодулин”, что благоприятствует эффективной активации PC. EPCR индуцирует примерно 9-кратное увеличение индекса активации PC на поверхности эндотелиальных клеток in vivo, поэтому он ответственен за присутствие 90% от всех уровней АРС в кровотоке. Кроме того, АРС может активировать активированный протеазой рецептор-1, но только, если он связан с EPCR, в результате чего будет генерироваться “цитопротективный” клеточный сигнал и блокироваться апоптоз.
EPCR экспрессируется, главным образом, в эндотелии вен и артерий, в частности в толстом или среднем слое эндотелия. Кроме того, он интенсивно экспрессируется синцитиотрофобластами. Присутствующий в этих участках EPCR предупреждает развитие тромбоза и стимулирует желательные функции как эндотелиальных клеток, так и синцитиотрофобластов. Эти все возрастающие убедительные данные позволяют предположить, что EPCR играет определенную роль в сохранении беременности, поскольку у мышей, дефицитных по гену EPCR, такая делеция гена приводит к тромбозу плаценты и к ранней гибели эмбриона.
Описание сущности изобретения
Настоящее изобретение относится к способу определения аутоантител против EPCR (IgG, IgА и IgМ) в образце, взятом у индивидуума. С другой стороны, было продемонстрировано, что эти аутоантитела присутствуют у пациентов с диагностированными аутоиммунными заболеваниями (APLS и диссеминированной красной волчанкой); у пациентов с сосудистыми заболеваниями (венозным и артериальным тромбозом); и у женщин с осложнениями беременности. Примеры, которые представлены в настоящем описании, иллюстрируют, среди прочих, тот факт, что уровень анти-EPCR аутоантител в сыворотке или в плазме увеличивается у пациентов с аутоиммунными заболеваниями (диагностированными у пациентов с APLS или с диссеминированной красной волчанкой), у пациентов с сосудистыми заболеваниями, такими как артериальный тромбоз, например инфаркт миокарда (диагностированный у пациентов с APLS или у пациентов, не страдающих APLS), ишемический инсульт (диагностированный у пациентов с APLS) или венозный тромбоз (диагностированный у пациентов с APLS), а также у пациенток с осложнениями беременности, такими как смерть плода (диагностированная у женщин с APLS или у женщин, не страдающих APLS) или многократные выкидыши (зарегистрированные у пациенток с APLS).
Авторами настоящего изобретения было обнаружено, что присутствие анти-EPCR аутоантител в сыворотке или в плазме пациентов с аутоиммунными заболеваниями и/или у пациентов с сосудистыми заболеваниями, и/или у пациенток с осложнениями беременности увеличено по сравнению с уровнем этих аутоантител в образцах, взятых у здоровых индивидуумов, не страдающих такими заболеваниями. Эти данные позволяют использовать указанные анти-EPCR аутоантитела в качестве маркера для in vitro оценки риска и восприимчивости индивидуума к развитию заболевания, ассоциированного с присутствием высоких уровней аутоантител против EPCR, такого как аутоиммунное заболевание, сосудистое заболевание или осложнения беременности.
Были проведены исследования на присутствие анти-EPCR аутоантител у пациентов с APLS и их связь со смертью плода. Была также проведена оценка влияния этих аутоантител на генерирование АРС на поверхности эндотелиальных клеток. Затем были проведены исследования на взаимосвязь присутствия анти-EPCR аутоантител со смертью плода в парных исследованиях, проводимых методом “случай - контроль” (т.е. путем парного сравнения каждого испытуемого с контролем). Полученные результаты подтверждают существующее мнение, что анти-EPCR аутоантитела являются фактором риска внутриутробной смерти плода. Предупреждение активации PC клеток, экспрессирующих EPCR на своей поверхности, может быть одним из механизмов, посредством которого эти аутоантитела осуществляют свои патологические функции.
Краткое описание графического материала
На фигуре 1 проиллюстрирована экспрессия rhsEPCR в Pichia pastoris. rhsEPCR был очищен из супернатанта стабильно трансформированных клеток P. pastoris, как описано в разделе “Материалы и методы” (см. примеры). 10 мкл каждой из трех фракций, содержащих rhsEPCR, выделяли с помощью электрофореза в ДСН-ПААГ, и белки детектировали с использованием синего GELCODE (А), или с помощью Вестерн-блот-анализа с использованием моноклонального анти-myc антитела (Invitrogen)(В).
На фигуре 2 проиллюстрировано сравнение уровней анти-EPCR аутоантител у пациентов с диагностированным APLS и в контрольном образце. На этой фигуре показаны уровни анти-EPCR аутоантител. Антитела изотипа IgМ: контроль (среднее = 45 AU, условных единиц), пациенты (среднее = 57 AU); антитела изотипа IgА: контроль (среднее = 31 AU), пациенты (среднее = 39 AU); антитела изотипа IgG: контроль (среднее = 72 AU), пациенты (среднее = 75 AU).
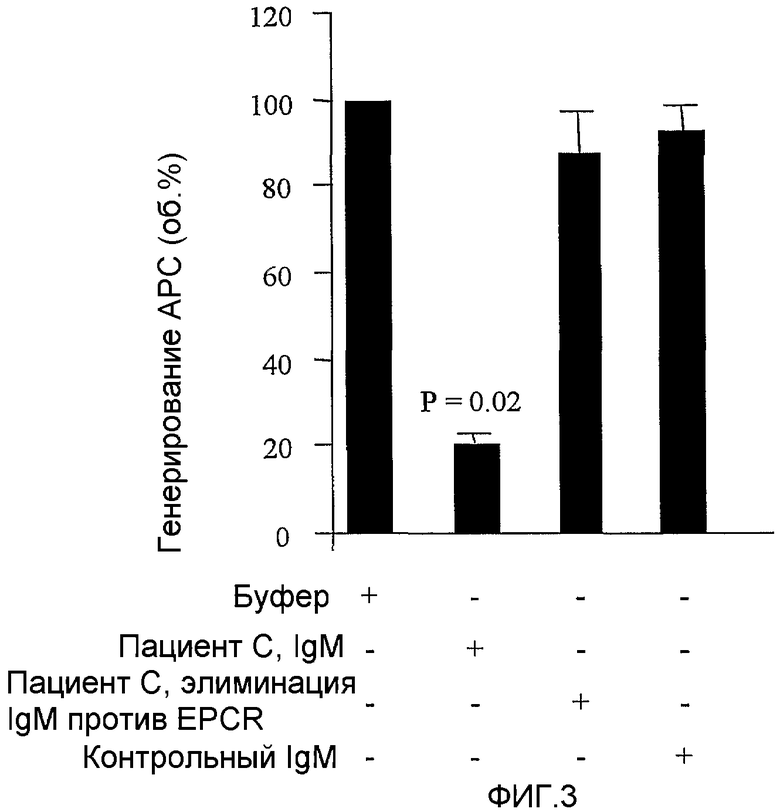
На фигуре 3 проиллюстрировано влияние анти-EPCR аутоантител на генерирование АРС эндотелиальными клетками, где генерирование АРС в присутствии анти-EPCR аутоантител изотипа М можно было наблюдать у пациента С по сравнению с генерированием АРС в отсутствии антитела и в присутствии не-ингибирующего антитела. Для каждого случая было проведено 2-4 независимых эксперимента.
Подробное описание изобретения
Определения
Для лучшего понимания настоящей патентной заявки ниже приводится объяснение некоторых терминов и выражений, используемых в контексте настоящего изобретения.
Термин “индивидуум” относится к члену определенного вида млекопитающих, но не ограничивающегося ими, и включает таких животных, как домашние питомцы, приматы и человек; при этом предпочтительным индивидуумом является человек (мужчина или женщина) любого возраста или любой расы.
Термин “аутоиммунное заболевание” означает нарушения, при которых иммунная система реагирует на ткани хозяев, что приводит к развитию широкого спектра заболеваний. Репрезентативными примерами таких заболеваний являются (среди прочих заболеваний) APLS, системная красная волчанка, ревматоидный артрит, аутоиммунный васкулит и т.п.
Термин “сосудистые заболевания” означает нарушения, которые поражают кровеносные сосуды. При поражении артерий недостаточная перфузия наблюдается и на других участках, орошаемых этими сосудами, и такое состояние является вторичным состоянием, возникающим вследствие окклюзии артерий, обусловленной атеросклеротическим поражением стенок сосудов или тромбозом, либо тем и другим одновременно. Венозные поражения, в свою очередь, характеризуются нарушением кровообращения, а именно нарушением возврата потока крови в сердце из пораженных периферических участков, и такие поражения обычно являются результатом образования венозных тромбов, приводящих к окклюзии сосудов. Если указанное поражение затрагивает капиллярное кровообращение, то оно характеризуется повреждением органа, в котором нарушено капиллярное кровообращение, необходимое для осуществления его функции. Примерами таких заболеваний являются (среди прочих) сосудистые заболевания, поражающие артерии, такие как инфаркт миокарда, инсульт, преходящие нарушения мозгового кровообращения, ишемия конечностей, атеросклероз, аневризмы и т.п., а также сосудистые заболевания, поражающие вены, такие как поверхностный и глубокий венозный тромбоз, эмболия легких и т.п., и патологии капиллярного кровообращения (тромбоз), проявляющиеся недостаточностью органов, наблюдаемой во время инфекций или на фоне аутоиммунных заболеваний.
Термин “осложнения беременности” означает нарушения, негативно влияющие на протекание беременности и возникающие у беременных в эмбрионе или в плоде. Примерами таких осложнений могут служить выкидыш, смерть плода, преждевременные роды, замедленное внутриутробное развитие плода, эклампсия и преэклампсия.
Термин “аутоантитела” означает антитела, продуцируемые индивидуумом и направленные против структур и тканей самого организма-хозяина (или специфичные к этим структурам и тканям), такие как, например, аутоантитела против тромбоцитов, аутоантитела против клеток щитовидной железы, аутоантитела против эритроцитов и т.п. В этом смысле термин “анти-EPCR аутоантитела” означает иммуноглобулины или антитела, продуцируемые указанным индивидуумом и специфичные к EPCR, присутствующим в тканях самого организма.
Используемый в настоящем изобретении термин “эпитоп” означает антигенную детерминанту белка, такую как его аминокислотная последовательность, распознаваемая рассматриваемым антителом.
Термины “пептид” и “полипептид” означают молекулярные цепи аминокислот, которые представляют собой фрагмент белка. Используемые здесь термины “белок” и пептид” являются взаимозаменяемыми.
Настоящее изобретение основано на обнаружении того факта, что продуцирование анти-EPCR аутоантител у пациентов с аутоиммунными заболеваниями, и/или у пациентов с сосудистыми заболеваниями, и/или у пациенток с осложнениями беременности усиливается по сравнению с продуцированием этих антител в образцах, взятых у здоровых индивидуумов, не страдающих указанными заболеваниями. Эти данные позволяют использовать указанные анти-EPCR аутоантитела в качестве маркера для in vitro оценки степени риска и восприимчивости индивидуума к развитию патологии, ассоциированной с присутствием высоких уровней аутоантител против EPCR.
Используемое с настоящем описании выражение “высокие уровни анти-EPCR аутоантител” означает уровни в AU (условных единицах), равные или превышающие 50-тый процентиль в группе нормальных индивидуумов, включая, например, уровни в AU, равные или превышающие 60-тый процентиль в группе нормальных индивидуумов, равные или превышающие 70-тый процентиль в группе нормальных индивидуумов, равные или превышающие 80-тый процентиль в группе нормальных индивидуумов, равные или превышающие 90-тый процентиль в группе нормальных индивидуумов и равные или превышающие 95-тый процентиль в группе нормальных индивидуумов. Из-за различий между индивидуумами (например, по расе и т.п.) очень трудно (а практически невозможно) определить абсолютные величины, характерные для высоких уровней анти-EPCR аутоантител, которые были бы универсальными для всех индивидуумов. Указанные процентили могут быть легко вычислены стандартным методом, включающим тестирование группы здоровых индивидуумов (то есть людей, у которых не были диагностированы аутоиммунные заболевания или предшествующие эпизоды сосудистого заболевания или осложнения беременности во время обследования) на уровни анти-EPCR аутоантитела. Обнаружение анти-EPCR аутоантител может быть осуществлено любым стандартным методом, например посредством ELISA-анализа, описанного в разделе “Материалы и методы” (пример 1). Логично отметить, что у каждого индивидуума присутствует определенный уровень (AU) анти-EPCR аутоантител, и может быть определен конкретный уровень анти-EPCR аутоантител, который будет превышать уровень указанных аутоантител у 50% обследованных индивидуумов. Это значение представляет собой 50-тый процентиль. Очевидно, что существует также величина (AU, условные единицы), выше которой будет обнаружен уровень анти-EPCR аутоантител у 40% нормальных индивидуумов, и эта величина будет соответствовать 60-тому процентилю. В свою очередь, могут быть определены и другие величины, выше которых будут обнаруживаться антитела у 30%, 20%, 10% и 5% нормальных индивидуумов, и эти величины соответствуют 70-, 80-, 90- и 95-му процентилю соответственно.
Настоящее изобретение относится к способу детекции присутствия высоких уровней аутоантител против эндотелиального рецептора белка С/активированного белка С (ЕРCR) в образце, где указанный способ отличается тем, что он предусматривает количественную оценку in vitro анти-EPCR аутоантител в указанном образце, взятом у индивидуума. Указанные высокие уровни аутоантител связаны с патологией, выбранной из аутоиммунного заболевания (например, APLS, системной красной волчанки, ревматоидного артрита, аутоиммунного васкулита и т.п.); сосудистого заболевания (например, артериального сосудистого заболевания, такого как инфаркт миокарда, инсульт, преходящие нарушения мозгового кровообращения, ишемия конечностей, атеросклероз, аневризмы, тромбоз и т.п., или венозного сосудистого заболевания, такого как поверхностный или глубокий венозный тромбоз, эмболия легких и т.п., или сосудистые патологии капиллярного кровообращения); и осложнения беременности (например, выкидыша, внутриутробной смерти плода, преждевременных родов, замедленного внутриутробного развития, эклампсии и преэклапсии). Таким образом, рассматриваемый способ согласно изобретению может быть применен для определения изменения уровней анти-EPCR аутоантител в течение данного периода времени. Такие определения согласно изобретению осуществляют путем их сравнения с нормальными уровнями анти-EPCR аутоантител.
Указанный способ включает стадию, в которой у индивидуума берут образец, такой как образец сыворотки или плазмы, который может быть получен любым стандартным методом, например путем забора крови.
Образцы могут быть взяты у индивидуумов, у которых ранее были диагностированы или не были диагностированы аутоиммунные заболевания или сосудистые заболевания или осложнения беременности. Эти образцы могут быть также взяты у индивидуумов, проходящих курс лечения, или у индивидуумов, которые ранее подвергались лечению по поводу указанных заболеваний или осложнений.
В зависимости от конкретного способа согласно изобретению детекцию и количественную оценку этих анти-EPCR аутоантител осуществляют посредством иммунологического теста, проводимого с использованием маркера, который позволяет детектировать и количественно определять уровень образования специфических комплексов антиген-антитело, например иммунохроматографического теста (с использованием латекса, коллоидного золота и т.п.) и иммунологического теста, в котором указанным маркером является флуоресцентное вещество, изотоп, тяжелый металл, фермент, люминесцентный маркер, хемилюминесцентный маркер, хромоген и т.п.
В настоящем изобретении могут быть применены хорошо известные тесты широкого ряда, включая использование немеченных антител (“первого антитела”) и меченного антитела (“второго” антитела). Такими методами являются Вестерн-блоттинг или Вестерн-перенос, ELISA (твердофазный иммуноферментный анализ), RIА (радиоиммуноанализ) и т.п.
В конкретном варианте изобретения предпочтительным иммунологическим тестом в способе согласно изобретению, который позволяет осуществлять детекцию и/или количественную оценку указанных анти-EPCR аутоантител, является ELISA-анализ, который предусматривает:
а) иммобилизацию на твердом носителе полипептида, содержащего последовательность аминокислот EPCR, или его фрагмента, содержащего, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом;
b) инкубирование указанного иммобилизованного полипептида с образцом, предположительно содержащим анти-EPCR аутоантитела и взятым от указанного индивидуума, в течение периода времени, достаточного для связывания антител с иммобилизованным полипептидом и образования комплексов “полипептид - анти-EPCR аутоантитело”;
с) удаление оставшегося образца, не связанного с иммобилизованным полипептидом;
d) инкубирование указанных комплексов “полипептид - анти-EPCR аутоантитело” со “вторым антителом”, конъюгированным с ферментом, где указанное “второе” антитело обладает способностью связываться с указанными анти-EPCR аутоантителами.
Таким полипептидом, содержащим аминокислотную последовательность EPCR или ее фрагмент, включающий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом, может быть полипептид, содержащий аминокислотную последовательность полноразмерного EPCR, или полипептид, содержащий аминокислотную последовательность фрагмента EPCR и содержащий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR антителом. В конкретном варианте изобретения вышеуказанным полипептидом является гибридный белок, содержащий:
(i) область А, состоящую из полипептида, содержащего аминокислотную последовательность EPCR или ее фрагмент, включающий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR антителом; и
(ii) область В, состоящую из полипептида, содержащего аминокислотную последовательность, используемую для выделения или очистки вышеупомянутого гибридного белка, и/или аминокислотную последовательность, используемую для иммобилизации вышеупомянутого гибридного белка на твердом носителе.
Эта область В может быть связана с амино-концом области А или с карбокси-концом области А.
В конкретном варианте изобретения область А содержит аминокислотную последовательность растворимой части человеческого EPCR.
Область В содержит аминокислотную последовательность, используемую для выделения или очистки определенного выше гибридного белка, и/или аминокислотную последовательность, используемую для иммобилизации вышеупомянутого гибридного белка на твердом носителе. В области В может присутствовать практически любая аминокислотная последовательность, которая может быть использована для выделения или очистки гибридного белка (обычно называемая общим термином пептидная “метка” (tag)), и/или любая аминокислотная последовательность, которая может быть использована для иммобилизации гибридного белка на твердом носителе. Иногда аминокислотная последовательность, используемая для выделения или очистки гибридного белка, может также действовать как аминокислотная последовательность, используемая для иммобилизации вышеупомянутого гибридного белка на твердом носителе, и наоборот. В конкретном варианте изобретения область В содержит аминокислотную последовательность, используемую для выделения или очистки гибридного белка, и аминокислотную последовательность, используемую для иммобилизации гибридного белка на твердом носителе.
В качестве примера такой аминокислотной последовательности, используемой для выделения или очистки гибридного белка, и/или аминокислотной последовательности, используемой для иммобилизации гибридного белка на твердом носителе, может служить Arg-метка, His-метка, FLAG-метка, Strep-метка, эпитоп, который может распознаваться антителом, такой как с-myc-метка, SВР-метка, S-метка; кальмодулин-связывающий пептид; домен, связывающийся с целлюлозой; хитин-связывающий домен; глутатион-S-трансферазная метка; белок, связывающийся с мальтозой; NusA, TrxA, DsbA, Avi-метка и т.п. (Terpe K., Appl. Microbiol. Biotechnol. (2003), 60:523-525), аминокислотная последовательность, такая как Ala-His-Gly-His-Arg-Pro (SEQ ID NO:4)(2, 4 и 8 копий), Pro-Ile-His-Asp-His-Asp-His-Pro-His-Leu-Val-Ile-His-Ser (SEQ ID NO:5), Gly-Met-Thr-Cys-X-X-Cys (SEQ ID NO:6)(6 повторов), β-галактозидаза, VSV-гликопротеин (YTDIEMNRLGK).
В конкретном варианте изобретения указанная область В состоит из полипептида, содержащего эпитоп, который может распознаваться антителом (такой как эпитоп с-myc, распознаваемый анти-с-myc антителом) и концевые гистидины (His-метку).
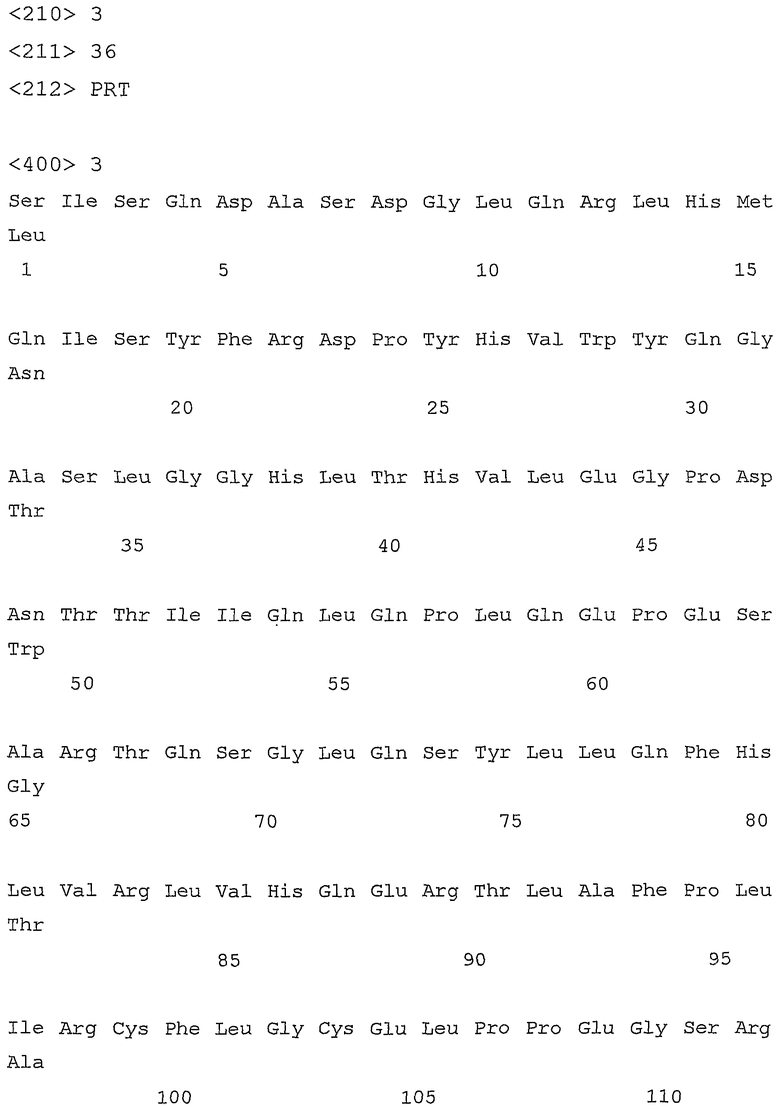
В примере, который приводится в данном описании, описано продуцирование полипептида, обозначенного rhsEPCR и состоящего из гибридного белка, содержащего аминокислотную последовательность растворимой части человеческого EPCR (hsEPCR), аминокислотную последовательность, соответствующую эпитопу с-myc, и концевые гистидины, то есть аминокислотную последовательность, представленную в SEQ ID NO:3.
Полипептид, используемый в способе согласно изобретению, может быть получен стандартными методами, например путем экспрессии в соответствующей экспрессионной системе.
“Вторым антителом”, используемым в вышеупомянутом ELISA-анализе, является антитело, специфичное к иммуноглобулину определенного изотипа и происходящее от вида, к которому не относится исследуемый индивидуум, что позволяет охарактеризовывать данный изотип анти-EPCR аутоантител. Так, например, это “второе” антитело, специфичное к иммуноглобулину данного изотипа, выбирают из антитела против человеческого IgG, антитела против человеческого IgМ, антитела против человеческого IgА и их смесей. В конкретном варианте изобретения указанное “второе” антитело конъюгируют с маркером, что позволяет осуществлять детекцию комплекса, такого как ферментный комплекс (например, с пероксидазой, щелочной фосфатазой и т.п.).
В другом своем аспекте настоящее изобретение относится к способу оценки риска и восприимчивости индивидуума к развитию патологии, ассоциированной с присутствием высоких уровней анти-EPCR аутоантител у данного индивидуума, где указанный способ предусматривает количественную оценку in vitro аутоантител против EPCR в образце, взятом у указанного индивидуума.
В конкретном варианте изобретения указанную патологию, ассоциированную с присутствием высоких уровней анти-EPCR аутоантител у индивидуума, выбирают из аутоиммунного заболевания, такого как APLS, системная красная волчанка, ревматоидный артрит, аутоиммунный васкулит и т.п.; сосудистого заболевания, такого как артериальное сосудистое заболевание, например инфаркт миокарда, инсульт, преходящие нарушения мозгового кровообращения, ишемия конечностей, атеросклероз, аневризмы, тромбоз и т.п., или венозного сосудистого заболевания, такого как поверхностный или глубокий венозный тромбоз, эмболия легких и т.п., или сосудистых патологий капиллярного кровообращения, таких как тромбоз капиллярных сосудов, недостаточность органов при инфекциях или при аутоиммунном заболевании и т.п.; и осложнений беременности, например выкидыша, смерти плода, преждевременных родов, замедленного внутриутробного развития, эклампсии и преэклапсии и т.п.
Указанный способ согласно изобретению основан на обнаружении того факта, что у индивидуумов, у которых было диагностировано аутоиммунное или сосудистое заболевание или осложнение беременности, присутствуют высокие уровни анти-EPCR аутоантител по сравнению с соответствующими уровнями у индивидуумов, в истории болезни которых отсутствуют указанные заболевания или осложнения беременности.
Способ согласно изобретению, применяемый для оценки (анализа) риска и восприимчивости индивидуума к развитию патологии, ассоциированной с присутствием высоких уровней анти-EPCR аутоантител, осуществляют путем сравнения уровней аутоантител, определяемых в образце обследуемого индивидуума, с нормальными уровнями (определяемыми как уровни, обнаруживаемые у группы нормальных индивидуумов, такие как уровни, упомянутые выше при определении термина “высокие уровни”). Указанный способ основан на иммунологических анализах, описанных в данном разделе.
В другом своем аспекте настоящее изобретение относится к способу in vitro мониторинга эффекта терапии, проводимой индивидууму с патологией, связанной с присутствием высоких уровней анти-EPCR аутоантител, где указанный способ предусматривает количественную оценку in vitro этих анти-EPCR аутоантител в образце, взятом у вышеупомянутого индивидуума. Этот способ проводят, как описано выше, однако в данном случае образцы берут у индивидуумов, у которых ранее были диагностированы некоторые из аутоиммунных или сосудистых заболеваний, или некоторые осложнения беременности, подвергаемые терапии. Этот способ позволяет оценивать эффект терапии, то есть ее эффективность или действенность для индивидуума, подвергаемого такой терапии, для того чтобы (например) решить, продолжать ли данную терапию или внести в нее определенные изменения.
В другом своем аспекте настоящее изобретение относится к применению анти-EPCR аутоантител в способе оценки присутствия высоких уровней аутоантител против EPCR в образце, взятом у индивидуума. В конкретном варианте изобретения такое присутствие высоких уровней анти-EPCR аутоантител связано с патологией, выбранной из аутоиммунного заболевания, сосудистого заболевания и осложнений беременности. Повышенный уровень анти-EPCR аутоантител у индивидуума ассоциируется с повышенным риском или восприимчивостью индивидуума к развитию заболевания, ассоциированного с присутствием высоких уровней аутоантител против EPCR, такого как аутоиммунное заболевание, сосудистое заболевание или осложнения беременности.
В другом своем аспекте настоящее изобретение относится к применению полипептида, содержащего последовательность аминокислот EPCR или его фрагмента, содержащего, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом, в способе анализа на присутствие аутоантител против эндотелиального рецептора EPCR в образце. Указанный способ предусматривает детекцию и количественную оценку in vitro анти-EPCR аутоантител в указанном образце. В конкретном варианте изобретения указанную патологию, ассоциированную с высокими уровнями анти-EPCR аутоантител, выбирают из аутоиммунного заболевания, сосудистого заболевания и осложнения беременности.
В конкретном варианте изобретения вышеупомянутым полипептидом, содержащим аминокислотную последовательность EPCR или ее фрагмент, содержащий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом, является такой полипептид, который был ранее определен в описании ELISA-теста, проводимого для детекции и/или количественной оценки анти-EPCR аутоантител. В конкретном варианте изобретения этот полипептид представляет собой так называемый rhsEPCR (см. пример), состоящий из гибридного белка, содержащего аминокислотную последовательность растворимой части человеческого EPCR (hsEPCR), аминокислотную последовательность, соответствующую эпитопу с-myc и концевые гистидины, то есть аминокислотную последовательность, представленную в SEQ ID NO:3.
В другом своем аспекте настоящее изобретение относится к набору, предназначенному для in vitro оценки высоких уровней анти-EPCR аутоантител и включающему полипептид, имеющий аминокислотную последовательность EPCR или ее фрагмент, содержащий, по меньшей мере, один эпитоп, который может распознваться анти-EPCR аутоантителом. В конкретном варианте изобретения вышеуказанным полипептидом, содержащим аминокислотную последовательность EPCR или ее фрагмент, содержащий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом, является такой полипептид, который был ранее определен в описании ELISA-теста, проводимого для детекции и/или количественной оценки анти-EPCR аутоантител. В конкретном варианте изобретения этот полипептид представляет собой так называемый rhsEPCR (см. пример), состоящий из гибридного белка, содержащего аминокислотную последовательность растворимой части человеческого EPCR (hsEPCR), аминокислотную последовательность, соответствующую эпитопу с-myc, и концевые гистидины, то есть аминокислотную последовательность, представленную в SEQ ID NO:3.
В другом аспекте настоящего изобретения указанный набор используют для оценки in vitro риска и восприимчивости индивидуума к развитию патологии, ассоциированной с присутствием высоких уровней анти-EPCR аутоантител и выбранной из аутоиммунного заболевания, сосудистого заболевания и осложнений беременности.
Нижеследующие примеры приводятся для иллюстрации настоящего изобретения.
Пример 1
Использование анти-EPCR аутоантител в качестве маркеров для оценки риска и восприимчивости индивидуума к развитию патологии, ассоциированной с присутствием высоких уровней указанных аутоантител
1. Материалы и методы
Пациенты
1. Пациенты с APLS и контроль
В программу исследований были включены всего 43 пациента (в возрасте 44 года ± 11 лет (среднее ± стандартное отклонение (ср.откл.)), а конкретно 39 женщин и 4 мужчин, у которых был диагностирован антифосфолипидный синдром (APLS) в соответствии с Международными диагностическими критериями [Wilson WA, Gharavi AE, Koike T., Lockshin MD, Branch DW, Piette JC, Brey R, Derksen R, Harris EN, Hughes GR, Triplett DA, Khamashta MA. International consensus statement on preliminary classification criteria for definite antiphosholipid syndrome: report of an international workshop. Arthritis Rheum. 1999; 42:1309-11; Brandt JT, Barna LK, Triplett DA. Laboratory identification of lupus anticoagulants: results of the Second International Workshop for Identification of Lupus Anticoagulants. On behalf of the Subcommittee on Lupus Anticoagulants/Antiphosholipids Antibodies of the ISTH. Thromb. Haemost. 1995; 74:1597-603], и эти исследования проводили с февраля 1998 до марта 2002. Все пациенты были охарактеризованы на присутствие волчаночных антикоагулирующих антител (АСL) и на наличие в истории болезни диагноза венозного тромбоза (n=17), или артериального тромбоза (n=13, из которых у 4 пациентов был диагностирован острый инфаркт миокарда (AMI), у 7 пациентов было диагностировано сердечно-сосудистое тромботическое заболевание (CVTD), а у 2 пациентов - заболевание других органов), либо того и другого [n=13, у всех этих пациентов был диагностирован глубокий венозный тромбоз + CVTD (n=8), AMI (n=1), CVTD+AMI (n=3) или артериальный тромбоз в мезентриальной области (n=1)]. У двадцати семи из этих пациентов была диагностирована системная красная волчанка (SLE). Пробы сыворотки брали в тот период времени, когда анализ на ACL был положительным, и, по крайней мере, через 3 месяца после последнего эпизода тромботического осложнения. Пробы хранили при -80°С до проведения обработки в целях детекции анти-EPCR аутоантител.
В контрольную группу входили 43 здоровых добровольца, у которых в истории болезни не был диагностирован тромбоз или ACL. Все пациенты и все индивидуумы контрольной группы давали информированное согласие на участие в исследовании.
2. Женщины, беременность которых заканчивалась смертью плода, и контроль
Было проведено парное исследование внутриутробной смерти плода методом “случай - контроль”. В исследовании участвовало 87 женщин, в возрасте от 19 лет до 31 года (средний возраст: 27 лет), и это исследование проводили с сентября 1996 до сентября 2002, то есть после первого эпизода внутриутробной смерти плода, зарегистрированной на десятую неделю после наступления аменореи, и в последнюю беременность. В это исследование были включены женщины с ранее диагностированным эпизодом осложнения тромбоза; женщины с диагностированными хроническими инфекционными заболеваниями и некоторыми известными системными заболеваниями, сахарным диабетом или ранее диагностированными патологиями беременности других типов (самопроизвольным выкидышем, эклампсией, ограниченным внутриутробным развитием плода), а также женщины с зарегистрированной внутриутробной смертью плода, вызванной определенными хромосомными аномалиями, негативно влияющими на кариотип, или морфологическим пороком развития плода. Внутриутробная смерть плода наблюдалась во время первой беременности у 58 женщин, во время второй беременности у 21 женщины и во время третьей беременности у остальных 8 женщин; при этом у 75 женщин внутриутробная смерть плода наблюдалась на 10-22 неделю беременности, а у остальных 12 женщин внутриутробная смерть плода наблюдалась на 22-36 неделю беременности (в среднем, на 17 неделю беременности).
В контрольную группу входили 87 здоровых рожавших женщин, распределенных по группам в зависимости от возраста, количества беременностей и времени, прошедшего после последней беременности; все женщины удовлетворяли критериям исключения, применяемым для группы женщин, у которых была зарегистрирована смерть плода. Одновременно, в то же самое время была набрана контрольная группа из женщин, наблюдающихся амбулаторно в гинекологическом отделении той же самой клиники для систематического медицинского обследования.
Разрешение на проведение таких исследований было дано Комитетом по этике Ассоциации изобретателей, и от всех индивидуумов было получено информированное согласие на их участие в исследованиях. Включение пациентов и контрольных групп в исследование, получение информированного согласия и забор проб крови проводили, по меньшей мере, через 6 месяцев (от 6 до 12 месяцев) после внутриутробной смерти плода. После сбора и обработки проб крови их хранили при -80°С в соответствии со стандартными процедурами. Протоколы взятия образцов у пациентов и контрольных образцов были одинаковыми.
Экспрессия рекомбинантного растворимого человеческого EPCR
Для экспрессии человеческого рекомбинантного EPCR в растворимой форме (rhsEPCR) проводили амплификацию последовательности человеческого растворимого EPCR (hsEPCR), содержащей внеклеточный домен без его сигнального пептида или трансмембранные и внутриклеточные домены (Entrez-Protein 21730830, остатки 1-193, пронумерованные в соответствии с нумерацией зрелой формы белка после процессинга сигнального пептида), посредством полимеразной цепной реакции (ПЦР) с использованием праймеров:
SEQ ID NO:1 и
SEQ ID NO:2,
которые вводят в рестрикционный ClaI-сайт и другой NotI-сайт у 5'- и 3'-концов, соответственно, с использованием кДНК эндотелиальных клеток в качестве матрицы. Эти модификации позволяют присоединять последовательность rhsEPCR к ClaI- и NotI-сайтам плазмиды pPICZαС (Stratagene, La Jolla, CA) после секреции сигнала фактора-α от Saccharomyces cerevisiae и обеспечивают эффективную секрецию многих белков во внеклеточную среду из дрожжевых клеток.
Вставку клонировали с сохранением рамки считывания эпитопа с-myc и 6-гистидиновой метки, присутствующих в векторе pPICZαС. В результате такого клонирования сериновый остаток и изолейциновый остаток были добавлены к амино-концу rhsEPCR, и при экспрессии rhsEPCR к его кабокси-концу присоединялась хвостовая последовательность или метка, содержащая эпитоп с-myc и 6 гистидинов, что облегчало очистку и связывание rhsEPCR со дном лунок микропланшета посредством моноклонального антитела против с-myc. Прямое секвенирование подтвердило, что последовательности вставки и вектора были “правильными”. В SEQ ID NO:3 показана последовательность полученного таким образом rhsEPCR, выведенная из ДНК-последовательности, где указанная последовательность содержит остатки, добавленные используемым методом клонирования, остатки внеклеточной области человеческого rhsEPCR, эпитопа с-myc и метки из 6 гистидинов.
Предварительно полученный экспрессионный вектор линеаризовали рестриктирующим ферментом PmeI, и клетки Pichia pastoris химически трансформировали этим вектором (Easy Comp, Invitrogen), в результате чего последовательность, кодирующая rhsEPCR, интегрировалась посредством гомологочной рекомбинации в эндогенный промотор, восприимчивый к метанолу. Продукт трансформации культивировали в присутствии зеоцина для отбора колоний P. pastoris, трансформированных вектором, содержащим последовательность, кодирующую rhsEPCR, которая, в свою очередь, содержит ген резистентности к зеоцину. Вкратце, трансформированные дрожжи культивировали в 4 мл среды BMY [1% (масс./об.) дрожжевого экстракта, 2% (масс./об.) пептона, 100 мМ фосфата калия (рН 6,0), 1,34% (масс./об.) сульфата аммония, являющегося источником азота дрожжей, 4×10-5% (масс./об.) биотина], в которую был добавлен 1% (об./об.) глицерина (BMGY), и инкубировали при 28-30°С в течение примерно 18 часов при перемешивании. Клетки собирали центрифугированием при 2000×g в течение 5 минут при комнатной температуре. Супернатант отбрасывали и экспрессию rhsEPCR индуцировали 1% метанолом в течение 18 часов. Для этого клетки ресуспендировали в 3 мл среды BMY с 0,5% (масс./об.) метанолом, а затем инкубировали при интенсивном перемешивании в течение 18 часов приблизительно при 28-30°С. После индуцирования образцы кондиционированной среды загружали на 12% бис-трис-гели NuPAGE (Invitrogen, Carlsbad, CA) и rhsEPCR детектировали с помощью Вестерн-блот-анализа с использованием моноклонального анти-myc антитела (Invitrogen). Для крупномасштабного продуцирования проводили отбор колоний, которые секретировали самую высокую концентрацию rhsEPCR. Колонии, отобранные по высокому продуцированию в них rhsEPCR, исследовали на метаболизм метанола (то есть оценивали на быстрый или медленный метаболизм), что позволяет таким образом определить оптимальные условия экспрессии для наиболее адекватной колонии. После оптимизации условий культивирования и индуцирования метанолом масштаб продуцирования увеличивали для получения больших количеств rhsEPCR.
Очистка рекомбинантного sEPCR.
Поскольку P. pastoris секретирует очень небольшое количество белков в среду, то высокое содержание белков, обнаруженных в культуральной среде, соответствовало белку rhsEPCR, что значительно облегчало процедуру его очистки. Вкратце, rhsEPCR очищали из супернатантов дрожжевых культур путем проведения трехстадийной процедуры очистки, включающей аффинную хроматографию на металле, анионообменную хроматографию и гель-фильтрацию. Для этого супернатант культуры концентрировали и диализовали против 100 мМ фосфата натрия, 10 мМ NаСl, рН 7,6, а затем проводили аффинную хроматографию на металле на 5 мл-колонке Hitrap (Amersham Bioscience, Little Chalfont, United Kingdom), нагруженной медью. Фракцию, которая связывалась с колонкой, элюировали буфером, содержащим этилендиаминтетрауксусную кислоту (EDTA), и диализовали против Трис-HCl, 20 мМ (рН 7,6), не содержащего NaCl. Затем проводили анионообменную хроматографию на колонке Resource Q (Amersham Biosciences) и осуществляли элюирование 0,0-300 мМ градиентом NaCl в объеме, эквивалентном объему 20 колонок. Элюированные фракции, содержащие rhsEPCR, объединяли и концентрировали путем центрифугирования-ультрацентрифугирования, а затем загружали на колонку с Superdex 75-HR10/30 (Amersham Biosciences) для гель-фильтрации. Концентрацию очищенного белка определяли с помощью теста на общий белок ВСА (Pierre, Rockford, IL) и с использованием стандартов альбумина бычьей сыворотки (BSA). Для детекции очищенного rhsEPCR образцы загружали на 12% бис-трис-гели NuPAGE (Invitrogen, Carlsbad, CA) и проводили электрофорез в восстанавливающих условиях с последующим окрашиванием кумасси синим. Один гель для электрофореза подвергали электроблоттингу и rhsEPCR детектировали с использованием моноклонального анти-myc антитела (Invitrogen). Для оценки молекулярной массы rhsEPCR в каждый гель для электрофореза включали стандарт молекулярной массы.
ELISA-анализ для определения уровней анти-EPCR аутоантител в сыворотке или в плазме
Были проведены отдельные измерения уровней анти-EPCR аутоантител, соответствующих изотипам IgG, IgА или IgМ, поскольку эти изотипы наиболее часто встречаются у пациентов с аутоиммунными нарушениями, при этом были детектированы антитела, направленные на некоторые структуры хозяев (аутоантитела).
Во всех трех случаях 96-луночные микропланшеты (Costar, Acton, МА, USA) сенсибилизировали 100 мкл/лунку моноклонального анти-с-myc антитела (Invitrogen, USA) при концентрации 1,5 мкг/мл в растворе Na2СO3 (100 ммоль/л), рН 9,6, в течение ночи при температуре 4°С. Это антитело использовали в виде иммобилизованного на лунке антитела, которое было направлено на присоединенную к rhsEPCR метку с-myc. Таким образом, rhsEPCR связывался с лункой с сохранением своих внеклеточных эпитопов. После промывки буфером ТВ (20 мМ трис, 150 мМ NаСl, 0,05% твина-20, рН 7,4) сайты неспецифического связывания блокировали 3% (масс./об.) ВSA в TB при комнатной температуре (к.т.) в течение 4,5 часа. Затем добавляли 100 мкл/лунку раствора, содержащего 3 мкг/мл rhsEPCR в TB с добавленной 1% ВSA (ТВ1), и инкубировали в течение 2 часов при комнатной температуре и при легком перемешивании. Одновременно с этим контрольные лунки инкубировали с ТВ1 в отсутствии rhsEPCR. После промывки TB в каждую лунку добавляли 100 мкл 1:100-разведения образца (плазмы или сыворотки) в TB1, а затем инкубировали в течение ночи при 4°С. После этого лунки промывали TB и анти-EPCR аутоантитела, которые оставались связанными с дном лунок, детектировали с использованием мышиного поликлонального антитела против человеческого IgА, конъюгированного с пероксидазой (Biotrend), мышиного поликлонального антитела против человеческого IgМ, конъюгированного с пероксидазой (Zymed), или мышиного поликлонального антитела против человеческого IgG, конъюгированного с щелочной фосфатазой (Zymed). После инкубирования в течение 2 часов при комнатной температуре и при легком перемешивании проводили промывку.
Для определения уровней анти-EPCR аутоантител изотипа IgА или IgМ добавляли 100 мкл раствора (0,4 мг/мл) орто-фенилендиамина (Kodak), содержащего 0,07М Nа2НРО4, 0,04М цитрата натрия и 0,02% (об./об.) H2O2, рН 5,0. После проявления в течение 5 и 8 минут в темноте для детекции IgА и IgМ, соответственно, к реакционной смеси добавляли 100 мкл Н2SO4 для прекращения реакции и через 5 минут проводили считывание оптической плотности при 492 нм в ридере для микропланшетов (iEMS REader, Labsystems, Finland).
В планшет, используемый для анализа анти-EPCR аутоантител изотипа IgG, добавляли 100 мкл раствора (1 нг/мл) 4-нитрофенилфосфатазы (Sigma) в 0,1М диэтаноламине, рН 10,3. Через 15 минут реакцию прекращали добавлением 100 мкл 1М NаОН и после стабилизации окраски регистрировали оптическую плотность при 405 нм в ридере для микропланшетов (iEMS REader). Все образцы анализировали, по меньшей мере, два раза в различных тестах.
Для подтверждения того, что все величины оптической плотности, измеренные в каждом планшете, соответствуют линейному диапазону, для каждого изотипа строили кривую с использованием серийных разведений образца, у которого была зарегистрирована наибольшая оптическая плотность. Для сравнения планшетов из каждого планшета брали образец для тестирования (стандартный образец), что позволяло вводить поправочный коэффициент. Условные единицы (AU) определяли следующим образом: для образца, взятого у каждого пациента (исследуемого образца), вычисляли удельную оптическую плотность путем вычитания оптической плотности контрольных лунок и умножения полученной величины на 1000 и на поправочный коэффициент, соответствующий отношению удельных оптических плотностей стандартного образца, тестируемого в данном планшете (контрольном планшете), и исследуемого образца, тестируемого в соответствующем планшете. Коэффициент вариации (КВ) для серии анализов и коэффициент вариации внутри отдельного анализа оценивали с использованием 5 образцов, тестируемых в 5 различных моментов времени, для вычисления коэффициента вариации для серии анализов (менее 5%), и в 3 различных момента времени, для вычисления коэффициента вариации внутри отдельного анализа (менее 10%).
Генерирование АРС в культивированных эндотелиальных клетках
Использовали клеточную линию EA.hy926, то есть линию трансформированных человеческих эндотелиальных клеток, сохраняющих способность экспрессировать тромбомодулин и EPCR (Stearns-Kurosawa DJ, Kurosawa S, Mollica JS, Ferrell GL, Esmon CT. The endothelial cell protein C receptor augments protein C activation by the thrombin-thrombomodulin complex. Proc. Natl. Acad. Sci. USA. 1996; 93:10212-6). 5×104 клеток/лунку инкубировали в 96-луночном планшете с 0,02 ед./мл тромбина (0,17 нМ) (ERL, Swansea, United Kingdom) и с возрастающими концентрациями РC (Baxter, Deerfield, IL, USA) в пределах от 50 до 1000 нМ в 20 мМ Трис-буфере, рН 7,4, в который было добавлено 150 мМ NaCl, 5 мМ СаCl2, 0,6 мМ MgCl2, 1% BSA, 0,001% Твина-20 и 0,02% NаN3. После выдерживания в течение 45 минут при комнатной температуре добавляли лепирудин (Schering AG, Berlin, Germany) при конечной концентрации 0,2 мкмоль/л для ингибирования тромбина и через 3-4 минуты добавляли хромогенный субстрат S-2366 (Chromogenix, Milan, Italy) при конечной концентрации 0,4 мМ для мониторинга его протеолиза под действием АРС. Увеличение оптической плотности при 405 нм кинетически регистрировали на ридере для микропланшетов (iEMS REader, Labsystems, Finland). Построение кривой по данным, вычисленным по уравнению Михаэлиса-Ментена, осуществляли с использованием программы Enzfitter (Biosoft, Cambridge, United Kingdom), которая позволяет вычислять Кm активации PC в данных условиях. Если необходимо, то 45 мкг/мл очищенных анти-EPCR аутоантител, взятых от пациентов (см. ниже), добавляли одновременно с тромбином и PC. Таким образом, может быть проанализировано влияние анти-EPCR аутоантител на активацию PC.
Очистка анти-EPCR антител
1. Очистка антител IgМ
Один миллилитр образцов сыворотки, содержащей анти-EPCR аутоантитела, разводили в забуференном фосфатом физиологическом растворе (PBS) (100 мМ фосфат натрия, 0,15 М NаСl, рН=7,4) и фильтровали через фильтр с размером пор 0,45 мкм. Фильтрат наносили на колонку HitTrap с NHS-активированной ПХ (Amersham Bioscience), на которой было предварительно иммобилизовано мышиное поликлональное антитело против человеческого IgМ (Maruyama S, Kubagawa H, Cooper MD. Activation of human B cells and inhibition of their terminal differentiation by monoclonal anti-murine antibodies. J. Immunol. 1985; 135:192-9). Человеческий IgМ элюировали 5 мл глицина, 0,1М, рН 2,5, и собирали в 100 мкл 1 М триса, рН 9,0. Фракцию, содержащую человеческий IgМ, концентрировали и диализовали против буфера TB, в который было добавлено 5 мМ СаCl2 и 0,6 мМ MgCl2, рН 7,4.
2. Очистка антител IgА
Один миллилитр образцов сыворотки разводили в PBS и вручную наносили на колонку с якалином (Pierce). Абсорбированную фракцию элюировали 2 мл 0,1М меллибиозы в PBS, а затем диализовали против PBS. Поскольку потребовалось проведение последующих стадий очистки, то для удаления контаминирующего IgG, образцы наносили на аффинную колонку HitTrap с G-белком, связанным с ПХ (Amersham Bioscience). Несвязанный продукт, содержащий фракцию IgА, диализовали против 50 мМ КН2РО4, рН 7,0, и наконец наносили на аффинную колонку HitTrap с сефарозой Blue, связанной с ПХ (Amersham Pharmacia Biotech), для удаления альбумина. Затем несвязанный материал, содержащий очищенную фракцию IgА, собирали и диализовали против буфера TB, в который было добавлено 5 мМ СаCl2 и 0,6 мМ MgCl2, рН 7,4.
3. Очистка антител IgG
Один миллилитр образцов сыворотки, содержащей анти-EPCR аутоантитела, разводили в забуференном фосфатом физиологическом растворе (PBS) (100 мМ фосфат натрия, 0,15 М NаСl, рН=7,4) и фильтровали через фильтр с размером пор 0,45 мкм. Фильтрат наносили на колонку HitTrap с G-белком, связанным с ПХ (Amersham Bioscience). Человеческий IgМ элюировали 5 мл глицина, 0,1М, рН 2,5, и собирали в 100 мкл 1 М триса, рН 9,0. Фракцию, содержащую человеческий IgМ, концентрировали и диализовали против буфера TB, в который было добавлено 5 мМ СаCl2 и 0,6 мМ MgCl2, рН 7,4.
Приготовление аффинной колонки с rhsEPCR
rhsEPCR (2 мг в 3 мл NaНСО3, 100 мМ, рН 8,5) связывали с аффинной колонкой HitTrap с NHS-активированной ПХ (Amersham Biosciences) в соответствии с инструкциями производителя. После прекращения реакции путем добавления 0,1 М глицина, колонку с rhsEPCR тщательно промывали 2М NаСl. Таким образом, с этой колонкой, содержащей rhsEPCR, мог связываться РC в буфере TBS, pH 7,4, в который были добавлены 20 мМ СаCl2 и 0,6 мМ MgCl2. PC мог элюироваться с колонки буфером TBS, в который был добавлен EDTA (данные не приводятся). Поскольку rhsEPCR, связанный с колонкой, сохранял свою способность связываться с PC, то можно с уверенностью сказать, что в данном случае сохранялись нативная конформация и эпитопы, распознаваемые указанными аутоантителами. Следовательно, приготовленная таким образом колонка является подходящей для элиминации анти-EPCR аутоантител из образца сыворотки или плазмы.
Статистические методы
При исследовании случаев заболевания APLS с использованием контроля проводили сравнение пациентов (случаев) с контролем по частоте появления высоких уровней анти-EPCR антител IgМ, IgА и IgG с использованием критерия “хи-квадрат”. Отношение вероятностей (OВ) (Martinez-Gonzales MA of Irala-Estevez J & Guillen Grima F, (1999), Que es una odds ratio?, Medicina Clinica, 112, 11:416-422) и 95% доверительный интервал (95% ДИ) вычисляли как показатель взаимосвязи между APLS и анти-EPCR аутоантителами.
В парном исследовании внутриутробной смерти плода методом “случай - контроль” сравнение между испытуемыми и контрольными индивидуумами осуществляли для непрерывных показателей и для категорийных показателей с использованием т-критерия для пар образцов и с использованием критерия Мак-Нимара соответственно. Взаимосвязь уровней анти-EPCR аутоантител, соответствующих изотипам IgG и IgM, с уровнями ACL и антител против кардиолипина изотипа IgM оценивали исходя из поправочных коэффициентов для непрерывных показателей и из критерия Манна-Уитни для категориийных показателей.
Для оценки риска внутриутробной смерти плода, ассоциированной с высокими уровнями анти-EPCR аутоантител изотипов IgG и IgМ, проводили множественный регрессионный анализ с использованием пар “случай-контроль”. Главными независимыми показателями являются уровни анти-EPCR аутоантител, соответствующих изотипам IgG и IgM, подчиняющимся распределению по категориям в соответствии с распределением этих иммуноглобулинов у контрольных индивидуума. Для определения уровней, ассоциированных с повышенным риском, использовали различные пороговые значения. Для построения кривой по данным известных факторов риска внутриутробной смерти плода осуществляли одномерный и мультимерный анализы. Включить факторы V Лейдена (FVL) и ACL в общую модель не представлялось возможным, а поэтому для оценки эффекта анти-EPCR аутоантител рассматривались две модели:
(1) модель одновременного введения анти-EPCR аутоантител, соответствующих изотипам IgМ и IgG, антител против кардиолипина изотипа IgМ, АСL и протромбина G20210А; и
(2) модель, идентичная модели 1, за исключением того, что вместо введения АСL она была скорректирована на присутствие/отсутствие FVL.
Модель (1) была использована для проверки гипотезы о том, что антитела против кардиолипина и АСL являются маркерами, а не этиологическими факторами, что указывает на то, протромботический статус индуцируется анти-EPCR аутоантителами. Все вычисления были проведены с использованием пакета программ для обработки статистических данных, SРSS, версии 10,0 (SРSS Inc.).
II. Результаты
Для исследования присутствия анти-EPCR аутоантител в плазме и сыворотке сначала получали rhsEPCR с использованием дрожжевой экспрессионной системы P. pastoris. В соответствии с описанным протоколом может быть проведена очистка более чем 5 мг rhsEPCR из культуры P. pastoris. С использованием электрофореза в полиакриламидном геле с додецилсульфатом натрия (ДСН-ПААГ) и Вестерн-блот-анализа с моноклональным анти-myc антителом было установлено, что rhsEPCR наблюдался в виде одиночной и слегка гетерогенной полосы, что указывало на различные степени гликозилирования, как сообщалось ранее (Fukudome K, Kurosawa S, Stearns-Kurosawa DJ, He X, Rezaie AR, Esmon CT. The endothelial cell protein C receptor. Cell surface expression and direct ligand binding by the soluble receptor. J. Biol. Chem. 1996; 271:17491-8)[см. фигуру 1].
rhsEPCR обладал способностью ингибировать антикоагулирующую активность АРС в тесте на свертывание крови, как было описано ранее (Regan LM, Stearns-Kurosawa DJ, Kurosawa S, Mollica J, Fukudome K, Esmon CT. The endothelial cell protein C receptor. Inhibition of activated protein C anticoagulant function without modulation of reaction with proteinase inhibitors. J. Biol. Chem. 1996; 271:17499-503)(данные не приводятся). Помимо связывания PC с ожидаемой аффинностью (см. ниже) активация PC тромбином на поверхности эндотелиальных клеток была охарактеризована по Кm=51±10 нМ. Такая активация значительно снижалась в присутствии 2 мкМ rhsEPCR (Кm приблизительно равно 1000 нМ), что указывает на то, что Кi приблизительно равно 70 нМ, и позволяет предположить, что rhsEPCR связывается с PC с такой же эффективностью, как и нативный EPCR, как сообщалось ранее (Fukudome K, Kurosawa S, Stearns-Kurosawa DJ, He X, Resaie AR, Esmon CT. The endothelial cell protein C receptor. Cell surface expression and direct ligand binding by the soluble receptor. J. Biol. Chem. 1996; 271:17491-8; Regan LM, Stearns-Kurosawa DJ, Kurosawa S, Mollica J, Fukudome K, Esmon CT. The endothelial cell protein C receptor. Inhibition of activated protein C anticoagulant function without modulation of reaction with proteinase inhibitors. J. Biol. Chem. 1996; 271:17499-503). Эти данные позволяют с полным основанием предположить, что нужная активность и “правильная” конформация rhsEPCR дает возможность использовать его для детекции антител против человеческого EPCR.
Анти-EPCR аутоантитела у пациентов с APLS
Если за высокие уровни принять уровни выше значений 97-го процентиля для каждой контрольной группы, то можно считать, что высокие уровни анти-EPCR аутоантител, соответствующих изотипам IgМ, IgА или IgG, ассоциируются с APLS [ОВ=4,47; 95% ДИ: 1,15-17,40] (см. таблицу 1). Исключительно высокие уровни анти-EPCR аутоантител (см. фигуру 2) детектировались лишь у индивидуумов с диагностированным APLS: у трех пациентов наблюдались очень высокие уровни анти-EPCR аутоантител изотипа IgМ (пациент А=407 AU, пациент В=301 AU и пациент С=293 AU), у двух пациентов с APLS наблюдались очень высокие уровни анти-EPCR аутоантител изотипа IgА (пациент D=795 AU и пациент В=475 AU, у которых также наблюдались высокие уровни анти-EPCR аутоантител изотипа IgМ), и у двух пациентов наблюдались высокие уровни анти-EPCR аутоантител изотипа IgG (пациент Е=230 AU и пациент F=220 AU). Все 6 пациентов были женщинами, в истории болезни которых был ранее диагностирован тромбоз, и это явилось одним из критериев отбора (инсульт у пациенток А, С, D и F; сердечно-сосудистое заболевание у пациентки Е и венозный тромбоз у пациенток А, В, D и F). Наиболее интересным наблюдением явился тот факт, что у всех женщин, у которых обнаруживались анти-EPCR аутоантитела изотипов IgМ и IgА (за исключением пациентки В, у которой оценку не проводили), было зарегистрировано несколько эпизодов внутриутробной смерти плода.
Исходя из этих данных был проведен анализ, направленный на выявление возможной взаимосвязи уровней анти-EPCR аутоантител с гибелью плода.
ОВ для APLS, ассоциированного с анти-EPCR антителами
(n=43)
(n=43)
Биохимическая характеризация анти-EPCR антител
Фракции анти-EPCR аутоантител изотипов IgМ, IgА и IgG, полученные от пациентов с очень высокими уровнями антител, очищали из 1 мл сыворотки. Фракция анти-EPCR аутоантител изотипа IgМ у пациента С способствовала снижению генерирования АРС культивированными эндотелиальными клетками в присутствии тромбина (20% от остаточной способности активировать PC, р = 0,02). Ингибирующий эффект был дозозависимым. Для иллюстрации того, что такой эффект фракции анти-EPCR аутоантител изотипа IgМ у пациента с APLS был обусловлен присутствием специфического антитела против EPCR, из образца полностью удаляли специфическое анти-EPCR аутоантитело путем его введения в аффинную колонку с иммобилизованным rhsEPCR. Полученная таким образом фракция теряла свое ингибирующее действие на генерирование АРС (87,6% от генерирования PC), что указывает на то, что агент, ответственный за данный феномен, должен представлять собой специфическое анти-EPCR аутоантитело. Ни одна из других фракций, выделенных у пациентов с APLS, не обладала способностью модифицировать уровень генерирования АРС в эндотелиальных клетках (фигура 3).
Анти-EPCR аутоантитела у женщин, у которых была зарегистрирована внутриутробная смерть плода
В таблице 2 указаны частота факторов риска, ассоциируемых, как было ранее установлено, с гибелью плода и с уровнем анти-EPCR аутоантител в группе пациентов и в контрольной группе.
Одномерные ОВ и их доверительные интервалы для пациенток с внутриутробной смертью плода, ассоциированной с различными исследуемыми переменными
(n=87)
(n=87)
95-тый процентиль уровней анти-EPCR аутоантитела изотипа IgМ в контрольной группе составлял 99 AU. Из 87 пациентов у 16 пациентов (18%) наблюдались уровни, превышающие пороговые величины по сравнению с уровнями у трех индивидуумов в контрольной группе (n=87). ОВ не корректировали за внутриутробную смерть плода у пациенток с уровнями анти-EPCR аутоантител изотипа IgМ, превышающими 95-тый процентиль, по сравнению с пациентками, у которых наблюдался более низкий уровень, равный 14 (95% доверительный интервал (ДИ): 1,8-106,4). Если пороговое значение было установлено равным значению 90-го процентиля (83 AU), то ОВ составляло 5,2 (95% ДИ: 1,8-15,3).
95-й процентиль уровней анти-EPCR аутоантитела изотипа IgG в контрольной группе составлял 94 АU. Из 87 пациентов у 13 пациентов (15%) наблюдались уровни, превышающие пороговые величины, по сравнению с уровнями у 4 индивидуумов в контрольной группе. ОВ не корректировали за внутриутробную смерть плода у пациенток с уровнями анти-EPCR аутоантител изотипа IgG, превышающими значение 95-того процентиля, которое составляло 4,3 (95% ДИ: 1,2-15,2). Если пороговое значение было установлено равным значению 90-го процентиля (88,4 AU), то ОВ составляло 2,3 (95% ДИ: 0,9-5,6).
Кроме того, был проведен многомерный анализ с поправкой за возможное смешивание факторов. Как указывалось выше, включить факторы FVL и ACL в одну и ту же многомерную модель не представлялось возможным, а поэтому рассматривались две различные модели: модель (1), скорректированная за антифосфолипидные антитела (то есть АСL и антитела против кардиолипина) и протромбин G20210А; и модель (2), включающая FVL, но не ACL. ОВ, ассоциированное с анти-EPCR аутоантителами изотипа IgМ, уровень которых превышает значение 95-го процентиля в модели (1), составляло 23,1 (95% ДИ: 2-266,3), а в модели (2) величина ОВ составляла 31,0 (95% ДИ: 2-384,3). ОВ, ассоциированное с анти-EPCR аутоантителами изотипа IgG, уровень которых превышает значение 95-го процентиля в модели (1), составляло 6,8 (95% ДИ: 1,2-38,4). В соответствии с моделью (2), которая включает фактор V Лейдена вместо АСL, величина ОВ, ассоциированная с анти-EPCR аутоантителами изотипа IgG, уровень которых превышает значение 95-го процентиля, составляла 11,0 (95% ДИ: 1,6-73,5). Результаты представлены в таблице 3.
Многомерные ОВ и их 95% доверительные интервалы, полученные в исследованиях внутриутробной смерти плода, ассоциированной с высокими уровнями анти-EPCR аутоантител
Эти результаты показали, что анти-EPCR аутоантитела изотипов IgМ и IgG являются независимыми факторами риска внутриутробной смерти плода. Однако значимой взаимосвязи высоких уровней IgА с внутриутробной смертью плода у женщин данной группы не наблюдалось.
III. Обсуждение
Был применен метод (в частности, ELISA-анализ), который позволяет детектировать присутствие аутоантител против человеческого EPCR. С использованием этой системы было проведено исследование группы пациентов с APLS, характеризующимся тромбозом и присутствием АСL, что указывало (впервые в патологии человека) на присутствие специфических анти-EPCR аутоантител изотипов IgМ, IgG и IgА. В центре этого исследования находилась подгруппа пациентов с APLS и АСL, поскольку они имели повышенный риск развития тромбоза, а следовательно, у этих индивидуумов, вероятно, должны были присутствовать аутоантитела, непосредственно ассоциированные с данными клиническими манифестациями. Было установлено, что, фактически, многие пациенты имели очень высокие уровни анти-EPCR аутоантител.
Присутствие этих аутоантител может служить объяснением наличия тромбоза и выкидышей, наблюдаемых у пациентов с APLS. Во-первых, EPCR представляет собой молекулу, экспрессируемую на эндотелии крупных кровеносных сосудов и на трофобласте. Иммуноглобулины IgМ и IgG могут связываться с комплементом и активировать этот комплемент, при этом, если указанные антитела направлены против EPCR, то они могут активировать комплемент на эндотелии и поражать этот эндотелий, стимулируя, тем самым, развитие тромбоза на этом уровне. Во-вторых, было обнаружено, что фракция IgМ у пациента с высокими уровнями анти-EPCR аутоантител изотипа IgМ может в значительной степени снижать уровень продуцирования АРС на эндотелиальных клетках в присутствии тромбина. Такой ингибирующий эффект исчезает после специфической элиминации IgМ, направленного против EPCR, путем совместного пропускания фракции IgМ через аффинную колонку с EPCR, а это означает, что такой ингибирующий эффект обусловлен присутствием анти-EPCR аутоантитела изотипа IgМ. Это антитело, вероятно, снижает уровни АРС in vivo, то есть создает ситуацию, которая сама по себе представляет серьезный фактор риска развития тромбоза.
При отборе пациентов в соответствии с критериями наличия венозного и/или артериального тромбоза невозможно оценить риск тромбоза, ассоциированного с анти-EPCR аутоантителами. В противоположность этому повышенные уровни анти-EPCR аутоантител, в частности изотипа IgМ, были детектированы у женщин, у которых в истории болезни была зарегистрирована внутриутробная смерть плода, в отличие от женщин, у которых ранее не наблюдались такие эпизоды. Исходя из результатов, полученных в экспериментальном исследовании, было принято решение о проведении парного исследования методом “случай-контроль” для оценки риска первого эпизода необъяснимой смерти плода у всех женщин, ассоциированной с присутствием анти-EPCR аутоантител. Было обнаружено, что высокие уровни анти-EPCR аутоантител изотипа IgМ (определенные как величина, превышающая 95-й процентиль распределения величин, полученных для контрольных индивидуумов), представляют высокий фактор риска первого внутриутробной смерти плода, при этом величина относительного риска составляет 23 или 31 по сравнению с более низкими уровнями. Высокие уровни анти-EPCR аутоантител изотипа IgG также представляют высокий фактор риска, хотя и меньший, чем в случае изотипа IgМ, при этом величина относительного риска составляет 7 или 11 в зависимости от используемой математической модели. В одномерном анализе АСL и антитело против кардиолипина изотипа IgМ ассоциируются с повышенным риском внутриутробной смерти плода, хотя такая взаимосвязь ослабляется в многомерной модели, возможно потому, что данные, полученные для классических антифосфолипидных антител, могут быть приписаны ассоциированным с ними анти-EPCR аутоантителам, которые могут представлять собой этиологический фактор внутриутробной смерти плода, а не просто показатель риска. Аналогичным образом было проведено исследование на присутствие FVL и протромбина G20210А, которые, как было недавно установлено, ассоциируются с повышенным риском поздней смерти плода, то есть с повышенным риском, установленным как в одномерном, так и в многомерном анализах, в сочетании с таким полиморфизмом. Однако этот риск не был статистически значимым, вероятно, из-за числа пациентов, участвующих в данном исследовании.
В заключение можно сказать, что это исследование впервые продемонстрировало присутствие анти-EPCR аутоантител у пациентов с APLS и тромбозом. Присутствие анти-EPCR аутоантител изотипов IgМ и IgG повышает риск первого эпизода смерти плода. Эти аутоантитела, по своей природе, могут способствовать развитию тромбоза и приводить к внутриутробной смерти плода у пациенток с APLS и у всех женщин в целом.
Пример 2
Детекция анти-EPCR аутоантител у женщин с инфарктом миокарда
Исследуемая группа: В эксперименте участвовали 142 женщины (в возрасте 39±5 лет, среднее ± стандартное отклонение) с инфарктом миокарда и 142 здоровых женщины (в возрасте 39±5 лет), имеющие тот же самый возраст и проживающие в одном и том же географическом регионе. В данном исследовании оценивали классические факторы риска инфаркта миокарда (гипертензию, гиперхолистеринемию, диабет, курение и прием пероральных противозачаточных средств). Были проведены анализы в целях оценки уровней анти-EPCR аутоантител изотипов IgG, IgМ и IgА в образцах плазмы в соответствии с протоколом ELISA-анализа, описанным в разделе “Материалы и методы” (пример 1).
Результаты: Высокие уровни анти-EPCR аутоантител, определенные как величины, превышающие 93-й процентиль распределения уровней анти-EPCR антител в контрольной группе, были ассоциированы с повышенным риском инфаркта миокарда. В многомерном анализе высокие уровни анти-EPCR антител были ассоциированы со скорректированным отношением вероятностей (ОВ), составляющим 3,5, при 95% доверительном интервале (95% ДИ), составляющим 1,4-8,9 для IgА, а в случае IgМ, как показано на фигурах, ОВ=3,0 при 95% ДИ, равном 1,2-7,5.
Вывод: Высокие уровни анти-EPCR аутоантител представляют собой независимый фактор риска инфаркта миокарда у женщин.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДИАГНОСТИКА ИНДУЦИРУЕМЫХ ГЛЮТЕНОМ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2548730C2 |
| СПОСОБ ДИАГНОСТИКИ АНТИФОСФОЛИПИДНОГО СИНДРОМА У ПАЦИЕНТОВ С ТРОМБОЗАМИ И/ИЛИ АКУШЕРСКОЙ ПАТОЛОГИЕЙ | 2022 |
|
RU2804231C1 |
| КОМПОЗИЦИЯ | 2015 |
|
RU2773344C2 |
| ПОЛИПЕПТИДНЫЕ ВАРИАНТЫ С ИЗМЕНЕННОЙ ЭФФЕКТОРНОЙ ФУНКЦИЕЙ | 2005 |
|
RU2367667C2 |
| КОМПОЗИЦИЯ | 2015 |
|
RU2728963C2 |
| ПРИМЕНЕНИЕ АНТИ-CD40-АНТИТЕЛ | 2006 |
|
RU2442606C2 |
| GLA ДОМЕНЫ В КАЧЕСТВЕ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2014 |
|
RU2705786C2 |
| СПОСОБ ВЫЯВЛЕНИЯ СТЕПЕНИ РИСКА АКУШЕРСКИХ ОСЛОЖНЕНИЙ | 2003 |
|
RU2239189C1 |
| СНИЖЕНИЕ КОЛИЧЕСТВА В-КЛЕТОК С ИСПОЛЬЗОВАНИЕМ CD37-СПЕЦИФИЧЕСКИХ И CD20-СПЕЦИФИЧЕСКИХ СВЯЗЫВАЮЩИХ МОЛЕКУЛ | 2006 |
|
RU2423381C2 |
| АНТИТЕЛА, МОДИФИЦИРУЮЩИЕ РАКОВЫЕ ЗАБОЛЕВАНИЯ | 2008 |
|
RU2468036C2 |




Изобретение относится к биологии и медицине, а именно к иммунодиагностике. Предложен способ оценки риска развития и предрасположенности к развитию патологии, ассоциированной с присутствием аутоантител против EPCR. Способ предусматривает определение уровня аутоантител против эндотелиального рецептора белка С/активированного белка С (EPCR) в образце. Присутствие высоких уровней аутоантител против EPCR ассоциировано с повышенным риском или восприимчивостью индивидуума к развитию аутоиммунных заболеваний, сосудистых заболеваний или осложнений беременности. 4 н. и 34 з.п. ф-лы, 3 ил., 3 табл.
1. Способ определения присутствия высоких уровней аутоантител против эндотелиального рецептора РС/активированного PC (EPCR) в образце, характеризующийся тем, что предусматривает количественную оценку аутоантител против EPCR in vitro в указанном образце, взятом у индивидуума.
2. Способ по п.1, отличающийся тем, что указанное присутствие высоких уровней аутоантител против EPCR ассоциировано с патологией, выбранной из аутоиммунного заболевания, сосудистого заболевания и осложнений беременности.
3. Способ по п.2, отличающийся тем, что указанное аутоиммунное заболевание выбрано из антифосфолипидного синдрома, системной красной волчанки, ревматоидного артрита и аутоиммунного васкулита.
4. Способ по п.2, отличающийся тем, что указанное сосудистое заболевание выбрано из артериального сосудистого заболевания, венозного сосудистого заболевания и тромбоза капиллярных кровеносных сосудов.
5. Способ по п.4, отличающийся тем, что указанное сосудистое заболевание выбрано из инфаркта миокарда, инсульта головного мозга, преходящего нарушения мозгового кровообращения, ишемии конечностей, атеросклероза, аневризмы, тромбоза, поверхностного венозного тромбоза, глубокого венозного тромбоза и эмболии легких.
6. Способ по п.2, отличающийся тем, что указанное осложнение беременности выбрано из выкидыша, внутриутробной смерти плода, преждевременных родов, замедленного внутриутробного развития, эклампсии и преэклампсии.
7. Способ по п.1, отличающийся тем, что указанным образцом является проба сыворотки или плазмы.
8. Способ по п.1, отличающийся тем, что указанным индивидуумом является человек.
9. Способ по п.1, отличающийся тем, что количественную оценку указанных анти-EPCR аутоантител осуществляют с помощью иммуноанализа с использованием маркера.
10. Способ по п.1, отличающийся тем, что количественную оценку указанных анти-EPCR аутоантител осуществляют с помощью ELISA-анализа, предусматривающего:
a) иммобилизацию на твердом носителе полипептида, содержащего аминокислотную последовательность EPCR или ее фрагмент, включающий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом;
b) инкубирование иммобилизованного полипептида с образцом, который, как предполагается, содержит анти-EPCR аутоантитела, и который был взят от указанного индивидуума, в течение периода времени, достаточного для связывания антител с иммобилизованным полипептидом, и образования комплексов "полипептид - анти-EPCR аутоантитело";
c) удаление оставшегося образца, не связанного с иммобилизованным полипептидом;
d) инкубирование комплексов "полипептид - анти-EPCR аутоантитело" со "вторым" антителом, конъюгированным с ферментом, где "второе" антитело способно связываться с указанными анти-EPCR аутоантителами.
11. Способ по п.10, отличающийся тем, что указанный полипептид выбран из:
а) полипептида, содержащего аминокислотные последовательности полноразмерного EPCR, и
b) полипептида, содержащего аминокислотную последовательность фрагмента EPCR, включающего, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR антителом.
12. Способ по п.10, отличающийся тем, что указанным полипептидом является гибридный белок, содержащий:
a) область А, состоящую из полипептида, содержащего аминокислотную последовательность EPCR или ее фрагмент, включающий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR антителом; и
b) область В, состоящую из полипептида, содержащего аминокислотную последовательность, используемую для выделения или очистки указанного гибридного белка, и/или аминокислотную последовательность, используемую для иммобилизации указанного гибридного белка на твердом носителе.
13. Способ по п.12, отличающийся тем, что указанная область В связана с амино-концом области А.
14. Способ по п.12, отличающийся тем, что указанная область В связана с карбокси-концом области А.
15. Способ по п.12, отличающийся тем, что указанная область А содержит аминокислотную последовательность растворимой части человеческого EPCR.
16. Способ по п.12, в котором аминокислотная последовательность, используемая для выделения или очистки указанного гибридного белка, и/или аминокислотная последовательность, используемая для иммобилизации указанного гибридного белка на твердом носителе, присутствующая в области В, содержит аминокислотную последовательность, выбранную из Arg-метки; His-метки; FLAG-метки; Strep-метки; эпитопа, который может распознаваться антителом; SBP-метки; S-метки; кальмодулин-связывающего пептида; домена, связывающегося с целлюлозой; хитин-связывающего домена; глутатион-S-трансферазной метки; белка, связывающегося с мальтозой; NusA, TrxA, DsbA, Avi-метки; Ala-His-Gly-His-Arg-Pro (SEQ ID NO:4) (2, 4 и 8 копий), Pro-Ile-His-Asp-His-Asp-His-Pro-His-Leu-Val-Ile-His-Ser (SEQ ID NO:5), Gly-Met-Thr-Cys-X-X-Cys (SEQ ID NO:6) (6 повторов), β-галактозидазы и VSV-гликопротеина.
17. Способ по п.12, отличающийся тем, что область В состоит из полипептида, содержащего эпитоп c-myc, который может распознаваться анти-с-myc антителом, и концевые гистидины (His-метку).
18. Способ по п.12, отличающийся тем, что указанный полипептид представляет собой гибридный белок, содержащий аминокислотную последовательность растворимой части человеческого EPCR, аминокислотную последовательность, соответствующую эпитопу с-myc и концевые гистидины (His-метку).
19. Способ по п.12, отличающийся тем, что указанным полипептидом является гибридный белок, аминокислотная последовательность которого представлена в SEQ ID NO:3.
20. Способ по п.10, отличающийся тем, что указанным "вторым антителом" является антитело, специфичное к иммуноглобулину определенного изотипа, и происходящее от вида, отличающегося от вида индивидуума, у которого был взят тестируемый образец.
21. Способ по п.20, отличающийся тем, что указанное "второе" антитело, специфичное к иммуноглобулину определенного изотипа, выбрано из антитела против человеческого IgG, антитела против человеческого IgM, антитела против человеческого IgA и их смесей.
22. Способ по п.20, отличающийся тем, что указанное "второе" антитело конъюгировано с ферментом, выбранным из пероксидазы и щелочной фосфатазы.
23. Способ по п.1, отличающийся тем, что он дополнительно предусматривает сравнение уровней анти-EPCR аутоантител, определенных в образце, взятом у индивидуума, с нормальными уровнями.
24. Способ по п.1, отличающийся тем, что он предусматривает определение изменения уровней анти-EPCR аутоантител в течение данного периода времени.
25. Способ по п.24, отличающийся тем, что указанный образец взят у индивидуума, у которого ранее было диагностировано аутоиммунное или сосудистое заболевание, или у пациентки, которая страдает осложнениями беременности и подвергается терапевтическому лечению.
26. Применение аутоантител против EPCR в способе обнаружения присутствия высоких уровней аутоантител против EPCR в образце.
27. Применение по п.26, отличающееся тем, что указанное присутствие высоких уровней аутоантител против EPCR в образце ассоциировано с патологией, выбранной из аутоиммунного заболевания, сосудистого заболевания и осложнений беременности.
28. Применение полипептида, содержащего аминокислотную последовательность EPCR или ее фрагмент, содержащий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом, в способе определения присутствия высоких уровней аутоантител против EPCR в образце, где указанное применение отличается тем, что оно включает количественную оценку in vitro аутоантител против EPCR в указанном образце.
29. Применение по п.28, отличающееся тем, что указанная патология, ассоциированная с присутствием высоких уровней аутоантител против EPCR, выбрана из аутоиммунного заболевания, сосудистого заболевания и осложнений беременности.
30. Применение по п.28, отличающееся тем, что указанным полипептидом является гибридный белок, содержащий:
а) область А, состоящую из полипептида, содержащего аминокислотную последовательность EPCR или ее фрагмент, включающий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR антителом; и
b) область В, состоящую из полипептида, содержащего аминокислотную последовательность, используемую для выделения или очистки указанного гибридного белка, и/или аминокислотную последовательность, используемую для иммобилизации указанного гибридного белка на твердом носителе.
31. Применение по п.30 полипептида, в котором указанная область А содержит аминокислотную последовательность растворимой части человеческого EPCR.
32. Применение по п.30, отличающееся тем, что указанный полипептид представляет собой гибридный белок, содержащий аминокислотную последовательность растворимой части человеческого EPCR, аминокислотную последовательность, соответствующую эпитопу c-myc, и концевые гистидины (His-метку).
33. Применение по п.28, отличающееся тем, что указанный полипептид представляет собой гибридный белок с аминокислотной последовательностью, представленной в SEQ ID NO:3.
34. Набор для in vitro определения присутствия высоких уровней анти-EPCR аутоантител в образце, отличающийся тем, что указанный набор содержит полипептид, включающий аминокислотную последовательность EPCR или ее фрагмент, содержащий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR аутоантителом.
35. Набор по п.34, отличающийся тем, что указанным полипептидом является гибридный белок, содержащий:
i) область А, состоящую из полипептида, содержащего аминокислотную последовательность EPCR или ее фрагмент, включающий, по меньшей мере, один эпитоп, который может распознаваться анти-EPCR антителом; и
ii) область В, состоящую из полипептида, содержащего аминокислотную последовательность, используемую для выделения или очистки указанного гибридного белка, и/или аминокислотную последовательность, используемую для иммобилизации указанного гибридного белка на твердом носителе.
36. Набор по п.35, в котором указанная область А отличается тем, что она содержит аминокислотную последовательность растворимой части человеческого EPCR.
37. Набор по п.35, отличающийся тем, что указанный полипептид представляет собой гибридный белок, содержащий аминокислотную последовательность растворимой части человеческого EPCR, аминокислотную последовательность, соответствующую эпитопу c-myc, и концевые гистидины (His-метку).
38. Набор по п.34, отличающийся тем, что указанный полипептид представляет собой гибридный белок с аминокислотной последовательностью, представленной в SEQ ID NO:3.
| OOSTING JD at al | |||
| Antiphospholipid antibodies directed against a combination of phospholipids with prothrombin, protein C, or protein S: an explanation for their pathogenic mechanism? Blood | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| Gu JM at al | |||
| Disruption of the endothelial cell protein С receptor gene in mice causes placental thrombosis and early embryonic | |||
Авторы
Даты
2009-12-10—Публикация
2005-02-03—Подача