Настоящее изобретение относится в целом к введению витамина Е в организм сельскохозяйственных животных с однокамерным желудком, таких как свиньи, а также птиц, рыб и креветок.
Витамин Е или d-α-токоферол в природе присутствует главным образом в растительных маслах; его получают разными синтетическими способами в виде рацемата d,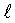 -α-токоферол (сокращенно Tol). Витамин Е в нативном виде представляет собой маслянистую, липофильную жидкость, смешивающуюся в любой пропорции с любой гидрофобной или липидной фазой. Витамин Е чрезвычайно нестабильный и легкоокисляемый, в окисленном состоянии теряет свое главное свойство: биологическую активность. Его биологическая доступность при нахождении в организме животного не превышает 50% после орального введения, так как, быстро окислившись, он в большинстве своем поглощается в окисленной неактивной форме. Поэтому в тех случаях, когда его назначают орально, витамин Е применяют в виде более стабильного производного, которое выбирается, как правило, из сложных эфиров, например ацетата, и солей витамина Е.
-α-токоферол (сокращенно Tol). Витамин Е в нативном виде представляет собой маслянистую, липофильную жидкость, смешивающуюся в любой пропорции с любой гидрофобной или липидной фазой. Витамин Е чрезвычайно нестабильный и легкоокисляемый, в окисленном состоянии теряет свое главное свойство: биологическую активность. Его биологическая доступность при нахождении в организме животного не превышает 50% после орального введения, так как, быстро окислившись, он в большинстве своем поглощается в окисленной неактивной форме. Поэтому в тех случаях, когда его назначают орально, витамин Е применяют в виде более стабильного производного, которое выбирается, как правило, из сложных эфиров, например ацетата, и солей витамина Е.
Прежде чем рассмотреть наиболее близкий прототип изобретения и проблемы, не решенные в этом прототипе, а также описать изобретение, ниже приводится определение понятия биологической доступности вещества, как оно понимается далее в описании. Биологическая доступность витамина Е или производного витамина Е определяется концентрацией этого витамина, поступившего в кровь, по отношению к концентрации витамина Е в рационе животного или по отношению к концентрации, выраженной в эквиваленте витамина Е его производного, введенного в рацион животного в случае назначения применения производного витамина. Следовательно, такое определение понятия биологической доступности витамина Е предполагает всасывание витамина Е или его производного кишечником во время пищеварительного пассажа.
Согласно Т.Julianto и др., International Journal of Pharmaceutics, №200, 2000 г., стр.53-57, готовили раствор витамина Е в пальмовом масле с добавлением смеси эмульгаторов, разводили водой и исследовали биологическую доступность витамина Е в организме человека, а затем сравнили ее с биологической доступностью витамина Е, вводимого в виде желатиновых капсул. Оказалось, что при введении витамина Е в виде указанного выше раствора его доступность витамина Е в три раза выше. Однако, принимая во внимание нестабильность витамина Е в неэтерифицированном виде, такой раствор не может найти применения в качестве пищевой добавки.
Известны разные кормовые добавки для животных, в частности добавки, производимые заявителем, в которые витамин Е вводится в виде ацетата или ацетата d,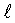 -α-токоферила (Тас) в адсорбированной форме на разных носителях, например на двуоксиде кремния, или в других формах, например в виде эмульсии “масло в воде”.
-α-токоферила (Тас) в адсорбированной форме на разных носителях, например на двуоксиде кремния, или в других формах, например в виде эмульсии “масло в воде”.
После публикации Н.Е.Gallo-Torres, Lipids, 1970 г., т.5, №4, стр.379-384, стало известно, что ацетат d, -α-токоферила непосредственно не усваивается человеком и животными и что он действительно подвергается гидролизу с превращением в витамин Е, происходящему в желудочно-кишечном тракте под действием панкреатических ферментов, так называемых холестерин-эстерогидролаз (сокращенно СЕН), при этом окончательное всасывание витамина Е происходит в тонком кишечнике. Однако ацетат d,
-α-токоферила непосредственно не усваивается человеком и животными и что он действительно подвергается гидролизу с превращением в витамин Е, происходящему в желудочно-кишечном тракте под действием панкреатических ферментов, так называемых холестерин-эстерогидролаз (сокращенно СЕН), при этом окончательное всасывание витамина Е происходит в тонком кишечнике. Однако ацетат d, -α-токоферила имеет ограниченную биологическую доступность, составляющую, например, 40%, независимо от того, какому животному он вводится.
-α-токоферила имеет ограниченную биологическую доступность, составляющую, например, 40%, независимо от того, какому животному он вводится.
Целью настоящего изобретения является повышение биологической доступности производных витамина Е, в частности ацетата d, -α-токоферила. Совершенно неожиданно было обнаружено, что присутствие специального эмульгатора существенно повышает биологическую доступность производного витамина Е, причем указанное производное витамина Е является гидролизуемым и превращается в усвояемую форму витамина Е. Указанный эмульгатор является кормовым и выбирается из неэтоксилированных сложных эфиров сорбитола и жирных кислот.
-α-токоферила. Совершенно неожиданно было обнаружено, что присутствие специального эмульгатора существенно повышает биологическую доступность производного витамина Е, причем указанное производное витамина Е является гидролизуемым и превращается в усвояемую форму витамина Е. Указанный эмульгатор является кормовым и выбирается из неэтоксилированных сложных эфиров сорбитола и жирных кислот.
Из документа SU-1676572 известна композиция, содержащая ацетат витамина Е, полиэтоксилированный эмульгатор и этанол. Эта композиция добавляется в питье для птиц в количестве, обеспечивающем суточную дозу витамина Е в количестве около 3 мг за определенный период времени. Авторы проследили за усвояемостью витамина Е, при этом коэффициент выживания и прибавка веса птиц несколько превысили те же показатели, получаемые при использовании традиционных композиций.
Проблема, связанная с биологической доступностью витамина Е для сельскохозяйственных животных при добавке его в кормовой рацион, по-прежнему сохраняется ввиду очень низкой его биодоступности, обеспечиваемой с помощью известных композиций.
Заявитель обнаружил большее влияние эмульгатора на биологическую доступность витамина Е в составе композиции и, особенно, полиэтоксилированного эмульгатора. Им также было установлено, что данный эмульгатор способствует гидролизу производного витамина Е в желудочно-кишечном тракте с получением усваиваемой формы, причем это явление положительно влияет на высвобождение биологически эффективного витамина Е.
Подробнее изобретение описывается ниже, его преимущества приводятся в примерах, в частности в сравнительных примерах.
Согласно предпочтительному варианту осуществления изобретения эмульгатор выбирается из сложных эфиров жирной кислоты с длинной цепью, например, таких, как содержащих насыщенную или ненасыщенную углеводородную цепь, содержащую, по меньшей мере, 11 атомов углерода.
Таким образом, первым объектом изобретения является зоотехнический способ, позволяющий вводить в организм сельскохозяйственных животных с однокамерным желудком композицию из производного витамина Е, в которой витамин Е остается защищенным до своего поступления на участок всасывания и одновременно обладает высокой биологической доступностью. Способ согласно изобретению не является лечебным и состоит в оральном введении в организм сельскохозяйственных животных с однокамерным желудком стабильного производного витамина Е по отдельности или в виде смеси с добавкой и/или кормом, при этом указанное производное является гидролизуемым с превращением в усваиваемую форму витамина Е в присутствии, по меньшей мере, одного кормового эмульгатора, выбираемого из неэтоксилированных сложных эфиров сорбитола и жирных кислот.
Под жирной кислотой согласно изобретению понимается преимущественно монокарбоновая кислота с углеводородной цепью с n атомами углерода, при этом n означает целое число от 0 до 30, указанная цепь является насыщенной или ненасыщенной. Согласно более предпочтительному варианту жирные кислоты согласно изобретению содержат насыщенную или ненасыщенную углеводородную цепь, содержащую, по меньшей мере, 11 атомов углерода.
Способ согласно изобретению предусматривает введение в организм животного одновременно или последовательно производного витамина Е и эмульгатора, например сначала вводится эмульгатор, а затем производное витамина Е. Следовательно, производное витамина Е и/или эмульгатор или эмульгаторы могут быть примешаны к корму.
Также изобретение касается кормовой композиции для животных, позволяющей, в частности, применять описанный выше способ, в котором указанная композиция содержит стабильное производное витамина Е, причем это производное является гидролизуемым с превращением в усваиваемую форму витамина Е, и, по меньшей мере, один кормовой эмульгатор, выбираемый из неэтоксилированных сложных эфиров сорбитола и жирных кислот. Согласно одному из вариантов изобретения предпочтительно применять два кормовых эмульгатора, соответствующих приведенному выше определению.
Композиция согласно изобретению удовлетворяет преимущественно, по меньшей мере, одной из приведенных ниже характеристик.
Весовое отношение между эмульгатором или эмульгаторами и производным витамина может составлять от 10:1 до 1:200, преимущественно от 1:5 до 1:100.
Производное витамина Е представляет собой преимущественно сложный эфир витамина Е, в частности ацетат витамина Е.
Предпочтительным эмульгатором служит сложный эфир сорбитола, выбираемый из монолаурата, монопальмитата, моностеарата, моноолеата и тристеарата. Моноолеат является предпочтительным.
Как будет показано в приводимых ниже примерах, предпочтительная композиция согласно изобретению содержит ацетат витамина Е и, по меньшей мере, один эмульгатор, выбираемый из монолаурата сорбитола и моноолеата сорбитола.
Другим объектом изобретения является применение кормового эмульгатора, выбираемого из неэтоксилированных сложных эфиров сорбитола и жирных кислот и предназначенного для приготовления кормовой композиции для животных на основе производного витамина Е, при этом предпочтительно, чтобы указанные жирные кислоты соответствовали приведенному выше определению.
Еще одним объектом изобретения является применение описанного выше кормового эмульгатора, предназначенного для повышения биологической доступности витамина Е в организме сельскохозяйственных животных с однокамерным желудком, причем это производное является гидролизуемым с превращением в усваиваемую форму витамина Е.
Приводимые ниже примеры показывают влияние эмульгатора согласно изобретению на биологическую доступность производного витамина Е, его большую эффективность по сравнению с известными эмульгаторами и его влияние на гидролиз производного витамина Е, со ссылкой на чертежи, на которых:
фиг.1 представляет собой график, на котором показано эквивалентное количество витамина Е, связанного клеточной культурой, в нмолях/см2 в зависимости от количества инкубированного ацетата d, -α-токоферила в нмолях/см2, при этом ацетат d,
-α-токоферила в нмолях/см2, при этом ацетат d, -α-токоферила инкубируется без моноолеата (пустые колонки) и с применением 0,05% моноолеата (заштрихованные колонки);
-α-токоферила инкубируется без моноолеата (пустые колонки) и с применением 0,05% моноолеата (заштрихованные колонки);
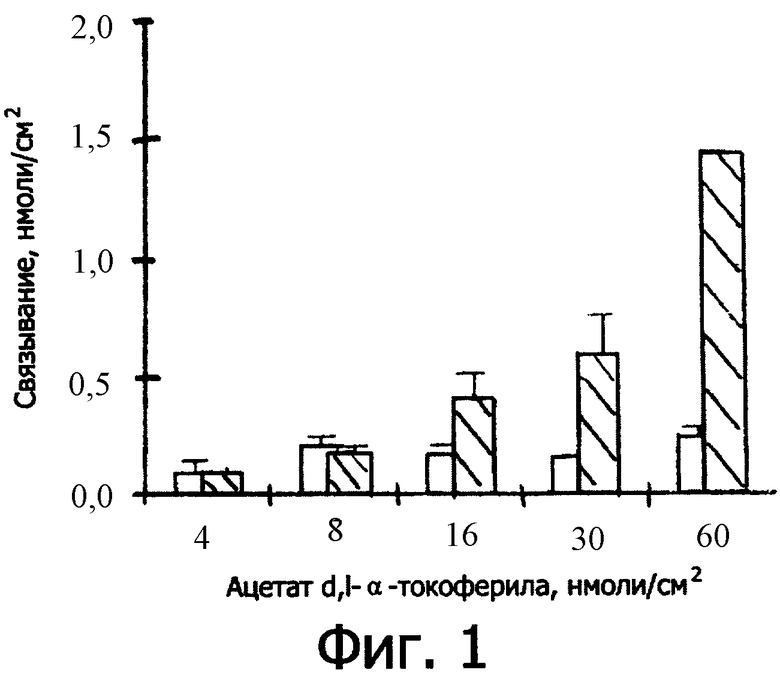
фиг.2 и 3 представляют собой графики, на которых показано эквивалентное количество связанного витамина Е, соответствующего ацетату ретинила (Rac, внутренний эталон) в черных колонках, ацетату d, -α-токоферила в заштрихованных колонках и ацетату d,
-α-токоферила в заштрихованных колонках и ацетату d, -α-токоферила в пустых колонках в зависимости от отсутствия или наличия и типа эмульгатора, инкубированного вместе с ацетатом d,
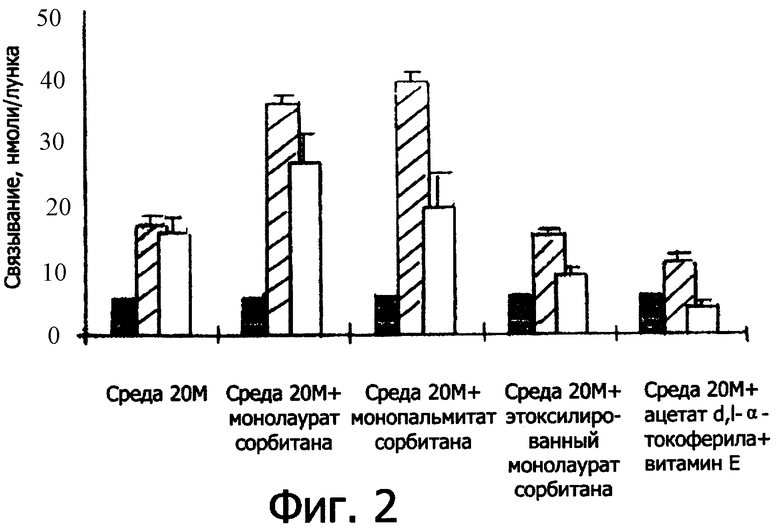
-α-токоферила в пустых колонках в зависимости от отсутствия или наличия и типа эмульгатора, инкубированного вместе с ацетатом d, -α-токоферила. Согласно фиг.2 соотношение между эмульгатором и эквивалентом витамина Е составляет 6, согласно фиг.3 это соотношение равно 1;
-α-токоферила. Согласно фиг.2 соотношение между эмульгатором и эквивалентом витамина Е составляет 6, согласно фиг.3 это соотношение равно 1;
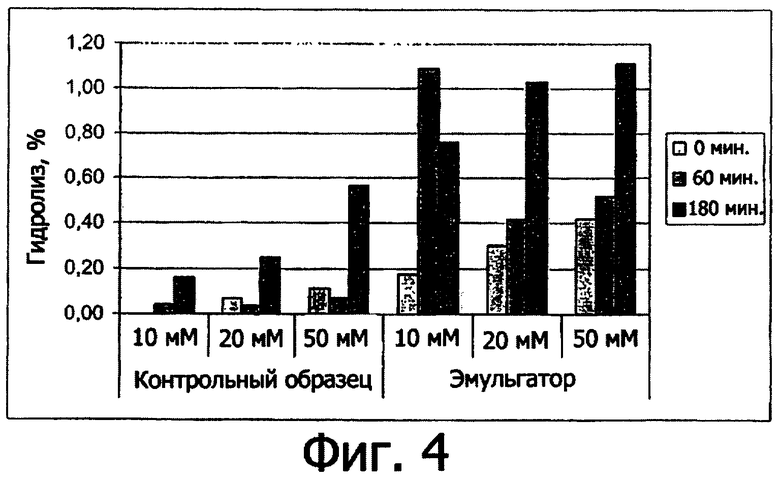
фиг.4 показывает степень гидролиза ацетата d, -α-токоферила и d,
-α-токоферила и d, -α-токоферола в зависимости от времени инкубации в условиях, описанных в примере 5, 5.2);
-α-токоферола в зависимости от времени инкубации в условиях, описанных в примере 5, 5.2);
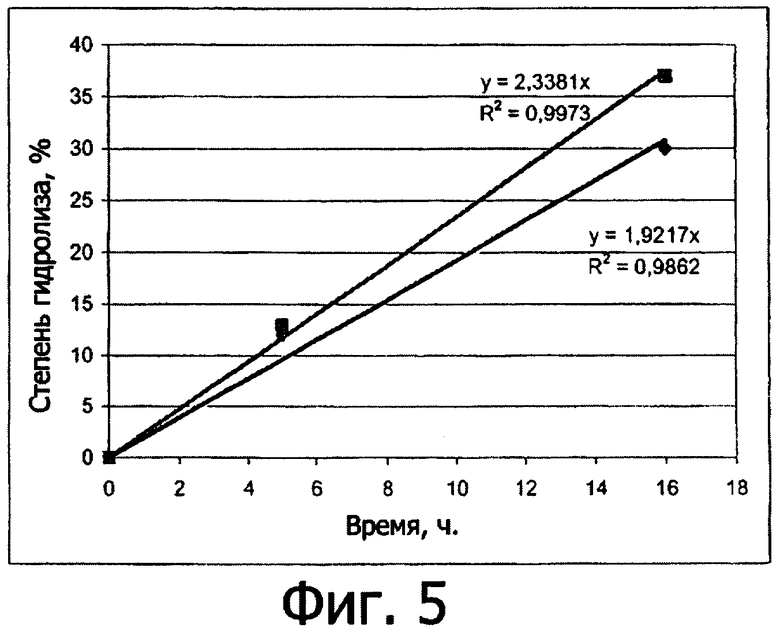
фиг.5 показывает степень гидролиза ацетата d,l-α-токоферила и d, -α-токоферола в зависимости от времени инкубации в условиях, описанных в примере 5, 5.1).
-α-токоферола в зависимости от времени инкубации в условиях, описанных в примере 5, 5.1).
Сведения, подтверждающие возможность осуществления изобретения
Пример 1. Влияние эмульгаторов на всасывание ацетата витамина Е (ацетат d, -α-токоферила) в клеточной системе in vitro
-α-токоферила) в клеточной системе in vitro
При проведении опытов in vitro на соответствующей клеточной модели определяли количество ацетата d, -α-токоферила, выраженное в эквиваленте витамина Е и связывающееся клеткой при инкубации соответствующей клеточной культуры, во-первых, в присутствии только одного ацетата d,
-α-токоферила, выраженное в эквиваленте витамина Е и связывающееся клеткой при инкубации соответствующей клеточной культуры, во-первых, в присутствии только одного ацетата d, -α-токоферила и, во-вторых, в присутствии ацетата d,
-α-токоферила и, во-вторых, в присутствии ацетата d, -α-токоферила и одного или нескольких кормовых эмульгаторов согласно изобретению.
-α-токоферила и одного или нескольких кормовых эмульгаторов согласно изобретению.
Применявшаяся клеточная модель представляла собой линию СаСО-2, доступную под номером НТВ-37 в American Type Culture Collection (ATCC).
Клеточную культуру указанной линии инкубировали в течение 3 часов с мицеллами ацетата d, -α-токоферила в воде.
-α-токоферила в воде.
Количество связавшихся с клеточной культурой мицелл определяли в нмолях/см2. Указанное количество составляло от 4 до 60 нмолей/см2.
По каждой концентрации ацетата d, -α-токоферила, введенного в клеточную культуру, измеряли количество ацетата d,
-α-токоферила, введенного в клеточную культуру, измеряли количество ацетата d, -α-токоферила, связанного клеточной культурой, выраженное в эквиваленте витамина Е в нмолях/см2, с одной стороны, без введенного в эту культуру эмульгатора и, с другой стороны, при содержании 0,05% (масса/объем) эмульгатора сорбитан моноолеата, при этом указанное процентное содержание было получено делением массы введенного в культуру эмульгатора на объем мицелл, введенных в эту же культуру.
-α-токоферила, связанного клеточной культурой, выраженное в эквиваленте витамина Е в нмолях/см2, с одной стороны, без введенного в эту культуру эмульгатора и, с другой стороны, при содержании 0,05% (масса/объем) эмульгатора сорбитан моноолеата, при этом указанное процентное содержание было получено делением массы введенного в культуру эмульгатора на объем мицелл, введенных в эту же культуру.
График на фиг.1 показывает количество связанного ацетата d, -α-токоферила, выраженное в эквиваленте витамина Е в нмолях/см2 по отношению к количеству инкубированного ацетата d,
-α-токоферила, выраженное в эквиваленте витамина Е в нмолях/см2 по отношению к количеству инкубированного ацетата d, -α-токоферила в нмолях/см2, при этом пустые колонки относятся к мицеллам, введенным без моноолеата, заштрихованные колонки - к мицеллам, введенным с использованием 0,05% моноолеата. При этом установлено, что чем больше количество инкубированного ацетата d,
-α-токоферила в нмолях/см2, при этом пустые колонки относятся к мицеллам, введенным без моноолеата, заштрихованные колонки - к мицеллам, введенным с использованием 0,05% моноолеата. При этом установлено, что чем больше количество инкубированного ацетата d, -α-токоферила, тем больше соответствующее эквивалентное количество витамина Е, причем в последнем опыте наблюдалось связывание ацетата d,
-α-токоферила, тем больше соответствующее эквивалентное количество витамина Е, причем в последнем опыте наблюдалось связывание ацетата d, -α-токоферила клетками, которое в шесть раз превышало связывание при использовании эмульгатора моноолеат.
-α-токоферила клетками, которое в шесть раз превышало связывание при использовании эмульгатора моноолеат.
Пример 2. Влияние эмульгаторов на всасывание ацетата витамина Е (ацетата d, -α-токоферила) и витамина Е в клеточной системе in vitro
-α-токоферила) и витамина Е в клеточной системе in vitro
2.1) Протокол эксперимента
Опыты по всасыванию проводились с той же линией клеток, которая описана выше, при инкубации клеток в течение 3 часов в физиологической среде, близкой к среде кишечника и содержавшей холестерин-эстерогидралазу (СЕН), панкреатитный фермент, гидролизующий ацетат d, -α-токоферила в организме животного в витамин Е, и таурохолат натрия, относящийся к желчным солям. Эта среда имеет вид эмульсии “масло в воде”, вид мицелл, и известна под коммерческой маркой М20. В нее вносили ацетат d,
-α-токоферила в организме животного в витамин Е, и таурохолат натрия, относящийся к желчным солям. Эта среда имеет вид эмульсии “масло в воде”, вид мицелл, и известна под коммерческой маркой М20. В нее вносили ацетат d, -α-токоферила и при необходимости исследуемый эмульгатор. Эквивалентная концентрация витамина Е, введенного в каждую лунку в виде ацетата d,
-α-токоферила и при необходимости исследуемый эмульгатор. Эквивалентная концентрация витамина Е, введенного в каждую лунку в виде ацетата d, -α-токоферила, составила 156 мкМ.
-α-токоферила, составила 156 мкМ.
Для каждого опыта применили по три планшеты с 6 лунками (площадь каждой лунки 9,6 см2), содержавшими указанную выше среду и соответственно разные эмульгаторы. Каждый опыт проводился трижды.
2.2) Весовое отношение добавленного в ацетат d, -α-токоферила эмульгатора (в эквивалентном количестве витамина Е) среды М20 составило около 6
-α-токоферила эмульгатора (в эквивалентном количестве витамина Е) среды М20 составило около 6
В данном опыте концентрация эмульгатора, введенного в среду М20, составила 0,05%, масса эмульгатора (эмульгаторов) к объему среды 20М, что приблизительно соответствует весовому отношению эмульгатора, добавленного в ацетат d, -α-токоферила среды 20М, равному около 6.
-α-токоферила среды 20М, равному около 6.
Было проведено шесть опытов, каждый из которых осуществляли трижды, при этом протоколом предусматривалась инкубация в течение 3 часов следующим образом:
1) только среда 20М из расчета 2 мМ среды М20 на лунку; следовательно, ацетат d, -α-токоферила применялся без эмульгатора;
-α-токоферила применялся без эмульгатора;
2) среда М20 + эмульгатор монолаурат сорбитана;
3) среда М20 + эмульгатор монопальмитат сорбитана;
4) среда М20 + эмульгатор полиоксиэтилированный монолаурат сорбитана;
5) среда М20 + смесь из 150 мкМ ацетата d, -α-токоферила и 156 мкМ d,
-α-токоферила и 156 мкМ d, -α-токоферола;
-α-токоферола;
6) внутренний стандарт, так называемый ацетат ретинила, служащий для проверки анализа.
На графике фиг.2 показаны результаты каждого опыта в нмолях эквивалента витамина Е, связанного лункой:
- количество ацетата ретинила, приведенное в черной колонке,
- количество ацетата d, -α-токоферила, связанное клетками и приведенное в заштрихованных колонках,
-α-токоферила, связанное клетками и приведенное в заштрихованных колонках,
- количество витамина Е, полученное гидролизом с последующим связыванием, приведенное в пустых колонках.
Как было обнаружено во время опытов 2) и 3), количество витамина Е, всасываемого клеточной культурой, возросло приблизительно на 50% по сравнению с всасываемым количеством с применением только одной среды М20.
Напротив, с помощью опыта 4) было установлено, что по сравнению с опытом 1) без эмульгатора эмульгатор полиоксиэтилированный монолаурат сорбитана, соответствующий этоксилированному эмульгатору (монолаурат сорбитана) в опыте 2), препятствует всасыванию ацетата d,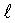 -α-токоферила и витамина Е.
-α-токоферила и витамина Е.
Неожиданно было установлено, что этоксилирование эмульгатора снижает положительное воздействие эмульгатора согласно изобретению на всасывание ацетата d, -α-токоферила и витамина Е.
-α-токоферила и витамина Е.
2.3) Весовое отношение эмульгатора, добавленного в ацетат d, -α-токоферила (в эквивалентном количестве витамина Е) среды М20, составило около 1.
-α-токоферила (в эквивалентном количестве витамина Е) среды М20, составило около 1.
В данном опыте концентрация эмульгатора, введенного в среду М20, составила 0,01%, выраженная в массе эмульгатора (эмульгаторов) к объему среды 20М, что приблизительно соответствует весовому отношению эмульгатора, добавленного в ацетат d, -α-токоферила среды 20М, равному около 1.
-α-токоферила среды 20М, равному около 1.
Было проведено шесть опытов, каждый из которых осуществляли трижды, при этом протоколом предусматривалась инкубация в течение 3 часов следующим образом:
1) только среда 20М из расчета 2 мМ среды М20 на лунку; следовательно, применялись только таурохолат натрия и ацетат d, -α-токоферила;
-α-токоферила;
2) среда М20 + эмульгатор монолаурат сорбитана;
3) среда М20 + эмульгатор монопальмитат сорбитана;
4) среда М20 + эмульгатор монолаурат сорбитана и эмульгатор монопальмитат сорбитана;
5) среда М20 + эмульгатор моноолеат сорбитана;
6) внутренний эталон, так называемый ацетат ретинила, для проверки анализа.
График на фиг.3 показывает по каждому опыту в нмолях эквивалента витамина Е для каждой лунки:
- количество ацетата ретинила, приведенное в черной колонке,
- количество ацетата d, -α-токоферила, связанное клетками и приведенное в заштрихованных колонках,
-α-токоферила, связанное клетками и приведенное в заштрихованных колонках,
- количество витамина Е, полученное гидролизом с последующим связыванием, приведенное в пустых колонках.
Даже при низком соотношении эмульгатора к количеству ацетата d, -α-токоферила (по сравнению с 2.2)) отмечается влияние эмульгатора согласно изобретению на всасывание ацетата d,
-α-токоферила (по сравнению с 2.2)) отмечается влияние эмульгатора согласно изобретению на всасывание ацетата d, -α-токоферила или витамина Е.
-α-токоферила или витамина Е.
Пример 3. Сравнение влияния эмульгаторов согласно изобретению с влиянием соответствующих этоксилированных эмульгаторов на всасывание ацетата d, -α-токоферила и витамина Е в клеточной системе in vitro
-α-токоферила и витамина Е в клеточной системе in vitro
3.1) Протокол эксперимента
Общие условия протокола по проведению эксперимента были идентичны условиям в примере 2, 2.1), разными были только площадь поверхности лунок и концентрация ацетата d, -α-токоферила, введенного в среду 20М. Площадь поверхности лунок составила 6,5 см2, концентрация ацетата d,
-α-токоферила, введенного в среду 20М. Площадь поверхности лунок составила 6,5 см2, концентрация ацетата d, -α-токоферила - 23,7 мкМ/см2.
-α-токоферила - 23,7 мкМ/см2.
3.2) Сравнение монолаурата сорбитана, монопальмитата сорбитана и полиоксиэтилированного монолаурата сорбитана
Было проведено четыре опыта, каждый из которых осуществляли трижды, при этом протоколом предусматривалась инкубация в течение 1 часа при 37°С следующим образом:
1) только среда 20М из расчета 2 мМ; следовательно, использовался только ацетат d, -α-токоферила без эмульгатора;
-α-токоферила без эмульгатора;
2) среда М20 + эмульгатор монолаурат сорбитана;
3) среда М20 + эмульгатор монопальмитат сорбитана;
4) среда М20 + эмульгатор этоксилированный монолаурат сорбитана.
По каждому из опытов 2), 3) и 4) весовое отношение эмульгатора, добавленного в ацетат d,l-α-токоферила (в эквивалентном количестве витамина Е), составило 1:6,9.
Полученные результаты представлены в таблице 1.
 -α-токоферол
-α-токоферол -α-токоферила
-α-токоферила
На основе этих результатов можно заключить, что эмульгаторы согласно изобретению позволяют увеличить всасывание d, -α-токоферола и ацетата d,
-α-токоферола и ацетата d, -α-токоферила при эквивалентном количестве витамина Е в 1,9 раза при использовании монолаурата сорбитана и в 1,78 раза при использовании монопальмитата сорбитана по сравнению с опытом 1), в котором применялся контрольный образец без эмульгатора.
-α-токоферила при эквивалентном количестве витамина Е в 1,9 раза при использовании монолаурата сорбитана и в 1,78 раза при использовании монопальмитата сорбитана по сравнению с опытом 1), в котором применялся контрольный образец без эмульгатора.
Напротив, было отмечено, что этоксилированный эмульгатор (полиоксиэтилированный монолаурат сорбитана) снижает всасывание витамина Е в 0,76 раза по сравнению с опытом 1).
3.3) Сравнение монолаурата сорбитана, монопальмитата сорбитана и этоксилированного моноолеата сорбитана
Было проведено четыре опыта, каждый из которых осуществляли трижды, при этом протоколом предусматривалась инкубация в течение 1 часа при 37°С следующим образом:
1) только среда 20М; следовательно, использовался только ацетат d, -α-токоферила без эмульгатора;
-α-токоферила без эмульгатора;
2) среда М20 + эмульгатор монолаурат сорбитана;
3) среда М20 + эмульгатор монопальмитат сорбитана;
4) среда М20 + эмульгатор этоксилированный моноолеат сорбитана.
В каждом из опытов 2), 3) и 4) весовое отношение эмульгатора, добавленного в ацетат d, -α-токоферила (в эквивалентном количестве витамина Е), составило 1:6,9.
-α-токоферила (в эквивалентном количестве витамина Е), составило 1:6,9.
Полученные результаты представлены в таблице 2.
 -α-токоферол
-α-токоферол -α-токоферила
-α-токоферила
На основе этих результатов можно снова заключить, что эмульгаторы согласно изобретению позволяют существенно увеличить всасывание d, -α-токоферола и ацетата d,
-α-токоферола и ацетата d, -α-токоферила при эквивалентном количестве витамина Е в 1,92 раза при использовании монолаурата сорбитана и в 1,81 раза при использовании монопальмитата сорбитана по сравнению с опытом 1), в котором применялся контрольный образец без эмульгатора.
-α-токоферила при эквивалентном количестве витамина Е в 1,92 раза при использовании монолаурата сорбитана и в 1,81 раза при использовании монопальмитата сорбитана по сравнению с опытом 1), в котором применялся контрольный образец без эмульгатора.
Также было обнаружено, что этоксилированный эмульгатор (этоксилированный моноолеат сорбитана) незначительно улучшает всасывание витамина Е по сравнению с опытом 1).
Пример 4. Влияние эмульгатора согласно изобретению на высвобождение ацетата d, -α-токоферила из своего носителя
-α-токоферила из своего носителя
В данном примере исследовали влияние эмульгатора согласно изобретению, моноолеата сорбитана, на высвобождение ацетата d, -α-токоферила, связанного двуоксидом кремния. С этой целью наносили ацетат d,
-α-токоферила, связанного двуоксидом кремния. С этой целью наносили ацетат d,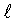 -α-токоферила на носитель из двуоксида кремния при весовом отношении 1:1 для проведения опыта без эмульгатора и ацетат d,
-α-токоферила на носитель из двуоксида кремния при весовом отношении 1:1 для проведения опыта без эмульгатора и ацетат d, -α-токоферила + эмульгатор (моноолеат сорбитана) на двуоксиде кремния при весовом отношении 50:5:45.
-α-токоферила + эмульгатор (моноолеат сорбитана) на двуоксиде кремния при весовом отношении 50:5:45.
Инкубировали 10 г ацетата d, -α-токоферила (при необходимости + моноолеат сорбитана) на упомянутом выше двуоксиде кремния (при этом конечная концентрация ацетата d,
-α-токоферила (при необходимости + моноолеат сорбитана) на упомянутом выше двуоксиде кремния (при этом конечная концентрация ацетата d, -α-токоферила составила 10 мМ) в течение 2,5 ч при перемешивании при 38°С в условиях с разными значениями показателя pH в следующих растворах:
-α-токоферила составила 10 мМ) в течение 2,5 ч при перемешивании при 38°С в условиях с разными значениями показателя pH в следующих растворах:
- либо раствор фосфата при 35 мМ, рН 6,5, NaCl 0,15 мМ,
- либо НСl / глицин при 35 мМ, pH 2,5.
Полученные результаты приведены в таблице 3.
 -α-токоферила без эмульгатора
-α-токоферила без эмульгатора -α-токоферила + моноолеат сорбитана
-α-токоферила + моноолеат сорбитана
При pH 2,5 добавление моноолеата сорбитана увеличило высвобождение ацетата d, -α-токоферила из своего носителя (двуоксида кремния) в 1,18 раза, т.е. более чем на 18%.
-α-токоферила из своего носителя (двуоксида кремния) в 1,18 раза, т.е. более чем на 18%.
При pH 6,5 увеличение произошло в 1,21 раза (т.е. на 21%).
Пример 5. Влияние эмульгатора согласно изобретению на гидролиз ацетата d, -α-токоферила с образованием d,l-α-токоферола, in vitro
-α-токоферила с образованием d,l-α-токоферола, in vitro
5.1) Влияние моноолеата сорбитана
В данном примере исследовали влияние эмульгатора моноолеата сорбитана на гидролиз ацетата d, -α-токоферила с образованием d,
-α-токоферила с образованием d, -α-токоферола. Для этого в опыте без эмульгатора применили ацетат d,
-α-токоферола. Для этого в опыте без эмульгатора применили ацетат d, -α-токоферила и ацетат d,
-α-токоферила и ацетат d, -α-токоферила + моноолеат сорбитана при весовом отношении 10:1.
-α-токоферила + моноолеат сорбитана при весовом отношении 10:1.
0,5 г ацетата d,l-α-токоферила (при необходимости + моноолеат сорбитана), т.е. при конечной концентрации ацетата d,l-α-токоферила 10 мМ, инкубировали в течение 16 часов при перемешивании при 38°С в следующем растворе:
фосфат 35 мМ, pH 6,5, NaCl 0,15 мМ, панкреатин при весовом отношении между панкреатином и ацетатом d, -α-токоферила 2:1, весовое отношение между желчными солями и ацетатом d,
-α-токоферила 2:1, весовое отношение между желчными солями и ацетатом d, -α-токоферила составило 5:1.
-α-токоферила составило 5:1.
Панкреатин представляет собой панкреатиновую вытяжку, содержащую, в частности, холестерин-эстерогидролазу, при этом желчные соли содержат активатор холестерин-эстерогидролазы.
В разное время инкубации, проводившейся в указанных выше условиях, измеряли степень высвобождения витамина Е по отношению к начальному количеству ацетата d, -α-токоферила.
-α-токоферила.
На фиг.5 показана степень гидролиза, выраженная концентрацией d, -α-токоферола в % (процентное соотношение массы) в растворе в зависимости от времени инкубации.
-α-токоферола в % (процентное соотношение массы) в растворе в зависимости от времени инкубации.
Можно отметить, что моноолеат сорбитана (■) повысил степень гидролиза ацетата d, -α-токоферила с образованием d,
-α-токоферила с образованием d, -α-токоферола на 22% (рассчитано на основе наклона кривых гидролиза) по сравнению с опытом без эмульгатора (♦).
-α-токоферола на 22% (рассчитано на основе наклона кривых гидролиза) по сравнению с опытом без эмульгатора (♦).
5.2) Влияние моноолеата сорбитана в зависимости от концентрации желчных кислот в инкубационном растворе
В данном опыте исследовали влияние эмульгатора согласно изобретению, моноолеата сорбитана, на гидролиз ацетата d, -α-токоферила с образованием d,
-α-токоферила с образованием d, -α-токоферола. Для этого применили ацетат d,
-α-токоферола. Для этого применили ацетат d, -α-токоферила в опыте без эмульгатора и ацетат d,
-α-токоферила в опыте без эмульгатора и ацетат d, -α-токоферила + моноолеат сорбитана при весовом отношении 10:1.
-α-токоферила + моноолеат сорбитана при весовом отношении 10:1.
4 мг ацетата d, -α-токоферила (при необходимости + моноолеат сорбитана), т.е. при конечной концентрации ацетата d,
-α-токоферила (при необходимости + моноолеат сорбитана), т.е. при конечной концентрации ацетата d, -α-токоферила 8,45 мкМ, инкубировали в течение 3 часов при перемешивании при 37°С в следующем растворе:
-α-токоферила 8,45 мкМ, инкубировали в течение 3 часов при перемешивании при 37°С в следующем растворе:
фосфат 35 мМ, pH 6,5, NaCl 0,15 мМ, панкреатин 2 мг, т.е. весовое отношение между панкреатином и ацетатом d, -α-токоферила составило 1:2, желчные соли имели разную концентрацию.
-α-токоферила составило 1:2, желчные соли имели разную концентрацию.
Проводились следующие опыты:
1) ацетат d, -α-токоферила без эмульгатора с применением желчных солей при 10 мМ,
-α-токоферила без эмульгатора с применением желчных солей при 10 мМ,
2) ацетат d, -α-токоферила + моноолеат сорбитана с применением желчных солей при 10 мМ,
-α-токоферила + моноолеат сорбитана с применением желчных солей при 10 мМ,
3) ацетат d, -α-токоферила без эмульгатора с применением желчных солей при 20 мМ,
-α-токоферила без эмульгатора с применением желчных солей при 20 мМ,
4) ацетат d, -α-токоферила + моноолеат сорбитана с применением желчных солей при 20 мМ,
-α-токоферила + моноолеат сорбитана с применением желчных солей при 20 мМ,
5) ацетат d, -α-токоферила без эмульгатора с применеием желчных солей при 50 мМ,
-α-токоферила без эмульгатора с применеием желчных солей при 50 мМ,
6) ацетат d, -α-токоферила + моноолеат сорбитана с применеием желчных солей при 50 мМ.
-α-токоферила + моноолеат сорбитана с применеием желчных солей при 50 мМ.
Перед инкубацией и после инкубации в течение соответственно 1 и 3 часов в приведенных выше условиях измерили степень высвобождения витамина Е по отношению к начальному количеству ацетата d, -α-токоферила.
-α-токоферила.
На фиг.4 показана степень гидролиза, выраженная в % (процентное соотношение массы) d, -α-токоферола в растворе.
-α-токоферола в растворе.
Снова было обнаружено, что моноолеат сорбитана существенно повышает степень гидролиза ацетата d, -α-токоферила с образованием d,
-α-токоферила с образованием d, -α-токоферола, активируя при этом холестерин-эстерогидролазу. Такое повышение определяется концентрацией желчных солей: оно возрастает в два раза при концентрации желчных солей 50 мМ, в 4,1 раза при концентрации 20 мМ и в 4,7 раза при концентрации 10 мМ.
-α-токоферола, активируя при этом холестерин-эстерогидролазу. Такое повышение определяется концентрацией желчных солей: оно возрастает в два раза при концентрации желчных солей 50 мМ, в 4,1 раза при концентрации 20 мМ и в 4,7 раза при концентрации 10 мМ.
Пример 6. Влияние эмульгатора согласно изобретению на биологическую доступность витамина Е в ацетате d, -α-токоферила, измеренную совокупным влиянием эмульгатора на высвобождение ацетата d,
-α-токоферила, измеренную совокупным влиянием эмульгатора на высвобождение ацетата d, -α-токоферила из своего носителя и гидролизом ацетата d,
-α-токоферила из своего носителя и гидролизом ацетата d, -α-токоферила с высвобождением d,
-α-токоферила с высвобождением d, -α-токоферола
-α-токоферола
В этом примере исследовали влияние эмульгатора согласно изобретению, т.е. моноолеата сорбитана. Для этого применили ацетат d, -α-токоферила на носителе из двуоксида кремния при весовом отношении 1:1 для проведения опыта без применения эмульгатора и ацетат d,
-α-токоферила на носителе из двуоксида кремния при весовом отношении 1:1 для проведения опыта без применения эмульгатора и ацетат d, -α-токоферила + эмульгатор моноолеат сорбитана на двуоксиде кремния при весовом отношении 50:5:45.
-α-токоферила + эмульгатор моноолеат сорбитана на двуоксиде кремния при весовом отношении 50:5:45.
8 мг ацетата d,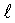 -α-токоферила (при необходимости + моноолеат сорбитана) на указанном выше двуоксиде кремния (т.е. при конечной концентрации ацетата d,
-α-токоферила (при необходимости + моноолеат сорбитана) на указанном выше двуоксиде кремния (т.е. при конечной концентрации ацетата d, -α-токоферила 16,9 мкМ) инкубировали в течение 3 часов при перемешивании при 37°С в следующих растворах:
-α-токоферила 16,9 мкМ) инкубировали в течение 3 часов при перемешивании при 37°С в следующих растворах:
фосфат 35 мМ, pH 6,5, NaCl 0,15, панкреатин (2 мг) и желчные соли (20 мМ).
Перед инкубацией и после инкубации в течение соответственно 1 и 3 ч в указанных условиях замерили концентрацию витамина Е в растворе по отношению к начальному количеству ацетата d, -α-токоферила.
-α-токоферила.
Полученные результаты приведены в таблице 4.
 -α-токоферила без эмульгатора
-α-токоферила без эмульгатора -α-токоферила + моноолеат сорбитана
-α-токоферила + моноолеат сорбитана
Добавка моноолеата сорбитана повысила биологическую доступность ацетата d, -α-токоферила, что определяется по доступности высвобождения ацетата d,
-α-токоферила, что определяется по доступности высвобождения ацетата d, -α-токоферила из своего носителя из двуоксида кремния и по доступности гидролиза ацетата d,
-α-токоферила из своего носителя из двуоксида кремния и по доступности гидролиза ацетата d, -α-токоферила с образованием d,
-α-токоферила с образованием d, -α-токоферола. Такое повышение составило свыше 90% через три часа инкубации, что явилось следствием возросшего высвобождения и ускоренного гидролиза.
-α-токоферола. Такое повышение составило свыше 90% через три часа инкубации, что явилось следствием возросшего высвобождения и ускоренного гидролиза.
Пример 7. Влияние эмульгаторов на экскрецию витамина Е в организме петухов
Провели две серии опытов на петухах. В первой серии использовалось 32 петуха, во второй - 51. Их откармливали “влажным кормом” с содержанием в нем ацетата d, -α-токоферила (ацетата витамина Е) или ацетата d,
-α-токоферила (ацетата витамина Е) или ацетата d, -α-токоферила с содержанием одного или двух кормовых эмульгаторов согласно изобретению в разных пропорциях. Ацетат d,
-α-токоферила с содержанием одного или двух кормовых эмульгаторов согласно изобретению в разных пропорциях. Ацетат d, -α-токоферила или ацетат d,
-α-токоферила или ацетат d, -α-токоферила с эмульгаторами приготовили в виде желатиновых капсул, которые получили нанесением определенного количества ацетата d,
-α-токоферила с эмульгаторами приготовили в виде желатиновых капсул, которые получили нанесением определенного количества ацетата d, -α-токоферила или ацетата d,
-α-токоферила или ацетата d, -α-токоферила с эмульгаторами с помощью пипетки на половинку капсулы, которую затем закрывали другой половинкой.
-α-токоферила с эмульгаторами с помощью пипетки на половинку капсулы, которую затем закрывали другой половинкой.
Через 48 часов после дачи корма фекальные массы собрали в банку и определили экскрецию витамина в них. Для этого витамин Е извлекли растворителем, например гексаном, затем определили извлеченное количество с помощью высокоэффективной жидкостной хроматографии. Количество переваренного витамина Е вычли из выделившегося количества.
7.1) Первая серия
 -α-токоферила
-α-токоферила
Отсюда следует, что способ согласно изобретению обеспечивает усвояемость витамина Е вплоть до 31% по отношению к контрольному образцу.
7.2) Вторая серия
 -α-токоферила
-α-токоферила
рат сорбитана
Как и в первой серии, в этой серии была обнаружена возросшая усвояемость витамина Е после его введения согласно изобретению. Такое увеличение может достигнуть 40,5% от усвояемости, получаемой только с помощью одного ацетата d, -α-токоферила.
-α-токоферила.
Пример 8. Влияние эмульгаторов на гидролиз производных витамина Е
8.1)
Опыты проводились в следующих условиях:
- клеточная модель: клетки СаСо2,
- площадь поверхности лунок: 6,5 см2,
- количество ацетата d, -α-токоферила: 67 нмолей/см2,
-α-токоферила: 67 нмолей/см2,
- применявшийся раствор: мицелла М40 согласно Mathias и др. (Mathias P.M., Harries J.T., Muller D.P.R., 1981 г. Optimization and validation of assays to estimate pancreatic ester activity using well-characterized micellar solutions of cholesteryl oleate and tocopheryl acetate. Journal of Lipid Research 22, стр.177-184) в сочетании с 1,34 нмоля/см2 холестерин-эстерогидролазы (ЕС 3.1.1.13).
Обработка:
А: без применения эмульгатора;
В: с применением эмульгатора (смесь из монолаурата сорбитана и моностеарата сорбитана при соотношении 1:1), соотношение между ацетатом d, -α-токоферила и эмульгатором: 100:1;
-α-токоферила и эмульгатором: 100:1;
С: с применением эмульгатора (смесь из монопальмитата сорбитана и моноолеата сорбитана при соотношении 1:1), соотношение между ацетатом d, -α-токоферила и эмульгатором: 100:1.
-α-токоферила и эмульгатором: 100:1.
Продолжительность инкубации: 1 ч при 37°С.
Анализ: анализ ацетата d, -α-токоферила в среде для расчета степени гидролиза.
-α-токоферила в среде для расчета степени гидролиза.
Результаты приведены в таблице 7.
 -α-токоферила, %
-α-токоферила, %
Из таблицы следует, что присутствие эмульгаторов увеличило в два раза степень гидролиза ацетата d, -α-токоферила. Эмульгаторы согласно изобретению улучшили условия гидролиза холестерин-эстерогидролазой.
-α-токоферила. Эмульгаторы согласно изобретению улучшили условия гидролиза холестерин-эстерогидролазой.
8.2)
Опыты проводились в следующих условиях:
- клеточная модель: клетки СаСо-2,
- площадь поверхности лунок: 4,2 см2,
- количество ацетата d, -α-токоферила: 67 нмолей/см2,
-α-токоферила: 67 нмолей/см2,
- применявшийся раствор: мицелла М 40 согласно Mathias и др. Обработка:
А: без применения эмульгатора;
В: с применением эмульгатора (смесь из монопальмитата сорбитана и моноолеата сорбитана при соотношении 1:1), соотношение между ацетатом d, -α-токоферила и эмульгатором: 100:1.
-α-токоферила и эмульгатором: 100:1.
Продолжительность инкубации: 2 ч при 37°С.
Анализ: анализ ацетата d, -α-токоферила в среде над клетками для расчета степени гидролиза.
-α-токоферила в среде над клетками для расчета степени гидролиза.
Результаты приведены в таблице 8.
 -α-токоферила, %
-α-токоферила, %
Присутствие эмульгаторов улучшило гидролиз ацетата d, -α-токоферила на 44%. Как и в 8.1) эмульгаторы улучшили условия проведения гидролиза холестерин-эстерогидролазой.
-α-токоферила на 44%. Как и в 8.1) эмульгаторы улучшили условия проведения гидролиза холестерин-эстерогидролазой.
Изобретение относится к зоотехническому, нелечебному способу орального введения в организм сельскохозяйственных животных с однокамерным желудком стабильного производного витамина Е. Способ предусматривает оральное введение в организм сельскохозяйственных животных с однокамерным желудком стабильного производного витамина Е, раздельно или в смеси с добавкой и/или кормом. Производное витамина Е является гидролизуемым с превращением в усваиваемую форму витамина Е. Указанное производное витамина Е наносят на носитель диоксид кремния и вводят животным в присутствии, по меньшей мере, одного кормового эмульгатора, выбираемого из неэтоксилированных сложных эфиров сорбита и жирных кислот, усиливающих биологическую усвояемость витамина Е и обеспечивающих отделение указанного производного от носителя - диоксида кремния. Изобретение касается также применения кормового эмульгатора, выбираемого из неэтоксилированных сложных эфиров сорбита и жирных кислот при приготовлении питательной композиции для кормления животных на основе производного витамина Е, нанесенного на носитель диоксид кремния, для усиления биологической усвояемости витамина Е и для обеспечения отделения указанного производного от носителя - диоксида кремния. Изобретение позволяет повысить биологическую доступность производного витамина Е. 2 н. и 13 з.п. ф-лы, 5 ил., 8 табл.
1. Зоотехнический нелечебный способ орального введения в организм сельскохозяйственных животных с однокамерным желудком стабильного производного витамина Е раздельно или в смеси с добавкой и/или кормом, причем это производное является гидролизуемым с превращением в усваиваемую форму витамина Е, отличающийся тем, что указанное производное витамина Е наносят на носитель диоксид кремния и вводят животным в присутствии, по меньшей мере, одного кормового эмульгатора, выбираемого из неэтоксилированных сложных эфиров сорбита и жирных кислот, усиливающих биологическую усвояемость витамина Е и обеспечивающих отделение указанного производного от носителя - диоксида кремния.
2. Способ по п.1, отличающийся тем, что производное витамина Е и, по меньшей мере, один из указанных эмульгаторов вводят животным одновременно.
3. Способ по п.1, отличающийся тем, что указанный эмульгатор вводят животным до введения витамина Е.
4. Способ по п.2, отличающийся тем, что производное витамина Е и/или указанный, по меньшей мере, один эмульгатор примешивают к корму.
5. Способ по п.3, отличающийся тем, что производное витамина Е и/или указанный, по меньшей мере, один эмульгатор примешивают к корму.
6. Способ по п.1, отличающийся тем, что указанный, по меньшей мере, один эмульгатор выбирают из сложных эфиров сорбита и жирных кислот с насыщенной или ненасыщенной углеводородной цепью, содержащей, по меньшей мере, 11 атомов углерода.
7. Способ по п.1, отличающийся тем, что эмульгатор представляет собой сложный эфир сорбита, выбираемый из монолаурата, монопальмитата, моностеарата, моноолеата и тристеарата.
8. Способ по п.1, отличающийся тем, что производное витамина Е вводят в присутствии двух кормовых эмульгаторов, выбираемых из неэтоксилированных сложных эфиров сорбита и жирных кислот.
9. Способ по п.1, отличающийся тем, что весовое отношение между эмульгатором или эмульгаторами и производным витамина Е изменяется от 10 : 1 до 1: 200.
10. Способ по п.9, отличающийся тем, что весовое отношение между эмульгатором или эмульгаторами и производным витамина Е составляет от 1: 5 до 1: 100.
11. Способ по п.1, отличающийся тем, что производное витамина Е представляет собой сложный эфир витамина Е.
12. Способ по п.1, отличающийся тем, что производное витамина Е представляет собой ацетат витамина Е.
13. Способ по п.1, отличающийся тем, что производное витамина Е представляет собой ацетат витамина Е и вводится в присутствии, по меньшей мере, одного эмульгатора, выбираемого из монолаурата сорбита и моноолеата сорбита.
14. Способ по п.1, отличающийся тем, что ацетат витамина Е и моноолеат сорбита наносят на диоксид кремния при весовом отношении 50:5:45.
15. Применение кормового эмульгатора, выбираемого из неэтоксилированных сложных эфиров сорбита и жирных кислот при приготовлении питательной композиции для кормления животных на основе производного витамина Е, нанесенного на носитель диоксид кремния, для усиления биологической усвояемости витамина Е и для обеспечения отделения указанного производного от носителя - диоксида кремния.
| WO 9842319 А, 01.10.1998 | |||
| Рабочий орган сельскохозяйственной машины | 1977 |
|
SU654206A1 |
| СПОСОБ ВЫРАБОТКИ КОЖ | 1995 |
|
RU2056709C1 |
| Витаминный кормовой аппарат "Диспервит Е" для птиц | 1989 |
|
SU1676572A1 |
Авторы
Даты
2009-12-20—Публикация
2004-10-22—Подача