Настоящее изобретение относится к применению системы, состоящей из сильнокислотной ионообменной смолы в качестве катализатора и (со)олигомеризационной добавки в качестве каталитической системы для олигомеризации с раскрытием цикла лактида и гликолида. Настоящее изобретение также относится к способу (со)олигомеризации лактида и гликолида, включающему применение такой каталитической системы.
В настоящее время все возрастающее внимание уделяют синтетическим полимерам для создания искусственных органов и композиций лекарственных веществ [Chem. Eng. News 2001, 79 (6), 30]. Полимеры, о которых идет речь, должны удовлетворять определенному количеству критериев и, в особенности, они должны быть биосовместимыми. Способность к биодеградации является дополнительным преимуществом, если полимер необходимо удалять после соответствующего периода имплантации в организме. В этом отношении сополимеры на основе молочной и гликолевой кислоты (PLGA) представляют большой интерес, поскольку они подвержены гидролизу и расщепляются in vivo с выделением нетоксичных продуктов. Область применения PLGA очень широка (Adv. Mater. 1996, 8, 305 и Chemosphere 2001, 43, 49). В хирургии их используют в качестве многожильных нитей, шовного материала, имплантантов, протезов и т.д. В фармакологии их применяют для инкапсулирования, доставки и контролируемого выделения активных ингредиентов.
Для всех этих применений ключевым фактором является скорость деградации PLGA, которая, конечно, зависит от их структуры (длины цепи, степени полидисперсности, соотношения компонентов, стереохимии и способа присоединения мономеров и т.д.). Поэтому в последние годы множество работ посвящено разработке катализаторов и/или промоторов (со)олигомеризации, т.е. полимеризации или сополимеризации лактида и гликолида, позволяющих получать PLGA контролируемой структуры.
Применение металлических систем обычно приводит к загрязнению получаемых таким образом сополимеров солями металлов, что создает серьезные ограничения, зависящие от предполагаемых применений. Поэтому разработка неметаллических систем, осуществляющих контролируемую сополимеризацию лактида и гликолида, является важным выходом. Настоящее изобретение попадает в эту категорию и больше относится к низкомолекулярным (со)полимерам лактида и гликолида, т.е. к (со)олигомерам лактида и гликолида.
Поэтому заявитель предлагает применение простой каталитической системы, состоящей из катализатора и (со)олигомеризационной добавки и позволяющей контролировать не только длину цепи, но также и природу концевых групп получаемых (со)олигомеров. Применение ионообменной смолы в качестве катализатора позволяет отделять олигомеры от катализатора простым и эффективным способом, причем катализатор может быть повторно использован без потери активности.
Поэтому целью настоящего изобретения является применение каталитической системы, образованной
(a) полимерным катализатором (1) на основе сильнокислотной ионообменной смолы и
(b) (со)олигомеризационной добавкой общей формулы (2)
R 1 -E-R 2
(2)
в которой
Е представляет собой элемент 16-й группы;
R1 представляет собой атом водорода или дейтерия;
R2 представляет собой атом водорода или дейтерия или группу в формуле -E14(R14)(R'14)(R''14);
E14 является элементом 14-й группы;
R14, R'14, R''14 представляют собой, независимо, атом водорода; атом дейтерия; один из следующих замещенных или незамещенных радикалов - алкил, циклоалкил или арил, и в котором указанный заместитель или заместители выбраны из галогена, гидрокси, алкила, алкокси, циклоалкила, циклоалкокси, арила, арилокси, карбокси, алкоксикарбонила, циклоалкоксикарбонила и арилоксикарбонила,
для (со)олигомеризации лактида и гликолида с раскрытием цикла.
Термин галоген означает фтор, хлор, бром или иод и предпочтительно хлор. Термин алкил означает алкильный радикал, содержащий от 1 до 20 атомов углерода. Этот термин включает в себя алкильные радикалы, содержащие от 1 до 6 атомов углерода с линейной или разветвленной структурой, и особенно алкильные радикалы, содержащие от 1 до 4 атомов углерода, например метильный, этильный, пропильный, изопропильный, бутильный, изобутильный, втор-бутильный и трет-бутильный радикалы. Этот термин также включает в себя радикалы, содержащие более 6 атомов углерода, например гептильный, октильный, нонильный, децильный, ундецильный, додецильный, тридецильный, тетрадецильный, пентадецильный, гексадецильный, гептадецильный, октадецильный, нонадецильный и эйкозильный радикалы.
Термин алкоксил означает радикалы, в которых алкильный радикал представляет собой радикал, содержащий от 1 до 6 атомов углерода, как было указано выше, например метоксильный, этоксильный, пропилоксильный или изопропилоксильный радикалы, а также линейные вторичные или третичные бутоксильный и пентилоксильный радикалы. Термин алкоксикарбонил означает радикалы, в которых алкоксильный радикал, который, как было указано выше, представляет собой радикал, например метоксикарбонил, этоксикарбонил.
Циклоалкильные радикалы выбраны из группы насыщенных и ненасыщенных моноциклических циклоалкилов. Насыщенные моноциклические циклоалкильные радикалы могут быть выбраны из радикалов, содержащих от 3 до 7 атомов углерода, например циклопропильный, циклобутильный, циклопентильный, циклогексильный или циклогептильный радикалы. Ненасыщенные циклоалкильные радикалы могут быть выбраны из циклобутенового, циклопентенового, циклогексенового, циклопентадиенового, циклогексадиенового радикалов. Термин циклоалкоксил означает радикалы, в которых циклоалкильный радикал, как было указано выше, представляет собой радикал, например циклопропилоксильный, циклобутилоксильный, циклопентилоксильный, циклогексилоксильный, циклогептилоксильный, циклобутенилоксильный, циклопентенилоксильный, циклогексенилоксильный, циклопентадиенилоксильный, циклогексадиенилоксильный радикалы. Термин циклоалкоксикарбонил означает радикалы, в которых циклоалкоксильный радикал, как было указано выше, представляет собой радикал, например циклопропилоксикарбонильный, циклобутилоксикарбонильный, циклопентилоксикарбонильный, циклогексилоксикарбонильный, циклогептилоксикарбонильный, циклобутенилоксикарбонильный, циклопентенилоксикарбонильный, циклогексенилоксикарбонильный радикалы.
Арильные радикалы могут принадлежать к моно- или полициклическому типу. Моноциклические арильные радикалы могут быть выбраны из фенильных радикалов, необязательно замещенных одним или более алкильными радикалами, например толильным, ксилильным, мезитильным, куменильным. Полициклические арильные радикалы могут быть выбраны из нафтильного, антрильного, фенантрильного радикалов. Термин арилокси означает радикалы, в которых арильный радикал, как было указано выше, представляет собой радикал, например фенилоксильный, толилоксильный, нафтилоксильный, антрилоксильный и фенантрилоксильный радикалы. Термин арилоксикарбонил предпочтительно означает радикалы, в которых арилоксильный радикал, как было указано выше, представляет собой, например, фенилоксикарбонильный, толилоксикарбонильный радикал.
В настоящей заявке термин (со)олигомеризация означает олигомеризацию или (со)олигомеризацию со степенями полимеризации (DP) менее 30. Таким образом, (со)олигомеризация лактида и гликолида включает в себя не только олигомеризацию лактида, олигомеризацию гликолида, но и соолигомеризацию лактида и гликолида.
Предпочтительно в каталитической системе в соответствии с настоящим изобретением количество мономера по отношению к (со)олигомеризационной добавке находится в диапазоне между 2 и 30 молярных эквивалентов и предпочтительно между 4 и 10 молярных эквивалентов.
Более конкретно, целью настоящего изобретения является применение каталитической системы, как было указано выше, содержащей полимерный катализатор (1), представляющий собой макропористую смолу на основе стирола и дивинилбензола, содержащую кислые сульфогруппы в качестве заместителей.
Предпочтительно в каталитической системе, описанной выше, полимерный катализатор (1) представляет собой полимерную смолу типа Amberlyst® или Dowex® и наиболее предпочтительно смолу типа Amberlyst®.
В соответствии с настоящим изобретением используемая (со)олигомеризационная добавка формулы (2) играет роль инициатора (или промотора) (со)олигомеризации. Его присутствие необходимо, поскольку в отсутствие указанного соединения формулы (2) реакции (со)олигомеризации протекают гораздо медленнее, что приводит к более низким выходам, низкой воспроизводимости, и поэтому не могут быть использованы в промышленном масштабе.
Более конкретно, целью настоящего изобретения является применение каталитической системы, описанной выше, содержащей соединение общей формулы (2), в которой
Е представляет собой атом кислорода или серы;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу в формуле -E14(R14)(R'14)(R''14);
E14 является атомом углерода или кремния;
R14, R'14, R''14 представляют собой, независимо, атом водорода или один из следующих замещенных или незамещенных радикалов - алкил, циклоалкил или арил, и в которых указанный заместитель или заместители выбраны из галогена, алкила, циклоалкила, фенила, нафтила, карбоксила и алкоксикарбонила,
и более конкретно
Е представляет собой атом кислорода;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу в формуле -E14(R14)(R'14)(R''14);
E14 является атомом углерода;
R14, R'14, R''14 представляют собой, независимо, атом водорода или замещенные или незамещенные алкильные радикалы, в которых указанный заместитель или заместители выбраны из алкила, карбоксила и алкоксикарбонила;
и наиболее предпочтительно
Е представляет собой атом кислорода;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу формулы -E14(R14)(R'14)(R''14), в которой E14 является атомом углерода и R14, R'14, R'14 представляют собой, независимо, атом водорода или алкильный радикал.
Более конкретно, целью данного изобретения является применение каталитической системы, указанной выше и отличающейся тем, что (со)олигомеризационная добавка формулы (2) представляет собой воду или спирт. В соответствии с настоящим изобретением указанный спирт имеет формулу R2-OH, в которой радикал R2 представляет собой группу, определенную выше. Среди спиртов следует отметить, например, метанол, этанол, пропанол, н-пропанол, изопропанол, н-бутанол, пентан-1-ол, длинные линейные спирты, например додеканол или замещенные спирты, например этиллактат. Предпочтительно спирт, используемый в каталитической системе, указанной выше, является алифатическим спиртом, и наиболее предпочтительно алифатический спирт выбирают из изопропанола, пентан-1-ола и додекан-1-ола.
Целью данного изобретения является также способ (со)олигомеризации лактида и гликолида с раскрытием цикла, который состоит в соединении рассматриваемых мономера или мономеров, каталитической системы, состоящей, как указано выше, из полимерного катализатора (1) на основе сильнокислотной ионообменной смолы и (со)олигомеризационной добавки общей формулы (2) в растворителе для проведения олигомеризации.
Растворитель для проведения реакции выбирают из растворителей, которые не мешают протеканию самой каталитической реакции. В качестве примера таких растворителей могут быть упомянуты ароматические углеводороды (например, толуол, ксилол или мезитилен), необязательно замещенные одной или более нитрогруппами (например, нитробензол), простые эфиры (например, метил-трет-бутиловый эфир, тетрагидрофуран или диоксан), алифатические или ароматические галогениды (например, дихлорметан, хлороформ, дихлорэтан или дихлорбензол).
В соответствии со способом настоящей заявки реакцию проводят при температурах, находящихся в диапазоне между -20°C и приблизительно 150°C, предпочтительно между 20°C и 80°C. Времена реакции находятся в диапазоне между одним часом и 64 часами и предпочтительно между 14 и 48 часами. Количество мономера по отношению к (со)олигомеризационной добавке находится в диапазоне между 2 и 30 молярными эквивалентами и наиболее предпочтительно между 4 и 10 молярными эквивалентами. Выход согласно (со)олигомеризационному способу в соответствии с настоящим изобретением обычно превышает 80% и может даже достигать 100% в относительно мягких условиях (40°C, несколько часов), как это показано в примерах.
Более конкретно, другой целью данного изобретения является способ (со)олигомеризации лактида и гликолида, как указано выше, с помощью каталитической системы, состоящей, как указано выше, и в которой полимерный катализатор (1) представляет собой макропористую смолу на основе стирола и дивинилбензола, содержащую кислые сульфогруппы. Предпочтительно полимерный катализатор (1) представляет собой макропористую смолу типа Amberlyst® или Dowex® и очень предпочтительно смолу типа Amberlyst®.
Более конкретно, другой целью данного изобретения является способ (со)олигомеризации, как указано выше, с помощью каталитической системы, указанной выше, и соединения общей формулы (2), в которой
Е представляет собой атом кислорода или серы;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу в формуле -E14(R14)(R'14)(R''14);
E14 является атомом углерода или кремния;
R14, R'14, R''14 представляют собой, независимо, атом водорода или один из следующих замещенных или незамещенных радикалов: алкил, циклоалкил или арил, в которых указанный заместитель или заместители выбраны из галогена, алкила, циклоалкила, фенила, нафтила, карбоксила и алкоксикарбонила,
и более конкретно
Е представляет собой атом кислорода;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу в формуле -E14(R14)(R'14)(R''14);
E14 является атомом углерода;
R14, R'14, R''14 представляют собой, независимо, атом водорода или замещенные или незамещенные алкильные радикалы из числа алкила, циклоалкила или арила, и в которых указанный заместитель или заместители выбраны из алкила, карбоксила и алкоксикарбонила;
и наиболее предпочтительно
Е представляет собой атом кислорода;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу в формуле -E14(R14)(R'14)(R''14), в которой E14 является атомом углерода и R14, R'14, R''14 представляют собой, независимо, атом водорода или алкильный радикал.
Более конкретно, целью данного изобретения является способ (со)олигомеризации лактида и гликолида, как указано выше, с помощью каталитической системы, в которой в качестве (со)олигомеризационной добавки используют воду или спирт. Предпочтительно спирт является алифатическим спиртом, и очень предпочтительно алифатический спирт выбирают из изопропанола, пентан-1-ола и додекан-1-ола.
Поэтому в соответствии с настоящим изобретением способ (со)олигомеризации лактида и гликолида с раскрытием цикла позволяет регулировать природу концевых групп (со)олигомеров и особенно подходит для получения (со)олигомеров с кислотной - спиртовыми и сложноэфирными - спиртовыми концевыми группами, как показано в экспериментальной части. После завершения реакции смола может быть отделена от олигомера обычным фильтрованием реакционной смеси, и таким образом регенерированная смола может быть повторно использована без потери активности.
Способ (со)олигомеризации лактида и гликолида в соответствии с настоящим изобретением особенно подходит для получения (со)олигомеров с молекулярной массой, находящейся в диапазоне между 300 и 5000 дальтон, более конкретно между 500 и 3000 дальтон.
Способ (со)олигомеризации лактида и гликолида в соответствии с настоящим изобретением имеет много преимуществ, в частности,
- каталитическая система состоит из сильнокислотной ионообменной смолы и (со)олигомеризационной добавки, которые легко доступны и недороги;
- использование в качестве добавки инициатора (со)олигомеризации позволяет не только очень существенно улучшить способ (со)олигомеризации, но также точно регулировать длину цепи, которая практически равна отношению мономера к инициатору;
- использование в качестве добавки инициатора (со)олигомеризации позволяет регулировать природу концевых групп полученных (со)олигомеров;
- (со)олигомеризация может быть проведена в относительно мягких температурных условиях, например при 40°C, причем времена проведения реакции, необходимые для полного превращения мономера или мономеров, превышают несколько часов или не более 48 часов;
- молекулярно-массовое распределение полученных (со)олигомеров очень невелико; степени полидисперсности (со)олигомеров, полученных в соответствии с настоящим изобретением, в действительности находятся в диапазоне между 1,0 и 1,4;
- полученные (со)олигомеры могут быть легко, быстро и эффективно очищены без изменения их свойств, смола может быть количественно отделена обычным фильтрованием.
- таким образом регенерированная смола сохраняет свои свойства и может быть повторно использована без заметной потери активности.
Наконец, данное изобретение относится к олигомерам лактида и гликолида, которые получены или могут быть получены с применением описанного выше способа. Такие (со)олигомеры характеризуются молекулярной массой, находящейся в диапазоне между 300 и 5000 дальтон и более конкретно между 500 и 3000 дальтон. Такие (со)олигомеры могут также иметь регулируемые кислотно-спиртовые или сложноэфирные-спиртовые концевые группы.
Продукты общей формулы (1) и (2) коммерчески доступны или могут быть получены способами, известными специалистам в данной области.
За исключением других определений, все технические и научные термины, используемые в настоящей заявке, имеют такое же значение, которое обычно используют специалисты в той области, к которой относится данное изобретение. Аналогично, все публикации, патентные заявки и все другие ссылки, упоминаемые в настоящей заявке, включены в виде ссылок.
Для иллюстрации вышеописанных процессов приведены следующие примеры, которые ни в коем случае не сужают масштаб изобретения.
Пример 1
Получение олигомера (D,L-лактида) со сложноэфирными-спиртовыми концевыми группами (M w ~1000 Дa)
3,00 г D,L-лактида (0,021 моль), 20 мл дихлорметана, 3,00 г смолы типа Amberlyst® 15 (0,0135 моль кислотных групп) и 0,41 мл пентан-1-ола (0,0037 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании при 40°C в течение 45 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (1 мл) и выливали при перемешивании в пентан (15 мл). Отделяли супернатант и после высушивания в вакууме получали 2,8 г олигомеров (83%) в виде бесцветной вязкой жидкости. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 400000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=1036 дальтон, Mw/Mn=1,22). Природу сложноэфирных-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
Пример 2
Получение олигомера (D,L-лактида) с кислотно-спиртовыми концевыми группами (M w ~1000 Дa)
23,80 г D,L-лактида (0,165 моль), 20 мл дихлорметана, 23,73 г смолы типа Amberlyst® 15 (0,111 моль кислотных групп) и 0,74 мл воды (0,041 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании при 40°C в течение 48 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (6 мл) и выливали при перемешивании в пентан (120 мл). Отделяли супернатант и после высушивания в вакууме получали 20,1 г олигомеров (82%) в виде бесцветной вязкой жидкости. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 400000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=917 дальтон, Mw/Mn=1,16). Природу кислотно-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
Пример 3
Получение олигомера (D,L-лактида) со сложноэфирными-спиртовыми концевыми группами (M w <1000 Дa)
3,00 г D,L-лактида (0,021 моль), 20 мл дихлорметана, 3,12 г смолы типа Amberlyst® 15 (0,014 моль кислотных групп) и 0,59 мл пентан-1-ола (0,0054 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании при 40°C в течение 40 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (1 мл) и выливали при перемешивании в пентан (15 мл). Отделяли супернатант и после высушивания в вакууме получали 3,2 г олигомеров (89%) в виде бесцветной вязкой жидкости. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 400000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=597 дальтон, Mw/Mn=1,3). Природу сложноэфирных-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
Пример 4
Получение олигомера (D,L-лактида/гликолида) со сложноэфирными-спиртовыми концевыми группами (M w <1000 Дa)
1,40 г D,L-лактида (0,0097 моль), 0,30 г гликолида (0,026 моль), 15 мл дихлорметана, 1,20 г смолы Amberlyst® 15 (0,006 моль кислотных групп) и 0,23 мл пентан-1-ола (0,002 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании при 40°C в течение 40 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Соотношение интегралов, соответствующих сигналам, относящимся к фрагментам полилактида (5,2 ч./млн) и полигликолида (4,85 ч./млн), позволяет оценить состав сополимера при содержании лактида, равном 79%, и гликолида, равном 21%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (1 мл) и выливали при перемешивании в пентан (15 мл). Отделяли супернатант и после высушивания в вакууме получали 1,45 г олигомеров (86%) в виде бесцветной вязкой жидкости. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 400000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=568 дальтон, Mw/Mn=1,28). Природу сложноэфирных-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
Пример 5
Получение олигомера (D,L-лактида/гликолида) со сложноэфирными-н-пентил-спиртовыми концевыми группами (M w >1000 Дa)
5,00 г D,L-лактида (0,035 моль), 5,00 г гликолида (0,043 моль), 60 мл дихлорметана, 10,00 г смолы Amberlyst® 15 (0,050 моль кислотных групп) и 1,83 мл пентан-1-ола (0,0168 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании и кипячении с обратным холодильником (45°C) в течение 40 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Соотношение интегралов, соответствующих сигналам, относящимся к фрагментам полилактида (5,20 ч./млн) и полигликолида (4,85 ч./млн), позволяет оценить состав сополимера при содержании лактида, равном 49%, и гликолида, равном 51%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (3 мл) и выливали при перемешивании в пентан (44 мл). Отделяли супернатант и после высушивания в вакууме получали 7,50 г олигомеров (65%) в виде бесцветно-беловатой вязкой жидкости. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 400000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=1550 дальтон, Mw/Mn=1,19). Природу сложноэфирных-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
Пример 6
Получение (50/50) со-олигомера (D,L-лактида/гликолида) со сложноэфирными-н-додецил-спиртовыми концевыми группами (M w >1000 Дa)
5,00 г D,L-лактида (0,035 моль), 5,00 г гликолида (0,043 моль), 60 мл дихлорметана, 10,00 г смолы Amberlyst® 15 (0,050 моль кислотных групп) и 3,82 мл пентан-1-ола (0,0168 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании и кипячении с обратным холодильником (45°C) в течение 40 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Соотношение интегралов, соответствующих сигналам, относящимся к фрагментам полилактида (5,20 ч./млн) и полигликолида (4,85 ч./млн), позволяет оценить состав сополимера при содержании лактида, равном 53%, а гликолида, равном 47%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (3 мл) и выливали при перемешивании в пентан (44 мл). Отделяли супернатант и после высушивания в вакууме получали 9,50 г олигомеров (72%) в виде бесцветно-беловатой вязкой жидкости. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 400000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=1470 дальтон, Mw/Mn=1,17). Природу сложноэфирных-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
Пример 7
Получение олигомера (D,L-лактида) со сложноэфирными-н-додецил-спиртовыми концевыми группами (M w >1000 Дa)
5,00 г D,L-лактида (0,035 моль), 30 мл дихлорметана, 5,00 г смолы Amberlyst® 15 (0,025 моль кислотных групп) и 1,42 мл додекан-1-ола (0,0063 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании и кипячении (45°C) в течение 40 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (1,5 мл) и выливали при перемешивании в пентан (22 мл). Отделяли супернатант и после высушивания в вакууме получали 4,70 г олигомеров (76%) в виде бесцветной вязкой жидкости. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 400000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=1209 дальтон,
Mw/Mn=1,3). Природу сложноэфирных-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
Пример 8
Получение олигомера (D,L-лактида) со сложноэфирными-н-пентил-спиртовыми концевыми группами (M w >2000 Дa)
10,00 г D,L-лактида (0,070 моль), 69 мл дихлорметана, 6,50 г смолы Amberlyst® 15 (0,0326 моль кислотных групп) и 0,50 мл додекан-1-ола (0,0046 моль) последовательно вносили в колбу Шленка, снабженную магнитной мешалкой и продуваемую аргоном. Реакционную смесь оставляли при перемешивании и кипячении (45°C) в течение 168 часов. Олигомеры были охарактеризованы спектрами протонного ЯМР; степень превращения мономера составляет величину, превышающую 95%. Реакционную смесь фильтровали для отделения смолы и упаривали растворитель при пониженном давлении. Осадок переносили в дихлорэтан (3 мл) и выливали при перемешивании в пентан (44 мл). Отделяли супернатант и после высушивания в вакууме получали 8,20 г олигомеров (79%) в виде белого порошка. Согласно данным ГПХ (GPC, гель-проникающая хроматография), в которой для калибровки используют полистирольные стандарты (ПС) с массами в диапазоне от 400 до 5000, образец состоит из олигомеров, имеющих близкие по величине массы (Mw=2096 дальтон,
Mw/Mn=1,27). Природу сложноэфирных-спиртовых концевых групп определяли методом масс-спектрометрии (ионизацией электроспреем, определением в режиме положительных ионов, образец растворяли в ацетонитриле, содержащем следы гидроокиси аммония).
| название | год | авторы | номер документа |
|---|---|---|---|
| ИСПОЛЬЗОВАНИЕ ЦИНКОВЫХ ПРОИЗВОДНЫХ В КАЧЕСТВЕ КАТАЛИЗАТОРОВ ПОЛИМЕРИЗАЦИИ ЦИКЛИЧЕСКИХ СЛОЖНЫХ ЭФИРОВ | 2002 |
|
RU2294336C2 |
| КАТАЛИТИЧЕСКАЯ СИСТЕМА (CO) ПОЛИМЕРИЗАЦИИ ЛАКТИДА И ГЛИКОЛИДА | 2004 |
|
RU2318836C2 |
| ПРИМЕНЕНИЕ СТАННИЛЕНОВ И ГЕРМИЛЕНОВ В КАЧЕСТВЕ КАТАЛИЗАТОРОВ ПОЛИМЕРИЗАЦИИ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ | 2001 |
|
RU2282640C2 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ МЕТАЛЛОВ С ТРИДЕНТАТНЫМ ЛИГАНДОМ КАК КАТАЛИЗАТОРЫ ПОЛИМЕРИЗАЦИИ | 1998 |
|
RU2197494C2 |
| СОЕДИНЕНИЯ, ИМЕЮЩИЕ ЭЛЕМЕНТ ГРУППЫ III ПЕРИОДИЧЕСКОЙ СИСТЕМЫ ЭЛЕМЕНТОВ Д.И.МЕНДЕЛЕЕВА, СВЯЗАННЫЙ С МОНО- ИЛИ ДИАНИОННЫМ ТРИДЕНТАТНЫМ ЛИГАНДОМ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ КАТАЛИЗАТОРОВ ПОЛИМЕРИЗАЦИИ | 1997 |
|
RU2180664C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРОВ С РАЗЛИЧНОЙ СТРУКТУРОЙ ПУТЕМ ИНИЦИАЦИИ АМИНАМИ | 2011 |
|
RU2592848C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗВЕЗДООБРАЗНЫХ ПОЛИМЕРОВ | 2011 |
|
RU2589876C2 |
| ЛИГАНДЫ И ВКЛЮЧАЮЩИЕ ИХ КАТАЛИТИЧЕСКИЕ СИСТЕМЫ ДЛЯ ОЛИГОМЕРИЗАЦИИ ЭТИЛЕНА С ПОЛУЧЕНИЕМ ЛИНЕЙНЫХ АЛЬФА-ОЛЕФИНОВ | 2002 |
|
RU2292343C2 |
| СПОСОБ СИНТЕЗА 2,5-ДИОКСАН-1,4-ДИОНОВ | 2005 |
|
RU2382774C2 |
| КАТАЛИТИЧЕСКИЕ СИСТЕМЫ ДЛЯ ОЛИГОМЕРИЗАЦИИ ЭТИЛЕНА В ЛИНЕЙНЫЕ АЛЬФА-ОЛЕФИНЫ | 2003 |
|
RU2315658C2 |
Изобретение относится к (со)олигомерам лактида и гликолида, находящим применение в качестве биосовместимых полимеров в хирургии и фармакологии. Описывается применение каталитической системы для (со)олигомеризации лактида и гликолида с раскрытием цикла. Каталитическая система образована полимерным катализатором на основе сильнокислотной ионообменной смолы (1) и (со)олигомеризационной добавки формулы (2) R1-E-R2, в которой Е - элемент 16-й группы, R1 - атом водорода или дейтерия, R2 - атом водорода или дейтерия или группа в формуле -E14(R14)(R'14)(R''14), где Е14 - элемент 14-й группы, R14, R'14, R''14 - атом водорода, атом дейтерия, замещенный или незамещенный алкил, циклоалкил или арил. Предложенная каталитическая система позволяет контролировать длину цепи и природу концевых групп (со)олигомеров, отделять (со)олигомеры от катализатора простым и эффективным способом и исключить потери активности катализатора. 2 н. и 12 з.п. ф-лы.
1. Применение каталитической системы, образованной
(a) полимерным катализатором (1) на основе сильнокислотной ионообменной смолы и
(b) (со)олигомеризационной добавкой общей формулы (2)
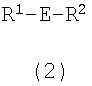
в которой Е представляет собой элемент 16-й группы;
R1 представляет собой атом водорода или дейтерия;
R2 представляет собой атом водорода или дейтерия или группу в формуле E14(R14)(R'14)(R''14);
E14 является элементом 14-й группы;
R14, R'14, R''14 представляют собой независимо атом водорода; атом дейтерия; один из следующих замещенных или незамещенных радикалов - алкил, циклоалкил или арил, и в котором указанный заместитель или заместители выбраны из галогена, гидроксила, алкила, алкоксила, циклоалкила, циклоалкоксила, арила, арилокси, карбоксила, алкоксикарбонила, циклоалкоксикарбонила и арилоксикарбонила,
для (со)олигомеризации лактида и гликолида с раскрытием цикла, причем количество мономера по отношению к (со)олигомеризационной добавке находится в диапазоне между 2 и 30 молярных эквивалентов и предпочтительно между 4 и 10 молярных эквивалентов.
2. Применение по п.1, отличающееся тем, что полимерный катализатор (1) представляет собой макропористую смолу на основе стирола и дивинилбензола, содержащую кислые сульфогруппы в качестве заместителей.
3. Применение по п.2, отличающееся тем, что полимерный катализатор (1) представляет собой смолу типа Amberlyst® или Dowex®.
4. Применение по п.3, отличающееся тем, что полимерный катализатор (1) представляет собой смолу типа Amberlyst®.
5. Применение по п.1, отличающееся тем, что соединение общей формулы (2) представляет собой соединение, в котором Е представляет собой атом кислорода или серы;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу в формуле E14(R14)(R'14)(R''14);
E14 является атомом углерода или кремния;
R14, R'14, R''14 представляют собой независимо атом водорода или один из следующих замещенных или незамещенных радикалов - алкил, циклоалкил или арил, в которых указанный заместитель или заместители выбраны из галогена, алкила, циклоалкила, фенила, нафтила, карбоксила и алкоксикарбонила.
6. Применение по п.5, отличающееся тем, что соединение общей формулы (2) представляет собой соединение, в котором Е является атомом кислорода;
R1 является атомом водорода;
R2 представляет собой атом водорода или группу в формуле E14(R14)(R'14)(R''14),
E14 является атомом углерода;
R14, R'14, R''14 представляют собой независимо атом водорода или замещенные или незамещенные алкильные радикалы, в которых указанный заместитель или заместители выбраны из алкила, карбоксила и алкоксикарбонила.
7. Применение по п.6, отличающееся тем, что соединение общей формулы (2) представляет собой соединение, в котором Е представляет собой атом кислорода;
R1 представляет собой атом водорода;
R2 представляет собой атом водорода или группу формулы E14(R14)(R'14)(R''14), в которой E14 является атомом углерода, a R14, R'14, R''14 представляют собой независимо атом водорода или алкильный радикал.
8. Применение по п.1, отличающееся тем, что соединение общей формулы (2) представляет собой либо воду, либо спирт.
9. Применение по п.8, отличающееся тем, что спирт является алифатическим спиртом.
10. Применение по п.9, отличающееся тем, что алифатический спирт выбран из изопропанола, пентан-1-ола и додекан-1-ола.
11. Способ (со)олигомеризации лактида и гликолида с раскрытием цикла, данный способ состоит в соединении рассматриваемых мономера или мономеров каталитической системы, как указано выше в одном из пп.1-10, и растворителя для проведения олигомеризации.
12. Способ по п.11, отличающийся тем, что температура находится в диапазоне между -20 и приблизительно 150°С.
13. Способ по п.12, отличающийся тем, что реакцию проводят в растворе при температуре, находящейся в диапазоне между 20 и 80°С.
14. Способ по одному из пп.11-13, отличающийся тем, что время реакции находится в диапазоне между одним часом и 64 ч и предпочтительно между 14 и 48 ч.
| US 6355772 B1, 12.03.2002 | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| Способ лечения врожденного вывиха бедра | 1977 |
|
SU624613A1 |
| Способ получения сложных полиэфиров | 1989 |
|
SU1685952A1 |
Авторы
Даты
2010-01-27—Публикация
2005-03-15—Подача