Данная заявка имеет дату приоритета на основании предварительной заявки США № 60/443,744, поданной 29 января 2003, Раздел 35,119(е) Кодекса законов США.
Известный уровень техники
Фторэластомеры и, в частности, перфторэластомеры известны как материалы, обладающие высокой химической стойкостью и плазмоустойчивостью, приемлемой остаточной деформацией при сжатии и удовлетворительными механическими свойствами. Поэтому фторэластомеры используются для изготовления уплотнителей, прокладок и изоляционных покрытий. В условиях высоких температур, агрессивных или неблагоприятных внешних условий, таких как коррозионные жидкости, растворители, смазочные материалы, или окислительно-восстановительные условия, предпочтительнее использовать перфторэластомеры. Фторэластомеры получают различными способами из фторированных мономеров. Перфторэластомеры, как правило, получают из перфторированных мономеров, содержащих какой-либо перфторированный функциональный сшивающий мономер, полимеризуя и вулканизируя (сшивая) композицию при помощи вулканизирующего агента, который реагирует с введенным функциональным сшивающим мономером с образованием материала, обладающего эластомерными свойствами. Подходящие функциональные сшивающие мономеры включают, наряду со многими другими, мономеры, имеющие нитрильные функциональные группы. Известны примеры использования первичных и вторичных нитрилсодержащих функциональных мономеров в технологических процессах. Предполагается, что такие соединения тримеризуют нитрильные функциональные мономеры образуя триазины.
Известными вулканизирующими агентами являются металлоорганические соединения и их гидроксиды, главным образом, оловоорганические соединения, такие как аллил-, пропаргил-, трифенил- и алленилолово и гидроксиды. Широко используются тетраалкил- и тетраарил-замещенные соединения олова, например тетрафенилолово. Тем не менее, такие вулканизирующие агенты обеспечивают сравнительно низкую скорость вулканизации, они токсичны и могут загрязнять образующиеся эластомеры металлсодержащими примесями.
Также использовались вулканизирующие агенты, содержащие аминогруппы. Бисаминофенолы, бисаминотиофенолы и бисамидразоны являются дополнительными вулканизаторами. Известны вулканизирующие соединения, содержащие два фенильных кольца, и имеющие на каждом фенильном кольце амино- и гидроксильную группы, диамино, амино- и тиогруппы, соединены структурой, включающей -SO2-, -О-, -СО-, алкильные группы, состоящие из 1-6 углеродных атомов, а также двойные углерод-углеродные связи. Хотя синтез перфторалкильных групп, содержащих от 1 до 10 углеродных атомов расплывчато описан в литературе, практически приемлемого способа синтеза и использование таких соединений в качестве вулканизирующих агентов до сих пор продемонстрировано не было. Материалы на основе дифенильных соединений, которые используются и применяются в синтезе, являются, прежде всего, соединениями, содержащими три углеродные алкильные группы, в которых фенильные группы присоединены к центральному (второму) атому углерода в бис положении. Например, наиболее известное вулканизирующее вещество такого типа - 2,2-бис[3-амино-4-гидроксифенил]гексафторпропан, также известный под названием диаминобисфенол AF 20 или ВОАР.
ВОАР представляет собой твердое кристаллическое вещество с температурой плавления около 245-248°С. ВОАР не слишком хорошо совмещается с перфторированными эластомерами, его трудно быстро и однородно диспергировать в перфторированных эластомерах, и поэтому он является сравнительно медленнодействующим вулканизирующим агентом.
Еверс [R. С. Evers, J. Polym. Sci. 16, 2833-2848 (1978)] описывает использование фторуглеродных эфиров бисаминофенола в качестве мономеров для получения полимеров фторуглеродных эфиров бибензоксазола. Эверс привел пример синтеза фторуглеродных эфиров бисаминофенола с использованием α, ω-дииодофторуглеродных эфиров в качестве промежуточных соединений. Хастед, Рейли и Браун в патенте US № 2676985 и статье JACS 78:6032 (1956), Григас и Тауринс в Can. J. Chem., vol. 39,414-419 (1961) и Can. J. Chem., vol. 39, 761-764 (1961) описывают ранее известные способы получения амидинов.
Что касается способов повышения скорости сшивания медленно вулканизирующих агентов, таких как ВОАР, то с этой целью используются традиционные ускорители, включающие органические или неорганические соли аммония, например перфтороктаноат, перфторацетат аммония, тиоцианат и сульфамат аммония; мочевина; трет-бутилкарбамат; ацетальдегид аммония; тетраалкилфосфониевые соли, тетраалкиламмонийные соли и триалкилсульфониевые соли, такие как бензилтрифенилфосфоний хлорид, бензилтрифенилфосфоний бромид, бензилтрифенилфосфоний фенолят бисфенола AF, тетрабутиламмоний сернокислый и тетрабутиламмонийбромид. Тем не менее, такие соединения вызывают побочные реакции, которые могут приводить к нежелательным побочным продуктам.
Таким образом, существует потребность в разработке улучшенного вулканизирующего агента, способного легче диспергироваться и с более высокой скоростью вулканизировать перфторэластомеры, в особенности, перфторированные эластомеры, сшиваемые с помощью нитрил содержащих функциональных групп. Также необходимо разработать ускорители вулканизации перфторированных эластомеров, которые способны повысить скорость вулканизации и поддерживать полезные свойства перфторированных эластомеров.
КРАТКОЕ СОДЕРЖАНИЕ ИЗОБРЕТЕНИЯ
Изобретение включает в себя вулканизирующие агенты, со-вулканизирующие агенты и ускорители вулканизации перфторэластомерных композиций на основе моноамидина и моноамидоксима. Изобретение включает вулканизирующие агенты общей формулы (I):
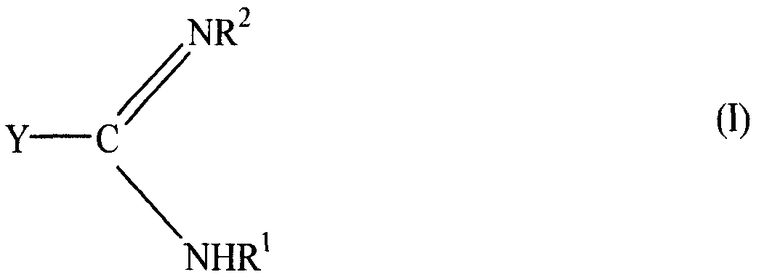
где Y выбран из группы, состоящей из замещенной алкильной, алкоксильной, арильной, аралкильной или аралкокси групп, включающих примерно от 1 до 22 углеродных атомов; замещеной или незамещенной галогенированной алкильной, алкокси, арильной, аралкильной или аралкокси групп, включающих примерно от 1 до 22 углеродных атомов, а также перфторалкильной, перфторалкокси, перфторарильной, перфтораралкильной или перфтораралкокси групп, включающих примерно от 1 до 22 углеродных атомов; R1 означает атом водорода; замещенную или незамещенную низшую алкильную или алкоксигруппу, включающую примерно от 1 до 6 углеродных атомов; и аминогруппу; и R2 означает R1 или гидроксильную группу.
Изобретение также включает вулканизирующие агенты, со-вулканизирующие агенты и ускорители вулканизации перфторэластомерных композиций на основе бисамидиновых производных, представленных формулой (II):
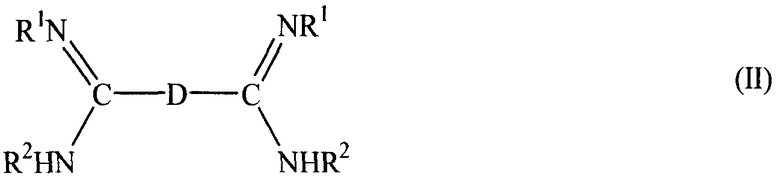
где D выбран из группы, состоящей из незамещенной или замещенной галогенированнои алкильной, алкокси, арильной, аралкильной или аралкоксигрупп, содержащих примерно от 1 до 22 углеродных атомов; и перфторалкильной, перфторалкокси, перфторарильной, перфтораралкильной или перфтораралкокси групп, включающих примерно от 1 до 22 углеродных атомов; R1 и R2, независимо друг от друга, означают атом водорода, низшую алкильную или алкоксигруппу, содержащую примерно от 1 до 6 углеродных атомов и аминогруппу.
Изобретение описывает вулканизируемую перфторэластомерную композицию, содержащую (а) перфторированный полимер, содержащий, по меньшей один, мономер, содержащий нитрил функциональную группу; и (b) по меньшей мере один вулканизирующий агент на основе моноамидина или моноамидоксима.
Изобретение также описывает вулканизируемую композицию перфторированных эластомеров, которая содержит (а) перфторированный полимер, имеющий, по меньшей мере, один функциональный сшивающий мономер, содержащий нитрильную группу; (b) функционализированный вулканизирующий агент на основе дифенила; и (c) ускоритель вулканизации, выбранный из группы, состоящей из, по меньшей мере, одного ускорителя вулканизации на основе моноамидина, по меньшей мере, одного ускорителя вулканизации на основе моноамидоксима, по меньшей мере, одного ускорителя вулканизации на основе бисамидина и их комбинаций. Также в изобретение включены предпочтительные вулканизируемые перфторэластомерные композиции, в которых функционализированные вулканизирующие агенты на основе дифенильных соединений имеют формулу (III):
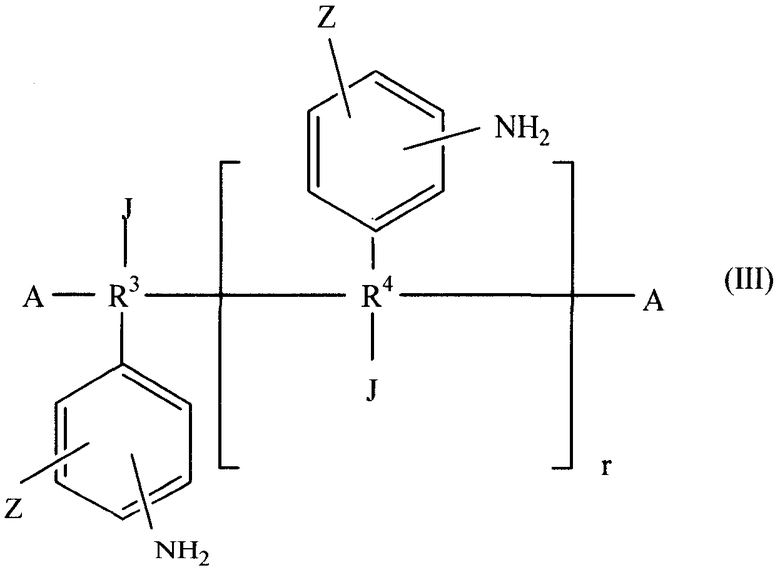
где r равно 0 или 1;
R3 и R4 каждый независимо выбраны из группы, содержащей атом углерода, незамещенные и замещенные группы, с разветвленной и линейной цепью на основе углерода, содержащие примерно от 2 до 22 атомов углерода, выбранные из группы, содержащей алкильные группы, галогеналкильные и перфторалкильные группы, углеродная цепь каждой из которых может прерываться, по меньшей мере, одним атомом кислорода;
каждый Z независимо выбирается из группы, состоящей из амино-, меркапто-, сульфгидрильной или гидроксильной группы;
каждый J независимо выбирается из группы, представленной формулой (IV):
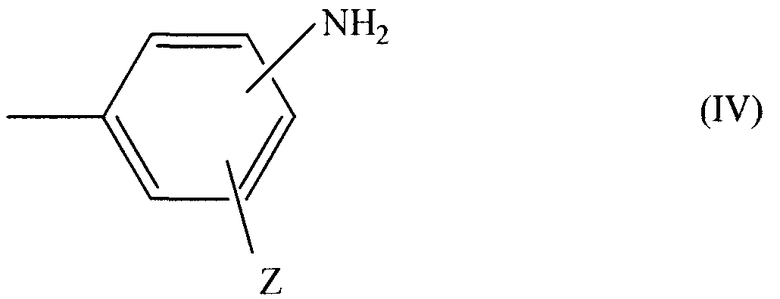
или А; и
каждый А независимо выбирается из группы, состоящей из формулы (IV); атома фтора; незамещенной и замещенной группы, с разветвленной и линейной цепью нa основе углерода, которые выбираются из группы, состоящей из алкильных, галогеналкильных и перфторалкильных групп, содержащих 1-22 атомов углерода; углеродная цепь каждой из групп может прерываться по меньшей мере одним атомом кислорода; в том случае, если r=0 и R3 - атом углерода, по меньшей мере, один из J и каждый А не должны представлять собой формулу (IV).
Кроме того, изобретение включает вулканизирующий агент для перфторэластомерной композиции, в которой вулканизирующий агент описывается формулой (III), показанной выше.
Изобретение включает вулканизирующий агент для перфторэластомерной композиции, содержащий вулканизирующий агент на основе функционализированного дифенила, который обладает достаточно высокой молекулярной массой, такой, чтобы его температура плавления не превышала примерно 240°С, а в некоторых предпочтительных вариантах была не выше примерно 230°С.
В изобретение также включен способ использования соединения формулы (I), приведенной ниже:
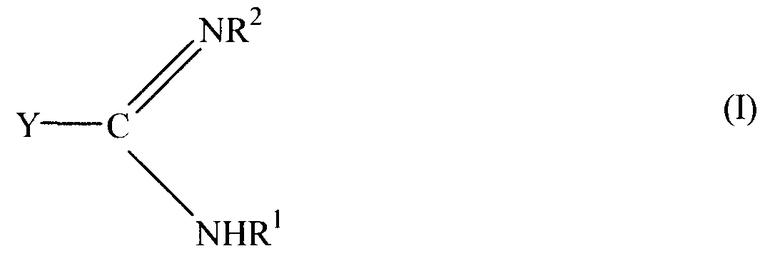
где Y выбран из группы, состоящей из замещенных алкильных, алкокси, арильных, аралкильных или аралкоксигрупп, включающих примерно от 1 до 22 углеродных атомов; замещенных или незамещенных галогенированных алкильных, алкокси, арильных, аралкильных или аралкоксигрупп, состоящих примерно из 1 до 22 углеродных атомов, а также перфторалкильных, перфторалкокси, перфторарильных, перфтораралкильных или перфтораралкоксигрупп, включающих примерно от 1 до 22 углеродных атомов; и R1 - атом водорода; замещенные или незамещенные низшие алкильные или алкоксигруппы из примерно 1-6 углеродных атомов и аминогруппа; и R2 означает R1 или гидроксильную группу, и это соединение используется в качестве вулканизирующего агента для перфторэластомерной композиции.
Также в изобретение включен способ вулканизации перфторэластомерной композиции, которая состоит из смеси (i) по меньшей мере одного соединения, выбранного из группы, состоящей из соединений на основе моноамидина, соединений на основе моноамидоксима и их смесей, и (ii) по меньшей мере одного соединения на основе бисамидина в качестве со-вулканизаторов для перфторэластомерной композиции.
Изобретение также описывает способ ускорения вулканизации перфторэластомерной композиции, который представляет собой использование ускорителя вулканизации для вулканизирующего агента, где ускоритель вулканизации выбран из группы, состоящей из соединения на основе моноамидина, соединения на основе моноамидоксина, соединения на основе бисамидина и или их комбинаций.
Изобретение также включает способ вулканизации перфторэластомерной композиции, включающий использование функционализированного вулканизирующего агента на основе дифенила, обладающего достаточно высокой молекулярной массой, такой чтобы его температура плавления не превышала примерно 240°С, а в некоторых предпочтительных вариантах была не выше примерно 230°С.
Также в изобретение включен способ получения вулканизирующего агента. Данный способ включает (а) взаимодействие органической алкилкислоты со спиртом для образования сложного алкилэфира; (b) взаимодействие сложного алкилэфира с аммиаком для получения алкилкарбоксиамида; (с) взаимодействие алкилкарбоксиамида с дегидратирующим реагентом для образования алкилнитрила; и (о) взаимодействие алкилнитрила с, по крайней мере, одним амином или аммиаком для получения вулканизирующего агента, который может вулканизировать или ускорять вулканизацию перфторэластомерной композиции.
Помимо вышеуказанного способа изобретение описывает способ получения вулканизирующего агента на основе бисаминофенола. Этот способ включает: (а) взаимодействие перфторацилфторида с фторидом калия, приводящую к образованию продукта реакции алкоголята калия; (b) взаимодействие продукта реакции алкоголята калия с перфтораллилфторсульфатом с образованием перфтораллилового эфира; (с) взаимодействие перфтораллилового эфира с окислителем для получения перфторглицидилового эфира; (d) взаимодействие перфторглицидильного эфира с хлоридом алюминия во фторированном растворителе для изомеризации эпоксидной группы в перфторглицидильном эфире в кетон; (e) взаимодействие кетонной группы с фенолом в присутствии фтороводорода для образования соединения на основе бисфенола; (f) нитрование соединения на основе бисфенола для получения соединения на основе биснитрофенола; и (g) восстановление полученного соединения на основе биснитрофенола для получения вулканизирующего агента на основе бисаминофенола, где вулканизирующий агент на основе биснитрофенола способен к вулканизации перфторэластомерной композиции.
Изобретение также включает вулканизирующий агент на основе замещенного бисаминофенила для перфорированных эластомеров, включающих нитрилсодержащие функциональные сшивающие мономеры. Вулканизирующий агент на основе бисаминофенила является замещенным вулканизирующим агентом на основе бисаминофенила, который имеет формулу (IIIа):
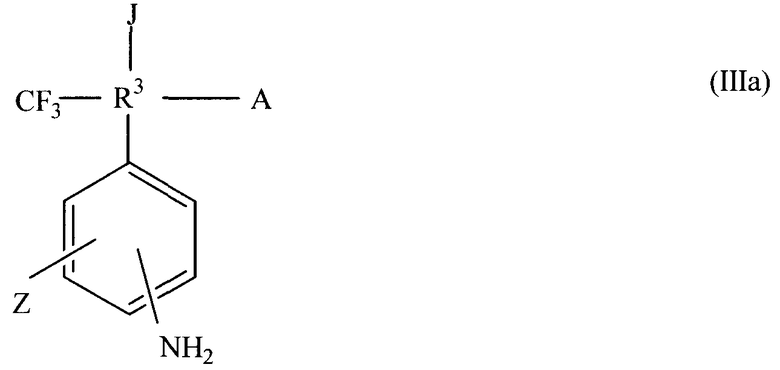
где R3 означает атом углерода; Z означает амино-, сульфгидрильную или гидроксильную группу; J описывается формулой (IV):

и А выбрана из группы, содержащей незамещенные и замещенные группы, с разветвленной и линейной цепью на основе углерода, где группы на основе углерода выбраны из группы, состоящей из перфторалкильных или перфторалкоксигрупп, содержащих примерно от 1 до 22 атомов углерода.
Изобретение также включает перфторэластомерную композицию, включающую вулканизирующий агент на основе бисаминофенила для перфторированных эластомеров, имеющих нитрилсодержащие функциональные сшивающие мономеры, где вулканизирующий агент является вулканизирующим агентом на основе бисаминофенила и имеет формулу (IIIa):
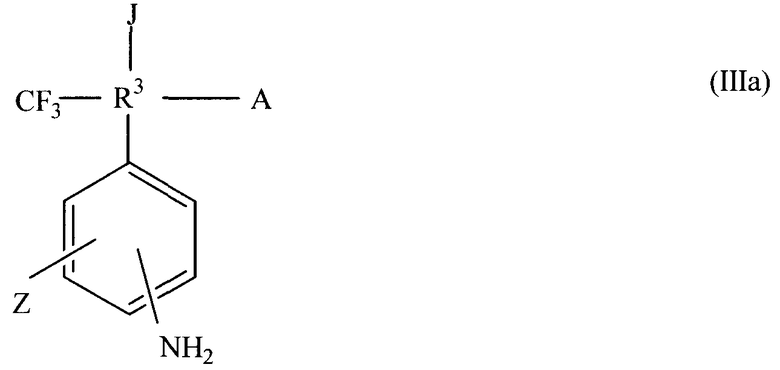
где R3 означает атом углерода; Z означает амино-, сульфгидрильную или гидроксильную группу; a J описывается формулой (IV):

и А выбрана из группы, состоящей из незамещенных и замещенных групп, с разветвленной и линейной цепью на основе углерода, где группы на основе углерода выбираются из группы, состоящей из перфторалкильных или перфторалкоксильных групп, содержащих примерно от 1 до 22 атомов углерода.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к вулканизирующим агентам и со-вулканизирующим агентам для перфторэластомерных композиций, имеющих низкую температуру плавления, предпочтительно на основе дифенила, предпочтительнее диаминофенила и более предпочтительно перфторированного диаминофенола, а также к новым способам синтеза предпочтительных функционализированных вулканизирующих агентов на основе дифенила. Также изобретение относится к ускорителям вулканизации, вулканизирующим агентам, со-вулканизирующим агентам на основе амидина для вулканизации перфторэластомеров. Вулканизирующие агенты и со-вулканизирующие агенты изобретения обладают улучшенной способностью к смешению с перфторэластомерными композициями, и вулканизирующими агентами, со-вулканизирующими агентами и ускорителями вулканизации, показывая более высокие скорости вулканизации по сравнению с обычными вулканизирующими агентами, такими как ВОАР. Дополнительно вулканизирующие агенты и ускорители вулканизации на основе амидина обеспечивают более быструю вулканизацию.
Используемый здесь перфторированный эластомер может представлять собой любой вулканизированный эластомерный материал, полученный вулканизацией перфторэластомерной композиции (как здесь определено), которая содержит вулканизируемый перфторированный полимер, имеющий функциональную группу, обеспечивающую возможность осуществления вулканизации. Перфторэластомер - это почти полностью фторированный полимер, что касается атомов углерода перфторполимера. Под этим подразумевается, на основе данного описания, что в некоторых композициях перфторированных эластомеров могут содержаться остаточные атомы водорода в функциональных сшивающих группах. Перфторированные полимеры, использованные в некоторых перфторэластомерных композициях для получения перфторэластомеров путем вулканизации, получены полимеризацией одного или более перфторированных мономеров, один из которых предпочтительно имеет функциональный сшивающий мономер, содержащий функциональную группу, обеспечивающую сшивку.
В качестве перфторэластомерной композиции здесь используется полимерная композиция, включающая вулканизируемый перфторированный полимер. Перфторированный полимер, как сказано выше, получают при полимеризации двух и более перфторированных мономеров и по меньшей мере одного перфторированного мономера, содержащего по меньшей мере одну функциональную группу, позволяющую осуществить процесс вулканизации, то есть должен присутствовать хотя бы один функциональный сшивающий перфторированный мономер. Такие материалы носят общее название FFKM (перфторэластомеры) в соответствии с определением (ASTM-D-1418-01а) Американского Общества по Тестированию Материалов (ASTM), полностью включенным в виде данной ссылки и описанным ниже в данном документе. Согласно определению перфторированный эластомер - это перфторированный каучук полиметиленового типа, все заместители полимерной цепи которого - фтор, перфторалкильные или перфторалкокси замещенные группы; небольшая часть таких групп может содержать функциональные группы, облегчающие вулканизацию. Перфторэластомерная композиция может содержать любой(ые) подходящий(ие) перфторированный(ые) полимер(ы) (FFKM), который(ые) может(гут) быть вулканизован(ы) с образованием перфторированного эластомера, и один или больше вулканизирующих агентов, таких, как описано в этом документе.
Такие перфторэластомерные композиции предпочтительно могут включать два или более различных перфторированных сополимера, по меньшей мере, одного фторсодержащего этилен-ненасыщенного мономера, такого как тетрафторэтилен (ТФЭ); перфторированный олефин, такой как гексафторпропилен (ГФП); и перфторалкилвиниловый эфир (ПАВЭ), который содержит разветвленные или линейные алкильные группы, и которые содержат одну и более эфирных связей, таких как перфтор(метилвиниловый эфир), перфтор(этилвиниловый эфир), перфтор(пропилвиниловый эфир) и подобные соединения. Примеры предпочтительных ПАВЭ включают соединения, описанные в патентах US № 5001278 и WO 00/08076, включенные в этот документ в виде ссылки. Другие подходящие ПАВЭ описаны, например, в патентах US №№ 5696189 и 4983697, и также включены сюда в виде ссылки.
Предпочтительными перфторированными полимерами также являются терполимеры или тетраполимеры ТФЭ, ПАВЭ и по меньшей мере один перфторированный сшивающий мономер, содержащий функциональную группу, обеспечивающую сшивку терполимера, по меньшей мере, один из которых является сшивающим мономером, который может быть вулканизирован вулканизирующими агентами и со-вулканизирующими агентами, являющиеся предметом данного изобретения. В одном из вариантов, сшивающий(ие) мономер(ы) обеспечивают сшивающие агенты, которые могут быть вулканизованы либо изобретенным вулканизующим агентом или изобретенным со-вулканизующим агентом или другими вулканизующими агентами, не являющиеся предметом изобретения, но которые могут обеспечить ускоренную вулканизацию действием ускорителей вулканизации данного изобретения.
Наиболее предпочтительные функциональные сшивающие мономеры включают нитрил-замещенные функциональные сшивающие соединения, вне зависимости от положения нитрильной группы, то есть первичные и вторичные нитрил-замещенные функциональные сшивающие мономеры. Примеры нитрил-замещенных функциональных сшивающих мономеров подробно описаны в настоящем патенте, и могут быть найдены, например, в патенте US № 4281092. Такие нитрил-замещенные функциональные сшивающие мономеры широко известны в производственных технологиях. В рамках данного изобретения также могут использоваться комбинации одного или более таких функциональных сшивающих мономеров друг с другом или с другими известными сшивающими мономерами.
Применимые функциональные сшивающие мономеры включают фторированные олефины и фторированные виниловые эфиры, имеющие в своем составе нитрильную группу. Общие примеры приведены далее:
CF2=CF-О-[CF2]n-CN, где n может быть примерно от 2 до 12, и предпочтительно примерно от 5 до 6;
CF2=CF-О-[CF2-CF(CF3)-O]n-CF2-CF(CF3)-CN, где n варьируется от 0 до примерно 4, предпочтительно от 0 до примерно 2;
CF2=CF-[OCF2CF(CF3)]m-О-[CF2]n-CN, где m изменяется примерно от 1 до 2, и n - примерно от 1 до 4; и
CF2=CF-О-[CF2]n-О-CF(CF3)-CN, где n - от 2 до примерно 4.
Конкретными примерами могут служить первичный функциональный сшивающий мономер, такой как CF2=CFOCF2CF(CF3)OCF2CF2CN (как правило называемый 8-CNVE) и вторичный функциональный сшивающий мономер, такой как CF2=CF-O[CF2]3-О-CF[CF3]-CN. Такие функциональные сшивающие мономеры могут быть использованы как в отдельности, так и в комбинации. В особенности предпочтительна комбинация сшивающих мономеров, как приведенная ниже фторполимерная или перфторполимерная цепь:
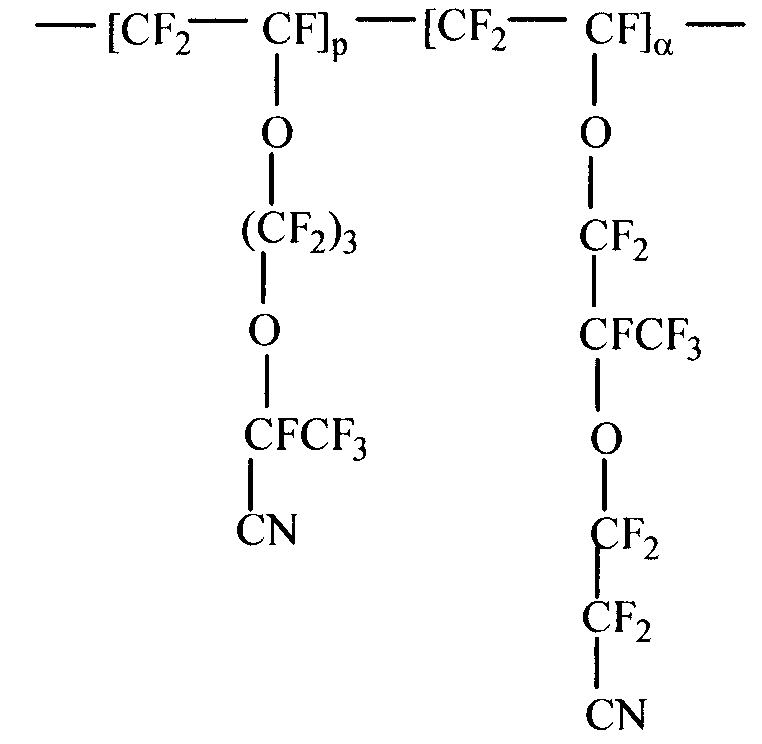
где р - вторичный функциональный сшивающий мономер, присутствующий во фторполимере или перфторированном полимере в количестве примерно от 0,1 до 12 мольных %, предпочтительно примерно от 1 до 4 мольных %, и α представляет собой первичный функциональный сшивающий мономер в количестве примерно от 0,1 до 12 мольных %, предпочтительно примерно от 1 до 7 мольных %. Предпочтительно, чтобы мольное отношение первичного сшивающего мономера ко вторичному сшивающему мономеру в сополимере составляло примерно от 1:1 до 10:1, и более предпочтительным является соотношение 9:1.
На основе данного описания будет понятно, что дополнительные типы сшивающих мономеров, которые содержат нитрильные группы в качестве функциональных сшивающих групп, и те, которые не содержат нитрильных групп, могут быть использованы дополнительно или, в некоторых случаях, вместо предпочитаемых сшивающих мономеров, указанных выше, при условии, что функциональные сшивающие мономеры могут быть вулканизованы при использовании предпочитаемых вулканизирующих агентов, со-вулканизирующих агентов и/или способны к вулканизации при использовании ускорителей вулканизации, описанных в данном изобретении и являющихся частью изобретения. Общие примеры других типов сшивающих мономеров включают олефины, включая частично или полностью галогенированные олефины, такие как этилен, фторвинилиден, фтористый винил, трифторэтилен, бромтетрафторбутен, бромтрифторэтилен, 1-гидропентафторпропен и 2-гидропентафторпропен. Такой(ие) дополнительный(ые) сшивающий(ие) мономер(ы) может(гут) присутствовать в количествах, указанных выше, и, в общем, предпочтительными являются количества примерно от 0,1 до 5 мольных процентов, более предпочтительны количества примерно от 0,1 до 2,5 мольных процентов, и самыми предпочтительными являются количества примерно от 0,3 до 1,5 мольных процентов.
Другие добавки, такие как со-вулканизирующие агенты, вулканизирующие агенты или ускорители, иные, чем описаны в данном изобретении, смазки; наполнители и прочие материалы также могут быть включены в качестве дополнительных компонентов перфторэластомерных композиций данного изобретения. Такие добавки включают наполнители, такие как графит, углерод, глина, диоксид кремния, фторполимерные частицы (например, мелкодисперсные порошки гомополимера и сополимера ТФЭ), сульфат бария, диоксид кремния, диоксид титана, акцептор кислоты, ускорители вулканизации, стекловолокно или полиарамидные волокна, такие как Кевлар, другие вулканизирующие агенты и/или пластификаторы или другие известные добавки или добавки, которые будут разработаны для применения в технологиях фторированных и перфторированных эластомеров. Предпочтительные перфторполимеры/перфторэластомеры включают продукты марки Simriz®, производимой немецкой компанией Фреденберг, марки Dyneon®, выпускаемой компанией Миннесота Майнинг энд Мэньюфэкчуринг в Миннесоте, Daiel-Perfluor®, производимой компанией Дайкин Индастриз Лтд в Осаке, Япония. Подобные материалы изготавливаются итальянской компанией Озимонт, а также в ФГУП Институте синтетического каучука им. С.В.Лебедева в России.
Предпочтительными вулканизирующими агентами и со-вулканизирующими агентами для фторэластомерных и перфторэластомерных композиций, описанных в данном изобретении, являются функционализированные дифенильные соединения, которые включают разветвленные или линейные алкильные цепи, галогенированные алкилы, пергалогенированные алкилы, и предпочтительнее соединения перфторалкильного типа, которые могут содержать или не содержать один или более атомов кислорода и которые могут быть замещенными или незамещенными, и которые содержат по меньшей мере, преимущественно две аминофенольных группы, но которые обладают достаточно высокой молекулярной массой (удлиненные цепи), такими чтобы их температуры плавления предпочтительно не превышали примерно 240°С, и более предпочтительно были не более примерно 230°С, и наиболее предпочтительно, чтобы температура плавления была примерно 225°С, таким образом повышая совместимость и повышая скорость вулканизации перфторэластомерных композиций, в частности, предпочтительных перфторэластомеров, содержащих нитрил-замещенные функциональные сшивающие мономеры.
Такими вулканизирующими агентами предпочтительно являются вулканизирующие агенты на основе дифенила, описываемые формулой (III):

В формуле (III), r может равняться 0 или 1. R3 и R4 (независимо выбраны друг от друга) означают атом углерода или группы на основе углерода разветвленного или линейного строения (замещенные или незамещенные), содержащие примерно от 2 до 22 атомов углерода в любой из таких цепей (разветвленной или линейной), предпочтительнее, чтобы такая цепь состояла из 10-22 атомов углерода, и такие группы могут выбираться из следующих примерных групп: алкильных групп, полностью или частично галогенированных алкильных групп, и предпочтительнее перфторированных алкильных групп, каждая из которых может прерываться по меньшей мере одним атомом кислорода, и в которых разветвленные цепи могут включать, например галогеналкильные, фторалкильные и трифторалкильные группы. Приемлемыми заместителями в формуле (III) и формулах, приведенных в данном документе в качестве замещаемых групп, включая предпочтительные структуры в соответствии с формулой (III), приведенной ниже, могут быть такие же заместители, что и в приведенных в этом документе формулах (I) и (II), при условии, что такие заместители способствуют реакции вулканизации. Предпочтительно, чтобы Z была амино-, меркапто-, тиофенольная, сульфгидрильная или гидроксильная группа, при этом наиболее предпочтительна гидроксильная группа.
Каждый J независимо друг от друга представляет собой формулу (IV):

или такой же заместитель, как А, при этом при этом каждый А может быть независимо выбран с любой стороны R3 в формуле (III) из группы (IV), атома водорода, атома фтора или разветвленной или линейной группы на основе углерода (замещенной или незамещенной), которая может быть выбрана из следующих групп: алкильной, частично или полностью галогенированной алкильной или перфторалкильной групп, наиболее предпочтительно, перфторалкильной группы, содержащей от одного до примерно 22 атомов углерода, углеродная цепь каждой из которых может прерываться по меньшей мере одним атомом кислорода, и разветвленные цепи которой могут включать такие группы, как, например, галогеналкильные, фторалкильные и трифторалкильные группы. Если r=0 и R3 означает атом углерода, то по меньшей мере один из J и каждый А не должен быть группой (IV). Если в рамках изобретения, А описывается формулой (IV), то желательно, чтобы только две таких группы присутствовало в вулканизирующих агентах формулы (III), таким образом, чтобы если r=0 и J описывается формулой (IV), приведенной выше, предпочтительно, чтобы ни одна из групп А не имела формулу (IV).
Предпочтительными являются структуры, в которых r=0 в формуле (III) и J соответствует формуле IV, приведенной выше, включая структуры, где R3 означает атом углерода и такие, где R3 означает разветвленную или линейную алкильную или перфторалкильную группу, которая может содержать или не содержать кислород. Далее предпочтительны структуры, в которых когда r=0, R3 означает атом углерода, J представляет собой формулу (IV), один из А означает трифторметил и другой А выбирается из группы, состоящей из разветвленной или линейной цепи перфторалкильных и перфторалкиэфирных групп, содержащих от 2 до 22 атомов углерода.
Предпочтительные структуры, в которых r равно 0, J удовлетворяет формуле IV и R3 означает атом углерода, включая следующие структуры (V)-(VII), в которых q предпочтительно варьируется от 0 до 6, хотя q большие 6 тоже находятся в рамках данного изобретения.
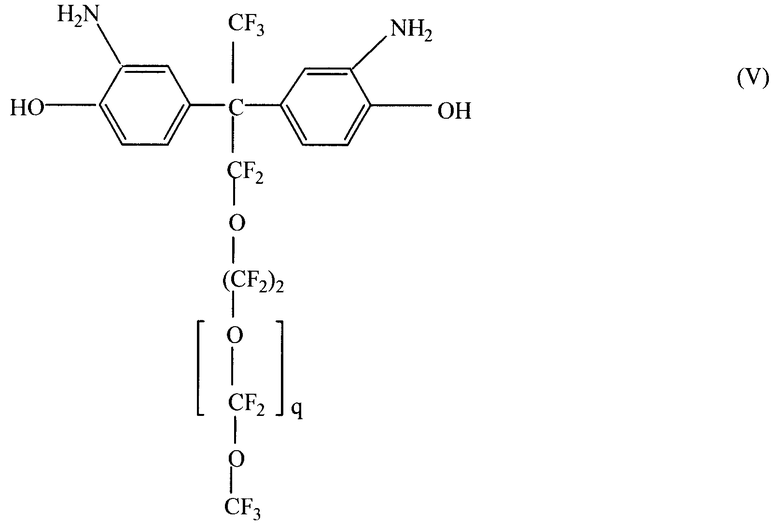
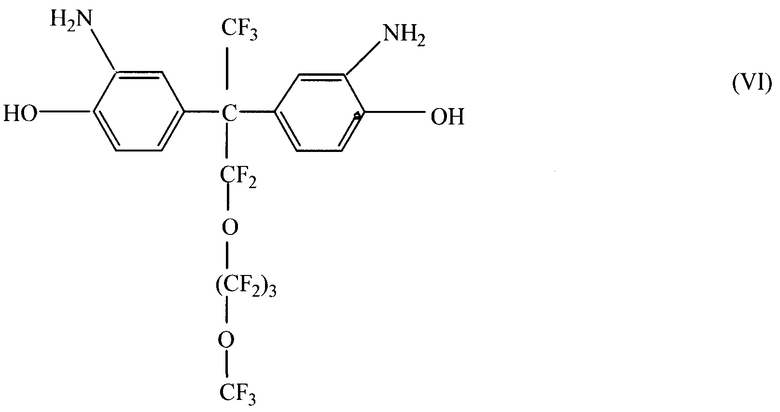
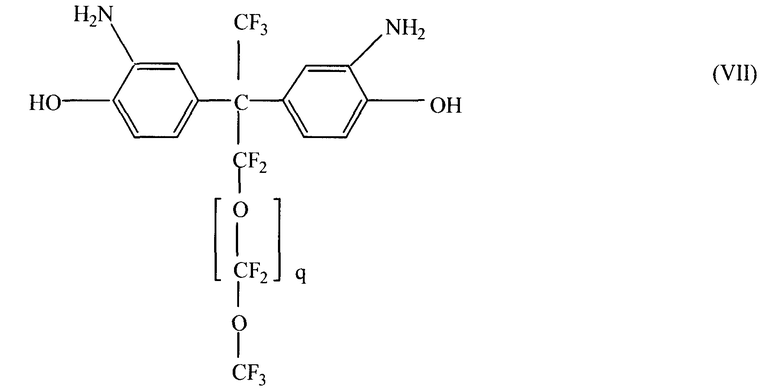
Далее, предпочтительные примеры соединений формулы III, в которых r=0, R3 - атом углерода, А с одной стороны R3 - это CF3 и А с другой стороны R3 - углеродная цепь различной длины, включают следующие материалы, приведенные ниже в Таблице 1 в соответствии со структурой цепи А, являющейся противоположной к А, которая является CF3. Как видно из Таблицы 1, предпочтительные соединения близки по цвету и виду, но имеют разные температуры плавления, обеспечивая широкий выбор вулканизирующих агентов относительно совместимости и скорости вулканизации фторэластомерных и перфторэластомерных композиций.
Предпочтительные примеры структур, где r=0 в формуле (III), J - такой же, как в формуле IV и R3 означает группу разветвленного или линейного строения, такую как алкил, галогеналкил, и предпочтительно перфторалкильная группа, которая может содержать или не содержать кислород, включая такие структуры как (VIII) и (IX), показанные ниже, в которых диаминофенильные группы находятся не в бис-положении, как в структурах, упоминавшихся выше, а находятся в терминальных положениях, разделенных цепью такой длины, чтобы молекулярный вес обеспечивал температуры плавления не выше примерно 240°С, и предпочтительно не более примерно 230°С, а наиболее предпочтительно, чтобы температуры плавления были примерно 225°С. В таких структурах А может быть такой, как описано выше. Если в рамках изобретения А описывается формулой (IV), то предпочтительно, чтобы в том случае, когда J то же, как в формуле (IV), то только две таких группы могут присутствовать в вулканизирующих агентах формулы (III) и желательно, чтобы в таких структурах А не была как в формуле (IV):
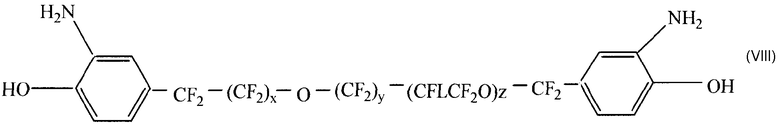
где х, у и z независимо выбираются из значений от 0 до примерно 20, предпочтительно от 0 до 10, причем также предпочтительно, чтобы сумма х+у+z была не больше, а лучше находилась в пределах примерно от 9 до 20; L - атом водорода, атом галогена, такой как фтор, хлор, бром и иод, алкил, галогеналкил и предпочтительно перфторалкилы, такие как трифторметил, наиболее предпочтительно, чтобы L был атомом фтора или трифторметильной группой. Еще один пример включает:
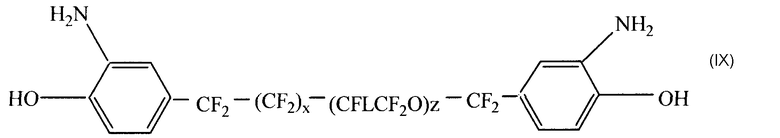
где L, x, z такие же, как определено выше, но х и z независимо преимущественно принимают значения от 0 примерно до 10, и сумма х+у желательно не должна превышать примерно 20, а более предпочтительно, чтобы она была в пределах примерно от 9 до 20. Следует понимать, что структуры в соответствии с формулой (III), в которых r=0 и R3 - алкильная или перфторалкильная группа разветвленного или линейного строения, содержащая или не содержащая кислород, включая вариации формул VIII и IX, где атомы фтора могут быть замещены, и/или L может быть разветвлен в более длинные структуры, как показано ниже, например, в формулах X-ХII:
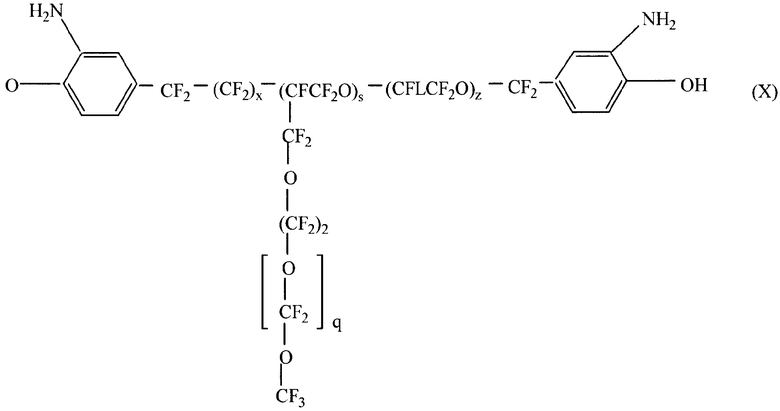
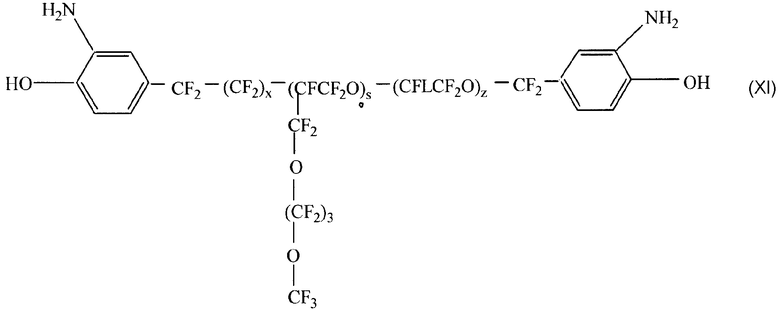
и
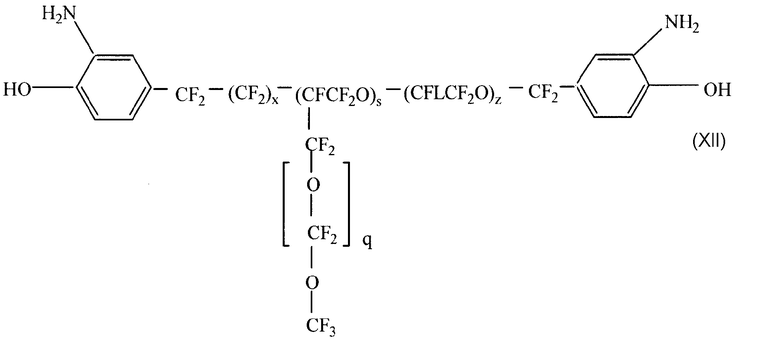
где s предпочтительно от 1 до примерно 6, и х, s и z принимают те же значения, как определено выше, причем сумма х+s+z не должна преимущественно превышать примерно 20 и более желательно должна быть как можно меньше, s=1 и х и z=0.
Когда в формуле (III) r не равно 0, то в рамки изобретения включены структуры, которые содержат хотя бы две аминофенильных группы, но в которых аминофенильные группы находятся не в бис-положении и/или желательно, в терминальном положении. В таких структурах хотя бы одна аминофенильная группа расположена на R3 и R4 в любом месте на цепях, где J и А такие же, как определено выше, но в предпочтительных вариантах соединение может содержать только две такие аминофенильные группы в целом, таким образом, когда другие такие группы уже присутствуют, предпочтительно, чтобы J и А не имели структуру (IV), даже если такие соединения ясно описываются данным изобретением. Примерами таких структур на основе бисаминофенола могут быть приведенные ниже структуры. Тем не менее, следует понимать, что вариации таких структур также включены в изобретение в соответствии с формулой (III):
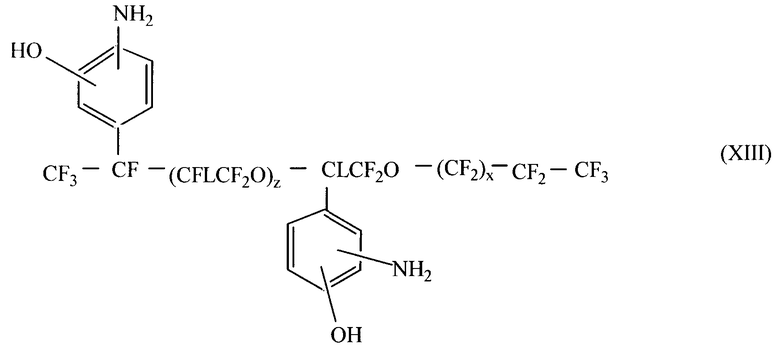
Например, в формуле XIII, приведенной выше, обе группы А означают CF3, R3 означает - 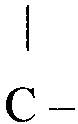
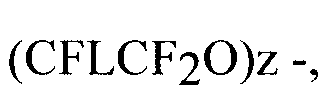 a R4 означает
a R4 означает 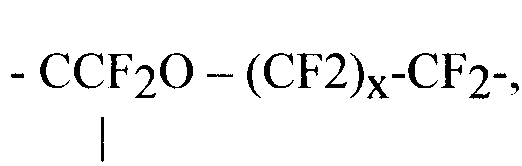 J группа в составе R3 означает F и J группа в составе R4 означает L, и х и z такие, как описано ниже. Такие примеры включают:
J группа в составе R3 означает F и J группа в составе R4 означает L, и х и z такие, как описано ниже. Такие примеры включают:
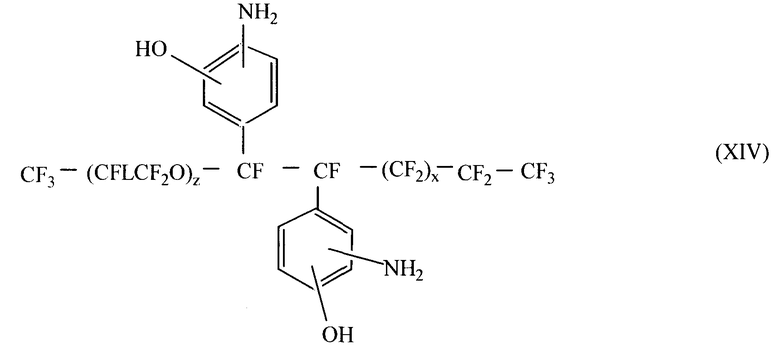
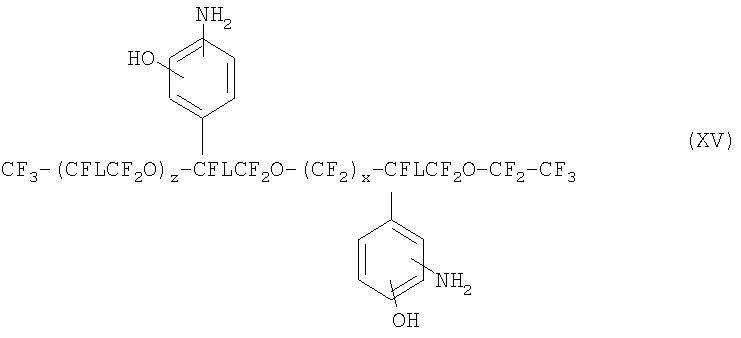
и
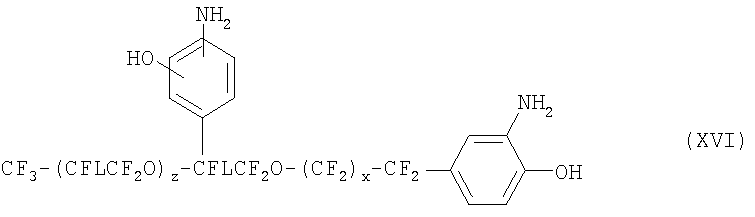
где L, x и z такие, как описано выше. Тем не менее, в формулах XIII, XIV, XV и XVI, предпочтительно, чтобы в итоге сумма х и z принимала значения не больше 19. Также желательно, чтобы во всех вышеупомянутых формулах L был фтором, перфторалкильной или перфторалкокси группой.
Другие предпочтительные структуры включают соединения формулы (III), где r=1, каждый А и каждый J - атомы фтора, R3 - атом углерода и R4 выбирается из группы, состоящей из линейной или разветвленной перфторалкиленовой и перфторалкилэфирной групп, содержащих от 2 до 22 атомов углерода, где один А и. один J оба присоединены к терминальному атому углерода R4.
Существуют и/или могут быть разработаны различные способы синтеза 15 разнообразных предпочитаемых вулканизирующих агентов формулы (III).
Вулканизирующие агенты являются частью данного изобретения вне зависимости от пути их получения. Существующие методы синтеза некоторых соединений формулы (III), как описанные в статье R. С. Evers, J. Polym. Sci. 16, 2833-2848 (1978), включены в данный документ в качестве ссылки. Настоящее изобретение включает несколько новых путей синтеза предпочтительных соединений в соответствии с формулой (III). Один из таких путей предполагает использование эпоксид-кетонной схемы, описываемой ниже, а другой метод заключается в применении магнийорганических соединений и также описан ниже в этом документе. Хотя здесь приводятся новые методы синтеза, следует понимать, что для синтеза новых вулканизирующих и со-вулканизирующих агентов, являющихся предметом изобретения, могут быть использованы любые другие методы. Таким образом, функционализированные вулканизирующие и со-вулканизирующие агенты на основе дифенила, которые имеют достаточно высокие молекулярные массы, такие что их температуры плавления составляют не более примерно 240°С, а предпочтительнее не больше примерно 230°С, или наиболее предпочтительно примерно 225°С, включены в изобретение наряду с соединениями общей формулы (III) вне зависимости от методов их синтеза.
Предпочтительные реакции включают взаимодействие перфторалкилацилгалогенида, предпочтительно перфторалкилацилфторида, т.е. соединения, содержащего ацильную группу, и лучше, перфторацилфторида, с фтористым калием с образованием алкоголята исходного соединения. Полученный продукт реакции алкоголят калия затем вводят в реакцию с перфтораллилфторсульфатом, которая приводит к образованию соответствующего перфтораллильного эфира.
Далее этот перфтораллильный эфир окисляют под действием какого-либо окислительного агента, где окислителем предпочтительно является, но не ограничиваясь этим, кислород, и получают перфторглицидиловый эфир. Далее проводят реакцию полученного эфира с хлоридом алюминия во фторированном растворителе для изомеризации эпоксидной группы перфторглицидного эфира в кетон. Затем кетон вводят в реакцию с фенилом, замещенным группой Z (с фенолом, если Z означает ОН, что наиболее предпочтительно) в присутствии фтороводорода для получения соединения на основе бисфенила, а предпочтительнее бисфенола.
Далее такое соединение на основе бисфенила или бисфенола нитруют азотной кислотой (или другим удобным нитрующим агентом) для введения нитрогруппы в каждое фенильное кольцо и получения соединения на основе биснитрофенила или бисаминофенола. Полученное нитросоединение затем восстанавливают подходящим восстановителем и получают целевое соединение, имеющее бисаминофенильные, или предпочтительнее, бисаминофенольные группы, каждая из которых также имеет Z радикал (предпочтительно бисаминофенольные группы), и имеющие формулу IV, и которое обеспечивает вулканизацию перфторэластомерной композиции.
Такой примерный синтетический путь получения новых вулканизирующих и со-вулканизирующих агентов в соответствии с изобретением может быть продемонстрирован на примере формул V и VI и похожих соединений, в которых один А в формуле III означает CF3, R3 означает атом углерода, J представляет собой формулу IV и r=0, и включает следующую основную схему реакции, где R' представляет собой часть цепочки А группы (CF2-O-CF2-R') находящейся напротив А, которая является -CF3:
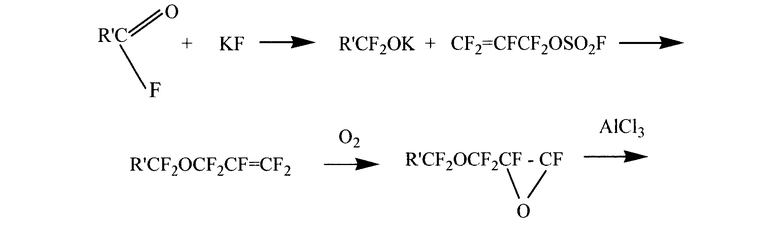
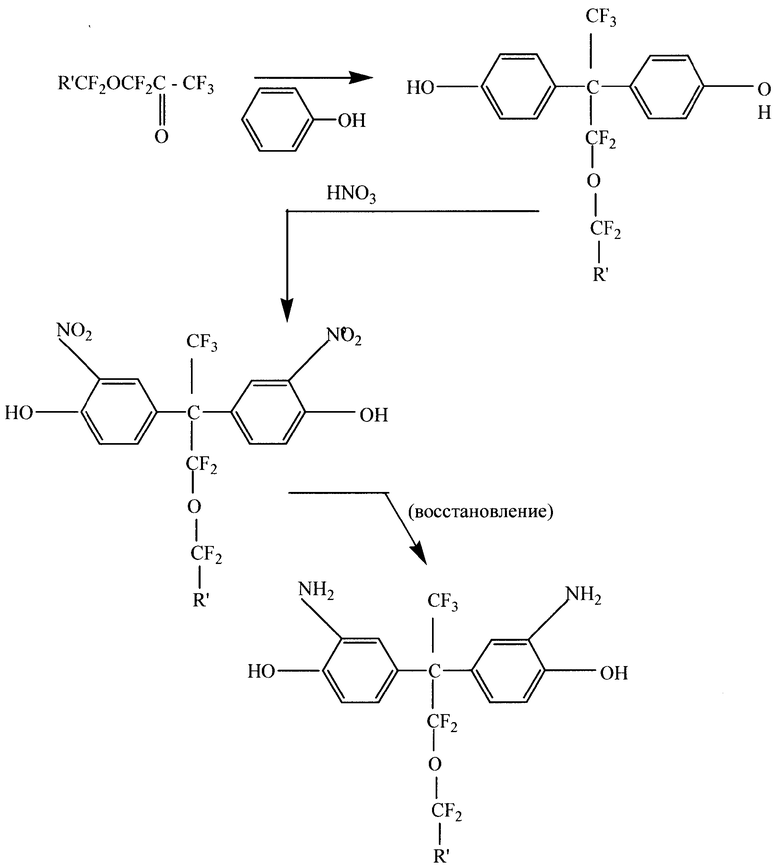
Следующая примерная схема получения соединений общей формулы (III), где R3 означает атом углерода, r=0, J описывается формулой (IV), одна А группа означает CF3 и другая А группа (обозначенная ниже на схеме как А') означает CF3O(CF2O)qCF2- как в соединениях (VII) и родственных соединениях, включает метод, в котором применяются магнийорганические соединения. При этом алкилмагнийгалогенид, галогеналкилмагнийгалогенид или перфторалкилмагнийгалогенид, и предпочтительнее перфторалкилмагнийиодид, такой как трифторметилмагнийиодид, вводят в реакцию с алкилом, галогенированным алкилом или перфторированным ацилгалогенидом (таким, как А цепь в формуле (III)), где ацилгалогенид содержит галогенированную кетогруппу. Образующееся соединение освобождает галогенид магния и оставляет кетогруппу на ацилгалогениде. Этот кетон далее вводят в реакцию с ароматическим соединением, замещенным функциональной группой Z (желательно гидроксильной), для получения бисфенильной функциональной группы (предпочтительнее бисфенол) в месте кетоновой группы, затем соединение нитруют и впоследствии восстанавливают, подобно методу описанному ранее. Пример подобного механизма показан ниже:
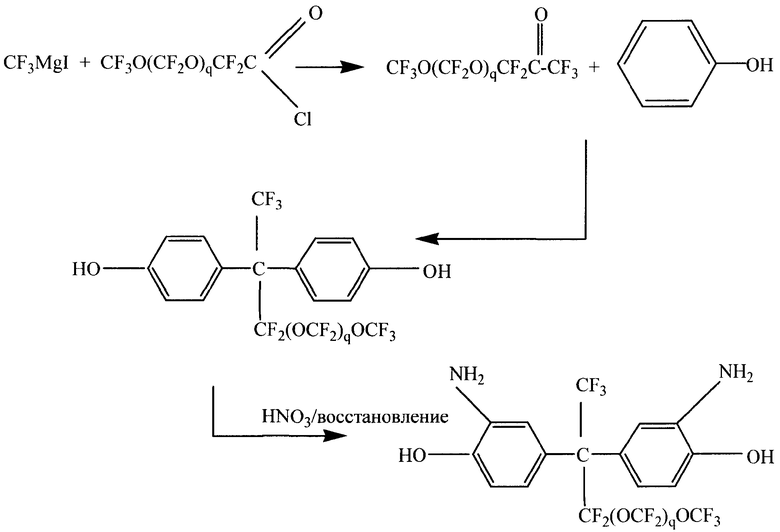
С другой стороны, каждая из двух фенильных групп могут быть присоединены к R3 или R4 в разных положениях и/или в терминальных положениях при использовании известных реакций замещения и путей получения других соединений общей формулы (III). Один из таких способов замещения описан Эверсом, и был уже упомянут ранее, заключающийся в получении фторуглеродных бисаминофенолов (некоторые из которых представлены формулой (III)) по реакции дииодперфторалканов с иодфенилацетатом, последующем гидролизе продукта для получения бисфенола, который затем нитровали и восстанавливали динитробисфенол для образования бисаминофенола.
Также можно использовать и другие вулканизирующие агенты или более одного вулканизирующего агента в зависимости от присутствующих функциональных сшивающих мономеров, такие как органические пероксиды и металлоорганические соединения, такие как, оловоорганические соединения, диамины, амидины, традиционные бисаминофенолы и/или бисаминотиофенолы и т.д. или их смеси. Также перфторированные полимеры могут быть вулканизованы путем радиационной вулканизации для содействия или для вулканизации других сшивающих мономеров, не вулканизованных вулканизирующими и со-вулканизирующими агентами, являющимися предметом данного изобретения.
Количество и тип вулканизирующего или со-вулканизирующего агента в соответствии с изобретением должны быть выбраны таким образом, чтобы оптимизировать желаемые свойства вулканизованного фторированного или перфторированного эластомера (включая его химическую устойчивость, относительное удлинение на разрыв, остаточную деформацию при сжатии, модуль изгиба, прочность на разрыв, твердость и проч.). Это количество зависит от желаемой степени сшивки, типа и числа функциональных сшивающих мономеров, которые будут вулканизованы изобретенными вулканизирующими агентами, и числа других функциональных сшивающих мономеров, не входящих в данное изобретение, и желаемой скорости вулканизации. Предпочтительными количествами вулканизирующего агента является эквивалентное количество с небольшим избытком по сравнению с количеством, требуемым для реакции со сшивающими мономерами, присутствующими в композиции фторированных или перфторированных эластомеров, которые могут вступать в реакции с вулканизирующими и со-вулканизирующими агентами, разработанными в рамках данного изобретения. Предпочтительными являются количества от примерно 0,1 до примерно 10 частей по массе вулканизирующего агента на примерно 100 частей используемого фторполимера или перфторполимера, и более предпочтительными являются количества от примерно 1 до примерно 4 частей по массе. При использовании вещества в качестве со-вулканизирующего агента, следует брать меньшие количества, поскольку протекают другие реакции вулканизации. Тем не менее, это количество также зависит от количества функциональных сшивающих мономеров и других параметров, указанных выше.
Настоящее изобретение включает вулканизирующие агенты на основе амидина и амидоксима, которые могут выполнять функции как вулканизирующих или со-вулканизирующих агентов, так и ускорителей вулканизации, и могут применяться как отдельно, так и совместно с вулканизирующими и со-вулканизирующими агентами на основе бифенила, являющимися предметом изобретения, как здесь описано, или с другими вулканизаторами, не покрываемыми данным изобретением, или могут использоваться для дальнейшего увеличения скорости вулканизации вулканизирующих и со-вулканизирующих агентов на основе бифенила, описанных в изобретении, или каких-либо других агентов вулканизации перфторированных эластомеров, не входящих в объем данного изобретения.
Подходящие вулканизирующие агенты и ускорители вулканизации на основе амидина и амидоксима включают моноамидины, моноамидоксимы и бисамидины, такие, как описаны в данном документе. Другие известные ускорители вулканизации, такие как органические или неорганические соли аммония, например перфтороктаноат, перфторацетат аммония, тиоцианат аммония, сульфамат аммония, мочевина, трет-бутилкарбамат, ацетальдегид аммония, тетраалкилфосфониевые соли, тетраалкиламмонийные соли и триалкилсульфониевые соли, такие как бензилтрифенилфосфоний хлорид, бензилтрифенилфосфоний бромид, бензилтрифенилфосфоний фенолят бисфенола AF, тетрабутиламмоний сернокислый и тетрабутиламмонийбромид, также при желании могут быть использованы совместно с новыми вулканизаторами и со-вулканизаторами на основе бифенила, разработанными в данном изобретении. Тем не менее, что касается ускорителей, требуемых для новых вулканизаторов и со-вулканизаторов на основе бифенила, описанных в изобретении, то предпочтительно, чтобы для ускорения вулканизации вулканизаторов и со-вулканизаторов на основе бифенила, являющихся предметом изобретения использовались ускорители вулканизации на основе амидина и амидоксима.
Предпочтительными ускорителями вулканизирующих и со-вулканизирующих агентов на основе бифенила, описанных в данном изобретении, являются вулканизирующие агенты на основе амидина и амидоксима, которые самостоятельно могут действовать, как вулканизирующие или со-вулканизирующие агенты для перфторэластомерных композиций. Такие материалы на основе амидина и амидоксима включают моноамидины и моноамидоксимы следующей формулы (I) и бисамидины формулы (II), описанные ниже. Моноамидины и моноамидоксимы могут быть представлены формулой (I)
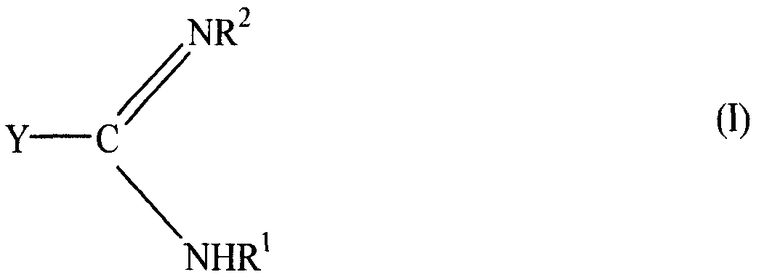
где Y может быть замещенная алкильная, алкоксильная, арильная, аралкильная или аралокси группа; или замещенная или незамещенная, полностью или частично галогенированная алкильная, алкокси, арильная, аралкильная или аралкокси группа, состоящая из примерно 1-22 углеродных атомов. Y также может быть, и предпочтительно является перфторалкильной, перфторалкокси, перфторарильной, перфтораралкильной или перфтораралокси группой, из примерно 1-22 атомов углерода и, более предпочтительно, перфторалкильной или перфторалкокси группой из примерно 1-12 атомов углерода, и более предпочтительно из 1-9 атомов углерода; R1 может быть атомом водорода; замещенной или незамещенной низшей алкильной или алкоксильной группами из примерно 1-6 углеродных атомов или аминогруппой. R2 независимо может быть любой группой из перечисленных для R1 или гидроксильной группой. Заместители в Y, R1 или R2 включают, но не ограничиваются, галокеналкилами, пергалогенированными алкилами, галогеналкокси, пергалогеналкокси, тио-, амино-, имино-, амидо-, имидогруппами, водородом, карбоксильной, сульфонильной, гидроксильной группами и т.п. Предпочтительными вариантами являются соединения, в которых R2 означает гидроксильную группу, атом водорода или замещенную или незамещенную алкильную или алкокси группы, состоящие из 1-6 атомов водорода, более предпочтительно гидроксильная группа или атом водорода. Также предпочтительными являются соединения, в которых R1 - атом водорода, аминогруппа или замещенная или незамещенная низшая алкильная группа из 1-6 атомов углерода, тогда как R2 - гидроксильная группа или атом водорода. Наиболее предпочтительными являются структуры, в которых R1 означает атом водорода. Также предпочтительные варианты включают соединения, в которых Y является перфторалкильными, перфторалкокси, замещенными или незамещенными арильными группами и замещенными или незамещенными галогенарильными группами с такой длиной цепи, как было указано выше.
Примеры вулканизирующих и со-вулканизирующих агентов на основе моноамидина и моноамидоксима в соответствии с формулой (I) включают перфторалкиламидины, ариламидины, перфторалкиламидоксимы, ариламидоксимы и перфторалкиламидразоны. Конкретные примеры включают перфтороктанамидин, гептафторбутириламидин, бензамидин, трифторметилбензамидоксим и трифторметоксилбензамидоксим. Вулканизирующие агенты, соответствующие формуле (1), могут использоваться самостоятельно или в комбинациях, таких как комбинации соединений, которые будут перечислены далее.
Вулканизирующие агенты, соответствующие формуле (I), могут вулканизовать перфторэластомерные композиции, в частности те, в которых содержится по меньшей мере один функциональный нитрилсодержащий сшивающий мономер. Вулканизирующие агенты, соответствующие формуле (I) данного изобретения, также являются ускорителями вулканизации на основе моноамидина и моноамидоксима, которые могут ускорять вулканизацию перфторэластомерных композиций, которые содержат хотя бы один функциональный нитрилсодержащий сшивающий мономер, и более предпочтительны композиции, которые также включают вулканизирующие агенты на основе дифенила (включая новые вулканизирующие агенты на основе дифенила, входящие в объем изобретения), такие как бисаминофенол и его производные. Подходящие примеры моноамидинов включают бензамидины и перфторалкиламидины. Конкретными примерами подходящих соединений являются перфтороктанамидин и перфторгептанами дин.
Изобретение также включает вулканизирующие агенты и ускорители вулканизации фторэластомерных и перфторэластомерных композиций на основе бисамидина, представленные формулой (II):
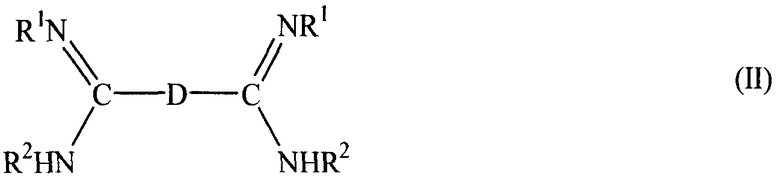
где D может быть замещенная или незамещенная, полностью или частично галогенированная алкильная, алкокси, арильная, аралкильная или аралкокси группа, состоящая из примерно 1-22 углеродных атомов, или, более предпочтительно, перфторалкильная, перфторалкокси, перфторарильная, перфтораралкильная или перфтораралкокси группа, и примерно 1-22 атомов углерода, и более предпочтительно, перфторалкильная или перфторалкокси группа из примерно 1-12 атомов углерода; R1 или R2 - такие, как определено выше для формулы (I), тем не менее, в формуле (II), R2 - не гидроксильная группа, и выбирается независимо из заместителей, приведенных для R1 выше. Далее, каждый из D, R1 или R2 может быть замещен одной и более группами, указанными выше для формулы (I). Более предпочтительными вариантами соединений формулы (II) являются те из них, где оба
R1 и R2 - атомы водорода.
Предпочтительно, чтобы Y, R1 и R2 содержали атомы кислорода в виде эфирных связей. Хотя предпочтительно, чтобы Y была разветвленной или линейной структурой, в рамках изобретения она также может иметь циклическую или ароматическую структуру, которая может быть замещенной таким же образом, как описано выше.
Что касается бисамидинов формулы (II), предпочтительнее, чтобы D была фторированной, и более предпочтительно перфторированной группой. Если D только частично галогенирована, тем не менее, предпочтительно, чтобы атомы углерода, примыкающие к амидиновой группе, каждый имели два водородных заместителя для стабилизации соединения. Предпочтительно, чтобы D содержала атомы кислорода в виде простых эфирных связей. Хотя предпочтительно, чтобы D была разветвленной или линейной цепью, в рамках изобретения она также может иметь циклическую или ароматическую структуру, которая также может быть замещенной. Конкретные подходящие примеры таких бисамидинов включают перфторсуберамидин и перфторсебацамидин. Подходящие перфторалкилмоноамидины и бисамидины могут быть приобретены в компании СинКвест Лабораториз, Лтд. во Флориде. Такие материалы также коммерчески доступны в ФГУП Институте синтетического каучука им. С.В.Лебедева в России.
Бисамидины, входящие в данное изобретение, могут быть использованы в качестве ускорителей вулканизации перфторэластомеров, в частности, если перфторэластомерная композиция содержит по крайней мере один нитрил-содержащий функциональный сшивающий мономер. Примеры предпочтительных бисамидинов в соответствии с изобретением включают перфторсуберамидин и перфторсебацамидин.
Понятно, что когда вышеперечисленные материалы на основе амидина и амидоксима используются в качестве ускорителей, их количество берется исходя из конкретной выбранной перфторэластомерной композиции, выбранных вулканизирующих и/или со-вулканизирующих агентов, а также желаемых свойств вулканизата, таких как время, необходимое для достижения требуемой минимальной вязкости по Муни, устойчивость к деформации, максимальный крутящий момент, измеряемый ротационным реометром. Подходящими являются количества от около 0,1 до около 5 частей ускорителя на около 100 частей перфторированного полимера.
Что касается получения моноамидинов, моноамидоксимов и бисамидинов, то изобретение не ограничено каким-либо определенным способом их получения. Могут быть использованы любые способы синтеза и/или коммерчески доступные моноамидины, моноамидоксимы и бисамидины. Тем не менее, в изобретение включен новый способ синтеза этих соединений, описанный в данном документе. При получении полезных для целей изобретения моноамидинов сначала алкилкарбоновую кислоту (то есть, органическую кислоту, такую как соединение, содержащее карбоксильную кислоту), галогеналкилкарбоновую кислоту и, предпочтительнее, перфторалкилкарбоновую кислоту сначала переводят в нитрильную форму посредством проведения реакции карбоновой кислоты (или подобного соединения, как указано выше) со спиртом, таким как алканол, то есть, метанол или этанол, в присутствии неорганической кислоты, например, серной. Реакционную массу кипятят, промывают водой и сушат, используя подходящий материал, например MgSO4. В результате получают сложный эфир алкилкарбоновой, галогеналкилкарбоновой или перфторалкилкарбоновой кислоты, который вводят в реакцию с азотсодержащим реагентом, таким как аммиак, предпочтительно газообразный. Реакция проводится при тщательном температурном контроле, и продуктом реакции является карбоксиамидная структура, такая как алкилкарбоксиамид. Продукт этой реакции затем смешивают с дегидратирующим агентом, таким как, например, Р2О5, кипятят с обратным холодильником и, в результате, получают алкилнитрильное соединение, такое как нитрил-замещенные алкилы, включая алкилнитрил, галогеналкилнитрил или перфторалкилнитрильные соединения. Затем полученный алкилнитрил помещают в реакционную камеру, содержащую хотя бы одно азотсодержащее соединение, такое как, предпочтительно, аминсодержащий состав или аммиак, газообразный или жидкий, предпочтительно жидкий. Азотсодержащее соединение, такое как аммиак, предпочтительно использовать примерно в 10-кратном избытке по отношению к добавленному алкилнитрилу (нитрилсодержащему соединению). После прибавления алкилнитрила в камеру с азотсодержащим соединением, температуру поднимают, предпочтительно медленно, до комнатной температуры, и избыток азотсодержащего соединения (такого как аммиак) удаляют. В результате получают алкил-, галогеналкил- или перфторалкиламидины, которые, как правило, представляют собой кристаллические вещества белого цвета. Хотя предложенный синтетический метод является предпочитаемым методом синтеза моноамидинов, в соответствии с изобретением, также может быть применен любой другой известный или новый метод получения бисамидинов, моноамидинов или моноамидоксимов данного изобретения, что не выходит за рамки данного изобретения. Как уже было указано выше, получающиеся моноамидины и моноамидоксимы, входящие в изобретение, являются полезными вулканизирующими веществами, которые могут вулканизировать или ускорять вулканизацию перфторэластомерных композиций. Предпочтительные соединения, полученные по описанному выше методу, включают перфторгептанамидин.
Перфторэластомерная композиция смешивается или перемешивается с одной из вышеперечисленных добавок любым удобным способом или при помощи какого-либо удобного устройства, включая двухвалковые вальцы и закрытые резиносмесители. Например, композиции могут быть смешаны при помощи закрытых резиносмесителей, таких как смесители Бэнбэри фирмы С.В.Брадендер Инструментс, Лтд. Нью-Джерси или Морияма, из Фармингдэйл, Нью-Йорк. Предпочтительно прибавлять вулканизирующие и со-вулканизирующие агенты и/или ускорители вулканизации по изобретению одновременно, и после того, как все другие ингредиенты композиции уже перемешаны. Однако стоит понимать, что порядок прибавления этих материалов не ограничивает рамки изобретения. Композиции могут быть переработаны и вулканизованы/сшиты под действием нагревания или под давлением для формования эластомерных деталей, таких как уплотнители. Для улучшения физических свойств материала может быть желательна дополнительная вулканизация, которая тоже находится в рамках данного изобретения.
Дополнительные примеры предпочитаемых ускорителей вулканизации на основе моноамидина, которые могут использоваться в качестве прямых вулканизирующих или со-вулканизирующих агентов приведены в Таблице 2, где R1 и R2 оба являются атомами водорода, и где соединения упорядочены в соответствии со структурой Y в формуле (I), приведенной выше.
Далее изобретение будет подробно описано в следующих не ограничивающих примерах:
ПРИМЕР 1
Было получено бисаминофенольное производное соответствующее формуле (III) (2,2-бис[3-амино-4-гидроксифенил]4,7,9,11-тетраокса-1,1,1,3,3,5,5,6,6,8,8,10,10,12,12,12
гескадекафтордодекан), в котором R3 означает атом углерода, r=0, J соответствует структуре формулы (IV), где один из А означает CF3 и другой А - CF2OCF2CF2(OCF2)2OCF3. Такая структура представлена выше формулой (V). Чтобы приготовить это соединение, сначала был получен перфторированный эфир кетон в соответствии с полиэпокси-кетонным методом, подробно описанным далее. В колбу под постоянным током сухого азота поместили 11,6 г (0,2 моль) фторида калия и 100 мл диглима, высушенного перегонкой над СаН2. Реакционную смесь перемешивали 15 минут. Затем при хорошем перемешивании к смеси в течение 1-1,5 часов при комнатной температуре добавили 60 г (0,19 моль) 3,5,7-триокса-2,2,4,4,6,6,8,8,8-нонафтороктаноилфторида. По окончании прибавления реакционную массу перемешивали еще 2 часа пока весь фторид калия не растворился и не образовалась соль алкоголят калия CF3O(CF2O)2CF2CF2OK. Наличие алкоголята в смеси и окончание реакции подтверждалось исчезновением полосы поглощения в ИК-спектре при 1890 см-1 соответствующего связи фтор-карбонил:
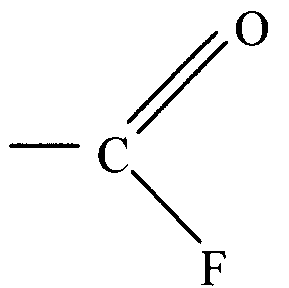
Схема реакции, описанной выше, следующая:
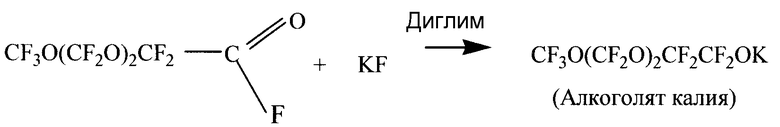
По окончании реакции колбу с алкоголятом калия охладили до 10°С и к колбе присоединили капельную воронку. Далее медленно (по каплям) при 10-15°С добавили 48 г (0,21 моль) перфтораллилфторсульфата. После дополнительных двух часов перемешивания образовалось два жидких слоя. Слои были разделены и верхний слой перегнали при 60°С и вакууме 0,5 мм рт.ст. Дистиллят объединили с нижним слоем и промыли водой для удаления соли KOSO2F. Слои разделили, и верхний водный слой удалили. Нижний слой высушили перегонкой над Р2О5 и получили неочищенный перфтораллильный эфир (4,7,9,11-тетраокса-1,1,2,3,3,5,5,8,8,10,10,12,12,12-гексадекафтордодецен) с 95% выходом. Неочищенный перфтораллильный эфир разделили фракционной перегонкой и была собрана фракция, кипящая при 88°С, и проанализирована с помощью ИК спектроскопии (полоса поглощения при 1795 см-1 отвечает -CF=CF2) и ЯМР F19, а также при помощи элементного анализа. Получены следующие результаты элементного анализа:
Рассчитано C8F16O4: С, 20,68%; F, 65,51%.
Экспериментально найдено: С, 20,24%; F, 65,63%. Схема реакции следующая:
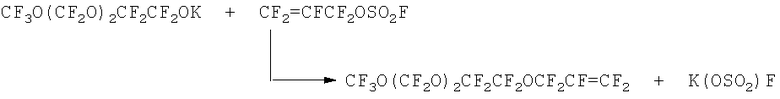
Полученный перфтораллиловый эфир окислили в хорошо перемешиваемом реакторе из нержавеющей стали объемом 1 литр. Реакцию проводили в течение 12 часов при температуре от 80 до 120°С и под давлением кислорода от 12 до 20 атмосфер (от 150 до 300 psig). Реакционную массу перегнали при 90°С и давлении 100 мм рт.ст. и получили перфторглицидиловый эфир
(4,7,9,11-тетраокса-1,1,2,3,3,5,5,6,6,8,8/10,10,12,12,12-гескадекафтордодекан-1,2-оксиран) с выходом 85%. Строение соединения было подтверждено методом спектроскопии ЯМР F19 и ИК-спектроскопии, где присутствует сигнал при 1530 см-1 (эпоксид), соответствующая эпоксиду 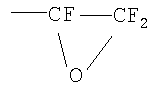 , а также отсутствует полоса поглощения при 1795 см-1 (отсутствует группа -CF=CF2-). Схема этой реакции представлена ниже:
, а также отсутствует полоса поглощения при 1795 см-1 (отсутствует группа -CF=CF2-). Схема этой реакции представлена ниже:
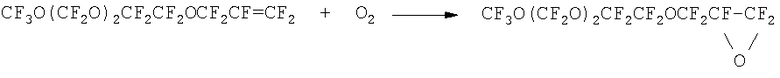
В колбу поместили 3 г АlСl3 и 10 мл фреона 113, смесь перемешивали в течение 40 минут при комнатной температуре. Большая часть фреона была удалена в вакууме, и в результате была получена пастообразная масса. К этой массе по каплям в течение 10-15 минут добавили при перемешивании 30 г полученного перфторглицидилового эфира. Реакционную массу перемешивали при 50°С в течение 2 часов. Протекание реакции изомеризации контролировали по спектрам ИК. По мере прохождения реакции полоса поглощения эпоксида при 1530 cм-1 переходила в полосу поглощения кетогруппы при 1796 см-1. Неочищенный перфторированный кетон был получен с 90% выходом путем перегонки реакционной массы при 60°С и 100 мм рт.ст. Чистый перфторкетон (4,7,9,11-тетраокса-1,1,1,3,3,5,5,6,6,8,8,10,10,12,12,12-гексадекафтордодекан-2-он) был получен фракционной перегонкой при 114°С. Строение соединения было подтверждено методом спектроскопии ЯМР F19, а чистота была подтверждена методом газо-жидкостной хроматографии. Конечная реакция образования перфторкетона представлена ниже:
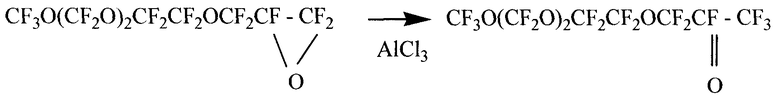
В металлическую ампулу поместили 94 г фенола, 240 г перфторкетона и 100 г фтороводорода, плотно закрыли и нагрели в течение 10 часов при 95°С. Фтороводород отогнали и твердый бисфенольный продукт очистили перекристаллизацией из толуола и хлороформа. В результате выделили чистый бисфенол (2,2-бис[4-гидроксифенил]4,7,9,11-тетраокса-1,1,1,3,3,5,5,6,6,8,8,10,10,12,12,12- гексадекафтордодекан) с 89% выходом. Структура соединения была подтверждена методом спектроскопии ЯМР F19.
В четырехгорлую колбу, снабженную мешалкой, обратным холодильником, капельной воронкой и термометром, поместили раствор 39,2 г бисфенола и 0,1 г NaNO2 в 130 мл ледяной уксусной кислоты. К раствору при 40-45°С добавили раствор азотной кислоты и 20 мл ледяной уксусной кислоты. По окончании прибавления реакционную массу нагревали в течение 2-х часов при 60°С, и затем 3 часа при 80°С. Добавили воду, и образовавшееся масло красно-желтого цвета отделили, растворили в толуоле и высушили над MgSO4. Толуол упарили при 200-300 мм рт.ст. на водоструйном насосе. Получили 54,7 г (выход 81,1%) бисаминофенола (2,2-бис[3-нитро-4-гидроксифенил]4,7,9,11-тетраокса-1,1,1,3,3,5,5,6,6,8,8,10,10,12,12,12-гексадекафтордодекан).
В четырехгорлую колбу, снабженную мешалкой, обратным холодильником, капельной воронкой и термометром, поместили раствор бисаминофенола в 100 мл этанола и добавили 1,5 г катализатора (5% платина на углероде). При перемешивании добавили 12 г 100% перекиси водорода и смесь кипятилась с обратным холодильником в течение 4 часов. Реакционную массу охладили, катализатор отфильтровали и разбавили тремя объемами воды. Водный раствор подкислили уксусной кислотой до рН ниже 6. Выпавший в осадок продукт отфильтровали, высушили на воздухе и перекристаллизовали из этилацетата. Получили 45,7 г (91,0%) чистого бисаминофенола (2,2-бис[3-амино-4-гидроксифенил]4,7,9,11-тетраокса-1,1,1,3,3,5,5,6,6,8,8,10,10,12,12,12- гексадекафтордодекан), т.п. 142єС. Структура соединения была подтверждена методом спектроскопии ЯМР F19.
ПРИМЕР 2
При получении производных на основе бисаминофенола, таких как в Примере 1, также применялся другой метод синтеза перфторкетона, основанный на применении магнийорганического соединения, и который заключался в конденсации трифторметилмагнийиодида с перфторалканоилгалогенидом. Этот синтез описан в J.Am.Chem.Soc, pp. 1273-77 (1954):
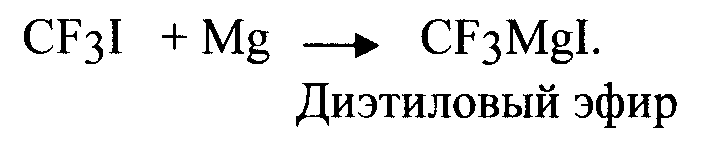
Колбу, содержащую 28,8 г Mg и несколько кристалликов иода нагревали при перемешивании при 60°С пока цвет йода не исчез. Колбу охладили до комнатной температуры и добавили 300 мл диэтилового эфира. Колбу охладили до -40°С и по каплям в течение 3 часов добавили 19,0 г CF3I, в результате получили раствор, содержащий 8,8 г (40% выход) CF3MgI. Температуру подняли до 30°С и при перемешивании в течение часа добавили 3,5,7-триокса-2,2,4,4,6,6,8,8,8-нонафтороктаноилхлорид. После дополнительных 7 часов перемешивания при комнатной температуре перегонкой при пониженном давлении (т.к. 1°С при 15 мм рт.ст.) был выделен перфторкетон (4,6,8-триокса-1,1,1,3,3,5,5,7,7,9,9,9-додекафторнонан-2-он). Структура соединения была подтверждена методом спектроскопии ЯМР F19. Из этого перфторкетона в несколько стадий, описанных в Примере 1, может быть получен бисаминофенол (2,2-бис[3-амино-4-гидроксифенил]4,6,8-тетраокса-1,1,1,3,3,5,5,7,7,9,9,9-
додекафторнонан), имеющий температуру плавления 115°С.
ПРИМЕР 3
Моноамидины были получены в соответствии с методом, являющимся частью изобретения, следующим образом. В четырехгорлую колбу, снабженную мешалкой, обратным холодильником, капельной воронкой и термометром, поместили 41,1 г (0,01 моль) сухого C7F15COOH и смешали с 32,0 г метанола и 19 мл концентрированной H2SO4. Реакционную массу кипятили в течение 6 часов, затем промыли водой и высушили над MgSO4. Полученный сложный эфир перегнали (Ткип=158°С). В соответствии с методикой, опубликованной в патенте US №2570116 (1951) выход составил 90-95% (39,2 г). Далее, в четырехгорлую колбу, снабженную мешалкой, обратным холодильником, термометром и трубкой для подачи газа, поместили 39,2 г
C7F15COOCH3 и 100 мл диэтилового эфира. Дополнительно, через колбу, охлаждаемую льдом, пропускали аммиак до тех пор, пока в эфирном растворе не исчез
С7F15СООСН3 (контролировали по ГЖХ). Этиловый эфир отогнали, твердый продукт высушили на воздухе. Получили 37,0 г C7F15CONH2 (выход 97,9%), Ткип=90°С. В круглодонную колбу, снабженную обратным холодильником, поместили 37,0 г растертого в мелкий порошок C7F15CONH2 (0,0896 моль) и 63,6 г Р2O5. При тщательном перемешивании смесь нагревали при 100-200°С, используя обратный холодильник. Получили 30,1 г
C7F15-CN (выход 85%), Ткип=90°С.
Схема реакции представлена ниже:
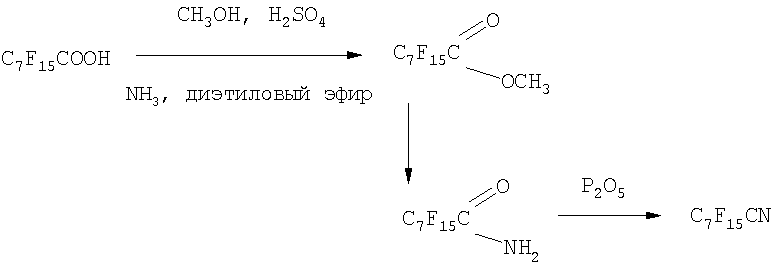
Такое терминально нитрил-замещенное соединение затем было переведено в моноамидин по методике, описанной ниже в Примере 4.
ПРИМЕР 4
Десятикратный избыток безводного аммиака (50 мл) конденсировали в четырехгорлой колбе, снабженной мешалкой, обратным холодильником, капельной воронкой, термометром и трубкой с осушителем (КОН), охлаждающей баней со смесью этанола и сухого льда. Аммиак конденсировался в колбу через трубку с осушителем. При хорошем перемешивании и охлаждении в колбу медленно добавили 60 г перфторгептанонитрила, полученного по методике, описанной в Примере 4 для превращения перфторкислоты в нитрил, имеющий формулу C7F13CN. По окончании прибавления, температуру медленно подняли до комнатной температуры для испарения избытка аммиака. Остаток, представляющий собой твердое вещество белого цвета, высушили на воздухе и получили 62,0 г перфторгептанамидина следующей структуры (выход 98,5%, т.п. 75-76°С):
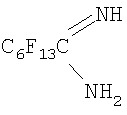
УФ-спектр продукта продемонстрировал характерную полосу поглощения амидиновой группы 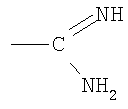 при 212 нм с коэффициентом затухания ε=6098.
при 212 нм с коэффициентом затухания ε=6098.
ПРИМЕР 5
В этом разделе описывается методика приготовления различных перфторэластомерных композиций на основе перфторэластомера, представляющих собой тетраполимеры, полученные периодической полимеризацией в водной эмульсии, как подробно описано в патентной заявке WO 00/08076, приведенной здесь в виде ссылки. Мономеры, входящие в состав тетраполимера включают тетрафторэтилен, перфторметилвиниловый эфир и два функциональных сшивающих мономера: вторичный нитрилсодержащий сшивающий мономер CF2=CFO(CF2)3OCF(CF3)CN и первичный нитрилсодержащий сшивающий мономер CF2=CFOCF2CF(CF3)O(CF2)2CN. Полимеризации проводили в водной эмульсии, содержащей 1,1,2-трихлор-1,2,2-трифторэтан, в присутствии инициатора окислительно-восстановительной реакции - персульфата аммония или композиции персульфата аммония с сульфитом натрия. Поверхностно-активная смесь включала перфторгептаноат и перфторнонаноат аммония. В качестве буфера использовали К2НРО4. Тетраполимеры были выделены коагуляцией хлоридом магния, промыты горячей водой и спиртом и высушены при 60°С. Структура соединения была подтверждена методом спектроскопии ЯМР F19 и элементным анализом на углерод и фтор. Вязкость по Муни измеряли при 100°С на вискозиметре TechPro® viscTECH TPD-1585. На основе вышеописанного метода и композиции были получены следующих четыре тетраполимера:
Полимер А: окисл.-восст. тип, вязкость по Муни 45.
Полимер В: не окисл.-восст., вязкость по Муни 65.
Полимер С: не окисл.-восст., вязкость по Муни 64.
Полимер D: не окисл.-восст., вязкость по Муни 93.
К вышеперечисленным полимерам, использованным в этих смесях, были добавлены различные вулканизирующие агенты и комбинации вулканизирующих агентов, включая: перфторсебацамидин и перфтороктанамидин, оба приобретены в компании SynQuest Laboratories, Inc., Флорида, а также перфторсуберамидин и перфторгептанамидин (получены из ФГУП Института синтетического каучука им. С.В.Лебедева, Россия). В различных композициях в качестве добавки также использовалось перфторуглеродное эфирное масло, было получено из DuPont Specialty Chemicals, Вилмингтон, Делавер. Стандартный ВОАР (2,2-бис[3-амино-4-гидроксифенол]гексафторпропан) был закуплен в TCI, Америка, Портленд, Орегон. Оба бисаминофенольных вулканизирующих агента, использованных в смесях (вулканизирующие агенты А и В) были получены из ФГУП Института синтетического каучука им. С.В.Лебедева, Россия. Вулканизирующие агенты А и В имели следующие структуры: (2,2,-бис[3-амино-4-гидроксилфенол]R). В соединении A, R означает -CF2(OCF2)3OCF3, вулканизирующий агент А имеет температуру плавления 120°С и молекулярную массу 630 дальтон. В соединении В, R означает -CF2OCF2CF2(OCF2)2OCF3, его температура плавления примерно от 142 до 145°С и молекулярная масса 680 дальтон. В эти смеси был добавлен углерод, а именно углерод технический N990.
Образцы для испытаний были получены путем смешения тетраполимера с вулканизирующими агентами для получения перфторэластомерной композиции и добавления углерода при помощи закрытого резиносмесителя Brabender (емкостью
100 г или 600 г). Смеси формировали в кольца круглого сечения, которые затем вулканизировали при прессовании и затем поствулканизировали, получая таким образом кольцевые изделия размером 214 в соответствии с условиями, приведенными в таблицах ниже. Кольца были протестированы на растяжение с помощью методики В ASTM-D-412, и были зафиксированы следующие параметры: Тb (растяжение на разрыв в МПа); Еb (удлинение на разрыв в %); и М100 (модуль упругости при растяжении на 100% в МПа). Остаточная деформация при сжатии была определена в соответствии с ASTM-D-395, Метод В. Характеристики вулканизации были зафиксированы на приборе Monsanto MDR 2000 при следующих условиях:
Были зафиксированы следующие параметры вулканизации: МH (максимальный крутящий момент в Нм); ML (минимальный крутящий момент в Нм); tS2 (время в минутах, затрачиваемое на повышение ML на 0,23 Нм); и tC90 (время в минутах, затрачиваемое на достижение 90% МH).
В Таблицах 3 и 4 (Образцы №1-12) приведены данные по использованию новых вулканизирующих агентов, вулканизирующих агентов А и В; использованию новых ускорителей вулканизации на основе амидинов и бисамидинов для этих вулканизирующих агентов и также стандартного агента ВОАР, и включают использование ВОАР в отдельности в качестве стандартного образца (Образец №11). Композиции включают тетраполимер, один из полимеров A-D, углерод технический N990 и Fluorogard PCA. В Таблице 4 показаны вулканизирующие характеристики (кроме указанных), полученные при помощи MDR, 1 ч при 160°С. В Таблице 3 обозначены рецептуры, и Таблица 4 включает данные, полученные на основании этих рецептур. В Таблице 5 приведены данные, демонстрирующие эффективность действия бисамидинов и моноамидинов данного изобретения в качестве вулканизирующих агентов (Образцы №13-19). Каждая из этих композиций основывалась на полимере А и включала Fluorogard PCA и технический углерод N990 в качестве добавок. В каждом из образцов 13-19 были смешаны 100 рhr (частей на 100 частей полимера) Полимера А с 25 phr технического углерода N990 и 1,5 phr Fluorogard PCA в качестве добавок. Результаты экспериментов, в которых варьировалась концентрация вулканизирующих агентов, приведены в Таблице 5 для каждой перфторэластомерной композиции. В Таблице 5 используется параметр G, который представляет собой последовательность условий поствулканизации и включает: повышение температуры от 25°С до 94°С в течение 1,5 ч и затем до 149°С в течение 1 часа. Температура поствулканизации 149°С поддерживается в течение 0,5 ч и далее поднимается до 204°С в течение 1 часа и поддерживается в течение 18 часов. Затем температуру повышают до 260°С в течение часа и поддерживают ее еще 18 часов. Затем температуру понижают до 25°С в течение двух часов.
В Таблицах 6 и 7 приведены рецептуры и результаты экспериментов, в которых бисамидины и моноамидины, соответственно, использовались в качестве ускорителей вулканизации перфторэластомерных композиций, содержащих А вулканизирующий агент ВОАР. Образцы № 20-30 содержали по 100 phr полимера А, В и D, 25 phr технического углерода N990, 1,5 phr Fluorogard PCA и различные количества ВОАР и амидинов. Эти данные демонстрируют ускоряющее воздействие разработанных в изобретении ускорителей на основе амидина на процесс вулканизации.
Ґ 2,27 ммоль
Ј 3,2 ммоль
α 2,8 ммоль
N2
N2
N2
Как видно из приведенных данных, новые вулканизирующие агенты, описанные в Примерах, обеспечивают физические свойства, сходные с полученными при обычном использовании ВОАР, но поскольку они характеризуются более низкими температурами плавления и большей совместимостью вулканизирующих агентов А и В и быстродействующими вулканизирующими агентами и ускорителями на основе амидинов, то ускорители вулканизации и вулканизирующие агенты, описанные в данном изобретении, обеспечивают большую скорость и более надежную вулканизацию перфторированных полимеров, приводящую к получению перфторированных эластомеров.
ПРИМЕР 6
Дополнительные образцы были приготовлены с использованием полимеров, имеющих те же мономеры, как и в Примере 5, однако в данном примере полимеры представляли собой смеси молекулярных цепей полимера В (упомянутых выше в Примере 5), имеющие две различные молекулярные массы. Эти композиции показаны ниже в таблице 8. Полимеры были полимеризованы одним и тем же способом; вязкость по Муни измерялась при температуре 100°С с помощью вискозиметра TechPro® viscTECH TPD-1585. К вышеупомянутым полимерам, применяемым в этих композициях, добавлялся гептафторбутириламидин в качестве вулканизатора и ускорителя вулканизации. Гептафторбутириламидин был приобретен у лаборатории SynQuest Laboratories, Inc., Alachua, Florida. Все остальные компоненты соответствуют описанным выше в Примере 5.
Образцы для испытаний были приготовлены путем смешения тетраполимера и вулканизаторов для образования перфторэластомерной композиции с добавлением к этой композиции углерода с помощью резиносмесителя Брабендер. После смешения этой массы из нее формовали кольцевые заготовки и подвергали их прессованию для получения уплотнительных элементов, затем подвергали их поствулканизации, чтобы получить кольца круглого сечения размером 214 в соответствии с условиями вулканизации и поствулканизации, представленными ниже в таблице 9. Испытание колец на растяжение производилось согласно стандарту ASTM-D-412, метод В; при этом регистрировались следующие параметры: ТВ (предел прочности на разрыв в МПа); ЕВ (относительное удлинение в % при разрыве); и М100 (модуль в МПа при относительном удлинении 100%). Остаточная деформация образцов колец круглого сечения при сжатии определялась согласно стандарту ASTM-D-395, метод В. Характеристики отверждения измерялись с помощью прибора Monsanto MDR 2000 при следующих условиях:
Таблица 9 содержит данные, иллюстрирующие влияние моноамидина, упомянутого в качестве вулканизатора для перфторэластомерной композиции и в качестве ускорителя вулканизации для перфторэластомерной композиции, содержащей ВОАР. В образцах №№ 31-34 композиции полимера В, каждая из которых включала в себя 100 phr полимера и 25 phr технического углерода N990 и ВОАР, как представлено в таблице 8, подвергались вулканизации и/или ускорению вулканизации амидином, как указано. Данные в таблице 8 выражены в частях на 100. Образец №31 является контрольным. В таблице 9, для данных по остаточной деформации при сжатии, результаты измерений в процентах отображают процентное отклонение; при этом данные основаны на образцах, подвергнутых поствулканизации. Эти данные демонстрируют вулканизирующий и ускоряющий эффект амидиновых ускорителей вулканизации в данном изобретении
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕРФТОРЭЛАСТОМЕР, ВУЛКАНИЗУЕМЫЙ ПЕРОКСИДНЫМ СПОСОБОМ, СМЕСЬ, СОДЕРЖАЩАЯ ПЕРФТОРЭЛАСТОМЕР, И ПРОМЫШЛЕННОЕ ИЗДЕЛИЕ | 2002 |
|
RU2296774C2 |
| НИЗКОТЕМПЕРАТУРНЫЕ ФТОРУГЛЕРОДНЫЕ ЭЛАСТОМЕРЫ | 1999 |
|
RU2261871C2 |
| ВУЛКАНИЗУЕМАЯ ФТОРЭЛАСТОМЕРНАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2152962C1 |
| ВУЛКАНИЗУЕМЫЙ ФТОРЭЛАСТОМЕР, СМЕСЬ, СОДЕРЖАЩАЯ ПЕРФТОРЭЛАСТОМЕР, И ПРОМЫШЛЕННОЕ ИЗДЕЛИЕ | 2002 |
|
RU2301235C2 |
| ФТОРПОЛИМЕРНЫЕ КОМПОЗИЦИИ | 2003 |
|
RU2332427C2 |
| ПЕРФТОРЭЛАСТОМЕРНЫЕ ГЕЛИ | 2005 |
|
RU2394043C2 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ФТОРЭЛАСТОМЕРНЫХ СОПОЛИМЕРОВ | 1993 |
|
RU2133761C1 |
| ФТОРОПЛАСТОВЫЕ ПОЛИМЕРЫ, ИМЕЮЩИЕ АЗОТСОДЕРЖАЩИЕ ЦЕНТРЫ ВУЛКАНИЗАЦИИ | 2003 |
|
RU2337112C2 |
| Фториодированные соединения для фторполимеров | 2013 |
|
RU2645156C2 |
| ВУЛКАНИЗУЕМАЯ ФТОРЭЛАСТОМЕРНАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2158281C2 |
Описан способ получения вулканизирующего агента, способного вулканизировать или ускорять вулканизацию перфторэластомерной композиции, включающий: (а) взаимодействие органической перфторалкилкислоты со спиртом с образованием сложного перфторалкилэфира; (b) взаимодействие сложного перфторалкилэфира с аммиаком с образованием фторсодержащего алкилкарбоксиамида; (с) взаимодействие фторсодержащего алкилкарбоксиамида с дегидратирующим агентом с образованием фторсодержащего алкилнитрила; и (d) взаимодействие фторсодержащего алкилнитрила с, по меньшей мере, аммиаком или амином с получением фторсодержащего амидина - вулканизирующего агента. Также описан способ получения вулканизирующего агента на основе бисаминофенола, где бисаминофенольный вулканизирующий агент способен вулканизировать перфторэластомерную композицию и способ получения вулканизирующего агента на основе дифенильного соединения, который имеет формулу (III):
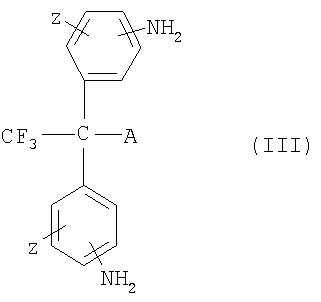
где Z означает амино-, сульфгидрильную или гидроксильную группу и А выбрано из группы, состоящей из незамещенных и замещенных групп, с разветвленной и линейной цепью на основе углерода, причем группы на основе углерода выбирают из группы, состоящей из перфторалкильных и перфторалкокси групп, содержащих от 1 до примерно 22 атомов углерода; где бисаминофенильный вулканизирующий агент способен вулканизировать перфторэластомерную композицию. 3 н. и 6 з.п. ф-лы, 9 табл.
1. Способ получения вулканизирующего агента, способного вулканизировать или ускорять вулканизацию перфторэластомерной композиции, включающий:
(a) взаимодействие органической перфторалкилкислоты со спиртом с образованием сложного перфторалкилэфира;
(b) взаимодействие сложного перфторалкилэфира с аммиаком с образованием фторсодержащего алкилкарбоксиамида;
(c) взаимодействие фторсодержащего алкилкарбоксиамида с дегидратирующим агентом с образованием фторсодержащего алкилнитрила и
(d) взаимодействие фторсодержащего алкилнитрила с, по меньшей мере, аммиаком или амином с получением фторсодержащего амидина - вулканизирующего агента.
2. Способ по п.1, где вулканизируемая перфторэластомерная композиция содержит, по меньшей мере, один функциональный сшивающий мономер, содержащий нитрильную группу.
3. Способ по п.1, где в качестве вулканизирующего агента получают перфторгептанамидин.
4. Способ по п.1, где фторсодержащий алкилнитрил добавляют к избытку аммиака или амина.
5. Способ по п.4, где, по меньшей мере, аммиак или амин представляет собой жидкий аммиак, и избыток этого жидкого аммиака является десятикратным.
6. Способ получения вулканизирующего агента на основе бисаминофенола, где бисаминофенольный вулканизирующий агент способен вулканизировать перфторэластомерную композицию, включающий:
(a) взаимодействие перфторацилфторида с фторидом калия с образованием продукта реакции алкоголята калия;
(b) взаимодействие продукта реакции алкоголята калия с перфтораллилфторсульфатом с образованием перфтораллилового эфира;
(c) взаимодействие перфтораллилового эфира с окислителем с образованием перфторглицидилового эфира;
(d) взаимодействие перфторглицидилового эфира с хлоридом алюминия во фторированном растворителе для изомеризации эпоксидной группы перфторглицидилового эфира в кетон;
(e) взаимодействие кетоновой группы с фенолом в присутствии фтористого водорода с образованием соединения на основе бисфенола;
(f) нитрование соединения на основе бисфенола с получением соединения на основе биснитрофенола и
(g) восстановление соединения на основе биснитрофенола с образованием бисаминофенольного вулканизирующего агента.
7. Способ по п.6, где вулканизируемая перфтороэластомерная композиция содержит, по меньшей мере, один функциональный сшивающий мономер, содержащий нитрильную группу.
8. Способ получения вулканизирующего агента на основе дифенильного соединения, который имеет формулу (III):
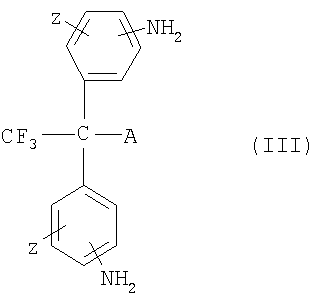
где Z означает амино-, сульфгидрильную или гидроксильную группу;
и А выбрано из группы, состоящей из незамещенных и замещенных групп, с разветвленной и линейной цепью на основе углерода, причем группы на основе углерода выбирают из группы, состоящей из перфторалкильных и перфторалкокси групп, содержащих от 1 до примерно 22 атомов углерода, где бисаминофенильный вулканизирующий агент способен вулканизировать перфторэластомерную композицию, включающий
(a) взаимодействие перфторацилфторида с фторидом калия для образования продукта реакции алкоголята калия;
(b) взаимодействие продукта реакции алкоголята калия с перфтораллилфторсульфатом с образованием перфтораллилового эфира;
(c) взаимодействие перфтораллилового эфира с окислителем с образованием перфторглицидилового эфира;
(d) взаимодействие перфторглицидилового эфира с хлоридом алюминия во фторированном растворителе для изомеризации эпоксидной группы перфторглицидилового эфира в кетон;
(e) взаимодействие кетона с фенилом, замещенным группой Z, в присутствии фтористого водорода с образованием дифенильного соединения;
(f) нитрование дифенильного соединения с получением соединения на основе биснитрофенила и
(g) восстановление соединения на основе биснитрофенила с образованием бисаминофенильного вулканизирующего агента.
9. Способ по п.8, где А содержит от 3 до 10 атомов углерода.
| US 6281296 B1, 28.08.2001 | |||
| Химическая энциклопедия, "Большая Российская энциклопедия" | |||
| - М., 1998, т.1, с.127, кол | |||
| Канальная печь-сушильня | 1920 |
|
SU230A1 |
| Химическая энциклопедия, "Большая Российская энциклопедия" | |||
| - М., 1992, т.3, с.261, кол | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРОДУКТОВ КОНДЕНСАЦИИ ФЕНОЛОВ С ФОРМАЛЬДЕГИДОМ ИЛИ ЕГО ПОЛИМЕРАМИ | 1925 |
|
SU513A1 |
| Химическая энциклопедия, "Большая Российская энциклопедия" | |||
| - М., 1999, т.5, с.509, кол | |||
| СПОСОБ ОБРАБОТКИ БУМАГИ ДЛЯ ТЕЛЕГРАФНЫХ ЛЕНТ С ЦЕЛЬЮ МНОГОКРАТНОГО ИСПОЛЬЗОВАНИЯ ИХ | 1923 |
|
SU1010A1 |
| УСТРОЙСТВО ДЛЯ ИСПОЛЬЗОВАНИЯ ЭНЕРГИИ МОРСКИХ ВОЛН | 1923 |
|
SU1011A1 |
| US 4144221 А, | |||
Авторы
Даты
2010-01-27—Публикация
2004-01-29—Подача