Область техники, к которой относится изобретение
Настоящее изобретение в основном относится к пиперидинзамещенным индолам или их гетеропроизводным, а также к их применению в качестве модуляторов активности хемокиновых рецепторов, к фармацевтическим композициям, содержащим эти соединения, и к способам их применения в качестве агентов для лечения и профилактики воспалительных заболеваний, таких как астма и аллергические заболевания, а также для лечения и профилактики аутоиммунных патологий, таких как ревматоидный артрит и атеросклероз.
Предшествующий уровень техники
Хемокины представляют собой хемотаксические цитокины с молекулярной массой 6-15 кДа, которые высвобождаются из многих клеток для того, чтобы привлекать и активировать, в частности, такие клетки, как макрофаги, Т и В лимфоциты, эозинофилы, базофилы и нейтрофилы (см. обзоры: Luster, New Eng, J. Med., т.338, сс.436-445 (1998), Rollins, Blood, т.90, сс.909-928 (1997)).
Существуют два основных класса хемокинов, СХС и СС, название которых определяется тем, являются ли первые два цистеиновых остатка (С) в аминокислотной последовательности разделенными одним аминокислотным остатком (СХС) или расположены рядом (СС). СХС хемокины, такие как интерлейкин-8 (IL-8), нейтрофил-активирующий белок-2 (NAP2) и белок - стимулятор активности роста меланомы (MGSA) являются хемотаксичными прежде всего в отношении нейтрофилов и Т лимфоцитов, в то время как СС хемокины, такие как RANTES, MIP-1a, MIP-1 (3, моноцитные хемотаксические белки (МСР-1, МСР-2, МСР-3, МСР-4 и МСР-5) и эотаксины (-1, -2 и -3) вызывают хемотаксис других клеток, в частности клеток таких типов как макрофаги, Т лимфоциты, эозинофилы, дендритные клетки и базофилы. Также существуют хемокины - лимфотактин-1, лимфотактин-2 (оба - С хемокины) и фракталкин (СХХХС хемокин), которые не входят в основные подсемейства хемокинов.
Хемокины связываются со специфическими рецепторами поверхности клетки, которые относятся к семейству сопряженных белков, имеющих семь трансмембранных доменов и сопряженных с G-белком (обзор см.: Horuk, Trends Pharm. Sci., т.15, сс.159-165 (1994)), которые называют "хемокиновыми рецепторами". Посредством связывания со своими когнатными лигандами хемокиновые рецепторы передают внеклеточный сигнал через ассоциированные тримерные G белки, что приводит, наряду с другими откликами, к быстрому росту концентрации кальция внутри клетки, изменению формы клетки, увеличению выделений молекул клеточной адгезии, дегранулированию и стимулированию миграции клеток. Существует по меньшей мере десять хемокиновых рецепторов человека, которые связываются с СС хемокинами или реагируют на СС хемокины, типичными являются следующие: CCR1 (или"СКR-1"или"СС-СКR-1") [MIP-1a, МСР-3, МСР-4, RANTES] (Ben-Barruch, и др., Cell, т.72, сс.415-425 (1993), Luster, New Eng. J. Med., т.338, сс.436-445 (1998)); CCR-2A и CCR-2B (или "CKR-2A"/"CKR-2B", или"СС-СКR-2А"/"СС-CKR-2B") [МСР-1, MCP-2, МСР-3, МСР-4, МСР-5] (Charo и др., Рrос.Natl. Acad. Sci. USA, т.91. сс.2752-2756 (1994), Luster, New Eng. J. Med., т.338, сс.436-445 (1998)); CCR-3 (или "СКR-3" или "СС-СКR-3") [эотаксин-1, эотаксин-2, RANTES, МСР-3, МСР-4] (Combadiere, и др., J. Biol. Chem., т.270, сс.16491-16494 (1995), Luster, New Eng. J. Med., т.338, сс.436-445 (1998)); CCR-4 (или"СКR-4", или"СС-СКR-4") [TARC, MIP-la, RANTES, MCP-1] (Power и др., J. Biol. Chem., т.270, cc.19495-19500 (1995), Luster, New Eng. J. Med., т.338, сс.436-445 (1998)); CCR-5 (или "СКR-5", или "CCCKR-5") [MIP-1a, RANTES, MIP-1p] (Sanson, и др., Biochemistry, т.35, сс.3362-3367 (1996)); CCR-6 (или "CKR-6", или "CC-CKR-6") [LARC] (Baba и др., J. Biol. Chem., т.272, сс.14893-14898 (1997)); CCR-7 (или"СКR-7", или"СС-СКR-7") [ELC] (Yoshie и др., J. Leukoc. Biol., т.62, сс.634-644 (1997)); CCR-8 (или "СКR-8", или "СС-СКR-8") [1-309, TARC, MIP-lp] (Napolitano и др., J. Immunol, т.157, cc.2759-2763 (1996), Bernardini и др., Eur. J. Immunol, т.28, cc. 582-588 (1998)); и CCR-10 (или "СКR-10", или "СС-СКR-10") [MCP-1, МСР-3] (Bonini и др., DNA and Cell Biol., т.16, cc.1249-1256 (1997)).
Было показано, что в дополнение к хемокиновым рецепторам млекопитающих цитомегаловирусы, вирусы герпеса и поксвирусы (вирусы группы оспы) экспрессируют в инфицированных клетках белки, обладающие способностью связываться таким же образом, как и хемокиновые рецепторы (см. обзор: Wells и Schwartz, Curr. Opin. Biotech., т.8, cc.741-748 (1997)). CC хемокины человека, такие как RANTES и МСР-3, могут вызывать быструю иммобилизацию кальция посредством таких кодированных вирусом рецепторов. Инфицирование может допускать синтез рецепторов, учитывая изменение контроля нормальной иммунной системы и реакцию на инфекцию. Дополнительно, хемокиновые рецепторы человека, такие как CXCR-4, CCR-2, CCR-3, CCR-5 и CCR-8, могут работать как сорецепторы в случае инфицирования клеток млекопитающих микробами, например, такими как вирус иммунодефицита человека (HIV).
Хемокиновые рецепторы рассматривают как имеющие большое значение медиаторы воспалительных, инфекционных и иммунорегуляторных нарушений, расстройств и заболеваний, включая астму и аллергические заболевания, а также аутоиммунные патологии, такие как ревматоидный артрит и атеросклероз. Например, хемокиновый рецептор CCR-3 играет центральную роль в привлечении эозинофилов в зоны аллергического воспаления и в последующей активации этих клеток. Хемокиновые лиганды рецептора CCR-3 индуцируют быстрый рост внутриклеточной концентрации кальция, увеличивают выделение молекул клеточной адгезии, дегрануляцию клеток и стимулирование миграции эозинофилов. В соответствии с этим агенты, которые являются модуляторами хемокиновых рецепторов, могли бы быть полезны при таких нарушениях, расстройствах и заболеваниях. В дополнение, агенты, которые являются модуляторами хемокиновых рецепторов, могли бы быть полезны при инфекционных заболеваниях, например, посредством блокирования инфицирования CCR-3 экспрессирующих клеток вирусом иммунодефицита человека (ВИЧ) или предотвращения воздействия на иммунные отклики клеток таких вирусов, как цитомегаловирусы.
Предшествующий уровень техники
В патенте US 5521197 описаны пиперидин-замещенные индолы в качестве агонистов 5-HT1F.
В опубликованной международной патентной заявке WO 98006402 раскрыто применение этих соединений для лечения простуды или аллергического ринита.
В опубликованной международной патентной заявке WO 98011895 описаны эти соединения, предназначенные для лечения мигрени.
Аналогичные соединения описаны в опубликованной международной патентной заявке WO 2001043740, эти соединения также применяют в качестве модуляторов 5-НТ.
В опубликованной международной патентной заявке WO 2002008223 описаны пиперидинзамещенные индолы, присоединенные к арильным кольцам, замещенным пептидами, в качестве D4 - модуляторов, но также и с частичным воздействием на
5-HT2A или 5-НТ2C рецепторы.
В опубликованной международной патентной заявке WO 99037304 описаны замещенные производные пиперидина и пиперазина, предназначенные для ингибирования фактора ХA.
В опубликованной международной патентной заявке WO 2000075130 описаны производные индоилпиперидинов в качестве противоастматических и противоаллергических агентов, что включает лечение бронхиальной астмы.
Проблема, на решение которой направлено настоящее изобретение, заключается в разработке новых модуляторов хемокинового рецептора CCR-3. Неожиданно было обнаружено, что некоторые пиперидинзамещенные индолы весьма подходят в качестве модуляторов хемокинового рецептора CCR-3.
Краткое описание сущности изобретения
В соответствии с этим целью настоящего изобретения являются новые пиперидинзамещенные производные индола или их гетеропроизводные формулы 1:

в которой R1, R5, R6, А, В, D-E, X-W-V, Y, i, j и m являются такими, как указано ниже.
Другой целью настоящего изобретения является получение агонистов, или антагонистов рецепторов CCR-3, или фармацевтически приемлемых солей этих соединений, в частности получение фармацевтических композиций, включающих фармацевтически приемлемый носитель и терапевтически эффективное количество по меньшей мере одного из соединений согласно настоящему изобретению или фармацевтически приемлемой соли такого соединения. Эти и другие задачи будут более понятны из приведенного ниже подробного описания настоящего изобретения.
Подробное описание изобретения
Настоящее изобретение относится к соединениям формулы 1,
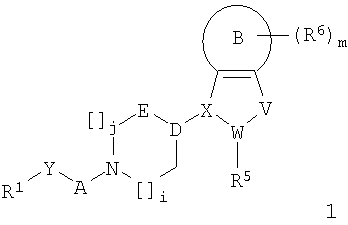
в которой
R1 представляет собой арил, гетероциклил или аннелированные фрагменты на их основе, где гетероциклил представляет собой гетероциклический фрагмент и аннелированные фрагменты включают аннелированный арилгетероциклил, аннелированный гетероциклиларил или аннелированный гетероциклилгетероциклил, каждый из указанных арилов или гетероциклилов может быть замещенным одним, двумя или тремя радикалами R2;
R2 каждый независимо означает (С1-С6)алкил, (С3-С6)циклоалкил, (С1-С6)галогеноалкил, (С1-С6)аралкил, галоген, CN, COOR3, COR3, CONR3R4, NR3R4, NR3SO2R4, OR3, NO2, SR3, SOR3, SO2R3 или SO2NR3R4;
R3 представляет собой Н, (С1-С6)алкил, (С3-С8)циклоалкил или (С3-8-циклоалкил)-(С1-С6)алкил;
R4 представляет собой Н, (С1-С6)алкил, (С3-С8)циклоалкил или (С3-С8)циклоалкил-(С1-С6)алкил или
R3 и R4 вместе с расположенным между ними атомом азота или группой N-SO2- образуют необязательно замещенную азотсодержащую гетероциклическую 3-8-членную кольцевую систему,
R5 представляет собой (С1-С6)алкил, (С1-С6)алкокси, (С1-С6)ацилокси, (С1-С6)аралкил, (С3-С6)циклоалкил, (С3-С6циклоалкил)-(С1-С6)алкил, (С1-С6)галогеноалкил, (С1-С6)тиоалкил, галоген, NO2, CN;
R6 каждый независимо означает (С1-С6)алкил, (С1-С6)алкокси, (С1-С6)ацилокси, (С1-С6)аралкил, (С3-С6)циклоалкил, (С1-С6)галогеноалкил, (С1-С6)тиоалкил, галоген, OR3, SR3, CN, NO2, COOR3, COR3, CONR3R4, NR3R4, NR3COR4, NR3SO2R4, SOR3, SO2R3, SO2NR3R4, арил или гетероциклил;
А представляет собой (С3-С6) циклоалкил-(С2-С8)алкилен, (С2-С8)алкилен с линейной или разветвленной цепью, необязательно замещенный галогеном или группой ОН;
В представляет собой арил или гетероциклил;
D-E представляет собой СН-СН2- или С=СН;
X-W-V представляет собой N-C=CR7 или C=C-NR7;
R7 представляет собой Н или (С1-С6)алкил;
Y представляет собой CF2, NR4, O, S(O)n;
i, j каждый независимо означает 0, 1 или 2;
n означает 0, 1 или 2;
m означает 0, 1, 2, 3 или 4;
и к их фармацевтически приемлемым солям.
Соединения, описанные в тексте настоящей заявки, могут содержать асимметрические центры. Соединения согласно настоящему изобретению, в которых имеется какой-либо асимметрически замещенный атом, могут быть выделены в оптически активной или рацемической форме. Из предшествующего уровня техники хорошо известно, как получить оптически активные формы, например, посредством разделения рацематов или посредством синтеза из оптически активных исходных соединений. Геометрическая изомерия олефинов и соединений подобного типа также может иметься в соединениях, которые описаны в тексте настоящей заявки, и все такие стабильные изомеры входят в объем настоящего изобретения. Цис- и транс- геометрические изомеры соединений согласно настоящему изобретению описаны и могут быть выделены как смесь изомеров, так и отдельные изомерные формы. Все хиральные, диастереомерные, рацемические формы и все геометрические изомеры предлагаемой структуры входят в объем настоящего изобретения, если специально не указана конкретная стереохимия или изомерная форма.
Термины и определения
Термины, для которых в тексте настоящей заявки не приводится специальное определение, следует рассматривать в таком значении, в котором специалист в данной области техники рассматривает этот термин, с учетом описания настоящего изобретения и контекста. Тем не менее, при использовании в тексте настоящей заявки, если не указано иное, приведенные ниже термины используются в указанном значении и используются следующие обозначения.
При указании групп, радикалов или фрагментов, определение которых приводится ниже, количество атомов углерода часто указывается перед названием группы, например, (С1-С6)алкил означает алкильную группу или алкильный радикал, содержащие от 1 до 6 атомов углерода. Как правило, в случае групп, включающих две или несколько подгруппы, группа, указанная последней, является местом присоединения радикала, например, "тиоалкил" означает моновалентный радикал формулы HS-Alk-. Если ниже специально не указано иное, то при указании всех формул и групп предполагаются общепринятые обозначения и термины.
Как правило, при указании химической структуры или соединения допускаются все таутомерные формы и изомерные формы и смеси, такие как индивидуальные геометрические изомеры, или оптические изомеры, или рацемические, или нерацемические смеси изомеров, если только конкретная стереохимия или конкретная изомерная форма специально не приводится в наименовании или структуре соединения.
Термин "замещенный" при использовании в тексте настоящей заявки, означает, что один или несколько атомов водорода у указанного атома замещается с возможностью выбора из указанной группы, при условии, что не превышается нормальная валентность указанного атома и что введение такого заместителя приводит к получению стабильной структуры.
Фраза "фармацевтически приемлемые" используется в тексте настоящей заявки для обозначения таких соединений, веществ, материалов, композиций и/или дозированных форм, которые в рамках медицинского заключения подходят для применения в контакте с тканями организма человека или животного и не обладают чрезмерной токсичностью, не вызывают раздражение, аллергические реакции и не создают другие проблемы или осложнения, несоразмерные с обоснованным соотношением пользы и риска.
При использовании в тексте настоящей заявки термин «фармацевтически приемлемые соли» относится к производным указанных соединений, где исходное соединение модифицируют посредством получения его соли с кислотой или основанием. Примеры фармацевтически приемлемых солей включают, но не ограничиваются указанным, минеральные или органические соли с кислотами, образованные остатками основного характера, например, с участием аминогрупп; щелочные или органические соли остатков кислотного характера, таких как включающие группы карбоновых кислот, и т.п. Фармацевтически приемлемые соли включают общеизвестные нетоксичные соли или четвертичные аммониевые соли исходных соединений, образованные, например, с нетоксичными неорганическими или органическими кислотами. Например, такие общеизвестные нетоксичные соли включают такие соли, полученные с использованием неорганических кислот, например, таких как хлороводородная кислота, бромоводородная кислота, серная кислота, сульфаминовая кислота, фосфорная кислота, азотная кислота и т.п.; и соли, полученные с использованием органических кислот, например, таких как уксусная кислота, пропионовая кислота, янтарная кислота (бутандикислота), гликолевая кислота, стеариновая кислота, молочная кислота, яблочная кислота, винная кислота, лимонная кислота, аскорбиновая кислота, 4,4'-метиленбис(3-гидрокси-2-нафтойная кислота), малеиновая кислота, гидроксималеиновая кислота, фенилуксусная кислота, глутаминовая кислота, бензойная кислота, салициловая кислота, сульфаниловая кислота, 2-ацетоксибензойная кислота, фумаровая кислота, толуолсульфоновая кислота, метансульфоновая кислота, этандисульфоновая кислота, щавелевая кислота, изотионовая кислота и т.п.
Фармацевтически приемлемые соли согласно настоящему изобретению могут быть получены общепринятыми химическими методами, исходя из соединений, которые содержат фрагмент основной или кислотной природы. Как правило, такие соли могут быть получены посредством взаимодействия соединения в виде свободной кислоты или свободного основания со стехиометрическим количеством соответствующего основания или кислоты в воде, или в среде органического растворителя, или в смеси двух, как правило, неводных сред, предпочтительно таких как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечень подходящих солей можно найти в руководстве Remington, такие соли высвобождают активное исходное соединение in vivo, в том случае, когда такое пролекарство вводят пациенту - млекопитающему. Пролекарства согласно настоящему изобретению получают посредством модификации функциональных групп, присутствующих в соединении, таким образом, чтобы модифицирующая группа отщеплялась, либо при обычных манипуляциях, либо in vivo, с образованием при этом целевого соединения. Пролекарства включают соединения согласно настоящему изобретению, в которых гидроксигруппа, аминогруппа или сульфгидрильная группа присоединены к какой-либо другой группе, которая в том случае, когда пролекарство согласно настоящему изобретению вводят пациенту - млекопитающему, отщепляется с образованием при этом свободной гидроксигруппы, аминогруппы или сульфгидрильной группы соответственно. Примеры пролекарств включают, но не ограничиваются указанным, ацетат-, формиат- и бензоатпроизводные функциональных спиртовых групп и аминогрупп соединений согласно настоящему изобретению.
Термин "арил" при использовании в тексте настоящей заявки или по отдельности, или в комбинации с другим заместителем означает либо ароматическую моноциклическую систему, либо ароматическую мультициклическую систему, содержащую атомы углерода. Например, арил включает фенильную или нафтильную кольцевую систему, где арил означает, как правило, ароматическую систему, например фенил.
Термин "гетероциклил" при использовании в тексте настоящей заявки или по отдельности, или в комбинации с другим заместителем означает моновалентный заместитель, полученный в результате удаления водорода из пяти-, шести- или семичленного насыщенного или ненасыщенного (включая ароматический) гетероцикла, содержащего атомы углерода и один, два, три или четыре гетероатома, входящих в кольцо, выбранные из азота, кислорода и серы. Примеры подходящих гетероциклов включают тетрагидрофуран, тиофен, диазепин, изоксазол, пиперидин, диоксан, морфолин, пиперазин или
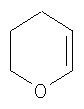
Хотя термин "гетероарил" подпадает под термин "гетероциклил", при использовании в тексте настоящей заявки "гетероарил" строго означает ненасыщенный гетероцикл, в котором двойные связи образуют ароматическую систему. Подходящие примеры гетероароматической системы включают пиридин, пиримидин,
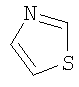 ;
; 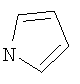 ;
; 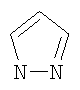 ;
; 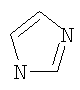 ;
;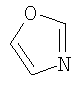 ;
; 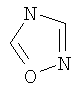 или
или 
Термин "аннелированные фрагменты на основе арила или гетероциклила" при использовании в тексте настоящей заявки или по отдельности, или в комбинации с другим заместителем, где присутствуют аннелированные фрагменты в виде арил-гетероциклила (а), гетероциклил-арила (б) или гетероциклил-гетероциклила (в),означает моновалентный заместитель, получаемый при удалении одного атома водорода из:
а) ароматической моноциклической системы или ароматической мультициклической системы, содержащей атомы углерода, которая является аннелированной с пяти-, шести- или семичленным насыщенным или ненасыщенным (включая ароматический) гетероциклом, содержащим атомы углерода и один, два, три или четыре гетероатома, входящих в кольцо, выбранные из азота, кислорода и серы, или
б) пяти-, шести- или семичленного насыщенного или ненасыщенного (включая ароматический) гетероцикла, содержащего атомы углерода и один, два, три или четыре гетероатома, входящие в кольцо, выбранные из азота, кислорода и серы, который является аннелированным с ароматической моноциклической системой или ароматическими мультициклическими системами, содержащими атомы углерода, или
в) пяти-, шести- или семичленного насыщенного или ненасыщенного (включая ароматический) гетероцикла, содержащего атомы углерода и один, два, три или четыре гетероатома, входящие в кольцо, выбранные из азота, кислорода и серы, который является аннелированным с пяти-, шести- или семичленным насыщенным или ненасыщенным (включая ароматический) гетероциклом, содержащим атомы углерода и один, два, три или четыре гетероатома, входящие в кольцо, выбранные из азота, кислорода и серы.
Подходящие примеры аннелированных фрагментов на основе арила или гетероциклила включают хинолинил, 1-индоил, 3-индоил, 5-индоил, 6-индоил, индолизинил, бензимидазил или пуринил.
Термин "галоген" при использовании в тексте настоящей заявки означает заместитель - галоген, выбранный из фтора, хлора, брома или иода.
Термин "-(С1-С6)алкил" при использовании в тексте настоящей заявки либо по отдельности, либо в комбинации с другим заместителем означает ациклический, алкильный заместитель с линейной или разветвленной цепью, содержащий от одного до шести атомов углерода, и включает, например, метил, этил, пропил, бутил, гексил, 1-метилэтил, 1-метилпропил, 2-метилпропил или 1,1-диметилэтил.
Термин "-(С3-С8)циклоалкил" при использовании в тексте настоящей заявки либо по отдельности, либо в комбинации с другим заместителем означает циклоалкильный заместитель, содержащий от трех до шести атомов углерода, и включает циклопропил, циклобутил, циклопентил или циклогексил.
Термин "-(C1-С6)галогеноалкил" при использовании в тексте настоящей заявки или по отдельности или в комбинации с другим заместителем означает ациклический, алкильный заместитель с линейной или разветвленной цепью, содержащий до шести атомов углерода, причем один или несколько атомов водорода замещены на атом галогена, выбранный из брома, хлора, фтора или иода. В соответствии с этим "-(С2-С6)-галогеноалкил" имеет то же самое значение, с тем исключением, что цепь содержит от двух до шести атомов углерода. Предпочтительно термин (С1-С6)галогеноалкил означает (С1-С6)-фторалкил, например, такой как трифторметил, 2,2,2-трифторэтил или перфторэтил.
Термин "-(С1-С6)алкокси" при использовании в тексте настоящей заявки или по отдельности, или в комбинации с другим заместителем означает заместитель (С1-С6)алкил-O-, где алкил является таким, как определено выше, и содержит до шести атомов углерода. Алкокси включает метокси, этокси, пропокси, 1-метилэтокси, бутокси или 1,1-диметилэтокси. Последний заместитель, как известно, обычно называют трет-бутокси.
Термин "-(С1-С6)ацилокси" при использовании в тексте настоящей заявки или по отдельности, или в комбинации с другим заместителем означает заместитель (С1-С6)алкил-(СО)O-, где алкил является таким, как определено выше, и содержит до шести атомов углерода. Ацилокси включает МеСОО-, EtCOO-, н-PrСОО-, изо PrСОО-, н-BuСОО-, втор-BuCOO- или трет-BuСОО-.
Термин "-(С1-С6)аралкил" при использовании в тексте настоящей заявки или по отдельности, или в комбинации с другим заместителем означает заместитель -арил -(С1-С6)алкил, где алкил является таким, как определено выше, и содержит до шести атомов углерода. Аралкил включает бензил, фенилэтил, фенилпропил, 1-фенил-1-метилэтил, фенилбутил или 1-фенил-1,1-диметилэтокси.
Термин "-(С1-С6)тиоалкил" при использовании в тексте настоящей заявки или по отдельности, или в комбинации с другим заместителем означает ациклический, алкильный заместитель с линейной или разветвленной цепью, содержащий до шести атомов углерода и тиольную (HS) группу в качестве заместителя. Примером тиоалкильной группы служит тиопропил, например HS-CH2CH2CH2-.
Термин "-С2-С8-алкилен" при использовании в тексте настоящей заявки означает бивалентный алкильный заместитель, полученный при удалении одного атома водорода с каждого конца алифатического углеводорода с линейной или разветвленной цепью, который содержит от двух до восьми атомов углерода и включает, например, СН2СН2С(СН3)2СН2СН2-. В соответствии с этим "-(С1-С3)алкилен" имеет то же самое значение, с тем исключением, что цепь содержит от одного до трех атомов углерода.
Предпочтительные варианты осуществления изобретения
Предпочтительными являются соединения формулы 1, где Y представляет собой S или S=O, и R1, R5, R6, А, В, D-E, X-W-V, i, j и m являются такими, как указано выше. Особенно предпочтительными являются соединения формулы 1а или 1б:
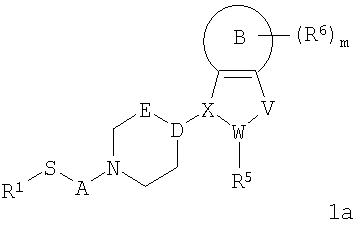
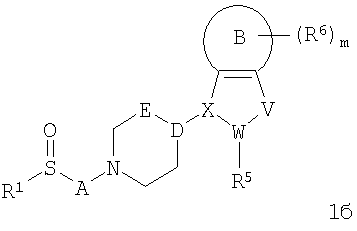
где R1, R5, R6, А, В, D-E, X-W-V и m являются такими, как указано выше. Также предпочтительными являются соединения формулы 1, 1а или 1б, где:
R1 представляет собой арил или гетероциклил, оба из которых
необязательно замещены одним, двумя или тремя радикалами R2 и
В означает фенил.
Также предпочтительными являются соединения формулы 1, 1а или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2 и
В означает фенил.
Также предпочтительными являются соединения формулы 1, 1а или 1б, где:
В означает фенил и
D-E представляет собой СН-СН2-.
Также предпочтительными являются соединения формулы 1, 1а или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2 и
В означает фенил,
D-E означает СН-СН2-.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E означает СН-СН2- и
А означает СН2-СН2-СН2-.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E означает СН-СН2- и
А означает С(СН3)2-СН2-СН2-.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2 и
В означает фенил,
D-E означает СН-СН2-,
A означает 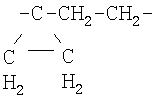 .
.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E означает СН-СН2-,
А представляет собой 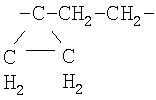 и
и
R7 означает Н.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E означает СН-СН2-,
A означает 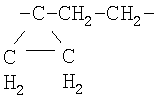 и
и
R7 означает Me.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил, и
D-E означает С=СН-.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя
радикалами R2,
В означает фенил,
D-E означает С=СН- и
А означает СН2-СН2-СН2-.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E означает С=СН- и
А означает С(СН3)2-СН2-СН2-.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E означает С=СН- и
A означает 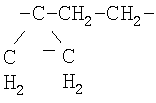
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E означает С=СН-
A означает  и
и
R7 означает Н.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2,
В означает фенил,
D-E представляет собой С=СН-,
А представляет собой 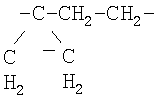 и
и
R7 представляет собой Me.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где
R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2 и
R2 каждый независимо означает COOR3, COR3, СОNR3R4, NR3SO2R4, SOR3, SO2R3 или SO2NR3R4; в частности COOR3 или SO2R3;
R3 представляет собой Н или (С1-С6)алкил; в частности Н или метил;
R4 представляет собой Н или (С1-С6)алкил; в частности Н или метил.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где
R1 означает фенил, необязательно замещенный одним радикалом R2 и R2 представляет собой
COOR3 или SO2R3;
R3 представляет собой Н или метил;
R4 означает Н или метил.
Также предпочтительными являются соединения формулы 1, 1a или 1б, где:
R5 представляет собой (С1-С6)алкил, (С3-С6)циклоалкил или (С2-С6)галогеноалкил; или
R2 представляет собой СF3 или галоген, в частности фтор; или
R6 предпочтительно представляет собой галоген, в частности фтор. Также предпочтительным является способ получения соединений формулы 1 или 1а, отличающийся тем, что соединение формулы 2:

подвергают взаимодействию с соединением формулы 3:

где R1, R5, R6, А, В, X-W-V, i, j и m являются такими, как указано выше, и
LG представляет собой подходящую отщепляемую группу, в частности галоген, мезилат, трифлат, тозилат или брозилат.
Соединения формулы 1 или 1а могут быть получены с использованием реакций и методов, описанных ниже. Взаимодействие проводят в среде растворителя, который подходит для используемых веществ и реагентов и пригоден для эффективного осуществления превращения. Специалисту в области органического синтеза будет понятно, что функциональные группы, имеющиеся в молекуле, должны быть совместимыми с условиями осуществления предполагаемого превращения. Это иногда может потребовать изменения порядка проведения стадий синтеза или предпочтительного выбора конкретной схемы осуществления способа, для того чтобы получить целевое соединение согласно настоящему изобретению. Необходимо также отметить, что другим важным условием планирования синтеза является разумный выбор защитной группы, используемой для защиты реакционно-способных функциональных групп, имеющихся в соединениях, описанных в тексте настоящей заявки. Авторитетным источником, в котором описано множество альтернатив для специалиста в области органической химии, является руководство: Greene, Wuts (Protective Groups In Organic Synthesis, Wiley and Sons, 1991).
Соединения согласно настоящему изобретению пригодны для получения лекарственного средства для профилактики и/или лечения заболеваний, опосредованных активностью CCR-3-рецептора.
Предпочтительным является получение лекарственного средства для профилактики и/или лечения широкого круга воспалительных, инфекционных и иммунорегуляторных нарушений, расстройств и заболеваний, включая астму и аллергические заболевания, инфицирование патогенными микробами (которые, по определению, включают вирусы), а также включая аутоиммунные патологии, такие как ревматоидный артрит и атеросклероз.
Наиболее предпочтительным является получение лекарственного средства для профилактики и/или лечения, например, воспалительных или аллергических заболеваний и состояний, включая респираторные аллергические заболевания, такие как астма, аллергический ринит, заболевания, связанные с гиперчувствительностью легкого, аллергический пневмонит, эозинофильный целлюлит (эозинофильное воспаление рыхлой клетчатки) (например, синдром Велла), эозинофильная пневмония (например, синдром Леффлера (Loeffler), хроническая эозинофильная пневмония), атонический (эозинофильный) фасциит (например, синдром Шульмана), аллергия замедленного типа, интерстициальный легочный процесс (ИЛП) (например, идиопатический (неясного происхождения) легочный фиброз) или ИЛП, связанный с ревматоидным артритом, системная красная (системная эритематозная) волчанка, анкилозирующий спондилит, системный склероз, синдром Шегрена, полимиозит или дерматомиозит; общая анафилактическая реакция или аллергические реакции, лекарственная аллергия (например, к пенициллину, цефалоспоринам), эозинофильно-миалгический синдром вследствие приема пищи, загрязненной триптофаном, аллергическая реакция на укус насекомого; аутоиммунные заболевания, такие как ревматоидный артрит, псориатический артрит, рассеянный склероз, системная красная (системная эритематозная) волчанка, астенический бульбарный паралич (бульбоспинальный паралич), юношеский диабет; гломерулонефрит, аутоиммунный тиреоидит, синдром Бехчета; отторжение трансплантата (например, при трансплантации), включая отторжение аллотрансплантата или реакция трансплантат против хозяина; воспалительные заболевания кишечника, такие как болезнь Крона (гранулематозная болезнь) и язвенный колит; спондилоартрит; склеродерма; псориаз (включая псориаз, опосредованный Т-клетками) и воспалительные болезни кожи, такие как дерматит, экзема, атопический дерматит, аллергический контактный дерматит, крапивница; васкулит (воспаление стенок кровеносных сосудов) (например, некротизированный, кожный и аллергический васкулит); эозинофильный миозит, атонический (эозинофильный) фасциит; с лейкоцитарной инфильтрацией кожи или органов.
Синтез
Азотзамещенные соединения формулы 2а получают посредством восстановительной конденсации кольцевой структуры В, замещенной по меньшей мере одной функциональной аминогруппой и содержащей водород в орто-положении, с функциональной кетогруппой защищенного азацикла:
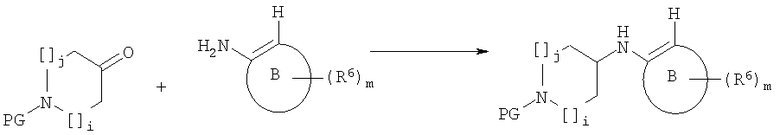
После конденсации атом водорода замещают ацилированием по Фриделю-Крафтсу с использованием производного α-галоген-ацетилгалогенида или замещенного α-галоген-ацетонитрила и затем подвергают гидролизу с образованием при этом α-кетосоединения:
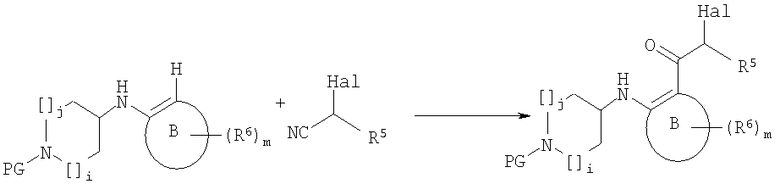
(Hal означает Сl или Вr). После ацилирования проводят замыкание кольца в присутствии кислоты:

где значения R5, R6, В, i, j и m на всех стадиях способа являются такими, как указано выше, и
PG представляет собой защитную группу для азота, предпочтительно бензильную группу.
Замещенные по углероду соединения формулы 2в или 2г получают посредством С-С конденсации в условиях реакции Бухвальда (Buchwald) кольцевой структуры В, замещенной по меньшей мере одной функциональной нитрогруппой и галогеном орто-положении, с α-С-атомом функциональной кетогруппы:
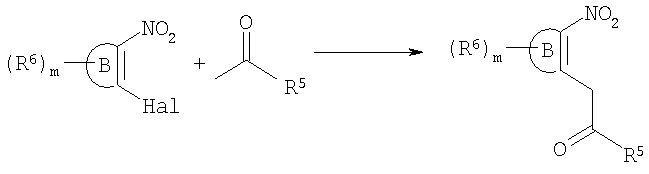
(Hal означает Cl или Вr). После реакции конденсации проводят замыкание кольца в восстановительных условиях:

Затем осуществляют конденсацию вновь образовавшегося кольца с функциональной кетогруппой азацикла в присутствии кислоты:

с последующим, в случае соединения 2 г, гидрированием двойной связи азацикла:
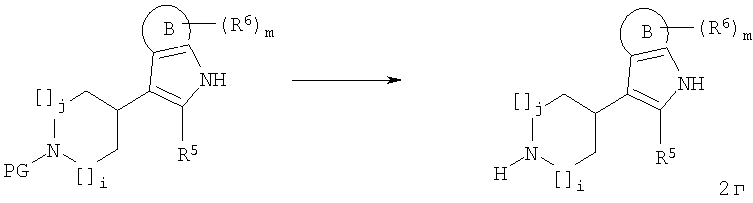
где на всех стадиях способа R5, R6, В, D-E, i, j и m являются такими, как указано выше.
Соединения формул 1б-г могут быть получены взаимодействием соединений 2б-г с соединением формулы 3:
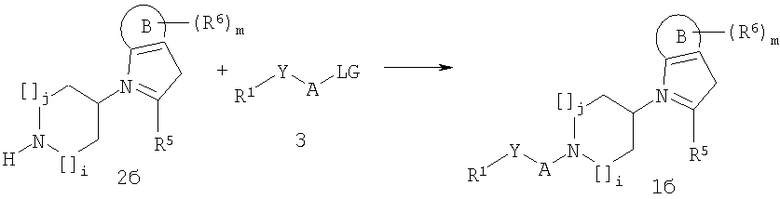
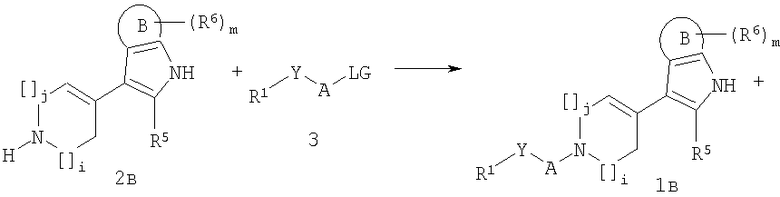
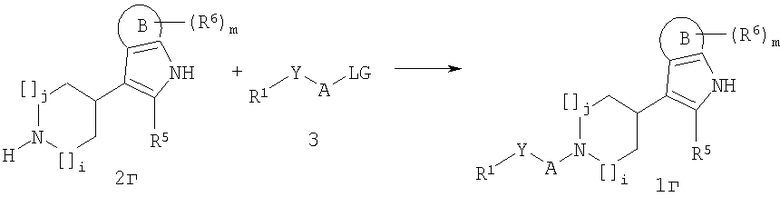
где R1, R5, R6, А, В, Y, i, j и m являются такими, как указано выше; и
LG представляет собой подходящую отщепляемую группу, в частности галоген, мезилат, трифлат, тозилат или брозилат.
N-Метилированные соединения формул 1д или 1е могут быть получены осредством метилирования соединений 1в или 1г.
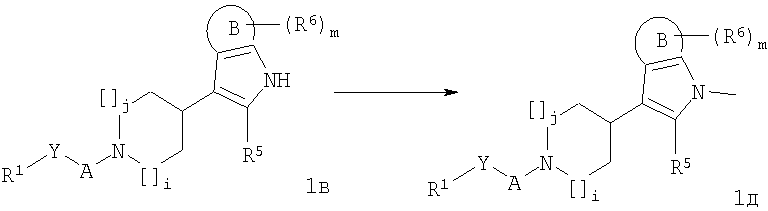
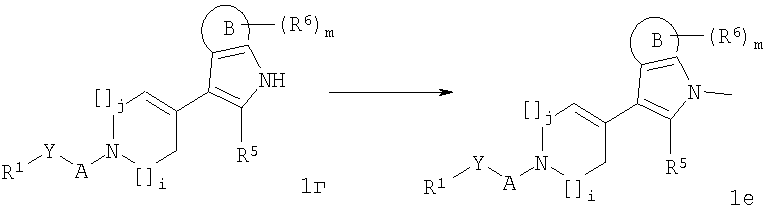
где R1, R5, R6, А, В, Y, i, j и m являются такими, как указано выше.
Как будет понятно специалисту в данной области техники, возможны многочисленные модификации и варианты настоящего изобретения, выполняемые в соответствии с изложенным выше. Таким образом, необходимо понимать, что в объеме, определяемом прилагаемой формулой изобретения, настоящее изобретение может быть осуществлено и иначе, чем, в частности, описано в тексте настоящей заявки.
Пример 1
1-(3-Бромпропилсульфанил)-4-фторбензол
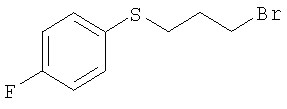
К раствору n-фтортиофенола (20,8 мл) и 1-3-дибромпропана (60 мл) в ацетонитриле (250 мл) добавляют К2СО3 (55,0 г) небольшими порциями и полученную смесь кипятят с обратным холодильником в течение 3 часов. Затем полученную соль и растворитель удаляют, продукт перегоняют. Т. кип. 112-115°С/1 мбар.
Пример 2
(1-Бензилпиперидин-4-ил)-(4-фторфенил)амин

Раствор 4-фторанилина (32,7 г), N-бензилпиперидинона (106,0 г) и уксусной кислоты (106,0 г) в 1,2-дихлорэтане (1200 мл) охлаждают до температуры ниже 15°С. К перемешиваемому раствору постепенно добавляют суспензию уксусной кислоты (495,0 г) и боргидрид натрия (31,2 г). Через 2 часа перемешивания при 15°С и дополнительно 2 часа при комнатной температуре растворитель удаляют в вакууме. Добавляют этилацетат (500 мл) и воду (700 мл) при перемешивании и реакционную смесь нейтрализуют карбонатом натрия (приблизительно 250 г). Органическую фазу отделяют, промывают 2 М раствором NaHCO3 (100 мл) и водой (100 мл) и высушивают, используя сульфат натрия. После удаления растворителя и перекристаллизации из эфира/петролейного эфира получают 53,8 г продукта в виде оранжевых кристаллов, т.пл.90-92°С.
Пример 3
1-[2-(1-Бензилпиперидин-4-иламино)фенил]-2-хлорбутан-1-он
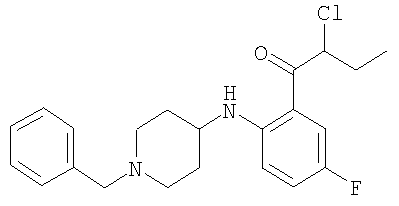
(1-Бензилпиперидин-4-ил)-(4-фторфенил)амин (51,2 г) растворяют в 180 мл бензола и охлаждают на ледяной бане. Добавляют по каплям трихлорид бора (180 мл, 1 М раствор в гексане) в течение 30 минут. Добавляют 2-хлорбутиронитрил (18,6 г) и алюминийтрихлорид (24,0 г) и полученную смесь кипятят с обратным холодильником в течение 15 ч. Затем полученную смесь охлаждают, добавляют 180 мл 2 н. раствора НСl и полученную смесь дополнительно кипятят с обратным холодильником. Добавляют 200 мл воды и 200 мл СН2Сl2 и затем полученную смесь доводят до значения рН5, добавляя порциями карбонат натрия. Фазы разделяют, органическую фазу высушивают, используя сульфат натрия, и затем растворитель удаляют. Полученное маслянистое вещество очищают колоночной экспресс-хроматографией (CH2Cl2:MeOH в соотношении 96:4). Выход составляет 20,7 г бесцветного маслянистого вещества.
1H ЯМР (300 Мгц, CDCl3): 1,10 (3Н, t), 1,62-1,79 (3Н, m), 2,01-2,36 (6H, m), 2,80-2,92 (2H, m), 3,43-3,57 (1H, m), 3,59 (2H, s), 5,03 (1H, dd), 6,75 (1H, dd), 7,16-7,22 (1H, m), 7,23-7,42 (4H, m), 7,43 (1H, dd), 8,92 (1H, br d).
Пример 4
1-(1-Бензилпиперидин-4-ил)-2-этил-5-фтор-1Н-индол
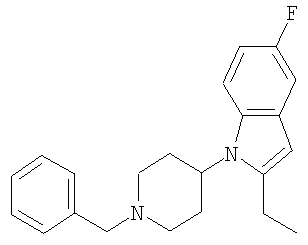
1-[2-(1-Бензилпиперидин-4-иламино)фенил]-2-хлорбутан-1-он (20,7 г) смешивают с 250 мл диоксана, 27 мл воды и 2,3 г боргидрида натрия и затем нагревают до 120°С. Через 12 часов кипячения с обратным холодильником добавляют дополнительно 3,3 г боргидрида натрия и полученную смесь кипятят с обратным холодильником дополнительно 16 ч. Затем удаляют растворитель, добавляют 200 мл воды и экстрагируют смесь, используя 150 мл CH2Cl2, затем высушивают над сульфатом натрия и концентрируют в вакууме. Полученное маслянистое вещество очищают колоночной экспресс-хроматографией (CH2Cl2:MeOH в соотношении 96:4). Выход составляет 11,9 г бледно-желтого маслянистого вещества.
1Н ЯМР (400 Мгц, ДМСО): 1,25 (3Н, t), 1,72 (2Н, br d), 2,19 (2H, br t), 2,39-2,48 (2H, m), 2,79 (2H, q), 2,98 (2H, br d), 3,59 (2H, s), 4,12-4,25 (1H, m), 6,19 (1H, s), 6,88 (1H, td), 7,19 (1H, dd), 7,21-7,31 (1H, m), 7,31-7,39 (4H, m), 7,49-7,52 (1H, m).
Пример 5
1-(Пиперидин-4-ил)-2-этил-5-фтор-1Н-индол
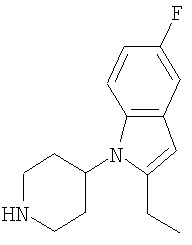
Раствор 1-(1-бензилпиперидин-4-ил)-2-этил-5-фтор-1Н-индола (11,9 г) и уксусной кислоты (4,1 мл) в метаноле (250 мл) гидрируют в течение 8 часов (50°С/1013 мбар). Полученную смесь затем отфильтровывают и концентрируют в вакууме. Добавляют CH2Cl2 (250 мл), NaHCO3 (100 мл) и воду (300 мл) и затем полученную смесь перемешивают в течение 10 минут. Органический слой экстрагируют, используя СНСl3, и затем высушивают (MgSO4) и концентрируют в вакууме. Перекристаллизацией из эфира/петролейного эфира получают 6,4 г чистого продукта (выход 73%) в виде бесцветных кристаллов.
1Н ЯМР (400 МГц, ДМСО): 1,25 (3Н, t), 1,65 (2Н, br d), 1,83 (1Н, s), 2,22-2,37 (2Н, m), 2,62 (2Н, td), 2,79 (2Н, q), 3,10 (2Н, br d), 4,20-4,31 (1Н, m), 6,18 (1Н, s), 6,83 (1Н, td), 7,19 (1Н, dd), 7,59-7,14 (1Н, m).
Пример 6
2-Этил-5-фтор-1-{1-[3-(4-фторфенилсульфанил)пропил] пиперидин-4-ил}-
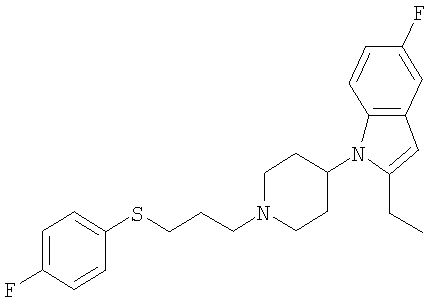
Смесь 1-(1-бензилпиперидин-4-ил)-2-этил-5-фтор-1Н-индола (2,4 г), 1-(3-бромпропилсульфанил)-4-фторбензола (2,4 г), ацетонитрила и карбоната калия нагревают при кипячении с обратным холодильником в течение 5 ч. Растворитель удаляют и полученное маслянистое вещество очищают колоночной экспресс-хроматографией (этилацетат : петролейный эфир в соотношении 1:1). Фракцию, содержащую продукт, вымораживают из растворителя и затем полученное маслянистое вещество перекристаллизовывают из этанола. Выход составляет 1,2 г (30%) бесцветных кристаллов.
Т.пл.: 82-84°С; 1Н ЯМР (300 МГц, CDCl3): 1,33 (3Н, t, J 7,5), 1,77-1,87 (4Н, m), 2,10 (2Н, td, J 12,5, J 2,5), 2.48-2.66 (4Н, m), 2,75 (2Н, q, J 7,5), 2,94-3,08 (4Н, m), 4,02-4,15 (1Н, m), 6,20 (1Н, s), 6,83 (1Н, td, J 9,5, J 2,5), 6,98-7,04 (2Н, m), 7,16 (1Н, dd, J 9,5, J 2,5), 7,36-7,40 (2Н, m), 7,47 (1Н, dd, J 9,0, J 4,0). 13C ЯМР (75 Мгц, CDCl3): 13,23, 21,12, 26,95, 30,62, 33,10, 53,88, 54,11, 57,10, 98,85, 104,70, 105,00, 108,12, 108,46, 112,07, 115,98. 116,27, 129,30, 132,22, 132,33, 144,20, 156,05, 159,15, 160,21, 163,48.
Пример 7
1-(2-Нитро-4-фторфенил)бутан-2-он

К раствору 1-бром-2-нитро-4-фторфенила (6,2 г), Pd2dba3 (260 мг), 2-дициклогексилфосфино-2'-(N,N-диметиламино)бифенила (455 мг), К3РO4 (13,7 г) и 4-метоксифенола (700 мг) в толуоле (60 мл) добавляют 2-бутанон (5,6 мл) и полученную смесь нагревают до 60°С в течение 24 часов в атмосфере аргона. Затем полученную смесь экстрагируют водой и этилацетатом (в соотношении 1:1) и промывают 2 М раствором NaOH и водой. Растворитель удаляют и оставшийся продукт очищают экспресс-хроматографией (циклогексен : этилацетат в соотношении 9:1), получая при этом 2,6 г (выход 44%) чистого продукта в виде светло-желтых кристаллов.
1Н ЯМР (400 МГц, ДМСО): 0,98 (3Н, t), 2,56 (2Н, q), 4,22 (2Н, s), 7,51 (1H, dd), 7,63 (1H, td), 7,98 (1H, dd).
Пример 8
2-Этил-6-фтор-1Н-индол
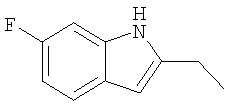
Раствор 1-(2-нитро-3-фторфенил)бутан-2-она (2,5 г) в этаноле (25 мл) нагревают до 70°С. Добавляют Na2S2O4 (10,7 г) в воде (30 мл) и полученную смесь нагревают при кипячении с обратным холодильником в течение 1 часа. Этанол удаляют перегонкой, полученный остаток экстрагируют два раза этилацетатом, затем органический слой промывают водой и высушивают. Растворитель удаляют и оставшийся продукт очищают от примесей экспресс-хроматографией (циклогексан : этилацетат в соотношении 9:1). Получают 1,3 г (выход 67%) чистого продукта в виде белого кристаллического твердого вещества.
1Н ЯМР (400 МГц, ДМСО): 1,26 (3Н, t), 2,72 (2Н, q), 6,12 (1H, s), 6,73-6,80 (1H, m), 7,02 (1H, br d), 7,37 (1H, dd), 10,98 (1H, br s).
Пример 9
2-Этил-6-фтор-3-(1,2,3,6-тетрагидропиридин-4-ил)-1Н-индол

К суспензии 2-этил-5-фтор-1Н-индола (1,2 г) в уксусной кислоте (21 мл) при 90°С добавляют смесь 4-пиперидона (3,4 г) и 2 н. фосфорной кислоты (7 мл). Реакционную смесь перемешивают при 95°С в течение 4 ч, затем добавляют воду (50 мл) и реакционной смеси дают охладиться до комнатной температуры. Значение рН доводят до 11 концентрированным раствором NaOH и затем полученную смесь экстрагируют этилацетатом. Промывают водой, высушивают над сульфатом магния и концентрируют в вакууме. Полученный остаток промывают (эфир) и высушивают на вакуумном фильтре, получая при этом 1,5 г (выход 84%) продукта в виде белого кристаллического твердого вещества. Т. пл. 194-6°С.
Пример 10
2-Этил-6-фтор-3-[1-(4-фторфенилсульфанилпропил)-1,2,3,6-тетрагидропиридин-4-ил]-1Н-индол
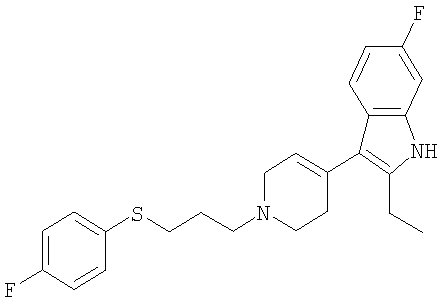
Раствор 2-этил-6-фтор-3-(1,2,3,6-тетрагидропиридин-4-ил)-1Н-индола (1,5 г), 1-(3-бромпропилсульфанил)-4-фторбензола (1,7 г), иодида калия (20 мг) и карбоната калия (1,1 г) в ДМФ (10 мл) нагревают при 95°С в течение 1 ч. Затем добавляют этилацетат (80 мл) и воду (35 мл) и органическую фазу дополнительно экстрагируют этилацетатом. Полученные экстракты промывают водой, высушивают (MgSO4) и концентрируют в вакууме. Неочищенный продукт очищают экспресс-хроматографией (СН2Сl2:МеОН в соотношении 100:2) и получают его соль - гидрохлорид взаимодействием в ацетоне с подходящим количеством эфирного раствора НСl, получая при этом 1,7 г чистого продукта (выход 55%) в виде белых кристаллов. Т.пл.135°С.
Пример 11
2-Этил-6-фтор-3-пиперидин-4-ил-1Н-индол
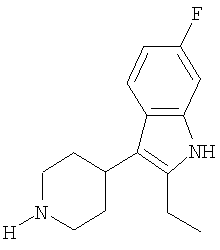
3-(1-Бензил-1,2,3,6-тетрагидропиридин-4-ил)-2-этил-6-фтор-1Н-индол (1,4 г) гидрируют в течение 1 часа (при комнатной температуре и давлении 1013 мбар) в присутствии катализатора - 10% Pd/C (0,3 г) и метанола (25 мл). Катализатор удаляют посредством фильтрации, растворитель упаривают и полученный остаток промывают небольшими порциями эфира. Получают 1,2 г (выход 85%) чистого продукта.
1Н ЯМР (400 Мгц, ДМСО): 1,20 (3Н, t), 1,52 (2Н, br d), 1,90-2,04 (2Н, m), 2,59-2,71 (4Н, m), 2,71-2,83 (1H, m), 3,07 (2Н, br d), 6,74 (1H, t), 6,99 (1H, d), 7,52-7,60 (1H, m), 10,72 (1H, br s).
Пример 12
2-Этил-6-фтор-3-{1-[3-(4-фторфенилсульфанил)пропил]пиперидин-4-ил}-1Н-индол
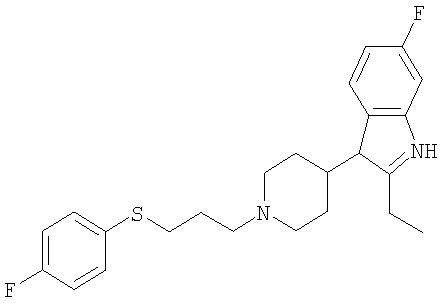
Смесь 2-этил-6-фтор-3-пиперидин-4-ил-1Н-индола (0,9 г), 1-(3-бром-пропилсульфанил)-4-фторбензола (1,0 г), иодида калия (20 мг) и карбоната калия (0,7 г) в ДМФ (10 мл) нагревают при 100°С в течение 3 ч и затем дают охладиться до комнатной температуры в течение ночи. Добавляют этилацетат (50 мл) и воду (25 мл) и затем органическую фазу промывают водой, высушивают и концентрируют в вакууме. Неочищенный продукт очищают экспресс-хроматографией (CH2Cl2:MeOH в соотношении 95:5) и получают его соль - гидрохлорид взаимодействием в ацетоне с подходящим количеством эфирного раствора НСl с получением при этом, после перекристаллизации из эфира, 1,1 г чистого продукта (выход 70%) в виде белых кристаллов.
1Н ЯМР (400 МГц, ДМСО): 1,19 (3Н, t), 1,75 (2Н, br d), 1,92-2,02 (2H, m), 2,35 (2H, br q), 2,59 (2H, q), 2,92-3,09 (5H, m), 3,10-3,20 (2H, m), 3,47 (2H, br d), 6,71-6,79 (1H, m), 7,01 (1H, dd), 7,22 (2H, br t), 7,44-7,49 (2H, m), 7,58-7,62 (1H, m), 10,87 (1H, br s).
Пример 13
2-Этил-6-фтор-3-{1-[3-(4-фторфенилсульфанил)пропил]пиперидин-4-ил}-1-метил-1Н-индол
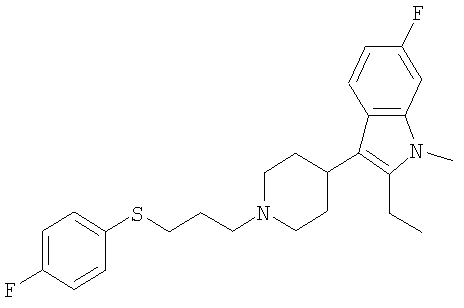
К раствору 2-этил-6-фтор-3-{1-[3-(4-фтор-фенилсульфанил)-пропил]пиперидин-4-ил}-1Н-индола (0,4 г) в ДМФ (5 мл) при 5°С добавляют гидрид натрия (0,1 г) и полученную смесь перемешивают в течение 15 мин при комнатной температуре. Затем полученную смесь охлаждают до 5°С, добавляют МеI (0,1 мл) и перемешивают смесь в течение 30 минут при комнатной температуре. Добавляют этилацетат (50 мл) и воду (50 мл), органический слой промывают водой, высушивают над MgSO4 и концентрируют в вакууме. Соль гидрохлорид получают взаимодействием в ацетоне с подходящим количеством эфирного НСl с получением при этом, после перекристаллизации из эфира, 0,2 г чистого продукта (выход 46%) в виде белых кристаллов.
1Н ЯМР (400 МГц, ДМСО): 1,12 (3Н, t), 1,74 (2H, br d), 1,92-2,01 (2H, m), 2,29-2,42 (2H, m), 2,78 (2H, q), 2,92-3,08 (5H, m), 3,10-3,17 (2H, m), 3,46 (2H, br d), 3,62 (3Н, s), 6,79 (1H, br t), 7,18-7,27 (3Н, m), 7,47 (2H, dd), 7,66 (1H, dd).
Примеры 14-17
2-Этил-6-фтор-3-{1-[3-(4-фторфенилсульфанил)пропил]-1,2,3,6-тетрагидропиридин-4-ил}-1-метил-1Н-индол
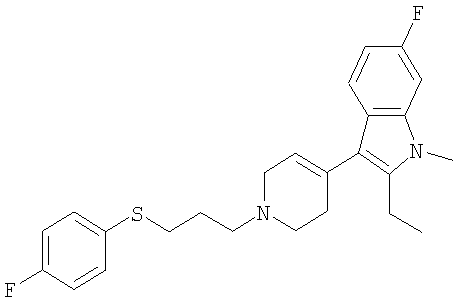
1Н ЯМР (400 МГц, ДМСО): 1,19 (3Н, t), 1,19-2,10 (2Н, m), 2,50-2,62 (1Н, m), 2,75-2,90 (3Н, m), 3,05 (2Н, t), 3,31-3,39 (3Н, m), 3,56-3,63 (1Н, m), 3,68 (3Н, s), 3,70-3,81 (1Н, m), 3,93-4,02 (1Н, m), 5,62 (1Н, br s), 6,86 (1Н, br t), 7,22 (2Н, t), 7,29 (1Н, dd), 7,45-7,50 (3Н, m).
2-Этил-5-фтор-1-1-(3-n-трифторметилфенилсульфанилпропил)пиперидин-4-ил]-1Н-индол
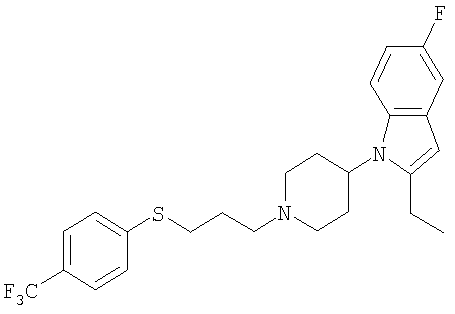
1H ЯМР (400 МГц, ДМСО): 1,25 (3Н, t), 1,90 (2Н, br d), 2,00-2,12 (2Н, m), 2,66-2,83 (4H, m), 2,99-3,23 (6H, m), 3,51 (2Н, br d), 4,47-4,60 (1Н, m), 6.20 (1Н, s), 6,83 (1Н, td), 7,21 (1Н, dd), 7,54 (2Н, dd), 7,62-7,70 (3Н, m).
2-Этил-5-фтор-1-{1-[3-(4-фторфенилсульфанил)-3-метил-бутил]пиперидин-4-ил}-1Н-индол
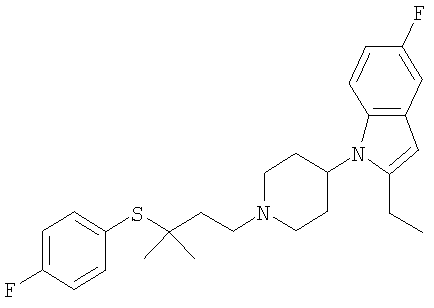
2-Этил-5-фтор-1-(1-{2-[1-(4-фторфенилсульфанил)циклопропил]этил}-пиперидин-4-ил)-1Н-индол

Примеры 18-20
2-Этил-6-фтор-3-[1-(3-n-трифторметилфенилсульфанилпропил)пиперидин-4-ил]-1Н-индол
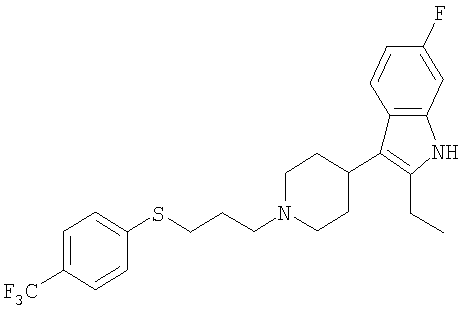
2-Этил-6-фтор-3-{1-[3-(4-фтор-фенилсульфанил)-3-метил-бутил]пиперидин-4-ил}-1Н-индол
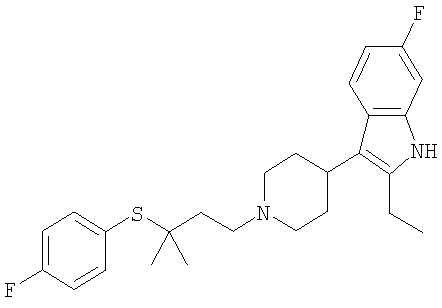
2-Этил-6-фтор-3-(1-{2-[1-(4-фтор-фенилсульфанил)циклопропил]-этил}-пиперидин-4-ил)-1Н-индол
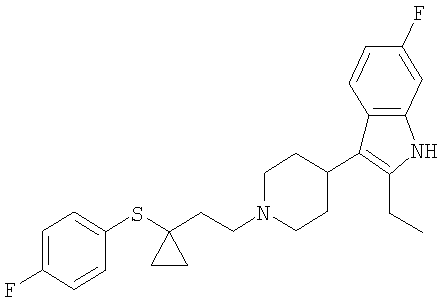
Примеры 21-23
2-Этил-6-фтор-1-метил-3-[1-(3-n-трифторметилфенилсульфанилпропил)-пиперидин-4-ил]-1Н-индол

2-Этил-6-фтор-3-{1-[3-(4-фторфенилсульфанил)-3-метилбутил]пиперидин-4-ил}-1-метил-1Н-индол

2-Этил-6-фтор-3-(1-{2-[1-(4-фтор-фенилсульфанил)циклопропил]этил}-пиперидин-4-ил)-1-метил-1Н-индол
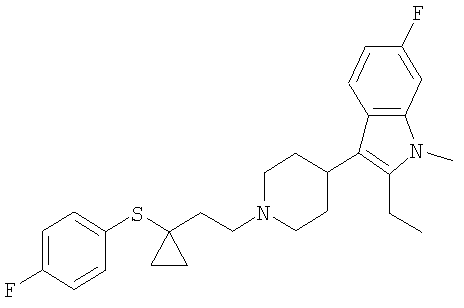
Примеры 24-26
2-Этил-6-фтор-3-[1-(3-n-трифторметилфенилсульфанилпропил)-1,2,3,6-тетрагидропиридин-4-ил]-1Н-индол

2-Этил-6-фтор-3-{1-[3-(4-фтор-фенилсульфанил)-3-метил-бутил]-1,2,3,6-тетрагидропиридин-4-ил}-1Н-индол

2-Этил-6-фтор-3-(1-{2-[1-(4-фторфенилсульфанил)циклопропил]этил}-1,2,3,6-тетрагидропиридин-4-ил)-1Н-индол
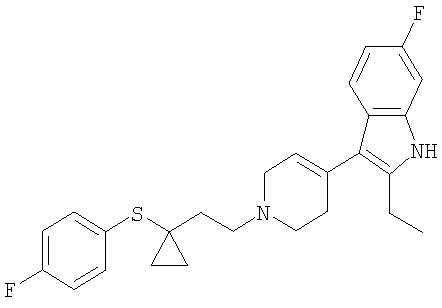
Примеры 27-29
2-Этил-6-фтор-1-метил-3-[1-(3-n-трифторметилфенилсульфанилпропил)-1,2,3,6-тетрагидропиридин-4-ил]-1Н-индол
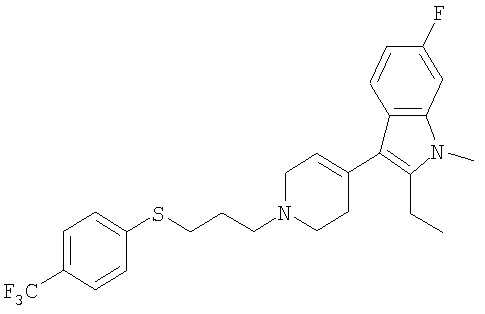
2-Этил-6-фтор-3-{1-[3-(4-фтор-фенилсульфанил)-3-метил-бутил]-1,2,3,6-тетрагидропиридин-4-ил}-1-метил-1Н-индол

2-Этил-6-фтор-3-(1-{2-[1-(4-фтор-фенилсульфанил)циклопропил]этил}-1,2,3,6-тетрагидропиридин-4-ил)-1 -метил-1Н-индол
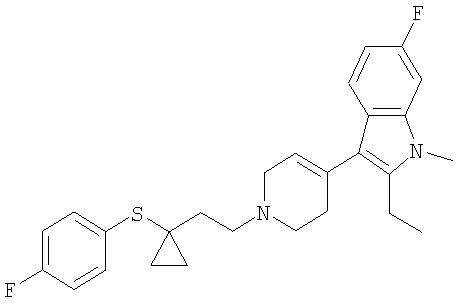
Примеры 30-37
3-{3-[4-(2-Этил-5-фториндол-1-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропилсульфанил}-[1,2,4]триазоло[4,3-а] пиридин
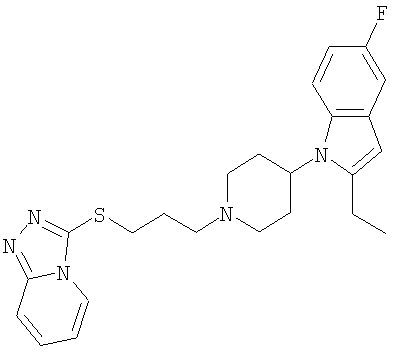
1Н ЯМР (400 МГц, ДМСО): 1,22 (3Н, t), 1,63 (2H, br d), 1,73-1,83 (2H, m), 1,98-2,11 (2H, m), 2,19-2,34 (2H, m), 2,43 (2H, t), 2,73 (2H, q), 2,83 (2H, br d), 3,15 (1H, t), 3,25-3,31 (1H, m), 4,08-4,19 (1H, m), 6,18 (1H, s), 6,86 (1H, td), 7,12 (1H, t), 7,17 (1H, dd), 7,37 (1H, dd), 7,42 (1H, dd), 7,82 (1H, d), 8,48 (1H, d).
2-{3-[4-(2-Этил-5-фториндол-1-ил)-3,6-дигидро-2Н-пиридин-1-ил]пропилсульфанил}тиазоло[5,4-b]пиридин

1H ЯМР (400 МГц, ДМСО): 1,25 (3Н, t), 1,75 (2H, br d), 1,97-2,08 (2H, m), 2,20-2,33 (2H, m), 2,41-2,51 (2H, m), 2,56-2,65 (2H, m), 2,78 (2H, q), 3,12 (2H, br d), 3,49 (2H, t), 4,18-4,30 (1H, m), 6,20 (1H, s), 6,87 (1H, td), 7,19 (1H, dd), 7,48-7,53 (2H, m), 8,21 (1H, dd), 8,50 (1H, dd).
5-Хлор-2-{3-[4-(2-этил-5-фториндол-1-ил)-пиперидин-1-ил]пропилсульфанил}бензотиазол
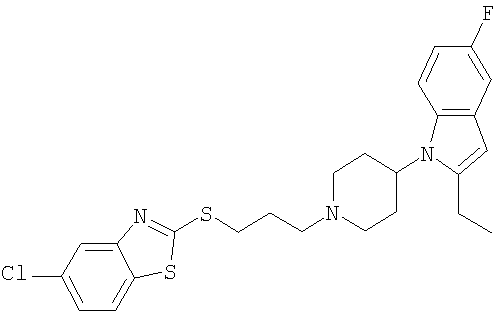
1H ЯМР (400 МГц, ДМСО): 1,25 (3Н, t), 1,93 (2H, br d), 2,30-2,42 (2H, m), 2,81 (2H, q), 2,99 (2H, br q), 3,13-3,32 (4H, m), 3,56 (2H, t), 3,60-3,81 (2H, m), 4,53-4,65 (1H, m), 6.22 (1H, m), 6,82 (1H, br t), 7,21 (1H, dd), 7,43 (1H, dd), 7,91-8,02 (2H, m), 8,08 (1H, dd).
2-{3-[4-(2-Этил-5-фториндол-1-ил)-3,6-дигидро-2Н-пиридин-1-ил] пропилсульфанил} бензооксазол
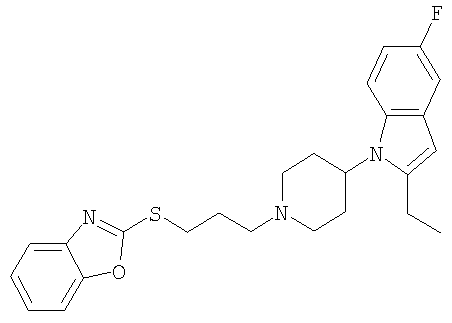
1H ЯМР (400 МГц, ДМСО): 1,27 (3Н, t), 1,76 (2H, br d), 1,99-2,09 (2H, m), 2,19-2,27 (2H, m), 2,40-2,53 (2H, m), 2,59 (2H, t), 2,77 (2H, q), 3,11 (2H, br d), 3,43 (2H, t), 4,17-4,28 (1H, m), 6,20 (1H, s), 6,85 (1H, td), 7,18-7,22 (2H, m), 7,30-7,35 (2H, m), 7,47-7,55 (1H, m), 7,62-7,67 (1H, m).
2-Этил-5-фтор-1-{1-[3-(5-трифторметилпиридин-2-илсульфанил)пропил]-1,2,3,6-тетрагидропиридин-4-ил}-1Н-индол

1H ЯМР (400 МГц, ДМСО): 1,25 (3Н, t), 1,73 (2H, br d), 1,73-1,82 (2H, m), 2,12 (2H, br t), 2,32-2,44 (3Н, m), 2,78 (2H, q), 3,02 (2H, br d), 3,24-3,32 (3Н, m), 4,13-4,23 (1H, m), 6,20 (1H, s), 6,85 (1H, td), 7,20 (1H, dd), 7,46-7,51 (1H, m), 7,53 (1H, m), 7,99 (1H, dd), 8,81 (1H, s).
2-Этил-6-фтор-3-{1-[3-(4-фторфенилсульфанил)пропил]пиперидин-3-ил}-1H-индол
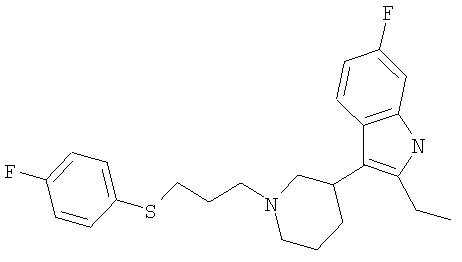
1Н ЯМР (400 МГц, ДМСО): 1,19 (3Н, t), 1,51-1,85 (6Н, m), 1,96 (1Н, br. t), 2,30-2,44 (3Н, m), 2,64-2,72 (3Н, m), 2,83-2,90 (2H, m), 2,93 (2H, t), 6,70-6,78 (1Н, m), 6,99 (1Н, dd), 7,13 (2H, t), 7,35-7,41 (2H, m), 7,49-7,54 (1Н, m), 10,77 (1Н, s).
Этиловый эфир 3-{3-[4-(2-этил-5-фториндол-1-ил)пиперидин-1-ил]пропилсульфанил}бензойной кислоты
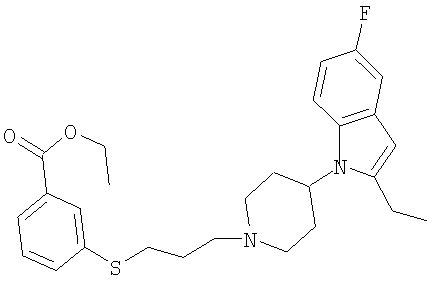
Т.пл.179-181°С.
3-{3-[4-(2-Этил-5-фториндол-1-ил)пиперидин-1-ил]пропилсульфанил}-бензойная кислота
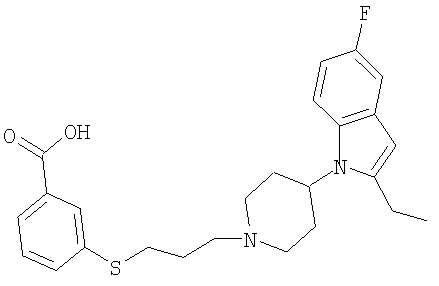
1Н ЯМР (400 МГц, ДМСО): 1,25 (3Н, t), 1,90 (2H, br. d), 1,98-2,10 (2H, m), 2,72-2,88 (4H, m), 3,02-3,21 (7H, m), 3,44-3,60 (2H, m), 4,53 (1Н, br.s), 6,21 (1Н, s), 6,88 (1Н, td), 7,22 (1Н, dd), 7,49 (1Н, t), 7,68 (1Н, br. d), 7,70-7,80 (2H, m), 7,88 (1H, s).
Способ лечения
Таким образом, настоящее изобретение относится к соединениям, которые могут быть использованы при лечении и/или профилактике широкого круга воспалительных, инфекционных и иммунорегуляторных заболеваний, включая астму и аллергические заболевания, инфицирование патогенными микробами (которые, по определению, включают вирусы), а также включая аутоиммунные патологии, такие как ревматоидный артрит и атеросклероз.
Например, соединения согласно настоящему изобретению, которые ингибируют одну или несколько функций хемокинового рецептора млекопитающего (например, хемокинового рецептора человека), могут быть введены для того, чтобы ингибировать (т.е. ослабить или предотвратить) воспаление или инфекционное заболевание. В результате ингибируется один или несколько воспалительных процессов, такие как эмиграция лейкоцитов, адгезия, хемотаксис, экзоцитоз (например, ферментов, гистамина) или высвобождение воспалительных медиаторов. Например, проникновение эозинофилов в зоны воспаления (например, при астме или при аллергическом рините) может быть ослаблено в соответствии со способом согласно настоящему изобретению. В частности, соединение, описанное в приведенном ниже примере, обладает активностью в отношении блокирования миграции клеток, синтезирующих CCR-3 рецептор, с использованием соответствующих хемокинов, по данным вышеуказанных исследований.
Аналогичным образом, соединения согласно настоящему изобретению, которые являются промоторами одной или несколько функций хемокинового рецептора млекопитающего (например, хемокинов человека), в результате введения стимулируют (индуцируют или усиливают) иммунную или воспалительную реакцию, такую как эмиграция лейкоцитов, адгезия, хемотаксис, экзоцитоз (например, ферментов, гистамина) или высвобождение медиаторов воспаления, что приводит к полезному стимулированию воспалительных процессов. Например, эозинофилы могут привлекаться для подавления паразитарных инфекций. В дополнение, также может рассматриваться лечение вышеуказанных воспалительных, аллергических и аутоиммунных заболеваний с использованием соединений согласно настоящему изобретению, которые промотируют одну или несколько функций хемокинового рецептора млекопитающего, если предполагается доставка достаточного количества соединения, что вызывает согласно настоящему изобретению снижение синтеза рецептора клеткой посредством индуцирования интернализации (включения в клетку) хемокинового рецептора или посредством доставки соединения таким образом, что это приводит к изменению направления миграции клеток.
В дополнение к приматам, например в дополнение к человеку, лечению в соответствии со способом согласно настоящему изобретению может быть подвергнуто множество других млекопитающих. Например, могут быть подвергнуты лечению млекопитающие, включая, но без ограничения указанным, коров, овец, коз, лошадей, собак, морских свинок, крыс или других представителей семейств крупного рогатого скота, овечьих, лошадиных, собачьих, кошачьих, представителей грызунов или мышиных, или крысиных. Однако способ может быть использован и для других представителей, например для лечения птиц. Пациент, подлежащий лечению согласно описанному выше способу, представляет собой млекопитающее, мужского или женского пола, которому необходимо модулирование активности хемокинового рецептора. Термин "модулирование" при использовании в тексте настоящей заявки, как предполагается, означает антагонизм, агонизм, частичный антагонизм и/или частичный агонизм.
Заболевания или состояния человека или других млекопитающих, при которых необходимо лечение ингибиторами функционирования хемокиновых рецепторов, включают, но не ограничиваются указанным: воспалительные или аллергические заболевания и состояния, включая респираторные аллергические заболевания, такие как астма, аллергический ринит, аллергические заболевания легких, аллергический пневмонит, эозинофильный целлюлит (эозинофильное воспаление рыхлой клетчатки) (например, синдром Велла), эозинофильная пневмония (например, синдром Леффлера (Loeffler), хроническая эозинофильная пневмония), атонический (эозинофильный) фасциит (например, синдром Шульмана), аллергия замедленного типа, интерстициальный легочный процесс (ИЛП) (например, идиопатический легочный фиброз, или ИЛП, связанный с ревматоидным артритом, системная красная (системная эритематозная) волчанка, анкилозирующий спондилит, системный склероз, синдром Шегрена, полимиозит или дерматомиозит); общая анафилактическая реакция или аллергические реакции, лекарственная аллергия (например, к пенициллину, цефалоспоринам), эозинофильно-миалгический синдром вследствие приема пищи, загрязненной триптофаном, аллергическая реакция на укусы насекомого, аутоиммунные заболевания, такие как ревматоидный артрит, псориатический артрит, рассеянный склероз, системная красная (системная эритематозная) волчанка, астенический бульбарный паралич (бульбоспинальный паралич), юношеский диабет; гломерулонефрит, аутоиммунные тиреоидит, синдром Бехчета; отторжение трансплантата (например, при трансплантации), включая аллоотторжение трансплантата или реакцию трансплантат против хозяина; воспалительные заболевания кишечника, такие как болезнь Крона (гранулематозная болезнь) и язвенный колит; спондилоартрит; склеродерма; псориаз (включая псориаз, опосредованный Т-клетками) и воспалительные болезни кожи, такие как дерматит, экзема, атопический дерматит, аллергических контактный дерматит, крапивница; васкулит (воспаление стенок кровеносных сосудов) (например, некротизированный, кожный) и гиперчувствительный васкулит (воспаление стенок кровеносных сосудов); эозинофильный миозит, атонический (эозинофильный) фасциит; злокачественные опухоли с лейкоцитарной инфильтрацией кожи или органов. Возможно также проводить лечение других заболеваний или состояний, при которых могут быть приостановлены нежелательные воспалительные состояния, включая, но не ограничиваясь указанным, реперфузионные нарушения, атеросклероз, некоторые злокачественные гематологические заболевания, цитокин-индуцированнная токсичность (например, септический шок, эндотоксический шок), полимиозит, дерматомиозит. Инфекционные заболевания или состояния человека или других организмов, которые могут быть подвергнуты лечению ингибиторами функционирования хемокинового рецептора, включают, но не ограничиваются указанным, вирус иммунодефицита человека (ВИЧ).
Заболевания или состояния человека или других организмов, которые могут быть подвергнуты лечению промоторами функционирования хемокинового рецептора, включают, но не ограничиваются указанным: иммуносупрессию (подавление иммунитета), например, у пациентов с синдромом иммунодефицита, таким как синдром приобретенного иммунодефицита (СПИД) или другие вирусные инфекции, лечение пациентов, перенесших радиотерапию (лучевую терапию), химиотерапию, терапию в отношении аутоиммунных заболеваний или лекарственную терапию (например, кортикостероидную терапию), которые приводят к иммуносупрессии (подавлению иммунитета); иммуносупрессия вследствие врожденного дефицита функции рецептора или вследствие других причин; и инфекционные заболевания, такие как заболевания, вызванные паразитами, включая, но без ограничения указанным, заражение нематодами (круглыми глистами); (трихиуриаз, энтеробиоз, аскаридоз, анкилостомоз, стронгилоидоз, трихинеллез, филяриатоз); трематодоз (парагонимоз) (шистосомоз, клонорхоз), заражение цестодами (ленточными гельминтами) (эхинококкоз, тениоз - заражение Taeniasis saginata, цистицеркоз); инфицирование висцеральными червями-паразитами, висцеральная форма синдрома "блуждающей личинки" (larva migrans), (например, токсороз), эозинофильный гастроэнтерит (например, при заражении Anisaki sp., Phocanema sp.), кожная форма синдрома "блуждающей личинки" (larva migrans) (заражение Ancylostona braziliense, Ancylostoma caninum). В соответствии с этим соединения согласно настоящему изобретению могут применяться при профилактике и лечении множества воспалительных, инфекционных и иммунорегуляторных нарушений, расстройств и заболеваний. В дополнение, лечение вышеуказанных воспалительных, аллергических и аутоиммунных заболеваний также может рассматриваться в отношении промоторов функционирования хемокинового рецептора, если предполагают осуществить доставку такого количества соединения, которое достаточно для того, чтобы вызвать ослабление выделения рецепторов клеткой посредством индуцирования интернализации (включения в клетку) хемокинового рецептора или доставки соединения таким образом, что это приводит к изменению направления миграции клеток.
В соответствии с еще одним аспектом настоящее изобретение может быть использовано для оценки предполагаемых специфических агонистов или антагонистов рецепторов, сопряженных с G-белком. Настоящее изобретение относится к применению указанных соединений при получении и проведении скрининговых исследований соединений, которые модулируют активность хемокиновых рецепторов. Кроме того, соединения согласно настоящему изобретению могут применяться для установления или определения участков связывания других соединений с хемокиновыми рецепторами, например, посредством конкурентного ингибирования или в качестве базового соединения при проведении исследования, предполагающего сравнение соединения с известной активностью и соединения с неизвестной активностью. В том случае, когда разрабатывают новый способ или методику исследования, соединения согласно настоящему изобретению могут быть использованы для проверки их эффективности.
В частности, такие соединения могут быть представлены для продажи в виде набора, например, для применения при проведении фармакологических исследований, связанных с вышеуказанными заболеваниям. Соединения согласно настоящему изобретению также могут быть использованы для оценки предполагаемых конкретных модуляторов хемокиновых рецепторов. В дополнение, можно использовать соединения согласно настоящему изобретению для проверки специфичности рецепторов, сопряженных с G-белком, которые, как полагают, не являются хемокиновыми рецепторами, либо используя в качестве примера соединений, которые не связываются с такими рецепторами, либо используя соединения согласно настоящему изобретению в качестве структурных вариантов соединений, активных в отношении указанных рецепторов, что может способствовать определению специфических участков взаимодействия.
Фармацевтические формы
Соединения формулы 1 вводят млекопитающему в терапевтически эффективном количестве. Термин "терапевтически эффективное количество" означает такое количество соединения формулы 1, введение которого млекопитающему по отдельности или в комбинации с другим терапевтическим агентом является эффективным для профилактики или ослабления симптомов заболевания, опосредованного активностью CCR-3-рецептора, или развития этого заболевания.
Соединения согласно настоящему изобретению могут быть введены в виде таких дозированных форм для перорального введения, как таблетки, капсулы (каждая из которых включает составы с замедленным высвобождением или с рассчитанным по времени высвобождением), пилюли, порошки, гранулы, эликсиры, настойки, суспензии, сиропы и эмульсии. Соединения согласно настоящему изобретению также могут быть введены с использованием формы для внутривенного введения (болюс или состав для вливания), формы для интраперитонеального введения, формы для подкожного введения или формы для внутримышечного введения, все используемые дозированные формы хорошо известны специалисту в области фармацевтики. Соединения согласно настоящему изобретению могут быть введены по отдельности, но, как правило, их вводят вместе с фармацевтически приемлемыми носителями, выбранными в зависимости от предполагаемого способа введения, с учетом обычной фармацевтической практики.
Режим дозирования соединений согласно настоящему изобретению будет, безусловно, в значительной степени зависеть от известных факторов, таких как фармакодинамические характеристики конкретного агента и способ и методика его введения, а также от конкретного вводимого соединения, от возраста, пола, состояния здоровья пациента и медицинских показаний, а также массы тела пациента; природы и степени выраженности симптомов; вида сопутствующего лечения; частоты приема; способа введения, состояния почек и печени пациента и требующегося эффекта. Лечащий врач или ветеринар сможет определить и выписать эффективное количество лекарственного средства, необходимое для профилактики, контроля или прекращения прогрессирования заболевания.
Как общее руководство, дневная дозировка при пероральном приеме каждого активного ингредиента, при использовании для достижения указанного действия, будет варьироваться в интервале от приблизительно 0,001 до 1000 мг/кг массы тела, предпочтительно приблизительно от 0,01 до 100 мг/кг массы тела в день и наиболее предпочтительно приблизительно от 1,0 до 20 мг/кг/день. При внутривенном введении наиболее предпочтительные дозы находятся в интервале от приблизительно 1 до приблизительно 10 мг/кг/минута при вливании с постоянной скоростью. Соединения согласно настоящему изобретению могут быть введены в виде одной дозы в день, или суммарная дневная доза может быть введена разделенной на несколько дозировок, например два, три или четыре раза в день.
Соединения согласно настоящему изобретению могут быть введены в виде интраназальной формы при местном применении с использованием подходящего интраназального наполнителя или могут быть введены трансдермально с использованием трансдермальных пластырей для кожи. В том случае, когда соединения вводят в виде системы трансдермальной доставки, вводимая доза, безусловно, в большей степени будет вводиться непрерывно, чем периодически.
Соединения формулы 1 обычно вводят в виде смеси с фармацевтически приемлемыми разбавителями, наполнителями, эксципиентами или носителями (обобщенно называемыми в тексте настоящей заявки фармацевтически приемлемыми носителями), подходящим образом выбранными в соответствии с предполагаемым способом введения, то есть для получения таблеток для перорального введения, капсул, эликсиров, сиропов и т.п., и с учетом общепринятой фармацевтической практики.
Например, для перорального введения в виде таблетки или капсулы активный лекарственный ингредиент может быть использован в сочетании с любым пригодным для перорального введения нетоксичным фармацевтически приемлемым инертным носителем, например, таким как лактоза, крахмал, сахароза, глюкоза, метилцеллюлоза, магний стеарат, дикальций фосфат, сульфат кальция, маннит, сорбит и тому подобными носителями; для перорального введения в жидкой форме лекарственный компонент для перорального введения может быть использован в сочетании с любым пригодным для перорального введения нетоксичным фармацевтически приемлемым инертным носителем, например, таким как этанол, глицерин, вода и т.п. Кроме того, когда это целесообразно или необходимо, в состав композиции могут быть также введены подходящие связующие, скользящие вещества (вспомогательные вещества при производстве таблеток), агенты, способствующие распаду лекарственной формы, и подкрашивающие агенты. Подходящие связующие включают крахмал, желатину, природные сахара, такие как глюкоза или бета-лактоза, сахаристое вещество из кукурузы (подсластитель), природные и синтетические смолы, такие как акация, трагакантовая камедь или альгинат натрия, карбоксиметилцеллюлоза, полиэтиленгликоль, воски и т.п. вещества. Смазочные вещества, используемые при получении таких дозированных форм, включают олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Вещества, способствующие распаду лекарственной формы, включают, в частности, крахмал, метилцеллюлозу, агар, бентонит, ксантановую смолу и т.п.
Соединения согласно настоящему изобретению также могут быть введены в виде системы липосомной доставки, например, такой как небольшие однослойные липосомы, крупные однослойные липосомы, многослойные липосомы. Липосомы могут быть получены из различных фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины.
Соединения согласно настоящему изобретению могут быть также использованы в сочетании с растворимыми полимерами, такими как носители, обеспечивающие доставку лекарственного средства к мишени. Такие полимеры могут включать поливинилпирролидон, пирановые сополимеры, полигидроксипропилметакриламидамидфенол, полигидроксиэтиласпартамидфенол или полиэтиленоксидполилизин, замещенный пальмитоиловыми остатками.
Кроме того, соединения согласно настоящему изобретению могут быть также использованы в сочетании с рядом биодеградируемых полимеров, которые могут быть использованы для получения форм с контролируемым высвобождением лекарственного средства, например, таких как полимолочная (α-оксипропионовая) кислота, полигликолевая кислота, сополимеры полимолочной и полигликолевой кислот, поли-эпсилон-капролактон, полигидроксимасляная кислота, поли-орто-сложные эфиры, полиацетали, полидигидропираны, полицианоацилаты и сшитые или амфипатические блоксополимеры - гидрогели.
Дозированные формы (фармацевтические композиции), подходящие для введения, могут содержать от приблизительно 1 миллиграмма до приблизительно 100 миллиграммов активного ингредиента на единичную дозированную форму.
В таких фармацевтических композициях активный ингредиент будет обычно присутствовать в количестве приблизительно 0,5-95% по массе в расчете на суммарную массу композиции.
Желатиновые капсулы могут содержать активный ингредиент и порошкообразные носители, такие как лактоза, крахмал, производные целлюлозы, стеарат магния, стеариновая кислота и т.п. Для получения прессованных таблеток могут быть использованы подобные разбавители. Как таблетки, так и капсулы могут быть приготовлены в виде продуктов с замедленным высвобождением для обеспечения постоянного высвобождения лекарственного средства в течение нескольких часов. Спрессованные таблетки могут иметь покрытие из сахара или могут быть покрыты пленкой для того, чтобы замаскировать неприятный вкус и защитить таблетку от воздействия атмосферных факторов, или могут иметь энтеросолюбильное покрытие для селективного распада в желудочно-кишечном тракте.
Жидкие дозированные формы для перорального введения могут содержать подкрашивающие агенты и агенты, улучшающие вкус и запах для повышения привлекательности для пациента.
Как правило, подходящими носителями для растворов для парентерального введения, являются вода, подходящее масло, физиологический раствор, водная декстроза (глюкоза) и растворы аналогичных сахаров, а также гликоли, такие как пропиленгликоль или полиэтиленгликоль. Растворы для парентерального введения предпочтительно содержат водорастворимую соль активного ингредиента, подходящие стабилизирующие агенты и, если необходимо, буферные вещества. Подходящими стабилизирующими агентами являются бисульфит натрия, сульфит натрия или аскорбиновая кислота или по отдельности, или в комбинации. Также используют лимонную кислоту и ее соль и натриевую соль ЭДТК (этилендиаминтетрауксусной кислоты). В дополнение, растворы для парентерального введения могут содержать консерванты, такие как бензалконий хлорид, метил- или пропилпарабен и хлорбутанол.
Подходящие фармацевтические носители описаны в Reminqton's Pharmaceutical Sciences, Mack Publishing Company - общепринятом руководстве в данной области.
В том случае, когда вместе с соединением формулы 1 вводят два или несколько вышеупомянутых других терапевтических агента, как правило, количество каждого компонента в типовой дневной дозировке и типовой дозированной форме может быть снижено по сравнению с обычной дозировкой агента, если он вводится по отдельности, вследствие аддитивного или синергетического эффекта терапевтического агента, когда он вводится в комбинации.
В частности, при получении единичной дозированной формы существует потенциальная возможность взаимодействия между объединенными активными ингредиентами. По этой причине в том случае, когда соединение формулы 1 и второй терапевтический агент объединяют в виде одной единичной дозированной формы, композицию приготавливают таким образом, что, хотя активные ингредиенты и объединяют в единичной дозированной форме, физический контакт между активными ингредиентами минимизирован (то есть уменьшен). Например, один активный ингредиент может иметь энтеросолюбильное покрытие. Используя энтеросолюбильное покрытие для одного активного ингредиента, возможно не только минимизировать контакт между входящими в комбинацию активными ингредиентами, но также возможно контролировать высвобождение одного из этих компонентов в желудочно-кишечном тракте таким образом, чтобы один активный ингредиент не высвобождался в желудке, но в основном высвобождался в кишечнике. Один из активных ингредиентов также может быть покрыт веществом, которое служит для достижения эффекта замедленного высвобождения в желудочно-кишечном тракте и также позволяет минимизировать физический контакт между входящими в комбинацию активными ингредиентами.
Кроме того, компонент, предназначенный для замедленного высвобождения, может дополнительно иметь энтеросолюбильное покрытие, таким образом, что высвобождение этого компонента происходит только в кишечнике. Еще один вариант включает приготовление комбинированного продукта, в котором один компонент покрывают полимером для замедленного высвобождения или покрывают энтеросолюбильным полимерным покрытием и на другой компонент также наносят покрытие из полимера с низкой вязкостью, например, такого как гидроксипропилметилцеллюлоза (НРМС), или используют другие подходящие вещества, известные из предшествующего уровня техники, для того чтобы дополнительно отделить друг от друга активные ингредиенты. Полимерное покрытие служит для получения дополнительного барьера для взаимодействия с другим компонентом.
Эти и другие способы минимизации контакта между компонентами комбинированного продукта согласно настоящему изобретению при введении как в виде единичной дозированной формы, так и при введении в виде отдельных форм, но в то же самое время и тем же самым способом будут вполне понятны специалисту в данной области техники в соответствии с описанием настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ, МОДУЛИРУЮЩИЕ ЭСТРОГЕНОВЫЕ РЕЦЕПТОРЫ | 2019 |
|
RU2826635C2 |
| ИНГИБИТОРЫ АКТИВНОСТИ ПРОТЕИНТИРОЗИНКИНАЗЫ | 2009 |
|
RU2533827C2 |
| СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ФИЗИОЛОГИЧЕСКИХ И/ИЛИ ПАТОФИЗИОЛОГИЧЕСКИХ СОСТОЯНИЙ, ОПОСРЕДУЕМЫХ РЕЦЕПТОРАМИ, СТИМУЛИРУЮЩИМИ СЕКРЕЦИЮ ГОРМОНА РОСТА, ТРИАЗОЛЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2415134C9 |
| ПРОИЗВОДНЫЕ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБЫ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ И ЗАБОЛЕВАНИЙ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2001 |
|
RU2265011C2 |
| ИНГИБИТОРЫ ДЕАЦЕТИЛАЗ ГИСТОНОВ (HDACS) | 2013 |
|
RU2629947C2 |
| ПРОИЗВОДНЫЕ ГЕТЕРОАРЕНКАРБОКСАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРИМЕНЕНИЕ | 2003 |
|
RU2320656C2 |
| (АЗА)ИНДОЛ-, БЕНЗОТИОФЕН- И БЕНЗОФУРАН-3-СУЛЬФОНАМИДЫ | 2017 |
|
RU2767904C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ CRTH2 В ТЕРАПИИ | 2004 |
|
RU2412934C2 |
| НОВЫЕ ЗАМЕЩЕННЫЕ ИНДОЛЫ | 2003 |
|
RU2288914C2 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА, СОДЕРЖАЩИЕ ИХ КОМПОЗИЦИИ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2004 |
|
RU2346938C2 |
Изобретение относится к соединениям формулы (1) и их фармацевтически приемлемым солям в качестве модулятора активности хемокинового рецептора CCR3, фармацевтической композиции на их основе, к способу их получения и их применению. Соединения могут найти применение для лечения и профилактики заболеваний, опосредованных активностью хемокинового рецептора CCR3, таких как воспалительные или аллергические заболевания и др. В общей формуле (1)
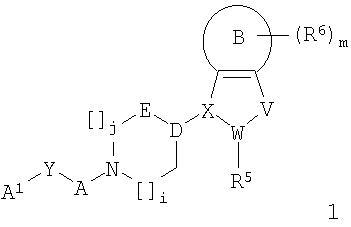
R1 представляет собой фенил, [1,2,4]триазоло[4,3-а]пиридинил, тиазоло[5,4-b]пиридинил, бензотиазолил, бензоксазолил, пиридинил, причем каждый из указанных фенила или гетероциклилов может быть замещен одним, двумя или тремя радикалами R2; R2 каждый независимо означает (С1-С6)галогеналкил, галоген, COOR3; CONR3R4; R3 представляет собой Н или (С1-С6)алкил; R4 представляет собой Н или (С1-С6)алкил, R5 представляет собой (С1-С6)алкил, (С1-С6)алкокси, (С3-С6)циклоалкил; R6 каждый независимо означает (С1-С6)алкокси, (С1-С6)галогеналкил, галоген, OR3, CN, CONR3R4; А представляет собой С(СН3)2-СН2-СН2-, СН2-СН2-СН2- или 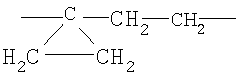 ; В представляет собой фенил; D-E представляет собой СН-СН2- или С=СН-, X-W-V представляет собой
; В представляет собой фенил; D-E представляет собой СН-СН2- или С=СН-, X-W-V представляет собой
N-C=CR7 или C=C-NR7; R7 представляет собой Н или (С1-С6)алкил; Y представляет собой NR4, О,
S(O)n; i, j, m каждый означает 1; n означает 0 или 2. 5 н. и 8 з. п. ф-лы.
1. Соединение формулы 1
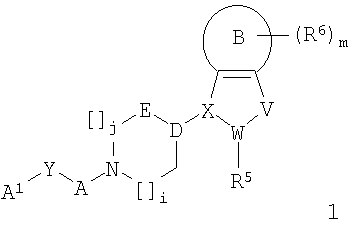
где R1 представляет собой фенил, [1,2,4]триазоло[4,3-а]пиридинил, тиазоло[5,4-b]пиридинил, бензотиазолил, бензоксазолил, пиридинил, причем каждый из указанных фенила или гетероциклилов может быть замещен одним, двумя или тремя радикалами R2;
R2 каждый независимо означает (С1-С6)галогеналкил, галоген, COOR3; CONR3R4;
R3 представляет собой Н или (С1-С6)алкил;
R4 представляет собой Н или (С1-С6)алкил;
R5 представляет собой (С1-С6)алкил, (С1-С6)алкокси, (С3-С6)никлоалкил;
R6 каждый независимо означает (С1-С6)алкокси, (С1-С6)галогеналкил, галоген, OR3, CN, CONR3R4;
А представляет собой С(СН3)2-СН2-СН2-, СН2-СН2-СН2-или 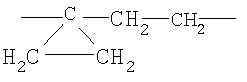 , необязательно замещенный галогеном или группой ОН;
, необязательно замещенный галогеном или группой ОН;
В представляет собой фенил;
D-E представляет собой СН-СН2- или С=СН-;
X-W-V представляет собой N-C=CR7 или C=C-NR7;
R7 представляет собой Н или (С1-С6)алкил;
Y представляет собой NR4, О, S(O)n;
i, j, m каждый означает 1;
n означает 0 или 2;
и его фармацевтически приемлемые соли.
2. Соединение формулы 1a
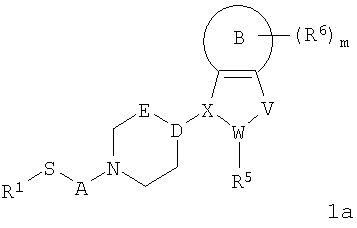
и R1, R5, R6, A, B, D-E, X-W-V, i, j и m являются такими, как указано в п.1.
3. Соединение по п.1 или 2, где R1 представляет собой фенил, необязательно замещений одним, двумя или тремя радикалами R2.
4. Соединение по любому из пп.1-3, где D-E означает СН-СН2-.
5. Соединение по любому из пп.1-4, где А означает СН2-СН2-СН2-.
6. Соединение по любому из пп.1-4, где А означает С(СН3)2-СН2-СН2-.
7. Соединение по любому из пп.1-4, где А означает
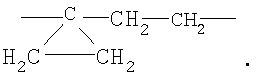
8. Соединение по любому из пп.1-7, где X-W-V представляет собой N-C=CR7.
9. Соединение по любому из пп.1-8,
где R1 означает фенил, необязательно замещенный одним, двумя или тремя радикалами R2 и
R2 каждый независимо означает COOR3 или CONR3R4;
R3 представляет собой Н или (С1-С6)алкил;
R4 представляет собой Н или (С1-С6)алкил;
10. Способ получения соединений формулы 1 или 1а, заключающийся в том, что соединение формулы 2
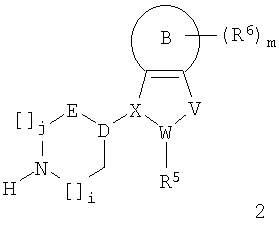
подвергают взаимодействию с соединением формулы 3
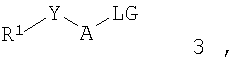
где R1, R5, R6, A, B, D-E, X-W-V, i, j и m являются такими, как указано в п.1, и
LG представляет собой подходящую отщепляемую группу, выбранную из галогена, мезилатной группы, трифлатной группы, тозилатной группы или брозилатной группы.
11. Фармацевтическая композиция, обладающая свойствами модулятора активности хемокинового рецептора CCR3, отличающаяся тем, что она содержит одно или несколько соединений формулы 1 или 1а по одному из пп.1-9.
12. Соединение формулы 1 или 1а по любому из пп.1-9 в качестве лекарственного средства, модулирующего активность хемокинового рецептора CCR3.
13. Применение соединений формулы 1 или 1а по одному из пп.1-9 для получения лекарственного средства, предназначенного для профилактики и/или лечения заболеваний, при которых терапевтически полезным является использование модулятора активности хемокинового рецептора CCR3.
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| WO 00/75130 A, 14.12.2000 | |||
| RU 2000112403 A, 10.09.2002. | |||
Авторы
Даты
2010-02-20—Публикация
2004-11-11—Подача