Дофамин считается важным нейротрансмиттером центральной нервной системы. Дофамин действует, связываясь с пятью разными дофаминовыми рецепторами. По их морфологии и способу сигнальной трансмиссии их можно классифицировать как D1-подобные (D1 и D5) и D2-подобные (D2, D3 и D4) рецепторы (Neve, K.A. The Dopamine Receptor. Human Press, 1997). В частности, подтипы семейства D2 играют важную роль в регуляторных процессах центральной нервной системы. В то время как D2-рецепторы главным образом экспрессируются в базальных ганглиях, где они контролируют нейромоторные цепи, D3-рецепторы главным образом находятся в лимбической системе, где контролируются эмоциональные и когнитивные процессы. Нарушения сигнальной трансдукции этих рецепторов приводят к многочисленным невропатологическим ситуациям. В частности, D3-рецептор считается перспективной мишенью для разработки активных ингредиентов для лечения психиатрических заболеваний, таких как шизофрения или униполярная депрессия, расстройства сознания, а также для лечения нейродегенеративных заболеваний, таких как болезнь Паркинсона, а также для лечения наркомании (Pulvirenti, L. et al. Trends Pharmacol. Sci. 2002, 23, 151-153).
Соединения, имеющие арилпиперазиновую структуру, уже описаны как лиганды, активные в отношении дофаминовых рецепторов (Robarge, M.J. J.Med.Chem. 2001, 44, 3175-3186). Бензамиды и нафтамиды, имеющие частично арилпиперазиновую структуру, также известны как лиганды дофаминовых рецепторов (Perrone, R. J.Med.Chem. 1998, 41, 4903-4909; ЕР 0779284 А1). Фенилпиперазинилнафтамид недавно описан как селективный D3-частичный агонист, демонстрирующий в животных моделях перспективную активность, которую можно использовать для лечения пристрастия к кокаину (Pilla, M. et al. Nature 1999, 400, 371-375).
Описано несколько примеров арилпиперазиниламидов, имеющих компоненты, представляющие собой кислород-, серо- или азотсодержащие гетероареновые кислоты (ES 2027898, ЕР 034961, US 3646047, US 3734915). С другой стороны, цианзамещенные и теллурсодержащие производные с частично ферроцениловой структурой не известны в литературе.
В ходе экспериментов по влиянию структуры лигандов дофамина авторы настоящего изобретения открыли новые соединения формул (I)-(IV), которые показывают ранее неизвестные свойства высокоаффинного и высокоселективного связывания с D3-рецептором в анализах in vitro. Эти соединения могут, таким образом, быть ценными терапевтическими агентами для лечения заболеваний центральной нервной системы, таких как шизофрения, различные формы депрессии, нейродегенеративные расстройства, сексуальная дисфункция, а также пристрастие к кокаину, опиатам и никотину.
Другими конкретными областями применения являются глаукома, когнитивные расстройства, синдром беспокойных ног, синдром гиперактивности (ADHS), гиперпролактинемия, гиперпролактинома, нарушения локомоции, связанные с болезнью Паркинсона, нарушения локомоции, индуцированные лечением L-ДОФА (L-3,4-дигидроксифенилаланином) и нейролептиками, например акатизия, ригидность, дистония и дискинезия.
Предметом настоящего изобретения являются производные амидов 2-гетероаренкарбоновых кислот, имеющие частично арилпиперазиниловую структуру, в форме свободного основания и в форме солей, нижеследующих формул (I) и (II):
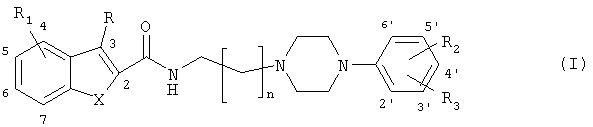
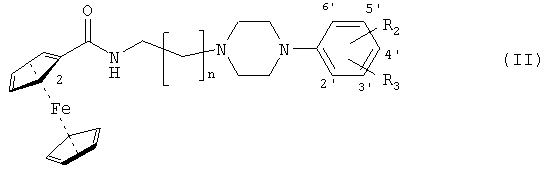
где в формуле (I)
- n равно 1-4 и
- R является водородом, алкилом или галогеном, и
(а) Х представляет собой S или О:
(1) когда R1 представляет собой гидрокси, алкилокси, алкенил, алкинил, арил, ацил, алкоксикарбонил или циано, каждый из R2 и R3 независимо выбран из водорода, гидрокси, алкилокси, алкила, алкенила, алкинила, арила, галогена, трифторметила, ацила, алкоксикарбонила и циано,
(2) когда R1 представляет собой водород, алкил, галоген или трифторметил, R2 выбран из гидрокси, алкенила, алкинила, арила, ацила, алкоксикарбонила и циано и R3 выбран из водорода, гидрокси, алкилокси, алкила, алкенила, алкинила, арила, галогена, трифторметила, ацила, алкоксикарбонила и циано, или
(б) Х представляет собой NH:
R1 выбран из водорода, гидрокси, алкила, алкилокси, алкенила, алкинила, арила, трифторметила, ацила, алкоксикарбонила, галогена и циано, и каждый из R2 и R3 независимо выбран из водорода, гидрокси, алкилокси, алкила, алкенила, алкинила, арила, галогена, трифторметила, ацила, алкоксикарбонила и циано при условии, что это соединение не является N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамидом,
или
(в) Х представляет собой Те:
R1 выбран из водорода, гидрокси, алкила, алкилокси, алкенила, алкинила, арила, галогена, трифторметила, ацила, алкоксикарбонила и циано, и каждый из R2 и R3 независимо выбран из водорода, гидрокси, алкилокси, алкила, алкенила, алкинила, арила, галогена, трифторметила, ацила, алкоксикарбонила и циано.
В одном воплощении изобретения в формуле (I)
- n равно 1-4 и
- Х представляет собой Те, когда R является водородом, алкилом или галогеном, и R1 замещен радикалами водород, гидрокси, алкил, алкилокси, алкенил, алкинил, арил, галоген, трифторметил, ацил, алкоксикарбонил или циано, и R2 и R3 отдельно или совокупно замещены радикалами водород, гидрокси, алкилокси, алкил, алкенил, алкинил, арил, галоген, трифторметил, ацил, алкоксикарбонил или циано,
или
- Х представляет собой S или О, когда R является водородом, алкилом или галогеном, и R1 замещен радикалами гидрокси, алкилокси, алкенил, алкинил, арил, ацил, алкоксикарбонил или циано, и R2 и R3 отдельно или совокупно замещены радикалами водород, гидрокси, алкилокси, алкил, алкенил, алкинил, арил, галоген, трифторметил, ацил, алкоксикарбонил или циано,
или
- Х представляет собой S или О, когда R является водородом, алкилом или галогеном, и R1 замещен радикалами водород, алкил, галоген или трифторметил, и R2 и R3 отдельно или совокупно замещены радикалами гидрокси, алкенил, алкинил, арил, ацил, алкоксикарбонил или циано,
или
- Х представляет собой NH, когда R является водородом, алкилом или галогеном, и R1 замещен радикалами гидрокси, алкил, алкилокси, алкенил, алкинил, арил, трифторметил, ацил, алкоксикарбонил или циано, при этом алкил и алкилокси содержат по меньшей мере два атома углерода, и R2 и R3 отдельно или совокупно замещены радикалами водород, гидрокси, алкилокси, алкил, алкенил, алкинил, арил, галоген, трифторметил, ацил, алкоксикарбонил или циано, при этом алкилокси содержит по меньшей мере два атома углерода.
В формуле (II)
n равно 1-4 и R1 и R2 отдельно или совокупно представляют собой радикалы водород, гидрокси, алкилокси, алкил, алкенил, алкинил, арил, галоген, трифторметил, ацил, алкоксикарбонил или циано.
В частности, изобретение относится к физиологически приемлемым солям соединений по изобретению.
Специалист-практик знает, что в зависимости от выбора заместителей соединения могут представлять собой оптически активные соединения. В данном случае предметом настоящего изобретения являются как рацематы, так и каждая из чистых энантиомерных форм.
Заместители, перечисленные в этом описании и прилагаемой формуле изобретения, содержат, в частности, группы, которые обсуждаются ниже.
"Алкил" может представлять собой разветвленную или неразветвленную алкильную группу, которая предпочтительно содержит от 1 до 10 атомов углерода, особенно предпочтительно от 1 до 6 атомов углерода и наиболее предпочтительно 1, 2 или 3 атома углерода, например метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, mpem-пентил, 1-метилбутил, 2-метилбутил, 1-этилпропил, 1,2-диметилпропил и н-гексил. Алкильные группы могут также быть замещенными одним или более заместителями, например галогеном или одной или более фенильными группами.
"Алкенил" и "алкинил" имеют по меньшей мере одну двойную или тройную связь. Они могут быть разветвленными или неразветвленными и предпочтительно содержат от 2 до 6 атомов углерода. Алкенилы или алкинилы предпочтительно связаны с гетероареновым или фенильным кольцом каркасной структуры соединения таким образом, что двойная или тройная связь сопряжена с ароматическим кольцом. Алкенил и алкинил могут также быть замещенными одним или более заместителями, предпочтительно фенилом, и в этом случае фенильная группа предпочтительно локализована на атоме углерода 2 (если алкенил или алкинил связаны с гетероареновым или фенильным кольцом каркасной структуры через атом углерода 1). Алкенилы или алкинилы предпочтительно являются незамещенными.
"Алкилокси" представляет собой O-алкильную группу, где алкил предпочтительно выбран из групп, перечисленных выше для "алкила". Предпочтительно алкилокси представляет собой C1-C6-алкилоксигруппу, в частности метокси. В другом воплощении алкилокси может быть также C2-C6-алкилоксигруппой.
"Арил" предпочтительно представляет собой фенил. Возможно, фенил независимо может также быть замещенным в одном или более положениях 2, 3 и 4, например, алкокси, трифторметилом или галогеном, предпочтительно метокси.
"Ацил", в частности, содержит группы -С(O)-алкил и -С(O)-арил, где алкил и арил предпочтительно выбраны из групп, указанных для "алкила" и "арила" выше, в частности -С(O)-C1-C6-алкил. Например, ацил может представлять собой ацетил, пропионил, бутирил или -С(O)-фенил.
"Алкоксикарбонил" представляет собой -С(O)-O-алкильную группу, где алкил предпочтительно выбран из групп, указанных для "алкила" выше. Предпочтительно алкоксикарбонил представляет собой (C1-C6-алкил)оксикарбонильную группу.
"Галоген" представляет собой предпочтительно фтор, хлор, бром или йод.
"Физиологически приемлемые соли" включают нетоксичные соли основания, в частности соли соединения формулы (I) в форме свободного основания с органическими или неорганическими кислотами. Примерами неорганических кислот являются HCI, HBr, серная кислота и фосфорная кислота. Органические кислоты включают уксусную кислоту, пропионовую кислоту, пировиноградную кислоту, масляную кислоту, α-, β- или δ-гидроксимасляную кислоту, валериановую кислоту, гидроксивалериановую кислоту, капроновую кислоту, гидроксикапроновую кислоту, каприловую кислоту, каприновую кислоту, лауриновую кислоту, миристиновую кислоту, пальмитиновую кислоту, стеариновую кислоту, гликолевую кислоту, молочную кислоту, D-глюкуроновую кислоту, L-глюкуроновую кислоту, D-галактуроновую кислоту, глицин, бензойную кислоту, гидроксибензойную кислоту, галловую кислоту, салициловую кислоту, ванилиновую кислоту, кумариновую кислоту, кофейную кислоту, гиппуровую кислоту, оротовую кислоту, L-винную кислоту, D-винную кислоту, D,L-винную кислоту, мезо-винную кислоту, фумаровую кислоту, L-яблочную кислоту, D-яблочную кислоту, D,L-яблочную кислоту, щавелевую кислоту, малоновую кислоту, янтарную кислоту, малеиновую кислоту, щавелевоуксусную кислоту, глутаровую кислоту, гидроксиглутаровую кислоту, кетоглутаровую кислоту, адипиновую кислоту, кетоадипиновую кислоту, пимелиновую кислоту, глутаминовую кислоту, аспарагиновую кислоту, фталевую кислоту, пропантрикарбоновую кислоту, лимонную кислоту, изолимонную кислоту, метансульфоновую кислоту, толуолсульфоновую кислоту и трифтометансульфоновую кислоту.
Соединения формулы (I), в которой Х представляет собой NH, S или О, можно назвать предпочтительными структурами.
Предпочтительными воплощениями соединений формулы (I) по изобретению являются следующие соединения общей формулы (Ia) или (Ib):
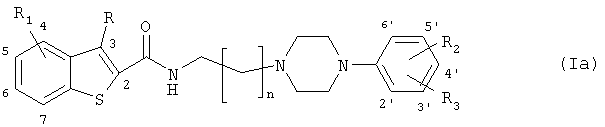
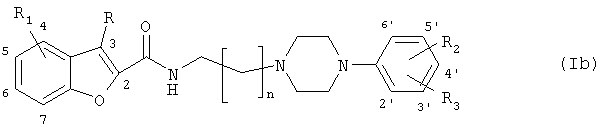
где n равно 1-4,
- R является водородом, C1-C6-алкилом или галогеном,
- когда R1 представляет собой гидрокси, C1-C6-алкилокси, C2-C6-алкенил, C2-C6-алкинил, фенил, который возможно может быть замещенным метоксигруппой или галогеном, C1-C6-ацил, C1-C6-алкоксикарбонил или циано, каждый из R2 и R3 независимо выбран из водорода, гидрокси, C1-C6-алкилокси, C1-C6-алкила, C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, галогена, трифторметила, C1-C6-ацила, C1-C6-алкоксикарбонила и циано,
- когда R1 представляет собой водород, C1-C6-алкил, галоген или трифторметил, R2 выбран из гидрокси, C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, C1-C6-ацила, C1-C6-алкоксикарбонила и циано, и R3 выбран из водорода, гидрокси, C1-C6-алкила, C1-C6-алкилокси, C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, галогена, трифторметила, C1-C6-ацила, C1-C6-алкоксикарбонила и циано,
и их фармацевтически приемлемые соли, причем предпочтительными заместителями-галогенами являются фтор, хлор и бром.
Другим предпочтительным воплощением соединений формулы (I) по изобретению являются следующие соединения общей формулы (Ic):
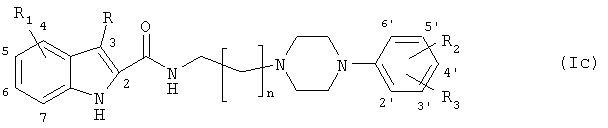
где n равно 1-4,
- R является водородом, C1-C6-алкилом или галогеном,
- R1 выбран из водорода, гидрокси, C1-C6-алкила, C1-C6-алкокси, C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, трифторметила, C1-C6-ацила, C1-C6-алкоксикарбонила, фтора, хлора, брома и циано,
- каждый из R2 и R3 независимо выбран из водорода, гидрокси, C1-C6-алкила, C1-C6-алкилокси, C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, галогена, трифторметила, C1-C6-ацила, C1-C6-алкоксикарбонила и циано,
и фармацевтически приемлемые соли этих соединений при условии, что соединение не является N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамидом.
В другом предпочтительном воплощении изобретения в соединениях общей формулы (Ic)
(а) когда R1 представляет собой гидрокси, C2-C6-алкенил, C2-C6-алкинил, фенил, который возможно может быть замещенным метоксигруппой или галогеном, трифторметил, C1-C6-ацил, C1-C6-алкоксикарбонил или циано, каждый из R2 и R3 независимо выбран из водорода, гидрокси, C1-C6-алкила, C1-C6-алкилокси, C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, галогена, трифторметила, C1-C6-ацила, C1-C6-алкоксикарбонила и циано,
и
(б) когда R1 представляет собой водород, C1-C6-алкил, C1-C6-алкилокси или галоген, R2 выбран из гидрокси, C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, C1-C6-ацила, C1-C6-алкоксикарбонила и циано, и R3 выбран из водорода, гидрокси, C1-C6-алкила, C1-C6-алкилокси,C2-C6-алкенила, C2-C6-алкинила, фенила, который возможно может быть замещенным метоксигруппой или галогеном, галогена, трифторметила, C1-C6-ацила, C1-C6-алкоксикарбонила и циано.
В другом предпочтительном воплощении изобретения, в соединениях общих формул (I), (Ia), (Ib) и (Ic)
- заместитель R1 находится в положении 5 или 6 гетероцикла и
- заместители R2 и R3 находятся соответственно в положениях 2 или 3 или соответственно в положениях 2 или 4 фенильного кольца, и в случае, когда один из двух заместителей R2 и R3 является атомом водорода, соответственный другой заместитель находится в положении 2 фенильного кольца.
В особенно предпочтительном воплощении изобретения в соединениях формул (I), (Ia), (Ib) и (Ic) n равно 3.
Предпочтительные соединения общей формулы (II), как определено выше, представляют собой соединения, в которых каждый из R1 и R2 независимо выбран из водорода, гидрокси, C1-C6-алкилокси, C1-C6-алкила, C2-C6алкенила, C2-C6-алкинила, арила, фтора, хлора, брома, трифторметила, C1-C6-ацила, C1-C6-алкоксикарбонила и циано.
Конкретными соединениями общей формулы (II) являются
(B16): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-ферроценилкарбамид и
(B17): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-ферроценилкарбамид.
В другом аспекте настоящее изобретение относится к соединениям общей формулы (IV)
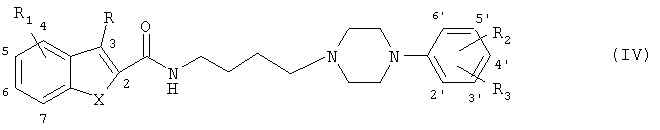
где X представляет собой S, NH или О,
- R выбран из водорода, C1-C6-алкила, фтора, хлора и брома,
- R1 выбран из водорода,C1-C6-алкокси, C1-C6-алкила, фтора, хлора, брома, трифторметила и циано, причем R1 находится в положении 5 или 6 гетероцикла,
- R2 и R3 независимо выбраны из водорода, C1-C6-алкилокси, C1-C6-алкила, фтора, хлора, брома и трифторметила, причем R2 и R3 находятся соответственно в положениях 2 или 3 или соответственно в положениях 2 или 4 фенильного кольца, и в случае, когда один из двух заместителей R2 и R3 является атомом водорода, соответственный другой заместитель находится в положении 2 фенильного кольца,
и фармацевтически приемлемым солям этих соединений при условии, что соединение не является N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамидом.
В предпочтительном аспекте изобретением являются соединения общей формулы (IV), как определено выше, где
- когда Х представляет собой NH, тогда R1 выбран из водорода, C1-C3-алкилокси, C1-C3-алкила, фтора, хлора, брома и циано, и
- когда Х представляет собой S или О, тогда R1 выбран из водорода, C1-C3-алкила, фтора, хлора, брома, циано и трифторметила.
Следующие соединения являются конкретными воплощениями соединений по изобретению:
(B18): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-циано-2 бензо[b]тиофенилкарбамид
(B19): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-циано-2-бензо[b]тиофенилкарбамид
(B20): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-6-циано-2-бензо[b]тиофенилкарбамид
(B21): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-6-циано-2-бензо[b]тиофенилкарбамид
(B1): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]тиофенилкарбамид
(B2): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]тиофенилкарбамид
(B22): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]тиофенилкарбамид
(B23): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]тиофенилкарбамид
(B10): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-индолилкарбамид
(B11): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-циано-2-индолилкарбамид
(B12): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-бром-2-индолилкарбамид
(B13): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-6-циано-2-индолилкарбамид
(B14): N-4-(4-(2,3-дихпорфенил)пиперазин-1-ил)бутил-5-бром-2-индолилкарбамид
(B15): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-6-циано-2-индолилкарбамид
(В25): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-циано-2-индолилкарбамид
(В7): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-циано-2-бензо[b]фуранилкарбамид
(B3): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]фуранилкарбамид
(B4): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]фуранилкарбамид
(B5): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-бром-
бензо[b]фуранилкарбамид
(В6): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]фуранилкарбамид
(B8): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]теллурофенилкарбамид
(B9): N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]теллурофенилкарбамид
и фармацевтически приемлемые соли этих соединений.
В частности, соединения формул (I), (Ia), (Ib), (Ic), (II) и (IV), как они определены выше, пригодны для терапевтического применения в качестве дофамин-D3 лигандов. Особое предпочтение отдается соединениям общей формулы (I) или их фармацевтически приемлемым солям, в которых Х представляет собой NH, S или О, и соединениям формул (Ia), (Ib), (Ic) и (IV) или их фармацевтически приемлемым солям.
Термин "высокоаффинные D3 лиганды" включает в себя соединения, которые показывают связывание с человеческими дофаминовыми D3-рецепторами, имеющее величину Ki предпочтительно не более 10 нМ, особенно предпочтительно не более 1 нМ, в эксперименте с радиолигандом (смотри Hübner, H. et al. J.Med. Chem. 2000, 43, 756-762, и следующий ниже раздел "Биологическая активность").
В одном аспекте настоящее изобретение относится к селективным D3 лигандам. Термин "селективные D3 лиганды" включает в себя соединения с величиной Ki в эксперименте с радиолигандом для D3-рецептора, описанном в следующем ниже разделе "Биологическая активность", которая ниже по меньшей мере в 10 раз для по меньшей мере пяти из семи следующих рецепторов: дофаминовых D1, D2long, D2short и D4.4 рецепторов, серотониновых 5-НТ1А и 5-НТ2 рецепторов и альфа-1-адренорецепторов.
В другом аспекте изобретение относится к высокоселективным дофамин-D3 лигандам. Термин "высокоселективные D3 лиганды" включает в себя соединения с величиной Ki в эксперименте с радиолигандом для D3-рецептора, описанном в следующем ниже разделе "Биологическая активность", которая ниже по меньшей мере в 100 раз для по меньшей мере трех и предпочтительно всех дофаминовых D1, D2long, D2short и D4.4 рецепторов.
D3 лиганды могут проявлять агонистическую, антагонистическую или частично агонистическую активность в отношении D3-рецептора. Соответствующие собственные активности соединений по изобретению могут быть измерены в анализах митогенеза, как описано в литературе (Hübner, H. et al. J.Med. Chem. 2000, 43, 4563-4569, и Löber, S. Bioorg. Med. Chem. Lett. 2002, 12.17, 2377-2380). В зависимости от патофизиологии основного заболевания может быть желательной более сильная агонистическая, более сильная антагонистическая или частично агонистическая активность. Настоящее изобретение, таким образом, обеспечивает превосходную возможность тонкой настройки желаемой активности.
Таким образом, еще одним предметом изобретения является терапевтический агент, содержащий одно или более из соединений общих формул (I), (Ia), (Ib), (Ic), (II) и (IV) или одно из конкретных соединений, как они определены выше, возможно в форме фармацевтически приемлемой соли. Предпочтительно это одно или более из соединений общих формул (I), (Ia), (Ib), (Ic) и (IV) или их фармацевтически приемлемых солей, в которых Х представляет собой NH, S или О.
Данное изобретение также относится к применению одного или более из соединений общих формул (I), (Ia), (Ib), (Ic), (II) и (IV) или одного из конкретных перечисленных соединений, возможно в форме фармацевтически приемлемой соли, для лечения, включая лечение и предупреждение, по приведенным здесь показаниям и для приготовления терапевтического агента для указанных показаний.
Для приготовления терапевтических агентов предпочтительно выбирать соединения по изобретению, которые представляют собой селективные D3 лиганды. Высокоселективные D3 лиганды являются особенно предпочтительными.
Соединения по изобретению имеют потенциальное применение в лечении или предупреждении целого ряда расстройств, в частности расстройств, сопровождающихся дисфункцией дофаминового метаболизма или дофаминергического сигнального каскада.
Примерами таких расстройств являются пристрастие к кокаину, алкоголю, опиатам и никотину, нейродегенеративные расстройства, в частности болезнь Паркинсона, сексуальная дисфункция, в частности эректильная дисфункция у мужчин, депрессия, в частности эндогенная монофазная депрессия ("тяжелая депрессия") и шизофрения.
Другими примерами расстройств, поддающихся лечению или предупреждению соединениями по изобретению, являются гиперпролактинемия, гиперпролактинома, глаукома, когнитивные расстройства, синдром беспокойных ног, синдром гиперактивности (ADHS), нарушения локомоции, связанные с болезнью Паркинсона, например ригидность, дистония и дискинезия, L-ДОФА-индуцированные расстройства, такие как тревога, нарушенние сна, психозы, дискинезии и дистонии, идиопатические дистонии, особенно синдром Сегавы, индуцированная нейролептиками (поздняя) дискинезия, дистония и акатизия.
Соединения по изобретению особенно хорошо подходят для приготовления терапевтического агента для лечения чувствительных к ДОФА нарушений локомоции. Такими нарушениями локомоции могут быть, например, дискинезии, дистонии, ригидность и тремор. Термин "чувствительный к ДОФА" означает, что на нарушение локомоции можно благоприятным образом воздействовать путем введения лекарственных средств, которые влияют на дофаминергическую сигнальную трансмиссию. Типичным примером является синдром Сегавы, идиопатическая дистония, при которой ответную реакцию на L-ДОФА можно использовать как диагностический критерий.
Предпочтительным применением является приготовление терапевтического агента для лечения дискинезий и дистоний, которые могут случаться спонтанно в связи с болезнью Паркинсона, но могут также быть индуцированы лекарственными средствами. Среди дискинезий и дистоний, индуцируемых лекарственными средствами, можно упомянуть в частности те из них, которые индуцируются нейролептиками и антагонистами дофамина или агонистами дофамина, или L-ДОФА.
Кроме того, эти терапевтические агенты можно использовать в медикаментозной аблактации после беременности.
Наконец, терапевтические агенты по изобретению можно использовать в виде сложного препарата для одновременного или последовательного введения в зависимости от заболевания, подлежащего лечению.
Например, одна выставляемая на продажу единица, которая содержит лекарственное средство L-ДОФА для лечения болезни Паркинсона, может также содержать фармацевтический препарат, который содержит одно из соединений по данному изобретению, например, с высокоселективным, частично-агонистическим профилем действия. L-ДОФА и соединение по данному изобретению могут присутствовать в одном и том же фармацевтическом препарате, например в сложной таблетке, или в разных единицах применения, например в форме двух отдельных таблеток. По мере необходимости эти два активных ингредиента можно вводить одновременно или в разные моменты времени.
В сложном препарате последовательного введения можно достичь, предоставив форму введения, например пероральную таблетку, имеющую два разных слоя с разными профилями высвобождения для разных фармацевтически активных компонентов. Специалисту-практику понятно, что в контексте данного изобретения возможны различные формы введения и схемы применения, каждая из которых является предметом изобретения.
Одно из воплощений данного изобретения, таким образом, относится к терапевтическому агенту, который содержит L-ДОФА или нейролептик, а также соединение по изобретению для одновременного или последовательного введения пациенту.
В общем, терапевтический агент по изобретению представляет собой фармацевтическую композицию, которая в дополнение к D3 лигандам, описанным выше, содержит по меньшей мере один фармацевтически приемлемый носитель или эксципиент.
Специалисту-практику ясно, что в зависимости от намеченного пути применения фармацевтический препарат может иметь разные формы. Например, фармацевтический препарат может быть адаптирован для внутривенного, внутримышечного, внутрикожного, подкожного, перорального, буккального, сублингвального, назального, трансдермального, ингаляционного, ректального или интраперитонеального введения.
Подходящие препараты и фармацевтические носители и эксципиенты, пригодные для этой цели, такие как наполнители, разрыхлители, связывающие агенты, смазывающие агенты, стабилизаторы, корригенты, антиоксиданты, консерванты, диспергирующие агенты или растворители, буферы или электролиты, известны специалистам в фармацевтической области и раскрыты в стандартный работах, например Sucker, Fuchs and Speiser ("Pharmazeutische Technologie", Deutscher Apotheker Verlag, 1991) и Remington ("The Science и Practice of Pharmacy", Lippincott, Williams & Wilkins, 2000).
В предпочтительном воплощении изобретения фармацевтические композиции, содержащие соединения по изобретению, можно вводить перорально и можно предоставлять, например, в форме капсулы, таблетки, порошка, гранулята, таблетки, покрытой оболочкой, или в жидкой форме.
Если желательно быстрое начало действия, препарат может быть приготовлен для введения в форме быстрого высвобождения. Подходящие пероральные препараты описаны в ЕР 0548356 или ЕР 1126821.
С другой стороны, если желательно растянутое во времени высвобождение, то можно выбрать препарат замедленного высвобождения активного ингредиента. Такие пероральные препараты также известны из предшествующего уровня техники.
Альтернативными фармацевтическими препаратами могут быть, например, растворы для инфузии или инъекции, масла, суппозитории, аэрозоли, спреи, пластыри, микрокапсулы или микрочастицы.
Другим предметом изобретения является применение соединения общей формулы (III)
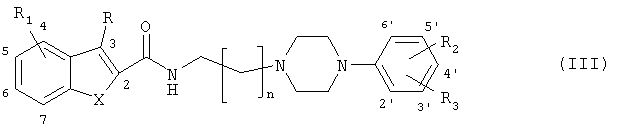
где n равно 1-4, X представляет собой S, О или NH, когда R является водородом, алкилом или галогеном, и R1 замещен радикалами водород, алкил, галоген, трифторметил, и каждый из R2 и R3 отдельно или совокупно замещен радикалами водород, гидрокси, алкилокси, алкил, алкенил, алкинил, арил, галоген, трифторметил, ацил, алкоксикарбонил или циано,
для приготовления фармацевтического агента
для лечения одного из следующих заболеваний или расстройств:
пристрастие к кокаину, алкоголю, опиатам и никотину, шизофрения, различные формы депрессии, в частности эндогенная монофазная депрессия ("тяжелая депрессия") или депрессивные фазы биполярных (маниакально-депрессивных) расстройств, нейродегенеративные расстройства, в частности болезнь Паркинсона, сексуальная дисфункция, гиперпролактинемия, гиперпролактинома, глаукома, когнитивные расстройства, синдром беспокойных ног, синдром гиперактивности (ADHS), нарушения локомоции, связянные с болезнью Паркинсона, например ригидность, дистония и дискинезия, L-ДОФА-индуцированные расстройства, такие как тревога, нарушение сна, психозы, дискинезии и дистонии, идиопатические дистонии, в частности синдром Сегавы, индуцированная нейролептиками (поздняя) дискинезия, дистония и акатизия.
В частности, соединение общей формулы (III) можно использовать для приготовления терапевтического агента для лечения чувствительных к ДОФА нарушений локомоции. Они могут случаться спонтанно в связи с болезнью Паркинсона, но могут также быть индуцированы лекарственными средствами. Среди нарушений локомоции, индуцированных лекарственными средствами, можно упомянуть, в частности, нарушения, индуцируемые нейролептиками или антагонистами дофамина, или L-ДОФА-индуцированные дискинезии и дистонии.
Для приготовления терапевтических агентов по изобретению предпочтительно использовать соединения общей формулы (III), в которых
- R выбран из водорода, C1-C6-алкила, фтора, хлора и брома,
- R1 выбран из водорода, C1-C6-алкокси, C1-C6-алкила, фтора, хлора, брома и трифторметила, и
- каждый из R2 и R3 независимо выбран из водорода, C1-C6-алкилокси, C1-C6-алкила, фтора, хлора, брома и трифторметила.
Предпочтительно также использовать соединения формулы (III), в которых
- заместитель R1 находится в положении 5 или 6 гетероцикла, и
- заместители R2 и R3 находятся соответственно в положениях 2 или 3 или соответственно в положениях 2 или 4 фенильного кольца, и в случае, когда один из двух заместителей R2 и R3 является атомом водорода, соответственный другой заместитель находится в положении 2 фенильного кольца.
Предпочтительным соединением общей формулы (III) для приготовления терапевтических агентов по данному изобретению, в частности для лечения L-ДОФА-индуцированной дискинезии, является нижеследующее соединение:
(В24): N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамид.
Соединения формул (I)-(IV) были получены способами, описанными в литературе (Glennon, R. A. et al. J.Med. Chem. 1988, 31, 1968-1971).
Для этой цели кислотные производные типа (А), которые либо были приобретены, либо были синтезированы, как описано в литературе, активировали в форме хлорангидридов их карбоновых кислот и подвергали взаимодействию со свободным основанием типа (В) с получением производных формулы (I) (в том числе (Ia), (Ib) и (Ic)), (III) или (IV)
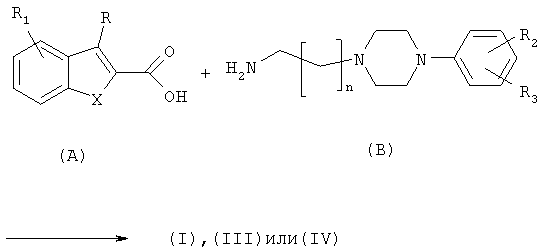
где n, R, R1, R2 и R3 такие, как определено выше для (I), (III) и (IV) соответственно.
В качестве альтернативы вышеупомянутому способу активации кислотных производных можно использовать другие реакции, например активацию кислот гидроксиазабензтриазолом (Kienhofer, A. Synlett 2001, 1811-1812). Например, соединения формулы (II) могут быть получены активацией ферроцен-2-карбоновой кислоты HATU (О-(7-азабензотриазол-1-ил)-N, N, N', N'-тетраметилурония гексафторфосфатом) с последующим взаимодействием с основаниями типа (В).
Коммерчески доступные 2-метокси- или 2,3-дихлорфенилпиперазины могут быть алкилированы бромбутилфталимидом в ксилоле с получением арилпиперазиниламинов типа (В). Последующий гидразинолиз фталимидзамещенных структур дает первичные амины типа (В). Это иллюстрируется следующей иллюстративной реакционной схемой:
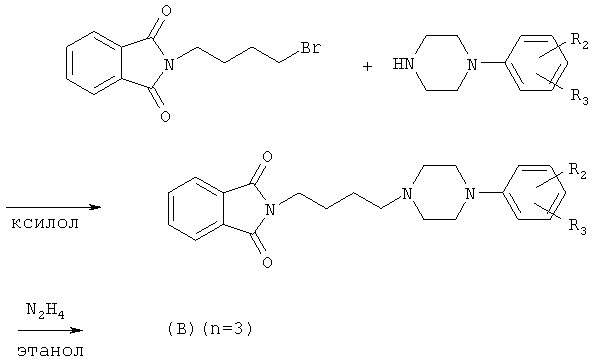
ПРИМЕРЫ
Синтез аминов типа (В)
4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутиламин
2,3 г (10 ммоль) 2,3-дихлорфенилпиперазина в форме свободного основания растворяют в 10 мл ксилола и нагревают до 70°С. Затем 1,4 г (5 ммоль) 4-бромбутилфталимида растворяют в 20 мл ксилола и медленно по каплям добавляют в раствор пиперазина. Эту реакционную смесь нагревают при 125°С течение 24 часов. После охлаждения до 0°С смесь фильтруют и фильтрат упаривают. Полученный N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутилфталимид очищают флэш-хроматографией на SiO2 с использованием этилацетата. Выход 4,0 г (92%).
Раствор 80% гидразингидрата (0,45 мл, 2,5 экв.) в 5 мл этанола по каплям добавляют в суспензию N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутилфталимида в 40 мл этанола. Эту смесь нагревают при температуре дефлегмации в течение 3 часов, затем охлаждают до комнатной температуры, выпавшее в осадок твердое вещество отфильтровывают и этанольный раствор упаривают в вакууме.
Очистка флэш-хроматографией с использованием СН2CCl2-МеОН-Me2EtN:90-8-2 дает основание 4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутиламин с выходом 900 мг (60%).
МС (масс-спектр): m/z 301 (M+); ИК (инфракрасный спектр): (NaCl): 3397; 2939; 2817; 1641; 1572; 1500; 1482; 1452; 1376; 1240; 1152; 1118; 1023; 917; 791; 749; 698; 661. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д. (миллионные доли)): 1.48-1.64 (m, 4H, CH2-CH2); 2.41-2.46 (t, J=7.6, 2Н, CH2N); 2.64 (m, 4H, пиперазин); 2.72-2.76 (m, 2Н, CH2NCO); 3.07 (m, 4H, пиперазин); 6.93-6.99 (m, 1H, Н5, фенил); 7.11-7.17 (m, 2H, H4, Н6, фенил).
Пример 1
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]тиофенилкарбамид
0,4 ммоль бензтиофен-2-карбоновой кислоты (0,071 г) растворяют в 4 мл сухого толуола и 4 мл сухого хлороформа. Добавляют 0,02 мл сухого диметилформамида (DMF) и 0,11 мл (1,51 ммоль) SOCI2, а затем нагревают в масляной бане до 90°С в течение 30 минут. Растворитель затем удаляют отгонкой на роторном испарителе и сушат в глубоком вакууме. Хлорангидрид кислоты растворяют в 40 мл хлороформа и добавляют при перемешивании при 0°С к раствору 0,4 ммоль 4-(4-(2-метоксифенил)пиперазин-1-ил)бутиламина (0,105 г) и 0,17 мл Et3N в 5 мл хлороформа. После взаимодействия в течение 14 часов реакционную среду промывают водным раствором NaHCO3, органический растворитель сушат с использованием MgSO4 и выпаривают в вакууме. Очистка флэш-хроматографией на силикагеле с использованием CH2Cl2-МеОН:9-1 дает 114 мг (выход 68% за 2 реакцирнные стадии) N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-бенз[b]тиофенилкарбамида.
Т.пл. 147°С; МС: m/z 423 (М+); ИК (NaCl): 3316; 2938; 2817; 1735; 1629; 1544; 1500; 1241; 1026; 731. 1Н-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.65-1.74 (m, 4H, CH2-CH2); 2.47 (t, 2H, CH2N, J=6.7 Гц); 2.65 (m, 4H, пиперазин); 3.08 (m, 4H, пиперазин); 3.48-3.53 (m, 2H, CH2NCO); 3.85 (s, 3H, ОСН3); 6.72 (t, 1H, NH, J=4.3 Гц); 6.84-7.01 (m, 4H, фенил); 7.36-7.44 (m, 2H, H5, H6); 7.76 (s, 1H, Н3); 7.79-7.85 (m, 2H, Н7, H4). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 162.4; 152.3; 141.2; 140.7; 139.1; 138.7; 126.2; 125.0; 124.9; 122.9; 122.7; 120.9; 118.2; 111.2; 57.9; 55.3; 53.4; 50.5; 40.0; 27.4; 24.3.
С Н N (%): C24H29N3O2S
Рассчитано: С 68,05; Н 6,90; N 9,92; S 8.15. Найдено: С 68,11; Н 6,95; N 9,93; S 8,09.
Пример 2
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]тиофенилкарбамид
Синтез аналогичен примеру 1.
Выход 126 мг (68% за 2 реакционные стадии).
Т.пл. 153°С. МС: m/z 462 (M+). ИК (NaCl): 3298; 2967; 2934; 2809; 1640; 1599; 1576; 1530; 1442; 1420; 1301; 1167; 1131; 962; 882; 808; 781; 712. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.63-1.76 (m, 4H, СН2-СН2); 2.48 (t, J=6.9 Гц, 2Н, CH2N); 2.66 (m, 4H, пиперазин); 3.05 (m, 4H, пиперазин); 3.49-3.54 (m, 2H, CH2NCO); 6.79 (br, t, J=5.3 Гц, 1Н, NH); 6.84-6.86 (dd, J=1.6 Гц, J=7.5 Гц, 1Н, фенил); 7.08-7.16 (m, 2H, фенил); 7.37-7.44 (m, 2H, H5, H6); 7.77-7.78 (s, 1H, Н3); 7.80-7.90 (m; 2H, Н4, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 157.9; 156.1; 152.3; 151.1; 141.2; 129.9; 127.8; 123.0; 121.0; 11-8.2; 113.0; 112.3; 106.6; 109,7; 107.9; 57.9; 53.5; 50.5; 39.4; 27.4; 24.3.
С Н N (%): C23H25CI2N3OS
Рассчитано: С 60,25; Н 6,11; N 8,78. Найдено: С 59,94; Н 6,04; N 8,81.
Пример 3
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]фуранилкарбамид
Синтез аналогичен примеру 1.
Выход 75,2 мг (выход 56% за 2 реакционные стадии).
Т.пл. 121°С. МС: m/z 431 (М+). ИК (NaCl): 3311,2; 3060; 2937; 2815; 2216; 1654; 1592; 1500; 1321; 1240; 1178; 1145; 748.
1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.67-1.74 (m, 4H, СН2-СН2); 2.49 (t, 2H, CH2N, J=6.9 Гц); 2.69 (m, 4H, пиперазин); 3.13 (m, 4H, пиперпзин); 3.56-3.50 (m, 2H, CH2NCO); 3.86 (s, 3Н, ОСН3); 6.85-6.87 (m, 1H, фенил); 6.90-6.93 (m, 2H фенил); 6.99-7.02 (m, 2H, фенил и NH); 7.26-7.31 (m, 1H, Н3); 7.37-7.42 (m, 1H, Н6); 7.46-7.48 (m, 2H, Н4, Н3); 7.77-7.79 (m, 1H, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 158.9; 154.7; 152.3; 148.9; 141.3; 127.7; 126.7; 123.6; 122.9; 122.7; 120.9; 118.2; 111.7; 111.2; 110.2; 58.0; 55.3; 53.5; 50.5; 39.2; 27.5; 24.3.
С Н N (%): C24H29N3O3·0,3H2O
Рассчитано: С 69,81; Н 7,23; N 10,18. Найдено: С 69,84; Н 7,33; N 10,21.
Пример 4
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]фуранилкарбамид
Синтез аналогичен примеру 1.
Выход 105 мг (выход 58% за 2 реакционные стадии).
Т.пл. 150°С. МС: m/z 446 (M+). ИК (NaCl): 3310; 2939; 2819; 1652; 1595; 1577; 1520; 1448; 1421; 1299; 1257; 1241; 1176; 1141; 1044; 960; 908; 780; 748; 713, 669, 645. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.67-1.75 (m, 4H, СН2-СН2); 2.52 (t, J=6.7 Гц, 2Н, CH2N); 2.69 (m, 4 Н, пиперазин); 3.13 (m, 4H, пиперазин); 3.51-3.56 (m, 2H, CH2NCO); 6.92-6.95 (dd, J=2.3 Гц, 7.3 Гц, 1Н, фенил); 7.00 (brt, J=4.3 Гц, 1Н, NHCO); 7.10-7.17 (m, 2H, фенил); 7.26-7.31 (m, 1H, Н4); 7.38-7.43 (m, 1H, Н6); 7.46-7.48 (m, 2H, Н3, H5); 7.66-7.68 (m; 1H, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 158.9; 154.7; 151.2; 148.2; 134.0; 127.7; 127.5; 127.4; 126.8; 124.6; 123.7; 122.7; 118.6; 111.6; 110.2; 57.9; 53.3; 51.1; 39.2; 27.5; 24.2.
С Н N (%): С23Н25Cl2N3O2
Рассчитано: С 61,89; Н 5,65; N 9,41. Найдено: С 61,74; Н 5,86; N 9,05.
Пример 5
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]фуранилкарбамид
Синтез аналогичен примеру 1. 5-Бром-2-бензо[b]фуранилкарбоновую кислоту получали способом, описанным в литературе (Dann, О. Liebigs Ann. Chenz. 1986,438-455).
Выход 107,8 мг (выход 56% за 2 реакционные стадии).
Т.пл. 124°С. МС m/z 485 (М+). ИК (NaCl): 3450,0; 3289,9; 3068,2; 2927,4; 2765; 1650; 1567; 1535; 1500; 1438; 1238; 1178; 1022; 802; 748. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.67-1.74 (m, 4H, СН2-СН2); 2.49 (t, J=6.9 Гц, 2H, CH2N); 2.69 (m, 4H, пиперазин); 3.13 (m, 4H, пиперазин); 3.56-3.60 (m, 2H, CH2NCO); 3.86 (s, 3Н, ОСН3); 6.85-6.87 (m, 1H, фенил); 6.91-6.93 (m, 2H, фенил); 6.97-7.00 (m, 1H, фенил); 7.00 (brt, J=4.8 Гц, 1H, NH); 7.32-7.35 (d, J=8.9 Гц, 1H, H4); 7.38-7.39 (m, 1H, Н3); 7.48 (dd, J=8.7 Гц, J=2.0 Гц, 1H, H6); 7.79-7.80 (m, 1H, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 158.4; 153.3; 152.3; 150.1; 141.2; 129.7; 129.6; 125.2; 122.9; 120.9; 120.9; 118.2; 116.7; 113.1; 111.2; 109.4; 64.8; 57.9; 55.3; 53.5; 50.4; 39.3; 27.5; 24.3.
С Н N (%): С24Н29BrN3O2
Рассчитано: С 59,26; Н 5,80; N 8,64. Найдено: С 59,05; Н 5,81; N 8,68.
Пример 6
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]фуранилкарбамид
Синтез аналогичен примеру 5.
Выход 102 мг (выход 47% за 2 реакционные стадии).
Т.пл. 145°С. МС m/z 524 (M+); ИК (NaCl): 3400; 2937; 2815; 2227; 1666; 1594; 1527; 1500; 1294; 1240; 1141; 1118; 1025; 842; 746. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.63-1.74 (m, 4H, СН2-СН2); 2.49-2.52 (t, J=6,7 Гц, 2Н, CH2N); 2.68 (m, 4H, пиперазин); 3.09 (m, 4H, пиперазин); 3.49-3.56 (m, 2H, CH2NCO); 6.92-6.94 (dd, J=2.1 Гц, J=7.5 Гц, 1Н, фенил); 6.98-7.01 (brt, J=3.0 Гц, 1Н, NH); 7.33-7.36 (d, J=5.3 Гц, 1Н, Н4); 7.39 (m, 1Н, Н3); 7.48-7.51 (dd, J=8.7 Гц, J=2.0 Гц, 1Н, H6); 7.80-7.81 (d, J=2.0 Гц; 1Н, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 157.9; 156.1; 152.3; 151.1; 141.2; 129.9; 127.8; 123.0; 121.0; 118.2; 113.0; 112.3; 106.6; 109.7; 107.9; 57.9; 55.4; 53.5; 50.5; 39.4; 27.4; 24.3; 21.0.
С Н N (%): С23Н24BrCl2N3O2
Рассчитано: С 52,57; Н 4,67; N 8,03. Найдено: С 52,63; Н 4,67; N 8,03.
Пример 7
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-5-циано-2-бензо[b]фуранилкарбамид
0,37 ммоль (141 мг) HATU и 0,37 ммоль (69 мг) 5-циано-2-бензо[b]фуранилкарбоновой кислоты (Dann, O. Liebigs Ann. Chem. 1986, 438-455) растворяют в 1 мл DMF при 0°С и добавляют 0,74 ммоль (0,13 мл) диизопропилэтиламина (DIEA). Затем 0,33 ммоль (87 мг) 4-(4-(2-метоксифенил)пиперазин-1-ил)бутиламина растворяют в DMF и по каплям добавляют в реакционный раствор при 0°С. Через один час реакционную среду переносят в CHCl3 и промывают раствором NaHCO3 и водой. После сушки с использованием MgSO4 растворитель выпаривают и остаток очищают флэш-хроматографией (SiO2; петролейный эфир-этилацетат: 1-1, затем этилацетат).
Выход 41 мг (28%).
Т.пл. 96°С. МС m/z 432 (М+). ИК (NaCl): 3400; 2937; 2815; 2227; 1666; 1594; 1527; 1500; 1294; 1240; 1141; 1118; 1025; 842; 746.
1H-ЯМР (CDCl3, 360 МГц) δ (м.д.): 1.67-1.74 (m, 4H, CH2-CH2); 2.49 (t, J=6.9 Гц, 2Н, CH2N); 2.69 (m, 4Н, пиперазин); 3.13 (m, 4H, пиперазин); 3.56-3.60 (m, 2H, CH2NCO); 3.86 (s, 3Н, ОСН3); 6.84-7.02 (m, 4H, фенил); 7.12-7.15 (brt, J=5.1 Гц, 1Н, NH); 7.50-7.51 (m, 1H, Н4); 7.55-7.57 (m, 1H, Н3); 7.65-7.68 (m, 1H, H6); 8.03-8.04 (m, 1H, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 157.9; 156.1; 152.3; 151.1; 141.2; 129.9; 127.8; 123.0; 121.0; 118.2; 113.0; 112.3; 106.6; 109.7; 107.9; 57.9; 55.4; 53.5; 50.5; 39.4; 27.4; 24.3; 21.0.
Пример 8
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]теллурофенилкарбамид
Синтез аналогичен примеру 7.
Выход 73 мг (58%).
Т.пл. 85°С. МС m/z 521 (М+). ИК (KBr): 3320; 3047; 2933; 2815; 1616; 1566; 1541; 1375; 1498; 1240; 1023; 748.
1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.):1.62-1.66 (m, 4H, СН2-СН2); 2.42-2.45 (t, J=6.7 Гц, 2H, CH2N); 2.63 (m, 4H, пиперазин); 3.04 (m, 4H, пиперазин); 3.38-3.43 (m, 2H, CH2NCO); 3.78 (s, 3H, ОСН3); 6.70-6.76 (brt, J=4.3 Гц, 1H, NH); 6.77-6.83 (m, 3Н, фенил); 6.94-6.96 (m, 1H, фенил); 7.09-7.14 (m, 1H, H6); 7.28-7.32 (m, 1H, Н5); 7.74-7.76 (d, J=7,5 Гц, 1H, Н4); 7.84-7.86 (d, J=7.8 Гц, 1H, Н7); 8.13 (s, 1H, Н3). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 166.1; 152.3; 147.9; 141.2; 140.2; 134.8; 132.3; 129.3; 125.8; 125.5; 122.9; 121.0; 118.2; 111.2; 57.9; 55.3; 53.3; 50.5; 40.4; 27.4; 24.4.
Пример 9
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]теллурофенилкарбамид
Синтез аналогичен примеру 7.
Выход 92 мг (45%)
Т.пл. 92°С. МС m/z 560 (М+). ИК (NaCl): 3288; 2938; 2819; 1651; 1578; 1557; 1448; 1242; 1044; 734. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.63-1.74 (m, 4H, СН2-СН2); 2.48-2.52 (t, J=7.1 Гц, 2H, CH2N); 2.66 (m, 4H, пиперазин); 3.05 (m, 4 Н, пиперазин); 3.46-3.51 (m, 2H, CH2NCO); 6.70-6.72 (brt, J=4.8 Гц, 1Н, NH); 6.83-6.86 (dd, J=1.8 Гц, J=7.8 Гц, 1Н, фенил); 7.07-7.22 (m, 3H, фенил, H6); 7.36-7.41 (m, 1H, Н5); 7.81-7.83 (d, J=7.6 Гц, 1H, H4); 7.91-7.94 (d, J=7.6 Гц, 1H, Н7); 8.17 (m, 1Н, Н3). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.):166.1; 151.1; 147.9; 140.2; 135.0; 134.9; 134.0; 132.3; 129.2; 127.5; 127.4; 125.8; 125.5; 124.6; 118.6; 58.0; 53.3; 51.2; 40.4; 27.5; 24.4.
Пример 10
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-2-индолилкарбамид
Синтез аналогичен примеру 1.
Выход 48 мг (выход 58% за две реакционные стадии).
Т.пл. 148°С. МС m/z 444 (M+). ИК (NaCl): 3258; 3059; 2938; 2821; 1636; 1577; 1555; 1507; 1448; 1420; 1308; 1241; 1139; 1044; 961; 908; 779; 747; 733; 669; 647. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.67-1.74 (m, 4H, СН2-СН2); 2.47-2.51 (t, J=6.9 Гц, 2Н, СН2N); 2.67 (m, 4H, пиперазин); 3.13 (m, 4H, пиперазин); 3.53-3.55 (m, 2H, CH2NCO); 6.59-6.66 (brt, J=4.3 Гц, 1H, NHCO); 6.85 (s, 1H, Н3); 6.90-6.93 (m, 1H, фенил); 7.07-7.17 (m, 3H, фенил, Н3); 7.28-7.30 (m, 1H, Н6); 7.43-7.46 (m, 1H, Н7); 7.62-7.65 (m, 1H, Н4); 9.56 (s, 1H, NH). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 161.7; 160.4; 151.1; 136.2; 134.0; 130.9; 127.5; 127.4; 121.8; 120.8; 118.5; 111.9; 101.8; 68.2; 57.9; 53.3; 51.1; 39.5; 27.5; 24.3.
Пример 11
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-циан-2-индолилкарбамид
Синтез аналогичен примеру 7.
Выход 109 мг (42%).
Т.пл. 170°С. МС m/z 431 (М+). 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.74-1.78 (m, 4H, СН2-СН2); 2.54-2.65 (t, J=6.7 Гц, 2H; CH2N); 2.79 (m, 4H, пиперазин); 3.17 (m, 4H, пиперазин); 3.55-3.59 (m, 2H, CH2NCO); 3.85 (s, 3H, ОСН3); 6.84-6.87 (d, J=8.5 Гц, 1H, Н3); 6.88-6.90 (m, 3H, фенил); 6.99-7.05 (m, 2H, фенил, Н4); 7.07-7.12 (brt, J=3.9 Гц, 1H, NHCO); 7.47-7.50 (dd, J=1.4 Гц, J=8.5 Гц, 1H, H6); 7.52-7.54 (d, J=8.5 Гц, 1H, Н7); 8.01 (s, 1H, Н3); 10.14 (s, 1H, NH). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 152.2; 140.7; 137.7; 133.3; 127.8; 127.3; 126.7; 123.4; 121.1; 120.2; 118.3; 111.3; 103.9; 102.9; 57.6; 55.4; 53.5; 50.0; 39.2; 27.0; 24.2.
Пример 12
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-5-бром-2-индолилкарбамид
Синтез аналогичен примеру 7.
Выход 112 мг (60%).
Т.пл. 188°С. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.64-1.74 (m, 4H, СН2-СН2); 2.46-2.51 (t, J=7.1 Гц, 2Н, CH2N); 2.68 (m, 4H, пиперазин); 3.12 (m, 4H, пиперазин); 3.49-3.64 (m, 2H, CH2NCO); 3.83 (s, 3H, ОСН3); 6.68-6.71 (brt, J=5.3 Гц, 1Н, NHCO); 6.76-6.77 (d, J=1.8 Гц, 1Н, Н4); 6.85-6.87 (d, J=7.8 Гц, 1Н, фенил); 6.92-6.93 (d, J=3.9 Гц, 2H, фенил); 6.98-7.03 (m, 1H, фенил); 7.31-7.38 (m, 2H, Н6, Н7); 7.76-7.77 (m, 1H, Н3); 9.64 (s, 1H, NH).
Пример 13
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-6-циан-2-индолилкарбамид
Синтез аналогичен примеру 1.
Выход 112 мг (выход 58% за 2 реакционные стадии).
Т.пл. 174°С. МС m/z 431 (M+). ИК (NaCl): 2940; 2909; 2803; 2753; 2216; 1645; 1548; 1498; 1321; 1237; 1148; 820; 754; 742. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.67-1.82 (m, 4H, СН2-СН2); 2.47-2.51 (t, J=6.7 Гц, 2H, CH2N); 2.66 (m, 4H, пиперазин); 3.68-3.70 (m, 2H, CH2NCO); 3.85 (s, 3H, ОСН3); 3.09 (m, 4H, пиперазин); 6.84-6.94 (m, 4H, фенил, Н3); 6.99-7.02 (m, 1H, фенил); 7.13-7.16 (brt, J=5.5 Гц, 1H, NHCO); 7.31-7.34 (m, 1H, Н3); 7.67-7.69 (d, J=8.5 Гц, Н4); 7.84 (s, 1H, Н7); 11.22 (s, 1H, NH). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 161.2; 152.2; 141.1; 135.2; 134.3; 130.5; 123.0; 122.9; 122.7; 120.9; 120.2; 118.1; 117.4; 111.2; 106.6; 102.2; 57.8; 55.3; 53.8; 53.4; 50.4; 39.8; 30.1; 27.3; 24.3.
CHN (%): C25H29N5O2·1,4Н2O
Рассчитано: С 65,74; Н 7,02; N 15,33. Найдено: С 65,98; Н 7,30; N 14,87.
Пример 14
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-индолилкарбамид
0,24 ммоль (58 мг) HATU, 0,24 ммоль HOAt (33 мг) и 0,24 ммоль (69 мг) 5-бром-2-индолкарбоновой кислоты растворяют в 5 мл DMF при 0°С и добавляют 0,48 ммоль (0,094 мл) DIEA. Затем 0,26 ммоль (78 мг) 4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутиламина растворяют в DMF и по каплям добавляют в реакционный раствор при 0°С. Через три часа реакционную среду переносят в CHCl3 и промывают раствором NaHCO3 и водой. После сушки с использованием MgSO4 растворитель выпаривают и остаток очищают флэш-хроматографией (SiO2; CHCl3:ММ, 98:2). Выход 94 мг (74%).
МС m/z 524 (М+). ИК (NaCl): 3234; 2932, 2821; 1637; 1577; 1545; 1282; 1046; 733. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.57-1.73 (m, 4H, CH2-CH2); 2.51 (t, J=6.9 Гц, 2Н, CH2N); 2.66 (m, 4H, пиперазин); 3.07 (m, 4H, пиперазин); 3.51-3.63. (m, 2H, CH2NCO); 6.64 (brt, J=5.3 Гц, 1Н, NHCO); 6.77 (d, J=1.8 Гц, 1Н, фенил, Н4); 6.90 (dd, J=2.1 Гц, J=7.5 Гц, 1Н, фенил); 7.10-7.17 (m, 2H, фенил); 7.31-7.38 (m, 2H, Н6, Н3); 7,76-7,77 (m, 1H, Н7); 9.68 (s, 1H, NH).
Пример 15
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-6-циано-2-индолилкарбамид
Синтез аналогичен примеру 7.
Выход 102 мг(59%).
Т.пл. 174°С. МС m/z 470(M+). ИК (NaCl): 3215; 2926; 2821; 1634; 1570; 1506; 1239; 1034; 734. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.69-1.82 (m, 4H, СН2-СН2); 2.51 (t, J=6.9 Гц, 2H, СН2N); 2.66 (m, 4H, пиперазин); 3.06 (m, 4H, пиперазин); 3.58-3.63 (m, 2H, CH2NCO); 6.85 (brt, J=5.5 Гц, 1H, NHCO); 6.88-6.91 (m, 2H, фенил, Н3); 7.09-7.17 (m, 2H, фенил); 7.35 (dd, J=1.4 Гц, J=8.2 Гц, 1Н, H5); 7.70 (d, J=8.5 Гц, Н4); 7.84 (s, 1H, Н7); 10.65 (s, 1H, NH).
Пример 16
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-2-ферроценилкарбамид
Синтез аналогичен примеру 7.
Выход 155 мг (71%).
МС m/z 475 (М+). ИК (NaCl): 3318, 2939, 2816, 1630, 1543, 1500, 1241, 1027, 748. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.66-1.69 (m, 4H, CH2-CH2); 2.57 (t, J=6.7 Гц, 2H, CH2N); 2.77 (m, 4H, пиперазин); 3.16 (m, 4H, пиперазин); 3.39-3.44 (m, 2H, CH2NCO); 3.86 (s, 3Н, ОСН3); 4.17-4.21 (m, 3H, Ferr); 4.32-4.33 (m, 2H, Ferr); 4.68-4.69 (m, 2H, Ferr); 6.02 (brt, J=5.3 Гц, 1H, NH); 6.85-6.94 (m, 3H, фенил); 6.99-7.03 (m, 1H, фенил). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 170.3; 152.2; 140.9; 123.1; 120.9; 118.3; 111.2; 77.2; 76.3; 70.3; 69.7; 68.1; 57.9; 55.3; 53.4; 50.1; 39.2; 27.7; 23.8.
Пример 17
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-2-ферроценилкарбамид
Синтез аналогичен примеру 7.
Выход 85 мг (69%).
МС m/z 514 (M+). 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.63-1.66 (m, 4H, СН2-СН2); 2.48 (t, J=6.9 Гц, 2Н, CH2N); 2.65 (m, 4H, пиперазин); 3.08 (m, 4H, пиперазин); 3.39-3.44 (m, 2H, СН2NCO); 4.17-4.21 (m, 3H, Ferr); 4.33-4.34 (m, 2H, Ferr); 4.64-4.65 (m, 2H, Ferr); 5.38 (brt, J=5.1 Гц, 1H, NH); 6.92-6.98 (m, 1H, фенил); 7.11-7.17 (m, 2H, фенил).
Пример 18
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-5-циано-2-бензо[b]тиофенилкарбамид
Растворяют 0,012 ммоль (94 мг) HATU и 0,012 ммоль (25 мг) 5-циано-2-бензо[b]тиофенкарбоновой кислоты (Bridges, A.J.Tetr. Lett. 1992, 7499-7502) в 1 мл DMF и 4 мл CH2Cl2 при 0°С и добавляют 0,024 ммоль (0,06 мл) DIEA. Затем 0,013 ммоль (34 мг) 4-(4-(2-метоксифенил)пиперазин-1-ил)бутиламина растворяют в СН2Cl2 и по каплям добавляют в реакционный раствор при 0°С. Через два часа реакционную среду переносят в CHCl3 и промывают раствором NaHCO3 и водой. После сушки с использованием MgSO4 растворитель выпаривают и остаток очищают флэш-хроматографией (SiO2; метиленхлорид-метанол : 98-2).
Выход 60 мг (91%).
Т.пл. 147°С. МС m/z 448 (М+). ИК (KBr): 3336; 2929; 2816; 2225; 1635; 1500; 1240; 1028; 750. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.73-1.77 (m, 4H, СН2-СН2); 2.59 (t, J=6.4 Гц, 2H, CH2N); 2.78 (m, 4H, пиперазин); 3.14 (m, 4H, пиперазин); 3.49-3.53 (m, 2H, CH2NCO), 3.85 (s, 3H, ОСН3); 6.84-6.92 (m, 5H, фенил, NH); 6.99-7.04 (m, 1H, фенил); 7.60 (dd, J=1.4 Гц, J=8.5 Гц, 1Н, H6); 7.88 (s, 1H, Н3); 7.95 (d, J=8.5 Гц, 1H, Н7); 8.12 (d, J=1.1 Гц, 1H, H4). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 170.3; 152.2; 140.9; 123.1; 120.9; 118.3; 111.2; 77.2; 76.3; 70.3; 69.7; 68.1; 57.9; 55.3; 53.4; 50.1; 39.2; 27.7; 23.8.
CHN (%) С24Н25Cl2N5O·1Н2O
Рассчитано: С 64,35; Н 6,48; N 12,01; S 6.87. Найдено: С 64,59; Н 6,13; N 11,77; S 6,44.
Пример 19
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-5-циан-2-бензо[b]тиофенилкарбамид
Синтез аналогичен примеру 18.
Выход 57 мг (96%).
Т.пл. 190°С. МС m/z 487 (М+). ИК (KBr): 3319; 2929; 2819; 2227; 1633; 1560; 1448; 1242; 1045; 755. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.65-1.76 (m, 4H, СН2-СН2); 2.49 (t, J=6.7 Гц, 2Н, CH2N); 2.65 (m, 4H, пиперазин); 3.04 (m, 4H, пиперазин); 3.49-3.55 (m, 2H, CH2NCO); 6.78 (br, t, J=5.0 Гц, 1Н, NH); 6.85 (dd J=1.8 Гц, J=7.8 Гц, 1H, фенил); 7.09-7.17 (m, 2H, фенил); 7.62 (dd, J=1.4 Гц, J=8.5 Гц, 1H, Н6); 7.77 (s, 1H, Н3); 7.95 (d, J=8.2 Гц, Н7); 8.13 (d, J=1.4 Гц, 1H, H4). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 161.4; 151.1; 144.5; 142.0; 138.8, 134.1; 129.4, 127.9; 127.5, 127.4; 124.7; 123.9; 123.8; 118.9; 118.4; 108.9; 57.9; 53.3; 51.2; 40.2; 27.4; 24.3.
С Н N (%) С20Н26Cl2N4OS.1,46Н2O
Рассчитано: С 56,11; Н 5,28; N 10,90. Найдено: С 56,51; Н 5,06; N 10,45.
Пример 20
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-6-циано-2-бензо[b]тиофенилкарбамид
Синтез аналогичен примеру 18.
Выход 30 мг (43%).
Т.пл. 124°С. МС m/z 448 (М+). ИК (KBr): 3290; 2937; 2816; 2225; 1619; 1543; 1500; 1242; 1026; 751. 1H-ЯМР (COCl3, 360 Мгц) δ (м.д.): 1.72-1.90 (m, 4H, СН2-СН2); 2.90 (t, J=7.3 Гц, 2H, CH2N); 3.15 (m, 4H, пиперазин); 3.31 (m, 4H, пиперазин); 3.50-3.56 (m, 2H, CH2NCO), 3.82 (s, 3Н, ОСН3); 6.84-6.92 (m, 3H, фенил); 7.01-7.07 (m, 1H, фенил); 7.13 (br, t, J=5.7, 1H, NH); 7.53 (dd, J=1.4 Гц, J=8.2 Гц, 1H, Н5); 7.84 (d, J=7.8 Гц, 1H, Н4); 7.84 (s, 1H, Н3); 8.10-8.11 (m, 1H, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 161.5; 152.3; 141.9; 141.0; 140.4; 127.5; 127.4; 125.6; 124.2; 123.1; 120.9; 118.8; 11,8.1; 111.3; 109.5; 77.2; 76.3; 70.3; 69.7; 68.1; 57.9; 55.3; 53.4; 50.4; 40.1; 27.3; 24.2.
Пример 21
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-6-циано-2-бензо[b]тиофенилкарбамид
Синтез аналогичен примеру 18.
Выход 26 мг (43%).
Т.пл. 137°С. МС m/z 486 (М+). ИК (KBr): 3335; 2933; 2821; 2226; 1638; 1544; 1448; 1242; 1044; 735. 1H-ЯМР (COCl3, 360 Мгц) δ (м.д.): 1.67-1.74 (m, 4H, СН2-СН2); 2.49 (t, J=6.4 Гц, 2Н, CH2N); 2.65 (m, 4H, пиперазин); 3.04 (m, 4H, пиперазин); 3.49-3.54 (m, 2H, CH2NCO); 6.75 (br, t, J=4.1 Гц, 1Н, NH); 6.84 (dd, J=1.8 Гц, 7.8 Гц, 1Н, фенил); 7.08-7.17 (m, 2H, фенил); 7.60-7.62 (m, 1H, H5); 7.78 (s, 1H, Н3); 7.88-7.90 (m, 1H, Н4); 8.19 (br, s, 1H, Н7). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 161.4; 151.1; 143.6; 141.8; 140.3; 134.1; 127.5; 127.4; 125.2; 124.7; 124.2; 118.7; 118.4; 109.5; 109.5; 58.0; 53.3; 51.3; 51.2; 40.3; 27.4; 24.3.
С Н N (%): С24Н25Cl2N5O·Н2O
Рассчитано: С 59,02; Н 5,57; N 14,34.
Найдено: С 58,76; Н 5,30; N 14,19.
Пример 22
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]тиофенилкарбамид
Синтез аналогичен примеру 7.
Выход 73 мг (58%).
Т.пл. 156°С. МС m/z 502 (М+). ИК (КВг): 3316; 2934; 2821; 1633; 1558; 1500; 1242; 1026; 750. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.69-1.72 (m, 4H, СН2-СН2); 2.57 (t, J=6.5 Гц, 2H, CH2N); 2.77 (m, 4H, пиперазин); 3.12 (m, 4H, пиперазин); 3.49-3.51 (m, 2H, C2NCO); 3.85 (s, 3 Н, ОСН3); 6.83-6.91 (m, 4H, фенил); 7.01-7.06 (m, 1H, фенил); 7.15 (brt, J=4.9 Гц, 1H, NH); 7.42 (dd, J=8.5 Гц, J=1.8 Гц, 1H, H6); 7.60 (d, J=8.5 Гц, 1H, Н7); 7.73 (s, 1H, Н3); 7.86 (d, J=1.7 Гц, 1H, Н4).
13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 170.3; 152.2; 140.9; 123.1; 120.9; 118.3; 111.2; 77.2; 76.3; 70.3; 69.7; 68.1; 57.9; 55.3; 53.4; 50.1; 39.2; 27.7; 23.8.
С Н N (%): С24Н28BrN3O2S
Рассчитано: С 57,37; Н 5,62; N 8.36. Найдено: С 65,98; Н 7,30; N 14.87.
Пример 23
N-4-(4-(2,3-Дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]тиофенилкарбамид
Синтез аналогичен примеру 7.
Выход 78 мг (60%).
Т.пл. 178°С. МС m/z 541 (М+). ИК (KBr): 3316; 2929; 2821; 1631; 1560; 1242; 1068; 756. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.63-1.69 (m, 4H, СН2-СН2); 2.48 (t, J=6.7 Гц, 2Н, CH2N); 2.64 (m, 4H, пиперазин); 3.04 (m, 4H, пиперазин); 3.48-3.53 (m, 2Н, CH2NCO); 6.71 (br, t, J=5.1 Гц, 1H, NH); 6.83-6.86 (m, 1H, фенил); 7.09-7.17 (m, 2H, фенил); 7.51 (dd, J=1.8 Гц. J=8.5 Гц, 1H, H6); 7.67 (s, 1H, Н3); 7.72 (d, J=8.5 Гц, 1H, Н7); 7.95 (d, J=1.8 Гц, 1H, Н4). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 161.9; 160.8; 140.7; 140.6. 139.2; 134.1; 129.3; 127.4; 127.3; 124.6; 124.1:123.8.118.9; 118.5; 57.9; 55.3; 51.2; 40.2; 27.5; 24.4.
С Н N (%): С23Н24BrCl2N3OS·0,25Н2O
Рассчитано: С 50,61; Н 4,52; N 7,70; S 5,87;
Найдено: С 50,61; Н 4,49; N 7,64; S 5,87.
Пример 24
N-4-(4-(2-Метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамид
Синтез аналогичен примеру 7.
Выход 89 мг (55%).
МС m/z 406 (М+). ИК (NaCl): 3251; 3055; 2935; 2809; 1639; 1549; 1241; 1016; 746. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.67-1.74 (m, 4H, СН2-СН2); 2.48 (t, J=6.7 Гц, 2H, CH2N); 2.67 (m, 4H, пиперазин); 3.11 (m, 4H, пиперазин); 3.51-3.56 (m, 2H, CH2NCO); 3.85 (s, 1H, ОСН3); 6.59 (br, t, J=4.9 Гц, 1Н, NHCO); 6.83-6.94 (m, 3H, фенил); 6.97-7.02 (m, 1H, фенил); 7.11-7.15 (m, 1H, Н5); 7.25 (s, 1H, Н3); 7.29 (dd, J=1.1 Гц, J=7.1 Гц, 1H, H6); 7.43 (d, J=8.9 Гц, 1H, Н7); 7.63 (d, J=8.9 Гц, 1H, H4); 9.50(s, 1H).
Пример 25
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-циано-2-индолилкарбамид
Синтез аналогичен примеру 7.
Выход 102 мг (59%).
Т.пл. 96°С. МС m/z 470 (М+). ИК (KBr): 3315; 2926; 2821; 2218, 1634; 1570; 1506; 1239; 1043; 734. 1H-ЯМР (CDCl3, 360 Мгц) δ (м.д.): 1.69-1.82 (m, 4H, СН2-CH2); 2.51 (t, J=6.9 Гц, 2Н, CH2N); 2.66 (m, 4H, пиперазин); 3.06 (m, 4H, пиперазин); 3.58-3.63 (m, 2H, CH2NCO); 6.85 (br, t, J=5.5 Гц, 1Н, NHCO); 6.88-6.91 (m, 2H, фенил, Н3); 7.09-7.17 (m, 2H, фенил); 7.35 (dd, J=1.4 Гц, J=8.2 Гц, 1H, H5); 7.70 (d, J=8.5 Гц, Н4); 7.84 (s, 1 Н, Н7); 10.65 (s, 1H, NH). 13С-ЯМР (CDCl3, 90 Мгц) δ (м.д.): 161.2; 151.1; 135.2; 134.3; 134.0; 130.5; 127.5; 127.4; 124.6; 123.1; 122.8; 120.1; 118.5; 117.2; 106.9; 102.0; 58.7; 53.3; 51.2; 41.1; 39.9; 24.4.
CHN (%): С24Н25Cl2N5·Н2O
Рассчитано: С 59,02; Н 5,57; N 14,34. Найдено: С 58,76; Н 5,30; N 14,19.
БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ
Биологическую активность соединений по изобретению определяли анализами связывания радиолигандов. Все эксперименты с радиолигандами проводили методами, описанными авторами настоящего изобретения (Hübner, Н. et al. J.Med. Chem. 2000, 43, 756-762). Для измерения аффинностей к рецепторам семейства D2 использовали гомогенаты мембран клеток яичников китайского хомячка (клетки СНО), которые стабильно экспрессировали подтипы человеческих рецепторов D2long, D2short (Hayes, G. et al. Mol. Endocrinol. 1992, 6, 920-926), D3 (Sokoloff, P. et al. Eur. J.Pharmacol. 1992, 225, 331-337) или D4.4 (Asghari, V.J.Neurochem. 1995, 65, 1157-1165). В общем, анализы связывания проводили инкубацией гомогенатов рецепторов с радиолигандом [3H]-спиперон и тестируемым соединением в разных концентрациях. Аффинности к D1-рецепторам определяли с использованием гомогенатов нативных мембран, полученных из полосатого тела мозга свиньи, и D1-селективного радиолиганда [3H]-SCH23390.
Для определения сил связывания соединений с серотониновыми рецепторами подтипов 5-НТ1А и 5-НТ2 инкубировали мембраны коры головного мозга свиньи с радиолигандами [3H]-8-OH-DPAT (для 5-НТ1А) или [3Н]-кетансерин (5-НТ2) и соединениями по изобретению. Показатели одновременного связывания соединений с серотонинергическим 5-НТ2-рецептором и адренергическим рецептором подтипа α1 при мечении радиолигандом [3H]-кетансерин подтверждали в параллельном эксперименте с селективным блокированием α1-рецепторов празозином. Поэтому величины Ki, определенные в присутствии 10 мкМ празозина, представляют связь только с 5-НТ2-рецептором. Кроме того, аффинность к α1-рецепторам свиньи определяли в отдельном эксперименте с использованием α1-селективного радиолиганда [3H]-празозин.
Результаты анализов связывания с рецепторами по подтипам дофаминовых рецепторов суммированы в таблице 1.
Все соединения, тестированные в анализе связывания, показали хорошие и очень хорошие аффинности к дофаминовым рецепторам с четким предпочтением связывания с подтипами семейства D2. Независимо от частичной структуры всегда очевидна четкая селективность по отношению к D3-рецепторам. Самая высокая аффинность к D3 может быть достигнута, если в качестве гетероаренового компонента использовать бензо[b]тиофен или индол. Например, соединения примеров 1, 2, 10-13 и 19-22 имеют превосходные величины Ki, от 0,23 до 0,57 нМ.
Паттерн замещения арилпиперазинового компонента главным образом влияет на степень селективности аффинности к D3 по сравнению с другими подтипами рецепторов. Имея коэффициенты селективности более 1000, 2,3-дихлорфенилзамещенные соединения (примеры 2, 6, и 10) проявляют ранее не описанную селективность к D3 с сопутствующей субнаномолярной аффинностью. Интересно, что ферроцениловые производные примеров 16 и 17 отличаются высокой аффинностью к D4, причем соединение примера 17 с величиной Ki 0,47 нМ для D3-рецептора и 0,63 нМ для D4-рецептора демонстрирует экстраординарный профиль связывания с рецепторами.
Тесты для определения собственной активности соединений примеров проводили в анализе митогенеза, как описано в литературе (Hübner, H. et al. J.Med. Chem. 2000, 43, 4563-4569; Löber, S. Bioorg. Med. Chem. Lett. 2002, 12.17, 2377-2380). Иллюстративной для соединения примера 1 является частичная агонистическая активность, составляющая 49% от максимальной стимуляции рецепторов, которая может быть инициирована полным агонистом квинпиролом в качестве эталонного соединения. В результате вычислений по кривой концентрация-активность, полученной в этом тесте, получили величину EC50 0,38 нМ.
Результаты исследования аффинности к серотониновым рецепторам подтипов 5-НТ1А и 5-НТ2 и к адренергическому рецептору α1 приведены в таблице 2. Независимо от частичной структуры производных можно наблюдать предпочтительное связывание с подтипом 5-НТ1А по сравнению с 5-НТ2. Имея измеренные величины Ki от 8 до 19 нМ, соединения примеров 1, 3, 7, 8 и 16 отличаются высокой аффинностью к α1-рецептору.
Анализ соотношения структура/активность показывает четкую зависимость связывания этих рецепторов от паттерна замещения арилпиперазиновой части структуры. Как и в случае с дофаминовыми рецепторами, связывание с 5-НТ-рецептором и с α1-рецептором явно ниже у производных с 2,3-дихлорфенильным радикалом, что приводит к расширению спектра селективности по сравнению с аффинностью этих соединений к D3-рецептору.
b Величина Ki в случае одновременной инкубации с 10 мкМ празозина.
c Величина Ki, полученная для сайта связывания с высокой аффинностью в случае мечения [3H]-кетансерином.
d Величина Ki из конкурентного эксперимента с α1-селективным радиолигандом [3Н]-празозином.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОВИРУСНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2571662C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛЫ | 2001 |
|
RU2286343C2 |
| АНТАГОНИСТЫ АРИЛСУЛЬФОНАМИДА CCR3 | 2010 |
|
RU2539591C2 |
| НОВЫЕ СОЕДИНЕНИЯ, ИХ ИЗОМЕР ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ В КАЧЕСТВЕ АНТАГОНИСТА ВАНИЛОИДНОГО РЕЦЕПТОРА И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2007 |
|
RU2448108C2 |
| КОМПОЗИЦИИ, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СВЯЗАННЫХ С KIT | 2014 |
|
RU2706235C2 |
| ПРОИЗВОДНЫЕ 1,2,4-ТРИАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ СИГМА РЕЦЕПТОРА | 2007 |
|
RU2451015C2 |
| ПИРРОЛОХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ 5-НТ6 АНТАГОНИСТОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2013 |
|
RU2688161C2 |
| КОНДЕНСИРОВАННЫЕ ТРИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛОВ В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ TNF | 2014 |
|
RU2689777C1 |
| ПРОИЗВОДНОЕ 1,2,4-ТРИАЗОЛОНА | 2011 |
|
RU2566754C2 |
| ИНГИБИТОРЫ ГЛИКОЛАТОКСИДАЗЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2805308C2 |
Изобретение относится к активному по отношению к нейрорецепторам N-[(4-фенил-1-пиперазинил)алкил]-замещенному гетероаренкарбоксамиду общей формулы (I) и к структурно аналогичным 2-ферроцениловым соединениям общей формулы (II)
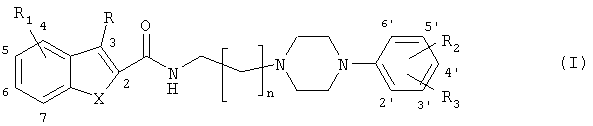
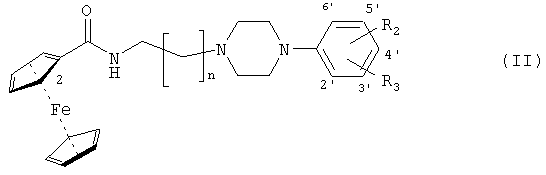
в которых R - водород, С1-6-алкил, галоген;
R1, R2 и R3 независимо выбраны из водорода, гидрокси, С1-6алкила, C1-6алкилокси, галогена, трифторметила и циано;
Х может представлять собой S, О, NH или Те.
Соединения могут быть использованы для лечения заболеваний центральной нервной системы (ЦНС). Описаны также способы получения соединений, фармацевтическая композиция на их основе и применение для получения лекарственного средства для лечения заболеваний ЦНС. 11 н. и 15 з.п. ф-лы, 2 табл.
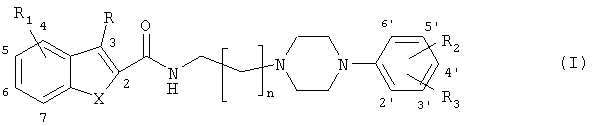
где n равно 1-4, и
R является водородом, С1-6алкилом или галогеном, и
(а) Х представляет собой S или О:
(1) когда R1 представляет собой гидрокси, алкилокси или циано, каждый из R2 и R3 независимо выбран из водорода, гидрокси, С1-6алкилокси, C1-6алкила, галогена, трифторметила и циано,
(2) когда R1 представляет собой водород, C1-6алкил, галоген или трифторметил, R2 выбран из гидрокси и циано, и R3 выбран из водорода, гидрокси, С1-6алкилокси, C1-6алкила, галогена, трифторметила и циано,
или
(б) Х представляет собой NH или Те:
R1, R2 и R3 независимо выбран из водорода, гидрокси, C1-6алкила, C1-6алкилокси, галогена, трифторметила и циано, и фармацевтически приемлемые соли этого соединения при условии, что это соединение не является N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамидом.
Х представляет собой S или О, и R1 выбран из радикалов гидрокси, С1-6алкилокси и циано, и R2 и R3 отдельно или совокупно выбраны из радикалов водород, гидрокси, С1-6алкилокси, С1-6алкил, галоген, трифторметил и циано,
или
Х представляет собой S или О, и R1 выбран из радикалов водород, С1-6алкил, галоген или трифторметил, и R2 и R3 отдельно или совокупно выбраны из радикалов гидрокси и циано,
или
Х представляет собой NH, и R1 выбран из радикалов гидрокси, С2-6алкил, С2-6алкилокси, трифторметил и циано, и R2 и R3 отдельно или совокупно выбраны из радикалов водород, гидрокси, С2-6алкилокси, С1-6алкил, галоген, трифторметил и циано.
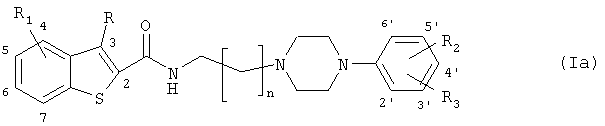
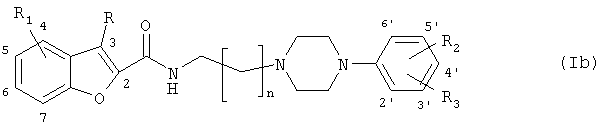
где n равно 1-4,
R является водородом, C1-С6-алкилом или галогеном,
когда R1 представляет собой гидрокси, C1-С6-алкилокси или циано, каждый из R2 и R3 независимо выбран из водорода, гидрокси, C1-С6-алкилокси, C1-С6-алкила, галогена, трифторметила и циано,
когда R1 представляет собой водород, C1-С6-алкил, галоген или трифторметил, R2 выбран из гидрокси и циано, и R3 выбран из водорода, гидрокси, C1-С6-алкила, C1-С6-алкилокси, галогена, трифторметила и циано, и его фармацевтически приемлемые соли.
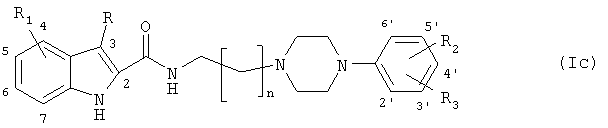
где n равно 1-4,
R является водородом, C1-С6-алкилом или галогеном,
R1 выбран из водорода, гидрокси, C1-С6-алкила, C1-С6-алкокси, трифторметила, фтора, хлора, брома и циано,
каждый из R2 и R3 независимо выбран из водорода, гидрокси, C1-С6-алкила, C1-С6-алкилокси, галогена, трифторметила и циано,
и фармацевтически приемлемые соли этого соединения при условии, что это соединение не является N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамидом.
(а) когда R1 представляет собой гидрокси, трифторметил или циано, каждый из R2 и R3 независимо выбран из водорода, гидрокси, C1-С6-алкила, C1-С6-алкилокси, галогена, трифторметила и циано,
и
(б) когда R1 представляет собой водород, C1-С6-алкил, C1-С6-алкилокси или галоген, R2 выбран из гидрокси и циано, и R3 выбран из водорода, гидрокси, C1-С6-алкила, C1-С6-алкилокси, галогена, трифторметила и циано, и фармацевтически приемлемые соли этого соединения.
заместитель R1 находится в положении 5 или 6 гетероцикла, и
заместители R2 и R3 находятся соответственно в положениях 2 или 3 или соответственно в положениях 2 или 4 фенильного кольца, и в случае, когда один из двух заместителей R2 и R3 является атомом водорода, соответственный другой заместитель находится в положении 2 фенильного кольца.
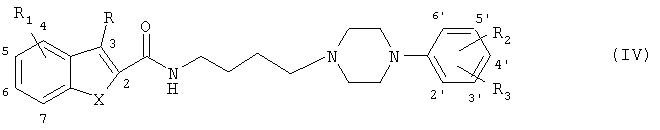
где Х представляет собой S, NH или О,
R выбран из водорода, C1-С6-алкила, фтора, хлора и брома,
R1 выбран из водорода, C1-С6-алкокси, C1-С6-алкила, фтора, хлора, брома, трифторметила и циано, причем R1 находится в положении 5 или 6 гетероцикла,
R2 и R3 независимо выбраны из водорода, C1-С6-алкилокси, C1-С6-алкила, фтора, хлора, брома и трифторметила, причем R2 и R3 находятся соответственно в положениях 2 или 3 или соответственно в положениях 2 или 4 фенильного кольца, и в случае, когда один из двух заместителей R2 и R3 является атомом водорода, соответственный другой заместитель находится в положении 2 фенильного кольца, и фармацевтически приемлемые соли этого соединения при условии, что это соединение не является N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-индолилкарбамидом.
когда Х представляет собой S или О, тогда R1 выбран из водорода, C1-С3-алкила, фтора, хлора, брома, циано и трифторметила.
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-циано-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-циано-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-6-циано-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-6-циано-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]тиофенилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-индолилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-циано-2-индолилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-бром-2-индолилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-6-циано-2-индолилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-индолилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-6-циано-2-индолилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-циано-2-индолилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-циано-2-бензо[b]фуранилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]фуранилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]фуранилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-5-бром-бензо[b]фуранилкарбамида,
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-5-бром-2-бензо[b]фуранилкарбамида,
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-бензо[b]теллурофенилкарбамида и
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-бензо[b]теллурофенилкарбамида,
и его фармацевтически приемлемые соли.
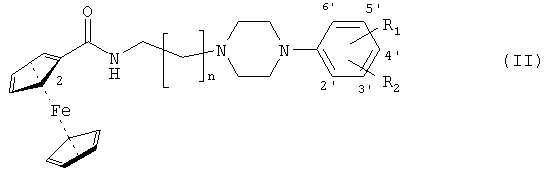
где n равно 1-4, и R1 и R2 отдельно или совокупно представляют собой радикалы водород, гидрокси, С1-С6-алкилокси, С1-С6-алкил, галоген, трифторметил или циано.
N-4-(4-(2-метоксифенил)пиперазин-1-ил)бутил-2-ферроценилкарбамида и
N-4-(4-(2,3-дихлорфенил)пиперазин-1-ил)бутил-2-ферроценилкарбамида.
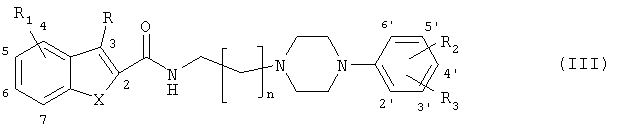
где n равно 1-4, и Х представляет собой S, О или NH, когда R является водородом, С1-С6-алкилом или галогеном, и R1 выбран из радикалов водород, С1-С6-алкил, галоген, трифторметил, и каждый из R2 и R3 отдельно или совокупно выбран из радикалов водород, гидрокси, С1-С6-алкилокси, С1-С6-алкил, галоген, трифторметил и циано,
для приготовления лекарственного средства для лечения или предупреждения пристрастия к кокаину, алкоголю, опиатам и никотину, нейродегенеративных расстройств, в частности болезни Паркинсона, или сексуальной дисфункции.
R выбран из водорода, С1-С6-алкила, фтора, хлора и брома,
R1 выбран из водорода, С1-С6-алкокси, С1-С6-алкила, фтора, хлора, брома и трифторметила, и
каждый из R2 и R3 независимо выбран из водорода, С1-С6-алкокси, С1-С6-алкила, фтора, хлора, брома и трифторметила.
заместитель R1 находится в положении 5 или 6 гетероцикла, и
заместители R2 и R3 находятся соответственно в положениях 2 или 3 или соответственно в положениях 2 или 4 фенильного кольца, и в случае, когда один из двух заместителей R2 и R3 является атомом водорода, соответственный другой заместитель находится в положении 2 фенильного кольца.
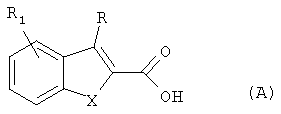
с соединением общей формулы (В)
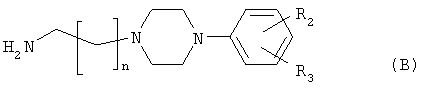
где n, R, R1, R2 и R3 такие, как определено для общих формул (I), (III) и (IV).
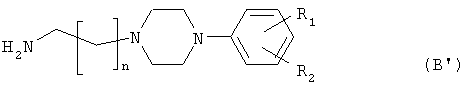
где n, R1 и R2 такие, как определено для формулы (II).
| US 3646047, 29.02.1972 | |||
| US 6090807, 18.07.2000 | |||
| Передающее стартстопное устройство | 1974 |
|
SU496692A1 |
Авторы
Даты
2008-03-27—Публикация
2003-07-02—Подача